文档内容
课时检测(八) 新情境下信息型方程式的书写
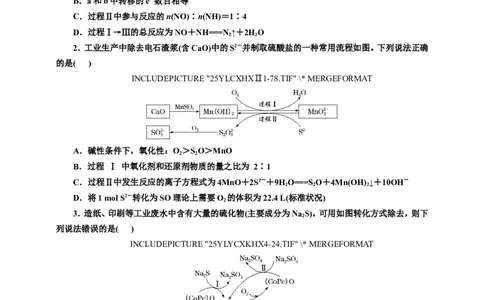
1.(2022·湖南等级考)科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海
洋中的NO转化为N 进入大气层,反应过程如图所示。
2
INCLUDEPICTURE "22HXHNGK-7.TIF" \* MERGEFORMAT
下列说法正确的是( )
A.过程Ⅰ中NO发生氧化反应
B.a和b中转移的e-数目相等
C.过程Ⅱ中参与反应的n(NO)∶n(NH)=1∶4
D.过程Ⅰ→Ⅲ的总反应为NO+NH===N ↑+2HO
2 2
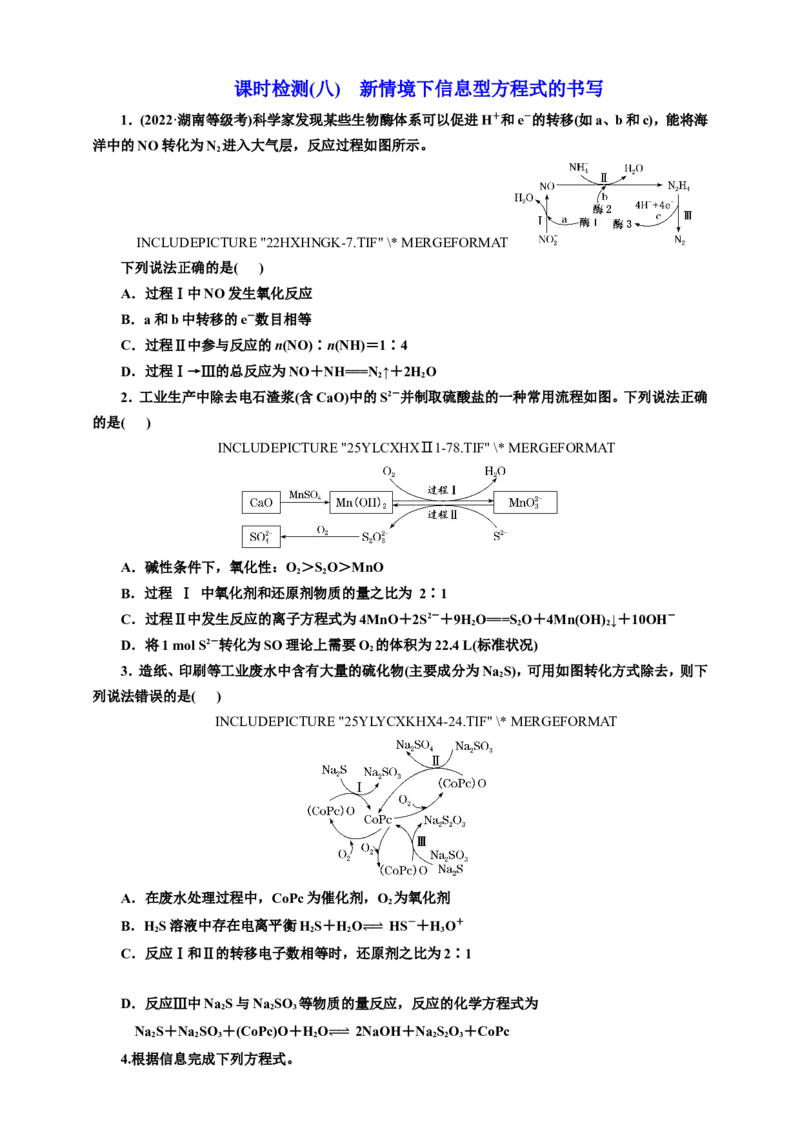
2.工业生产中除去电石渣浆(含CaO)中的S2-并制取硫酸盐的一种常用流程如图。下列说法正确
的是( )
INCLUDEPICTURE "25YLCXHXⅡ1-78.TIF" \* MERGEFORMAT
A.碱性条件下,氧化性:O>SO>MnO
2 2
B.过程 Ⅰ 中氧化剂和还原剂物质的量之比为 2∶1
C.过程Ⅱ中发生反应的离子方程式为4MnO+2S2-+9HO===S O+4Mn(OH) ↓+10OH-
2 2 2
D.将1 mol S2-转化为SO理论上需要O 的体积为22.4 L(标准状况)
2
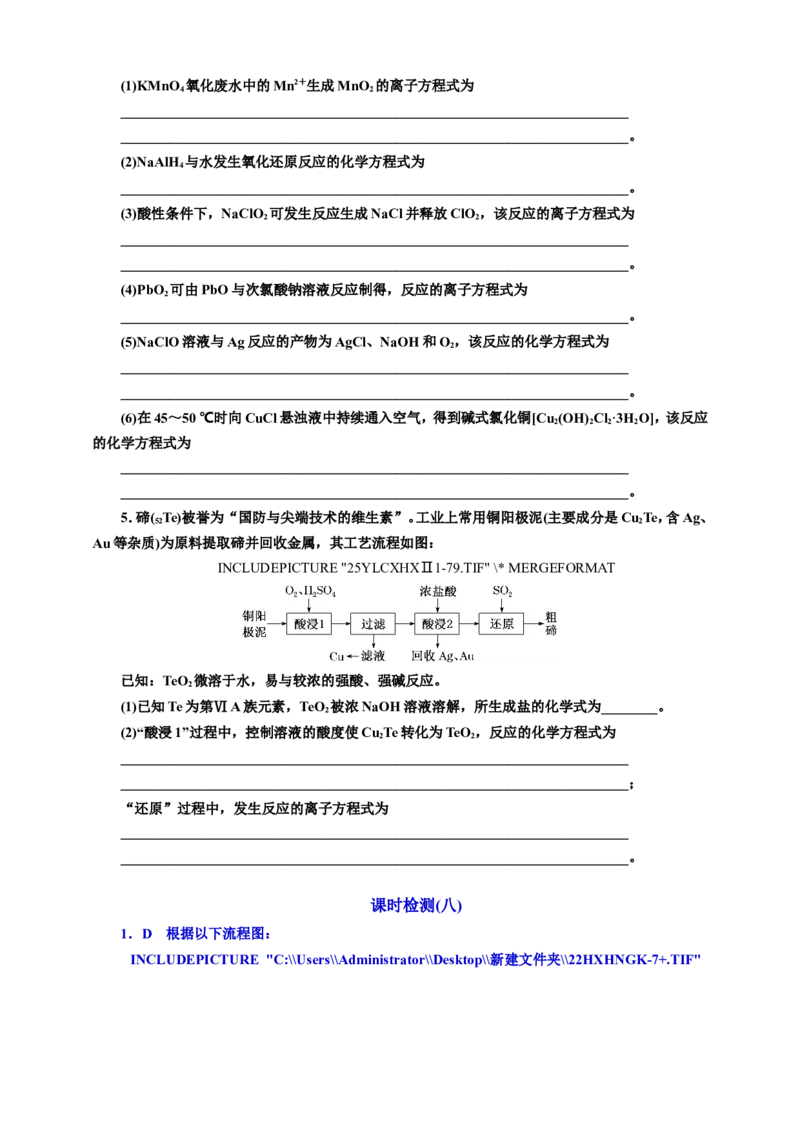
3.造纸、印刷等工业废水中含有大量的硫化物(主要成分为Na S),可用如图转化方式除去,则下
2
列说法错误的是( )
INCLUDEPICTURE "25YLYCXKHX4-24.TIF" \* MERGEFORMAT
A.在废水处理过程中,CoPc为催化剂,O 为氧化剂
2
B.HS溶液中存在电离平衡HS+HO HS-+HO+
2 2 2 3
C.反应Ⅰ和Ⅱ的转移电子数相等时,还
⥫
原
⥬
剂之比为2∶1
D.反应Ⅲ中Na S与Na SO 等物质的量反应,反应的化学方程式为
2 2 3
Na S+Na SO +(CoPc)O+HO 2NaOH+Na SO+CoPc
2 2 3 2 2 2 3
4.根据信息完成下列方程式。
⥫⥬(1)KMnO 氧化废水中的Mn2+生成MnO 的离子方程式为
4 2
________________________________________________________________________
________________________________________________________________________。
(2)NaAlH 与水发生氧化还原反应的化学方程式为
4
________________________________________________________________________。
(3)酸性条件下,NaClO 可发生反应生成NaCl并释放ClO ,该反应的离子方程式为
2 2
________________________________________________________________________
________________________________________________________________________。
(4)PbO 可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为
2
________________________________________________________________________。
(5)NaClO溶液与Ag反应的产物为AgCl、NaOH和O,该反应的化学方程式为
2
________________________________________________________________________
________________________________________________________________________。
(6)在45~50 ℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu (OH) Cl ·3HO],该反应
2 2 2 2
的化学方程式为
________________________________________________________________________
________________________________________________________________________。
5.碲( Te)被誉为“国防与尖端技术的维生素”。工业上常用铜阳极泥(主要成分是Cu Te,含Ag、
52 2
Au等杂质)为原料提取碲并回收金属,其工艺流程如图:
INCLUDEPICTURE "25YLCXHXⅡ1-79.TIF" \* MERGEFORMAT
已知:TeO 微溶于水,易与较浓的强酸、强碱反应。
2
(1)已知Te为第ⅥA族元素,TeO 被浓NaOH溶液溶解,所生成盐的化学式为________。
2
(2)“酸浸1”过程中,控制溶液的酸度使Cu Te转化为TeO ,反应的化学方程式为
2 2
________________________________________________________________________
________________________________________________________________________;
“还原”过程中,发生反应的离子方程式为
________________________________________________________________________
________________________________________________________________________。
课时检测(八)
1.D 根据以下流程图:
INCLUDEPICTURE "C:\\Users\\Administrator\\Desktop\\新建文件夹\\22HXHNGK-7+.TIF"\* MERGEFORMATINET
过程Ⅰ中NO得电子发生还原反应,A项错误;由以上分析知,a、b中转移电子数目不相等,B项
错误;由以上分析知,过程Ⅱ中参加反应的n(NO)与n(NH)之比为1∶1,C项错误;由以上分析知,总
反应为NH+NO===N ↑+2HO,D项正确。
2 2
2.C 由题图可知,过程Ⅰ中O 氧化Mn(OH) 生成MnO,则氧化性:O>MnO,过程Ⅱ中MnO
2 2 2
氧化S2-生成SO,则氧化性:MnO>SO,所以碱性条件下,氧化性:O>MnO>SO,故A错误;过程
2 2 2 2
Ⅰ中发生反应的离子方程式为2Mn(OH) +O +4OH-===2MnO+4HO,则氧化剂和还原剂物质的
2 2 2
量之比为1∶2,故B错误;过程Ⅱ中MnO得电子转化为Mn(OH) ,S2-失电子转化为SO,根据原子
2 2
守恒、得失电子守恒及电荷守恒可得反应的离子方程式为4MnO+2S2-+9HO===S O+4Mn(OH) ↓
2 2 2
+10OH-,故C正确;1 mol S2- 转化为SO理论上转移8 mol 电子,根据得失电子守恒可知,需要氧
气的物质的量为=2 mol,在标准状况下的体积为2 mol×22.4 L·mol-1=44.8 L,故D错误。
3.C 在废水处理过程中,CoPc参与反应但反应前后不变,为催化剂,O 参与反应且反应后化合价降
2
低,为氧化剂,A正确;HS是二元弱酸,分步电离,第一步电离产生HS-和氢离子或水合氢离子:HS
2 2
+HO HS-+HO+,B正确;反应Ⅰ中还原剂Na S被氧化成Na SO ,化合价升高6,而反应Ⅱ中
2 3 2 2 3
还原剂⥫N⥬a SO 被氧化成Na SO ,化合价升高2,当反应Ⅰ和Ⅱ转移电子数相等时,还原剂之比为
2 3 2 4
1∶3,C错误;反应Ⅲ中Na S与Na SO 等物质的量与(CoPc)O反应生成Na SO 和CoPc,D正确。
2 2 3 2 2 3
4.(1)2MnO+3Mn2++2HO===5MnO ↓+4H+
2 2
(2)NaAlH +4HO===Na[Al(OH) ]+4H↑
4 2 4 2
(3)4H++5ClO===Cl-+4ClO ↑+2HO
2 2
(4)PbO+ClO-===PbO +Cl-
2
(5)4Ag+4NaClO+2HO===4AgCl+4NaOH+O↑
2 2
(6)4CuCl+O+8HO=====2[Cu (OH) Cl ·3HO]
2 2 2 2 2 2
5.解析:Te与S同主族,SO 与氢氧化钠反应生成Na SO ,所以TeO 与浓NaOH溶液反应生成盐
2 2 3 2
的化学式为Na TeO 。
2 3
答案:(1)Na TeO
2 3
(2)Cu Te+2O+2HSO ===2CuSO +TeO +2HO Te4++2SO +4HO===2SO+ Te↓+8H+
2 2 2 4 4 2 2 2 2