文档内容
课时检测(五十) 化学平衡、化学反应方向及调控的基本知能评价
1.下列说法正确的是( )
A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行
B.反应NH HCO (s)===NH(g)+HO(g)+CO (g) ΔH=+185.7 kJ·mol-1能自发进行,原因是
4 3 3 2 2
体系有自发地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向
2.一定温度下,在恒容密闭容器中发生反应2HI(g)+Cl (g) 2HCl(g)+I(s)。下列事实不能说
2 2
明该反应达到平衡状态的是( ) ⥫⥬
A.容器内气体压强不再改变
B.容器内气体密度不再改变
C.容器内气体颜色不再改变
D.断裂1 mol Cl—Cl键的同时断裂1 mol H—Cl键
3.(2022·江苏等级考)用尿素水解生成的NH 催化还原NO,是柴油机车辆尾气净化的主要方法。
3
反应为4NH (g)+O(g)+4NO(g) 4N(g)+6HO(g),下列说法正确的是( )
3 2 2 2
A.上述反应ΔS<0
⥫⥬
B.上述反应平衡常数K=
C.上述反应中消耗1 mol NH ,转移电子的数目为2×6.02×1023
3
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
4.温度为T 时,将气体X和气体Y各1.6 mol充入10 L恒容密闭容器中,发生反应X(g)+Y(g)
1
2Z(g),一段时间后达到平衡。反应过程中测定的数据如表,下列说法正确的是( ) ⥫⥬
t/min 2 4 7 9
n(Y)/mol 1.2 1.1 1.0 1.0
A.前4 min的平均速率v(Z)=0.025 mol·L-1·min-1
B.T 时,反应的平衡常数K =1.2
1 1
C.其他条件不变,9 min后,向容器中再充入1.6 mol X,平衡向正反应方向移动,再次达到平衡时
X的浓度减小,Y的转化率增大
D.其他条件不变,若降温到T 达到平衡时,平衡常数K =4,则此反应的ΔH>0
2 2
5.(2024·浙江高三开学校联考)某2 L密闭容器中投入NO、O 分别为2 mol、1 mol,只发生反应:2NO
2
+O 2NO ,在不同温度下、相同时间(t min)内NO的转化率如表所示。则下列说法正确的是( )
2 2
⥫⥬ 温度/℃ 5 30 70 80
转化率/% 10 80 80 50
A.该反应是吸热反应
B.若温度为50 ℃,NO的转化率>80%
C.30 ℃、70 ℃温度下,t min时的NO 生成速率相等
2
D.80 ℃温度下,该反应的平衡常数为2
6.(2023·河北等级考)在恒温恒容密闭容器中充入一定量W(g),发生如下反应:2W(g)=====4X(g)+Y(g)
③ ②
2Z(g)
反应②和③的速率方程分别为v=kc2(X)和v=kc(Z),其中k、k 分别为反应②和③的速率常数,
2 2 3 3 2 3
反应③的活化能大于反应②。测得W(g)的浓度随时间的变化如下表。
t/min 0 1 2 3 4 5
c(W)/
0.160 0.113 0.080 0.056 0.040 0.028
(mol·L-1)
下列说法正确的是( )
A.0~2 min内,X的平均反应速率为
0.080 mol·L-1·min-1
B.若增大容器容积,平衡时Y的产率增大
C.若k=k,平衡时c(Z)=c(X)
2 3
D.若升高温度,平衡时c(Z)减小
7.(2023·重庆等级考)逆水煤气变换体系中存在以下两个反应:
反应Ⅰ:CO (g)+H(g) CO(g)+HO(g)
2 2 2
反应Ⅱ:CO
2
(g)+4H
2
(g⥫)⥬ CH
4
(g)+2H
2
O(g)
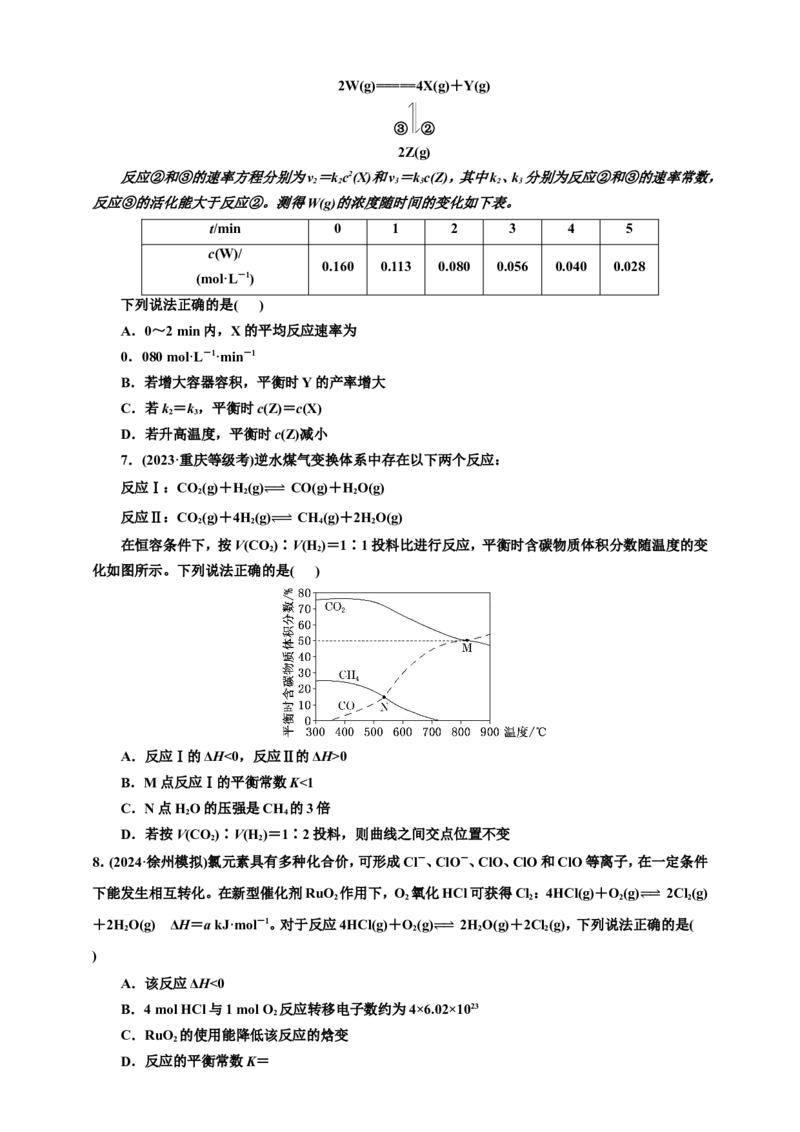
在恒容条件下,按V(CO 2⥫)∶ ⥬V(H
2
)=1∶1投料比进行反应,平衡时含碳物质体积分数随温度的变
化如图所示。下列说法正确的是( )
A.反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0
B.M点反应Ⅰ的平衡常数K<1
C.N点HO的压强是CH 的3倍
2 4
D.若按V(CO)∶V(H )=1∶2投料,则曲线之间交点位置不变
2 2
8.(2024·徐州模拟)氯元素具有多种化合价,可形成Cl-、ClO-、ClO、ClO和ClO等离子,在一定条件
下能发生相互转化。在新型催化剂RuO 作用下,O 氧化HCl可获得Cl :4HCl(g)+O(g) 2Cl (g)
2 2 2 2 2
+2HO(g) ΔH=a kJ·mol-1。对于反应4HCl(g)+O(g) 2HO(g)+2Cl (g),下列说法正⥫确⥬的是(
2 2 2 2
) ⥫⥬
A.该反应ΔH<0
B.4 mol HCl与1 mol O 反应转移电子数约为4×6.02×1023
2
C.RuO 的使用能降低该反应的焓变
2
D.反应的平衡常数K=9.(2024·张家界模拟)在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生
反应:Ni(s)+4CO(g) Ni(CO) (g),已知该反应平衡常数与温度的关系如表所示。下列说法不正确的
4
是( ) ⥫⥬
温度/℃ 25 80 230
平衡常数 5×104 2 1.9×10-5
A.上述生成Ni(CO) (g)的反应为放热反应
4
B.25 ℃时,反应Ni(CO) (g) Ni(s)+4CO(g)的平衡常数为2×10-5
4
C.80 ℃时,测得某时刻Ni(C⥫O⥬)
4
、CO的浓度均为0.5 mol·L-1,则此时v
正
>v
逆
D.80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO) 的平衡浓度为2 mol·L-1
4
10.甲醇是重要的化工原料,可用于制备丙烯、氢气等。
(1)MTO法由甲醇制备丙烯时的反应原理是甲醇先脱水生成二甲醚,然后二甲醚与甲醇的平衡混合物
脱水转化为含丙烯较多的低聚烯烃。某温度下,在密闭容器中加入 CH OH气体,发生脱水反应:
3
2CH OH(g) CH OCH (g)+HO(g),一段时间后测得各组分的浓度如表所示:
3 3 3 2
物质 CH OH CH OCH HO
⥫⥬ 3 3 3 2
5 min浓度/(mol·L-1) 0.44 0.6 0.6
10 min浓度/(mol·L-1) 0.04 0.8 0.8
15 min浓度/(mol·L-1) 0.04 0.8 0.8
该温度下,反应的平衡常数数值是__________,CH OH的平衡转化率是________。
3
(2)利用甲醇水蒸气重整制氢是获得氢气的重要方法。反应原理如下:
反应ⅰ(主反应):CH OH(g)+HO(g) CO (g)+3H(g) ΔH=+49 kJ·mol-1
3 2 2 2
反应ⅱ(副反应):H
2
(g)+CO
2
(g) C⥫O⥬(g)+H
2
O(g) ΔH=+41 kJ·mol-1
①温度高于300 ℃则会同时发生 ⥫C⥬H
3
OH转化为CO和H
2
的副反应,该反应的热化学方程式是
________________________________________________________________________
________________________________________________________________________。
②反应中,经常使用催化剂提高化学反应速率,但催化剂对反应具有选择性。一定条件下,测得
CH OH转化率及CO、CO 选择性随温度变化情况分别如图所示(CO、CO 的选择性:转化的CH OH
3 2 2 3
中生成CO、CO 的百分比)。
2
从图中可知,反应的适宜温度为______________,随着温度的升高,催化剂对________(填“反应
ⅰ”或“反应ⅱ”)的选择性降低。课时检测(五十)
1.B 反应的ΔH>0,固态物质分解为气态物质,反应的ΔS>0。
2.D 反应过程中压强、气体密度是变量,容器内压强、气体密度不再改变说明反应达到平衡;容
器内气体颜色不再改变,说明氯气的浓度不变,反应达到平衡状态;平衡时断裂1 mol Cl—Cl键的同
时断裂2 mol H—Cl键,因此D项不能说明该反应达到平衡状态。
3.B 由题给方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,ΔS>0,A错误;
由方程式可知,反应每消耗4 mol氨气,转移12 mol电子,则反应中消耗1 mol氨气转移电子的数目为
3×6.02×1023,C错误;实际应用中,加入尿素的量过多,尿素水解生成的氨气过量,柴油机车辆排放的
氨气对空气污染程度增大,D错误。
4.A 由题表中数据可求得前4 min内消耗的Y为0.50 mol,v(Y)====0.012 5 mol·L-1·min-
1,所以v(Z)=2v(Y)=0.025 mol·L-1·min-1,A正确;由题表中数据可知7 min 时反应达到平衡,反应的
三段式为
X(g)+Y(g) 2Z(g)
起始/(mol·L-1) 0.16 0.16 0⥫⥬
变化/(mol·L-1) 0.06 0.06 0.12
平衡/(mol·L-1) 0.1 0.1 0.12
所以平衡常数K ===1.44,B错误;其他条件不变,9 min时是平衡状态,再充入1.6 mol X,平衡
1
向正反应方向移动,再次达到平衡时Y的转化率增大,由于X加入量大于平衡移动消耗量,所以再次
达到平衡时,X的浓度增大,C错误;T 时,平衡常数K =1.44,降温到T 达到平衡时,平衡常数K =
1 1 2 2
4,说明降低温度平衡正向移动,所以该反应正向为放热反应,ΔH<0, D错误。
5.B 根据表格数据,随着温度升高,速率加快,5 ℃、30 ℃ t min内未达平衡,70 ℃、80 ℃温度下
t min内反应已经达到平衡,平衡转化率随温度升高而减小,该反应为放热反应,A错误;由A项分析
和表格数据可知,50 ℃时NO的转化率大于80%,B正确;30 ℃、70 ℃转化率相同,但温度不同,t min
时的NO 生成速率不一定相等,C错误;80 ℃反应t min时已建立该条件下的平衡,NO、O 的起始浓
2 2
度分别为1 mol·L-1、0.5 mol·L-1,NO的转化率为50%,则NO、O、NO 的平衡浓度分别为0.5 mol·L
2 2
-1、0.25 mol·L-1、0.5 mol·L-1,故K===4,D错误。
6.D 0~2 min内,Δc(W)=(0.160-0.080)mol·L-1=0.080 mol·L-1,生成Δc(X)=2Δc(W)=0.160
mol·L-1,但一部分X转化为Z,造成Δc(X)<0.160 mol·L-1,则v(X)<=0.080 mol·L-1·min-1,A错误;
过程②是可逆反应,增大容器容积相当于减小压强,4X(g) 2Z(g)平衡向气体体积增大的方向移动,
即逆向移动,X的浓度增大,但过程①是完全反应的,故平衡时Y的产率不变,B错误;由速率之比等
⥫⥬
于系数比,平衡时v (X)=2v (Z),即v=2v,kc(Z)=2kc2(X),若k=k,平衡时c(Z)=2c2(X),C错
逆 正 3 2 3 2 2 3
误;反应③的活化能大于反应②,ΔH=正反应活化能-逆反应活化能<0,即4X(g) 2Z(g) ΔH<0,
该反应是放热反应,升高温度,平衡逆向移动,则平衡时c(Z)减小,D正确。
⥫⥬
7.C 由题图可知,随温度升高,CO体积分数增大,说明反应Ⅰ平衡正向移动,为吸热反应;随温
度升高,CH 体积分数减小,说明反应Ⅱ平衡逆向移动,为放热反应。由分析可知,反应Ⅰ的ΔH>0,反
4
应Ⅱ的ΔH<0,A错误;M点二氧化碳和一氧化碳的体积分数相等,均为50%,甲烷的体积分数为0,说
明只发生反应Ⅰ,又因为起始时按V(CO)∶V(H )=1∶1的投料比进行反应,恰好为反应Ⅰ中反应物
2 2
的化学计量数之比,所以M点反应Ⅰ的平衡常数K=1,B错误;N点一氧化碳、甲烷的体积分数相等,
结合反应方程式可知,生成水的总物质的量为甲烷的物质的量的3倍,即N点HO的压强是CH 的3
2 4倍,C正确;反应Ⅰ为气体分子数不变的反应,反应Ⅱ为气体分子数减小的反应,若按V(CO)∶V(H )
2 2
=1∶2投料,氢气的投料量增加,相当于增大压强,会使反应Ⅱ平衡正向移动,甲烷含量增大,所以曲
线之间交点位置会发生改变,D错误。
8.A 对于反应4HCl(g)+O(g)2HO(g)+2Cl (g),生成物气体分子数小于反应物气体分子数,
2 2 2
即ΔS<0,该反应在催化剂RuO 作用下能自发进行,所以该反应ΔH<0,A正确;由于反应为可逆反
2
应,4 mol HCl与1 mol O 混合时,参加反应的HCl的物质的量小于4 mol,则反应转移电子数小于
2
4×6.02×1023,B不正确;RuO 为该反应的催化剂,催化剂只能降低反应的活化能,但不能改变反应的焓
2
变,C不正确;反应物和生成物都呈气态,反应的平衡常数K=,D不正确。
9.C 温度升高,平衡常数减小,故正反应为放热反应,A项正确;25 ℃ 时,逆反应的平衡常数K′
===2×10-5,B项正确;80 ℃时,若Ni(CO) 、CO的浓度均为0.5 mol·L-1,则Q===8>K,v <v ,
4 正 逆
C项错误;80 ℃达到平衡时,若n(CO)=0.3 mol,c(CO)=1 mol·L-1,故c[Ni(CO) ]=K·c4(CO)=2×14
4
mol·L-1=2 mol·L-1,D项正确。
10.解析:(1)由表格可知,10 min后,反应达到了平衡,根据反应2CH OH(g)CH OCH (g)+
3 3 3
HO(g),K===400;设甲醇的起始浓度为x mol·L-1,根据三段式:
2
2CH OH(g) CH OCH (g)+HO (g)
3 3 3 2
起始 x mol·L-1 ⥫ 0⥬ 0
转化 1.6 mol·L-1 0.8 mol·L-1 0.8 mol·L-1
平衡 0.04 mol·L-1 0.8 mol·L-1 0.8 mol·L-1
x=(1.6+0.04)mol·L-1=1.64 mol·L-1,则α(CHOH)=×100%≈97.56%。(2)①根据盖斯定律ⅰ+ⅱ可
3
得:CH OH(g) CO(g)+2H(g) ΔH=ΔH+ΔH=49 kJ·mol-1+41 kJ·mol-1=+90 kJ·mol-1。②
3 2 1 2
由题图可知,低⥫于⥬260 ℃时,CH OH的转化率较低,高于260 ℃时,CH OH的转化率较高,但在高于
3 3
260 ℃时,CO的选择性逐渐增大,CO 的选择性逐渐减小,所以最适宜温度为260 ℃;随着温度的升高,
2
催化剂对CO的选择性增大,CO 的选择性减小,所以温度升高,催化剂对反应ⅰ的选择性降低。
2
答案:(1)400 97.56%
(2)①CH OH(g) CO(g)+2H(g) ΔH=+90 kJ·mol-1 ②260 ℃ 反应ⅰ
3 2
⥫⥬