文档内容
成都七中 2023 届零诊模拟考试试卷
化 学
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。满分 100 分, 考试时间90 分
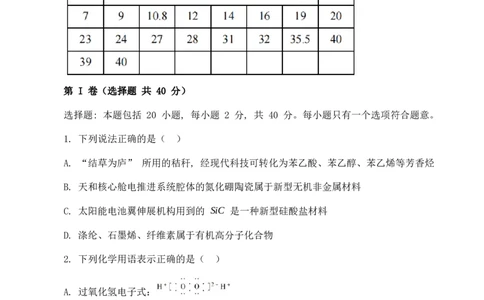
钟。 可能用到的相对原子质量:
第 I 卷(选择题 共 40 分)
选择题: 本题包括 20 小题, 每小题 2 分, 共 40 分。每小题只有一个选项符合题意。
1. 下列说法正确的是( )
A. “结草为庐” 所用的秸秆, 经现代科技可转化为苯乙酸、苯乙醇、苯乙烯等芳香烃
B. 天和核心舱电推进系统腔体的氮化硼陶瓷属于新型无机非金属材料
C. 太阳能电池翼伸展机构用到的 SiC 是一种新型硅酸盐材料
D. 涤纶、石墨烯、纤维素属于有机高分子化合物
2. 下列化学用语表示正确的是( )
A. 过氧化氢电子式:
B. 聚丙烯的链节: −CH −CH −CH −
2 2 2
14C
C. 原子结构示意图:
D. 乙炔的最简式: CH≡CH
3. 下列说法正确的是( )A. 淀粉通过水解可以直接生产乙醇和乙酸
B. 含 0.1mol 乙醇和 0.1mol 乙酸的混合物中加入足量钠, 最多置换出 2.24LH
2
C. 向酸性高锰酸钾溶液加入乙酸, 迅速导致紫红色裖色
D. 以生石灰除去乙醇水溶液中大部分水分, 后经蒸馏得到较纯的乙醇
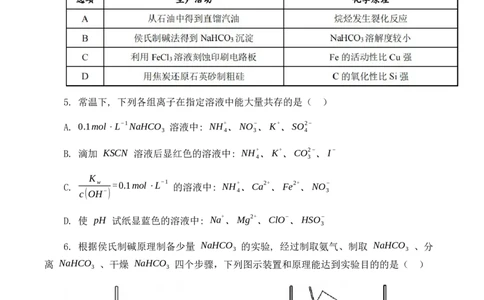
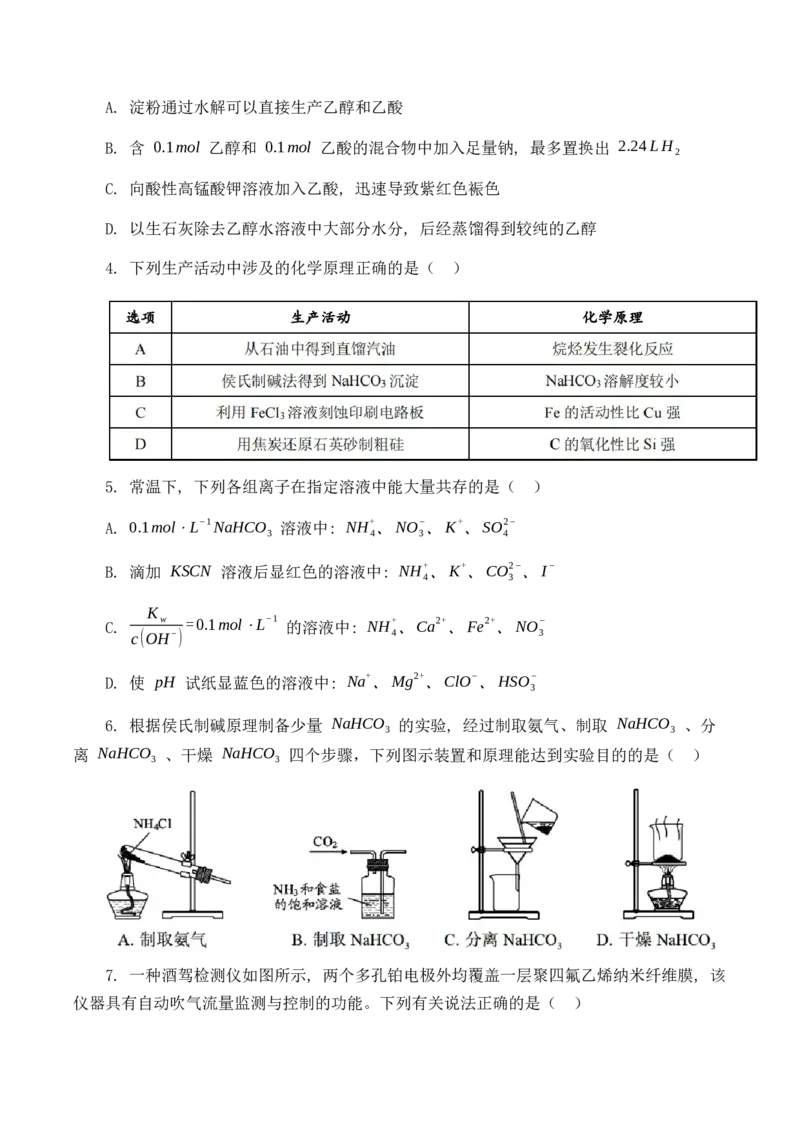
4. 下列生产活动中涉及的化学原理正确的是( )
5. 常温下, 下列各组离子在指定溶液中能大量共存的是( )
A. 0.1mol⋅L−1NaHCO 溶液中: NH+ 、NO−、K+ 、SO2−
3 4 3 4
B. 滴加 KSCN 溶液后显红色的溶液中: NH+ 、K+ 、CO2−、I−
4 3
K
C. w =0.1mol⋅L−1 的溶液中: NH+ 、Ca2+ 、Fe2+ 、NO−
c(OH−) 4 3
D. 使 pH 试纸显蓝色的溶液中: Na+ 、Mg2+ 、ClO−、HSO−
3
6. 根据侯氏制碱原理制备少量 NaHCO 的实验, 经过制取氨气、制取 NaHCO 、分
3 3
离 NaHCO 、干燥 NaHCO 四个步骤,下列图示装置和原理能达到实验目的的是( )
3 3
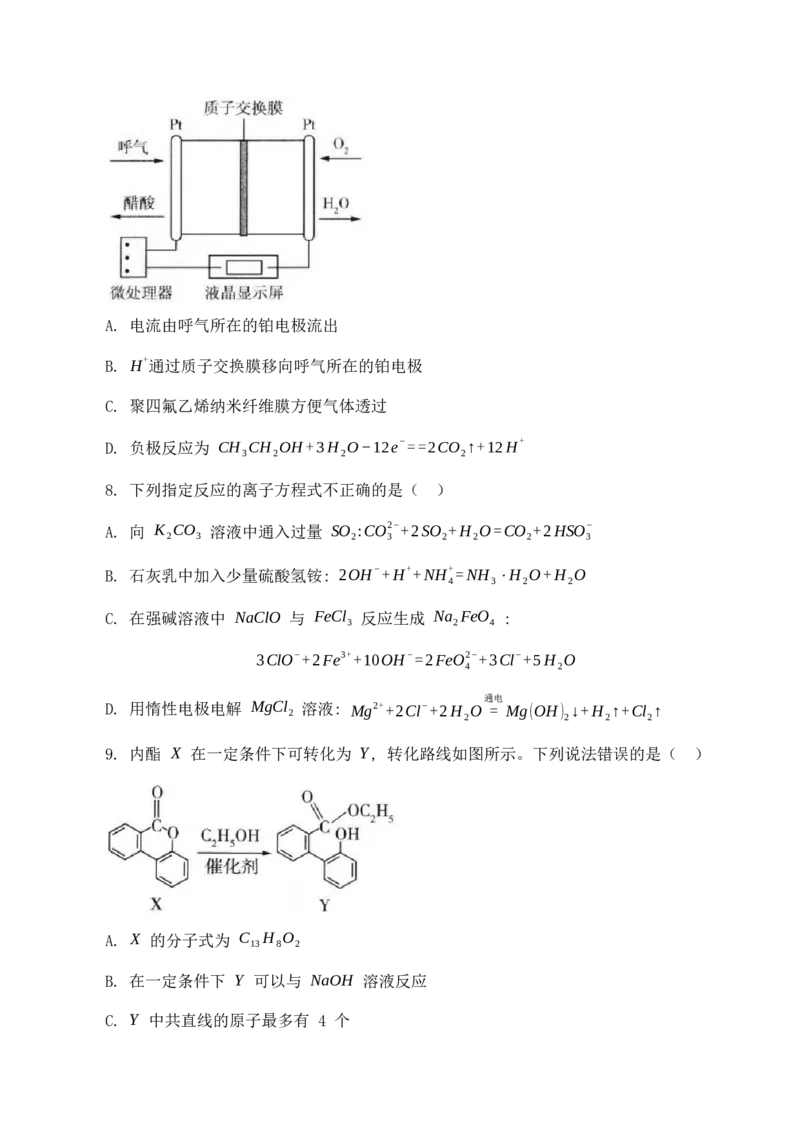
7. 一种酒驾检测仪如图所示, 两个多孔铂电极外均覆盖一层聚四氟乙烯纳米纤维膜, 该
仪器具有自动吹气流量监测与控制的功能。下列有关说法正确的是( )A. 电流由呼气所在的铂电极流出
B. H+通过质子交换膜移向呼气所在的铂电极
C. 聚四氟乙烯纳米纤维膜方便气体透过
D. 负极反应为 CH CH OH+3H O−12e−==2CO ↑+12H+
3 2 2 2
8. 下列指定反应的离子方程式不正确的是( )
A. 向 K CO 溶液中通入过量 SO :CO2−+2SO +H O=CO +2HSO−
2 3 2 3 2 2 2 3
B. 石灰乳中加入少量硫酸氢铵: 2OH−+H++NH+=NH ⋅H O+H O
4 3 2 2
C. 在强碱溶液中 NaClO 与 FeCl 反应生成 Na FeO :
3 2 4
3ClO−+2Fe3++10OH−=2FeO2−+3Cl−+5H O
4 2
通电
D. 用惰性电极电解 MgCl
2
溶液: Mg2++2Cl−+2H O = Mg(OH) ↓+H ↑+Cl ↑
2 2 2 2
9. 内酯 X 在一定条件下可转化为 Y, 转化路线如图所示。下列说法错误的是( )
A. X 的分子式为 C H O
13 8 2
B. 在一定条件下 Y 可以与 NaOH 溶液反应
C. Y 中共直线的原子最多有 4 个D. X 的一氯代物有 8 种
10. 设 N 为阿伏加德罗常数的值, 氯元素的 “价-类” 二维图如图所示, 下列分析
A
正确的是( )
A. 标准状况下, 11.2LCCl 中含有的极性键数目为 2N
4 A
B. 由 “价-类” 二维图推测 ClONO 具有强氧化性, 1molClONO 水解(生成两种酸)
2 2
转移电子数为 N
A
C. 工业上用 NaClO 和 SO 制备 1molClO 时, 消耗 SO 分子数为 0.5N
3 2 2 2 A
D. 常温下, 1L0.1mol/L 的 NaClO 溶液中 ClO−数目为 0.1N
A
11. 下列叙述中正确的是( )
A. 氢气可以在氯气中燃烧, 断键吸收的总能量多于成键放出的总能量
B. 向溶有 SO 的 BaCl 溶液中通入气体 X, 出现白色沉淀, 说明 X 具有强氧化性
2 2
C. 向 2 支均盛有 2mL1.0mol⋅L−1KOH 溶液的试管中分别加入 2 滴浓度均为
0.1mol⋅L−1 的 AlCl 和 MgCl 溶液, 一支试管出现白色沉淀, 另一支无明显现象, 说明
3 2
K [Al(OH) ]>K [Mg(OH) ]
sp 3 sp 2
D. 称取 14.3gNa CO ⋅10H O 固体于烧杯中, 加入少量蒸馏水溶解, 冷却后, 转移至
2 3 2
500mL 容量瓶中定容, 配制得到 0.10mol/LNa CO 溶液
2 3
12. 利用下表实验探究亚硝酸钠 (NaNO ) 的化学性质 (AgNO 是淡黄色微溶于水的固
2 2
体, Cr3+ 在溶液中显 绿色), 下列对实验现象的解释错误的是( )A. 实验(1), NaNO
2
溶液呈碱性: NO
2
−+H
2
O⇌HNO
2
+OH−
B. 实验(2), NaNO 可与某些盐发生复分解: NO −+Ag+==AgNO ↓
2 2 2
C. 实验(3), NaNO 具有氧化性: 2I−+2H++2NO −==I +2NO ↑+H O
2 2 2 2 2
D. 实验(4), NaNO 具有还原性: Cr O 2−+3NO −+8H+==3NO −+2Cr3++4H O
2 2 7 2 3 2
13. X、Y、Z、W 是原子序数依次增大的短周期主族元素, 其中 X、Z 位于同一主族。
X 原子的最外层电 子数是其电子层数的 3 倍, Y 原子的电子总数是其最外层电子数的 3
倍。 W 与 X 形成的一种气体常用于漂 白和消毒, 下列有关说法可能错误的是( )
A. 含氧酸的酸性: W>Z
B. X 与 Y、Z、W 可分别形成两种或两种以上化合物
C. 简单氢化物沸点: X>Z
D. 简单离子半径: Y>Z>W>X
14. 下列物质的转化在给定条件下能实现的是( )
15. 下列说法正确的是( )
A. 电解法精炼镍时, 粗镍作阴极, 纯镍作阳极
B. 反应 4Fe(OH) (s)+2H O(l)+O (g)=4Fe(OH) (s) 常温下能自发进行, 该反应的
2 2 2 3
ΔH>0
c(HCO−)
C. 常温下 Na CO 溶液中加入少量 Ca(OH) 固体, 溶液中 3 值减小
2 3 2 c(CO2−)
3D. 在一容积可变的密闭容器中反应 2SO (g)+O (g)⇌2SO (g) 达平衡后, 保持温度不
2 2 3
c2 (SO )
3
变, 缩小体积,平衡正向移动, 的值增大
c2 (SO )⋅c(O )
2 2
16. Fe O (s) 与 CO(g) 主要发生如下反应:
3 4
① Fe O (s)+CO(g)⇌3FeO(s)+CO (g)ΔH =+19.3kJ⋅mol−1
3 4 2 1
② Fe O (s)+4CO(g)⇌3Fe(s)+4CO (g)ΔH
3 4 2 2
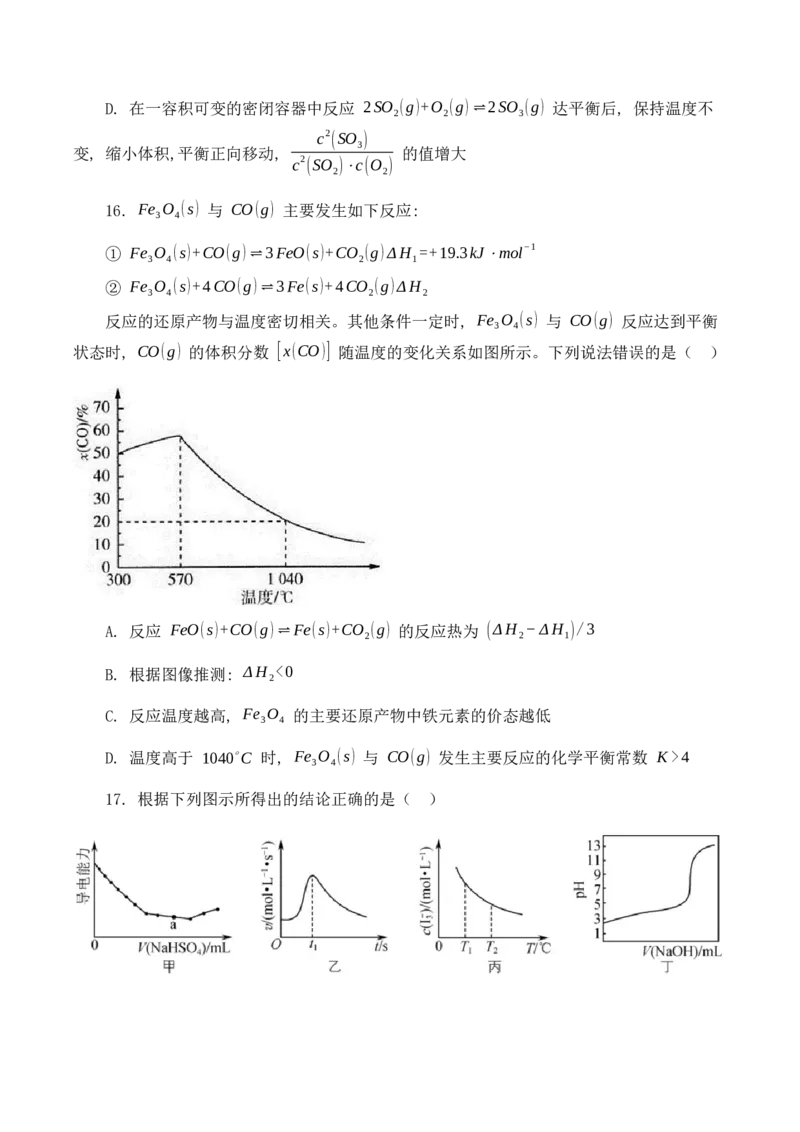
反应的还原产物与温度密切相关。其他条件一定时, Fe O (s) 与 CO(g) 反应达到平衡
3 4
状态时, CO(g) 的体积分数 [x(CO)] 随温度的变化关系如图所示。下列说法错误的是( )
A. 反应 FeO(s)+CO(g)⇌Fe(s)+CO (g) 的反应热为 (ΔH −ΔH )/3
2 2 1
B. 根据图像推测: ΔH <0
2
C. 反应温度越高, Fe O 的主要还原产物中铁元素的价态越低
3 4
D. 温度高于 1040∘C 时, Fe O (s) 与 CO(g) 发生主要反应的化学平衡常数 K>4
3 4
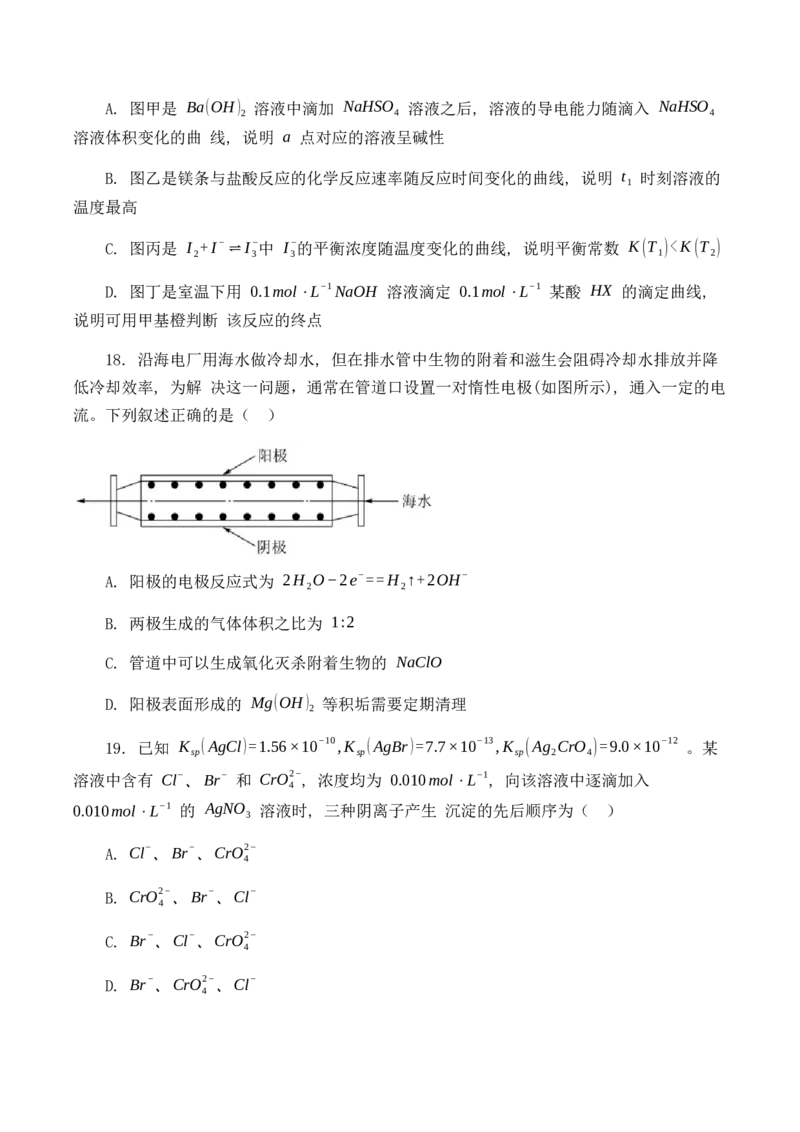
17. 根据下列图示所得出的结论正确的是( )A. 图甲是 Ba(OH) 溶液中滴加 NaHSO 溶液之后, 溶液的导电能力随滴入 NaHSO
2 4 4
溶液体积变化的曲 线, 说明 a 点对应的溶液呈碱性
B. 图乙是镁条与盐酸反应的化学反应速率随反应时间变化的曲线, 说明 t 时刻溶液的
1
温度最高
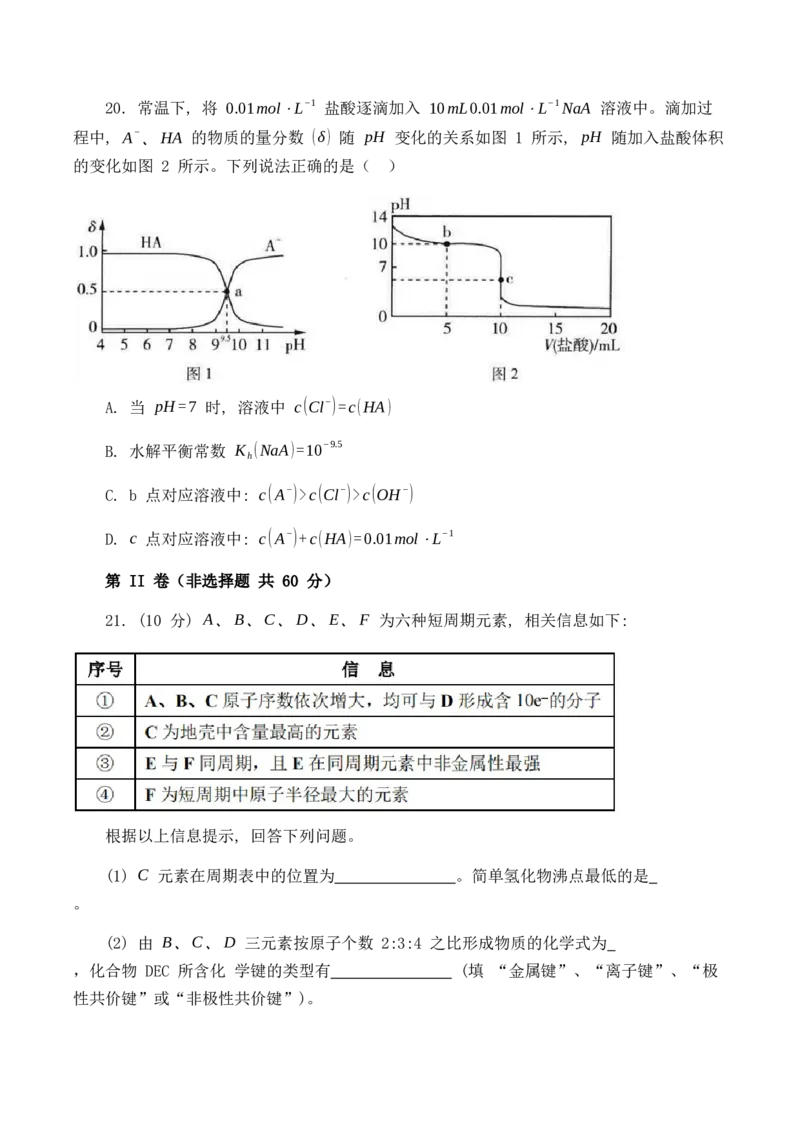
C. 图丙是 I +I− ⇌I−中 I−的平衡浓度随温度变化的曲线, 说明平衡常数 K(T )c(Cl−)>c(OH−)
D. c 点对应溶液中: c(A−)+c(HA)=0.01mol⋅L−1
第 II 卷(非选择题 共 60 分)
21. (10 分) A、B、C、D、E、F 为六种短周期元素, 相关信息如下:
根据以上信息提示, 回答下列问题。
(1) C 元素在周期表中的位置为 。简单氢化物沸点最低的是
。
(2) 由 B、C、D 三元素按原子个数 2:3:4 之比形成物质的化学式为
,化合物 DEC 所含化 学键的类型有 (填 “金属键”、“离子键”、“极
性共价键”或“非极性共价键”)。(3) 将 BD 通入到 FEC 溶液中可制得 B D 。该反应的离子方程式为
3 2 4
。
(4) 写出可使酸性高锰酸钾溶液褪色的 A 的含氧酸 (相对分子质量为 90 ) 的结构式
。
(5) 一种淡黄色固体 F C , 其电子式为 。该固体与硫酸亚铁溶液(按
2 2
物质的量之比为 1:1) 反应。反应过程中有气体生成, 则该反应的还原剂为
。
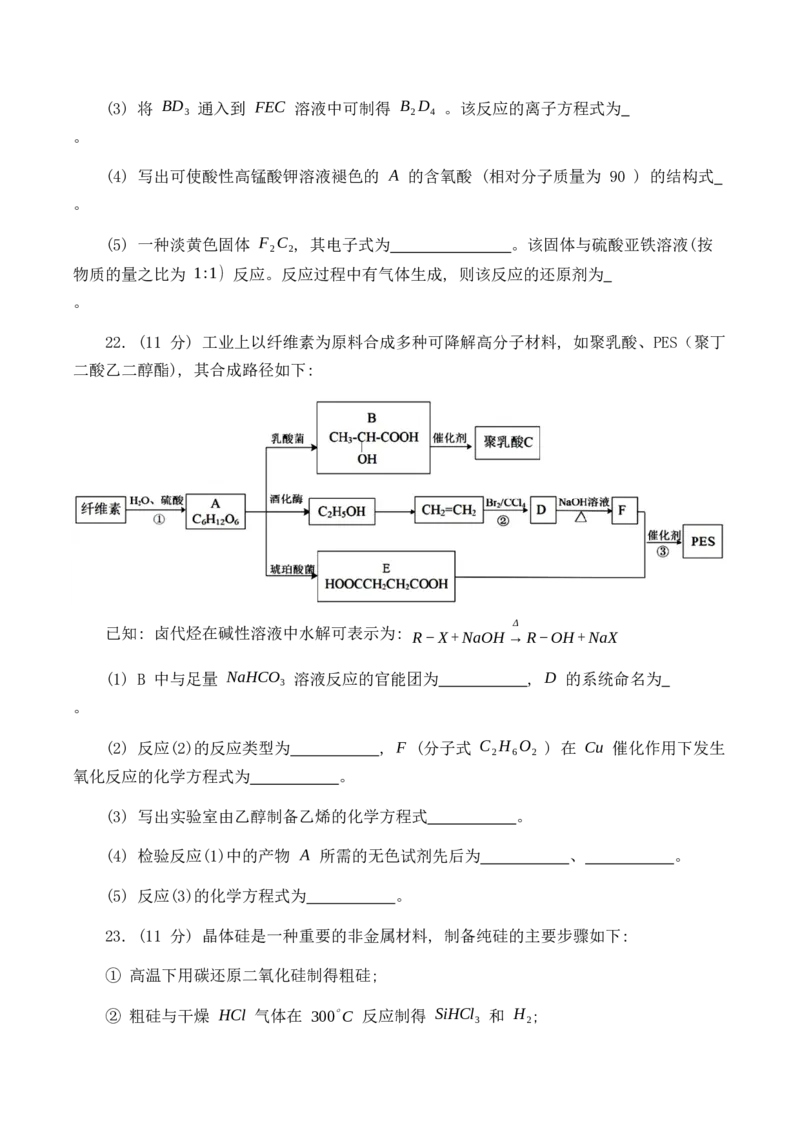
22. (11 分) 工业上以纤维素为原料合成多种可降解高分子材料, 如聚乳酸、PES(聚丁
二酸乙二醇酯), 其合成路径如下:
Δ
已知: 卤代烃在碱性溶液中水解可表示为: R−X+NaOH→R−OH+NaX
(1) B 中与足量 NaHCO 溶液反应的官能团为 , D 的系统命名为
3
。
(2) 反应(2)的反应类型为 , F (分子式 C H O ) 在 Cu 催化作用下发生
2 6 2
氧化反应的化学方程式为 。
(3) 写出实验室由乙醇制备乙烯的化学方程式 。
(4) 检验反应(1)中的产物 A 所需的无色试剂先后为 、 。
(5) 反应(3)的化学方程式为 。
23. (11 分) 晶体硅是一种重要的非金属材料, 制备纯硅的主要步骤如下:
① 高温下用碳还原二氧化硅制得粗硅;
② 粗硅与干燥 HCl 气体在 300∘C 反应制得 SiHCl 和 H ;
3 2③ SiHCl 与过量 H 在 1000∼1100∘C 反应制得纯硅。
3 2
(1) 第②步制备 SiHCl 的化学反应方程式为 。
3
(2) 整个制备过程必须严格控制无水无氧。 SiHCl 遇水剧烈反应生成 H SiO 、HCl
3 2 3
和另一种物质, 写出 配平的化学反应方程式 。
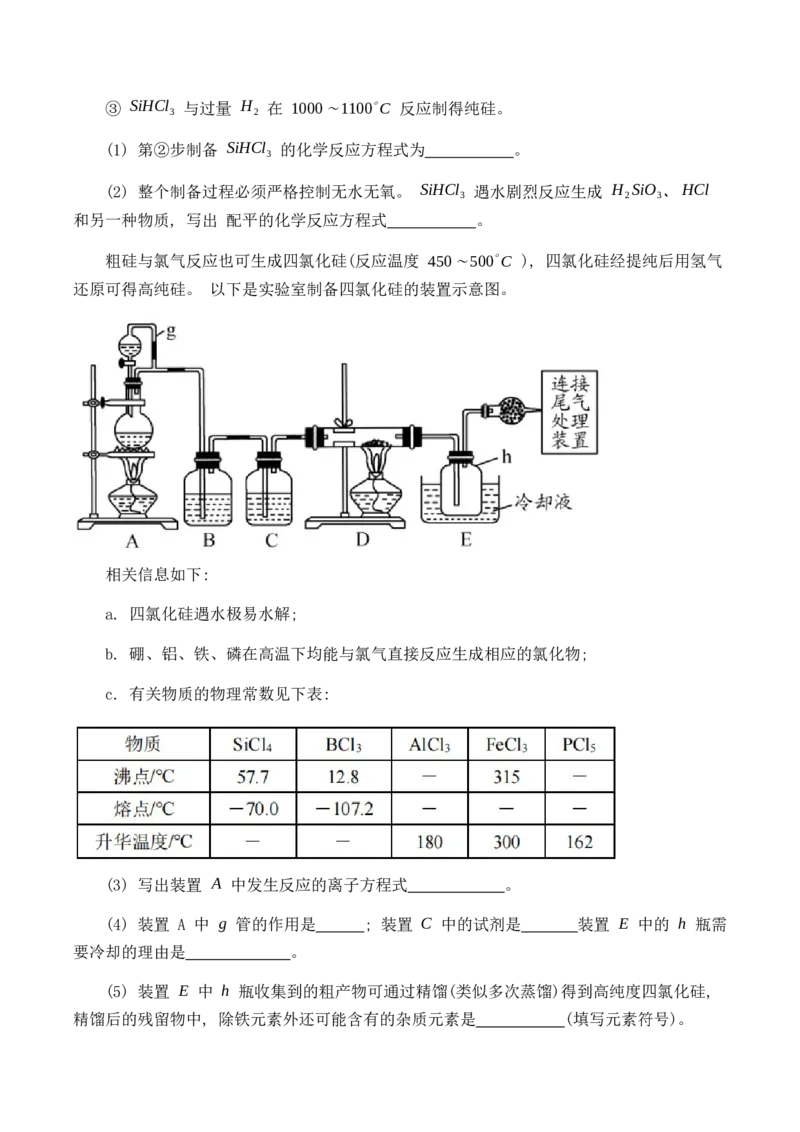
粗硅与氯气反应也可生成四氯化硅(反应温度 450∼500∘C ), 四氯化硅经提纯后用氢气
还原可得高纯硅。 以下是实验室制备四氯化硅的装置示意图。
相关信息如下:
a. 四氯化硅遇水极易水解;
b. 硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c. 有关物质的物理常数见下表:
(3) 写出装置 A 中发生反应的离子方程式 。
(4) 装置 A 中 g 管的作用是 ; 装置 C 中的试剂是 装置 E 中的 h 瓶需
要冷却的理由是 。
(5) 装置 E 中 h 瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,
精馏后的残留物中, 除铁元素外还可能含有的杂质元素是 (填写元素符号)。24. (8 分) (1) 二氧化氯 (ClO ) 是黄绿色、易溶于水的气体, 具有强氧化性, 可用于
2
烟气中 SO 和 NO 的脱 除。研究表明: ClO 氧化 SO 和 NO 的反应历程与下列反应有
2 2 2
关。
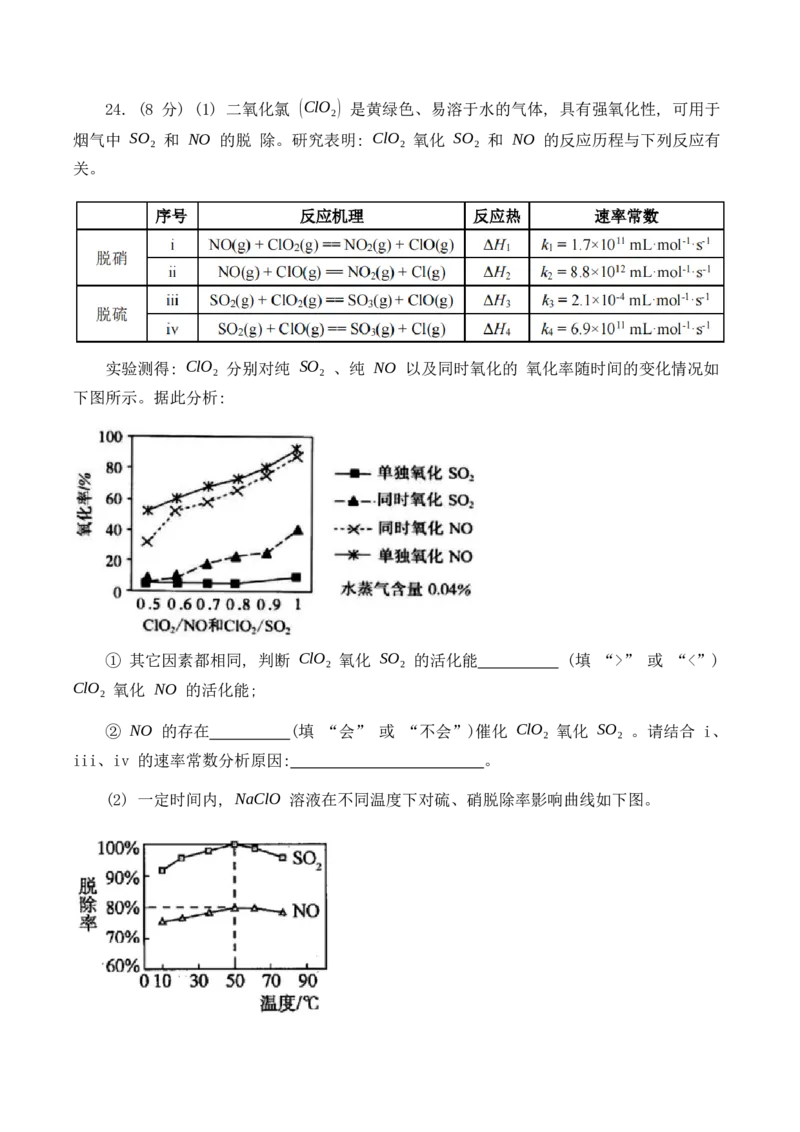
实验测得: ClO 分别对纯 SO 、纯 NO 以及同时氧化的 氧化率随时间的变化情况如
2 2
下图所示。据此分析:
① 其它因素都相同, 判断 ClO 氧化 SO 的活化能 (填 “>” 或 “<”)
2 2
ClO 氧化 NO 的活化能;
2
② NO 的存在 (填 “会” 或 “不会”)催化 ClO 氧化 SO 。请结合 i、
2 2
iii、iv 的速率常数分析原因: 。
(2) 一定时间内, NaClO 溶液在不同温度下对硫、硝脱除率影响曲线如下图。① SO 脱除率高于 NO, 可能的原因是 (写两条)。
2
② 烟气中 SO 和 NO 体积比为 4:1, 烟气与 50∘C 时的吸收液转化生成的
2
n(NO−):n(Cl−)= 。
3
25. (9 分) 以 Na SO 溶液和不同金属的硫酸盐溶液为实验对象, 探究盐的性质和盐
2 3
溶液间反应的多样性。
(1) 用离子方程式解释现象I: 。
(2) 经检验, 现象II的棕黄色沉淀中不含 SO2−, 含有 Cu+ 、Cu2+ 和 SO2− 。
4 3
已知: Cu+→
H+
Cu+Cu2+,Cu2+→
I−
CuI↓( 白色)+I 2 。
① 用稀硫酸证实沉淀中含有 Cu+的实验现象是 。
② 通过下列实验证实, 沉淀中含有 Cu2+ 和 SO2− : 将洗净的棕黄色沉淀中加入 KI 溶
3
液, 产生白色沉淀, 取上层清液分成两份, 一份加入淀粉溶液, 无明显现象, 另一份加入
, 产生 BaSO 白色沉淀。
4
(3) 已知: Al (SO ) 在水溶液中不存在。经检验, 现象III的白色沉淀中无 SO2−, 该
2 3 3 4
白色沉淀既能溶于 强酸, 又能溶于强碱, 还可使酸性 KMnO 溶液褪色。
4
①推测沉淀中含有亚硫酸根和 。
②对于沉淀中亚硫酸根的存在形式提出两种假设: i. 被 Al(OH) 所吸附; ii. 存在于
3
铝的碱式盐中。 对假设 ii 设计了对比实验, 证实了假设 ii 成立。将对比实验方案补充完
整:假设 ii 成立的实验证据是 。
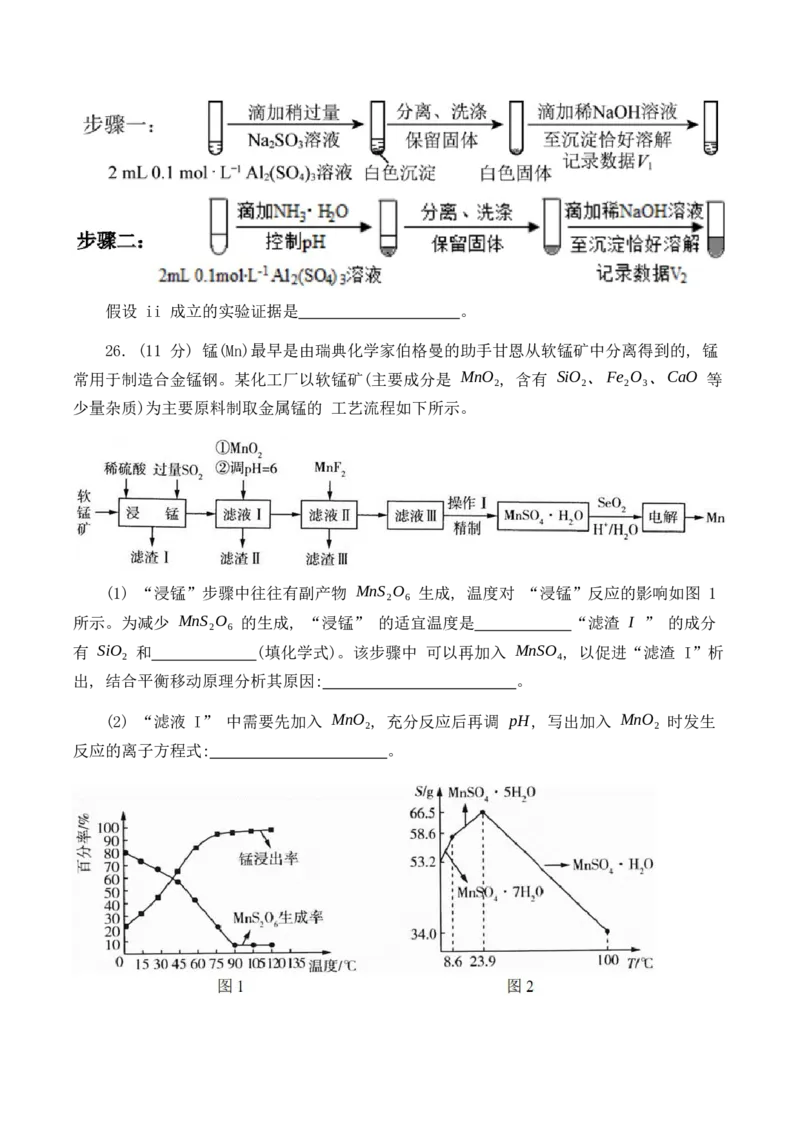
26. (11 分) 锰(Mn)最早是由瑞典化学家伯格曼的助手甘恩从软锰矿中分离得到的, 锰
常用于制造合金锰钢。某化工厂以软锰矿(主要成分是 MnO , 含有 SiO 、Fe O 、CaO 等
2 2 2 3
少量杂质)为主要原料制取金属锰的 工艺流程如下所示。
(1) “浸锰”步骤中往往有副产物 MnS O 生成, 温度对 “浸锰”反应的影响如图 1
2 6
所示。为减少 MnS O 的生成, “浸锰” 的适宜温度是 “滤渣 I ” 的成分
2 6
有 SiO 和 (填化学式)。该步骤中 可以再加入 MnSO , 以促进“滤渣 I”析
2 4
出, 结合平衡移动原理分析其原因: 。
(2) “滤液 I” 中需要先加入 MnO , 充分反应后再调 pH, 写出加入 MnO 时发生
2 2
反应的离子方程式: 。(3) “滤液 II” 中加入 MnF 的目的是进一步除去溶液中的 Ca2+, 已知 25∘C 时
2
K (CaF )=3.2×10−11, 则常温下 CaF 在纯水中的溶解度为 g/100gH O
sp 2 2 2 。
(4) 由 “滤液III” 可制得 MnSO ⋅H O, 已知硫酸锰在不同温度下的溶解度和析出
4 2
晶体的组成如图 2 所示。则从“滤液III”中获得较高纯度 MnSO ⋅H O 的“操作 I ”为
4 2
控制温度在 80−90∘C 蒸发结晶、 、用 80-90°C蒸馏水洗涤 2 3 次、真空干
燥。
(5) 电解时加入适量的 SeO 有利于 Mn 在电极上析出, SeO 与水反应生成的
2 2
H SeO (二元弱酸)在阴极 放电生成 Se 单质(对 Mn2+ 有特殊的吸附能力, 有利于 Mn2+
2 3
电还原沉积), 该电极反应为 。下载最新免费模拟卷,到公众号:一枚试卷君