文档内容
重庆八中 2022–2023 学年度高三入学考试
化学试题
命题:蒋小明 李小虎 审题:王宇轩 何远华 打印:李小虎 校对:李小虎
可能用到的相对原子质量D-2N-14O−16Na−23P−31Cl−35.5Fe−56
Co-59
第I卷(共42分)
一、选择题:本大题共14个小题,每小题3分,共42分。每小题只有一个选项符合题目要
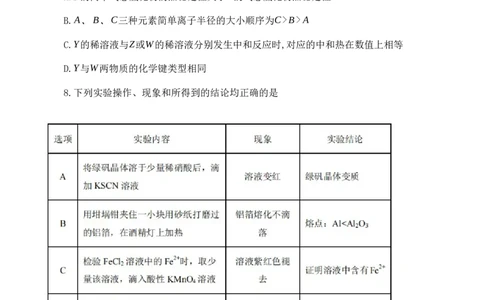
求。
1.化学与人类生活、社会可持续发展密切相关,下列说法错误的是
A.中国天眼传输信息用的光纤材料是硅
B.误食重金属盐会引起人体中毒,可以喝大量生牛奶解毒
C.漂粉精既可作棉、麻、纸张的漂白剂,又可用作泳池及环境的消毒剂
D.长征五号火箭的箭体蒙皮材料2219-铝合金,可一定程度上减轻火箭的质量
2.下列化学语言正确的是
CCl
4
A. 的比例模型:
B.有机物 的名称:2-二甲基丁烷
C.甲醛的结构式:
Mg2+
D. 结构示意图:
3.常温下,下列各组离子一定能在指定溶液中大量共存的是A.0.1mol/L的NH HCO 溶液中:K+ 、Al3+ 、NO ❑ −、Cl−B.K /c(H+)=10−13的溶液中:
4 3 3 w
NH+ 、Na+ 、Cu2+ 、Cl−
4
C.与Al反应能放出H 的溶液中:Cu2+ 、K+ 、NO −、SO 2−
2 3 4
D.由水电离产生的c(H+)=10−12mol/L的溶液中:Na+ 、Cl−、SO 2−、S2−
3
4.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,20gD O+ 中含有10N 个电子
3 A
B.标况下,2.24LCCl 所含共价键的数目是0.4N
4 A
C.0.1molN与足量的H 充分反应,生成NH 分子的数目为0.2N
2 3 A
D.100mLpH=1的H SO 和HCl的混合溶液中,H+的数目是0.01N
2 4 A
5.有机物M的分子式为C H O ,且能与NaHCO 溶液反应放出CO 气体,1molM与足量金
5 10 3 3 2
属钠反应可生成1molH ,则M可能的结构种类的数目为
2
A.9种
B.10种
C.12种
D.14种
6.下列事实一定能说明HA是弱酸的是
A.常温下,NaA溶液的pH大于7
B.HA能与Na CO 溶液反应,产生CO 气体
2 3 2
C.1mol⋅L−1HA的水溶液能使紫色石芯溶液变红
D.用HA溶液做导电性实验,灯光很暗
7.已知短周期元素A、B、C、D、E的最高价氧化物对应的水化物分别为
X、Y、M、Z、W ,B是短周期主族元素中原子半径最大的元素,常温下X、Y、Z、W均可
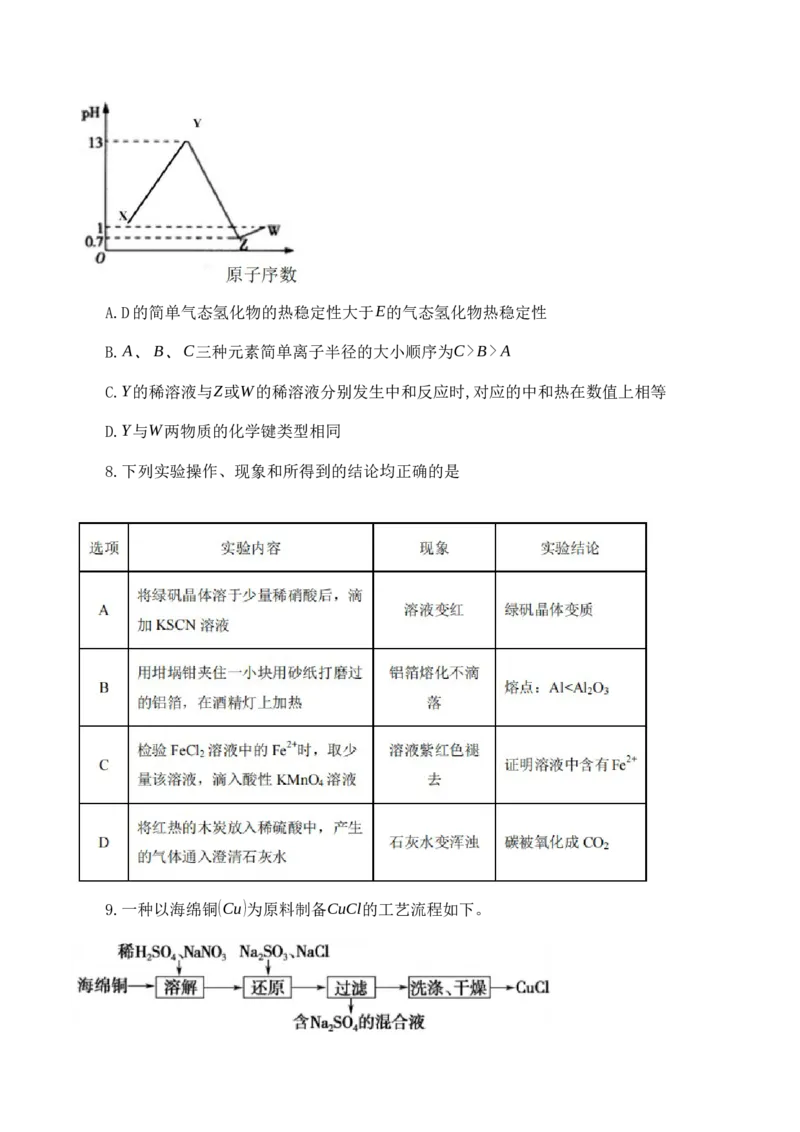
与M反应,A、B、D、E的原子序数及其对应0.1mol/LX、Y、Z、W溶液的pH如图所示。
下列说法正确的是A.D的简单气态氢化物的热稳定性大于E的气态氢化物热稳定性
B.A、B、C三种元素简单离子半径的大小顺序为C>B>A
C.Y的稀溶液与Z或W的稀溶液分别发生中和反应时,对应的中和热在数值上相等
D.Y与W两物质的化学键类型相同
8.下列实验操作、现象和所得到的结论均正确的是
9.一种以海绵铜(Cu)为原料制备CuCl的工艺流程如下。已知:CuCl白色粉末,微溶于水,不溶于乙醇,在潮湿的空气中易被氧化。下列说法错误是
A.“溶解”时可用热空气或H O 代替NaNO
2 2 3
B.“过滤”用到的玻璃仪器有漏斗、烧杯、玻璃棒
C.“还原”时发生的离子反应为:2Cu2++SO 2−+2Cl−+2OH−
3
=2CuCl↓+SO 2−+H O
4 2
D.为提高CuCl的产率和纯度,可采用乙醇洗涤、真空干燥
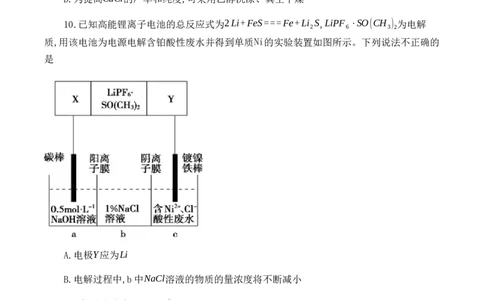
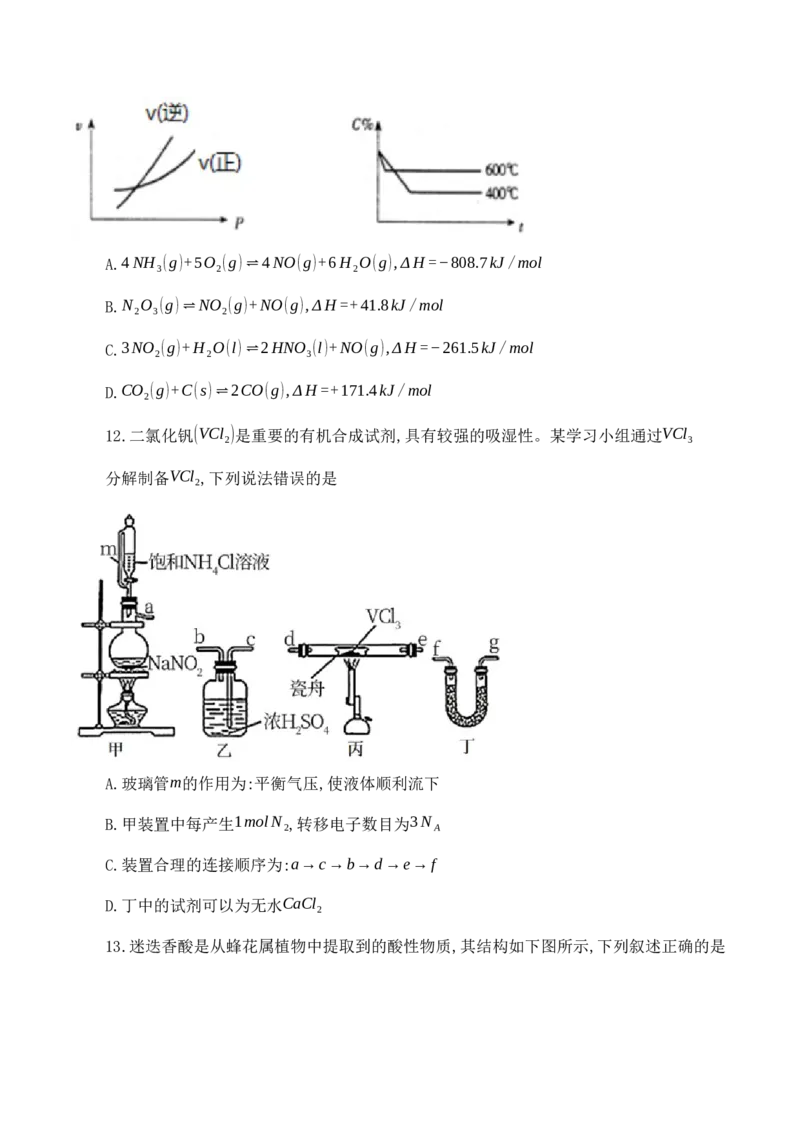
10.已知高能锂离子电池的总反应式为2Li+FeS===Fe+Li S,LiPF ⋅SO(CH ) 为电解
2 6 3 2
质,用该电池为电源电解含铂酸性废水并得到单质Ni的实验装置如图所示。下列说法不正确的
是
A.电极Y应为Li
B.电解过程中,b中NaCl溶液的物质的量浓度将不断减小
C.X极反应式为FeS+2Li++2e−===Fe+Li S
2
D.若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
11.下图中,C%表示某反应物在体系中的百分含量,同时符合以下两图像的反应是A.4NH (g)+5O (g)⇌4NO(g)+6H O(g),ΔH=−808.7kJ/mol
3 2 2
B.N O (g)⇌NO (g)+NO(g),ΔH=+41.8kJ/mol
2 3 2
C.3NO (g)+H O(l)⇌2HNO (l)+NO(g),ΔH=−261.5kJ/mol
2 2 3
D.CO (g)+C(s)⇌2CO(g),ΔH=+171.4kJ/mol
2
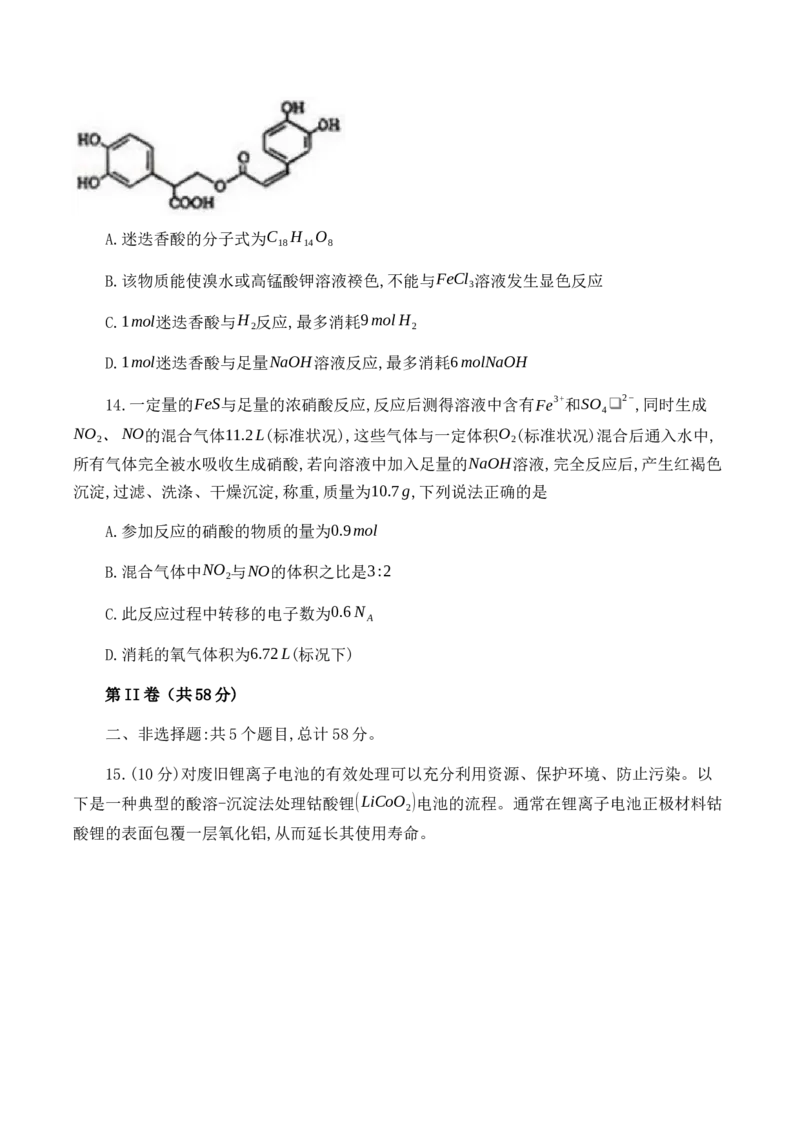
12.二氯化钒(VCl )是重要的有机合成试剂,具有较强的吸湿性。某学习小组通过VCl
2 3
分解制备VCl ,下列说法错误的是
2
A.玻璃管m的作用为:平衡气压,使液体顺利流下
B.甲装置中每产生1molN ,转移电子数目为3N
2 A
C.装置合理的连接顺序为:a→c→b→d→e→f
D.丁中的试剂可以为无水CaCl
2
13.迷迭香酸是从蜂花属植物中提取到的酸性物质,其结构如下图所示,下列叙述正确的是A.迷迭香酸的分子式为C H O
18 14 8
B.该物质能使溴水或高锰酸钾溶液䙆色,不能与FeCl 溶液发生显色反应
3
C.1mol迷迭香酸与H 反应,最多消耗9molH
2 2
D.1mol迷迭香酸与足量NaOH溶液反应,最多消耗6molNaOH
14.一定量的FeS与足量的浓硝酸反应,反应后测得溶液中含有Fe3+和SO
❑
2−,同时生成
4
NO 、NO的混合气体11.2L(标准状况),这些气体与一定体积O (标准状况)混合后通入水中,
2 2
所有气体完全被水吸收生成硝酸,若向溶液中加入足量的NaOH溶液,完全反应后,产生红褐色
沉淀,过滤、洗涤、干燥沉淀,称重,质量为10.7g,下列说法正确的是
A.参加反应的硝酸的物质的量为0.9mol
B.混合气体中NO 与NO的体积之比是3:2
2
C.此反应过程中转移的电子数为0.6N
A
D.消耗的氧气体积为6.72L(标况下)
第II卷(共58分)
二、非选择题:共5个题目,总计58分。
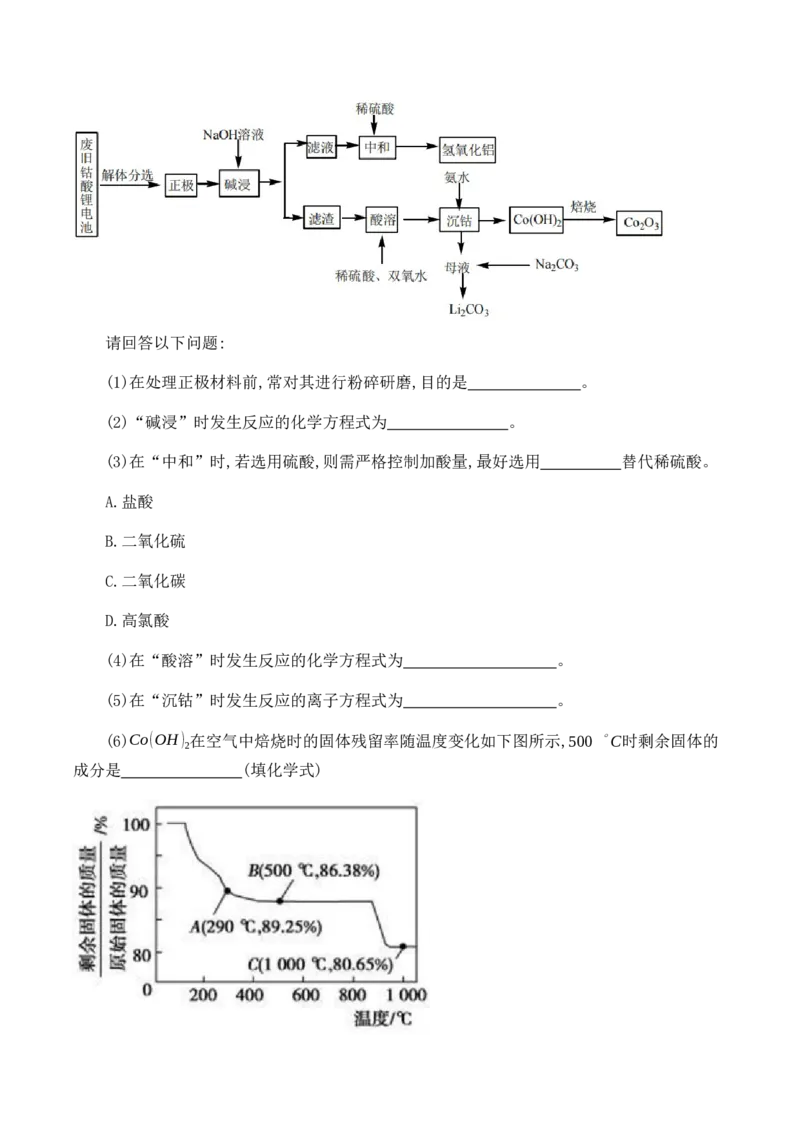
15.(10分)对废旧锂离子电池的有效处理可以充分利用资源、保护环境、防止污染。以
下是一种典型的酸溶-沉淀法处理钴酸锂(LiCoO )电池的流程。通常在锂离子电池正极材料钴
2
酸锂的表面包覆一层氧化铝,从而延长其使用寿命。请回答以下问题:
(1)在处理正极材料前,常对其进行粉碎研磨,目的是 。
(2)“碱浸”时发生反应的化学方程式为 。
(3)在“中和”时,若选用硫酸,则需严格控制加酸量,最好选用 替代稀硫酸。
A.盐酸
B.二氧化硫
C.二氧化碳
D.高氯酸
(4)在“酸溶”时发生反应的化学方程式为 。
(5)在“沉钴”时发生反应的离子方程式为 。
(6)Co(OH) 在空气中焙烧时的固体残留率随温度变化如下图所示,500 ∘C时剩余固体的
2
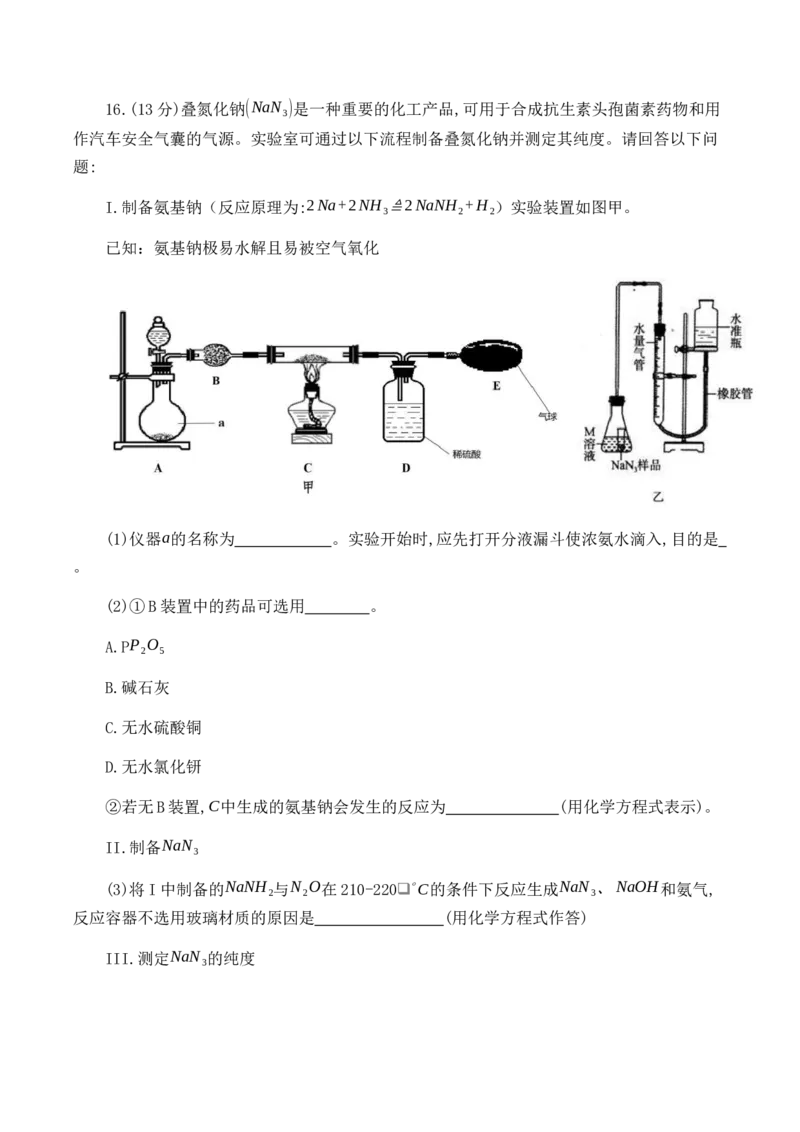
成分是 (填化学式)16.(13分)叠氮化钠(NaN )是一种重要的化工产品,可用于合成抗生素头孢菌素药物和用
3
作汽车安全气囊的气源。实验室可通过以下流程制备叠氮化钠并测定其纯度。请回答以下问
题:
I.制备氨基钠(反应原理为:2Na+2NH ≜2NaNH +H )实验装置如图甲。
3 2 2
已知:氨基钠极易水解且易被空气氧化
(1)仪器a的名称为 。实验开始时,应先打开分液漏斗使浓氨水滴入,目的是
。
(2)①B装置中的药品可选用 。
A.PP O
2 5
B.碱石灰
C.无水硫酸铜
D.无水氯化钘
②若无B装置,C中生成的氨基钠会发生的反应为 (用化学方程式表示)。
II.制备NaN
3
(3)将I中制备的NaNH 与N O在210-220❑∘C的条件下反应生成NaN 、NaOH和氨气,
2 2 3
反应容器不选用玻璃材质的原因是 (用化学方程式作答)
III.测定NaN 的纯度
3精确称量0.1500gNaN 样品,设计如图乙所示装置,连接好装置后使雉形瓶倾斜,使小试管
3
中的NaN 样品与M溶液接触,测量产生的气体体积从而测定其纯度(不考虑溶剂的挥发)。
3
已知:2NaN ∼3N (其他产物略),反应中放出大量的热。
3 2
(4)对量气管读数时,反应前后都需要进行的操作是 。
(5)常温下测得产生气体的体积为54.00mL(N 的密度为1.400g/L),计算NaN 样品的纯度
2 3
为 。(保留三位有效数字)
17.(14分)利用化学反应原理分析指导工业生产具有重要的现实意义。
I.工业合成氨的反应原理为:X(g)+3Y(g)⇌2Z(g)ΔH<0,T ❑∘C时在容积为4L的恒容密
1
闭容器中通入2molX和6molY发生反应。
(1)5min时反应达到平衡状态,气体总物质的量为6.4mol,求:
①达平衡时X(g)的转化率为 ,0∼5min内该反应的平均速率v(Y)=
;
②相同条件下,改变反应物的起始通入量,某时刻测得X、Y、Z的物质的量分别为2mol
、3.6mol、2mol,则此时反应v v (填“>”、“<”、或“=”);
正 逆
(2)对于该反应,既可以提高平衡体系中Z的百分含量,又能加快反应速率的措施
是 (填序号);
a.升高温度
b.将平衡体系中的Z(g)分离出来
c.向平衡体系中再通入一定量Z(g)
d.通入一定量氦气以增大体系压强
e.改为在恒压容器中进行反应
f.加入合适的催化剂
II.工业上以CO 、H 为原料合成CH OH的反应原理为:
2 2 3
CO (g)+3H (g)⇌CH OH(g)+H O(g)ΔH=−49.5kJ⋅mol−1,该反应由两个分步反应构成:
2 2 3 2
第一步:CO (g)+H (g)⇌CO(g)+H O(g)ΔH =+40.9kJ⋅mol−1
2 2 2 1第二步:CO(g)+2H (g)⇌CH OH(g)ΔH =−90.4kJ⋅mol−1
2 3 2
回答下列问题:
(1)一定条件下,向体积为2L的恒容密闭容器中通入1molCO 和3molH 合成CH OH,反
2 2 3
应达到平衡时,容器中CH OH(g)为0.4mol,CO为0.2mol,此时H O(g)的浓度为 mol⋅L−1
3 2
,第二步反应的平衡常数K= 。
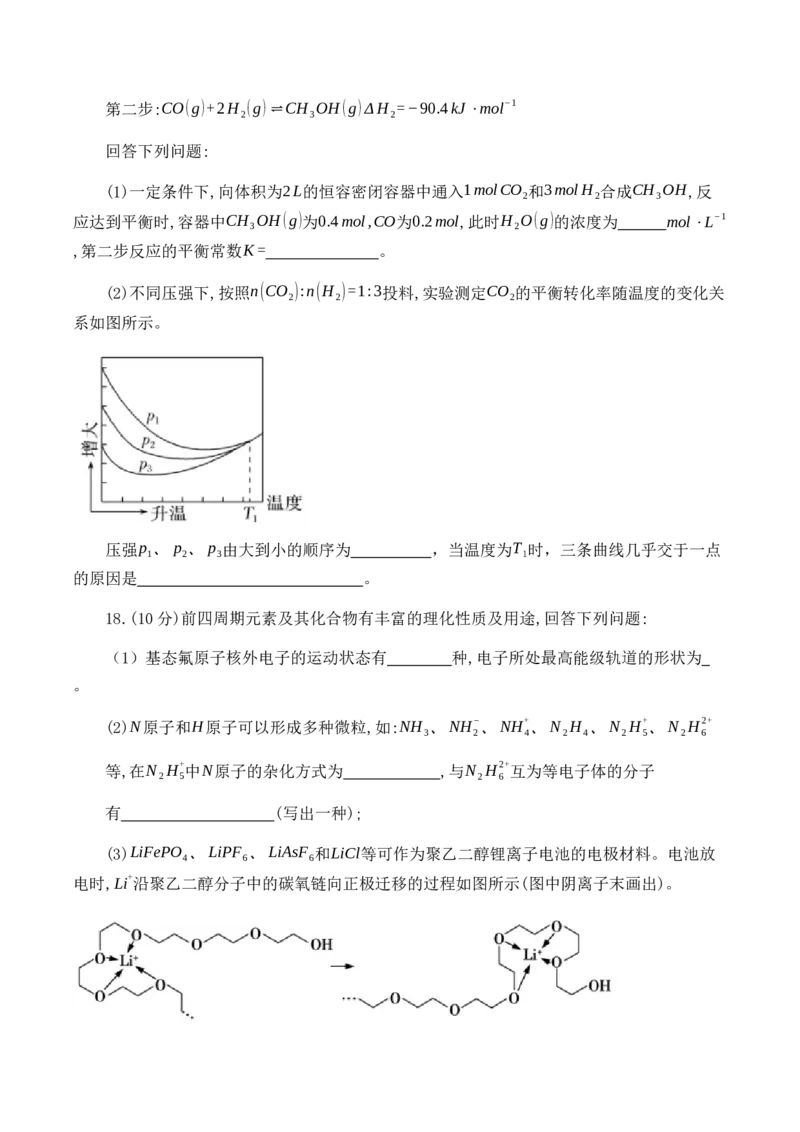
(2)不同压强下,按照n(CO ):n(H )=1:3投料,实验测定CO 的平衡转化率随温度的变化关
2 2 2
系如图所示。
压强p 、p 、p 由大到小的顺序为 ,当温度为T 时,三条曲线几乎交于一点
1 2 3 1
的原因是 。
18.(10分)前四周期元素及其化合物有丰富的理化性质及用途,回答下列问题:
(1)基态氟原子核外电子的运动状态有 种,电子所处最高能级轨道的形状为
。
(2)N原子和H原子可以形成多种微粒,如:NH 、NH−、NH+ 、N H 、N H+ 、N H2+
3 2 4 2 4 2 5 2 6
等,在N H+ 中N原子的杂化方式为 ,与N H2+互为等电子体的分子
2 5 2 6
有 (写出一种);
(3)LiFePO 、LiPF 、LiAsF 和LiCl等可作为聚乙二醇锂离子电池的电极材料。电池放
4 6 6
电时,Li+沿聚乙二醇分子中的碳氧链向正极迁移的过程如图所示(图中阴离子末画出)。相同条件下,电极材料 (填“LiPF ”或“LiAsF ”)中的Li+迁移较快,原因
6 6
是: 。
(4)PCl 能形成离子晶体,该晶体的立方晶胞如图所示:
5
若晶胞边长为apm,N 为阿伏加德罗常数的值,则该晶体的密度为
A
g⋅cm−3
(写出计算式即可)。
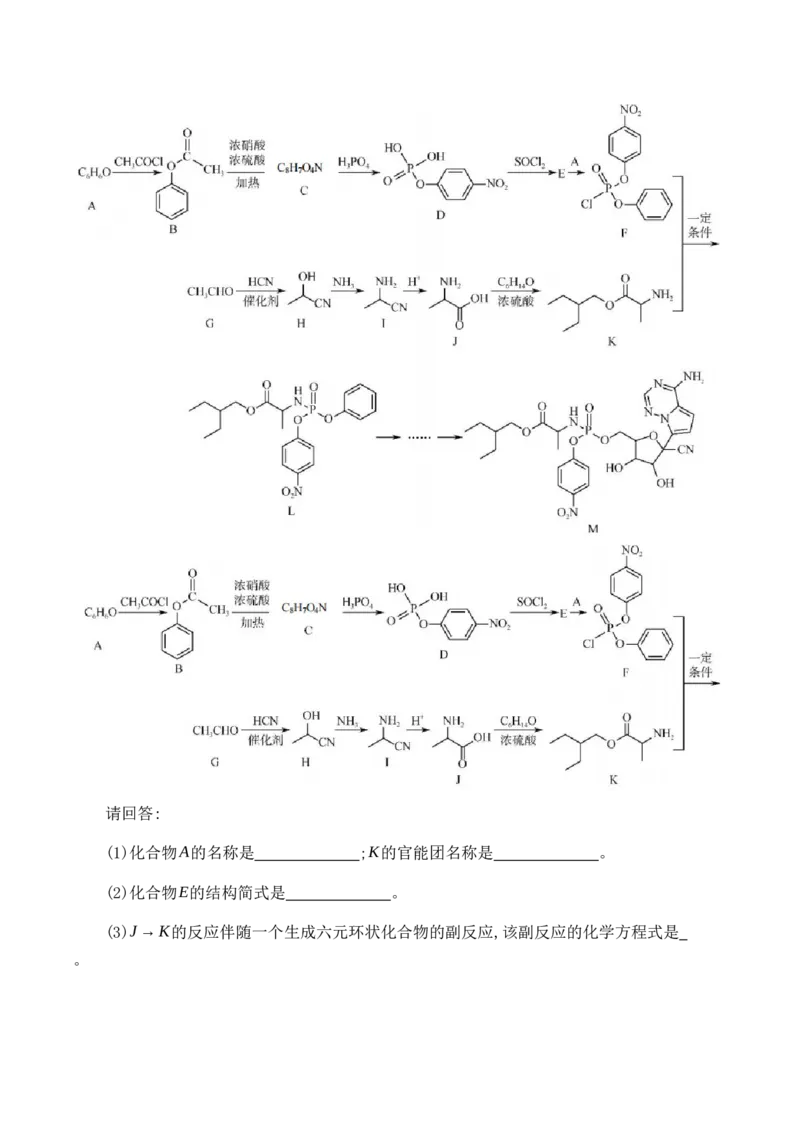
19.(11分)瑞德西韦是一种抗病毒药物,某课题组通过如下合成路线合成(部分条件省
略):请回答:
(1)化合物A的名称是 ;K的官能团名称是 。
(2)化合物E的结构简式是 。
(3)J→K的反应伴随一个生成六元环状化合物的副反应,该副反应的化学方程式是
。(4)B的同分异构体中属于芳香化合物的且能发生银镜反应,苯环上只有二个取代基的
种类有 种。
(5)写出同时符合下列条件的化合物C的同分异构体的结构简式(不包括立体异构体)
①包含苯环;②包含-COOH、−NO ;③苯环上含有两种不同环境的氢
2下载最新免费模拟卷,到公众号:一枚试卷君