文档内容
专练 26 元素位-构-性综合推断
一、单项选择题
1.[2022·湖南卷]科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W
为原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法
错误的是( )
A.原子半径:X>Y>Z
B.非金属性:Y>X>W
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族
2.[2022·河北唐山考试]W、N、X、Y、Z是原子序数依次增大的短周期主族元素。Y
所处的周期序数与族序数相等。甲、乙、丙、丁、戊是由这些元素组成的化合物,丁是氯
碱工业的一种产物,戊为二元化合物,常温下0.01 mol·L-1戊溶液的pH为2。上述物质的
转化关系如图所示。下列说法错误的是( )
A.原子半径:NY>Z>X
B.W,Y分別与X元素形成的简单化合物的沸点:Y>W
C.ZY和ZX都只存在离子键
2
D.v能抑制水的电离,u能促进水的电离4.已知A、B、C、D为短周期元素组成的四种物质,且D为强电解质。在一定条件下
有如下转化关系:A――→B――→C――→D(其他相关物质可能省略)。下列说法不正
确的是( )
A.A不可能为碳单质
B.若A为金属单质,则 A 一定位于第三周期第ⅠA族
C.若常温下D的浓溶液能使铁、铝钝化,则A可能是单质,也可能是化合物
D.若A是共价化合物,A的水溶液一定显碱性
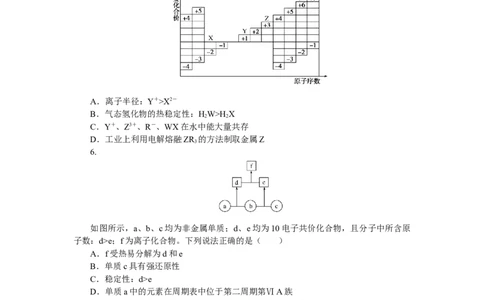
5.[2022·北京朝阳质检]如图是部分短周期元素主要化合价与原子序数的关系图,X、
Y、Z、W、R是其中的五种元素。下列说法正确的是( )
A.离子半径:Y+>X2-
B.气态氢化物的热稳定性:HW>H X
2 2
C.Y+、Z3+、R-、WX在水中能大量共存
D.工业上利用电解熔融ZR 的方法制取金属Z
3
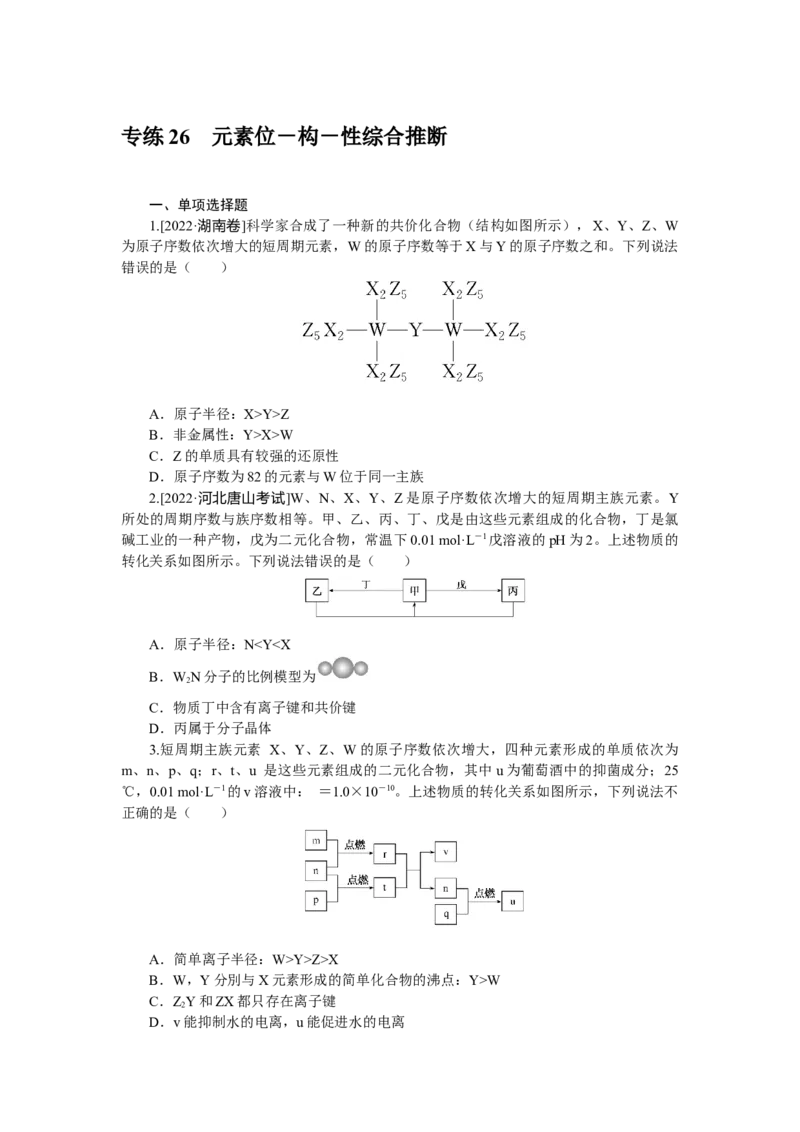
6.
如图所示,a、b、c均为非金属单质;d、e均为10电子共价化合物,且分子中所含原
子数:d>e;f为离子化合物。下列说法正确的是( )
A.f受热易分解为d和e
B.单质c具有强还原性
C.稳定性:d>e
D.单质a中的元素在周期表中位于第二周期第ⅥA族
7.短周期主族元素X、Y、Z、W的原子序数依次增大,X是地壳中含量最多的元素,
Y原子的最外层有2个电子,Z的单质晶体是应用最广泛的半导体材料,W与X位于同一
主族。下列说法正确的是( )
A.原子半径:r(W)>r(Z)>r(Y)>r(X)
B.由X、Y组成的化合物是离子化合物
C.Z的最高价氧化物对应水化物的酸性比W的强
D.W的简单气态氢化物的热稳定性比X的强
8.a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次
外层的电子数相同;c所在周期数与族数相同;d与a同族,下列叙述正确的是( )
A.原子半径:d>c>b>aB.4种元素中b的金属性最强
C.c的氧化物的水化物是强碱
D.d单质的氧化性比a单质的氧化性强
二、不定项选择题
9.有M、A、B、D、N、E六种短周期元素原子序数依次增大,M元素的单质是自然界
最轻的气体,N元素的原子半径是所在周期中最大的,A、B、D、E四种元素在周期表中
的相应位置如下图,它们的原子序数之和为37。下列说法不正确的是( )
A.沸点:MD>BM>AM
2 3 4
B.原子半径:r >r >r >r
E A B D
C.化合物AM 分子中既含有极性键又含有非极性键
n 2n
D.B元素的氢化物与D元素的单质在一定条件下能发生置换反应,且氧化剂与还原剂
的物质的量之比为4∶3
10.
[2022·全国百强校郑州一中高三摸底测试]已知X、Y、Z、W、M均为短周期元素。25
℃时,其最高价氧化物对应的水化物(浓度均为0.01 mol·L-1)溶液的pH 和原子半径的关
系如图所示。下列说法不正确的是( )
A.X、M简单离子半径大小顺序:Xd>c
B.a、c形成的化合物一定是共价化合物
C.W、X、Y中X的熔沸点最高
D.Y、Z均可用排水法收集
三、非选择题
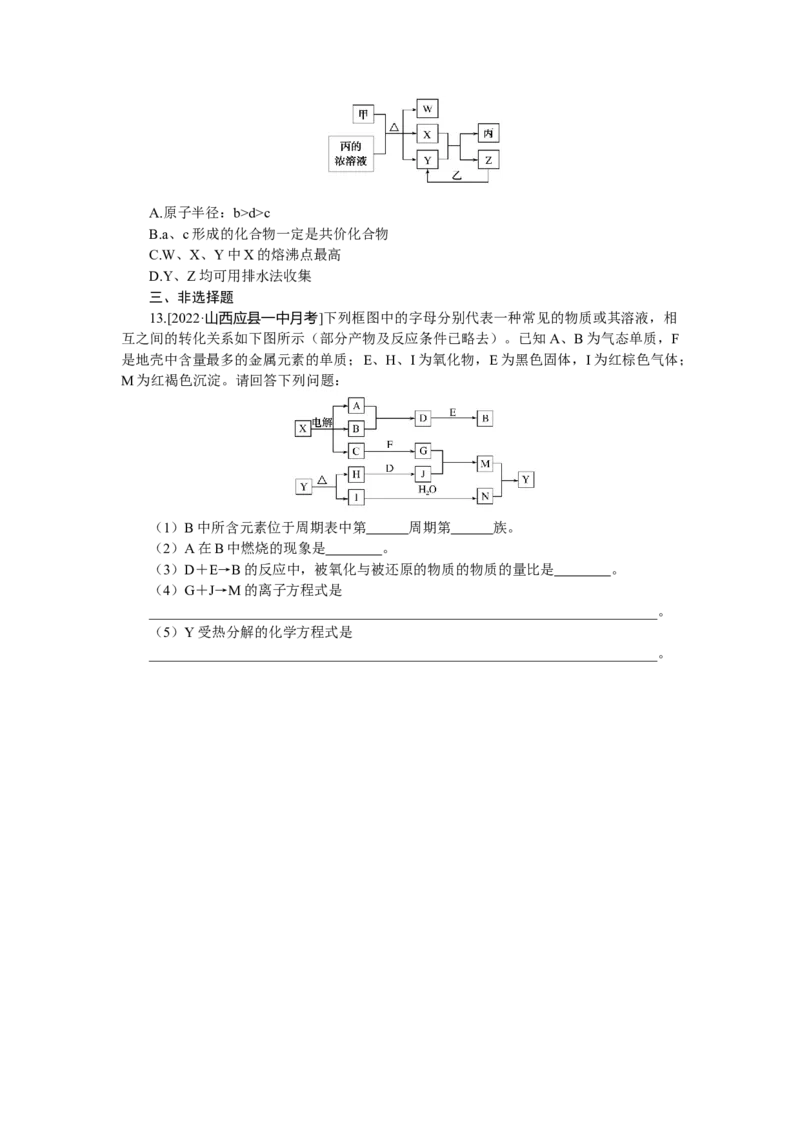
13.[2022·山西应县一中月考]下列框图中的字母分别代表一种常见的物质或其溶液,相
互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F
是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;
M为红褐色沉淀。请回答下列问题:
(1)B中所含元素位于周期表中第 周期第 族。
(2)A在B中燃烧的现象是 。
(3)D+E→B的反应中,被氧化与被还原的物质的物质的量比是 。
(4)G+J→M的离子方程式是
________________________________________________________________________。
(5)Y受热分解的化学方程式是
________________________________________________________________________。