文档内容
专练 27 化学反应中的能量变化及图像
1.[2022·安徽皖南八校联考]将盛有NH HCO 粉末的小烧杯放入盛有少量冰醋酸的大
4 3
烧杯中。然后向小烧杯中加入盐酸,反应剧烈,大烧杯中的冰醋酸逐渐凝固。下列有关小
烧杯中发生的反应的说法正确的是( )
A.该反应是放热反应
B.该反应过程中,吸收的热能转化为产物内部的能量
C.该反应的反应物的总能量高于生成物的总能量
D.该反应中化学键断裂吸收的能量比化学键形成放出的能量少
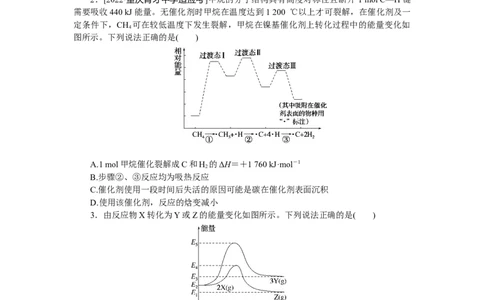
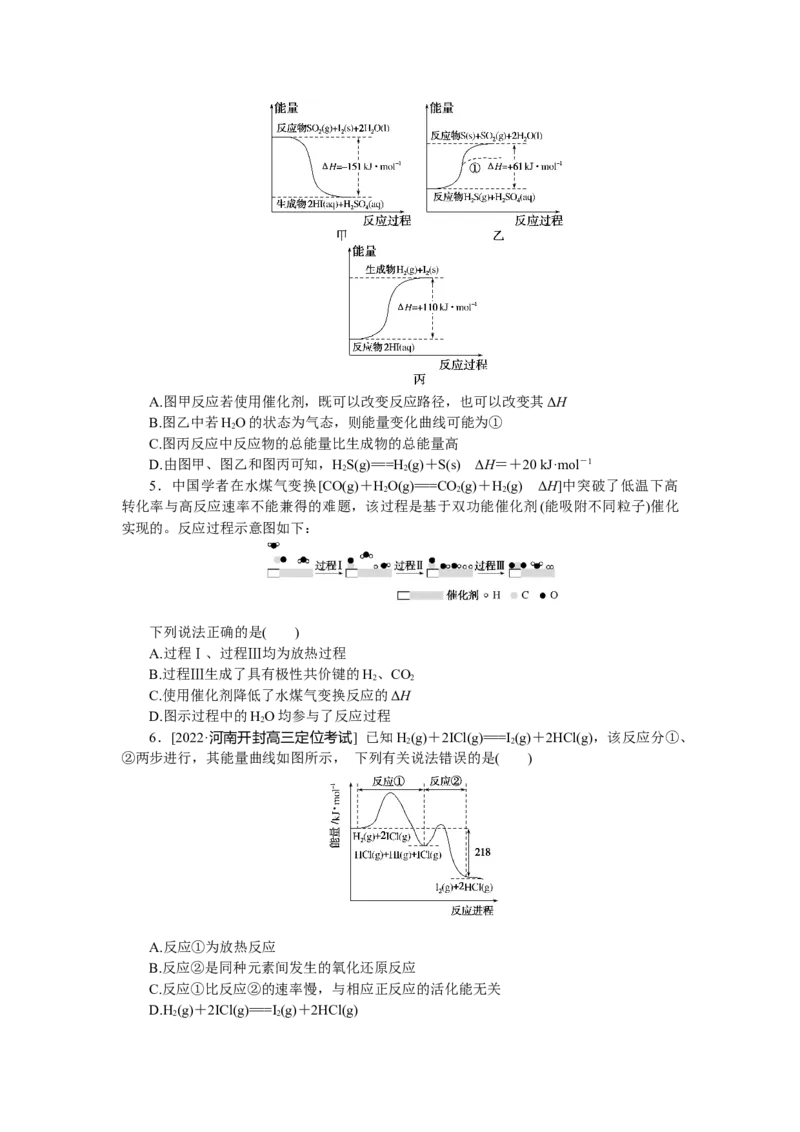
2.[2022·重庆育才中学适应考]甲烷的分子结构具有高度对称性且断开1 mol C—H键
需要吸收440 kJ能量。无催化剂时甲烷在温度达到1 200 ℃以上才可裂解,在催化剂及一
定条件下,CH 可在较低温度下发生裂解,甲烷在镍基催化剂上转化过程中的能量变化如
4
图所示。下列说法正确的是( )
A.1 mol甲烷催化裂解成C和H 的ΔH=+1 760 kJ·mol-1
2
B.步骤②、③反应均为吸热反应
C.催化剂使用一段时间后失活的原因可能是碳在催化剂表面沉积
D.使用该催化剂,反应的焓变减小
3.由反应物X转化为Y或Z的能量变化如图所示。下列说法正确的是( )
A.2X(g)===Z(g) ΔH=E-E
2 1
B.反应2X(g)===3Y(g)的活化能=E-E
3 2
C.2X(g)===Z(s) ΔHX(g)>Y(g)
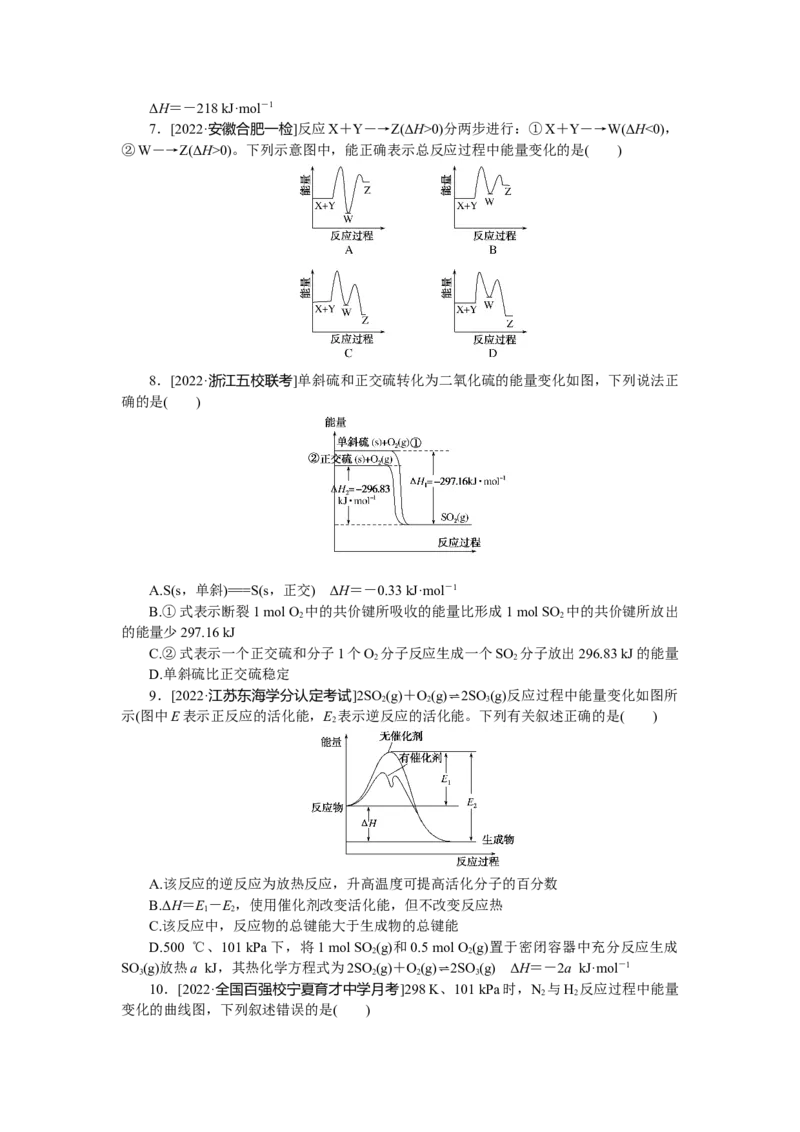
4.[2022·北京朝阳区期中]热化学硫碘循环分解硫化氢联产氢气、硫黄是能源研究领域
的重要课题。根据下图所给数据,下列说法正确的是( )A.图甲反应若使用催化剂,既可以改变反应路径,也可以改变其ΔH
B.图乙中若HO的状态为气态,则能量变化曲线可能为①
2
C.图丙反应中反应物的总能量比生成物的总能量高
D.由图甲、图乙和图丙可知,HS(g)===H (g)+S(s) ΔH=+20 kJ·mol-1
2 2
5.中国学者在水煤气变换[CO(g)+HO(g)===CO (g)+H(g) ΔH]中突破了低温下高
2 2 2
转化率与高反应速率不能兼得的难题,该过程是基于双功能催化剂(能吸附不同粒子)催化
实现的。反应过程示意图如下:
下列说法正确的是( )
A.过程Ⅰ、过程Ⅲ均为放热过程
B.过程Ⅲ生成了具有极性共价键的H、CO
2 2
C.使用催化剂降低了水煤气变换反应的ΔH
D.图示过程中的HO均参与了反应过程
2
6.[2022·河南开封高三定位考试] 已知H(g)+2ICl(g)===I (g)+2HCl(g),该反应分①、
2 2
②两步进行,其能量曲线如图所示, 下列有关说法错误的是( )
A.反应①为放热反应
B.反应②是同种元素间发生的氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.H(g)+2ICl(g)===I (g)+2HCl(g)
2 2ΔH=-218 kJ·mol-1
7.[2022·安徽合肥一检]反应X+Y―→Z(ΔH>0)分两步进行:①X+Y―→W(ΔH<0),
②W―→Z(ΔH>0)。下列示意图中,能正确表示总反应过程中能量变化的是( )
8.[2022·浙江五校联考]单斜硫和正交硫转化为二氧化硫的能量变化如图,下列说法正
确的是( )
A.S(s,单斜)===S(s,正交) ΔH=-0.33 kJ·mol-1
B.①式表示断裂1 mol O 中的共价键所吸收的能量比形成1 mol SO 中的共价键所放出
2 2
的能量少297.16 kJ
C.②式表示一个正交硫和分子1个O 分子反应生成一个SO 分子放出296.83 kJ的能量
2 2
D.单斜硫比正交硫稳定
9.[2022·江苏东海学分认定考试]2SO
2
(g)+O
2
(g)⇌2SO
3
(g)反应过程中能量变化如图所
示(图中E表示正反应的活化能,E 表示逆反应的活化能。下列有关叙述正确的是( )
2
A.该反应的逆反应为放热反应,升高温度可提高活化分子的百分数
B.ΔH=E-E,使用催化剂改变活化能,但不改变反应热
1 2
C.该反应中,反应物的总键能大于生成物的总键能
D.500 ℃、101 kPa下,将1 mol SO (g)和0.5 mol O (g)置于密闭容器中充分反应生成
2 2
SO
3
(g)放热a kJ,其热化学方程式为2SO
2
(g)+O
2
(g)⇌2SO
3
(g) ΔH=-2a kJ·mol-1
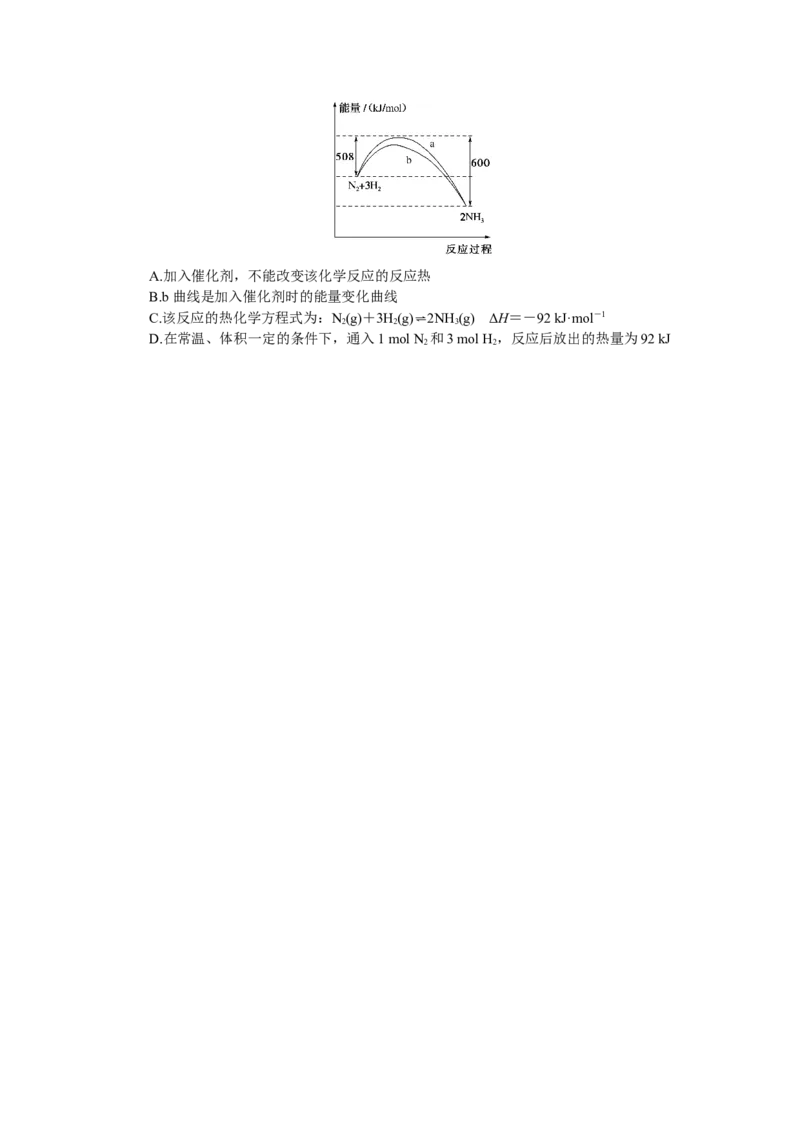
10.[2022·全国百强校宁夏育才中学月考]298 K、101 kPa时,N 与H 反应过程中能量
2 2
变化的曲线图,下列叙述错误的是( )A.加入催化剂,不能改变该化学反应的反应热
B.b曲线是加入催化剂时的能量变化曲线
C.该反应的热化学方程式为:N
2
(g)+3H
2
(g)⇌2NH
3
(g) ΔH=-92 kJ·mol-1
D.在常温、体积一定的条件下,通入1 mol N 和3 mol H ,反应后放出的热量为92 kJ
2 2