文档内容
第二篇 元素及其化合物
专项 17 陌生物质的推断
无机推断题是一种重要形式,浓缩了元素及其化合物知识,具有极强的学科特色,题材广、可考查内
容多且容易控制卷面难度的题型特点,成了高考命题中一种十分重要形式。近年来出现(浙江选考)已不囿
于传统的无机推断,改头换面以小流程结合定量计算进行推断的形式出现。
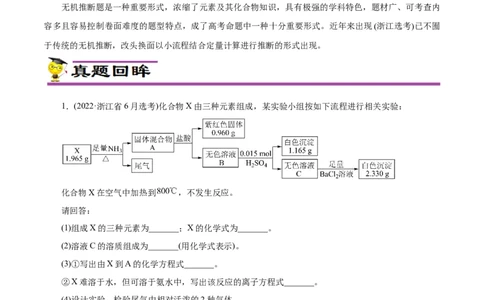
1.(2022·浙江省6月选考)化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到 ,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
(4)设计实验,检验尾气中相对活泼的2种气体_______。
【答案】(1) Ba、Cu、O BaCu O
3 4
(2)HCl、HSO
2 4
(3) 2NH +BaCu O Ba(OH) +3Cu+N +2H O BaCu O+12NH HO=3Cu(NH )2++Ba2++8OH-+8H O
3 3 4 2 2 2 3 4 3 2 3 4 2
(4)将湿润的红色石蕊试纸置尾气出口,若变蓝,说明尾气中有NH 。将尾气通入冷的集气瓶中,若有
3
液珠,说明有HO
2
【解析】化合物X由三种元素组成,在加热条件下和足量氨气反应生成固体混合物A,A和盐酸反应
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司生成0.960g紫红色固体应该是Cu,无色溶液B中加入0.015mol稀硫酸生成白色沉淀1.165g应该是
BaSO,无色溶液C中加入足量BaCl 溶液生成白色沉淀2.330g是BaSO。(1)根据以上分析可知Cu的物质
4 2 4
的量是0.96g÷64g/mol=0.015mol,第一次生成硫酸钡的物质的量是1.165g÷233g/mol=0.005mol,第二次生
成硫酸钡的物质的量是2.33g÷233g/mol=0.01mol,因此1.965gX中一定含有0.96gCu,Ba的质量是
0.005mol×137g/mol=0.685g,二者质量之和是1.645g<1.965g,相差0.32g,根据原子守恒可知应该是氧元
素,物质的量是0.32g÷16g/mol=0.02mol,则Ba、Cu、O三种原子的个数之比是1:3:4,所以组成X的
三种元素为Ba、Cu、O,X的化学式为BaCu O。(2)根据氯原子原子守恒以及溶液C仍然能与氯化钡反应
3 4
生成硫酸钡可知溶液C的溶质组成为HCl、HSO 。(3)①反应中Cu元素化合价降低,得到电子,则氨气中
2 4
氮元素化合价升高,被氧化生成氮气,根据原子守恒可知由X到A的化学方程式为2NH +BaCu O
3 3 4
Ba(OH) +3Cu+N +2H O。②X难溶于水,但可溶于氨水中,说明有Cu(NH ) 2+生成,所以该反应的离子方
2 2 2 3 4
程式为BaCu O+12NH HO=3Cu(NH ) 2++Ba2++8OH-+8H O。(4)反应中氨气可能过量,高温下水是气态,
3 4 3 2 3 4 2
氮气性质稳定,所以需要检验的是氨气和水蒸气,实验方案为:将湿润的红色石蕊试纸置尾气出口,若变
蓝,说明尾气中有NH 。将尾气通入冷的集气瓶中,若有液珠,说明有HO。
3 2
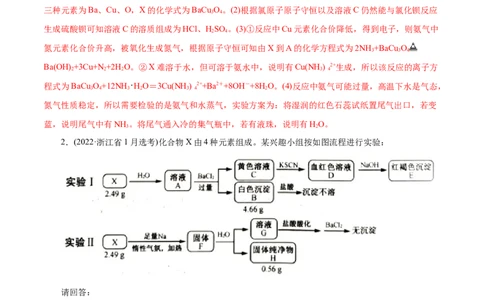
2.(2022·浙江省1月选考)化合物X由4种元素组成。某兴趣小组按如图流程进行实验:
请回答:
(1)组成X的元素有______,X的化学式为___________。
(2)溶液C中溶质的成分是______(用化学式表示);根据C→D→E的现象,给出相应微粒与阳离子结合
由弱到强的排序_____________________。
(3)X与足量Na反应生成固体F的化学方程式是_____________________。
(4)设计实验确定溶液G中阴离子____________________________________。
【答案】(1)Fe、S、O、H FeH(SO )
4 2
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司(2)FeCl 、HCl、BaCl Cl-、HO、SCN-、OH-
3 2 2
(3)2FeH(SO )+40Na 2Fe+4Na S+16Na O+H
4 2 2 2 2
(4)用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明存在OH-;取少量溶液G,加入足量
HO,用盐酸酸化,再加入BaCl 溶液,有白色沉淀,说明有S2-
2 2 2
【解析】X形成水溶液,与氯化钡反应生产白色沉淀,且沉淀不与盐酸反应说明生产硫酸钡,说明X
含有硫酸根,溶液加入KSCN变红说明含有Fe3+,B为4.66g则为0.02mol硫酸钡,说明X含有0.02mol的
硫酸根,H中为Fe单质,即为0.01mol,X中含有0.01molFe,由此可知X中应含有0.01的H。(1)由分析
可知,组成X的元素有:Fe、S、O、H;X的化学式为FeH(SO );(2)X 为FeH(SO ) 与氯化钡反应,溶液
4 2 4 2
C中溶质的成分是FeCl 、HCl以及过量的BaCl ;根据C为溶液,铁离子在水中会水解,C→D形成络合物,
3 2
D→E形成沉淀,相应微粒与阳离子结合由弱到强的排序:Cl-、HO、SCN-、OH-;(3)X与足量Na反应生
2
成固体F的化学方程式是:2FeH(SO )+40Na 2Fe+4Na S+16Na O+H;(4)设计实验确定溶液G中
4 2 2 2 2
阴离子:用玻璃棒蘸取溶液G,点在红色石蕊试纸上,若变蓝,说明存在OH-;取少量溶液G,加入足量
HO,用盐酸酸化,再加入BaCl 溶液,有白色沉淀,说明有S2-。
2 2 2
无机推断中,最为核心的是要依据条件、现象推断出物质,未知物质化学式的思维过程可概括为思维
起点的选择——推断题中的思维起点应是最具特征的某个条件(包括文字叙述或某个变化过程),即依物质
的特性或特征转化来确定“突破口”。
1.思维过程的展开——解题者在确定思维起点的基础上,利用题目所给信息,结合已有的化学知识
和解题经验进行推断。
(1)根据框图以及题给信息,结合“基础知识的梳理——元素化合物的性质”。常见的主要是特征现象,
比如沉淀的颜色、气体的颜色、气体的特殊性质以及焰色反应等,初步确定物质的元素组成。
(2)根据题给数据,运用元素守恒(质量守恒)、电荷守恒以及电子的是守恒等方法求解物质物各元素的
原子(离子)的物质的量,从而找出它们的个数之比,得出未知物质的化学式。
2.思维过程的检验——将上述思维过程的结果代入题中,检查一下是否符合题中条件。
解题方法及推理过程表示如下:
3
原创精品资源学科网独家享有版权,侵权必究!
3
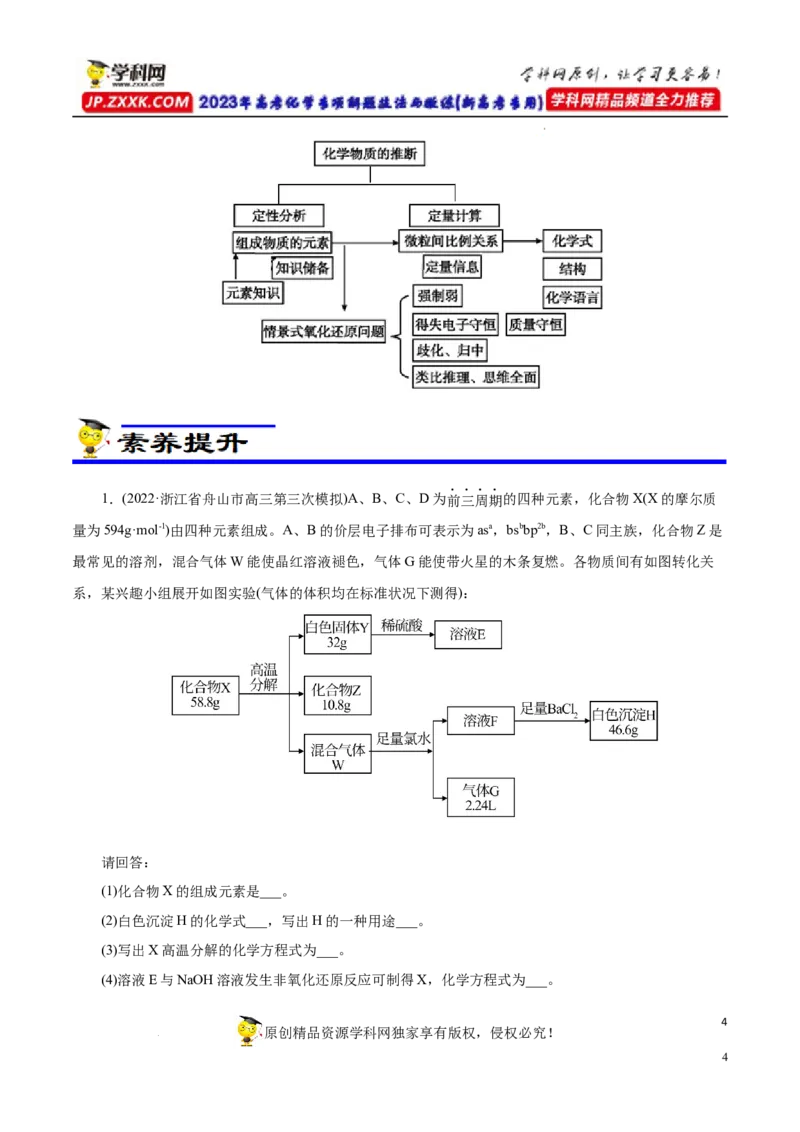
学科网(北京)股份有限公司1.(2022·浙江省舟山市高三第三次模拟)A、B、C、D为前三周期的四种元素,化合物X(X的摩尔质
量为594g·mol-1)由四种元素组成。A、B的价层电子排布可表示为asa,bsbbp2b,B、C同主族,化合物Z是
最常见的溶剂,混合气体W能使晶红溶液褪色,气体G能使带火星的木条复燃。各物质间有如图转化关
系,某兴趣小组展开如图实验(气体的体积均在标准状况下测得):
请回答:
(1)化合物X的组成元素是___。
(2)白色沉淀H的化学式___,写出H的一种用途___。
(3)写出X高温分解的化学方程式为___。
(4)溶液E与NaOH溶液发生非氧化还原反应可制得X,化学方程式为___。
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司(5)关于混合气体W能使品红溶液褪色的原因,一般认为:W混合气体能使品红褪色,不是其中某种
气体本身与品红作用,而是该气体与水反应的生成物使品红褪色。请设计实验证明___。
【答案】(1)Mg、O、H、S
(2) BaSO 医疗上做钡餐(或是制造其他钡盐的原料或白色颜料)
4
(3)2Mg (OH) SO 8MgO+2SO ↑+O ↑+6H O
4 6 4 2 2 2
(4)4MgSO +6NaOH=Mg (OH) SO +3Na SO
4 4 6 4 2 4
(5)配制品红无水乙醇溶液,通入二氧化硫,不褪色,品红溶液中加入亚硫酸钠固体,褪色更快
【解析】由“A、B的价层电子排布可表示为asa,bsbbp2b”,可推出A为H元素,B为O元素;由
“B、C同主族”,可推出C为S元素;由“白色固体Y可溶于稀硫酸”,可推出Y为MgO,从而得出D
为Mg元素。由“化合物Z是最常见的溶剂”,可推出Z为HO;由“混合气体W能使晶红溶液褪色,气
2
体G能使带火星的木条复燃”,可推出气体由SO 和O 组成,气体G为O。由“溶液F中加入BaCl 可生
2 2 2 2
成白色溶液H”,可推出H为BaSO,F为HSO 与HCl的混合物。(1)由以上分析可知,四种元素分别为
4 2 4
H、O、S、Mg,从而得出化合物X的组成元素是Mg、O、H、S;(2)由分析可知,H为HSO 与BaCl 反
2 4 2
应生成的难溶物BaSO,其用途为医疗上做钡餐(或是制造其他钡盐的原料或白色颜料);(3)n(MgO)=
4
,n(H O)= ,n(SO )= ,n(O )= ;
2 2 2
n(MgO):n(H O):n(SO ):n(O )=0.8mol:0.6mol:0.2mol:0.1mol=8:6:2:1,从而得出X的化学式为Mg(OH) SO 。
2 2 2 4 6 4
X高温分解的化学方程式为2Mg(OH) SO 8MgO+2SO +O +6H O;(4)由以上分析知,E为MgSO ,
4 6 4 2 2 2 4
MgSO 与NaOH溶液发生非氧化还原反应可制得Mg(OH) SO ,则反应的化学方程式为
4 4 6 4
4MgSO +6NaOH=Mg (OH) SO +3Na SO ;(5)设计实验时,一方面要创设非水溶液中的情境,即将SO 通入
4 4 6 4 2 4 2
无水品红溶液中,另一方面是在品红水溶液中加入含有SO 2-或HSO -的固体盐,从而得出实验方案为配制
3 3
品红无水乙醇溶液,通入二氧化硫,不褪色,品红溶液中加入亚硫酸钠固体,褪色更快。
2.(2022·浙江省五校高三联考)为探究由3种短周期元素构成的化合物X的性质。完成如图实验:
5
原创精品资源学科网独家享有版权,侵权必究!
5
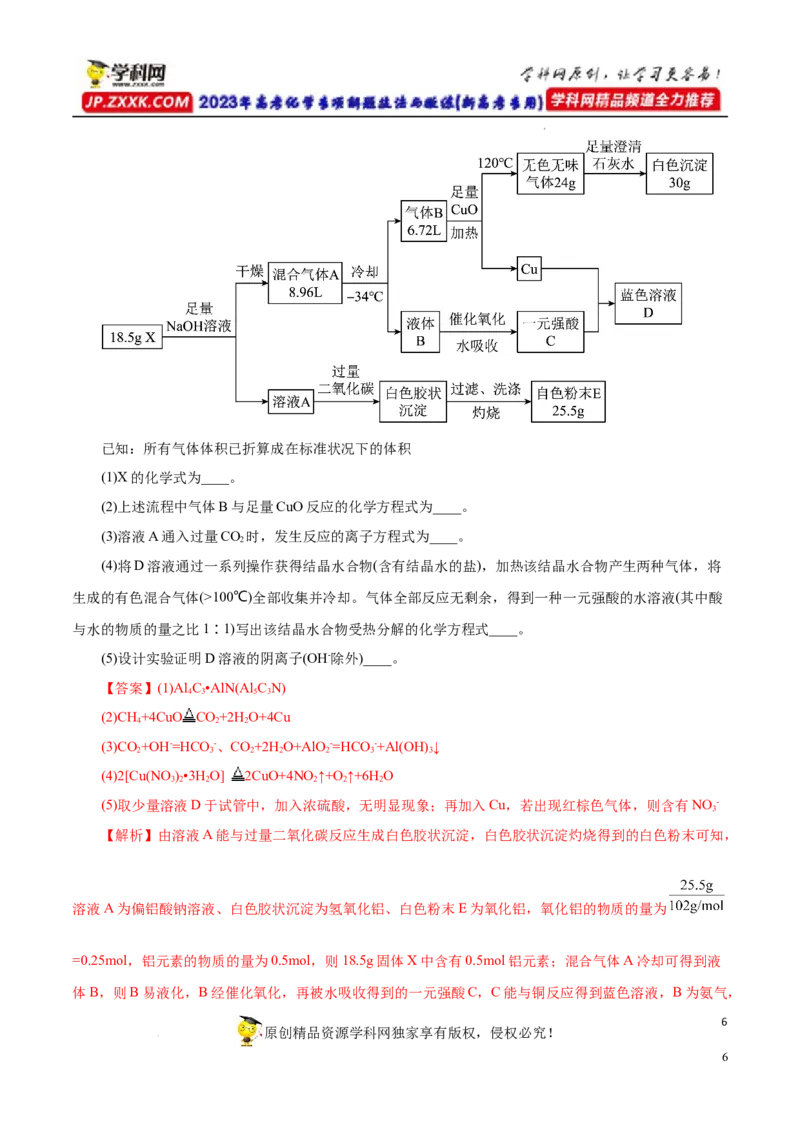
学科网(北京)股份有限公司已知:所有气体体积已折算成在标准状况下的体积
(1)X的化学式为____。
(2)上述流程中气体B与足量CuO反应的化学方程式为____。
(3)溶液A通入过量CO 时,发生反应的离子方程式为____。
2
(4)将D溶液通过一系列操作获得结晶水合物(含有结晶水的盐),加热该结晶水合物产生两种气体,将
生成的有色混合气体(>100℃)全部收集并冷却。气体全部反应无剩余,得到一种一元强酸的水溶液(其中酸
与水的物质的量之比1∶1)写出该结晶水合物受热分解的化学方程式____。
(5)设计实验证明D溶液的阴离子(OH-除外)____。
【答案】(1)AlC •AlN(Al C N)
4 3 5 3
(2)CH +4CuO CO+2H O+4Cu
4 2 2
(3)CO +OH-=HCO-、CO+2H O+AlO-=HCO-+Al(OH) ↓
2 3 2 2 2 3 3
(4)2[Cu(NO )•3H O] 2CuO+4NO ↑+O ↑+6H O
3 2 2 2 2 2
(5)取少量溶液D于试管中,加入浓硫酸,无明显现象;再加入Cu,若出现红棕色气体,则含有NO -
3
【解析】由溶液A能与过量二氧化碳反应生成白色胶状沉淀,白色胶状沉淀灼烧得到的白色粉末可知,
溶液A为偏铝酸钠溶液、白色胶状沉淀为氢氧化铝、白色粉末E为氧化铝,氧化铝的物质的量为
=0.25mol,铝元素的物质的量为0.5mol,则18.5g固体X中含有0.5mol铝元素;混合气体A冷却可得到液
体B,则B易液化,B经催化氧化,再被水吸收得到的一元强酸C,C能与铜反应得到蓝色溶液,B为氨气,
6
原创精品资源学科网独家享有版权,侵权必究!
6
学科网(北京)股份有限公司C为硝酸,D为硝酸铜,则固体X中含有氮元素;6.72L气体B即 =0.3mol气体B能与氧化铜共
热反应生成120℃时的无色无味气体24g,无色无味气体能与足量石灰水反应生成30g白色沉淀,白色沉淀
为碳酸钙,则固体X中含有碳元素,由碳原子个数守恒可知,二氧化碳的物质的量为 =0.3mol,
质量为0.3mol 44g/mol=13.2g,气体B则为烃,无色无味气体中的另外一种气体为水蒸气,质量为
24g-13.2g=10.8g,水蒸气的物质的量为 =0.6mol,则B中碳原子和氢原子的原子个数比为
0.3mol:0.6mol×2=1:4,B为甲烷;混合气体A的体积为8.96L,物质的量为 =0.4mol,则氨气的物
质的量为0.4mol-0.3mol=0.1mol,综上分析,X中含0.5mol铝元素、0.3mol碳元素、0.1mol氮元素,固体
X中铝元素、碳元素、氮元素的物质的量比为:0.5mol:0.3mol:0.1mol=5:3:1,固体X的质量为18.5g,物质
的量为0.1mol,固体X的化学式为Al C N,改写可得Al C ·AlN。(1)固体X的化学式为
5 3 4 3
Al C ·AlN(Al C N)。(2)甲烷与足量氧化铜共热反应生成铜、二氧化碳和水,反应的化学方程式为:
4 3 5 3
CH+4CuO CO+2H O+4Cu。(3)溶液A通入过量二氧化碳时发生的反应为:过量二氧化碳与氢氧化钠溶
4 2 2
液反应生成碳酸氢钠、过量二氧化碳与偏铝酸钠溶液反应生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程
式为:CO+OH-=HCO-、CO+2H O+AlO-=HCO-+Al(OH) ↓。(4)D为硝酸铜,将D溶液通过一系列操作获
2 3 2 2 2 3 3
得结晶水合物(含有结晶水的盐),加热该结晶水合物产生两种气体,生成有色混合气体,有色气体为二氧
化氮,将生成的有色混合气体(>100℃)全部收集并冷却,气体全部反应无剩余,得到一种一元强酸的水溶
液,一元强酸为硝酸,生成的两种气体为二氧化氮和氧气,二氧化氮和氧气在水溶液中完全反应的方程式
为4NO +O +2H O=4HNO ,由硝酸溶液中硝酸与水的物质的量之比1:1可知,气体中还有水,二氧化氮、
2 2 2 3
氧气和水的物质的量比为4:1:6,则硝酸铜结晶水合物的化学式为Cu(NO )·3H O,受热分解的化学方程式
3 2 2
为:2[Cu(NO )•3H O] 2CuO+4NO ↑+O ↑+6H O。(5)实验室用铜与浓硝酸反应生成红棕色气体的方法检
3 2 2 2 2 2
验硝酸根离子,则检验硝酸铜溶液中的硝酸根离子的操作为取少量溶液于试管中,加入浓硫酸,无明显现
象;再加入铜,若产生红棕色气体,则含有NO -。
3
3.(2022·浙江省温州市普通高中高三适应性测试三模考试)固体盐X由四种常见元素组成,其中仅含
7
原创精品资源学科网独家享有版权,侵权必究!
7
学科网(北京)股份有限公司一种金属元素,有如图转化关系:
已知:H中溶质仅为一种常见正盐。黄绿色气体C密度为相同条件下H 的33.75倍。
2
请回答:
(1)X的组成元素为_______________,固体F成分为_______________。
(2)固体X在水中也可反应生成气体B,同时生成一种的相对较稳定的白色沉淀,请写出该反应化学方
程式_____________________________________。
(3)向血红色溶液Ⅰ中加入足量的KI溶液,发生氧化还原反应,产物中含有与血红色物质组成元素相
同的微粒,请写出该反应可能的离子方程式____。
(4)气体C的化学式为_______________。将气体C通入KOH溶液,微热,恰好完全反应,生成两种物
质的量之比1∶5的盐,写出这两种盐的化学式__________________,设计定量实验方案验证上述比例关系
__________________________________________。
【答案】(1) Fe、H、C、O Fe O、KCO
2 3 2 3
(2)Fe(HCO )=FeCO +CO ↑+H O
3 2 3 2 2
(3)2Fe(SCN) +2I-=I +2 Fe(SCN) -
3 2 3
(4) ClO KCl、KClO 取适量溶液,加入过量硝酸银溶液,将沉淀过滤、洗涤、干燥、称量得固
2 3
体质量m;合并洗涤液和滤液,向其中加入足量亚硝酸钠溶液,再加入足量硝酸银和稀硝酸,将沉淀过滤、
1
洗涤、干燥、称量得固体质量m,若m=5m,则可验证上述比例关系
2 2 1
【解析】固体氧化物G与稀盐酸反应后与KSCN溶液反应,溶液呈血红色,说明含有Fe3+,则G为
Fe O,物质的量为 ,n(Fe3+)=0.02mol,黄绿色混合气体A+B+C通过浓硫酸后气体质量
2 3
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司减少0.36g,得到黄绿色混合气体B+C,则A为水蒸气,物质的量为 ,黄绿色混合气体
B+C与足量澄清石灰水反应生成白色沉淀D3.00g为碳酸钙,物质的量为 ,黄绿色气
体C密度为相同条件下H 的33.75倍,故B为CO,物质的量为0.03mol,气体C的相对分子质量为
2 2
33.75×2=67.5,可推知C为ClO ,H中溶质仅为一种常见正盐,且与足量稀盐酸反应产生无色气体CO,
2 2
根据固体X与氯酸钾反应可知H应该为钾盐,故为KCO;固体X在水中也可反应生成气体B,同时生成
2 3
一种的相对较稳定的白色沉淀,白色沉淀不为氢氧化亚铁,只能为FeCO。(1)综上分析,固体盐X由四种
3
常见元素组成,其中仅含一种金属元素,X的组成元素为Fe、H、C、O,固体F成分为Fe O、KCO;
2 3 2 3
(2)固体X在水中也可反应生成气体CO,同时生成一种的相对较稳定的白色沉淀FeCO,该反应化学方程
2 3
式Fe(HCO )=FeCO +CO ↑+H O;(3)向血红色溶液Ⅰ中加入足量的KI溶液,发生氧化还原反应,碘离子被
3 2 3 2 2
氧化生成碘单质,产物中含有与血红色物质组成元素相同的微粒,Fe(SCN) 被还原,铁元素价态降低,反
3
应可能的离子方程式为2Fe(SCN) +2I-=I +2 Fe(SCN) -;(4)气体C的化学式为ClO ;将气体ClO 通入KOH
3 2 3 2 2
溶液,微热,恰好完全反应,生成两种物质的量之比1∶5的盐,根据氧化还原反应原理,生成KCl,氯元
素化合价降5,则生成化合价比+4高的氧化产物的化合价应该为+5价,则生成KClO,两种盐的化学式
3
KCl、KClO;取适量溶液,加入过量硝酸银溶液,将沉淀过滤、洗涤、干燥、称量得固体质量m;合并
3 1
洗涤液和滤液,向其中加入足量亚硝酸钠溶液,再加入足量硝酸银和稀硝酸,将沉淀过滤、洗涤、干燥、
称量得固体质量m,若m=5m,则可验证上述比例关系。
2 2 1
4.(2022·浙江省Z20名校联盟高三第三次联考)固体化合物X有三种元素组成。某学习小组开展如下
探究实验:
请回答:
9
原创精品资源学科网独家享有版权,侵权必究!
9
学科网(北京)股份有限公司(1)组成X的元素有_______,X的化学式为_______。
(2)化合物X与液态氨也能发生类似的反应,请写出相应的化学方程式_______。
(3)固体A能溶于NaHF 的水溶液,产物中含一种正八面体的负三价阴离子,写出其相应的离子方程式
2
_______
(4)红褐色固体B在真空条件灼烧,反应完全后生成黑色粉末(纯净物),黑色粉末的成分可能是_______,
并用实验验证的方案是_______。
【答案】(1) Fe、Cl、O FeOCl(或FeCl ·Fe O)
3 2 3
(2) FeOCl+2NH = FeO(NH)+NHCl (写成3FeOCl+6NH = Fe(NH )+3NHCl+ Fe O 或
3 2 4 3 2 3 4 2 3
FeCl ·Fe O+6NH= Fe(NH )+3NHCl+ Fe O)
3 2 3 3 2 3 4 2 3
(3) FeO(OH)+3HF -= FeF 3-+2H O (或Fe(OH) ·Fe O+9HF-=3 FeF 3-+6H O
2 6 2 3 2 3 2 6 2
)
(4) Fe、FeO或Fe O 取适量固体于试管中,加入足量盐酸使固体溶解,若产生气泡,则是Fe;如
3 4
不产生气泡,向溶液中加入少量KSCN溶液,若出现血红色溶液,则是Fe O;若无上述现象,说明是
3 4
FeO
【解析】红褐色固体B为Fe O,物质的量为 =0.1mol,铁元素物质的量为0.2mol,氧元素物
2 3
质的量为0.3mol,固体A灼烧生成Fe O 和水,水的质量为17.8g-16.0g=1.8g,水的物质的量为
2 3
=0.1mol,氢元素物质的量为0.2mol,氧元素物质的量为0.1mol,固体A中Fe、O、H的原子个数比为:
0.2mol:0.2mol:0.4mol=1:1:2,A的化学式为:FeO(OH),化合物X中有铁元素0.2mol,质量为11.2g,无色
气体A通入到足量硝酸酸化的硝酸银溶液中产生白色沉淀B为AgCl,物质的量为 =0.2mol,无
色气体A为HCl,化合物X中含氯元素0.2mol,质量为7.1g,X中另一种元素的质量为
21.5g-11.2g-7.1g=3.2g,Fe、Cl原子个数比为0.2mol:0.2mol=1:1,依据正负化合价代数和为0的原则,另一
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司种元素不能为氢元素,应为氧元素,物质的量为 =0.2mol,则X的化学式为:FeOCl(或
FeCl ·Fe O)。(1)由分析可知,X的化学式为:FeOCl,组成X的元素有Fe、O、Cl。(2)FeOCl与水反应生
3 2 3
成FeO(OH)和HCl,则FeOCl与液态氨反应的化学方程式为:FeOCl+2NH = FeO(NH)+NHCl (写成
3 2 4
3FeOCl+6NH = Fe(NH )+3NHCl+ Fe O 或FeCl ·Fe O+6NH= Fe(NH )+3NHCl+ Fe O)。(3)由分析可知,
3 2 3 4 2 3 3 2 3 3 2 3 4 2 3
A的化学式为:FeO(OH),FeO(OH) 能溶于NaHF 的水溶液,产物中含一种正八面体的负三价阴离子,则
2
其中心原子价层电子对数为6,阴离子为FeF3-,反应的离子方程式为:FeO(OH)+3HF -= FeF 3-+2H O (或
6 2 6 2
Fe(OH) ·Fe O+9HF-=3 FeF 3-+6H O)。(4)红褐色固体B为Fe O,真空条件灼烧,反应完全后生成黑色粉末
3 2 3 2 6 2 2 3
(纯净物),依据元素守恒,黑色粉末的成分可能是Fe、FeO或Fe O,铁能与盐酸反应生成氢气,Fe O 能
3 4 3 4
与盐酸反应生成铁离子,FeO能与盐酸反应生成亚铁离子,因此检验固体成分的方案为:取适量固体于试
管中,加入足量盐酸使固体溶解,若产生气泡,则是Fe;如不产生气泡,向溶液中加入少量KSCN溶液,
若出现血红色溶液,则是Fe O;若无上述现象,说明是FeO。
3 4
5.(2022·浙江省山水联盟高三联考)由三种元素组成的化合物A(相对分子质量<100),按如下流程进
行实验:
已知:
①气体C能使白色硫酸铜固体变蓝色;Mg(ClO) 质量增重10.8g。
4 2
②化合物E和F既能溶于NaOH溶液也能溶于盐酸。
③CO与银氨溶液生成黑色沉淀:CO+2 Ag(NH)++2OH-=2Ag↓+2NH ++CO 2-+2NH
3 2 4 3 3
请回答:
(1)组成A的元素有_______(填元素符号);化合物A的化学式是_______。
(2)检测到化合物H中含有A的金属元素。若H只含2种元素,则H化学式为_______;若H只含3种
元素,则H化学式为_______。
(3)F中阳离子与OH-、Cl-、HO、F-结合能力由大到小排序:_______。
2
(4)足量白色固体E与少量的NaF溶液反应的离子方程式为_______。
11
原创精品资源学科网独家享有版权,侵权必究!
11
学科网(北京)股份有限公司(5)若气体B以较快速度通入灼热CuO粉末,将会收集到以下4种气体:_______(填化学式)。现验证
收集到的4种气体的成分,将所需的试剂填在空白上:混合气体→硫酸铜固体→_______→_______→碱石
灰→酒精灯火焰点燃且罩上内涂澄清石灰水的烧杯。
【答案】(1) Al、C、H Al(CH)
3 3
(2) AlH NaAlH 。
3 4
(3) F-、OH-、HO、Cl-
2
(4) 4Al(OH) +6F-=AlF 3-+3[Al(OH) ]-或4Al(OH) +6F-=AlF 3-+3AlO -+6H O
3 6 4 3 6 2 2
(5) CO、CO、HO(g)、CH 澄清石灰水 银氨溶液
2 2 4
【解析】化合物B与足量CuO加热反应生成气体C和气体D,气体C能使白色硫酸铜固体变蓝色,气
体C为HO(g),气体C和D的混合气用足量Mg(ClO) 吸收,Mg(ClO) 质量增重10.8g,则n[H O(g)]=
2 4 2 4 2 2
=0.6mol;气体D与足量澄清石灰水反应生成白色沉淀30g,气体D为CO,n(CO)=n(CaCO)=
2 2 3
=0.3mol,根据原子守恒,化合物B中一定含C、H元素,m(C)+m(H)=0.3mol×12g/
mol+0.6mol×2×1g/mol=4.8g与化合物B的质量相等,化合物B中不含O,化合物B中n(C):n(H)=0.3mol:
(0.6mol×2)=1:4,B的实验式为CH,由于实验式中H原子已经达到饱和,B的分子式为CH;白色固体
4 4
化合物E和白色固体F既能溶于NaOH溶液也能溶于盐酸,E高温灼烧生成F,则E为Al(OH) 、F为
3
Al O,Al O 的质量为5.1g,则n(AlO)= =0.05mol;化合物A与足量水反应生成化合物B和化合
2 3 2 3 2 3
物E,根据Al、C守恒,化合物A中含Al、C物质的量依次为0.1mol、0.3mol,m(Al)+m(C)=0.1mol×27g/
mol+0.3mol×12g/mol=6.3g,化合物A由三种元素组成,化合物A中另一元素的质量为7.2g-6.3g=0.9g,该
元素为H,H的物质的量为0.9g÷1g/mol=0.9mol,化合物A中n(Al):n(C):(H)=0.1mol:0.3mol:
0.9mol=1:3:9,A的实验式为AlC H,A的相对分子质量<100,则A的化学式为Al(CH)。(1)根据分
3 9 3 3
析,组成A的元素有Al、C、H,化合物A的化学式为Al(CH);(2)AlO 与C和Cl 加热反应生成化合物
3 3 2 3 2
G和气体D(CO ),根据原子守恒,化合物G为AlCl ,化合物G与NaH在一定条件下反应生成化合物H和
2 3
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司化合物I;检测到化合物H中含有A的金属元素,即H中含Al元素;若H只含2种元素,则H的化学式为
AlH,反应的化学方程式为AlCl +3NaH AlH+3NaCl;若H只含3种元素,则H的化学式为
3 3 3
NaAlH ,反应的化学方程式为AlCl +4NaH NaAlH +3NaCl;(3)F中阳离子为Al3+,Al3+与F-具有
4 3 4
很强的亲和性,能形成难电离的配离子AlF3-,AlF3-、Al(OH) 、水合铝离子、AlCl 给出Al3+的能力逐渐增
6 6 3 3
强,则Al3+与OH-、Cl-、HO、F-结合能力由大到小的顺序为F-、OH-、HO、Cl-;(4)足量Al(OH) 与少量
2 2 3
NaF反应生成NaAlF、Na[Al(OH)]或NaAlO ,反应的离子方程式为4Al(OH) +6F-=AlF 3-+3[Al(OH) ];(5)
3 6 4 2 3 6 4
气体B为CH,若CH 以较快速率通过灼热CuO粉末,CH 与CuO加热时,CuO可能将CH 氧化成CO、
4 4 4 4 2
CO,同时生成HO,由于CH 的速率较快,还有部分CH 来不及反应,故收集到的4种气体为CO、CO、
2 4 4 2
HO(g)、CH;用无水CuSO 检验气体HO(g),硫酸铜固体变蓝说明有HO(g);用澄清石灰水检验CO,
2 4 4 2 2 2
澄清石灰水变浑浊说明有CO;根据已知③,用银氨溶液检验CO,银氨溶液中产生黑色沉淀说明有CO,
2
同时银氨溶液吸收CO;用碱石灰将CO 和HO(g)吸收后,酒精灯火焰点燃且罩上内涂澄清石灰水的烧杯,
2 2
烧杯内壁变模糊说明有CH。
4
6.(2022·浙江省百校高三选考模拟检测)某合金X由两种元素组成,一定条件下将其完全溶于一定量
的稀硝酸中,可发生如下转化。其中溶液B、D均只含一种溶质,且具有相同的阴离子。
回答下列问题:
(1)合金X的化学式为_______,溶液D中溶质的化学式为_______。
(2)溶液B隔绝空气加热的化学方程式为_______。
(3)气体C和足量的氧气完全溶于NaOH溶液,写出反应的离子方程式:_______。
(4)在强碱性溶液中D与NaClO生成一种理想的水处理剂,写出反应的离子方程式:_______。
(5)溶液B长期露置于空气中易变质,请设计实验方案判断溶液B是否变质:_______。
【答案】(1) Fe C Fe (NO)
3 3 3
13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司(2)9 Fe(NO )+6H O=5Fe(NO )+3NO↑+4 Fe(OH) ↓
3 2 2 3 3 3
(3) 4NO+3O+4OH-=4NO-+2H O
2 3 2
(4) 2Fe3++10OH-+3ClO-=2FeO 2-+3Cl-+5H O
4 2
(5)取少量A溶液于试管中,滴入几滴KSCN溶液,若溶液呈血红色,说明变质,反之,说明没有变质
【解析】由E的颜色可知E为Fe(OH) ,F为Fe O,则X中含Fe;稀硝酸有强氧化性,则A中含
3 2 3
NO,由于NO不溶于石灰水,所以C为NO;溶液B、D均只含一种溶质,且具有相同的阴离子,则B、D
中含硝酸根离子,结合B→C+D+E可知B中有还原性离子Fe2+,则B的溶质为Fe(NO ),D的溶质为
3 2
Fe(NO );结合“A+足量石灰水→白色沉淀3g+C”可知A中含CO(由于第一步加了强氧化性的稀硝酸,则
3 3 2
A中不可能含SO ),白色沉淀是碳酸钙,综上所述,X含Fe和C,n(C)= ,
2
m(C)=0.03mol×12g/mol=0.36g,X中m(Fe)=5.4g-0.36g=5.04g,n(Fe)= =0.09mol,则n(Fe):n(C)=
0.09:0.03=3:1,X的化学式为Fe C 。(1)合金X的化学式为Fe C ;溶液D中溶质的化学式为Fe(NO );(2)
3 3 3 3
溶液B为硝酸亚铁,气体C为NO,溶液D为硝酸铁,E为氢氧化铁沉淀,溶液B隔绝空气加热的化学方
程式为9 Fe(NO)+6H O=5Fe(NO )+3NO↑+4 Fe(OH) ↓;(3)气体C为NO,和足量的氧气完全溶于NaOH溶
3 2 2 3 3 3
液发生氧化还原反应生成硝酸钠,N元素化合价升高,O元素降价,反应的离子方程式:4NO+3O +4OH-
2
=4NO-+2H O;(4)D为Fe(NO ),强碱性溶液中Fe3+与NaClO发生氧化还原反应生成高铁酸钠,反应的离
3 2 3 3
子方程式:2Fe3++10OH-+3ClO-=2FeO 2-+3Cl-+5H O;(5)溶液B为硝酸亚铁,若变质生成Fe3+,可用KSCN
4 2
溶液检验,实验方案为:取少量A溶液于试管中,滴入几滴KSCN溶液,若溶液呈血红色,说明变质,反
之,说明没有变质。
7.(2022·浙江省绍兴诸暨市高三二模)化合物X由5种元素组成且不含结晶水。某兴趣小组按如图流
程进行实验:
14
原创精品资源学科网独家享有版权,侵权必究!
14
学科网(北京)股份有限公司已知:
①上述流程中,除沉淀A→红棕色固体B的转化外,其余均为非氧化还原反应;
②气体B能使湿润的红色石蕊试纸变蓝,标准状况下测得体积为2.24L。
请回答:
(1)组成X的元素有_______,X的化学式是_______。
(2)红棕色固体B在KOH高温环境下,与KNO 反应,固体B中金属元素化合价升高。同时生成
3
KNO,写出该化学反应方程式_______。
2
(3)将气体B通入到CuSO 溶液中,先产生蓝色絮状沉淀,继续通入气体B,蓝色沉淀消失,呈深蓝色
4
透明溶液,请写出相应的离子反应方程式_______;_______。
(4)滤液A中溶质的成分是_______。
(5)设计实验方案,用化学方法确定沉淀A中阳离子的成分_______。
【答案】(1) Fe、H、N、O、S Fe(NH )SO ·2(NH )SO
3 6 4 4 2 4
(2)Fe O+3KNO +4KOH=2K FeO+3KNO +2H O
2 3 3 2 4 2 2
(3) Cu2++2NH·H O=Cu(OH) ↓+2NH+ Cu(OH) +4NH=[Cu((NH )]2++2OH-
3 2 2 4 2 3 3 4
(4)(NH )SO 、NH
4 2 4 3
(5)取少量沉淀A试管中,加入适量稀硫酸溶解,向其中加入少量KSCN溶液,无明显变化,继续加入
氯水,溶液呈红色,说明沉淀A中含有Fe2+
【解析】X加水溶解后过滤得到的沉淀A经过灼烧得到红棕色固体B,B为氧化铁,物质的量为
0.005mol,A为氢氧化铁,根据铁守恒,物质的量为0.01mol,X中含Fe元素;滤液A加NaOH溶液得到
气体B,气体为NH ,标况下体积为2.24L,物质的量为0.1mol,说明X中含N和H元素;滤液B加过量
3
的Ba(OH) 得到白色沉淀C,为硫酸钡,说明X中含硫酸根,物质的量为0.03mol,综上:X中含Fe元素
2
0.01mol,N元素0.1mol,硫酸根0.03mol,根据质量守恒,含氢元素的质量为:
,故氢元素的物质的量为0.34mol,故X的化学式为
Fe(NH )SO ·2(NH )SO 。(1)根据分析,X中含Fe、H、N、O、S;X化学式为Fe(NH )SO ·2(NH )SO ;
3 6 4 4 2 4 3 6 4 4 2 4
(2)红棕色固体B为氧化铁,高温下与KOH反应的化学方程式为:
Fe O+3KNO +4KOH=2K FeO+3KNO +2H O;(3)氨气通入硫酸铜溶液中,先产生氢氧化铜絮状沉淀,继
2 3 3 2 4 2 2
续通入氨气,生成的深蓝色溶液为硫酸四氨合铜溶液,离子反应方程式为:Cu2+
+2NH·H O=Cu(OH) ↓+2NH+,Cu(OH) +4NH=[Cu((NH )]2++2OH-;(4)根据X的化学式,滤液A 中含
3 2 2 4 2 3 3 4
15
原创精品资源学科网独家享有版权,侵权必究!
15
学科网(北京)股份有限公司(NH )SO 和NH ;(5)沉淀A为氢氧化铁,先用酸将沉淀溶解,再检验铁离子,方法为:取少量沉淀A试
4 2 4 3
管中,加入适量稀硫酸溶解,向其中加入少量KSCN溶液,无明显变化,继续加入氯水,溶液呈红色,说
明沉淀A中含有Fe2+。
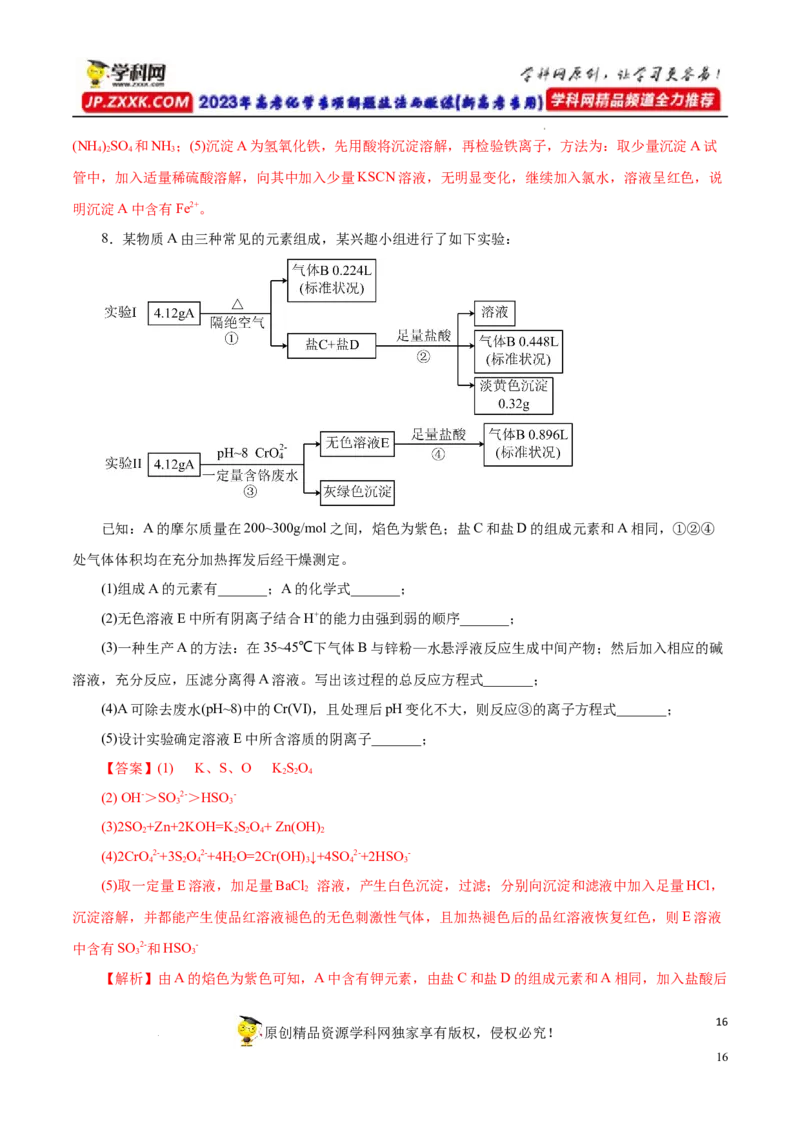
8.某物质A由三种常见的元素组成,某兴趣小组进行了如下实验:
已知:A的摩尔质量在200~300g/mol之间,焰色为紫色;盐C和盐D的组成元素和A相同,①②④
处气体体积均在充分加热挥发后经干燥测定。
(1)组成A的元素有_______;A的化学式_______;
(2)无色溶液E中所有阴离子结合H+的能力由强到弱的顺序_______;
(3)一种生产A的方法:在35~45℃下气体B与锌粉—水悬浮液反应生成中间产物;然后加入相应的碱
溶液,充分反应,压滤分离得A溶液。写出该过程的总反应方程式_______;
(4)A可除去废水(pH~8)中的Cr(VI),且处理后pH变化不大,则反应③的离子方程式_______;
(5)设计实验确定溶液E中所含溶质的阴离子_______;
【答案】(1) K、S、O KSO
2 2 4
(2) OH->SO 2->HSO -
3 3
(3)2SO +Zn+2KOH=K SO+ Zn(OH)
2 2 2 4 2
(4)2CrO 2-+3S O2-+4H O=2Cr(OH) ↓+4SO2-+2HSO -
4 2 4 2 3 4 3
(5)取一定量E溶液,加足量BaCl 溶液,产生白色沉淀,过滤;分别向沉淀和滤液中加入足量HCl,
2
沉淀溶解,并都能产生使品红溶液褪色的无色刺激性气体,且加热褪色后的品红溶液恢复红色,则E溶液
中含有SO 2-和HSO -
3 3
【解析】由A的焰色为紫色可知,A中含有钾元素,由盐C和盐D的组成元素和A相同,加入盐酸后
16
原创精品资源学科网独家享有版权,侵权必究!
16
学科网(北京)股份有限公司生成淡黄色沉淀和无色气体B可知,淡黄色沉淀为硫、气体B为二氧化硫,则A中含有钾元素、硫元素和
氧元素;由实验Ⅱ可知,A中含有硫元素的物质的量为 =0.04mol,由盐C和盐D生成0.32g硫和
0.448L二氧化硫可知,盐C和盐D中硫代硫酸钾的物质的量为 =0.1mol,亚硫酸钾的物质的量为
—0.01mol=0.01mol,则4.12gA隔绝空气受热分解生成0.01mol亚硫酸钾、0.01mol硫代硫酸钾
和 =0.01mol二氧化硫,由原子个数守恒可知A中钾元素、硫元素和氧元素的物质的量比为
0.01mol×4:0.04mol:(0.01mol×3+0.01mol×3+0.01mol×2)=1:1:2,由A的摩尔质量在200~300g/mol之间
和得失电子数目守恒可知,A的化学式为KSO。(1) A中含有钾元素、硫元素和氧元素,化学式为
2 2 4
KSO;(2)由A除去废水(pH~8)中的Cr(VI)时生成无色溶液E和灰绿色沉淀,且处理后pH变化不大可知,
2 2 4
反应③发生的反应为2CrO2-+3S O2-+4H O=2Cr(OH) ↓+4SO2-+2HSO -,则溶液E中含有的阴离子为氢氧根
4 2 4 2 3 4 3
离子、亚硫酸根离子、亚硫酸氢根离子,由碱性强的离子优先与氢离子反应可知,三种离子反应的顺序为
氢氧根离子、亚硫酸根离子、亚硫酸氢根离子,即OH->SO 2->HSO -;(3)由题意可知生成A的反应为二
3 3
氧化硫、锌和氢氧化钾溶液反应A和氢氧化锌,反应的化学方程式为2SO +Zn+2KOH=K SO+ Zn(OH) ;
2 2 2 4 2
(4)由A除去废水(pH~8)中的Cr(VI)时生成无色溶液E和灰绿色沉淀,且处理后pH变化不大可知,反应③
发生的反应为2CrO2-+3S O2-+4H O=2Cr(OH) ↓+4SO2-+2HSO -;(5)由A除去废水(pH~8)中的Cr(VI)时生成
4 2 4 2 3 4 3
无色溶液E和灰绿色沉淀,且处理后pH变化不大可知,反应③发生的反应为2CrO2-+3S O2-
4 2 4
+4H O=2Cr(OH) ↓+4SO2-+2HSO -,溶液E为亚硫酸钾和亚硫酸氢钾,亚硫酸根离子和亚硫酸氢根离子均能
2 3 4 3
与盐酸反应生成使品红溶液褪色的二氧化硫,所以检验溶液中亚硫酸根离子和亚硫酸氢根离子时,应先加
入氯化钡溶液使亚硫酸根离子转化为亚硫酸钡沉淀,过滤后向滤液和沉淀中加入稀盐酸观察是否有能使品
红溶液褪色的二氧化硫生成,具体操作为取一定量E溶液,加足量BaCl 溶液,产生白色沉淀,过滤;分
2
别向沉淀和滤液中加入足量HCl,沉淀溶解,并都能产生使品红溶液褪色的无色刺激性气体,且加热褪色
后的品红溶液恢复红色,则E溶液中含有SO 2-和HSO -。
3 3
9.(2022·浙江省杭州二中、温州中学、金华一中高三选考模拟)X是一种由4种短周期元素组成含结晶
水的盐。某兴趣小组按如下流程进行实验(所用试剂均足量):
17
原创精品资源学科网独家享有版权,侵权必究!
17
学科网(北京)股份有限公司其中:X微溶于水。溶液D中仅有一种溶质。红棕色沉淀H是一种钠盐。请回答:
(1)组成X的元素有_______,X的化学式为_______。
(2)无色溶液F中的溶质是(用化学式表示):_______。
(3)上图生红棕色沉淀H时,溶液D中的溶质与Cu(OH) 的物质的量之比为1:2,则其离子反应方程
2
式是_______。
(4)设计实验验证溶液D中的阴离子_______。
【答案】(1) Mg、Cl、O、H MgClO(OH) ·H O或Mg(ClO) ·3Mg(OH) ·2H O
2 3 2 2 2 2
(2)NaCl、NaSO 、NaOH
2 4
(3) 2Na++ClO-+2 Cu(OH) +2OH-=2NaCuO +Cl-+3H O
2 2 2
(4)取适量D溶液,滴加到pH试纸上,试纸先变蓝后褪色
【解析】溶液D中仅有一种溶质,D和新制氢氧化铜悬浊液反应生成红棕色沉淀H,H是一种钠盐,
可知H是NaCuO ,为氧化产物,说明D具有氧化性,F和硝酸银反应生成白色沉淀,则D的还原产物是
2
氯化钠,溶液D中的溶质与Cu(OH) 的物质的量之比为1:2,根据电子守恒,可知D为NaClO;反应生成
2
AgCl的物质的量是 ,3.37g X中含有0.02molClO-;3.37g X和氢氧化钠反应生成
2.32g白色沉淀E,E为氢氧化物沉淀,E加热生成1.6g白色固体B,B是氧化物, ,
假设x=1,R的相对原子质量为M, ,M=12;假设x=2,R的相对原子质量为M,
18
原创精品资源学科网独家享有版权,侵权必究!
18
学科网(北京)股份有限公司,M=24;Mg的相对原子质量是24,所以E是Mg(OH) ,物质的量为0.04mol,所以X中
2
Mg2+的物质的量是0.04mol;则3.37g X含0.01molMg(ClO) 、0.03molMg(OH) ,含结晶水的物质的量是
2 2
。(1)根据以上分析,组成X的元素有Mg、Cl、H、
O四种元素;3.37g X含0.01molMg(ClO) 、0.03molMg(OH) ,结晶水0.02mol,所以X的化学式为
2 2
Mg(ClO) ·3Mg(OH) ·2H O;(2)溶液D中仅有一种溶质NaClO,NaClO和新制氢氧化铜悬浊液反应生成
2 2 2
NaCuO 沉淀、NaCl,所以F中含有的溶质是NaCl、以及氢氧化铜悬浊液中的NaSO 、NaOH;(3)NaClO
2 2 4
和新制氢氧化铜悬浊液反应生成NaCuO 沉淀、NaCl,根据得失电子守恒,反应的离子方程式为2Na++ClO-
2
+2 Cu(OH) +2OH-=2NaCuO +Cl-+3H O;(4)D中溶质是NaClO,NaClO具有强氧化性,溶液呈碱性,取适
2 2 2
量D溶液,滴加到pH试纸上,试纸先变蓝后褪色,证明含有ClO-。
10.(2022·浙江省义乌市高三选考适应性考试)固体X由4种元素组成的化合物,它是一种重要的催化
剂。某学习小组开展了如图实验进行探究:
实验一:
实验二:
已知:黄色溶液A和无色溶液F仅含一种溶质。
(1)X的组成元素___,X的化学式____。
(2)写出固体X与氢氧化钠溶液反应的化学方程式____。
(3)溶液B和溶液C均含有与冰晶石中结构类似的阴离子,写出B转化成C的离子方程式____。
(4)黄色溶液A中的水合金属阳离子为浅紫色,溶液A呈黄色的原因是____。为了观察溶液A中的水
合金属阳离子为浅紫色,可以采取____的措施。
【答案】(1) Fe、S、H、O Fe (OH) (SO )
4 2 4 5
(2)Fe (OH) (SO )+10NaOH=5Na SO +4Fe(OH) ↓
4 2 4 5 2 4 3
19
原创精品资源学科网独家享有版权,侵权必究!
19
学科网(北京)股份有限公司(3)Fe(SCN) 3-+6F-=FeF 3-+6SCN-
6 6
(4) 铁离子水解产生氢氧化铁与水合铁离子两种颜色共同作用结果 向溶液中加入适量硫酸溶
液
【解析】7.38gX和0.1mol氢氧化钠反应生成红褐色沉淀D,则D为Fe(OH) ,Fe(OH) 加热分解为黑
3 3
色固体E,E是Fe O;n(Fe O)= ,根据铁元素守恒,7.38gX中含n(Fe3+)=0.04mol,n
2 3 2 3
[Fe(OH) ]=0.04mol,反应共消耗氢氧根离子的物质的量为0.12mol,所以7.38gX中含有0.02mol氢氧根
3
离子;7.38gX和0.06mol硫酸反应得到溶液A,溶液A仅含一种溶质,则A是Fe (SO ),根据铁元素守恒,
2 4 3
n[Fe (SO )]=0.02mol,根据S元素守恒,7.38gX中含(0.06-0.01)mol硫酸根离子。(1) 7.38gX中含有
2 4 3
0.02mol氢氧根离子、0.04molFe3+、0.05mol硫酸根离子,所以X的组成元素Fe、S、H、O,X的化学式
Fe (OH) (SO );(2)Fe (OH) (SO ) 与氢氧化钠溶液反应生成氢氧化铁沉淀和硫酸钠,反应的化学方程式为
4 2 4 5 4 2 4 5
Fe (OH) (SO )+10NaOH=5Na SO +4Fe(OH) ↓;(3)冰晶石中的阴离子为AlF3-,溶液B和溶液C均含有与冰
4 2 4 5 2 4 3 6
晶石中结构类似的阴离子,B转化成C的离子方程式Fe(SCN) 3-+6F-=FeF 3-+6SCN-。(4)黄色溶液A中的水
6 6
合金属阳离子为浅紫色,Fe3+易水解,溶液A呈黄色的原因是铁离子水解产生氢氧化铁与水合铁离子两种
颜色共同作用结果。为了观察溶液A中的水合金属阳离子为浅紫色,可以向溶液中加入适量硫酸溶液,抑
制Fe3+水解。
11.(2022·浙江省高三考前第三次模拟考试)液态化合物 是电镀行业的重要试剂,由中学阶段常见的
5种元素组成。某小组按如下流程进行实验:
实验1:
20
原创精品资源学科网独家享有版权,侵权必究!
20
学科网(北京)股份有限公司实验2:
已知:物质 与NaOH溶液的反应属于非氧化还原反应。请回答:
(1)组成 的元素有_______, 的化学式为_______。
(2) 与浓 溶液共热的化学方程式为_______。
(3)溶液 中的溶质有:HO、BaCl 、_______(填化学式)。
2 2 2
(4)溶液 中存在动态平衡,某同学欲探究物质浓度对该平衡的影响,已有方案:
①向溶液 中加 固体,观察现象;
②向溶液 中加浓FeCl 溶液,观察现象;
3
请设计方案③:_______(写出操作、现象及相应结论)。
【答案】(1) Fe、S、O、N、H Fe(SO NH )
3 2 2
(2)Fe(SO NH )+4NaOH 2NH ↑+Fe(OH) ↓+ 2Na SO
3 2 2 3 2 2 4
(3)HCl、NH Cl
4
(4)向溶液N中加铁粉,若红色变浅,说明溶液N中存在动态平衡
【解析】实验1中,X隔绝空气加热,生成固体A和混合气体,混合气体通入含有过氧化氢的BaCl
2
溶液中,生成的白色沉淀C是BaSO,BaSO 的物质的量是 ,说明混合气体中含有
4 4
0.03mol SO ;实验2中,物质 与 溶液的反应属于非氧化还原反应,反应生成1.344L标准状况下刺
2
激性气味的气体E,可知生成0.06mol NH ,所以7.44g X中含有0.06mol N元素;反应生成白色沉淀F,白
3
色沉淀F和氧气反应生成红褐色沉淀G,G是Fe(OH) ,F是Fe(OH) ,Fe(OH) 加热分解为红色粉末H,H
3 2 3
是Fe O,Fe O 的物质的量是 ;则X中含有0.03mol Fe;X和氢氧化钠反应后的溶液
2 3 2 3
中加入BaCl 溶液生成BaSO 沉淀,说明X中S元素为+6价;根据铁元素守恒,可以得知实验1中,固体
2 4
21
原创精品资源学科网独家享有版权,侵权必究!
21
学科网(北京)股份有限公司A的摩尔质量是 、A是0.03mol FeSO ,则根据硫元素守恒,7.44g X中含有0.06mol S
4
元素;根据氧元素守恒,7.44g X中含有氧元素0.03×4+0.03×2=0.18mol;X由5种元素组成,则H元素的
物质的量为 mol。(1)根据以上分析,组成X的元素有Fe、
S、O、N、H,根据个元素的物质的量比n(Fe):n(S):n(O):n(N):n(H)=0.03:0.06:0.18:0.06:
0.12=1:2:6:2:4,X的化学式为Fe(SO NH );(2)根据流程图,X与浓NaOH溶液共热生成氨气、硫酸
3 2 2
钠、氢氧化亚铁,反应的化学方程式为Fe(SO NH )+4NaOH 2NH ↑+Fe(OH) ↓+ 2Na SO ;(3)X分解的方
3 2 2 3 2 2 4
程式为3Fe(SO NH ) 3FeSO +3SO↑+4NH↑+N ↑,混合气体通入含有过氧化氢的BaCl 溶液中,发生反应
3 2 2 4 2 3 2 2
HO+SO+BaCl =BaSO ↓+2HCl,HCl+ NH =NHCl,溶液D中的溶质有:HO、BaCl 、HCl、NH Cl;(4)
2 2 2 2 4 3 4 2 2 2 4
溶液N中存在平衡Fe3++3SCN- Fe(SCN) ,向溶液N中加铁粉,发生反应2 Fe3++ Fe=3Fe2++,Fe3+浓度
3
减小,若红色变浅,说明溶液N中存在动态平衡。
12.(2022·浙江省东阳市高三选考模拟考试)化合物X由5种元素组成。某兴趣小组按如下流程进行实
验:
实验I
实验II
请回答:
(1)溶液F的溶质是_______,组成X的金属元素有_______(填元素符号),X的化学式为_______。
(2)2 0.1 mol·L-1溶液A中加入2 0.1 mol·L-1 ,再加几滴 、淀粉溶液,振荡后加入5滴
氯水,溶液先变红再变蓝。从上述现象中可以得到的结论有_______。
(3)C→D的总化学方程式是_______。
(4)溶液E中的紫色离子的平均组成可表示为 ,请设计定量实验测定紫色离子中的n值:_______。
【答案】(1) NaSO Fe、Na NaFe (SO )(OH)
2 4 2 3 4 2 4
22
原创精品资源学科网独家享有版权,侵权必究!
22
学科网(北京)股份有限公司(2)结论1:氧化性:Cl>Fe2+>I;结论2:Cl 氧化Fe2+的速率比Cl 氧化I-的速率快
2 2 2 2
(3) 4Fe(OH) +O =2 Fe O+4H O
2 2 2 3 2
(4)分别取两份20.00 mL 0.1 mol·L-1 FeCl 溶液,一份加足量苯酚溶液,将两份溶液均定容至100 mL
3
并测定稀释后溶液的pH,根据pH可计算n值
【解析】9.48g化合物X与40mL1mol/L的NaOH溶液反应生成白色沉淀C和溶液F,F与BaCl 溶液
2
反应生成9.32g BaSO 沉淀,F只含1种溶质,说明F是 NaSO ,n(BaSO)= ,则
4 2 4 4
n(Na SO )=0.04mol,则9.48g X中一定含有0.04mol SO 2-、(0.08-0.04×1mol/L) =0.04molNa+;白色沉淀C在
2 4 4
空气中加热搅拌得4.8g红褐色固体D,D与盐酸反应后的溶液中加入苯酚,溶液呈紫色,说明D是
Fe O,n(Fe O)= ,则C是Fe(OH) ,则9.48g X中一定含有0.06molFe2+;化合物X由5
2 3 2 3 2
种元素组成,9.48g X能与40mL1mol/L的硫酸恰好反应,说明X含有0.08molOH-。(1)根据以上分析,溶
液F的溶质是NaSO ;9.48g X中含有0.04molSO 2-、0.04molNa+、0.08molOH-、0.06mol Fe2+;组成X的金
2 4 4
属元素有Fe、Na,X的化学式为NaFe (SO )(OH) ;(2)A是FeSO 、NaSO 的混合液,2 mL 0.1 mol·L-1溶
2 3 4 2 4 4 2 4
液A中加入2 mL 0.1 mol·L-1KI,再加几滴KSCN、淀粉溶液,振荡后加入5滴氯水,溶液先变红再变蓝。
说明,氯气把Fe2+氧化为Fe3+,Fe3+又把I-氧化为I,从上述现象中可以得到的结论有:结论1:氧化性:
2
Cl>Fe2+>I;结论2:Cl 氧化Fe2+的速率比Cl 氧化I-的速率快。(3)C是Fe(OH) ,D是Fe O,C→D的总
2 2 2 2 2 2 3
化学方程式是4Fe(OH) +O = 2Fe O+4H O;(4)苯酚用HB表示,则反应方程式表示为
2 2 2 3 2
,分别取两份20.00 mL 0.1 mol·L-1 FeCl 溶液,一份加足量苯酚溶液,将两份溶液
3
均定容至100 mL并测定稀释后溶液的pH,根据pH可计算n值。
13.(2022·浙江省精诚联盟高三适应性考试)化合物A由4种元素组成,实验如下:
23
原创精品资源学科网独家享有版权,侵权必究!
23
学科网(北京)股份有限公司已知:除说明外,加入试剂均为足量;生成1molF时消耗3/4mol的HPO
3 2
回答下列问题:
(1)G的分子式为_______,A的化学式为_______。
(2)溶液B中溶质成分是_______(用化学式表示),根据C→D→E的现像,给出相应微粒与阳离子结合
由强到弱的排序_______。
(3)写出A与HPO 反应的化学方程式_______。
3 2
(4)检验溶液M的主要阴离子(任选2种)_______。
【答案】(1) H Cu (OH) SO
2 2 2 4
(2) HCl、CuCl 、CuSO S2->NH >Cl-
2 4 3
(3)2Cu (OH) SO +3H PO +2H O=4 CuH+2HSO +3H PO
2 2 4 3 2 2 2 4 3 4
(4)取溶液M滴加酚酞变红,证明溶液有OH-,另取溶液加足量盐酸,再加BaCl 溶液,产生白色沉淀,
2
证明有SO 2-;(或者)另取溶液加足量BaCl 产生白色沉淀,再加稀盐酸,发现白色沉淀部分溶解,说明溶
4 2
液存在SO 2-和PO 3-
4 4
【解析】根据图中信息可知,2.58gA与盐酸反应得到蓝绿色溶液B、B加氯化钡溶液得到白色沉淀为
不溶于酸的硫酸钡,n(BaSO)= ,则2.58gA中含0.01mol硫酸根离子,蓝绿色溶液B
4
转变为黄绿色溶液C,再加氨水得到深蓝色溶液D为铜氨配合物,含[Cu(NH )] 2+离子,溶液B、C中均含
3 4
有结构相似的配离子,则B含有CuCl 2-离子, C含[Cu(H O) ] 2+离子, E为CuS沉淀。2.58gA与HPO
4 2 4 3 2
反应,生成红棕色沉淀F1.32g,F在60°C时分解为紫红色固体1.28g H为Cu, 则n(Cu)=0.2mol,
m(Cu)=12.8g,则无色气体G为1.30g-1.28g=0.02g,F→H时铜元素化合价降低,则F→G时元素化合价升
高,按得失电子数守恒,G为H 时满足,则0.02g H、n(H )=0.01mol, n(H)=0.02mol,则F中铜与氢物质
2 2 2
的量之比为1:1,故F为CuH,满足已知条件:A与HPO 反应,生成1molF时消耗3/4mol的HPO ,则转
3 2 3 2
24
原创精品资源学科网独家享有版权,侵权必究!
24
学科网(北京)股份有限公司移电子3mol(铜从+2降低到+1、氢从+1降低到-1);化合物A由4种元素组成, 2.58gA中含0.01mol硫酸
根离子、质量为0.96g,n(Cu)=0.02mol,m(Cu)=1.28g,n(H)=0.02mol,m(H)=0.02g,剩余质量为0.32g,应
该还含有O元素,m(O)=0.32g,n(O)= 0.02mol,则A应该为碱式硫酸铜铜,根据化合价及元素比可知其化
学式为Cu (OH) SO 。(1) G的分子式为H,A的化学式为Cu (OH) SO 。(2)溶液B 为Cu (OH) SO 与盐酸
2 2 4 2 2 2 4 2 2 4
反应所得,则溶质成分是HCl、CuCl 、CuSO ;黄绿色溶液C含CuCl 2-离子,加氨水得到深蓝色溶液D含
2 4 4
[Cu(NH )] 2+离子,E为CuS沉淀,根据C→D→E转化关系,可得出相应微粒与阳离子铜离子结合由强到
3 4
弱的排序S2->NH >Cl-。(3)A为Cu (OH) SO ,与HPO 发生氧化还原反应,P从+1升高到+5、铜从+2降
3 2 2 4 3 2
低到+1、氢从+1降低到-1,得到CuH、磷酸和硫酸,化学方程式2Cu (OH) SO +3H PO +2H O=4
2 2 4 3 2 2
CuH+2HSO +3H PO 。(4)M含硫酸钠、磷酸钠和多余的氢氧根离子,检验溶液M的主要阴离子(任选2种)
2 4 3 4
的方法为 :取溶液M滴加酚酞变红,证明溶液有OH-,另取溶液加足量盐酸,再加BaCl 溶液,产生白色
2
沉淀,证明有SO 2-;(或者)另取溶液加足量BaCl 产生白色沉淀,再加稀盐酸,发现白色沉淀部分溶解,
4 2
说明溶液存在SO 2-和PO 3-。
4 4
14.(2022·浙江省浙大附中高三仿真模拟)化合物M由4种常见元素组成。某兴趣小组进行如下实验
(每一步反应均充分进行):
已知:①M易形成类似于氨基酸的内盐
②混合气体A中含有单质气体
③无色粘稠油状液体为纯净物。
请回答:
(1)组成M的元素是__________________(填元素符号)
(2)M的化学式为__________________
(3)写出无色溶液E中溶质__________________
25
原创精品资源学科网独家享有版权,侵权必究!
25
学科网(北京)股份有限公司(4)M能与次氯酸钠溶液反应,得到无色溶液G和无色气体C。
①写出该反应的化学方程式:________________________
②设计实验验证该无色溶液G中的阴离子:____________
【答案】(1)H、N、O、S
(2)H NSO H或NH SO
2 3 3 3
(3) NHCl、BaCl
4 2
(4) 2HNSO H+3NaClO=2H SO +3NaCl+N↑+H O
2 3 2 4 2 2
取少量无色溶液G于试管中,加入过量稀盐酸,若无明显现象,滴加氯化钡溶液,若有白色沉淀,
说明含有SO 2-;另取少量溶液G于试管中,加入过量硝酸钡,振荡,静置,取上层清液,滴加硝酸银溶液,
4
若有白色沉淀,说明有Cl-
【解析】实验II,M形成水溶液D,与氯化钡反应生成白色沉淀,结合实验I分解后生成粘稠油状液
体,反应说明生产硫酸钡,说明M含有硫,E溶液加入NaOH溶液产生使蓝色石蕊试纸变蓝的气体,说明
M的水溶液中含有铵根离子,白色沉淀为23.3g,则硫酸钡为0.1mol,说明D含有0.1mol的硫酸根,实验I
中,粘稠油状液体为4.9g即硫酸为0.05mol,A冷却后B为SO 、H、N,B通过碱石灰增重3.2g为二氧化
2 2 2
硫,由固体氧化铜减重1.6g ,得氢气的物质的量为0.1mol,无色气体C为氮气,所以,由实验I可得
9.7gM含有SO 、H、N、HSO 各3.2g,0.2g,1.4g,4.9g,所以组成M的元素是H、N、O、S,M的化
2 2 2 2 4
学式为HNSO H或NH SO 。(1)组成M的元素是H、N、O、S;(2) M的化学式为HNSO H或NH SO ;
2 3 3 3 2 3 3 3
(3)根据题目信息可知,无色溶液E中含有铵根及过量的氯化钡。所以E中溶质为:NH Cl、BaCl ;(4)M
4 2
与次氯酸钠溶液反应,得到无色溶液G和无色气体C,其中C为氮气,反应的化学方程式为:
2HNSO H+3NaClO=2H SO +3NaCl+N↑+H O;无色溶液G中的阴离子为硫酸根和氯离子,可取少量无色
2 3 2 4 2 2
溶液G于试管中,加入过量稀盐酸,若无明显现象,滴加氯化钡溶液,若有白色沉淀,说明含有SO 2-;另
4
取少量溶液G于试管中,加入过量硝酸钡,振荡,静置,取上层清液,滴加硝酸银溶液,若有白色沉淀,
说明有Cl-。
15.(2022·浙江省绍兴市高三选考科目适应性考试二模)结晶水合物X由4种元素组成。某兴趣小组按
如下流程进行实验:
26
原创精品资源学科网独家享有版权,侵权必究!
26
学科网(北京)股份有限公司请回答:
(1)组成X的元素除H、O外还有 ___________,X的化学式为 ___________。
(2)溶液D中属于盐的成分是 ___________ ( 用化学式表示);若溶液C中滴入少量氨水,则首先参与
反应的微粒是_____
(3)请写出E →F化学方程式___________。
(4)设计实验方案确定溶液H中的阴离子___________。
【答案】(1) Cu、Cl CuCl ∙2HO
2 2
(2) NH NO 、Ag(NH)NO 、Cu(NH )(NO ) H+
4 3 3 2 3 3 4 3 2
(3)2CuCl Cl+2CuCl
2 2
(4)取少量H溶液,滴加酚酞,若变红,则含有OH-;另取少量H溶液,加入硝酸酸化,再加硝酸银溶
液,若有白色沉淀生成,则含有Cl-
【解析】由实验Ⅰ可知,溶液C中加入过量氨水,生成蓝色沉淀D,则D中含有[Cu(NH )]2+,X中含
3 4
有铜元素;白色沉淀B为AgCl,n(AgCl)= ,20mL1.0mol/L盐酸中所含Cl-的物质的量
为0.02mol,则X中所含Cl-的物质的量为0.04mol-0.02mol=0.02mol,从而得出X中含有CuCl ,其物质的
2
量为0.01mol。由实验Ⅱ可知,结晶水的质量为1.71g-1.35g=0.36g,物质的量为 ,CuCl
2
27
原创精品资源学科网独家享有版权,侵权必究!
27
学科网(北京)股份有限公司的物质的量为0.01mol,生成Cl 的物质的量为 ,则固体G为CuCl。综合实验Ⅰ、Ⅱ,
2
X的化学式为CuCl ∙2HO。(1)由以上分析可知,组成X的元素除H、O外还有Cu、Cl,X的化学式为
2 2
CuCl ∙2HO;(2)由分析可知,溶液C中含有过量的AgNO、Cu(NO )、HNO 等,加入过量氨水,AgNO
2 2 3 3 2 3 3
最终生成Ag(NH)NO ,Cu(NO ) 最终生成Cu(NH )(NO ),另外还有NH NO 生成,则溶液D中属于盐的
3 2 3 3 2 3 4 3 2 4 3
成分是NH NO 、Ag(NH)NO 、Cu(NH )(NO );若溶液C中滴入少量氨水,则首先与HNO 反应,所以
4 3 3 2 3 3 4 3 2 3
首先参与反应的微粒是H+;(3)由分析知,E为CuCl 、F为Cl,则E →F化学方程式为2CuCl
2 2 2
Cl+2CuCl;(4)固体G为CuCl,加入过量氨水,则溶液H中所含阴离子可能为Cl-、OH-,确定溶液H中的
2
阴离子的方法是:取少量H溶液,滴加酚酞,若变红,则含有OH-;另取少量H溶液,加入硝酸酸化,再
加硝酸银溶液,若有白色沉淀生成,则含有Cl-。
16.(2022·浙江省高三下学期高考选考科目联考)化合物X由4种元素组成。某兴趣小组按如图流程进
行实验(每一步反应均充分进行):
请回答:
(1)组成X的4种元素是____(填元素符号)。
(2)无色溶液D中的溶质是____(填化学式)。
(3)无色气体A中的气体分子有____(填化学式)。
(4)气态X分子中,H原子与2种元素的原子形成共价键,但红外光谱和1H核磁共振谱均显示固态X
晶体中的H原子化学环境完全相同。且熔点明显高于相对分子量接近的分子晶体,原因是____。
(5)X能与氯酸钾在水溶液中反应,得到无色溶液F和无色气体C。
28
原创精品资源学科网独家享有版权,侵权必究!
28
学科网(北京)股份有限公司①写出该反应的化学方程式:____。
②设计实验验证该无色溶液F中的阴离子:____。
【答案】(1)H、N、O、S
(2)NH HSO 或HSO 、(NH )SO
4 4 2 4 4 2 4
(3)H O、SO 、SO 、H、N
2 3 2 2 2
(4)X分子中的氨基和磺酸基反应生成+HNSO -,类似氨基酸形成内盐,和铵根离子结构类似,故与N
3 3
原子结合的H原子化学环境相同
(5) 2HNSO H+KClO=2H SO +KCl+N ↑+H O 取少量无色溶液F于试管中,加入过量稀盐酸,若无
2 3 3 2 4 2 2
明显现象,滴加氯化钡溶液,若有白色沉淀,说明含有SO 2-;另取少量溶液F于试管中,加入过量硝酸钡,
4
振荡,静置,取上层清液,滴加硝酸银溶液,若有白色沉淀,说明有Cl-
【解析】实验Ⅱ,X形成水溶液D,与氯化钡反应生产白色沉淀,结合实验Ⅰ分解后生成粘稠油状液
体,反应说明生产硫酸钡,说明X含有硫,E溶液加入NaOH溶液产生使蓝色石蕊试纸变蓝的气体,说明
X的水溶液中含有铵根离子,白色沉淀为11.65g则为 =0.05mol硫酸钡,说明D含有0.05mol的
硫酸根,实验Ⅰ中,粘稠油状液体为 =0.025mol,A冷却后B为SO 、H、N,B通过碱石灰增
2 2 2
重1.6g为二氧化硫, =0.025mol,由固体氧化铜减重0.8g,得氢气的物质的量为,
=0.05mol,无色气体C为氮气,实验Ⅰ发生:
X水溶液D可以看成是0.025mol硫酸和0.025mol硫酸铵的混合物,X水溶液D也可以看成是
0.05molNH HSO ,由此可知X中应含有H、N、O、S,X为NH SO H,无色气体A中的气体分子有
4 4 2 3
HO、SO 、SO 、H、N。(1)组成X的4种元素是H、N、O、S(填元素符号);(2)无色溶液D中的溶质是
2 3 2 2 2
29
原创精品资源学科网独家享有版权,侵权必究!
29
学科网(北京)股份有限公司NH HSO 或HSO 、(NH )SO (填化学式);(3)无色气体A中的气体分子有HO、SO 、SO 、H、N;(4)X
4 4 2 4 4 2 4 4 2 3 2 2 2
为NH SO H,气态X分子中,H原子与2种元素的原子形成共价键,但红外光谱和1H核磁共振谱均显示
2 3
固态X晶体中的H原子化学环境完全相同。且熔点明显高于相对分子量接近的分子晶体,说明X晶体产生
了离子键,原因是X分子中的氨基和磺酸基反应生成+HNSO ,类似氨基酸形成内盐,和铵根离子结构类
3
似,故与N原子结合的H原子化学环境相同。故选X分子中的氨基和磺酸基反应生成+HNSO -,类似氨基
3 3
酸形成内盐,和铵根离子结构类似,故与N原子结合的H原子化学环境相同;(5)①X为NH SO H,X能
2 3
与氯酸钾在水溶液中反应,得到无色溶液F和无色气体C,C为氮气。反应的化学方程式:
2HNSO H+KClO=2H SO +KCl+N ↑+H O;②设计实验验证该无色溶液F中的阴离子:取少量无色溶液F
2 3 3 2 4 2 2
于试管中,加入过量稀盐酸,若无明显现象,滴加氯化钡溶液,若有白色沉淀,说明含有SO 2-;另取少量
4
溶液F于试管中,加入过量硝酸钡,振荡,静置,取上层清液,滴加硝酸银溶液,若有白色沉淀,说明有
Cl-,故选取少量无色溶液F于试管中,加入过量稀盐酸,若无明显现象,滴加氯化钡溶液,若有白色沉淀,
说明含有SO 2-;另取少量溶液F于试管中,加入过量硝酸钡,振荡,静置,取上层清液,滴加硝酸银溶液,
4
若有白色沉淀,说明有Cl-。
17.(2022·浙江省金丽衢十二校、七彩联盟高三阶段性联考)液态化合物 是电镀行业的重要试剂,由
中学阶段常见的5种元素组成。某小组按如下流程进行实验:
实验1:
实验2:
已知:物质 与NaOH溶液的反应属于非氧化还原反应。请回答:
30
原创精品资源学科网独家享有版权,侵权必究!
30
学科网(北京)股份有限公司(1)组成 的元素有_______, 的化学式为_______。
(2) 与浓NaOH溶液共热的化学方程式为_________________________。
(3)溶液 中的溶质有:HO、BaCl 、_______(填化学式)。
2 2 2
(4)溶液 中存在动态平衡,某同学欲探究物质浓度对该平衡的影响,已有方案:
①向溶液 中加 固体,观察现象;
②向溶液 中加浓FeCl 溶液,观察现象;
3
请设计方案③:_______(写出操作、现象及相应结论)。
【答案】(1) Fe、S、O、N、H Fe(SO NH )
3 2 2
(2)Fe(SO NH )+4NaOH 2NH ↑+Fe(OH) ↓+ 2Na SO
3 2 2 3 2 2 4
(3)HCl、NH Cl
4
(4)向溶液N中加铁粉,若红色变浅,说明溶液N中存在动态平衡
【解析】实验1中,X隔绝空气加热,生成固体A和混合气体,混合气体通入含有过氧化氢的BaCl
2
溶液中,生成的白色沉淀C是BaSO,BaSO 的物质的量是 ,说明混合气体中含有
4 4
0.03mol SO ;实验2中,物质X与NaOH溶液的反应属于非氧化还原反应,反应生成1.344L标准状况下刺
2
激性气味的气体E,可知生成0.06mol NH ,所以7.44g X中含有0.06mol N元素;反应生成白色沉淀F,白
3
色沉淀F和氧气反应生成红褐色沉淀G,G是Fe(OH) ,F是Fe(OH) ,Fe(OH) 加热分解为红色粉末H,H
3 2 3
是Fe O,Fe O 的物质的量是 ;则X中含有0.03mol Fe;X和氢氧化钠反应后的溶液
2 3 2 3
中加入BaCl 溶液生成BaSO 沉淀,说明X中S元素为+6价;根据铁元素守恒,可以得知实验1中,固体
2 4
A的摩尔质量是 、A是0.03mol FeSO ,则根据硫元素守恒,7.44g X中含有0.06mol S
4
元素;根据氧元素守恒,7.44g X中含有氧元素0.03×4+0.03×2=0.18mol;X由5种元素组成,则H元素的
物质的量为 mol。(1)根据以上分析,组成X的元素有Fe、
S、O、N、H,根据个元素的物质的量比n(Fe):n(S):n(O):n(N):n(H)=0.03:0.06:0.18:0.06:
31
原创精品资源学科网独家享有版权,侵权必究!
31
学科网(北京)股份有限公司0.12=1:2:6:2:4, 的化学式为Fe(SO NH );(2)根据流程图,X与浓NaOH溶液共热生成氨气、硫酸
3 2 2
钠、氢氧化亚铁,反应的化学方程式为Fe(SO NH )+4NaOH 2NH ↑+Fe(OH) ↓+ 2Na SO ;(3)X分解的方
3 2 2 3 2 2 4
程式为3Fe(SO NH ) 3FeSO +3SO↑+4NH↑+N ↑,混合气体通入含有过氧化氢的BaCl 溶液中,发生反应
3 2 2 4 2 3 2 2
HO+SO+BaCl =BaSO ↓+2HCl,HCl+ NH =NHCl,溶液D中的溶质有:HO、BaCl 、HCl、NH Cl;(4)
2 2 2 2 4 3 4 2 2 2 4
溶液N中存在平衡Fe3++3SCN- Fe(SCN) ,向溶液N中加铁粉,发生反应2Fe3++ Fe=3Fe2+,Fe3+浓度
3
减小,若红色变浅,说明溶液N中存在动态平衡。
32
原创精品资源学科网独家享有版权,侵权必究!
32
学科网(北京)股份有限公司33
原创精品资源学科网独家享有版权,侵权必究!
33
学科网(北京)股份有限公司