文档内容
第六篇 物质结构与性质
专项 44 晶胞的计算
晶胞计算是晶体考查的重要知识点之一,也是考查学生分析问题、解决问题能力的较好素材。晶胞的
有关计算是《物质结构和性质》综合试题中必考的命题点,涉及的晶胞结构复杂多样,综合性强、难度大,
旨在考查归纳总结构、迁移与运用以及识图解题能力和数学运算能力。与数学结合考查晶胞的立体结构,
是考生极易失分之处。晶体结构的计算常常涉及如下数据:晶体密度、N 、M、晶体体积、微粒间距离、
A
微粒半径、夹角等,密度的表达式往往是列等式的依据。解决这类题,一是要掌握晶体“均摊法”的原理,
二是要有扎实的立体几何知识,三是要熟悉常见晶体的结构特征,并能融会贯通,举一反三。
1.(2022•山东卷)Cu Se是一种钠离子电池正极材料,充放电过程中正极材料立方晶胞(示意图)的组成
2-x
变化如图所示,晶胞内未标出因放电产生的0价Cu原子。下列说法正确的是( )
A.每个Cu Se晶胞中Cu2+个数为x
2-x
B.每个NaSe晶胞完全转化为Cu Se晶胞,转移电子数为8
2 2-x
C.每个NaCuSe晶胞中0价Cu原子个数为1-x
D.当NaCu Se转化为NaCuSe时,每转移 电子,产生(1-x)mol原子
y 2-x
【答案】D
【解析】A项,由Cu Se晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,位于体内的
2-x
1
原创精品资源学科网独家享有版权,侵权必究!
1
学科网(北京)股份有限公司铜离子和亚铜离子的个数之和为8,设晶胞中的铜离子和亚铜离子的个数分别为a和b,则a+b=8-4x,由化
合价代数和为0可得2a+b=4×2,解得a=4x,故A错误;B项,由NaSe转化为Cu Se的电极反应式为
2 2-x
NaSe-e-+(2-x)Cu=Cu Se+Na+,由晶胞结构可知,位于顶点和面心的硒离子个数为8× +6× =4,则每个
2 2-x
晶胞中含有4个NaSe,转移电子数为4,故B错误;C项,由NaCuSe晶胞结构可知,位于顶点和面心的
2
硒离子个数为8× +6× =4,则每个晶胞中含有4个NaCuSe,晶胞中0价铜而个数为(4-4x),故C错误;
D项,由题意可知,NaCu Se转化为NaCuSe的电极反应式为NaCu Se+(1-y) e-+ Na+=NaCuSe+(1-x)Cu,
y 2-x y 2-x
所以每转移(1-y)电子,产生(1-x)mol铜,故D正确;故选D。
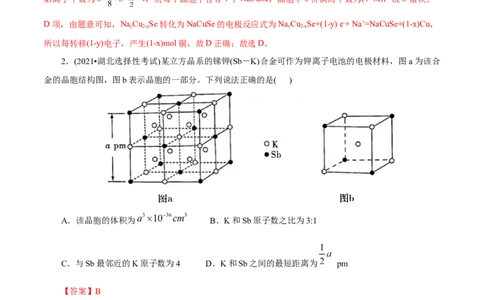
2.(2021•湖北选择性考试)某立方晶系的锑钾(Sb-K)合金可作为钾离子电池的电极材料,图a为该合
金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A.该晶胞的体积为 B.K和Sb原子数之比为3:1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 pm
【答案】B
【解析】该晶胞的边长为a×1010 cm,故晶胞的体积为(a×1010 cm)3=a3×1030 cm3,A项错误;该晶胞
中K的个数为12×+9=12,Sb的个数为8×+6×=4,故K和Sb原子个数之比为3:1,B项正确;以面心处
Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;K和Sb的最短距离为晶胞体对角线长度的,即
pm,D项错误。
2
原创精品资源学科网独家享有版权,侵权必究!
2
学科网(北京)股份有限公司3.(2022•全国甲卷节选)萤石(CaF )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子
2
是_______;若该立方晶胞参数为a pm,正负离子的核间距最小为_______pm。
【答案】Ca2+ a pm
【解析】根据萤石晶胞结构,浅色X离子分布在晶胞的顶点和面心上,则1个晶胞中浅色X离子共有
8× +6× =4个,深色Y离子分布在晶胞内部,则1个晶胞中共有8个深色Y离子,因此该晶胞的化学式
应为XY ,结合萤石的化学式可知,X为Ca2+;根据晶胞,将晶胞分成8个相等的小正方体,仔细观察
2
CaF 的晶胞结构不难发现F-位于晶胞中8个小立方体的体心,小立方体边长为 ,体对角线为 ,
2
Ca2+与F-之间距离就是小晶胞体对角线的一半,因此晶体中正负的核间距的最小的距离为 a pm。
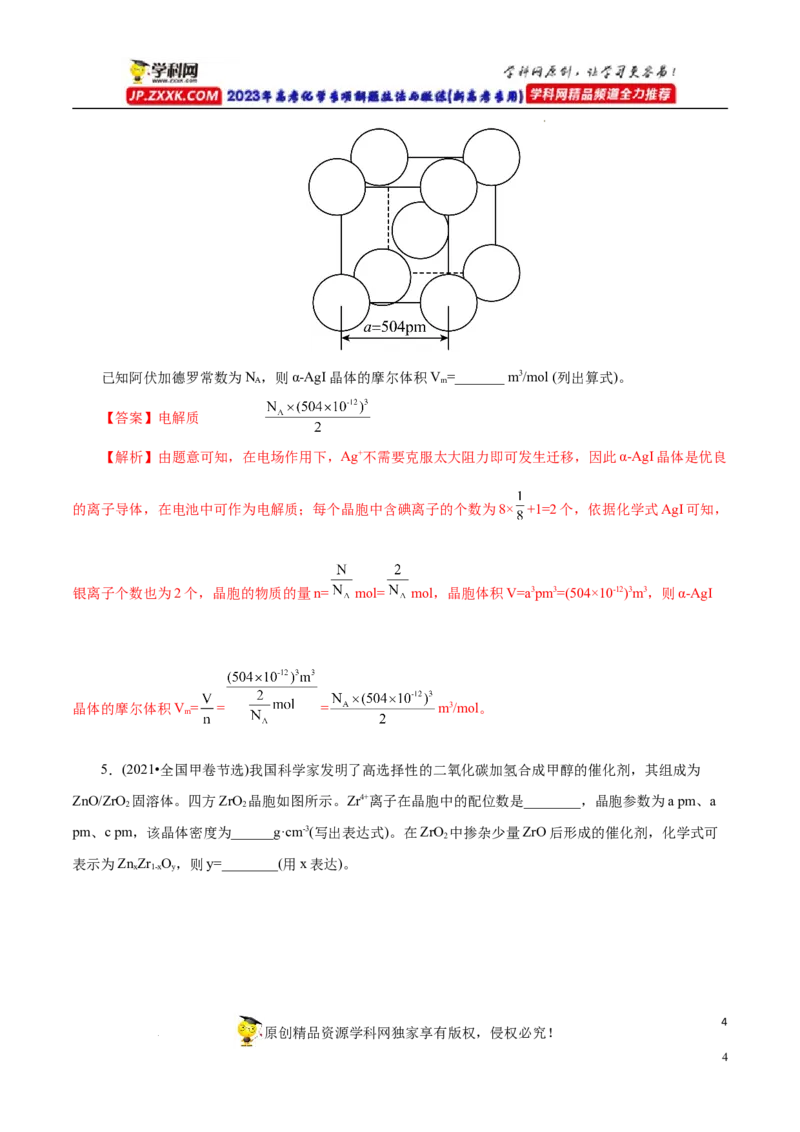
4.(2022•全国乙卷节选)α-AgI晶体中 离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四
面体、八面体等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在电
池中可作为_______。
3
原创精品资源学科网独家享有版权,侵权必究!
3
学科网(北京)股份有限公司已知阿伏加德罗常数为N ,则α-AgI晶体的摩尔体积V =_______ m3/mol (列出算式)。
A m
【答案】电解质
【解析】由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良
的离子导体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8× +1=2个,依据化学式AgI可知,
银离子个数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504×10-12)3m3,则α-AgI
晶体的摩尔体积V = = = m3/mol。
m
5.(2021•全国甲卷节选)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
ZnO/ZrO 固溶体。四方ZrO 晶胞如图所示。Zr4+离子在晶胞中的配位数是________,晶胞参数为a pm、a
2 2
pm、c pm,该晶体密度为______g·cm-3(写出表达式)。在ZrO 中掺杂少量ZrO后形成的催化剂,化学式可
2
表示为ZnZr O,则y=________(用x表达)。
x 1-x y
4
原创精品资源学科网独家享有版权,侵权必究!
4
学科网(北京)股份有限公司【答案】8 2-x
【解析】以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+连接最近且等距的O2-数为4,同理可知右
侧晶胞中有4个O2-与Zr4+相连,因此Zr4+离子在晶胞中的配位数是4+4=8;1个晶胞中含有4个ZrO 微粒,
2
1个晶胞的质量m= ,1个晶胞的体积为(a×10-10cm)×(a×10-10cm)×(c×10-
10cm)=a2c×10-30cm3,因此该晶体密度= = = g·cm-3;在ZrO 中掺杂少量
2
ZrO后形成的催化剂,化学式可表示为ZnZr O,其中Zn元素为+2价,Zr为+4价,O元素为-2价,根据
x 1-x y
化合物化合价为0可知2x+4×(1-x)=2y,解得y=2-x。
1.立方体(长方体)晶胞组成的计算方法
2.有关晶胞各物理量之间的关系
5
原创精品资源学科网独家享有版权,侵权必究!
5
学科网(北京)股份有限公司3.晶体微粒与M、ρ之间的关系
若1个晶胞中含有x个微粒,则1 mol晶胞中含有x mol微粒,其质量为xM g(M为微粒的相对“分
子”质量);又1个晶胞的质量为ρa3 g(a3为晶胞的体积),则1 mol晶胞的质量为ρa3 N g,因此有xM=
A
ρa3 N 。
A
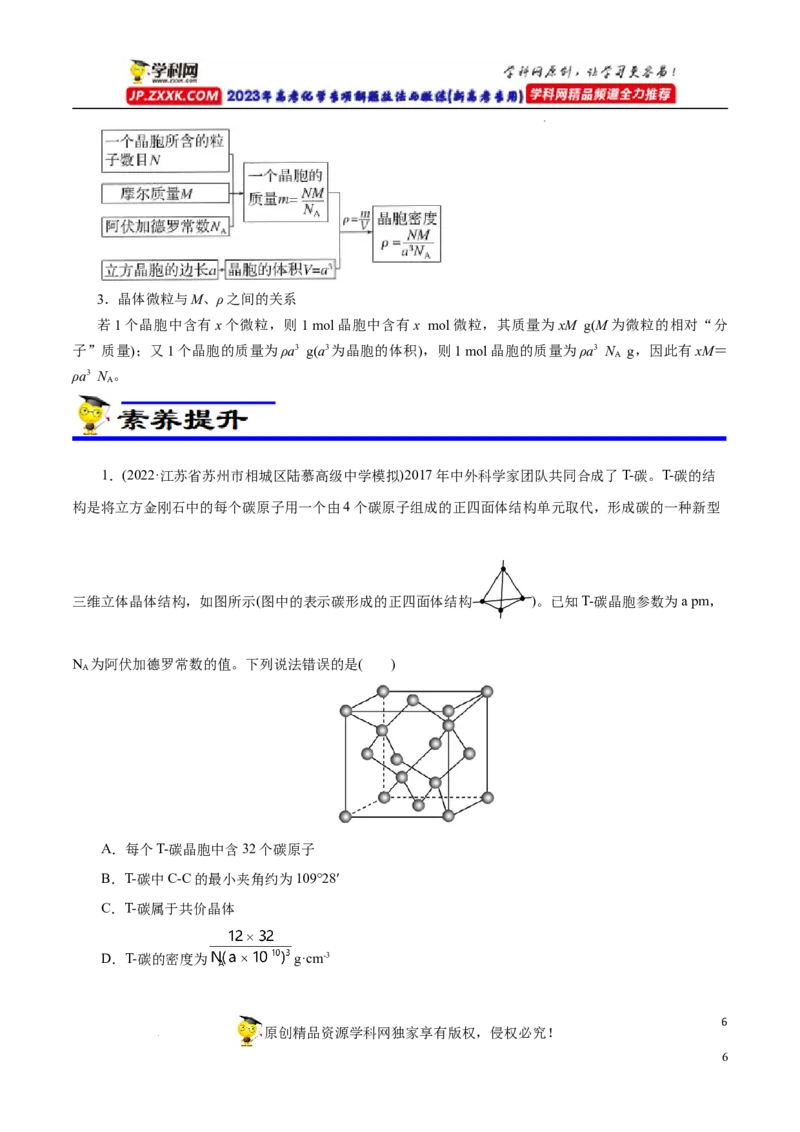
1.(2022·江苏省苏州市相城区陆慕高级中学模拟)2017年中外科学家团队共同合成了T-碳。T-碳的结
构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,形成碳的一种新型
三维立体晶体结构,如图所示(图中的表示碳形成的正四面体结构 )。已知T-碳晶胞参数为a pm,
N 为阿伏加德罗常数的值。下列说法错误的是( )
A
A.每个T-碳晶胞中含32个碳原子
B.T-碳中C-C的最小夹角约为109°28′
C.T-碳属于共价晶体
D.T-碳的密度为 g·cm-3
6
原创精品资源学科网独家享有版权,侵权必究!
6
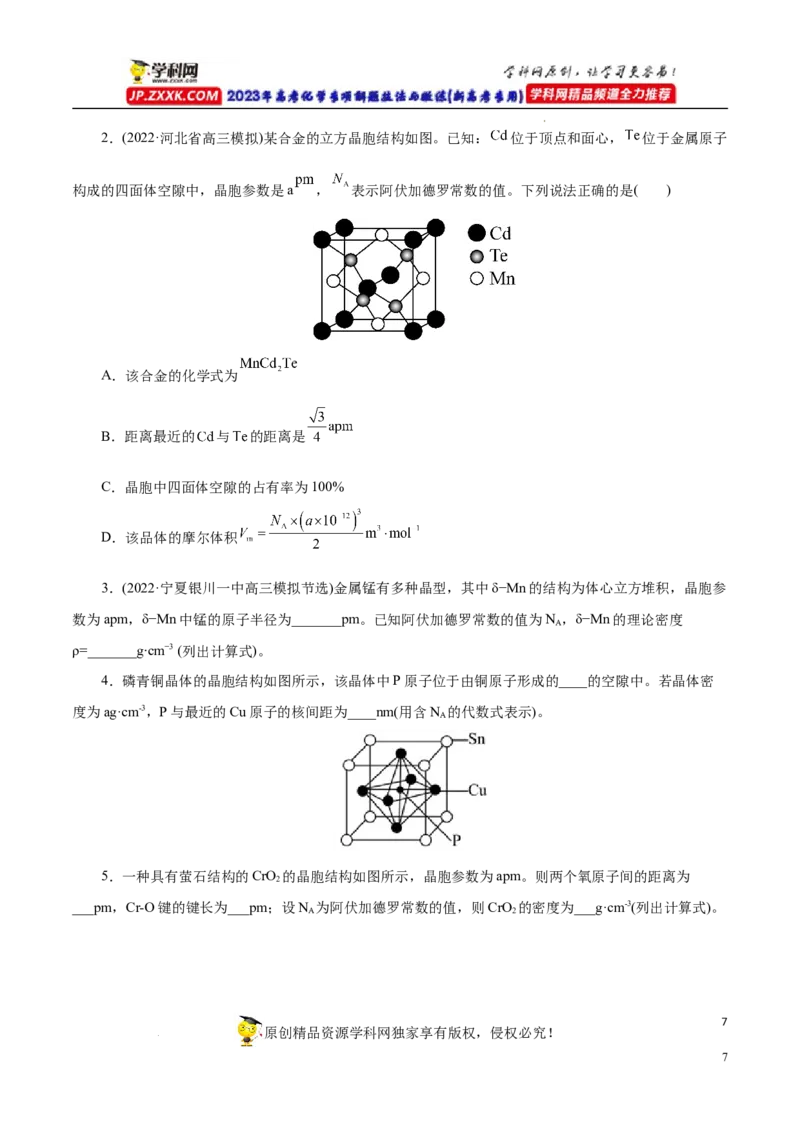
学科网(北京)股份有限公司2.(2022·河北省高三模拟)某合金的立方晶胞结构如图。已知: 位于顶点和面心, 位于金属原子
构成的四面体空隙中,晶胞参数是a , 表示阿伏加德罗常数的值。下列说法正确的是( )
A.该合金的化学式为
B.距离最近的 与 的距离是
C.晶胞中四面体空隙的占有率为100%
D.该品体的摩尔体积
3.(2022·宁夏银川一中高三模拟节选)金属锰有多种晶型,其中δ−Mn的结构为体心立方堆积,晶胞参
数为apm,δ−Mn中锰的原子半径为_______pm。已知阿伏加德罗常数的值为N ,δ−Mn的理论密度
A
ρ=_______g∙cm−3 (列出计算式)。
4.磷青铜晶体的晶胞结构如图所示,该晶体中P原子位于由铜原子形成的____的空隙中。若晶体密
度为ag·cm-3,P与最近的Cu原子的核间距为____nm(用含N 的代数式表示)。
A
5.一种具有萤石结构的CrO 的晶胞结构如图所示,晶胞参数为apm。则两个氧原子间的距离为
2
___pm,Cr-O键的键长为___pm;设N 为阿伏加德罗常数的值,则CrO 的密度为___g·cm-3(列出计算式)。
A 2
7
原创精品资源学科网独家享有版权,侵权必究!
7
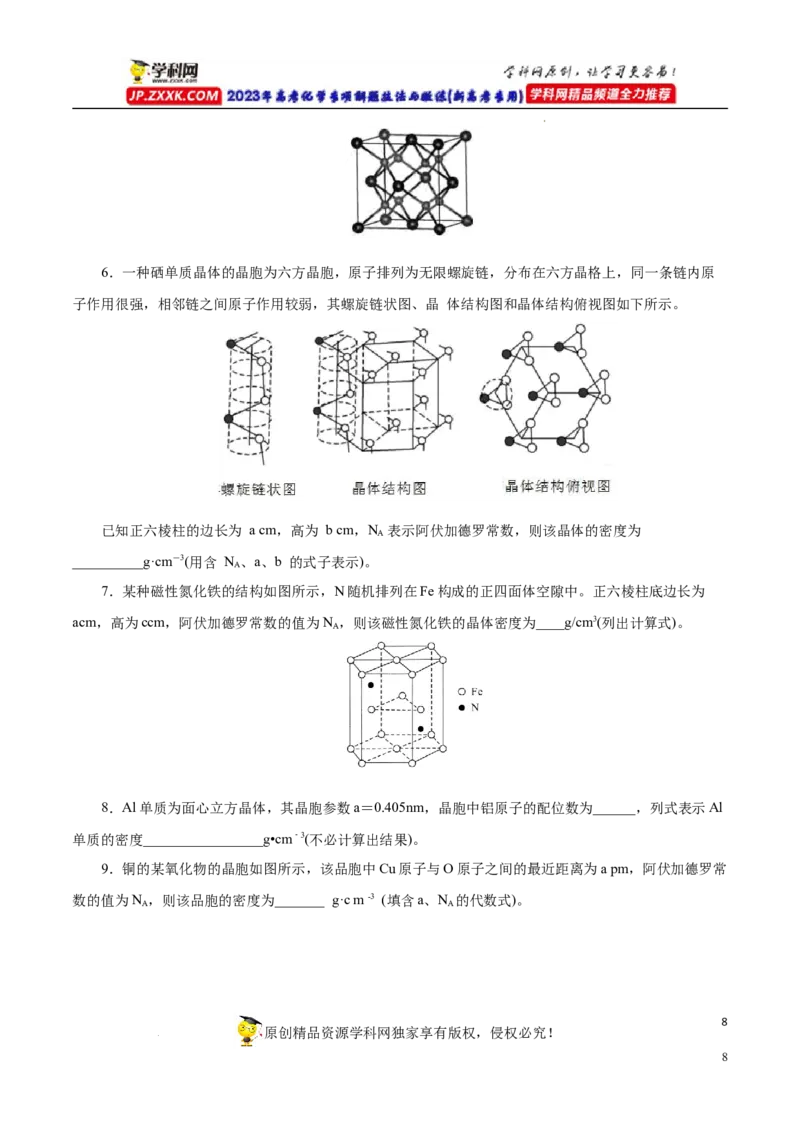
学科网(北京)股份有限公司6.一种硒单质晶体的晶胞为六方晶胞,原子排列为无限螺旋链,分布在六方晶格上,同一条链内原
子作用很强,相邻链之间原子作用较弱,其螺旋链状图、晶 体结构图和晶体结构俯视图如下所示。
已知正六棱柱的边长为 a cm,高为 b cm,N 表示阿伏加德罗常数,则该晶体的密度为
A
__________g·cm-3(用含 N 、a、b 的式子表示)。
A
7.某种磁性氮化铁的结构如图所示,N随机排列在Fe构成的正四面体空隙中。正六棱柱底边长为
acm,高为ccm,阿伏加德罗常数的值为N ,则该磁性氮化铁的晶体密度为____g/cm3(列出计算式)。
A
8.Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为______,列式表示Al
单质的密度_________________g•cm﹣3(不必计算出结果)。
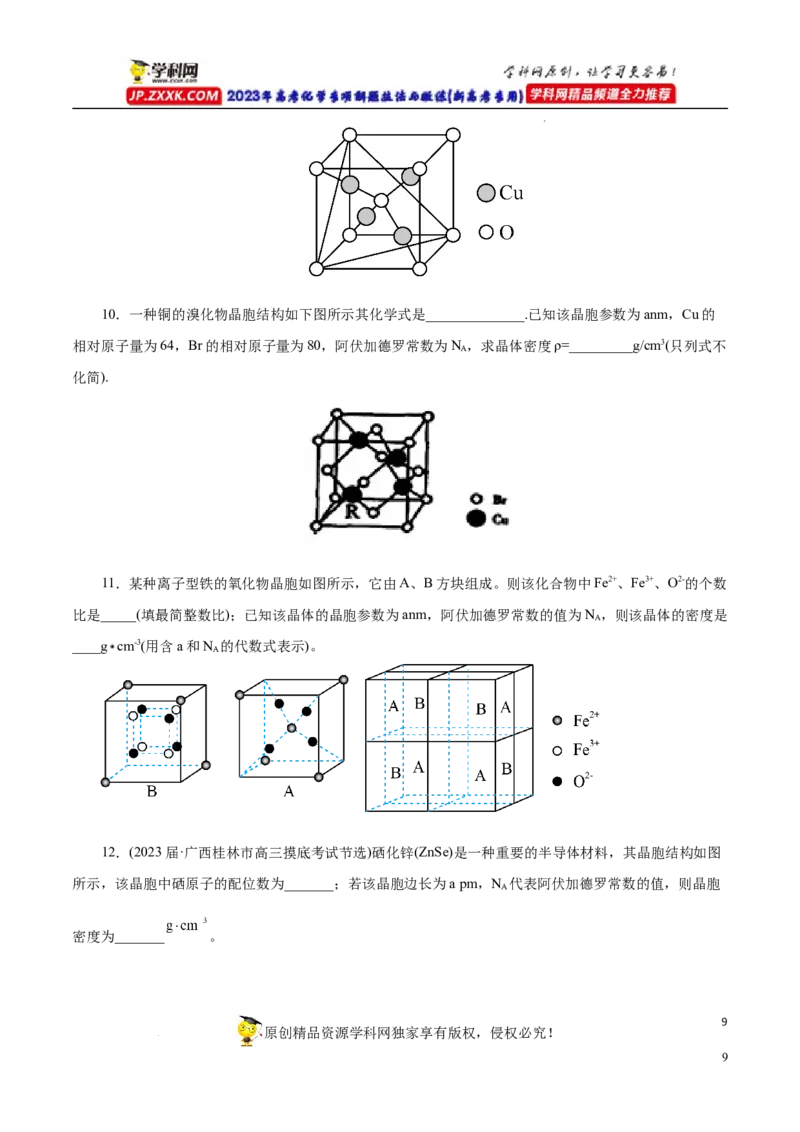
9.铜的某氧化物的晶胞如图所示,该品胞中Cu原子与O原子之间的最近距离为a pm,阿伏加德罗常
数的值为N ,则该品胞的密度为_______ g·c m -3 (填含a、N 的代数式)。
A A
8
原创精品资源学科网独家享有版权,侵权必究!
8
学科网(北京)股份有限公司10.一种铜的溴化物晶胞结构如下图所示其化学式是______________.已知该晶胞参数为anm,Cu的
相对原子量为64,Br的相对原子量为80,阿伏加德罗常数为N ,求晶体密度ρ=_________g/cm3(只列式不
A
化简).
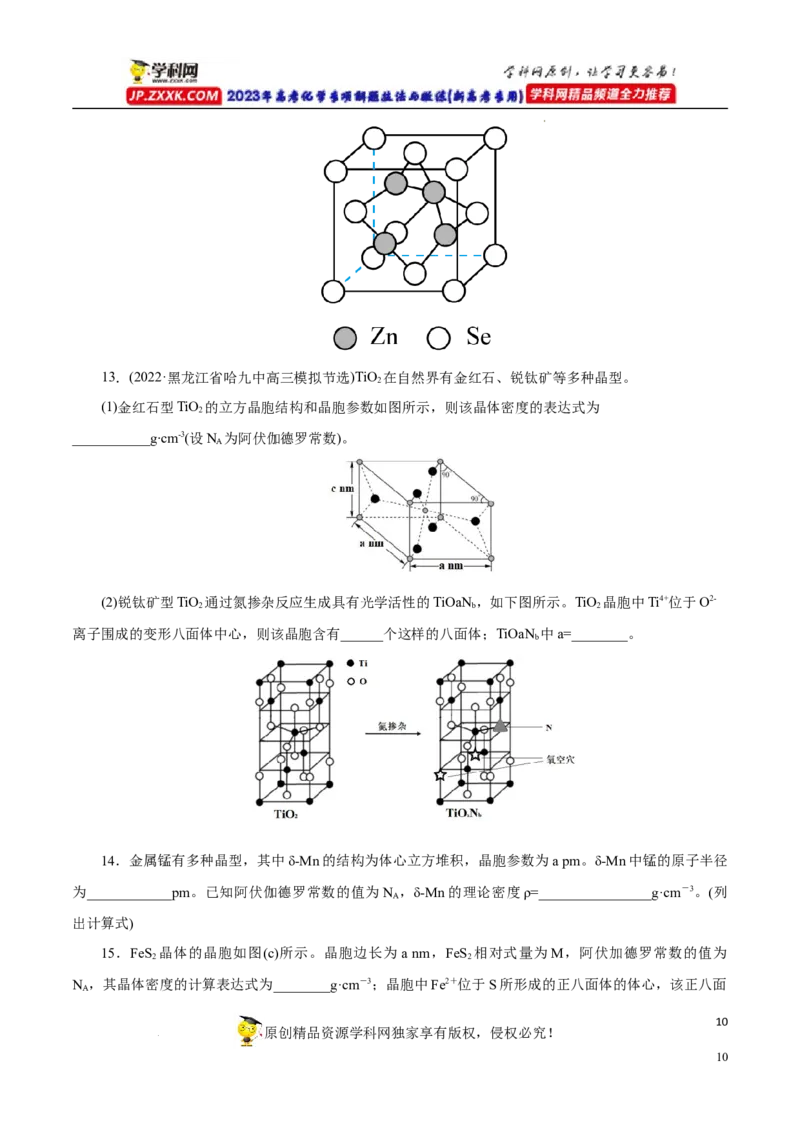
11.某种离子型铁的氧化物晶胞如图所示,它由A、B方块组成。则该化合物中Fe2+、Fe3+、O2-的个数
比是_____(填最简整数比);已知该晶体的晶胞参数为anm,阿伏加德罗常数的值为N ,则该晶体的密度是
A
____g cm-3(用含a和N 的代数式表示)。
A
12.(2023届·广西桂林市高三摸底考试节选)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图
所示,该晶胞中硒原子的配位数为_______;若该晶胞边长为a pm,N 代表阿伏加德罗常数的值,则晶胞
A
密度为_______ 。
9
原创精品资源学科网独家享有版权,侵权必究!
9
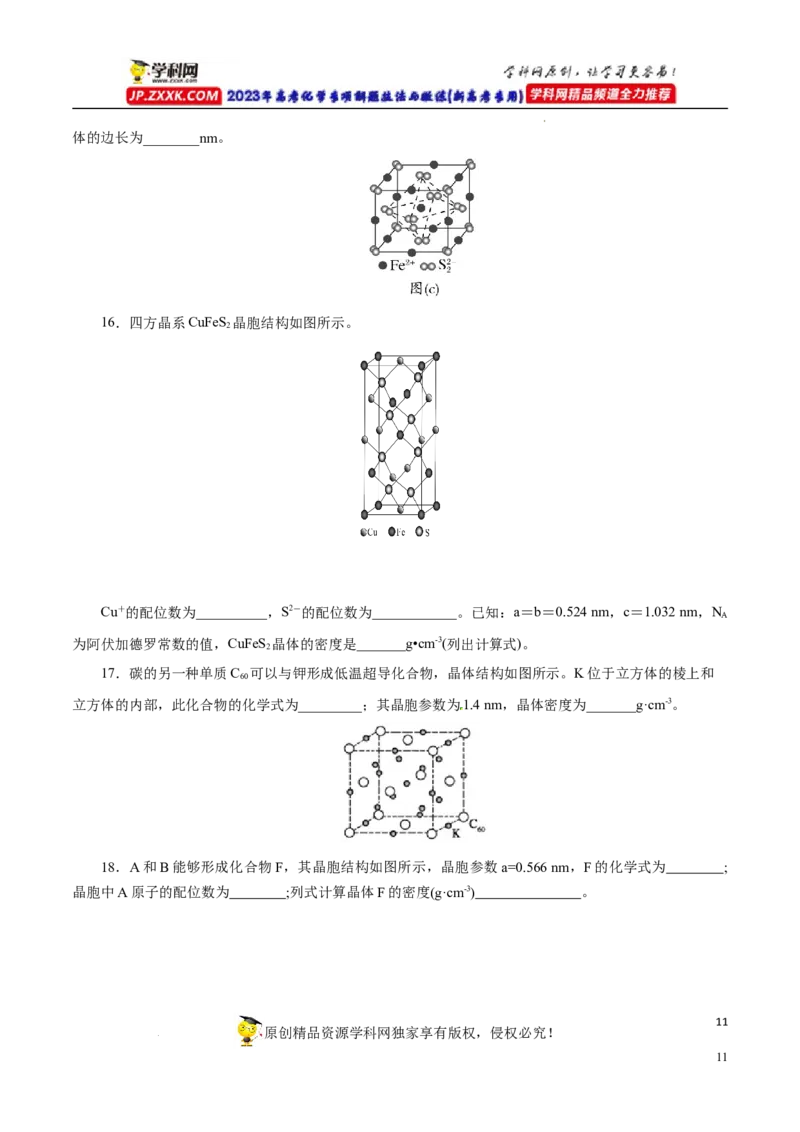
学科网(北京)股份有限公司13.(2022·黑龙江省哈九中高三模拟节选)TiO 在自然界有金红石、锐钛矿等多种晶型。
2
(1)金红石型TiO 的立方晶胞结构和晶胞参数如图所示,则该晶体密度的表达式为
2
___________g∙cm-3(设N 为阿伏伽德罗常数)。
A
(2)锐钛矿型TiO 通过氮掺杂反应生成具有光学活性的TiOaN,如下图所示。TiO 晶胞中Ti4+位于O2-
2 b 2
离子围成的变形八面体中心,则该晶胞含有______个这样的八面体;TiOaN 中a=________。
b
14.金属锰有多种晶型,其中δ-Mn的结构为体心立方堆积,晶胞参数为a pm。δ-Mn中锰的原子半径
为____________pm。已知阿伏伽德罗常数的值为N ,δ-Mn的理论密度ρ=________________g·cm-3。(列
A
出计算式)
15.FeS 晶体的晶胞如图(c)所示。晶胞边长为 a nm,FeS 相对式量为M,阿伏加德罗常数的值为
2 2
N ,其晶体密度的计算表达式为________g·cm-3;晶胞中Fe2+位于S所形成的正八面体的体心,该正八面
A
10
原创精品资源学科网独家享有版权,侵权必究!
10
学科网(北京)股份有限公司体的边长为________nm。
16.四方晶系CuFeS 晶胞结构如图所示。
2
Cu+的配位数为__________,S2-的配位数为____________。已知:a=b=0.524 nm,c=1.032 nm,N
A
为阿伏加德罗常数的值,CuFeS 晶体的密度是_______g•cm-3(列出计算式)。
2
17.碳的另一种单质C 可以与钾形成低温超导化合物,晶体结构如图所示。K位于立方体的棱上和
60
立方体的内部,此化合物的化学式为_________;其晶胞参数为1.4 nm,晶体密度为_______g·cm-3。
18.A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为 ;
晶胞中A原子的配位数为 ;列式计算晶体F的密度(g·cm-3) 。
11
原创精品资源学科网独家享有版权,侵权必究!
11
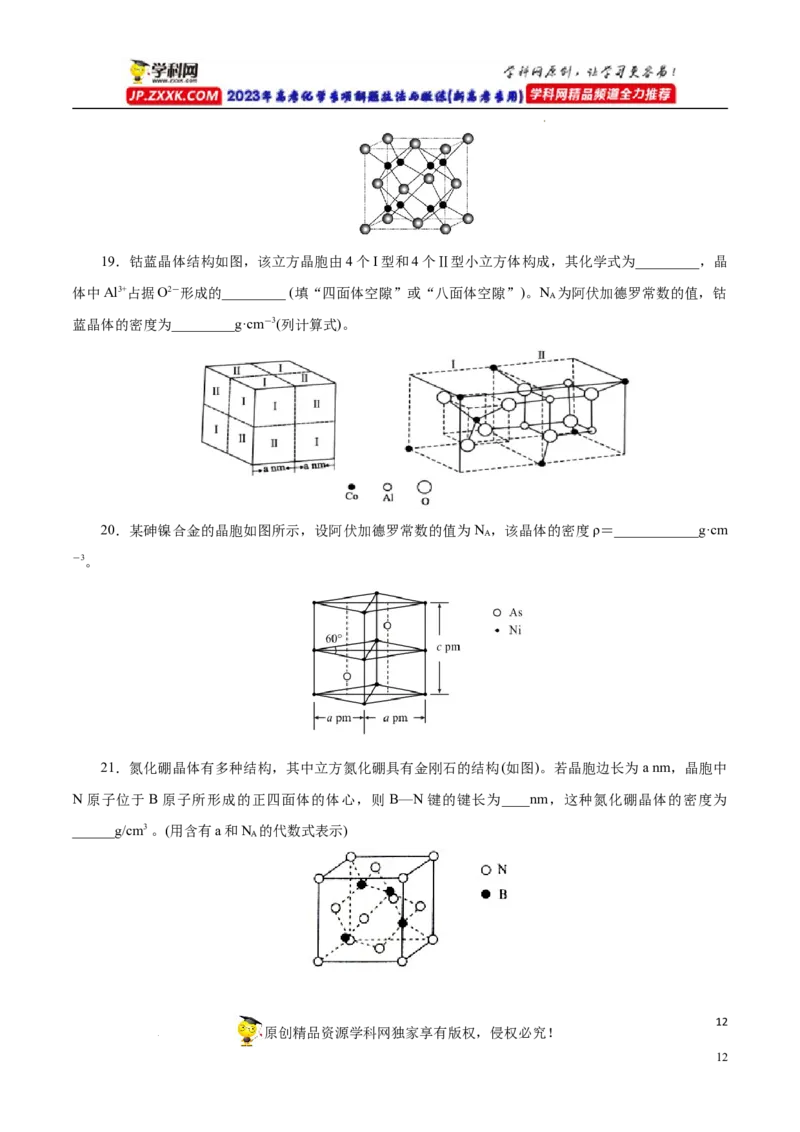
学科网(北京)股份有限公司19.钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为_________,晶
体中Al3+占据O2-形成的_________ (填“四面体空隙”或“八面体空隙”)。N 为阿伏加德罗常数的值,钴
A
蓝晶体的密度为_________g·cm-3(列计算式)。
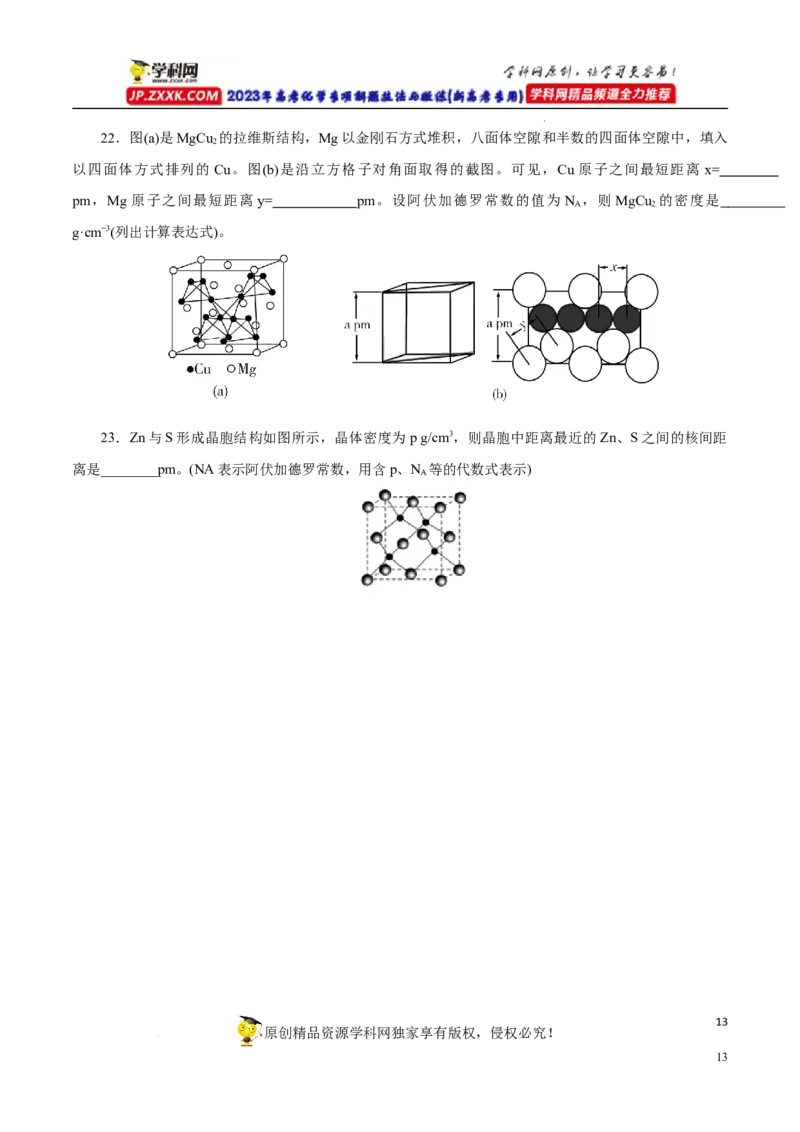
20.某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为N ,该晶体的密度ρ=____________g·cm
A
-3。
21.氮化硼晶体有多种结构,其中立方氮化硼具有金刚石的结构(如图)。若晶胞边长为a nm,晶胞中
N原子位于B原子所形成的正四面体的体心,则 B—N键的键长为____nm,这种氮化硼晶体的密度为
______g/cm3 。(用含有a和N 的代数式表示)
A
12
原创精品资源学科网独家享有版权,侵权必究!
12
学科网(北京)股份有限公司22.图(a)是MgCu 的拉维斯结构,Mg以金刚石方式堆积,八面体空隙和半数的四面体空隙中,填入
2
以四面体方式排列的 Cu。图(b)是沿立方格子对角面取得的截图。可见,Cu 原子之间最短距离 x=
pm,Mg 原子之间最短距离 y= pm。设阿伏加德罗常数的值为 N ,则 MgCu 的密度是
A 2
g·cm−3(列出计算表达式)。
23.Zn与S形成晶胞结构如图所示,晶体密度为p g/cm3,则晶胞中距离最近的Zn、S之间的核间距
离是________pm。(NA表示阿伏加德罗常数,用含p、N 等的代数式表示)
A
13
原创精品资源学科网独家享有版权,侵权必究!
13
学科网(北京)股份有限公司14
原创精品资源学科网独家享有版权,侵权必究!
14
学科网(北京)股份有限公司