文档内容
专题 06 水溶液中的离子平衡
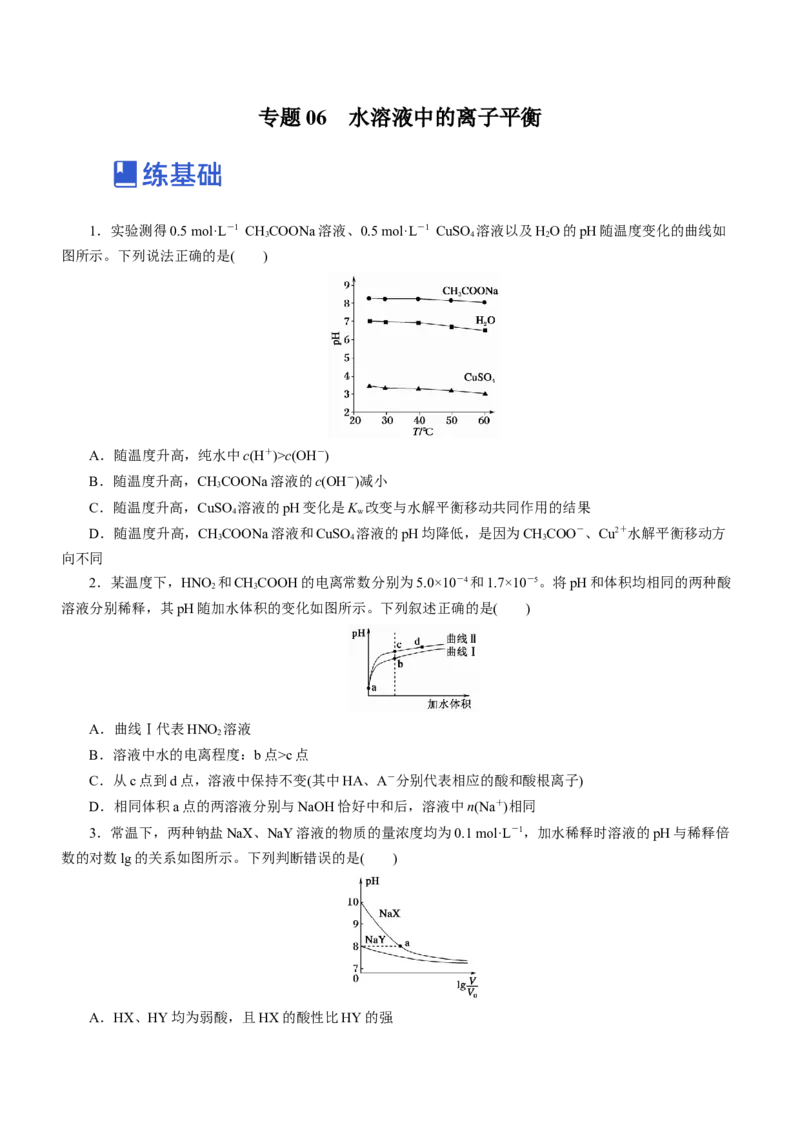
1.实验测得0.5 mol·L-1 CHCOONa溶液、0.5 mol·L-1 CuSO 溶液以及HO的pH随温度变化的曲线如
3 4 2
图所示。下列说法正确的是( )
A.随温度升高,纯水中c(H+)>c(OH-)
B.随温度升高,CHCOONa溶液的c(OH-)减小
3
C.随温度升高,CuSO 溶液的pH变化是K 改变与水解平衡移动共同作用的结果
4 w
D.随温度升高,CHCOONa溶液和CuSO 溶液的pH均降低,是因为CHCOO-、Cu2+水解平衡移动方
3 4 3
向不同
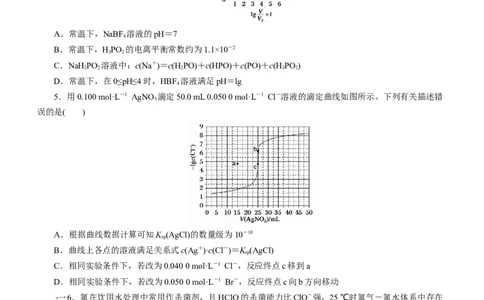
2.某温度下,HNO 和CHCOOH的电离常数分别为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸
2 3
溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是( )
A.曲线Ⅰ代表HNO 溶液
2
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中保持不变(其中HA、A-分别代表相应的酸和酸根离子)
D.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
3.常温下,两种钠盐NaX、NaY溶液的物质的量浓度均为0.1 mol·L-1,加水稀释时溶液的pH与稀释倍
数的对数lg的关系如图所示。下列判断错误的是( )
A.HX、HY均为弱酸,且HX的酸性比HY的强B.0.1 mol·L-1的NaX、NaY溶液中,前者对水的电离促进作用较大
C.a点NaX溶液中存在:c(Na+)>c(X-)
D.随着溶液的稀释,NaY溶液中逐渐减小
4.次磷酸(H PO 、一元弱酸)和氟硼酸(HBF )均可用于植物杀菌。常温时,有1 mol/L的HPO 溶液和1
3 2 4 3 2
mol/L的HBF 溶液,两者起始时的体积均为V,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的
4 0
pH变化曲线如图所示。下列说法错误的是( )
A.常温下,NaBF 溶液的pH=7
4
B.常温下,HPO 的电离平衡常数约为1.1×10-2
3 2
C.NaH PO 溶液中:c(Na+)=c(H PO)+c(HPO)+c(PO)+c(H PO )
2 2 2 3 2
D.常温下,在0≤pH≤4时,HBF 溶液满足pH=lg
4
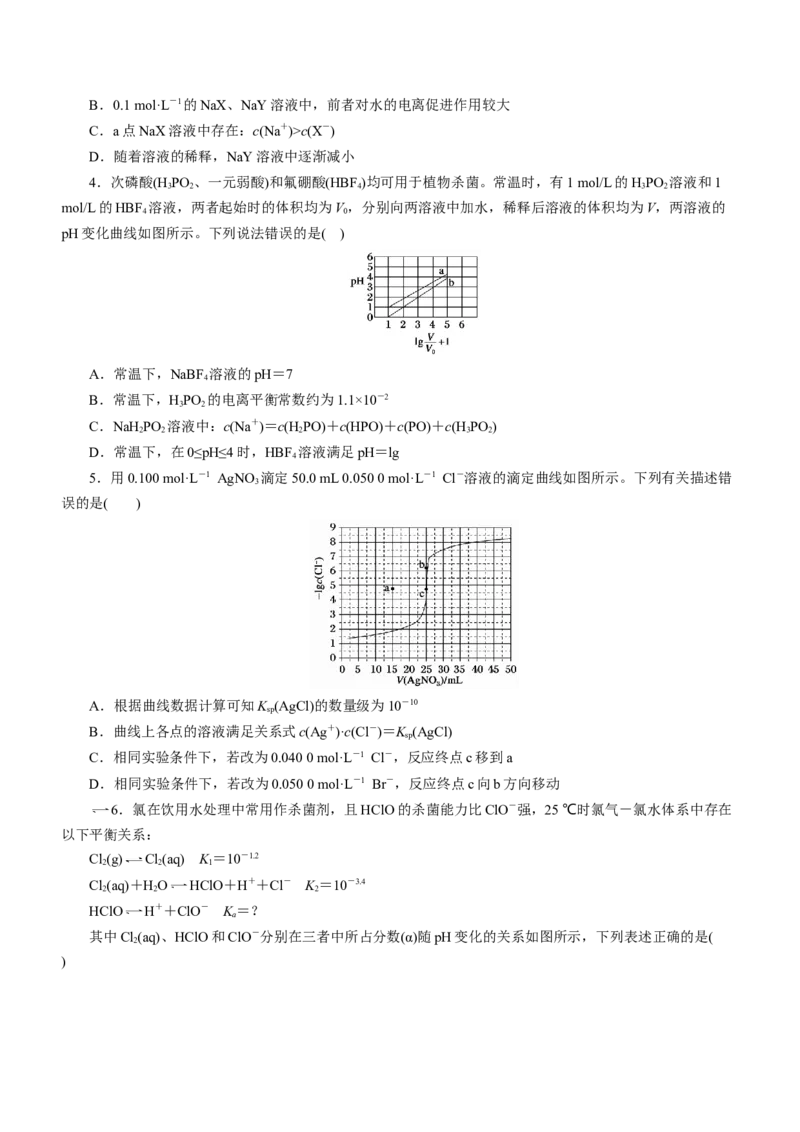
5.用0.100 mol·L-1 AgNO 滴定50.0 mL 0.050 0 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错
3
误的是( )
A.根据曲线数据计算可知K (AgCl)的数量级为10-10
sp
B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K (AgCl)
sp
C.相同实验条件下,若改为0.040 0 mol·L-1 Cl-,反应终点c移到a
D.相同实验条件下,若改为0.050 0 mol·L-1 Br-,反应终点c向b方向移动
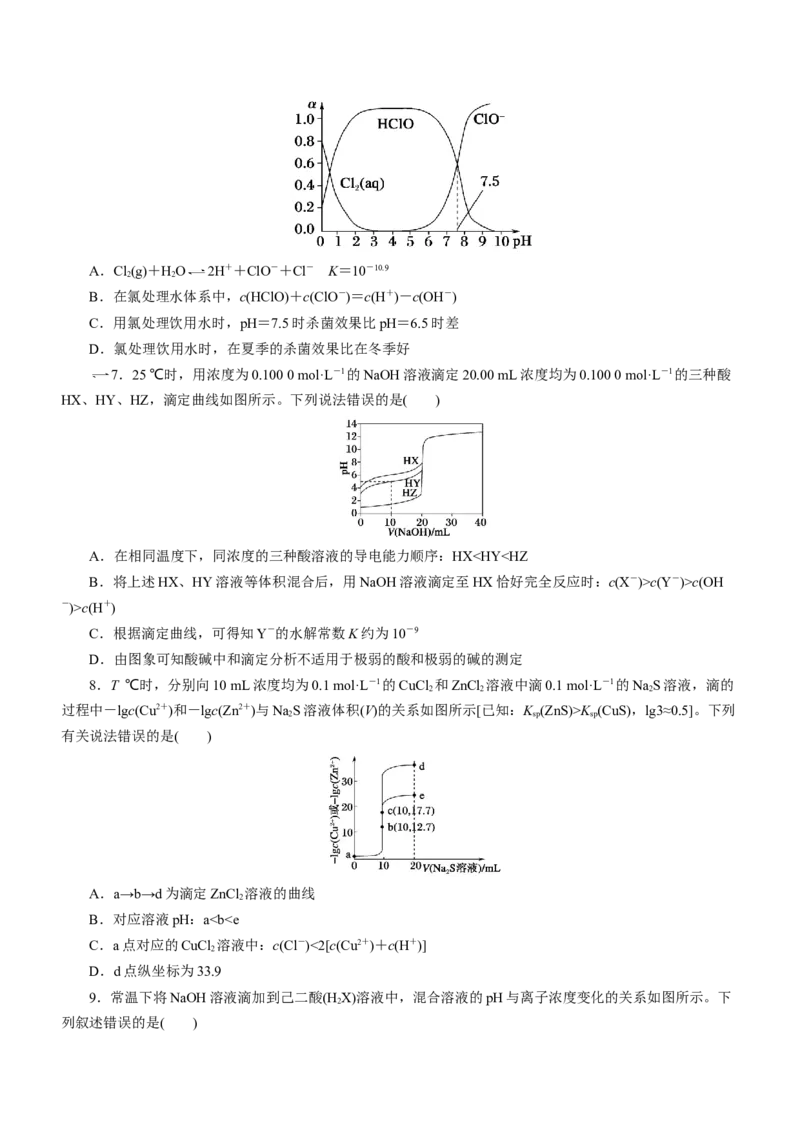
6.氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强,25 ℃时氯气-氯水体系中存在
以下平衡关系:
Cl(g) Cl(aq) K =10-1.2
2 2 1
Cl(aq)+HO HClO+H++Cl- K =10-3.4
2 2 2
HClO H++ClO- K =?
a
其中Cl(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示,下列表述正确的是(
2
)A.Cl(g)+HO 2H++ClO-+Cl- K=10-10.9
2 2
B.在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-)
C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
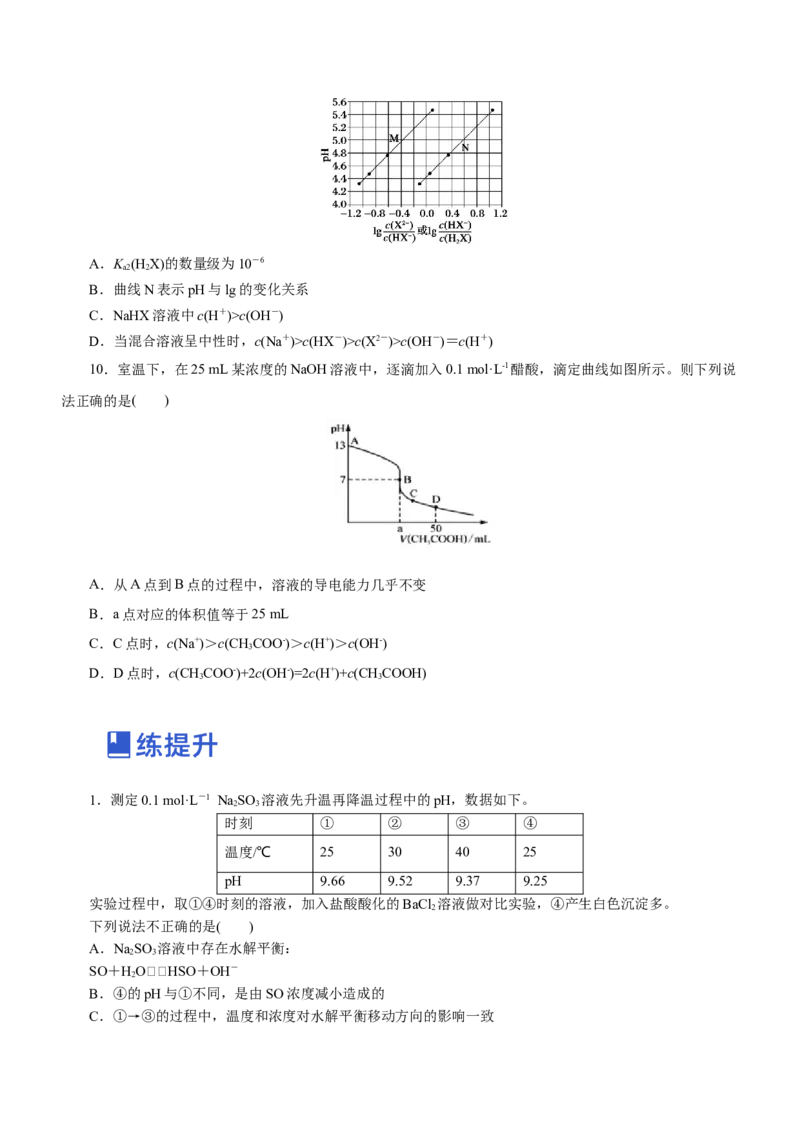
7.25 ℃时,用浓度为0.100 0 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.100 0 mol·L-1的三种酸
HX、HY、HZ,滴定曲线如图所示。下列说法错误的是( )
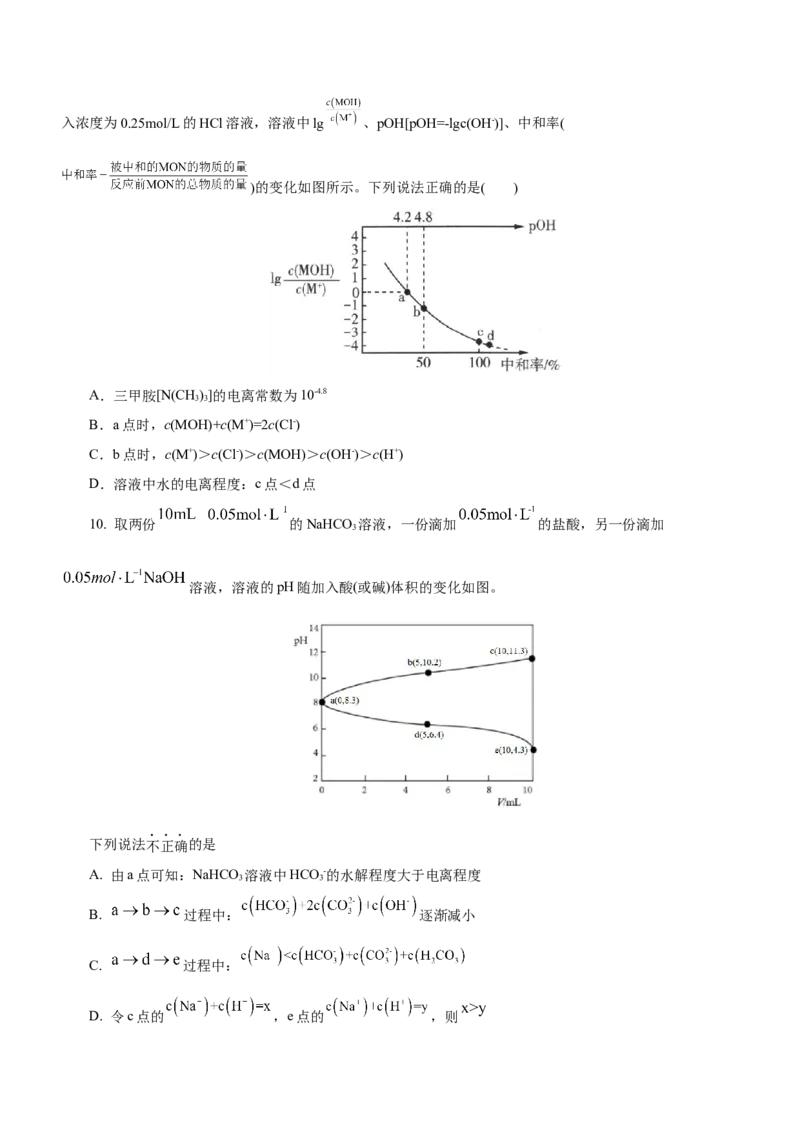
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HXc(Y-)>c(OH
-)>c(H+)
C.根据滴定曲线,可得知Y-的水解常数K约为10-9
D.由图象可知酸碱中和滴定分析不适用于极弱的酸和极弱的碱的测定
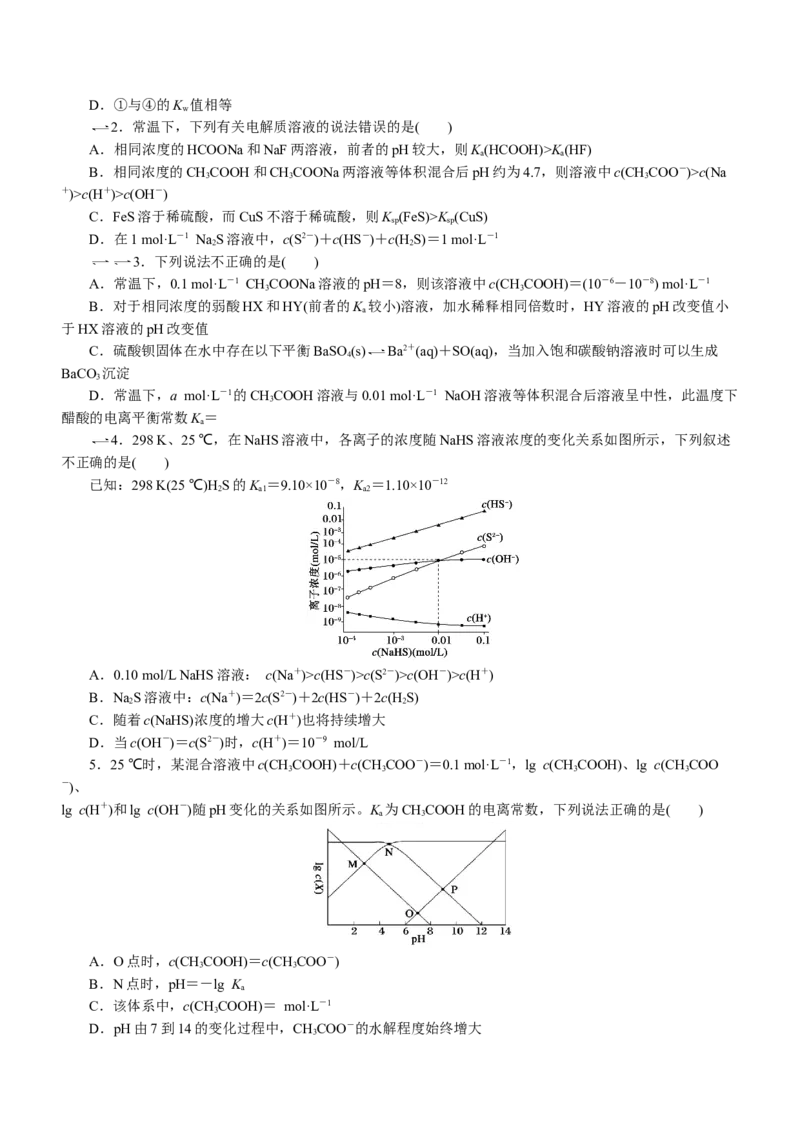
8.T ℃时,分别向10 mL浓度均为0.1 mol·L-1的CuCl 和ZnCl 溶液中滴0.1 mol·L-1的NaS溶液,滴的
2 2 2
过程中-lgc(Cu2+)和-lgc(Zn2+)与NaS溶液体积(V)的关系如图所示[已知:K (ZnS)>K (CuS),lg3≈0.5]。下列
2 sp sp
有关说法错误的是( )
A.a→b→d为滴定ZnCl 溶液的曲线
2
B.对应溶液pH:ac(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(OH-)=c(H+)
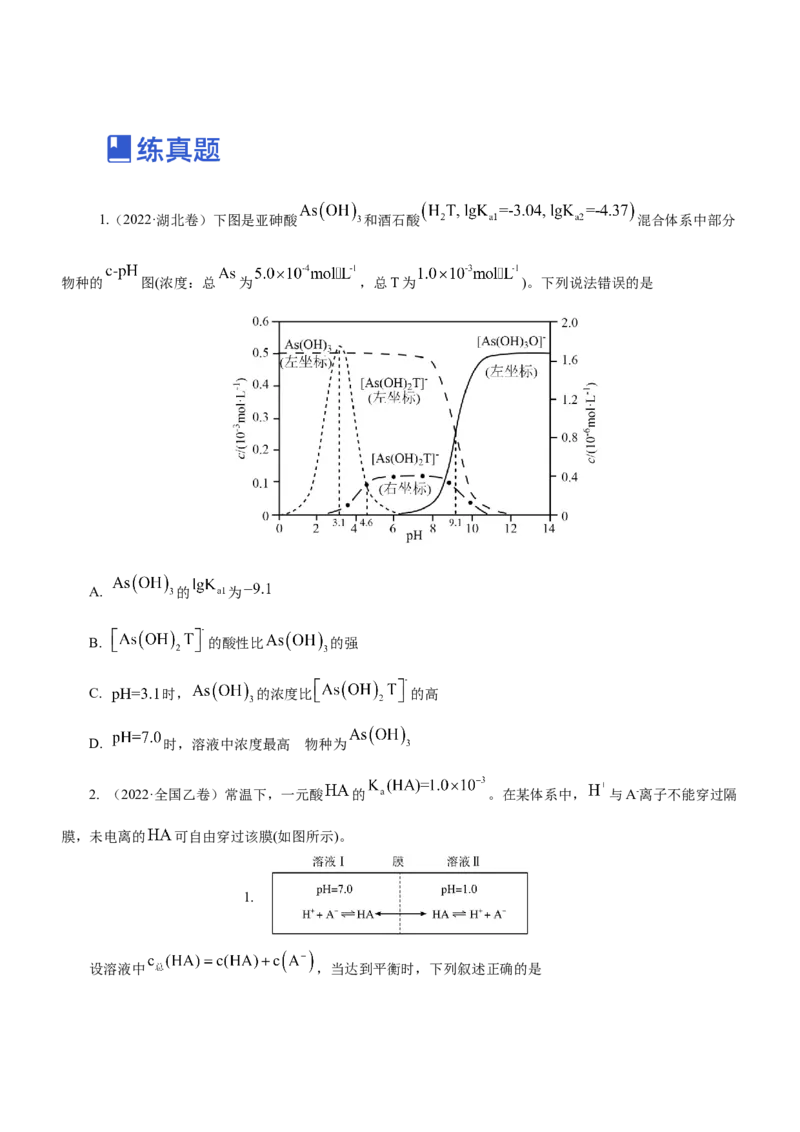
10.室温下,在25 mL某浓度的NaOH溶液中,逐滴加入0.1 mol·L-1醋酸,滴定曲线如图所示。则下列说
法正确的是( )
A.从A点到B点的过程中,溶液的导电能力几乎不变
B.a点对应的体积值等于25 mL
C.C点时,c(Na+)>c(CHCOO-)>c(H+)>c(OH-)
3
D.D点时,c(CHCOO-)+2c(OH-)=2c(H+)+c(CHCOOH)
3 3
1.测定0.1 mol·L-1 Na SO 溶液先升温再降温过程中的pH,数据如下。
2 3
时刻 ① ② ③ ④
温度/℃ 25 30 40 25
pH 9.66 9.52 9.37 9.25
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl 溶液做对比实验,④产生白色沉淀多。
2
下列说法不正确的是( )
A.NaSO 溶液中存在水解平衡:
2 3
SO+HOHSO+OH-
2
B.④的pH与①不同,是由SO浓度减小造成的
C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致D.①与④的K 值相等
w
2.常温下,下列有关电解质溶液的说法错误的是( )
A.相同浓度的HCOONa和NaF两溶液,前者的pH较大,则K(HCOOH)>K(HF)
a a
B.相同浓度的CHCOOH和CHCOONa两溶液等体积混合后pH约为4.7,则溶液中c(CHCOO-)>c(Na
3 3 3
+)>c(H+)>c(OH-)
C.FeS溶于稀硫酸,而CuS不溶于稀硫酸,则K (FeS)>K (CuS)
sp sp
D.在1 mol·L-1 Na S溶液中,c(S2-)+c(HS-)+c(H S)=1 mol·L-1
2 2
3.下列说法不正确的是( )
A.常温下,0.1 mol·L-1 CHCOONa溶液的pH=8,则该溶液中c(CHCOOH)=(10-6-10-8) mol·L-1
3 3
B.对于相同浓度的弱酸HX和HY(前者的K 较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值小
a
于HX溶液的pH改变值
C.硫酸钡固体在水中存在以下平衡BaSO(s) Ba2+(aq)+SO(aq),当加入饱和碳酸钠溶液时可以生成
4
BaCO 沉淀
3
D.常温下,a mol·L-1的CHCOOH溶液与0.01 mol·L-1 NaOH溶液等体积混合后溶液呈中性,此温度下
3
醋酸的电离平衡常数K=
a
4.298 K、25 ℃,在NaHS溶液中,各离子的浓度随NaHS溶液浓度的变化关系如图所示,下列叙述
不正确的是( )
已知:298 K(25 ℃)H S的K =9.10×10-8,K =1.10×10-12
2 a1 a2
A.0.10 mol/L NaHS溶液: c(Na+)>c(HS-)>c(S2-)>c(OH-)>c(H+)
B.NaS溶液中:c(Na+)=2c(S2-)+2c(HS-)+2c(H S)
2 2
C.随着c(NaHS)浓度的增大c(H+)也将持续增大
D.当c(OH-)=c(S2-)时,c(H+)=10-9 mol/L
5.25 ℃时,某混合溶液中c(CHCOOH)+c(CHCOO-)=0.1 mol·L-1,lg c(CHCOOH)、lg c(CHCOO
3 3 3 3
-)、
lg c(H+)和lg c(OH-)随pH变化的关系如图所示。K 为CHCOOH的电离常数,下列说法正确的是( )
a 3
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,pH=-lg K
a
C.该体系中,c(CHCOOH)= mol·L-1
3
D.pH由7到14的变化过程中,CHCOO-的水解程度始终增大
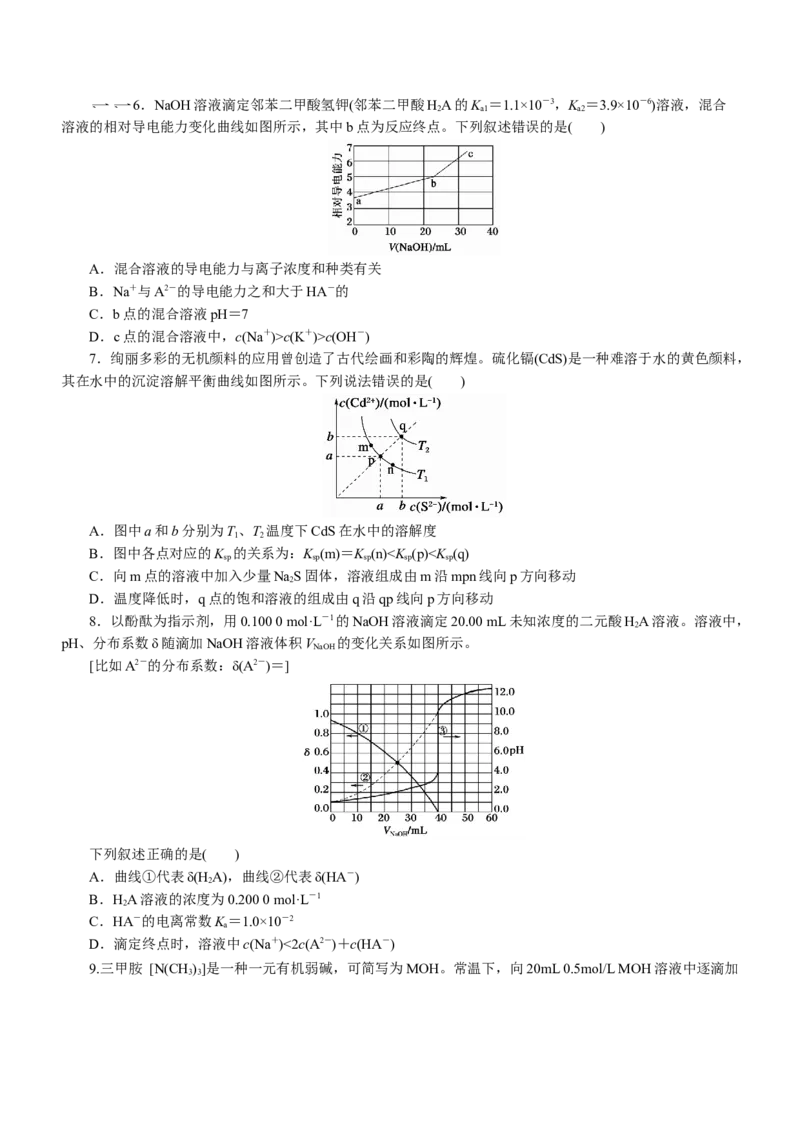
36.NaOH溶液滴定邻苯二甲酸氢钾(邻苯二甲酸HA的K =1.1×10-3,K =3.9×10-6)溶液,混合
2 a1 a2
溶液的相对导电能力变化曲线如图所示,其中b点为反应终点。下列叙述错误的是( )
A.混合溶液的导电能力与离子浓度和种类有关
B.Na+与A2-的导电能力之和大于HA-的
C.b点的混合溶液pH=7
D.c点的混合溶液中,c(Na+)>c(K+)>c(OH-)
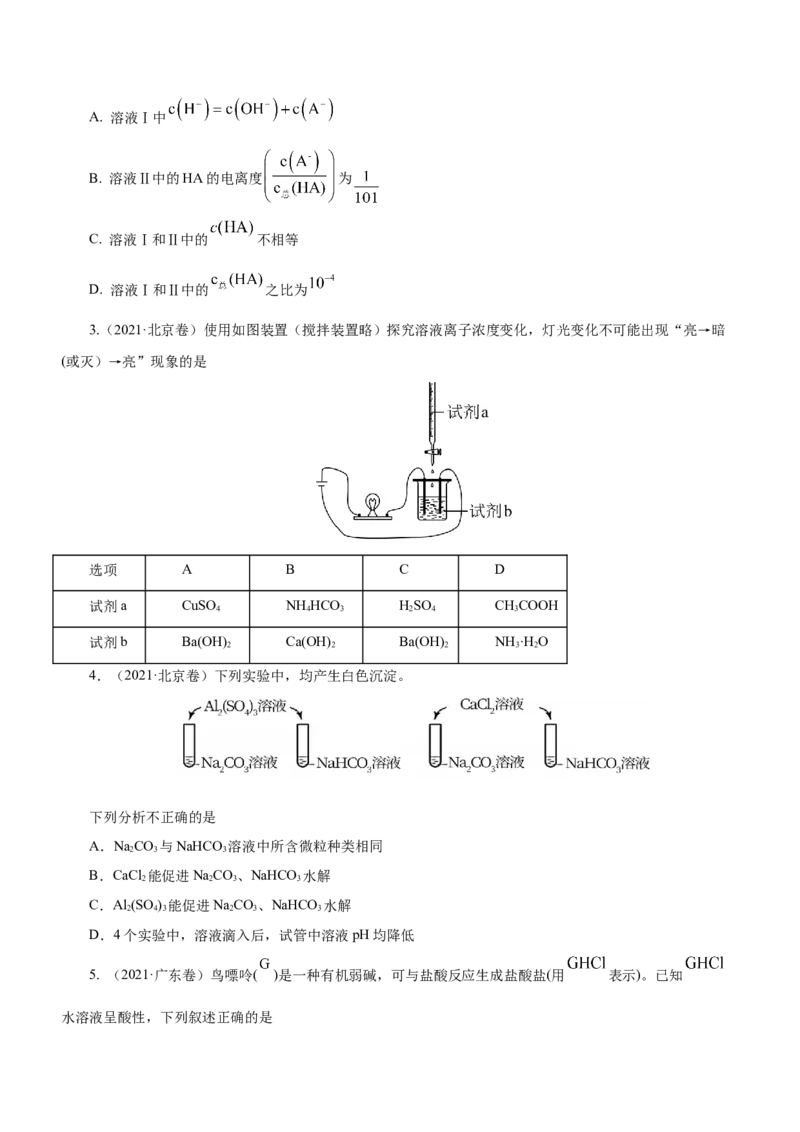
7.绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,
其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是( )
A.图中a和b分别为T、T 温度下CdS在水中的溶解度
1 2
B.图中各点对应的K 的关系为:K (m)=K (n) B. M点,c(Cl-) +c(OH-)+c(R-)=2c(H R+)+c(Na+)+c(H+)
2
C. O点,pH= D. P点,c(Na+)>c(Cl-)>c(OH-)>c(H+)
7. (2021·浙江卷)25℃时,下列说法正确的是
A. NaHA溶液呈酸性,可以推测HA为强酸
2
B. 可溶性正盐BA溶液呈中性,可以推测BA为强酸强碱盐
C. 0.010 mol·L-1、0.10mol·L-1的醋酸溶液的电离度分别为α 、α ,则α <α
1 2 1 2
D. 100 mL pH=10.00的NaCO 溶液中水电离出H+的物质的量为1.0×10-5mol
2 3
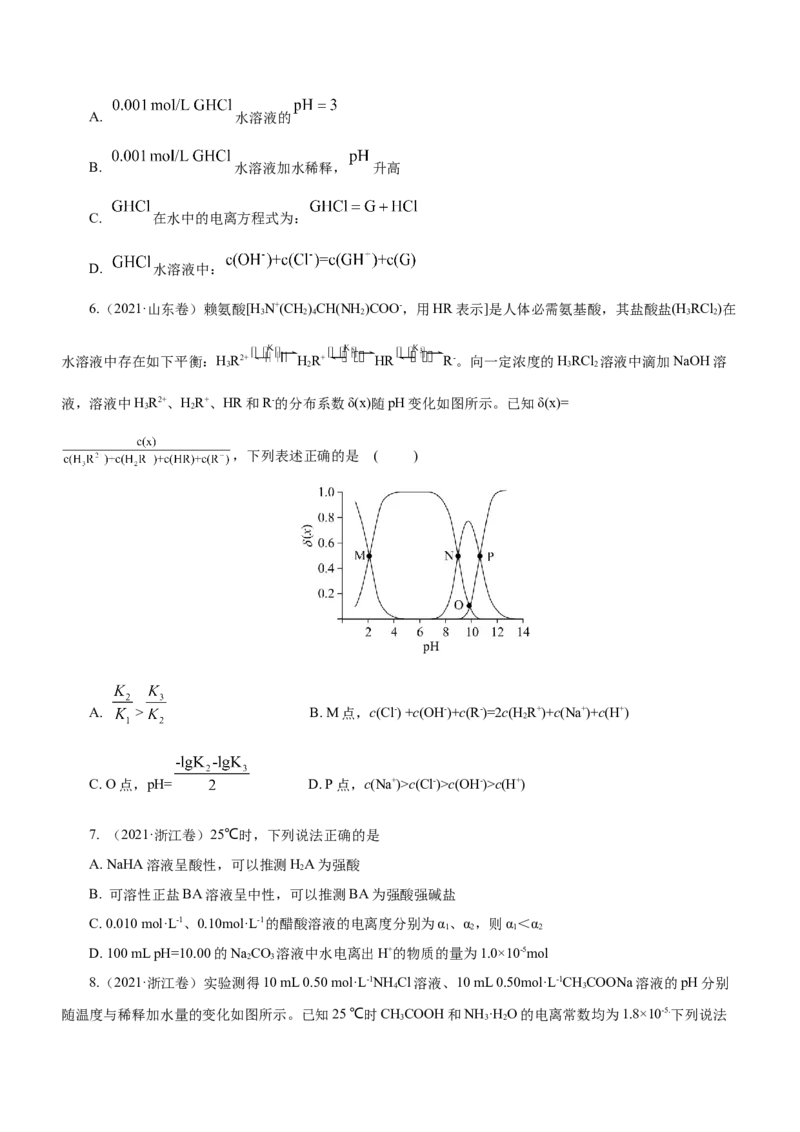
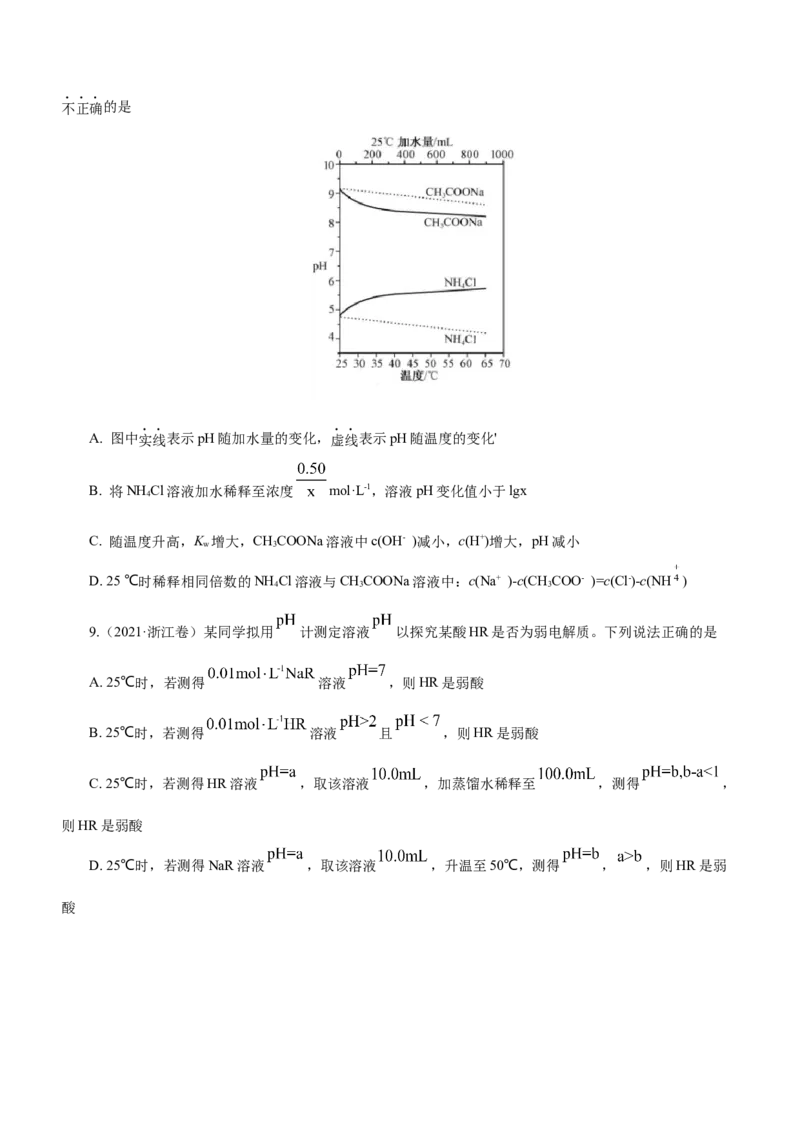
8.(2021·浙江卷)实验测得10 mL 0.50 mol·L-1NH Cl溶液、10 mL 0.50mol·L-1CHCOONa溶液的pH分别
4 3
随温度与稀释加水量的变化如图所示。已知25 ℃时CHCOOH和NH ·H O的电离常数均为1.8×10-5.下列说法
3 3 2不正确的是
A. 图中实线表示pH随加水量的变化,虚线表示pH随温度的变化'
B. 将NH Cl溶液加水稀释至浓度 mol·L-1,溶液pH变化值小于lgx
4
C. 随温度升高,K 增大,CHCOONa溶液中c(OH- )减小,c(H+)增大,pH减小
w 3
D. 25 ℃时稀释相同倍数的NH Cl溶液与CHCOONa溶液中:c(Na+ )-c(CHCOO- )=c(Cl-)-c(NH )
4 3 3
9.(2021·浙江卷)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确的是
A. 25℃时,若测得 溶液 ,则HR是弱酸
B. 25℃时,若测得 溶液 且 ,则HR是弱酸
C. 25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,
则HR是弱酸
D. 25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱
酸