文档内容
专题 08 元素周期律与元素周期表
考点01 原子结构与核外电子排布········································································1
考点02 元素周期表与元素周期律········································································4
考点03 微粒间的相互作用力·············································································11
考点 01 原子结构与核外电子排布
1.原子结构
(1)原子的构成
X
(2)核素(原子)的表示及其数量关系
①表示: 表示质子数为Z、质量数为A、中子数为 A - Z 的核素原子。
(3)阴、阳离子中的数量关系
①质量数=质子数+中子数。
②阴离子: :核外电子数=Z+n。
阳离子: :核外电子数=Z-n。
+c
(4)符号b Xd+中各数字的含义
a e
2.元素、核素、同位素
(1)“三素”关系同位素的“六同三不同”
(2)几种重要的核素及其应用
核素 U C H H O
用途 核燃料 用于考古断代 制氢弹 示踪原子
(3)氢元素的三种核素
H
3.核外电子排布
(1)核外电子排布规律
(2)原子结构示意图
1.1934年约里奥–居里夫妇在核反应中用α粒子(即氦核 )轰击金属原子 ,得到核素 ,开创了
人造放射性核素的先河: + → + 。其中元素X、Y的最外层电子数之和为8。下列叙述正确
的是
A. 的相对原子质量为26
B. X、Y均可形成三氯化物
C. X的原子半径小于Y的
D. Y仅有一种含氧酸
2.(2022·湖南省长郡中学高三模拟)用N 表示阿伏加德罗常数的值,35Cl和37Cl是Cl元素的两种核素,
A
下列说法正确的是( )
A.71 g 35Cl 和71 g 37Cl 均含2N 个Cl原子
2 2 A
B.35Cl和37Cl间的相互转化是化学变化
C.35Cl和37Cl核外电子排布方式相同
D.35Cl、H 形成的燃料电池,35Cl 在负极放电
2 2 2
3.(2022·辽宁省大连高三模拟)下列说法正确的是( )
A.IUPAC公布了118号元素Og,其中核素Og中中子数与质子数之差为179
B.18 g HO与20 g DO中质子数与中子数均为10N
2 2 A
C.a g X2-中核外电子数为(Z+2)N
AD.金刚石与石墨互为同位素
4.反应NH Cl+NaNO ===NaCl+N↑+2HO放热且产生气体,可用于冬天石油开采。下列表示反应中相关
4 2 2 2
微粒的化学用语正确的是( )
A.中子数为18的氯原子:Cl
B.N 的结构式:N===N
2
C.Na+的结构示意图:
D.HO的电子式:
2
5.(2022·河北衡水高三调研)全氮类物质具有高密度、超高能量及爆轰、产物无污染等优点。中国科学家
成功合成全氮阴离子N,N是制备全氮类物质NN的重要中间体。下列说法中,不正确的是( )
A.全氮类物质属于绿色能源
B.每个N中含有35个质子
C.NN属于离子化合物
D.NN结构中含共价键和离子键
考点 02 元素周期表与元素周期律
1.元素周期表的结构
①“七横七周期,三短三长一不全;十八纵行十六族,七主七副一Ⅷ一0”。
②从左到右族的分布:
ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ、ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
Ⅷ族:包括8、9、10三个纵列。
③0族:第18纵列,该族元素又称为稀有气体元素。
其原子序数为He 2,Ne 10,Ar 18,Kr 36,Xe 54,Rn 86。
④同周期第ⅡA和第ⅢA原子序数的差值可能为:1、11、25。
2.分区
①分界线:沿着元素周期表中硼、硅、砷、碲、砹与铝、锗、锑、钋的交界处画一条虚线,即为金属
元素区和非金属元素区的分界线。
②各区位置:分界线左下方为金属元素区,分界线右上方为非金属元素区。
③分界线附近元素的性质:既表现金属元素的性质,又表现非金属元素的性质。
3.元素周期表中的特殊位置
①过渡元素:元素周期表中部从Ⅲ B族到ⅡB族10个纵列共六十多种元素,这些元素都是金属元
素。
②镧系:元素周期表第6周期中,57号元素镧到71号元素镥共15种元素。
③锕系:元素周期表第7周期中,89号元素锕到103号元素铹共15种元素。
④超铀元素:在锕系元素中92号元素轴(U)以后的各种元素。
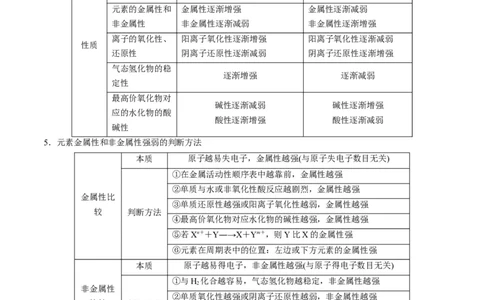
4.主族元素的周期性变化规律项目 同周期(左→右) 同主族(上→下)
核电荷数 逐渐增大 逐渐增大
电子层数 相同 逐渐增多
原子结
原子半径 逐渐减小 逐渐增大
构
阳离子逐渐减小阴离子逐渐减
离子半径 逐渐增大
小r(阴离子)>r(阳离子)
最高正化合价由+1→+7(O、F
相同,最高正化合价=主
化合价 除外)负化合价=-(8-主族序
族序数(O、F除外)
数)(H为-1价)
元素的金属性和 金属性逐渐增强 金属性逐渐减弱
非金属性 非金属性逐渐减弱 非金属性逐渐增强
离子的氧化性、 阳离子氧化性逐渐增强 阳离子氧化性逐渐减弱
性质
还原性 阴离子还原性逐渐减弱 阴离子还原性逐渐增强
气态氢化物的稳
逐渐增强 逐渐减弱
定性
最高价氧化物对
碱性逐渐减弱 碱性逐渐增强
应的水化物的酸
酸性逐渐增强 酸性逐渐减弱
碱性
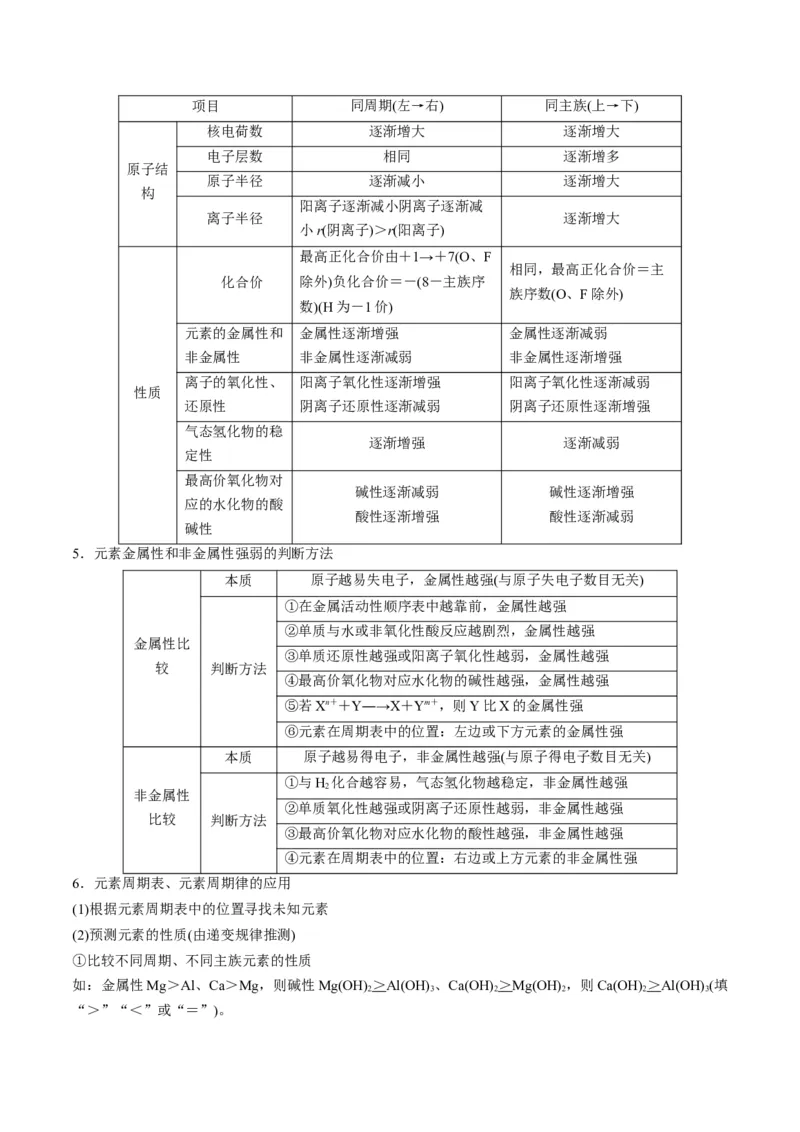
5.元素金属性和非金属性强弱的判断方法
本质 原子越易失电子,金属性越强(与原子失电子数目无关)
①在金属活动性顺序表中越靠前,金属性越强
②单质与水或非氧化性酸反应越剧烈,金属性越强
金属性比
③单质还原性越强或阳离子氧化性越弱,金属性越强
较 判断方法
④最高价氧化物对应水化物的碱性越强,金属性越强
⑤若Xn++Y―→X+Ym+,则Y比X的金属性强
⑥元素在周期表中的位置:左边或下方元素的金属性强
本质 原子越易得电子,非金属性越强(与原子得电子数目无关)
①与H 化合越容易,气态氢化物越稳定,非金属性越强
2
非金属性
②单质氧化性越强或阴离子还原性越弱,非金属性越强
比较 判断方法
③最高价氧化物对应水化物的酸性越强,非金属性越强
④元素在周期表中的位置:右边或上方元素的非金属性强
6.元素周期表、元素周期律的应用
(1)根据元素周期表中的位置寻找未知元素
(2)预测元素的性质(由递变规律推测)
①比较不同周期、不同主族元素的性质
如:金属性Mg>Al、Ca>Mg,则碱性Mg(OH) >Al(OH) 、Ca(OH) >Mg(OH) ,则Ca(OH) >Al(OH) (填
2 3 2 2 2 3
“>”“<”或“=”)。②推测未知元素的某些性质
如:已知Ca(OH) 微溶,Mg(OH) 难溶,可推知Be(OH) 难溶;再如:已知卤族元素的性质递变规律,可
2 2 2
推知砹(At)应为有色固体,与氢难化合,HAt不稳定,水溶液呈酸性,AgAt不溶于水等。
(3)启发人们在一定区域内寻找新物质
①半导体元素在金属与非金属分界线附近,如:Si、Ge、Ga等。
②农药中常用元素在右上方,如:F、Cl、S、P、As等。
③催化剂和耐高温、耐腐蚀合金材料主要在过渡元素中找,如:Fe、Ni、Rh、Pt、Pd等。
1.一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子
序数依次增大、且总和为24。下列有关叙述错误的是
A. 该化合物中,W、X、Y之间均为共价键
B. Z的单质既能与水反应,也可与甲醇反应
C. Y的最高化合价氧化物的水化物为强酸
D. X的氟化物XF 中原子均为8电子稳定结构
3
2.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和为 10。X与Z同族,Y最外层电子数等于
X次外层电子数,且Y原子半径大于Z。下列叙述正确的是( )
A.熔点:X的氧化物比Y的氧化物高
B.热稳定性:X的氢化物大于Z的氢化物
C.X与Z可形成离子化合物ZX
D.Y的单质与Z的单质均能溶于浓硝酸
3.科学家合成出了一种新化合物(如图所示),其中W、X、Y、Z为同一短周期元素,Z核外最外层电子数
是X核外电子数的一半,下列叙述正确的是( )
A.WZ的水溶液呈碱性
B.元素非金属性的顺序为X>Y>Z
C.Y的最高价氧化物的水化物是中强酸
D.该新化合物中Y不满足8电子稳定结构
4.今年是门捷列夫发现元素周期律150周年。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元
素,W与X的最高化合价之和为8。下列说法错误的是( )
A.原子半径:W<XB.常温常压下,Y单质为固态
C.气态氢化物热稳定性:Z<W
D.X的最高价氧化物的水化物是强碱
5.短周期元素W、X、Y和Z在周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为
21。下列关系正确的是( )
W X
Y Z
A.氢化物沸点:WW
C.化合物熔点:YX X>Y> Z B. 原子半径:Z>Y>X>W
C. 元素X的含氧酸均为强酸 D. Y的氧化物水化物为强碱
8.X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,Y元素与Z、M元
素相邻,且与M元素同主族;化合物 的电子总数为18个;Q元素的原子最外层电子数比次外层少一
个电子。下列说法不正确的是( )
A. 原子半径:
B. 最高价氧化物对应水化物的酸性:
C. 易溶于水,其水溶液呈碱性
D. X、Z和Q三种元素形成的化合物一定是共价化合物
考点 03 微粒间的相互作用力
1.共价键与离子键的比较
离子键 共价键非极性键 极性键
阴、阳离子通过静电
概念 原子间通过共用电子对而形成的化学键
作用所形成的化学键
成键粒子 阴、阳离子 原子
阴、阳离子的静电作 共用电子对不偏向任何 共用电子对偏向
成键实质
用 一方 一方原子
活泼金属元素与活泼
不同种元素原子
形成条件 非金属元素经电子得 同种元素原子之间成键
之间成键
失,形成离子键
非金属单质;某些共价 共价化合物或离
形成的物质 离子化合物
化合物或离子化合物 子化合物
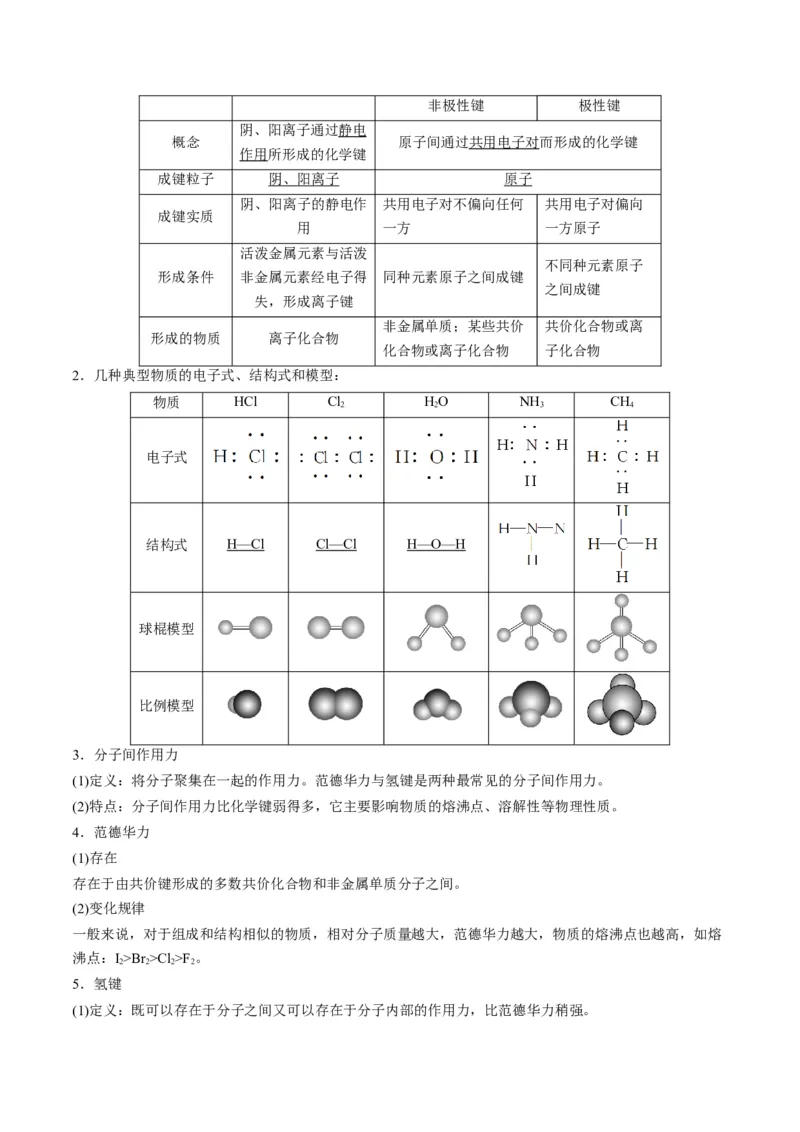
2.几种典型物质的电子式、结构式和模型:
物质 HCl Cl HO NH CH
2 2 3 4
电子式
结构式 H—Cl Cl—Cl H—O—H
球棍模型
比例模型
3.分子间作用力
(1)定义:将分子聚集在一起的作用力。范德华力与氢键是两种最常见的分子间作用力。
(2)特点:分子间作用力比化学键弱得多,它主要影响物质的熔沸点、溶解性等物理性质。
4.范德华力
(1)存在
存在于由共价键形成的多数共价化合物和非金属单质分子之间。
(2)变化规律
一般来说,对于组成和结构相似的物质,相对分子质量越大,范德华力越大,物质的熔沸点也越高,如熔
沸点:I>Br >Cl>F 。
2 2 2 2
5.氢键
(1)定义:既可以存在于分子之间又可以存在于分子内部的作用力,比范德华力稍强。(2)形成条件:非金属性强、原子半径小的O、F、N原子与H原子之间。
(3)存在:氢键存在广泛,如蛋白质分子、HO、NH 、HF等分子之间,有的物质分子内也存在氢键。分子
2 3
间氢键会使物质的熔点和沸点升高。
常用物质结构的化学用语
(1)四种符号
①元素符号:Al、S
②离子符号:Al3+、S2-、SO
③同位素符号:6C、6C
④化合价符号:Al O、HS
2 3 2
(2)七种图式
①化学式:NaO、NH Cl、SiO
2 2 4 2
②分子式:C H、NH
2 4 3
③最简式(实验式):CH、CHO
2 2
⑦原子结构示意图:
(3)两种模型
①比例模型,如甲烷的比例模型:
②球棍模型,如甲烷的球棍模型:
1.下列反应只需要破坏共价键的是( )
A.晶体硅熔化 B.碘升华 C.熔融 Al O D.NaCl 溶于水
2 3
2.下列表示不正确的是
A.羟基的电子式: B.乙烯的结构简式:CHCH
2 2
C.氯原子的结构示意图: D.NH 分子的球棍模型:
3
3.下列说法正确的是( )
A.35Cl和37Cl是两种不同的元素 B.单晶硅和石英互为同素异形体
C.HCOOH和HOCH CHO互为同系物 D.H与 在元素周期表中处于同一主族
24.下列说法正确的是( )
A.18O 和16O 互为同位素
2 2
B.正己烷和2,2−二甲基丙烷互为同系物
C.C 和C 是具有相同质子数的不同核素
60 70
D.HNCH COOCH 和CHCHNO 是同分异构体
2 2 3 3 2 2
5.下列说法正确的是( )
A.水的沸点较高是因为水分子间存在较强的化学键
B.离子晶体中可能存在共价键, 而分子晶体中一定存在共价键
C.CO 与 SiO 均为共价化合物,其固体熔化时,均破坏了分子间作用力
2 2
D.某物质熔点 1067°C, 易溶于水,其水溶液和熔融态均能导电,其晶体一定为离子晶体
1.(2022·湖南卷)下列说法错误的是
A.氢键,离子键和共价键都属于化学键
B.化学家门捷列夫编制了第一张元素周期表
C.药剂师和营养师必须具备化学相关专业知识
D.石灰石是制造玻璃和水泥的主要原料之一
2.(2022·广东卷)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对
应的水化物为强酸。下列说法不正确的是
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
3.(2022·全国甲卷)Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19。
Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍。下列说法正
确的是
A.非金属性: B.单质的熔点:
C.简单氢化物的沸点: D.最高价含氧酸的酸性:
4.(2022·湖南卷)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增
大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是A.原子半径:
B.非金属性:
C.Z的单质具有较强的还原性
D.原子序数为82的元素与W位于同一主族
5.(2022·浙江卷)X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其
周期数, 分子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期
中非金属性最强的元素。下列说法正确的是
A.X与Z形成的10电子微粒有2种
B.Z与Q形成的一种化合物可用于饮用水的消毒
C. 与 的晶体类型不同
D.由X、Y、Z三种元素组成的化合物的水溶液均显酸性
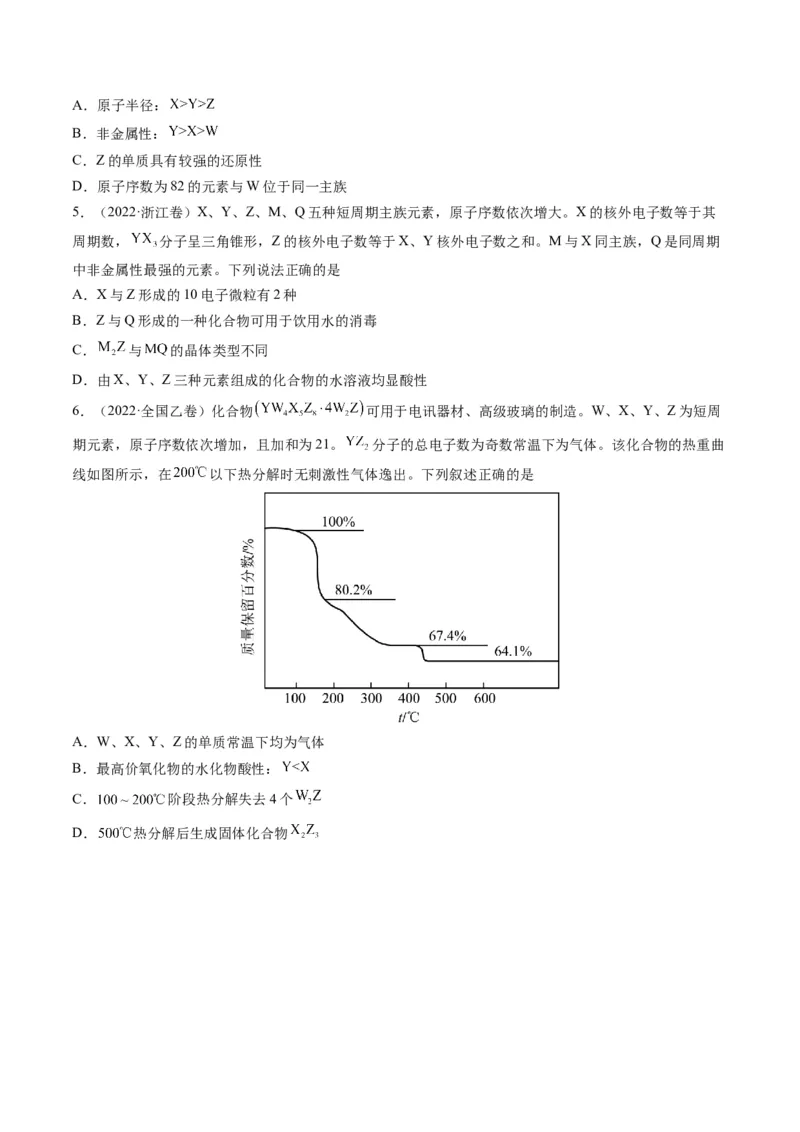
6.(2022·全国乙卷)化合物 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
期元素,原子序数依次增加,且加和为21。 分子的总电子数为奇数常温下为气体。该化合物的热重曲
线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是
A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个
D. 热分解后生成固体化合物