文档内容
专题 11 水溶液中离子反应
1.(2023·安徽省皖优联盟高三第二次阶段测试)下列有关NaHCO 的说法中错误的是( )
3
A.NaHCO 溶液中:c(OH―)>c(H+)
3
B.NaHCO 溶液中:n(Na+)= n(CO 2-)+ n(HCO -)+ n(H CO)
3 3 3 2 3
C.苏打是NaHCO 的俗称,可用于食品加工
3
D.加热滴加有酚酞的NaHCO 溶液时,溶液颜色会加深
3
【答案】C
【解析】A项,NaHCO 溶液中,HCO -既能水解又能电离且水解能力强于电离能力,故溶液显碱性,A
3 3
项正确;B项,由物料守恒知,n(Na+)= n(CO 2-)+ n(HCO -)+ n(H CO),B项正确;C项,NaHCO 的俗称是小
3 3 2 3 3
苏打,是发酵粉的主要成分之一,C项错误;D项,加热能促进HCO -水解,使溶液中:c(OH―)增大,加有酚
3
酞的NaHCO 溶液时,溶液颜色会加深,D项正确;故选C。
3
2.(2023·上海·卢湾高级中学高三期中)Na CO 溶液中存在水解平衡:CO2-+H O OH-+HCO-。下列
2 3 3 2 3
说法错误的是( )
A.通入CO,溶液pH减小 B.加入NaOH固体, 减小
2
C.加水稀释,溶液中所有离子的浓度都减小 D.升高温度,平衡常数增大
【答案】C
【解析】A项, 二氧化碳消耗氢氧根离子,pH减小,A正确;B项,加入NaOH固体,溶液中c(OH-)增
大,平衡逆向移动,c(HCO -)减小,c(CO2-)增大,所以该比值减小,B正确;C项,加水稀释,溶液碱性减弱,
3 3
氢离子浓度增大,C错误;D项,水解反应吸热,升高温度平衡正向移动,平衡常数增大,D正确;故选C。
3.(2023·广东省百校高三联考)苯甲酸钠(PhCOONa)是一种常用食品防腐剂。已知25℃,PhCOOH的
K=1.0×10-4.2。下列有关PhCOONa溶液说法不正确的是( )
a
A.PhCOONa溶液呈碱性
B.0.1mol/L PhCOONa溶液中: c(PhCOO-)<0.1mol/L
C. 25℃,pH=7的PhCOONa和PhCOOH的混合溶液中:c(PhCOOH)>c(PhCOO-) = c(Na+)
D.PhCOONa溶液加水稀释时,溶液中c(PhCOO-)减小
【答案】C【解析】A项, 由题干信息中苯甲酸的Ka可知,PhCOONa是强碱弱酸盐,由于PhCOO-+H O
2
PhCOOH+OH-,故PhCOONa溶液呈碱性,A正确;B项,由于PhCOO-+H O PhCOOH+OH-,根据物料
2
守恒可知,0.1mol/L PhCOONa溶液中有c(PhCOO-)+c(PhCOOH)=0.1mol/L,则c(PhCOO-)<0.1mol/L,B正确;
C项,25℃,pH=7的PhCOONa和PhCOOH的混合溶液中根据电荷守恒可知:c(Na+)+c(H+)=c(PhCOO-)
+c(OH-),则得到c(Na+)+c(H+)=c(PhCOO-),根据Ka= = =10-4.2,可得
c(PhCOO-)>c(PhCOOH),即有c(PhCOO-) = c(Na+)>c(PhCOOH),C错误;D项,PhCOONa溶液加水稀释时,
PhCOO-+H O PhCOOH+OH-平衡正向移动,故溶液中c(PhCOO-)减小,D正确;故选C。
2
4.(2023·浙江省宁波市高三选考模拟考试)下列说法正确的是( )
A.25℃时,将pH=5的醋酸溶液与pH=5的盐酸等体积混合,混合后溶液pH>5
B.25℃时,等浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸
C.25℃时,等体积、等pH的盐酸与醋酸分别用等浓度的NaOH溶液中和,盐酸消耗NaOH溶液多
D.25℃时,pH=3的一元酸HA溶液与pH=11的一元碱MOH溶液等体积混合后溶液呈酸性,则HA是强
酸
【答案】B
【解析】A项,pH=5的醋酸溶液与pH=5的盐酸中氢离子浓度相同,都是10-5mol/L,等体积混合后,氢
离子浓度不变,故pH为5,A错误;B项,等浓度的盐酸与醋酸分别稀释相同倍数后其浓度依然相同,醋酸
是弱酸,部分电离,氢离子浓度较小,pH大,B正确;C项,等体积、等pH的盐酸与醋酸,其中醋酸的浓度
大,用氢氧化钠中和时消耗的氢氧化钠较多,C错误;D项,混合后溶液呈酸性,说明酸的浓度较大,则酸
HA为弱酸,MOH是相对较强的碱,但是不一定是强碱,D错误;故选B。
5.已知某温度下CHCOOH和NH ·H O 的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CHCOOH溶
3 3 2 3
液中滴加相同浓度的氨水,在滴加过程中( )
A.水的电离程度始终增大
B.c(NH)/c(NH ·H O)先增大再减小
3 2
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10 mL时,c(NH)=c(CHCOO-)
3
【答案】D
【解析】开始滴加氨水时,水的电离程度增大,二者恰好完全反应时,水的电离程度最大,再继续滴加氨
水时,水的电离程度减小,A项错误;向醋酸中滴加氨水,溶液的酸性减弱,碱性增强,c(OH-)增大,由
NH ·H O NH+OH-可知K=,则=,故减小,B项错误;根据原子守恒知n(CHCOO-)与n(CHCOOH)
3 2 3 3之和不变,但滴加氨水过程中,溶液体积不断增大,故 c(CHCOO-)与c(CHCOOH)之和减小,C项错误;由
3 3
CHCOOH和NH ·H O的电离常数相等可知当二者恰好完全反应时,溶液呈中性,结合电荷守恒知 c(CHCOO
3 3 2 3
-)+c(OH-)=c(NH)+c(H+),则c(CHCOO-)=c(NH),D项正确。
3
6.某研究小组为测定食用白醋中醋酸的含量进行了如下操作,正确的是( )
A.用碱式滴定管量取一定体积的待测白醋放入锥形瓶中
B.称取4.0 g NaOH放到100 mL容量瓶中,加水至刻度线,配成1.00 mol/L NaOH标准溶液
C.用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时
为滴定终点
D.滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量
【答案】C
【解析】A项不能用碱式滴定管量取白醋,应用酸式滴定管,错误;B项应先在烧杯中溶解固体,不能直
接在容量瓶中溶解,错误;C项强碱滴定弱酸,用酚酞作指示剂,颜色变化符合滴定终点判断,正确;D项滴
定时眼睛应注视锥形瓶内溶液颜色变化,错误。
7.把Ca(OH) 放入蒸馏水中,一段时间后达到平衡:Ca(OH) (s) Ca2+(aq)+2OH-(aq)。下列说法
2 2
正确的是( )
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入NaCO 溶液,其中固体质量增加
2 3
D.向溶液中加入少量NaOH固体,Ca(OH) 固体质量不变
2
【答案】C
【解析】恒温下K 不变,加入CaO后,溶液仍为Ca(OH) 的饱和溶液,pH不变,A项错误;加热,
sp 2
Ca(OH) 的溶解度减小,溶液的pH降低,B项错误;加入NaCO 溶液,沉淀溶解平衡向右移动,Ca(OH) 固
2 2 3 2
体转化为CaCO 固体,固体质量增加,C项正确;加入NaOH固体,溶液温度升高,Ca(OH) 溶解度减小,且
3 2
溶液中c(OH-)增大,平衡向左移动,Ca(OH) 固体质量增加,D项错误。
2
8.已知Ag CrO 是砖红色沉淀,下列滴定反应中,指示剂使用不正确的是( )
2 4
A.用标准FeCl 溶液滴定KI溶液,选择KSCN溶液
3
B.用I 溶液滴定NaSO 溶液,淀粉作指示剂
2 2 3
C.用AgNO 溶液滴定NaCl溶液,NaCrO 作指示剂
3 2 4
D.用HO 溶液滴定KI溶液,淀粉作指示剂
2 2
【答案】D
【解析】A项,铁离子与碘离子反应,生成亚铁离子和碘单质,KSCN溶液遇铁离子显红色,当溶液显红色时,说明碘离子反应完全,达到滴定终点,正确;B项,淀粉遇碘单质显蓝色,当溶液显蓝色时,说明亚硫
酸根离子已经被碘单质充分氧化,碘单质剩余,达到滴定终点,正确;C项,Ag CrO 是砖红色沉淀,当溶液
2 4
中有砖红色沉淀时,待测液中的氯离子被充分沉淀,银离子剩余,正确;D项,待测液中的碘离子被双氧水氧
化生成碘单质,淀粉显蓝色,即开始滴定就出现蓝色,蓝色加深,碘离子反应完全时,蓝色不再加深,但是
不易观察,不能判断滴定终点,错误。
9.室温下,向20.00 mL 0.1000 mol·L−1盐酸中滴加0.1000 mol·L−1 NaOH溶液,溶液的pH随NaOH溶液
体积的变化如图,已知lg3=0.5。下列说法不正确的是( )
A.选择变色范围在pH突变范围内的指示剂,可减小实验误差
B.用移液管量取20.00 mL 0.1000 mol·L−1盐酸时,移液管水洗后需用待取液润洗
C.NaOH标准溶液浓度的准确性直接影响分析结果的可靠性,因此需用邻苯二甲酸氢钾标定NaOH溶液
的浓度,标定时采用甲基橙为指示剂
D.V(NaOH)=10.00 mL 时,pH约为1.5
【答案】C
【解析】A项,根据突变范围选择合适的指示剂,要求指示剂的指示范围与突变范围有重叠,所以选择变
色范围在pH突变范围内的指示剂,可减小实验误差,A正确;B项,移液管水洗后需用待取液润洗,这样不
改变盐酸的浓度,可减小实验误差,B正确;C项,甲基橙的指示范围是3.1~4.4,甲基红的指示范围是
4.4~6.2,二者差不多,而甲基红的指示范围与突变范围重叠更大,更能降低误差,因此应该使用甲基红,
C错误;D项,V(NaOH)=10.00 mL时,HCl过量,反应后相当于余下10mL的HCl,溶液为酸性,溶液中
c(H+)= = mol/L,所以溶液pH=-lgc(H+)=-lg1+lg30=1.5,D正确;故选C。
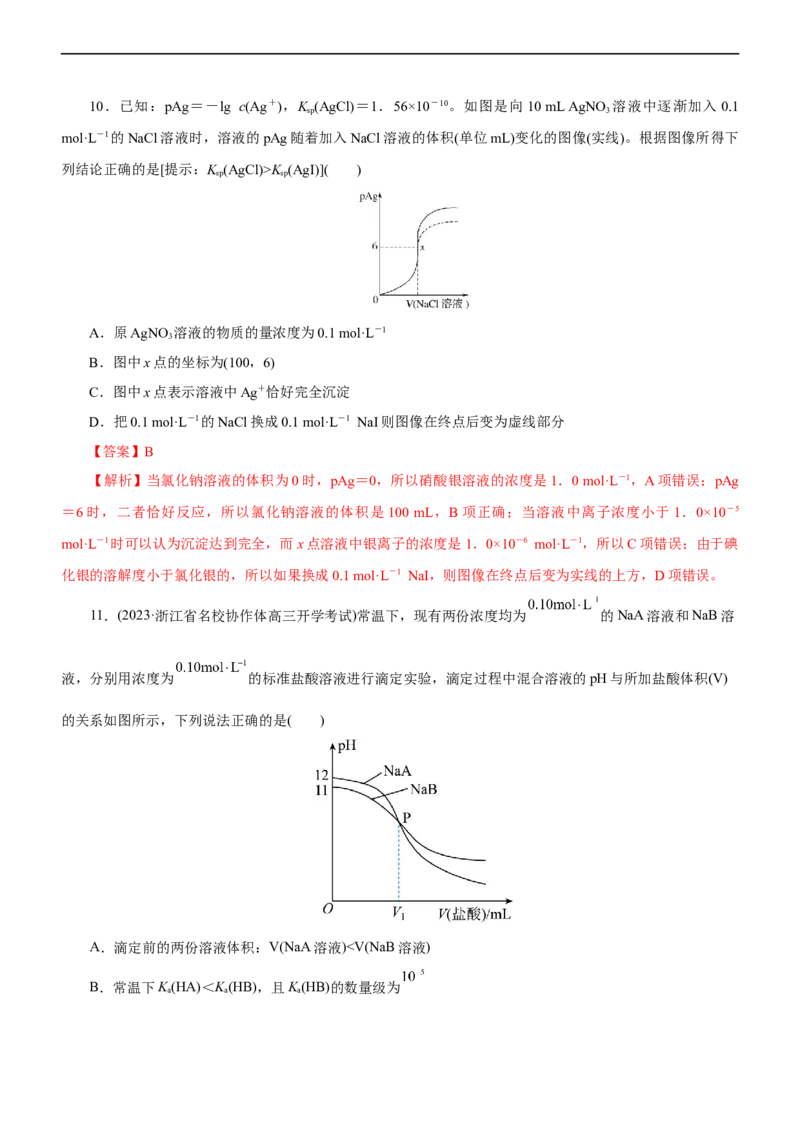
10.(2023·浙江省七彩阳光新高考研究联盟高三返校联考)已知HX、HY均为一元酸,室温下用
NaOH溶液分别滴定20.00mL等物质的量浓度的HX、HY溶液时的滴定曲线如下。下列有关说
法正确的是( )A.a=20
B.HX可能为强酸,HY一定是弱酸
C.若E为滴定终点,则室温下K(HY)<1.0×10-6
a
D.图中B、D两点对应的溶液中存在c(Y-)=c(X+)
【答案】B
【解析】常温下,0.1000mol/LNaOH溶液分别滴定20.00mL等物质的量浓度的两种一元酸HX、HY溶液,
起始时HX和HY两种酸的浓度相同,酸性越强,则溶液中c(H + ),pH就越小,结合溶液中的守恒思想和图象,
据此分析判断。A项,由图像可知浓度均为0.1000mol·L-1的两种一元酸,HY的pH=3,部分电离,为弱酸;
HX的pH=1溶液,全部电离,为强酸;HX溶液用NaOH溶液滴定呈中性时消耗20mLNaOH,则同样滴定到
中性的HY溶液消耗的NaOH溶液大于20mL,a﹥20,故A错误;B项,由图可知,HY一定是弱酸,HX酸
性比HY强,a﹥20,所以B、D两点对应溶液的总体积不相等,c(X+)和c(Y-)也不可能相等,故B正确;C项,
由图像可知浓度均为0.1000mol·L-1的两种一元酸,HY的pH=3,则室温下 ﹥10-
6,故C错误;D项,由图可知,HY一定是弱酸,HX酸性比HY强,a﹥20,所以B、D两点对应溶液的总体
积不相等,c(X+)和c(Y-)也不可能相等,故D错误;故选B。
11.(2022·江苏省泰州市高三联考)室温下,通过下列实验探究NaHS溶液的性质。
实验 实验操作和现象
1 向0.1mol•L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红
2 向0.1mol•L-1NaHS溶液中加入等体积0.1mol•L-1NaOH溶液充分混合
3 向0.1mol•L-1NaHS溶液中通入过氯气,无淡黄色沉淀产生
4 向0.1mol•L-1NaHS溶液中滴加过CuCl 溶液,产生黑色沉淀
2
下列有关说法正确的是( )A.0.1mol/LNaHS溶液中:c(HS-)>c(S2-)>c(H S)
2
B.实验2所得溶液中:c(Na+)-c(S2-)-c(HS-)-c(HS)=0.05mol•L-1
2
C.实验3证明HS-不能被氧化
D.实验4反应静置后的上层清液中有c(Cu2+)•c(S2-)c(CHCOOH)
3
【答案】C
【解析】a~b段,醋酸电离过程为吸热过程,电解质溶于水,扩散过程(电离)吸热,水合过程(形成水合
离子)放热,A错误;c~d段,醋酸浓度增大,c(H+)增加,醋酸电离程度减小,B错误;c点时,加入等体积
等浓度的NaOH溶液,根据物料守恒,有c(Na+)=c(CHCOO-)+c(CHCOOH),C正确;醋酸是弱酸,电离是
3 3
微弱的,在溶液中主要以分子的形式存在,故d点时,c(H+)
【答案】C
【解析】A项,NaS溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H S),A错误;
2 2
B项,向AgCl悬浊液加入足量氨水,溶液变澄清,得到银氨溶液,离子方程式为
AgCl+2NH•H O=[Ag(NH)]++Cl-+2H O,B错误;C项,反应2AgCl+S2- Ag S+2Cl-的平衡常数K=
3 2 3 2 2 2
= = = =2×1028,当浓度商Q= <K时,反应正向移动,C正
确;D项,根据题意沉淀发生转化,即体系中不会生成AgCl沉淀,所以c(Ag+)< ,D错误;故选
C。4.(2022·河南省名校联盟高三联考)天门冬氨酸( ,记为HY)是一种天然氨基酸,水溶液显
2
酸性,溶液中存在HY H++HY-,HY- H++Y2-,与足量NaOH反应生成NaY ,与盐酸反应生成
2 2
YH Cl。下列说法正确的是( )
3
A.常温下,0.05 mol·L-1的HY溶液的pH=1
2
B.pH=2.97的HY溶液稀释100倍,所得溶液pH=4.97
2
C.YH Cl水溶液中:c(H+)+c(YH-)= c(OH-)+ c(Cl-)+c(HY-)
3 3
D.NaY溶液中:c(OH-)=c(H+)+c(HY-)+ 2c(HY)+3c(YH -)
2 2 3
【答案】D
【解析】A项,HY部分电离,常温下,0.05 mol·L-1的HY溶液的pH>1,A错误;B项,稀释过程中电
2 2
离程度增大,pH=2.97的HY溶液稀释100倍,所得溶液pH<4.97,B错误;C项,根据电荷守恒知,YH Cl水
2 3
溶液中:c(H+)+c(YH-)= c(OH-)+ c(Cl-)+c(HY-)+ 2c(Y2-),C错误;D项,根据电荷守恒和物料守恒知,NaY溶
3 2
液中:c(OH-)=c(H+)+c(HY-)+ 2c(HY)+3c(YH -),D正确;故选D。
2 3
5.(2022·河南省实验中学高三期中)一种测定水样中溴离子浓度的实验步骤如下:
①向锥形瓶中加入处理后的水样25.00mL,加入几滴NH Fe(SO ) 溶液。
4 4 2
②加入V mL c mol∙L−1AgNO 溶液(过量),充分摇匀。
1 1 3
③用c mol∙L−1KSCN标准溶液进行滴定,至终点时消耗标准溶液VmL 。
2 2
已知:K (AgBr)=7.7×10−13,Ag++SCN-= AgSCN(白色)↓,K (AgSCN)=1×10−12,下列说法不正确的是
sp sp
( )
A.滴定终点时,溶液变为红色
B.该水样中溴离子浓度为:c(Br-)= mol∙L−1
C.AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数K=0.77
D.该实验需要严格控制水样的pH,若pH过高则测定结果将偏高
【答案】D
【解析】A项,加入几滴NH Fe(SO ) 指示剂,滴定终点时,KSCN过量,会与铁离子反应,因此溶液变
4 4 2
为红色,故A正确;B项,25mL溶液中Br-物质的量n(Br-)= V ×10−3 L×c mol∙L−1− V ×10−3 L×c
1 1 2 2
mol∙L−1=(V c − V c ) ×10−3 mol,因此该水样中溴离子浓度为:c(Br-)= mol∙L−1,故B正确;C项,
1 1 2 2AgBr(s)+SCN-(aq) AgSCN(s)+Br-(aq)的平衡常数 ,故C正
确;D项,该实验需要严格控制水样的pH,若pH过高,银离子会与氢氧根反应,则得到的溴离子物质的量减
少,则测定结果将偏低,故D错误。故选D。
6.(2023·浙江省强基联盟高三上学期10月统测)25℃时,按下表配制两份溶液。
一元弱酸溶液 加入的NaOH溶液 混合后所得溶液
溶液ⅠpH=5.0
溶液ⅡpH=4.0
下列说法不正确的是( )
A.溶液Ⅰ中:c(A-)>c(Na+)>c(H+)>c(OH-)
B.混合Ⅰ和Ⅱ:c(Na+)=c(A-)+c(HA)= c(B-)+c(HB)
C.Ⅰ和Ⅱ的pH相差1.0,说明
D.将等体积、等 的NaA、NaB溶液稀释相同倍数,pH变化更大的是NaA溶液
【答案】C
【解析】A项,溶液Ⅰ为等物质量的HA、NaA,溶液显酸性,则酸的电离程度大于盐的水解,故c(A-)>
c(Na+)>c(H+)>c(OH-),A正确;B项,混合Ⅰ和Ⅱ,则得到等物质的量的HA、NaA、HB、NaB,根据物料守
恒可知,c(Na+)=c(A-)+c(HA)= c(B-)+c(HB),B正确;C项,溶液Ⅰ为等物质量的HA、NaA,HA电离程度微
弱,c(A-) ≈c(HA), ,同理, ,则Ⅰ和Ⅱ的pH相差1.0,说明
,C错误;D项,由C分析可知,酸性HB>HA,将等体积、等pH的NaA、NaB溶液稀释相同
倍数,NaA水解程度变化更大,pH变化更大的是NaA溶液,D正确;故选C。
7.(2022·江苏省南通市海门区高三第二次诊断测试)室温下: 、 、
、 实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:实验 实验操作和现象
1 测定0.10mol•L-1NaHCO 溶液的pH约为8
3
测定0.10mol•L-1HCN与0.05mol•L-1NaOH溶液等体积混合,测得混合溶液的
2
pH>7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1NaCO 溶液中加入等体积0.02mol•L-1CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)+c(H+)= c(OH-)+c(CO 2-)+c(HCO-)
3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2 = CO2-+2HClO
2 2 3
D.实验4所得上层清液中的
【答案】D
【解析】由电离常数可知,弱酸和酸式根离子在溶液中的电离程度为HCO>HClO>HCO -;由实验1可
2 3 3
知,碳酸氢根离子在溶液中的水解趋势大于电离趋势,使溶液呈碱性;由实验2可知,0.10mol•L-1氢氰酸与
0.05mol•L-1氢氧化钠溶液等体积混合后反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电离程度小于
氰酸根离子的水解程度,使溶液呈碱性。A项,碳酸氢钠溶液中存在的电荷守恒关系为c(Na+)+c(H+)= c(OH-)
+2c(CO 2-)+c(HCO-),故A错误;B项,实验2中0.10mol•L-1氢氰酸与0.05mol•L-1氢氧化钠溶液等体积混合后
3 3
反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电离程度小于氰酸根离子的水解程度,使溶液呈碱性,
则氢氰酸的电离常数K(HCN)小于水解常数 ,故B错误;C.项,弱酸和酸式根离子在溶液
a
中的电离程度为HCO>HClO>HCO -,则次氯酸钠溶液与少量二氧化碳反应生成碳酸氢钠和次氯酸,反应的
2 3 3
离子方程式为CO+H O+ClO-= HCO -+HClO,故C错误;D项,由题意可知,VL0.01mol/L碳酸钠溶液和
2 2 3
VL0.02mol/L氯化钙溶液等体积混合反应后溶液中过量的钙离子浓度为
=0.005mol/L,由碳酸钙的溶度积可知溶液中碳酸根离子浓度为 = =2×10—6.55mol/L,故D正确;
故选D。8.(2023·江苏省南通市高三期中)室温下: , , ,
。实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:
实验 实验操作和现象
1 测定0.10mol•L-1 NaHCO 溶液的pH约为8
3
2 测定0.10mol•L-1HCN与0.05mol•L-1NaOH溶液等体积混合,测得混合溶液的pH>7
3 向NaClO溶液中通入少量的CO,测得pH降低
2
4 向0.01mol•L-1 Na CO 溶液中加入等体积0.03mol•L-1 CaCl 溶液,产生白色沉淀
2 3 2
下列所得结论正确的是( )
A.实验1溶液中存在:c(Na+)>c(H CO)>c(HCO -)>c(CO2-)>c(H+)
2 3 3 3
B.由实验2可得
C.实验3反应的离子方程式:CO+H O+2ClO-=CO 2-+2HClO
2 2 3
D.实验4所得上层清液中的c(CO2-)=1.0×10-6.55mol·L-1
3
【答案】D
【解析】由电离常数可知,弱酸和酸式根离子在溶液中的电离程度为HCO>HClO>HCO -;由实验1可
2 3 3
知,碳酸氢根离子在溶液中的水解趋势大于电离趋势,使溶液呈碱性;由实验2可知,0.10mol•L-1氢氰酸与
0.05mol•L-1氢氧化钠溶液等体积混合后反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电离程度小于
氰酸根离子的水解程度,使溶液呈碱性。A项,NaHCO 溶液中碳酸氢根离子浓度小于钠离子浓度,但远大于
3
碳酸分子浓度;NaHCO 溶液显碱性,说明碳酸氢根离子在溶液中的水解趋势大于电离趋势,故c(Na+)>
3
c(HCO -)>c(H CO) ,故A错误;B项,实验2中0.10mol•L-1氢氰酸与0.05mol•L-1氢氧化钠溶液等体积混合后
3 2 3
反应得到等浓度的氢氰酸和氰酸钠的混合溶液,氢氰酸的电离程度小于氰酸根离子的水解程度,使溶液呈碱性,
则氢氰酸的电离常数K(HCN)< , ,故B错误;C项,弱酸和酸式根离子在溶液中的
a
电离程度为HCO>HClO>HCO -,则次氯酸钠溶液与少量二氧化碳反应生成碳酸氢钠和次氯酸,反应的离子
2 3 3
方程式为CO+H O+ClO-=HCO-+HClO,故C错误;D项,由题意可知,VL0.01mol/L碳酸钠溶液和
2 2 3
VL0.03mol/L氯化钙溶液等体积混合反应后溶液中过量的钙离子浓度为 mol/L=0.01mol/L,由碳酸钙的溶度积可知溶液中碳酸根离子浓度为 ,故D正确;故选D。
9.常温下,有关物质的溶度积如下
物质 CaCO MgCO Ca(OH) Mg(OH) Fe(OH)
3 3 2 2 3
K 4.96×10-9 6.82×10-6 4.68×10-6 5.61×10-12 2.64×10-39
sp
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
B.常温下,除去NaCl溶液中的CaCl 杂质,选用NaOH溶液比NaCO 溶液效果好
2 2 3
C. 向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg 2+)∶c(Fe3+)
=2 .125×1021
D.将适量的Ca(OH) 固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.054×10-2mol/L],若保持温度不变,
2
向其中加入100mL 0.012mol/L的NaOH,则该溶液变为不饱和溶液。
【答案】B
【解析】A项, 因为MgCO 是微溶物,其溶度积远远大于Mg(OH) ,所以除去NaCl溶液中的MgCl 杂
3 2 2
质,选用NaOH溶液比NaCO 溶液效果好,A项正确;B项, 因为Ca(OH) 是微溶物,其溶度积远大于
2 3 2
CaCO ,所以除去NaCl溶液中的CaCl 杂质,选用NaCO 溶液比NaOH溶液效果好,B项错误;C项, 向含
3 2 2 3
有 Mg2+ 、 Fe3+ 的 溶 液 中 滴 加 NaOH 溶 液 , 当 两 种 沉 淀 共 存 且 溶 液 的 pH=8 时 ,
, , 所 以
,C项正确;D项,将适量的Ca(OH) 固体溶于100mL水中,刚
2
好达到饱和,c(Ca2+)=1.054×10-2mol/L,c(OH-)=2.108×10-2mol/L,若保持温度不变,向其中加入 100mL
0.012mol/L 的 NaOH , 混 合 后 , c(Ca2+)=0.527×10-2mol/L ,
, 此 时 Ca(OH) 的 离 子 积
2
,则该溶液变为不饱和溶液,D项正确;故选
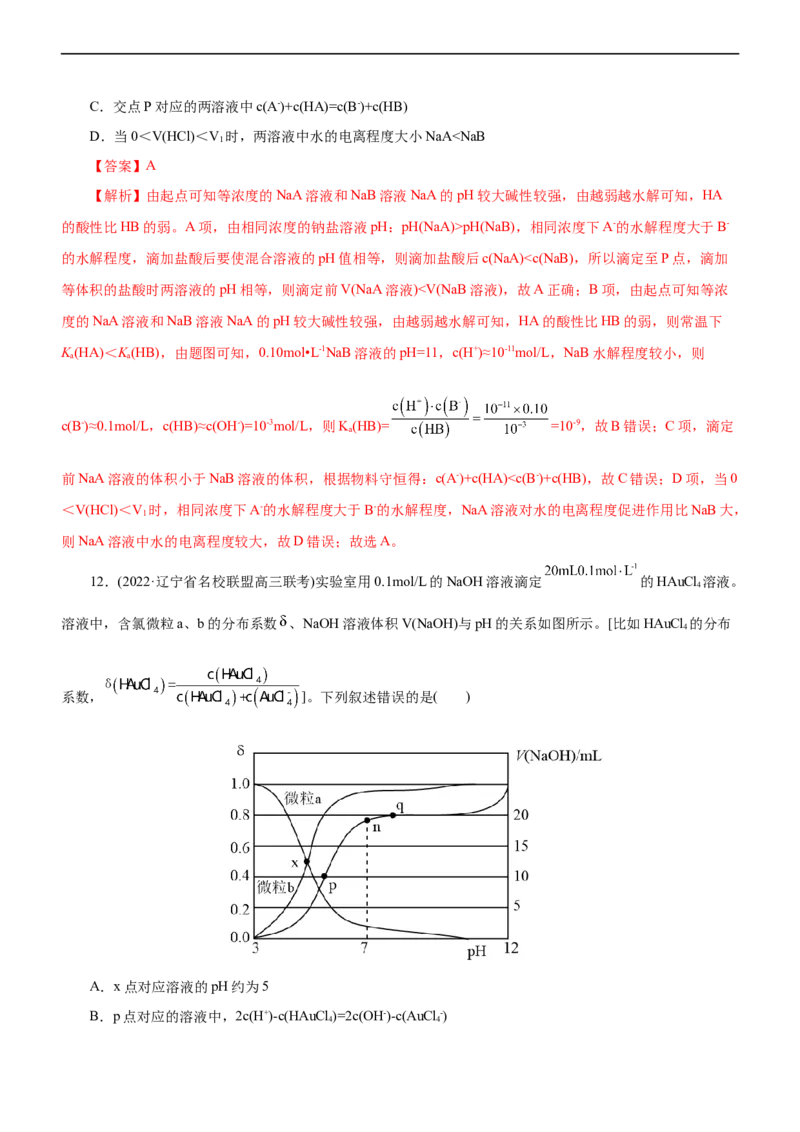
B。10.已知:pAg=-lg c(Ag+),K (AgCl)=1.56×10-10。如图是向10 mL AgNO 溶液中逐渐加入 0.1
sp 3
mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图像(实线)。根据图像所得下
列结论正确的是[提示:K (AgCl)>K (AgI)]( )
sp sp
A.原AgNO 溶液的物质的量浓度为0.1 mol·L-1
3
B.图中x点的坐标为(100,6)
C.图中x点表示溶液中Ag+恰好完全沉淀
D.把0.1 mol·L-1的NaCl换成0.1 mol·L-1 NaI则图像在终点后变为虚线部分
【答案】B
【解析】当氯化钠溶液的体积为0时,pAg=0,所以硝酸银溶液的浓度是1.0 mol·L-1,A项错误;pAg
=6时,二者恰好反应,所以氯化钠溶液的体积是100 mL,B项正确;当溶液中离子浓度小于1.0×10-5
mol·L-1时可以认为沉淀达到完全,而x点溶液中银离子的浓度是1.0×10-6 mol·L-1,所以C项错误;由于碘
化银的溶解度小于氯化银的,所以如果换成0.1 mol·L-1 NaI,则图像在终点后变为实线的上方,D项错误。
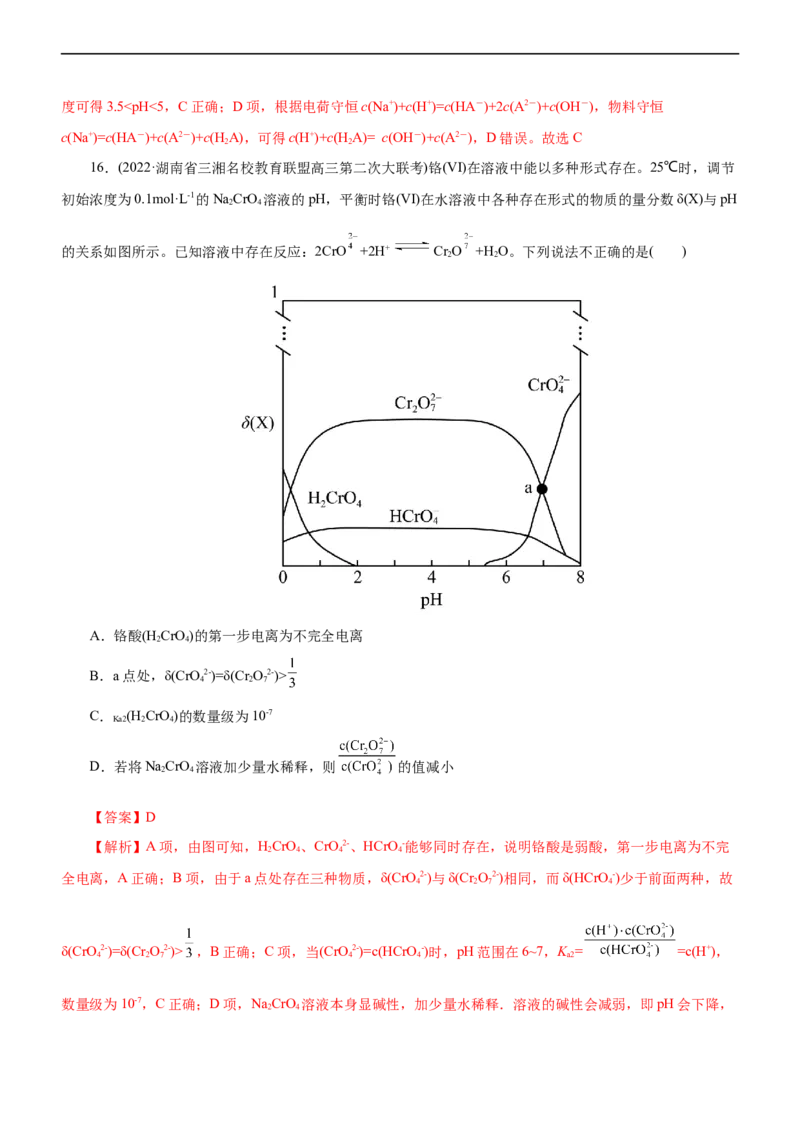
11.(2023·浙江省名校协作体高三开学考试)常温下,现有两份浓度均为 的NaA溶液和NaB溶
液,分别用浓度为 的标准盐酸溶液进行滴定实验,滴定过程中混合溶液的pH与所加盐酸体积(V)
的关系如图所示,下列说法正确的是( )
A.滴定前的两份溶液体积:V(NaA溶液)pH(NaB),相同浓度下A-的水解程度大于B-
的水解程度,滴加盐酸后要使混合溶液的pH值相等,则滴加盐酸后c(NaA)c(HA-)>c(H A)
2【答案】C
【解析】随pH增大,c(HA)逐渐减小,c(HA-)先增大后减小,c(A2-)逐渐增大,pc=-lgc,则pc(HA)逐渐
2 2
增大、pc(HA-)先减小后增大、pc(A2-)逐渐减小,即曲线Ⅰ、Ⅱ、Ⅲ分别代表的粒子为HA、A2-、HA-。A项,
2
随pH增大, c(HA-)先增大后减小,pc=-lgc,则pc(HA-)先减小后增大,即曲线Ⅲ代表c(HA-)变化,故A正确;
B项,曲线Ⅰ、Ⅱ、Ⅲ分别代表的粒子为HA、A2-、HA-,c点时c(HA-)=c(A2-),此时K =
2 a2
=c(H+)=10-pH=10-5.30,则 ,故B正确;C项,b点时,c(HA)= c(A2-)=10-3mol/L,c(H+)=10-
2
3.05mol/L,室温下c(OH-)= ,由电荷守恒:c(H+)+ c(Na+)= c(OH-)+ c(HA-)+2 c(A2-),则
c(Na+)= 2 c(A2-)+ c(OH-)- c(H+)+ c(HA-)= c(HA-),故C错误;D项,pH=6.00时,
由图知pc(HA-)> pc(A2-)> pc(HA),pc=-lgc,则c(A2-)>c(HA-)>c(H A),故D正确;故选C。
2 2
14.(2022·安徽省百校联盟高三联考)马来酸又称顺丁烯二酸,可简写为HX,主要用于制造不饱和聚酯树
2
脂、染色助剂和油脂防腐剂等。常温下,将 溶液滴加到 等浓度的HX溶液中,测得混合溶液的
2
与 或 浓度变化关系如图所示。下列叙述错误的是( )A.N代表 与 的变化曲线
B.a点时,加入NaOH溶液的体积为5mL
C.NaHX溶液中:c(Na+)>c(HX-)>c(X2-)>c(HX)
2
D.当pH=7时,加入NaOH溶液的体积大于
【答案】B
【解析】A项,由图可知,横坐标加纵坐标为 或 ,即 或 ,
由于 ,所以 ,所以N表示 与pH的变化曲线,A正确;B项,当
时, ,当 时, ,当加入NaOH溶液体积
为5mL时,溶液中为等物质的量浓度的HX和NaHX,HX的电离常数(10-12)远大于HX-的电离常数(10-6.0)和水
2 2
解常数(10-12.8),所以 ,而a点是两者相等的点,B错误;C项,HX-的电离常数为 ,水解
常数为 ,电离大于水解,NaHX溶液中离子浓度大小关系为c(Na+)>c(HX-)>c(X2-)>c(HX),C正
2
确;D项,NaHX溶液呈酸性,当溶液呈中性时,应为NaHX和NaX的混合溶液,加入NaOH溶液的体积大
2
于10mL,D正确。故选B。
15.(2022·山东省学情高三质量检测)常温下,用一定浓度稀盐酸滴定某二元弱酸盐 溶液,溶液中
和 或 和 关系如图所示,下列说法正确的是( )A.水的电离程度:M点>N点
B.滴定过程中,当pH=5时,c(Na+)-3c(HA-)>0
C.若c(HA-)>c(A2-)>c(H A),则pH范围3.5K ,可以肯定M线是-1g[c(H+)/c(H A)]和-1gc(HA-)的关系,那么N线就是-lg[c(H+)/c(HA-)]和-lgc(A2
a1 a2 2
-)的关系,M线是第一步电离,N线是第二步电离。A项,K =10-1×10-1=10-2,K =10-3×10-2=10-5,
a1 a2
K >K ,第一步电离程度大,相当于酸性强,故M点水的电离弱于N点,A错误;B项,当pH=5时,溶液呈
a1 a2
酸性,c(H+)=10-5由K =10-5,由K = 得c(A2-)=c(HA-)根据电荷守恒,c(Na+)+c(H+)=c(HA-)
a2 a2
+2c(A2-)+c(OH-),c(Na+)-3c(HA-)=c(OH-)-c(H+)<0,B错误;C项,c(HA-)>c(A2-)>c(H A)同时除以
2
c(H A)得 >1.由K ,K ,K ×K 的表达式可知上式为 ,解出c(H+)的浓
2 a1 a2 a1 a2度可得3.5
4 2 7
C. (H CrO)的数量级为10-7
Ka2 2 4
D.若将NaCrO 溶液加少量水稀释,则 的值减小
2 4
【答案】D
【解析】A项,由图可知,HCrO、CrO2-、HCrO -能够同时存在,说明铬酸是弱酸,第一步电离为不完
2 4 4 4
全电离,A正确;B项,由于a点处存在三种物质,δ(CrO 2-)与δ(Cr O2-)相同,而δ(HCrO -)少于前面两种,故
4 2 7 4
δ(CrO 2-)=δ(Cr O2-)> ,B正确;C项,当(CrO 2-)=c(HCrO-)时,pH范围在6~7,K = =c(H+),
4 2 7 4 4 a2
数量级为10-7,C正确;D项,NaCrO 溶液本身显碱性,加少量水稀释.溶液的碱性会减弱,即pH会下降,
2 4c(H+)上升,2CrO2--+2H+ Cr O2-+H O平衡右移,使n(CrO 2-)下降,n(CrO2-)上升,同一溶液中,
4 2 7 2 4 2 7
故比值增大,D错误;故选D。
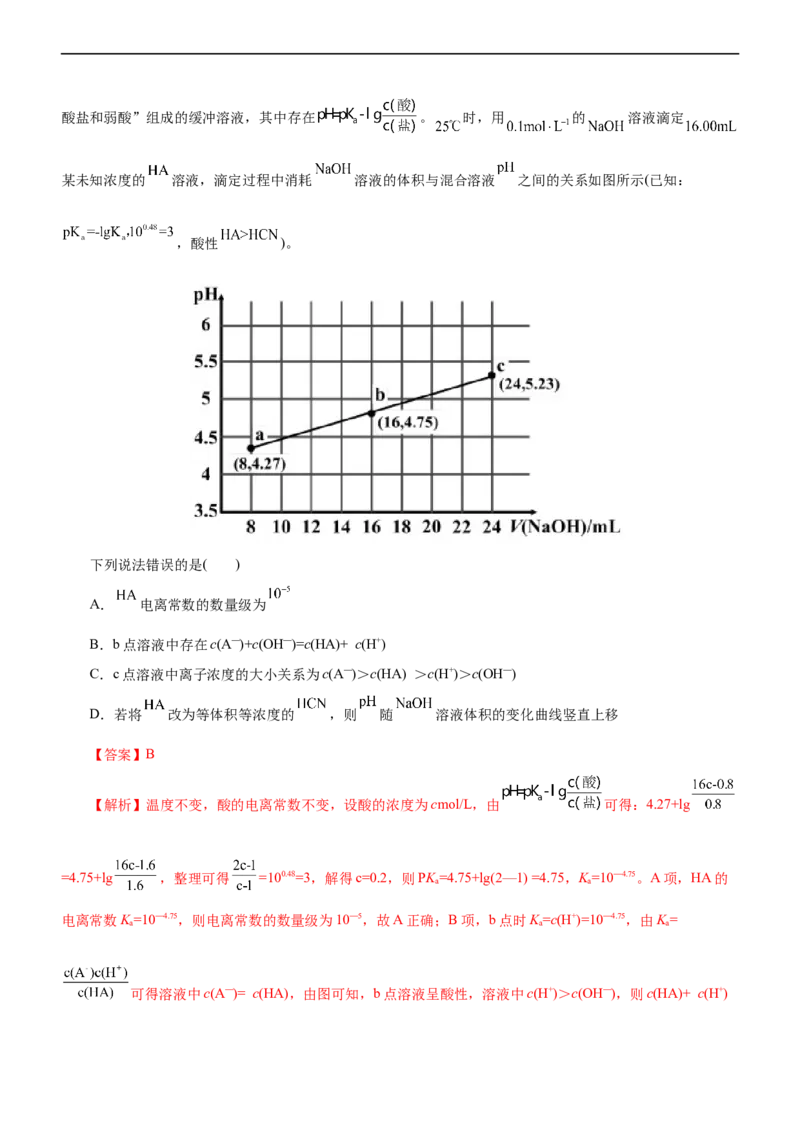
17.(2022·广东省高考研究测评研究院高三联考)常温下,向二元弱酸HA溶液中加入NaOH固体,配制
2
一组c(HA)+c(HA-)+ c(A2-)=0.01 mol·L-1的混合溶液,溶液中含A微粒的物质的量浓度随pH的变化曲线如下图
2
所示。下列说法不正确的是( )
A.K =10 K
a1 a2
B.M点溶液中, c(Na+)=0.01 mol·L-1
C.M点溶液中由水电离出的c(H+)小于N点溶液中由水电离出的c(H+)
D.NaHA溶液中,c(HA) 小于c(A2-)
2
【答案】B
【解析】由题干图示可知,二元弱酸的电离方程式为H HA-+H+,HA A2-+H+,图中实线为
2
HA,过M点的实线为HA-,过N点的虚线为A2-。A项,由图可知,pH=4.4时,c(HA)=c(HA-),则
2 2
,同理K =10-5.4,则K =10 K ,A确;B项,M点时,由电荷守恒可知:c(Na+)
a1 a1 a2
+c(H+)=2c(A2-)+ c(HA-)+c(OH-),又此时c(HA)= c(A2-),且c(H+)>c(OH-),则c(Na+)<c(HA)+c(HA-)+ c(A2-)<
2 2
0.01 mol·L-1,B错误;C项,M点时,NaOH滴定HA仍未到达生成NaA的滴定终点,此时水的电离程度一
2 2
直在增大,C正确;D项,由于K =10 K >K ,则NaHA的电离程度大于水解程度,c(HA)小于c(A2-),D正
a1 a2 W 2
确;故选B。
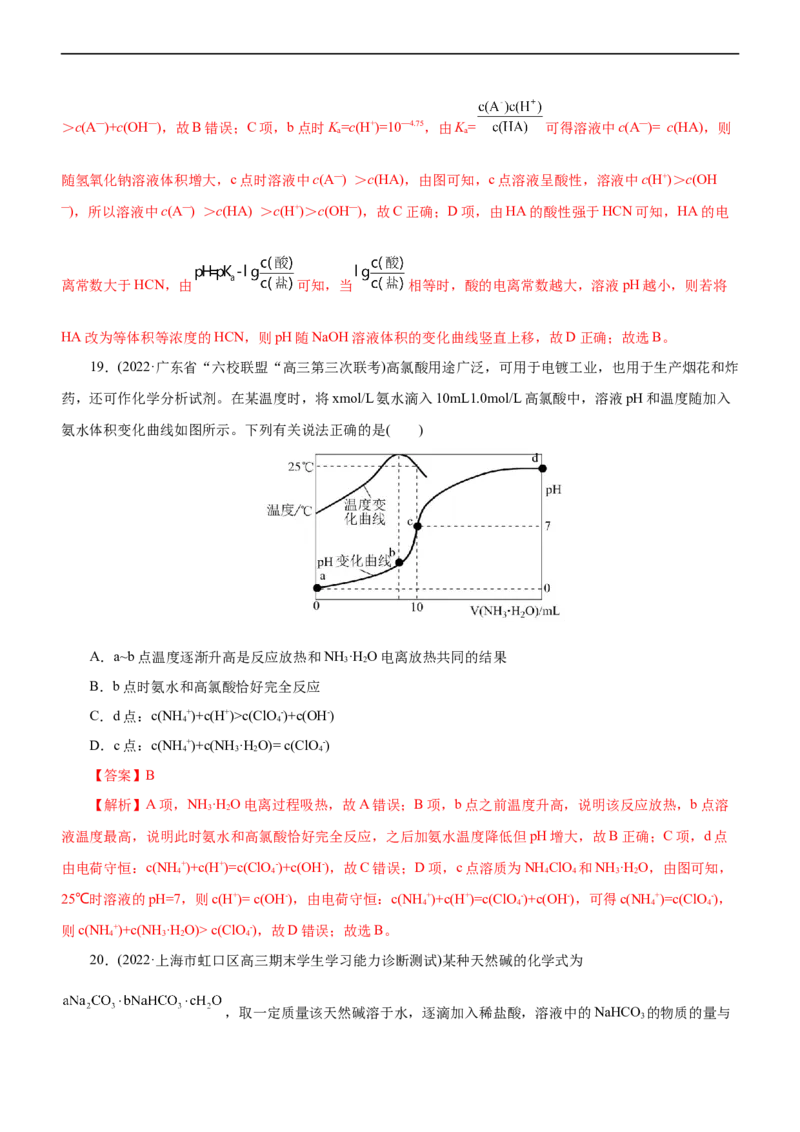
18.(2022·河北省石家庄市高三教学质量检测)用强碱滴定某一元弱酸时,弱酸被强碱部分中和后得到“弱酸盐和弱酸”组成的缓冲溶液,其中存在 。 时,用 的 溶液滴定
某未知浓度的 溶液,滴定过程中消耗 溶液的体积与混合溶液 之间的关系如图所示(已知:
,酸性 )。
下列说法错误的是( )
A. 电离常数的数量级为
B.b点溶液中存在c(A—)+c(OH—)=c(HA)+ c(H+)
C.c点溶液中离子浓度的大小关系为c(A—)>c(HA) >c(H+)>c(OH—)
D.若将 改为等体积等浓度的 ,则 随 溶液体积的变化曲线竖直上移
【答案】B
【解析】温度不变,酸的电离常数不变,设酸的浓度为cmol/L,由 可得:4.27+lg
=4.75+lg ,整理可得 =100.48=3,解得c=0.2,则PK=4.75+lg(2—1) =4.75,K=10—4.75。A项,HA的
a a
电离常数K=10—4.75,则电离常数的数量级为10—5,故A正确;B项,b点时K=c(H+)=10—4.75,由K=
a a a
可得溶液中c(A—)= c(HA),由图可知,b点溶液呈酸性,溶液中c(H+)>c(OH—),则c(HA)+ c(H+)>c(A—)+c(OH—),故B错误;C项,b点时K=c(H+)=10—4.75,由K= 可得溶液中c(A—)= c(HA),则
a a
随氢氧化钠溶液体积增大,c点时溶液中c(A—) >c(HA),由图可知,c点溶液呈酸性,溶液中c(H+)>c(OH
—),所以溶液中c(A—) >c(HA) >c(H+)>c(OH—),故C正确;D项,由HA的酸性强于HCN可知,HA的电
离常数大于HCN,由 可知,当 相等时,酸的电离常数越大,溶液pH越小,则若将
HA改为等体积等浓度的HCN,则pH随NaOH溶液体积的变化曲线竖直上移,故D正确;故选B。
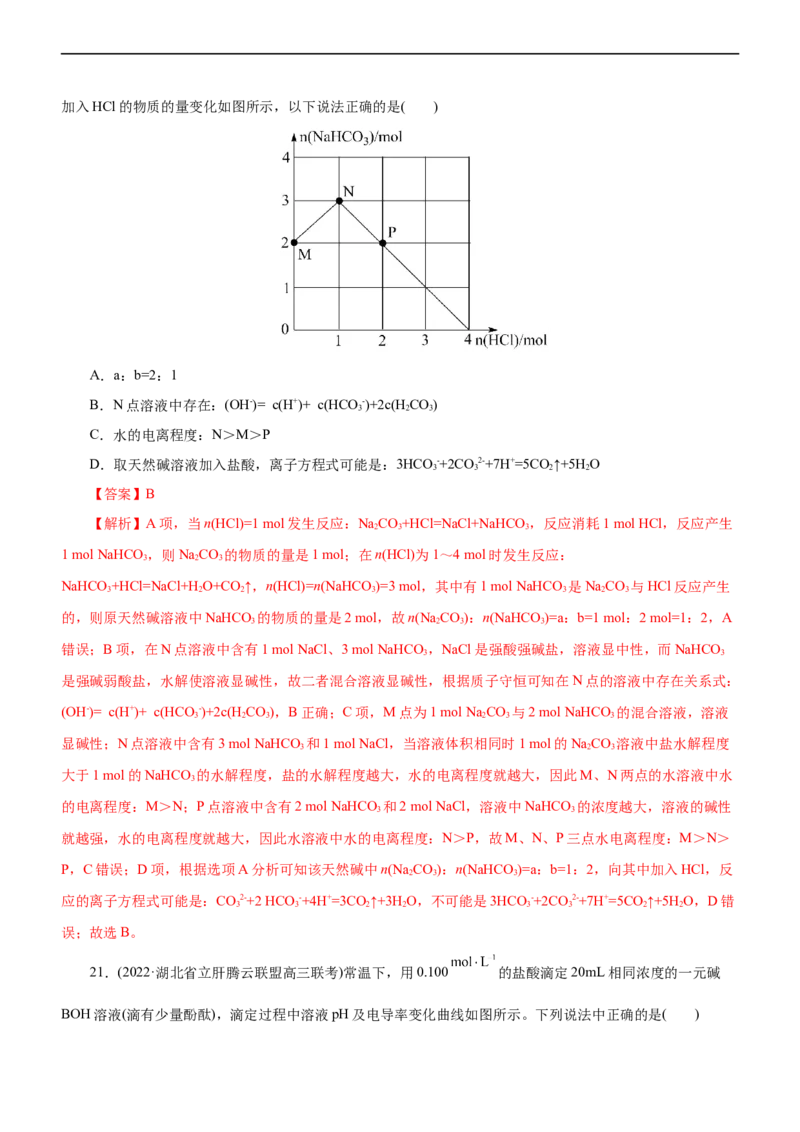
19.(2022·广东省“六校联盟“高三第三次联考)高氯酸用途广泛,可用于电镀工业,也用于生产烟花和炸
药,还可作化学分析试剂。在某温度时,将xmol/L氨水滴入10mL1.0mol/L高氯酸中,溶液pH和温度随加入
氨水体积变化曲线如图所示。下列有关说法正确的是( )
A.a~b点温度逐渐升高是反应放热和NH ·H O电离放热共同的结果
3 2
B.b点时氨水和高氯酸恰好完全反应
C.d点:c(NH +)+c(H+)>c(ClO -)+c(OH-)
4 4
D.c点:c(NH +)+c(NH·H O)= c(ClO-)
4 3 2 4
【答案】B
【解析】A项,NH ·H O电离过程吸热,故A错误;B项,b点之前温度升高,说明该反应放热,b点溶
3 2
液温度最高,说明此时氨水和高氯酸恰好完全反应,之后加氨水温度降低但pH增大,故B正确;C项,d点
由电荷守恒:c(NH +)+c(H+)=c(ClO -)+c(OH-),故C错误;D项,c点溶质为NH ClO 和NH ·H O,由图可知,
4 4 4 4 3 2
25℃时溶液的pH=7,则c(H+)= c(OH-),由电荷守恒:c(NH +)+c(H+)=c(ClO -)+c(OH-),可得c(NH +)=c(ClO -),
4 4 4 4
则c(NH +)+c(NH·H O)> c(ClO-),故D错误;故选B。
4 3 2 4
20.(2022·上海市虹口区高三期末学生学习能力诊断测试)某种天然碱的化学式为
,取一定质量该天然碱溶于水,逐滴加入稀盐酸,溶液中的NaHCO 的物质的量与
3加入HCl的物质的量变化如图所示,以下说法正确的是( )
A.a:b=2:1
B.N点溶液中存在:(OH-)= c(H+)+ c(HCO -)+2c(HCO)
3 2 3
C.水的电离程度:N>M>P
D.取天然碱溶液加入盐酸,离子方程式可能是:3HCO -+2CO 2-+7H+=5CO ↑+5H O
3 3 2 2
【答案】B
【解析】A项,当n(HCl)=1 mol发生反应:NaCO+HCl=NaCl+NaHCO ,反应消耗1 mol HCl,反应产生
2 3 3
1 mol NaHCO,则NaCO 的物质的量是1 mol;在n(HCl)为1~4 mol时发生反应:
3 2 3
NaHCO +HCl=NaCl+H O+CO↑,n(HCl)=n(NaHCO )=3 mol,其中有1 mol NaHCO 是NaCO 与HCl反应产生
3 2 2 3 3 2 3
的,则原天然碱溶液中NaHCO 的物质的量是2 mol,故n(Na CO):n(NaHCO )=a:b=1 mol:2 mol=1:2,A
3 2 3 3
错误;B项,在N点溶液中含有1 mol NaCl、3 mol NaHCO,NaCl是强酸强碱盐,溶液显中性,而NaHCO
3 3
是强碱弱酸盐,水解使溶液显碱性,故二者混合溶液显碱性,根据质子守恒可知在N点的溶液中存在关系式:
(OH-)= c(H+)+ c(HCO -)+2c(HCO),B正确;C项,M点为1 mol Na CO 与2 mol NaHCO 的混合溶液,溶液
3 2 3 2 3 3
显碱性;N点溶液中含有3 mol NaHCO 和1 mol NaCl,当溶液体积相同时1 mol的NaCO 溶液中盐水解程度
3 2 3
大于1 mol的NaHCO 的水解程度,盐的水解程度越大,水的电离程度就越大,因此M、N两点的水溶液中水
3
的电离程度:M>N;P点溶液中含有2 mol NaHCO 和2 mol NaCl,溶液中NaHCO 的浓度越大,溶液的碱性
3 3
就越强,水的电离程度就越大,因此水溶液中水的电离程度:N>P,故M、N、P三点水电离程度:M>N>
P,C错误;D项,根据选项A分析可知该天然碱中n(Na CO):n(NaHCO )=a:b=1:2,向其中加入HCl,反
2 3 3
应的离子方程式可能是:CO2-+2 HCO -+4H+=3CO ↑+3H O,不可能是3HCO -+2CO 2-+7H+=5CO ↑+5H O,D错
3 3 2 2 3 3 2 2
误;故选B。
21.(2022·湖北省立肝腾云联盟高三联考)常温下,用0.100 的盐酸滴定20mL相同浓度的一元碱
BOH溶液(滴有少量酚酞),滴定过程中溶液pH及电导率变化曲线如图所示。下列说法中正确的是( )A.BOH的电离常数K 约为
b
B.a点溶液中:
C.b点溶液的颜色为粉红色
D.滴定至pH=7时,
【答案】B
【解析】A项,0.10mol/LBOH溶液的pH=11,则该溶液中 ,BOH为弱
碱,其电离程度较小,则溶液中c(BOH)≈0.10mol/L,c(B+)≈c(OH-)=0.01mol/L,BOH的
,故A错误;B项,a点酸物质的量是碱物质的量的一半,则混合溶液
中溶质为等物质的量浓度的BOH、BCl,a点溶液中存在电荷守恒c(B+)+c(H+)=c(OH-)+c(Cl-)、存在物料守恒
c(B+)+c(BOH)=2c(Cl-),所以存在c(B+)+2c(H+)=2c(OH-)+c(BOH),故B正确;C项,b点加入酸碱物质的量相等,
二者恰好完全反应生成BCl,溶液中溶质为BCl,假设a点BOH不电离且B+不水解,b点B+不水解,a点
c(B+)= 、b点c(B+)= ,混合溶液中BOH电离程度
和B+水解程度都较小,则b点溶液几乎为中性,溶液应为无色,故C错误;D项,混合溶液pH=7时,溶液呈
中性,c(H+)=c(OH-),溶液中存在电荷守恒c(B+)+c(H+)=c(OH-)+c(Cl-),则c(B+)=c(Cl-),酸碱混合后导致溶液体积增大,则导致溶液中c(Cl-)减小,所以存在c(B+)=c(Cl-)<0.1mol•L-1,故D错误;故选B。
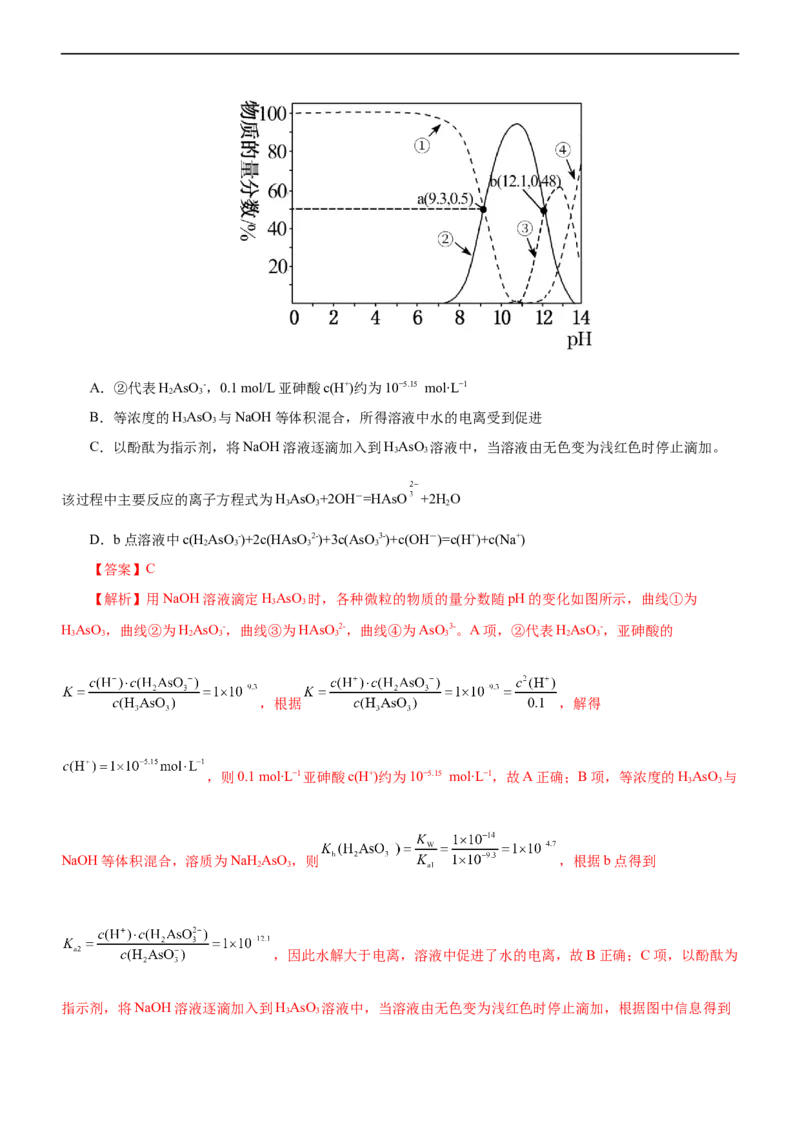
21.(2022·江苏省如皋市高三期中)草酸钠(Na C O)可作为基准物质测定KMnO 溶液的浓度。测定的方法
2 2 4 4
是准确称量一定质量的草酸钠固体,加水溶解后,加入硫酸酸化,用待测KMnO 溶液进行滴定。HC O 是一
4 2 2 4
种二元弱酸,C O2-能与Ca2+结合生成CaC O 沉淀。已知K (CaC O)=2.5×10-9,K (CaSO)=4.9×10-5。控制
2 4 2 4 sp 2 4 sp 4
NaC O 溶液的pH,溶液中HC O、HC O-和C O2-三种粒子的分布分数随溶液pH变化的关系如图所示。下
2 2 4 2 2 4 2 4 2 4
列说法正确的是( )
A.HC O 的电离平衡常数K =10-12
2 2 4 a1
B.pH=6时:c(C O2- )=10c(HC O-)
2 4 2 4
C.0.1mol·L-1NaHC O 溶液中:c(C O2-)>c(HC O)
2 4 2 4 2 2 4
D.用0.1mol·L-1NaSO 溶液浸泡CaC O 固体,会有少量CaSO 生成
2 4 2 4 4
【答案】C
【解析】HC O 在水溶液中的电离平衡:HC O HC O-+H+,HC O- C O2-+ H+,pH减小
2 2 4 2 2 4 2 4 2 4 2 4
(H+浓度增大)平衡逆向移动pH增大(H+浓度减小),平衡正向移动,所以,pH最小时,溶液中含碳粒子主要是
HC O 最大时,溶液中的含碳粒子主要是C O2-曲线σ 代表HC O 的含量曲线,σ 代表HC O-的含量曲线,σ
2 2 4 2 4 0 2 2 4 1 2 4 2
代表C O2-的含量。A项,σ 代表HC O 的含量曲线σ 与σ 交点数据计算,c(C O2-)=c(HC O-),pH=1.2,
2 4 0 2 2 4 0 1 2 4 2 4
HC O 的电离平衡常数K =10-1.2,A错误;B项,pH=6时:σ(C O2-)=1,σ(HC O-)=0,B错误;C项,
2 2 4 a1 2 4 2 4
0.1mol·L-1NaHC O 溶液中电荷守恒:c(Na+)+ c(H+)= c(HC O-)+2c(C O2-)+ c(OH -)①,物料守恒:
2 4 2 4 2 4
c(Na+)=c(H C O)+ c(C O2-)+ c(HC O-)②,①②联立可得:c(H+) +c(HC O)= c(OH -)+c(C O2-),NaHC O 为强
2 2 4 2 4 2 4 2 2 4 2 4 2 4
碱弱酸盐,c(H+) <c(OH -),则c(C O2-)>c(HC O),C正确;D项,K (CaC O)=2.5×10-9<
2 4 2 2 4 sp 2 4
K (CaSO)=4.9×10-5,不会有少量CaSO 生成,D错误;故选C。
sp 4 4
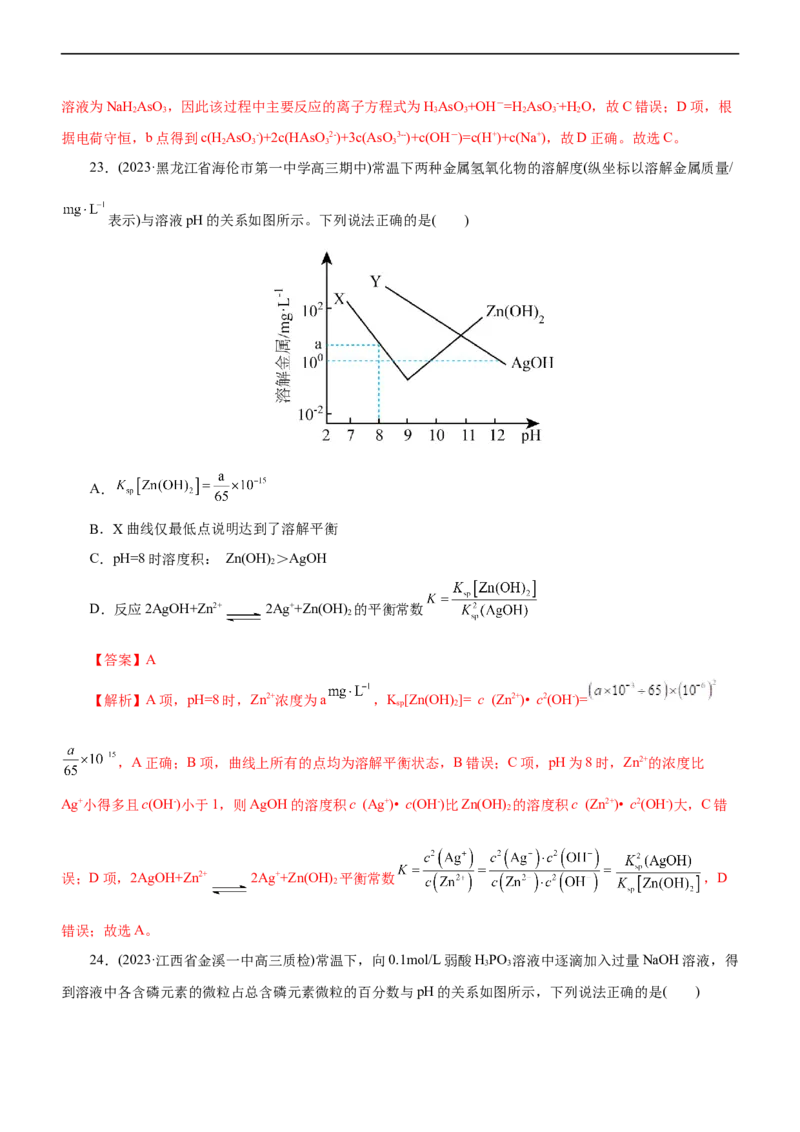
22.(2022·“四校八校”高三期中质量检测)亚砷酸(H AsO )作为一种化疗药物,常用于白血病的治疗,其
3 3
在水溶液中存在多种微粒形态。常温下,用NaOH溶液滴定HAsO 时,各种微粒的物质的量分数随pH的变
3 3
化如图所示。下列说法不正确的是( )A.②代表HAsO -,0.1 mol/L亚砷酸c(H+)约为10−5.15 mol∙L−1
2 3
B.等浓度的HAsO 与NaOH等体积混合,所得溶液中水的电离受到促进
3 3
C.以酚酞为指示剂,将NaOH溶液逐滴加入到HAsO 溶液中,当溶液由无色变为浅红色时停止滴加。
3 3
该过程中主要反应的离子方程式为HAsO +2OH-=HAsO +2H O
3 3 2
D.b点溶液中c(HAsO -)+2c(HAsO 2-)+3c(AsO 3-)+c(OH-)=c(H+)+c(Na+)
2 3 3 3
【答案】C
【解析】用NaOH溶液滴定HAsO 时,各种微粒的物质的量分数随pH的变化如图所示,曲线①为
3 3
HAsO ,曲线②为HAsO -,曲线③为HAsO2-,曲线④为AsO 3-。A项,②代表HAsO -,亚砷酸的
3 3 2 3 3 3 2 3
,根据 ,解得
,则0.1 mol∙L−1亚砷酸c(H+)约为10−5.15 mol∙L−1,故A正确;B项,等浓度的HAsO 与
3 3
NaOH等体积混合,溶质为NaH AsO ,则 ,根据b点得到
2 3
,因此水解大于电离,溶液中促进了水的电离,故B正确;C项,以酚酞为
指示剂,将NaOH溶液逐滴加入到HAsO 溶液中,当溶液由无色变为浅红色时停止滴加,根据图中信息得到
3 3溶液为NaH AsO ,因此该过程中主要反应的离子方程式为HAsO +OH-=H AsO -+H O,故C错误;D项,根
2 3 3 3 2 3 2
据电荷守恒,b点得到c(HAsO -)+2c(HAsO 2-)+3c(AsO 3--)+c(OH-)=c(H+)+c(Na+),故D正确。故选C。
2 3 3 3
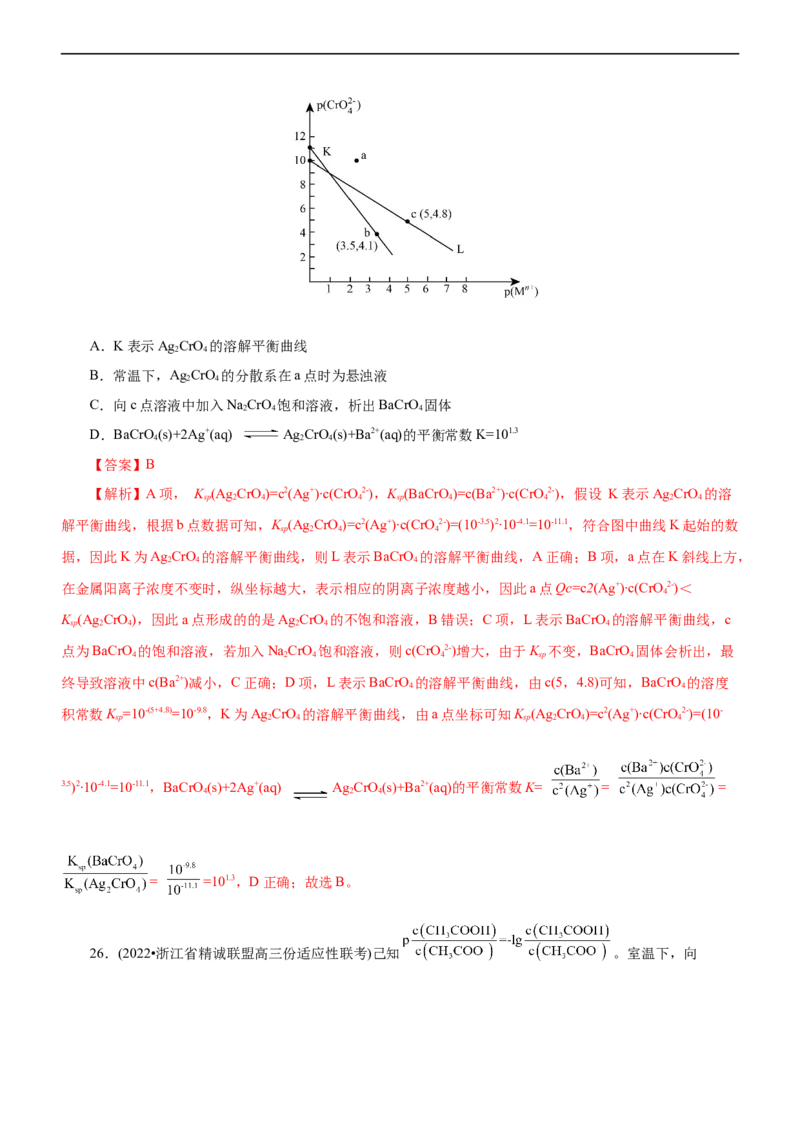
23.(2023·黑龙江省海伦市第一中学高三期中)常温下两种金属氢氧化物的溶解度(纵坐标以溶解金属质量/
表示)与溶液pH的关系如图所示。下列说法正确的是( )
A.
B.X曲线仅最低点说明达到了溶解平衡
C.pH=8时溶度积: Zn(OH) >AgOH
2
D.反应2AgOH+Zn2+ 2Ag++Zn(OH) 的平衡常数
2
【答案】A
【解析】A项,pH=8时,Zn2+浓度为a ,K [Zn(OH) ]= c (Zn2+)• c2(OH-)=
sp 2
,A正确;B项,曲线上所有的点均为溶解平衡状态,B错误;C项,pH为8时,Zn2+的浓度比
Ag+小得多且c(OH-)小于1,则AgOH的溶度积c (Ag+)• c(OH-)比Zn(OH) 的溶度积c (Zn2+)• c2(OH-)大,C错
2
误;D项,2AgOH+Zn2+ 2Ag++Zn(OH) 平衡常数 ,D
2
错误;故选A。
24.(2023·江西省金溪一中高三质检)常温下,向0.1mol/L弱酸HPO 溶液中逐滴加入过量NaOH溶液,得
3 3
到溶液中各含磷元素的微粒占总含磷元素微粒的百分数与pH的关系如图所示,下列说法正确的是( )A.HPO 为三元弱酸
3 3
B.HPO 的电离常数K 的数量级为10-8
3 3 a2
C.当c(HPO 2-)=c(H PO )时,横坐标数值为5.2
3 3 4
D.0.1mol·L-1NaH PO 溶液中,c(H PO -)>c(HPO 2-)>c(H PO )
2 3 2 3 3 3 4
【答案】D
【解析】A项, 由图像可知,溶液中含磷元素的微粒只有三种,故HPO 为二元弱酸,A错误;B项,
3 3
随着pH增大,碱性增强,HPO 的百分数减小,HPO -的百分数先增后减,HPO 2-的百分数逐渐增大,则当
3 3 2 3 3
HPO 2-、HPO -百分数相等即浓度相等时,pH=6.7,则K =10-6.7,数量级为10-7,B错误;C项,由图可知其
3 2 3 a2
K =10-1.5,则 ,则当
a1
c(HPO 2-)=c(H PO )时,c(H+)=1.0×10-4.1mol·L-1,pH=4.1,C错误;D项,HPO -的水解常数为 ,
3 3 4 2 3
小于其电离常数,则c(H PO -)>c(HPO 2-)>c(H PO ),D正确;故选D。
2 3 3 3 4
25.(2023·河北省部分学校高三联考)常温下,难溶物Ag CrO 与BaCrO 在水中的沉淀溶解平衡曲线如图
2 4 4
所示,若定义其坐标图示: , , 表示Ag+或Ba2+。下列说法错误
的是( )A.K表示Ag CrO 的溶解平衡曲线
2 4
B.常温下,Ag CrO 的分散系在a点时为悬浊液
2 4
C.向c点溶液中加入NaCrO 饱和溶液,析出BaCrO 固体
2 4 4
D.BaCrO(s)+2Ag+(aq) Ag CrO(s)+Ba2+(aq)的平衡常数K=101.3
4 2 4
【答案】B
【解析】A项, K (Ag CrO)=c2(Ag+)∙c(CrO2-),K (BaCrO)=c(Ba2+)∙c(CrO2-),假设 K表示Ag CrO 的溶
sp 2 4 4 sp 4 4 2 4
解平衡曲线,根据b点数据可知,K (Ag CrO)=c2(Ag+)∙c(CrO2-)=(10-3.5)2∙10-4.1=10-11.1,符合图中曲线K起始的数
sp 2 4 4
据,因此K为Ag CrO 的溶解平衡曲线,则L表示BaCrO 的溶解平衡曲线,A正确;B项,a点在K斜线上方,
2 4 4
在金属阳离子浓度不变时,纵坐标越大,表示相应的阴离子浓度越小,因此a点Qc=c2(Ag+)∙c(CrO2-)<
4
K (Ag CrO),因此a点形成的的是Ag CrO 的不饱和溶液,B错误;C项,L表示BaCrO 的溶解平衡曲线,c
sp 2 4 2 4 4
点为BaCrO 的饱和溶液,若加入NaCrO 饱和溶液,则c(CrO2-)增大,由于K 不变,BaCrO 固体会析出,最
4 2 4 4 sp 4
终导致溶液中c(Ba2+)减小,C正确;D项,L表示BaCrO 的溶解平衡曲线,由c(5,4.8)可知,BaCrO 的溶度
4 4
积常数K =10-(5+4.8)=10-9.8,K为Ag CrO 的溶解平衡曲线,由a点坐标可知K (Ag CrO)=c2(Ag+)∙c(CrO2-)=(10-
sp 2 4 sp 2 4 4
3.5)2∙10-4.1=10-11.1,BaCrO(s)+2Ag+(aq) Ag CrO(s)+Ba2+(aq)的平衡常数K= = =
4 2 4
= =101.3,D正确;故选B。
26.(2022•浙江省精诚联盟高三份适应性联考)己知 。室温下,向20.00mL0.10mol/LCH COOH溶液中逐滴滴加0.10mol/LNaOH溶液,溶液的pH随着 变化关系
3
如图所示。下列说法不正确的是( )
A.x=2.25
B.水的电离程度:a>b>c
C.当 =0时,加入NaOH溶液的体积小于10.00mL
D.当溶液加入10.00mLNaOH溶液时:c(H+)+2c(CH COOH)+c(CH COO-)=0.1mol/L+c(OH-)
3 3
【答案】BD
【解析】已知 , ,根据图上
,pH=3.75,故 , 。A项,
,pH=7时 ,故A正确B项,
,横坐标越大,则pH值越大,溶液中CHCOO-越大,水电离程度越
3
大,从a到c溶液的pH值逐渐增大,溶液中c(CHCOO-)增大,则水电离程度增大c>b>a,故B错误;C项,
3当 =0时,K=10-4.75,K= <K,说明等物质的量浓度的CHCOOH、CHCOONa
a h a 3 3
溶液中CHCOOH电离程度大于CHCOONa水解程度,如果加入10.00mLNaOH溶液,溶液中溶质为等物质的
3 3
量浓度的CHCOOH、CHCOONa溶液,CHCOOH电离程度大于CHCOO-水解程度,导致溶液中
3 3 3 3
c(CHCOOH)<c(CHCOO-),要使混合溶液中 =0即c(CHCOO-)=c(CH COOH),加入的NaOH
3 3 3 3
应该少一些,即加入NaOH溶液的体积小于10.00mL,故C正确;D项,当加入10.00mLNaOH溶液时,溶液
中溶质为等物质的量浓度的CHCOOH、CHCOONa溶液,溶液中存在电荷守恒c(H+)+c(Na+)=c(OH-)
3 3
+c(CH COO-)、存在物料守恒c(CHCOO-)+c(CH COOH)=2c(Na+),则c(CHCOO-)=2c(Na+)-c(CHCOOH),将
3 3 3 3 3
c(CHCOO-)=2c(Na+)-c(CHCOOH)代入电荷守恒等式得c(H+)+c(CH COOH)=c(Na+)+c(OH-),故D错误。
3 3 3
27.(2022•浙江省丽水市缙云中学等三校高三联考模拟)25℃时,用NaOH调节0.10 mol·L-1 HC O 溶液的
2 2 4
pH,假设不同pH下均有c(HC O)+c(HC O-)+c(C O2-)=0.10 mol·L-1。使用数字传感器测得溶液中各含碳微粒
2 2 4 2 4 2 4
的物质的量浓度随pH的变化如图所示。下列分析不正确的是( )
A.25℃时,HC O 溶液的K =1.0×10-4.2
2 2 4 a2
B.0.10 mol·L-1 HC O 溶液和0.10 mol·L-1NaC O 溶液中c(HC O-)前者大于后者
2 2 4 2 2 4 2 4
C.c(Na+)=0.10 mol·L-1的溶液中,c(H+)+c(HC O)= c(C O2-)+ c(OH―)
2 2 4 2 4
D.25℃时HClO溶液的 ,在足量的0.10 mol·L-1NaClO溶液中滴加少量0.10 mol·L-1HC O
2 2 4
溶液,发生反应2ClO-+ H C O=2HClO+ C O2-
2 2 4 2 4
【答案】D【解析】A项,由图可知:25℃时,HC O 溶液的 ,故A 正确;B项,由
2 2 4
图可知:HC O 溶液的Ka1=10-2.75,, ,NaC O 溶液的水解常数
2 2 4 2 2 4
,电离大于水解,所以 0.10 mol·L-1 HC O 溶液和0.10 mol·L-1 Na C O 溶液中
2 2 4 2 2 4
c(HC O-)前者大于后者,故B正确;C项,因为c(HC O)+c(HC O-)+c(C O2-)=0.10 mol·L-1,所以当溶液中
2 4 2 2 4 2 4 2 4
c(Na+)=0.10 mol·L-1时氢氧化钠和乙二酸恰好反应生成乙二酸氢钠,根据电荷守恒和物料守恒可知c(H+)
+c(HC O)= c(C O2-)+ c(OH―),故C正确;D项,25℃时HClO溶液的K=2.95×10-8,由图可知:HC O 溶液
2 2 4 2 4 a 2 2 4
的Ka1=10-2.75, ,所以酸性HC O>HC O->HClO,在足量的0.10 mol·L-1NaClO
2 2 4 2 4
溶液中滴加少量0.10 mol·L-1 HC O 溶液,发生反应ClO-+ H C O=HClO+ HC O-,故D错误;故选D。
2 2 4 2 2 4 2 4
28.(2022·山东省潍坊市高三学科核心素养测评)Cu2+与NH 可结合生成多种络合物,在水溶液中存在如下
3
平衡: [Cu(NH )]2+ [Cu(NH )]2+ [Cu(NH )]2+ [Cu(NH )]2+ Cu2+。向某浓度的硫酸铜溶液
3 4 3 3 3 2 3
中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数 ( )与溶液中游离氨的lgc(NH)关系如图所示。下列
3
说法错误的是( )
A.曲线b表示[Cu(NH )]2+
3B.
C.1gc(NH )=-4时,c(Cu2+)=c{[Cu(NH )]2+}>Cu(NH )]2+
3 3 3 2
D.M点时,
【答案】B
【解析】由图可知,曲线a在c(NH )最小时,物质的量分布分数最大,说明曲线a表示Cu2+,随着c(NH )
3 3
升高,c(Cu2+)逐渐减小,[Cu(NH )]2+的浓度逐渐增大,故曲线b是[Cu(NH )]2+,继续升高c(NH ),
3 3 3
[Cu(NH )]2+浓度逐渐减小,[Cu(NH )]2+的浓度逐渐增大,则曲线c表示c表示[Cu(NH )]2+,以此类推,曲线d
3 3 2 3 2
表示[Cu(NH )]2+,曲线e表示[Cu(NH )]2+。A项,曲线b表示[Cu(NH )]2+,故A正确;B项,曲线a表示
3 3 3 4 3
Cu2+,曲线b表示[Cu(NH )]2+,曲线c表示[Cu(NH )]2+,曲线d表示[Cu(NH )]2+,曲线e表示[Cu(NH )]2+,K=
3 3 2 3 3 3 4 1
,由图像可知,当c([Cu(NH )]2+)= c([Cu(NH )]2+)时,c(NH )=10-2mol/L,即K=10-2;
3 4 3 3 3 1
K= ,当c([Cu(NH )]2+)= c([Cu(NH )]2+),c(NH )≈10-2.6mol/L,即K=10-2.6;K=
2 3 2 3 3 3 2 4
,当c(Cu2+)=c([Cu(NH)]2+)时,c(NH )=10-4mol/L,即K=10-4; , ,所以
3 3 4
,故B错误;C项,根据图像分析,当1gc(NH )=-4时,c(Cu2+)=c{[Cu(NH )]2+}>Cu(NH )]2+,故C正
3 3 3 2
确;D项,结合以上分析可知,K= , K = ,K=
1 2 3
; = ,把K、K、K 带入上式,M点时,
1 2 3c([Cu(NH )]2+)=c([Cu(NH)]2+),经过化简后可得 =lgc3(NH )=3lgc(NH ),即满足M点时,
3 3 4 3 3
,故D正确;故选B。
29.(2022·山东省潍坊市高三联考)1,3-丙二胺[H N(CH )NH ]类似氨的性质。25°C时,1,3-丙二胺溶液
2 2 3 2
中各含氮微粒的分布系数δ(某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如图所示
(已知:25°C时,K =10-3.5,K =10-5.5)。下列说法不正确的是( )
b1 b2
A.曲线I代表的微粒符号为(H NCH CHNH )2+
3 2 2 3
B.HN(CH )NH 在水溶液中第一步电离的方程式:HN(CH )NH +H O HN(CH )NH ++OH-
2 2 3 2 2 2 3 2 2 2 2 3 3
C.曲线I与曲线II相交点对应pH=5.5
D.0.01mol·L-1HN(CH )NH Cl溶液中各离子浓度关系:c(Cl-)>c[H N(CH )NH +]>c(OH-)>c(H+)
2 2 3 3 2 2 3 3
【答案】C
【解析】A项,曲线I、II、III代表微粒分别为(H NCH CHNH )2+、HN(CH )NH +、HN(CH )NH ,A正
3 2 2 3 2 2 3 3 2 2 3 2
确;B项,HN(CH )NH 在水溶液中和水反应后部分电离且分步电离,其第一步电离生成HN(CH )NH +、
2 2 3 2 2 2 3 3
OH-,所以HN(CH )NH 在水溶液中第一步电离的方程式:HN(CH )NH +H O HN(CH )NH ++OH-,B
2 2 3 2 2 2 3 2 2 2 2 3 3
正确;C项,曲线Ⅰ与曲线Ⅱ交点c[(HNCH CHNH )2+]=c[H N(CH )NH +],则K =
3 2 2 3 2 2 3 3 b2
×c(OH-)=c(OH-)= =10-5.5,c(H+)= =10-8.5,溶液的pH=8.5,C错误;D项,HN(CH )NH +水解平衡常
2 2 3 3
数K= = =10-10.5<K ,说明HN(CH )NH +电离程度大于水解程度导致溶液呈碱性,则c(H+)<c(OH-),
h b2 2 2 3 3但其电离和水解程度都较小,则c(Cl-)>c(HN(CH )NH +),水电离程度较小,所以溶液中存在c(Cl-)>
2 2 3 3
c(HN(CH )NH +)>c(OH-)>c(H+),D正确;故选C。
2 2 3 3
30.(2023·浙江省浙里卷天下高三开学测试)亚磷酸(HPO )是二元弱酸,主要用于农药中间体以及有机磷
3 3
水处理药剂的原料。常温下,向1 mL0.5mol·L-1HPO 溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子
3 3
的物质的量分数 与溶液 的关系如图所示。下列说法正确的是( )
A.a、b两点时,水电离出的c(OH―) 之比为1.43:6.54
水
B.b点对应溶液中存在:c(Na+)=3c(HPO 2- )
3
C.反应HPO + HPO 2- 2HPO -的平衡常数为
3 3 3 2 3
D.当V(NaOH)=1L时,c(Na+)>c(H PO -)>c(OH―)>c(H+)
2 3
【答案】C
【解析】亚磷酸(HPO )是二元弱酸,常温下,向1 mL0.5mol·L-1HPO 溶液中滴加等浓度的NaOH溶液,
3 3 3 3
先后发生的反应为① HPO +OH-= H PO -+H O,②HPO -+OH-= HPO 2-+H O,则HPO 逐渐减少,HPO -先增
3 3 2 3 2 2 3 3 2 3 3 2 3
多后减少,HPO 2-逐渐增多,故 表示HPO 变化曲线, 表示HPO -变化曲线, 表示HPO 2-变化曲线。A
3 3 3 2 3 3
项,a、b两点均为酸性溶液,则水电离出的c(OH―) 分别为10-12.57 mol·L-1、10-7.46 mol·L-1,其之比为1:
水
105.11,A错误;B项,b点时,c(H PO -)=c(HPO 2-),根据电荷守恒可知,c(Na+)+c(H+)=c(OH―)+c(H PO -)
2 3 3 2 3
+2c(HPO 2-)=c(OH―)+3c(HPO 2-),因b点不是中性点,即c(OH―)≠c(H+),则c(Na+)≠3c(HPO 2-),B错误;C项,
3 3 3a点时,c(H PO )=c(H PO -),则反应HPO H++HPO -的平衡常数 ,b
3 3 2 3 3 3 2 3
点时,c(H PO -)=c(HPO 2-),则反应HPO - H++HPO 2-的平衡常数 ,反
2 3 3 2 3 3
应HPO + HPO 2- 2HPO -的平衡常数 ,C正确;D
3 3 3 2 3
项,当V(NaOH)=1L时,HPO 与NaOH反应生成NaH PO ,HPO -水解平衡常数 ,
3 3 2 3 2 3
所以HPO -电离程度大于水解程度,最终溶液呈酸性,则c(Na+)>c(H PO -)>c(H+)>c(OH―),D错误;故选
2 3 2 3
C。
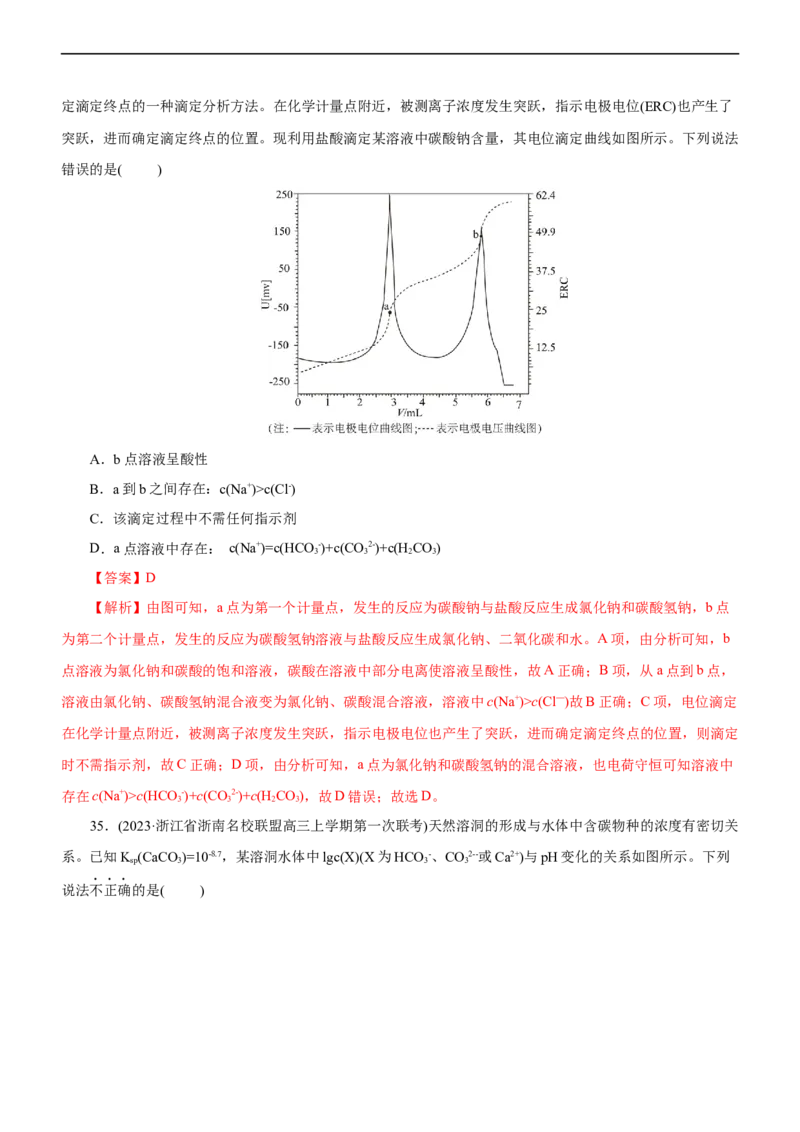
31.(2023届•浙江省舟山市普陀中学高三返校考试)一定温度下,两种钙盐的沉淀溶解平衡曲线如图所示
(M=CO2-、SO 2-,p表示以10为底的负对数)。已知:相同温度下,碳酸钙比硫酸钙更难溶。下列说法错误的
3 4
是( )
A.该温度下,K (CaCO)=10-8
sp 3
B.欲使反应CaSO+ CO2- CaCO + SO 2-正向进行,需满足
4 3 3 4
C.欲使c点移动到b点,可向c点的饱和溶液中加入适量CaCl 固体
2D.生活中,用饱和碳酸钠溶液浸泡硫酸钙后的滤液中一定存在
【答案】B
【解析】相同温度下,CaCO 比CaSO 更难溶,则X曲线代表CaSO 的沉淀溶解平衡曲线,Y曲线代表
3 4 4
CaCO 的沉淀溶解平衡曲线;由X曲线可得K (CaSO)=10-5,由Y曲线可得K (CaCO)=10-8。A项,该温度下
3 sp 4 sp 3
K (CaCO)=10-8,A项正确;B项,反应CaSO+ CO2- CaCO + SO 2-的平衡常数K= =
sp 3 4 3 3 4
= = =103,欲使反应CaSO+ CO2- CaCO + SO 2-正向进行,需满足
4 3 3 4
<103,B项错误;C项,c点存在的沉淀溶解平衡为CaCO (s) Ca2+(aq)+ CO2- (aq),向c点的饱
3 3
和溶液中加入适量CaCl 固体,Ca2+浓度增大,平衡逆向移动,CO2-浓度减小,K (CaCO)不变,可使c点移动
2 3 sp 3
到b点,C项正确;D项,生活中用饱和碳酸钠溶液浸泡硫酸钙可发生沉淀的转化生成CaCO ,滤液中为
3
CaCO 的饱和溶液,一定存在 ,D项正确;故选B。
3
32.(2023•浙江省舟山市舟山中学高三开学考试)25℃时,往20. 00mL 0. 1mol·L-1HX溶液中滴入0.
1mol·L-1NaOH溶液,体系中-1gc(HX)、 -lgc(X-)、 NaOH 溶液的体积与溶液pH的关系如图所示。下列说法正
确的是( )A.曲线②表示-lgc(HX)与溶液pH的关系
B.a点对应的溶液中: c(H+) +2c(HX)=c(OH- )-c(X -)
C.b点对应的溶液中: c(Na+)>c(X- )>c(OH-)>c(H+)
D.25℃时,HX的电离平衡常数的数量级为10-4
【答案】C
【解析】A项,往20.00mL 0.1mol·L−1 HX溶液中滴入0.1mol·L−1 NaOH溶液,发生反应:
NaOH+HX=NaX+H O,体系中−lgc(HX)随溶液pH的增大而增大,−lgc(X−) 随溶液pH的增大而减小,故曲线
2
①表示−lgc(HX)与溶液pH的关系,A错误;B项,a点对应的溶液中存在HX和NaX两种溶质,且二者的物
质的量之比为1∶1,该溶液中的电荷守恒式为c(Na+)+c(H+)=c(X−)+c(OH−),物料守恒式为2c(Na+)=c(X−)
+c(HX),联立电荷守恒式及物料守恒式可得:2c(H+)+c(HX)=2c(OH−)+c(X−),B错误;C项,b点对应的溶液
pH=10即c(OH−)>c(H+),此时溶液中的溶质为NaX和NaOH,结合电荷守恒式可得溶液中:c(Na+)>c(X−),故
c(Na+)>c(X−)>c(OH−)>c(H+),C正确;D项,曲线①、曲线②的交点处有−lgc(HX) =−lgc(X−),即c(HX)=
c(X−),HX的电离平衡常数K=c(H+)=10−4.76,其数量级为10−5,D错误;故选C。
a
33.(2023·浙江省浙里卷天下高三月联考)以酚酞为指示剂,用 的NaOH溶液滴定20.00mL
未知浓度的二元酸 溶液。溶液中,pH、分布系数 随滴加NaOH溶液体积 的变化关系如图所示。
[比如A2-的分布系数: ]下列叙述正确的是( )
A.HA第一步电离方程式为HA H++HA-,曲线②代表
2 2
B.加入20.00mLNaOH溶液显酸性的原因是HA-能水解,且水解能力明显小于HA-电离
C.滴定终点时,溶液中c(Na+)<c(HA-)+2c(A2-)
D.HA-的电离常数
【答案】D
【解析】根据题干分布系数的表达式,分母中c(H A)+c(HA-)+c(A2-)为定值,即分布系数大小与离子浓度
2
成正比;图中曲线①与曲线②表示的是分布系数 随NaOH溶液体积的变化关系,曲线③表示的是pH随
NaOH溶液体积的变化关系;二元酸HA在水溶液中第一步电离生成HA-,第二步电离生成A2-,再结合分布
2
曲线①一直下降,而曲线②一直升高可知,曲线①表示的是HA-的分布系数,曲线②表示的是A2-的分布系数,
且曲线②达到的最大值接近1,说明HA的第一步电离为完全电离。A项,据分析可知,HA第一步电离方程
2 2
式为HA=H++HA-,曲线①代表 ,A错误;B项,HA的第一步电离为完全电离,则HA-不能水解,
2 2
加入20.00mLNaOH溶液显酸性的原因是HA-电离产生氢离子,B错误;C项,当反应达到终点时,存在电荷
守恒c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),由于溶液显碱性,c(H+)<c(OH-),所以c(Na+)>c(HA-)+2c(A2-),C错
误;D项,由于HA的第一步电离为完全电离,根据图像,当V =0时,溶液pH=1,HA-的起始浓度为
2 NaOH
0.1000mol/L,HA-分布系数为0.9,A2-的分布系数为0.1,则HA-的电离常数
,D正确;故选D。
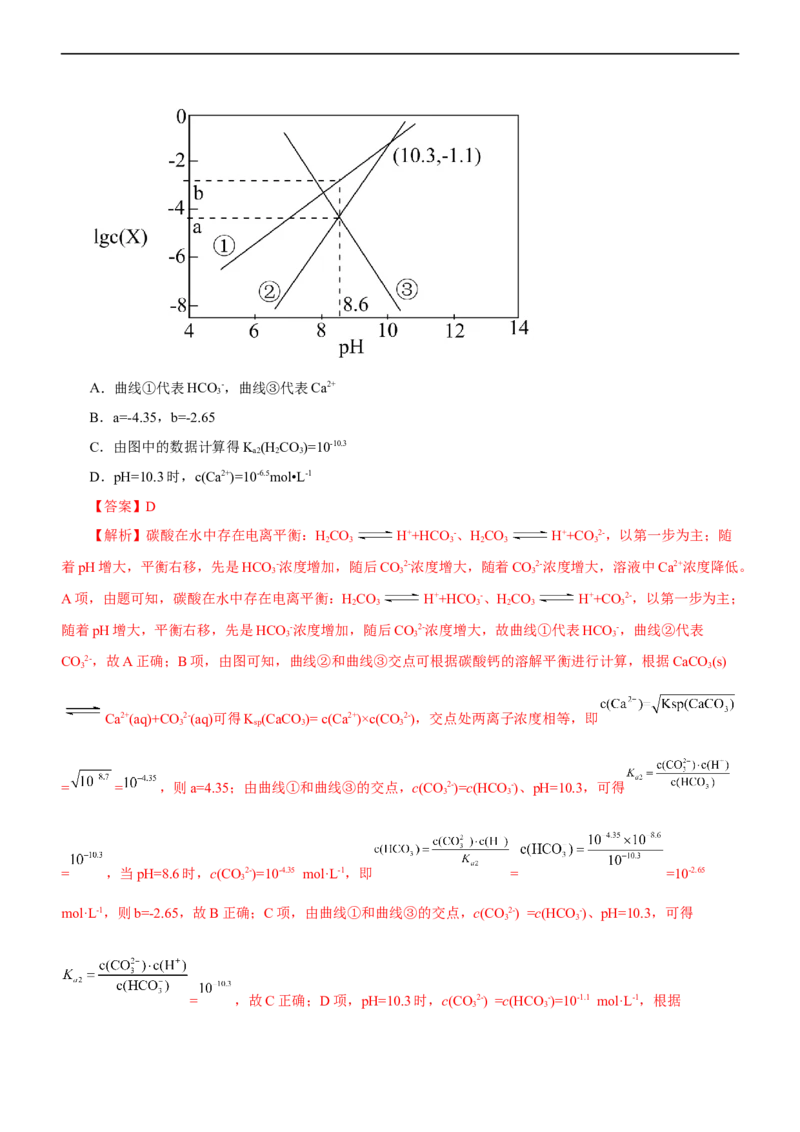
34.(2023·浙江省强基联盟高三上学期10月统测)电位滴定法是根据滴定过程中指示电极电位的变化来确定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极电位(ERC)也产生了
突跃,进而确定滴定终点的位置。现利用盐酸滴定某溶液中碳酸钠含量,其电位滴定曲线如图所示。下列说法
错误的是( )
A.b点溶液呈酸性
B.a到b之间存在:c(Na+)>c(Cl-)
C.该滴定过程中不需任何指示剂
D.a点溶液中存在: c(Na+)=c(HCO-)+c(CO 2-)+c(H CO)
3 3 2 3
【答案】D
【解析】由图可知,a点为第一个计量点,发生的反应为碳酸钠与盐酸反应生成氯化钠和碳酸氢钠,b点
为第二个计量点,发生的反应为碳酸氢钠溶液与盐酸反应生成氯化钠、二氧化碳和水。A项,由分析可知,b
点溶液为氯化钠和碳酸的饱和溶液,碳酸在溶液中部分电离使溶液呈酸性,故A正确;B项,从a点到b点,
溶液由氯化钠、碳酸氢钠混合液变为氯化钠、碳酸混合溶液,溶液中c(Na+)>c(Cl—)故B正确;C项,电位滴定
在化学计量点附近,被测离子浓度发生突跃,指示电极电位也产生了突跃,进而确定滴定终点的位置,则滴定
时不需指示剂,故C正确;D项,由分析可知,a点为氯化钠和碳酸氢钠的混合溶液,也电荷守恒可知溶液中
存在c(Na+)>c(HCO -)+c(CO2-)+c(H CO),故D错误;故选D。
3 3 2 3
35.(2023·浙江省浙南名校联盟高三上学期第一次联考)天然溶洞的形成与水体中含碳物种的浓度有密切关
系。已知K (CaCO)=10-8.7,某溶洞水体中lgc(X)(X为HCO -、CO2--或Ca2+)与pH变化的关系如图所示。下列
sp 3 3 3
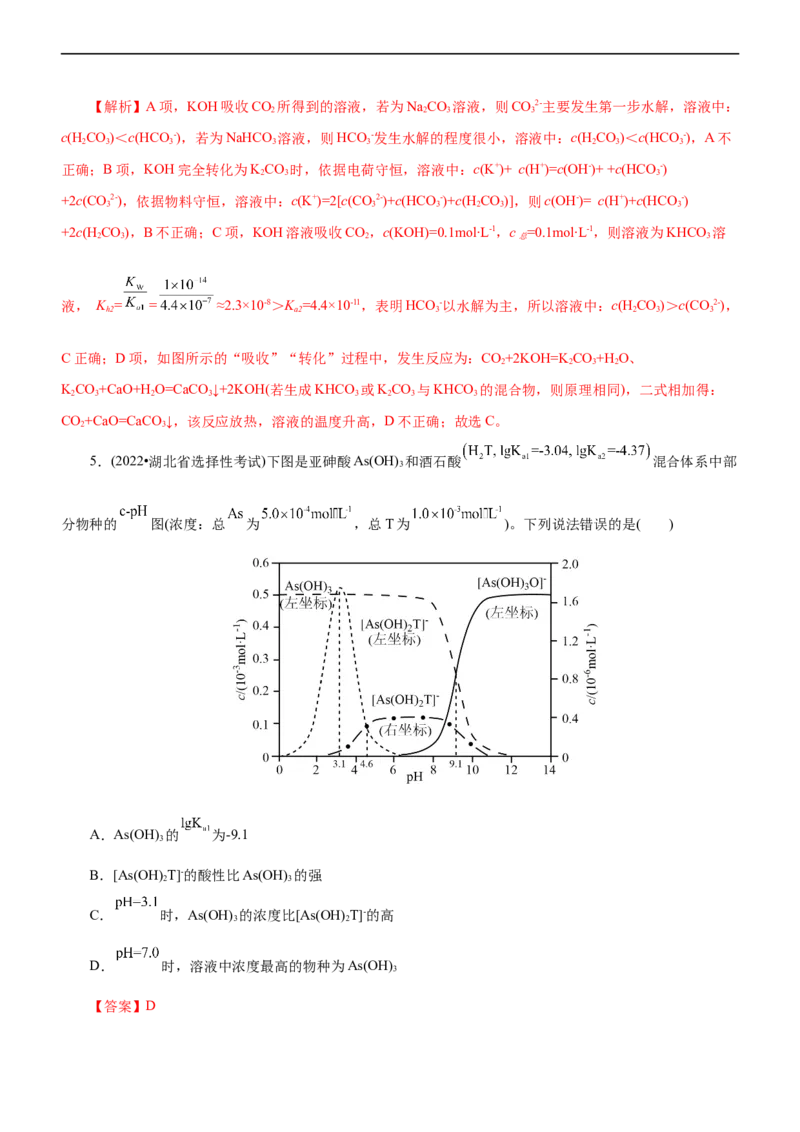
说法不正确的是( )A.曲线①代表HCO -,曲线③代表Ca2+
3
B.a=-4.35,b=-2.65
C.由图中的数据计算得K (H CO)=10-10.3
a2 2 3
D.pH=10.3时,c(Ca2+)=10-6.5mol•L-1
【答案】D
【解析】碳酸在水中存在电离平衡:HCO H++HCO-、HCO H++CO 2-,以第一步为主;随
2 3 3 2 3 3
着pH增大,平衡右移,先是HCO -浓度增加,随后CO2-浓度增大,随着CO2-浓度增大,溶液中Ca2+浓度降低。
3 3 3
A项,由题可知,碳酸在水中存在电离平衡:HCO H++HCO-、HCO H++CO 2-,以第一步为主;
2 3 3 2 3 3
随着pH增大,平衡右移,先是HCO -浓度增加,随后CO2-浓度增大,故曲线①代表HCO -,曲线②代表
3 3 3
CO2-,故A正确;B项,由图可知,曲线②和曲线③交点可根据碳酸钙的溶解平衡进行计算,根据CaCO (s)
3 3
Ca2+(aq)+CO2-(aq)可得K (CaCO)= c(Ca2+)×c(CO2-),交点处两离子浓度相等,即
3 sp 3 3
= = ,则a=4.35;由曲线①和曲线③的交点,c(CO2-)=c(HCO -)、pH=10.3,可得
3 3
= ,当pH=8.6时,c(CO2-)=10-4.35 mol·L-1,即 = =10-2.65
3
mol·L-1,则b=-2.65,故B正确;C项,由曲线①和曲线③的交点,c(CO2-) =c(HCO -)、pH=10.3,可得
3 3
= ,故C正确;D项,pH=10.3时,c(CO2-) =c(HCO -)=10-1.1 mol·L-1,根据
3 3K (CaCO)= c(Ca2+)×c(CO2-),可得 = =10-7.6 mol/L,故D错误;故选D。
sp 3 3
1.(2022•湖北省选择性考试)根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性
越强。已知:NH++NH=NH++N H,NH+CH COOH=N H++CH COO-,下列酸性强弱顺序正确的是( )
2 5 3 4 2 4 2 4 3 2 5 3
A.NH+>NH>NH + B.NH+>CHCOOH>NH +
2 5 2 4 4 2 5 3 4
C.NH >NH>CHCOO- D.CHCOOH>NH+>NH +
3 2 4 3 3 2 5 4
【答案】D
【解析】根据复分解反应的规律,强酸能制得弱酸,根据酸碱质子理论,给出质子(H+)的物质是酸,则反
应NH+CH COOH=N H++CH COO-中,酸性:CHCOOH>NH+,反应NH++NH=NH++N H 中,酸性:
2 4 3 2 5 3 3 2 5 2 5 3 4 2 4
NH+>NH +,故酸性:CHCOOH>NH+>NH +,故选D。
2 5 4 3 2 5 4
2.(2022•海南省选择性考试)NaClO溶液具有漂白能力,已知25℃时,K=(HClO)=4.0×10-8。下列关于
a
NaClO溶液说法正确的是( )
A.0.01mol/L溶液中,c(ClO-)<0.01mol/L
B.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO -+HClO
2 2 2 3
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
【答案】AD
【解析】A项,NaClO溶液中ClO-会水解,故0.01mol/L NaClO溶液中c(ClO-)<0.01mol/L,A正确;B项,
次氯酸钠溶液中的ClO-会发生水解生成HClO,HClO长期露置在空气中会分解,为HCl和O,不会释放Cl,
2 2
B错误;C项,将过量的SO 通入NaClO溶液中,SO 被氧化:SO +ClO−+H O=Cl-+SO2-+2H+,C错误;D项,
2 2 2 2 4
25℃,pH=7.0的NaClO和HClO的混合溶液中,存在电荷守恒:c(ClO-)+c(OH-)=c(H+)+c(Na+),则
c(ClO-)=c(Na+),又c(HClO)>c(ClO-),所以c(HClO)>c(ClO-)=c(Na+),D正确;故选AD。
3.(2022·浙江省6月选考) 时,向 浓度均为0.1mol·L-1的盐酸和醋酸的混合溶液中逐滴加入
0.1mol·L-1的NaOH溶液(醋酸的K=1.8×10-5;用0.1mol·L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点
a
的 突跃范围4.3~9.7)。下列说法不正确的是( )
A.恰好中和时,溶液呈碱性
B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H O
2C.滴定过程中,c(Cl-)=c(CH COO-)+c(CH COOH)
3 3
D. 时,c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH)
3 3
【答案】B
【解析】A项,恰好中和时,生成氯化钠溶液和醋酸钠溶液,其中醋酸根离子会水解,溶液显碱性,A正
确;B项,滴加NaOH溶液至pH=4.3的过程中,若只发生反应的离子方程式:H++OH-=H O,则滴加NaOH溶
2
液的体积为20mL,则根据电离常数,0.1mol·L-1的醋酸中,c(H+)≈c(CH COO-)= =
3
= >1.0×10-4.3,故用氢氧化钠滴定的过程中,醋酸也参加了反应,则离子方程式
为:H++OH-=H O和CHCOOH+OH-=CH COO-+H O,B错误;C项,滴定前盐酸和醋酸的浓度相同,故滴定
2 3 3 2
过程中,根据物料守恒可知:c(Cl-)=c(CH COO-)+c(CH COOH),C正确;D项,向20mL浓度均为0.1mol·L-1
3 3
的盐酸和醋酸的混合溶液中逐滴加入0.1mol·L-1的NaOH溶液,当盐酸的体积为20ml时,溶液为氯化钠和醋
酸的混合溶液,显酸性,需要再滴加适量的氢氧化钠,当加入的NaOH溶液的体积为30mL时,溶液为NaCl
和等浓度的CHCOONa、CHCOOH,根据Ka=1.8×10-5>Kh= 可知,此时溶液仍然呈酸性,需
3 3
继续滴加NaOH溶液,故有c(Na+)>c(Cl-)>c(CHCOO-)>c(CHCOOH),D正确;故选B。
3 3
4.(2022•江苏卷)一种捕集烟气中CO 的过程如图所示。室温下以0.1mol∙L-1KOH溶液吸收CO,若通入
2 2
CO 所引起的溶液体积变化和HO挥发可忽略,溶液中含碳物种的浓度c =c(H CO)+c(HCO - )+c(CO2-)。
2 2 总 2 3 3 3
HCO 电离常数分别为K =4.4×10-7、K =4.4×10-11。下列说法正确的是( )
2 3 a1 a2
A.KOH吸收CO 所得到的溶液中:c(H CO)>c(HCO -)
2 2 3 3
B.KOH完全转化为KCO 时,溶液中:c(OH-)= c(H+)+c(HCO -)+c(H CO)
2 3 3 2 3
C.KOH溶液吸收CO,c =0.1mol∙L-1溶液中:c(H CO)>c(CO2-)
2 总 2 3 3
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
【答案】C【解析】A项,KOH吸收CO 所得到的溶液,若为NaCO 溶液,则CO2-主要发生第一步水解,溶液中:
2 2 3 3
c(H CO)<c(HCO -),若为NaHCO 溶液,则HCO -发生水解的程度很小,溶液中:c(H CO)<c(HCO -),A不
2 3 3 3 3 2 3 3
正确;B项,KOH完全转化为KCO 时,依据电荷守恒,溶液中:c(K+)+ c(H+)=c(OH-)+ +c(HCO -)
2 3 3
+2c(CO2-),依据物料守恒,溶液中:c(K+)=2[c(CO2-)+c(HCO -)+c(H CO)],则c(OH-)= c(H+)+c(HCO -)
3 3 3 2 3 3
+2c(H CO),B不正确;C项,KOH溶液吸收CO,c(KOH)=0.1mol∙L-1,c =0.1mol∙L-1,则溶液为KHCO 溶
2 3 2 总 3
液, K = = ≈2.3×10-8>K =4.4×10-11,表明HCO -以水解为主,所以溶液中:c(H CO)>c(CO2-),
h2 a2 3 2 3 3
C正确;D项,如图所示的“吸收”“转化”过程中,发生反应为:CO+2KOH=K CO+H O、
2 2 3 2
KCO+CaO+H O=CaCO ↓+2KOH(若生成KHCO 或KCO 与KHCO 的混合物,则原理相同),二式相加得:
2 3 2 3 3 2 3 3
CO+CaO=CaCO ↓,该反应放热,溶液的温度升高,D不正确;故选C。
2 3
5.(2022•湖北省选择性考试)下图是亚砷酸As(OH) 和酒石酸 混合体系中部
3
分物种的 图(浓度:总 为 ,总T为 )。下列说法错误的是( )
A.As(OH) 的 为-9.1
3
B.[As(OH) T]-的酸性比As(OH) 的强
2 3
C. 时,As(OH) 的浓度比[As(OH) T]-的高
3 2
D. 时,溶液中浓度最高的物种为As(OH)
3
【答案】D【解析】由图分析,左侧纵坐标浓度的数量级为10-3mol/L,右坐标浓度的数量级为10-6mol/L,横坐标为
pH,随着pH的增大, 先变大,然后再减小,同时 变大,两者浓度均为右坐
标,说明变化的程度很小,当pH=4.6时, = ,Ka=10-4.6。pH继续增大,则
减小,同时 增大,当pH=9.1时, = ,
,二者用左坐标表示,浓度比较大,说明变化的幅度比较大,但混合溶液中存在着酒石酸,
电离常数远大于亚砷酸,且总T浓度也大于总As。A项, ,
,当pH=9.1时, = , ,
为-9.1,A正确;B项,[As(OH) T]- [As(OH)T]2-+H+ ,当pH=4.6时,
2
= ,Ka=10-4.6,而由A选项计算得HAsO 的 ,即Ka >
3 3
Ka1,所以[As(OH) T]-的酸性比As(OH) 的强,B正确;C项,由图可知As(OH) 的浓度为左坐标,浓度的数量
2 3 3
级为10-3mol/L,[As(OH) T]-的浓度为右坐标,浓度的数量级为10-6mol/L,所以pH=3.0时,As(OH) 的浓度比
2 3
[As(OH) T]-的高,C正确;D项,由可知条件,酒石酸 ,As(OH) 的
2 3
为-9.1,即酒石酸的第一部电离常数远大于亚砷酸的第一步电离常数,所以酒石酸的酸性远强于As(OH) ,另
3
外总As的浓度也小于总T的浓度,所以当pH=7.0时,溶液中浓度最高的物种不是As(OH) ,D错误;故选
3
D。
6.(2022•辽宁省选择性考试)甘氨酸(NH CHCOOH)是人体必需氨基酸之一、在 时,NH +CHCOOH、
2 2 3 2
NH +CHCOO-和NH CHCOO-的分布分数【如 】与溶液 关系如图。下列说
3 2 2 2法错误的是( )
A.甘氨酸具有两性
B.曲线c代表NH CHCOO-
2 2
C.NH +CHCOO-+H O NH +CHCOOH+OH-的平衡常数K=10-11.65
3 2 2 3 2
D.c 2(NH +CHCOO-)<c(NH +CHCOOH) · c(NH2CHCOO-)
3 2 3 2 2
【答案】D
【解析】A项,NH CHCOOH中存在-NH 和-COOH,所以溶液既有酸性又有碱性,故A正确;B项,氨
2 2 2
基具有碱性,在酸性较强时会结合氢离子,羧基具有酸性,在碱性较强时与氢氧根离子反应,故曲线a表示
NH +CHCOOH的分布分数随溶液pH的变化,曲b表示NH +CHCOO-的分布分数随溶液pH的变化,曲线c表
3 2 3 2
示NH CHCOO-的分布分数随溶液pH的变化,故B正确;C项,NH +CHCOO-+H O
2 2 3 2 2
NH +CHCOOH+OH-的平衡常数 , 时,根据a,b曲线交点坐标(2.35,0.50)
3 2
可知,pH=2.35时,c(NH +CHCOO-)=c(NH +CHCOOH),则 ,故C正确;D项,由
3 2 3 2
C项分析可知, ,根据b,c曲线交点坐标坐标(9.78,0.50)分析可得电离平衡
NH +CHCOO- NH CHCOO-+H+的电离常数为K=10-9.78, ,则
3 2 2 2 1,即c 2(NH +CHCOO-)>c(NH +CHCOOH) ·
3 2 3 2
c(NH CHCOO-),故D错误;故选D。
2 2
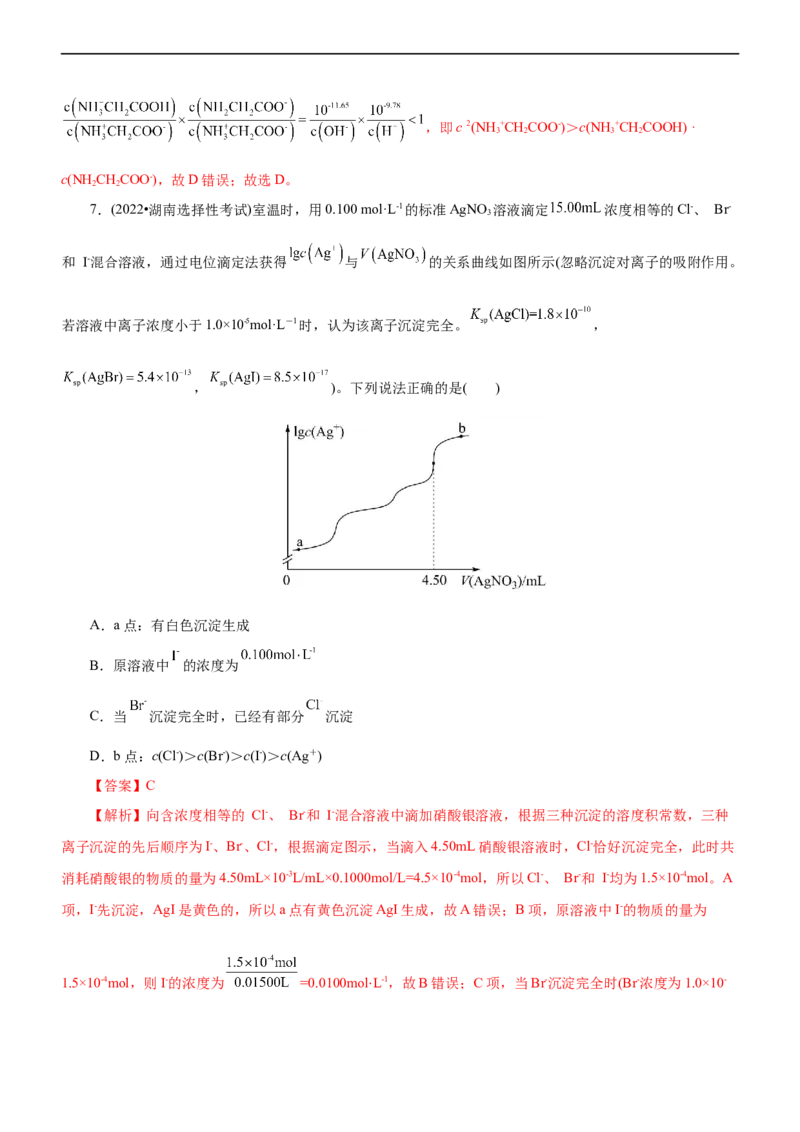
7.(2022•湖南选择性考试)室温时,用0.100 mol·L-1的标准AgNO 溶液滴定 浓度相等的Cl-、 Br-
3
和 I-混合溶液,通过电位滴定法获得 与 的关系曲线如图所示(忽略沉淀对离子的吸附作用。
若溶液中离子浓度小于1.0×10-5mol·L-1时,认为该离子沉淀完全。 ,
, )。下列说法正确的是( )
A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:c(Cl-)>c(Br-)>c(I-)>c(Ag+)
【答案】C
【解析】向含浓度相等的 Cl-、 Br-和 I-混合溶液中滴加硝酸银溶液,根据三种沉淀的溶度积常数,三种
离子沉淀的先后顺序为I-、Br-、Cl-,根据滴定图示,当滴入4.50mL硝酸银溶液时,Cl-恰好沉淀完全,此时共
消耗硝酸银的物质的量为4.50mL×10-3L/mL×0.1000mol/L=4.5×10-4mol,所以Cl-、 Br-和 I-均为1.5×10-4mol。A
项,I-先沉淀,AgI是黄色的,所以a点有黄色沉淀AgI生成,故A错误;B项,原溶液中I-的物质的量为
1.5×10-4mol,则I-的浓度为 =0.0100molL-1,故B错误;C项,当Br-沉淀完全时(Br-浓度为1.0×10-
⋅5mol/L),溶液中的c(Ag+)= =5.4×10-8mol/L,若Cl-已经开始沉淀,则此时溶液中的c(Cl-)=
=3.3×10-3mol/L,原溶液中的c(Cl-)= c(I-)=0.0100molL-1,则已经有部分Cl-沉淀,故C正
⋅
确;D项,b点加入了过量的硝酸银溶液,Ag+浓度最大,则b点各离子浓度为: c(Ag+) >c(Cl-)>c(Br-)>
c(I-)>,故D错误;故选C。
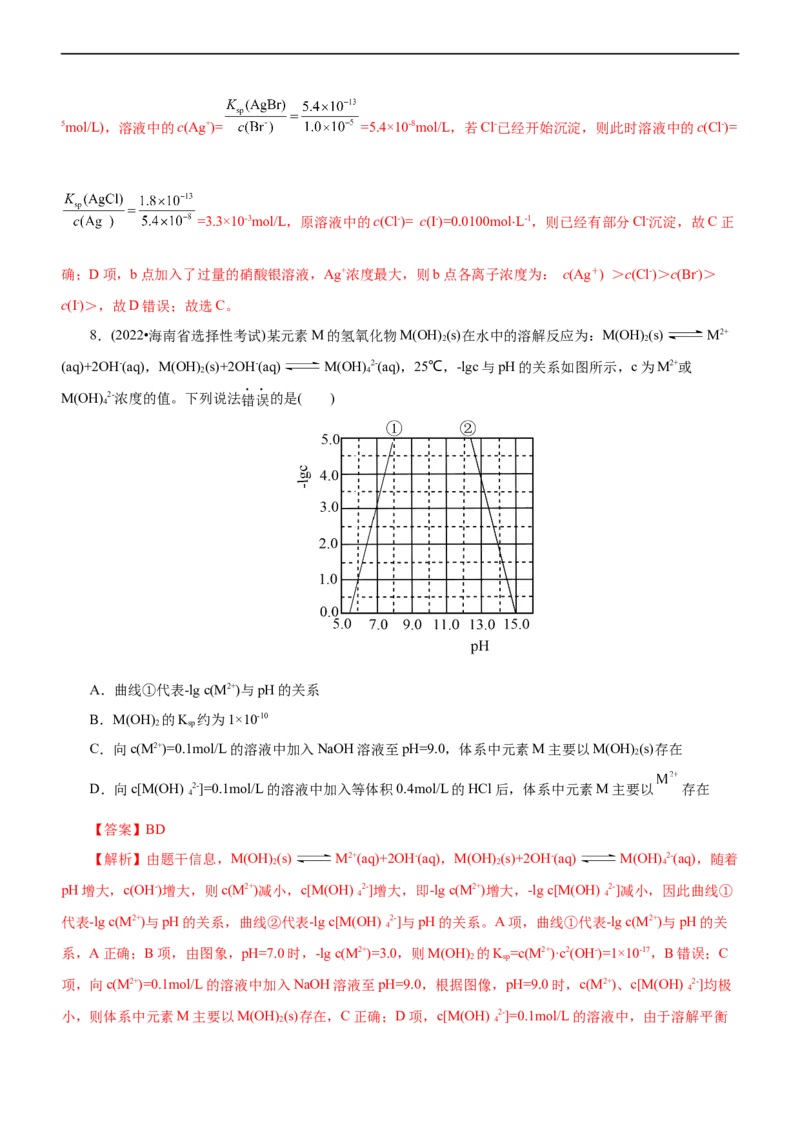
8.(2022•海南省选择性考试)某元素M的氢氧化物M(OH) (s)在水中的溶解反应为:M(OH) (s) M2+
2 2
(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) 2-(aq),25℃,-lgc与pH的关系如图所示,c为M2+或
2 4
M(OH) 2-浓度的值。下列说法错误的是( )
4
A.曲线①代表-lg c(M2+)与pH的关系
B.M(OH) 的K 约为1×10-10
2 sp
C.向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以M(OH) (s)存在
2
D.向c[M(OH) 2-]=0.1mol/L的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 存在
4
【答案】BD
【解析】由题干信息,M(OH) (s) M2+(aq)+2OH-(aq),M(OH) (s)+2OH-(aq) M(OH) 2-(aq),随着
2 2 4
pH增大,c(OH-)增大,则c(M2+)减小,c[M(OH) 2-]增大,即-lg c(M2+)增大,-lg c[M(OH) 2-]减小,因此曲线①
4 4
代表-lg c(M2+)与pH的关系,曲线②代表-lg c[M(OH) 2-]与pH的关系。A项,曲线①代表-lg c(M2+)与pH的关
4
系,A正确;B项,由图象,pH=7.0时,-lg c(M2+)=3.0,则M(OH) 的K =c(M2+)·c2(OH-)=1×10-17,B错误;C
2 sp
项,向c(M2+)=0.1mol/L的溶液中加入NaOH溶液至pH=9.0,根据图像,pH=9.0时,c(M2+)、c[M(OH) 2-]均极
4
小,则体系中元素M主要以M(OH) (s)存在,C正确;D项,c[M(OH) 2-]=0.1mol/L的溶液中,由于溶解平衡
2 4是少量的,因此加入等体积的0.4mol/L的HCl后,体系中元素M仍主要以M(OH) 2-存在,D错误;故选BD。
4
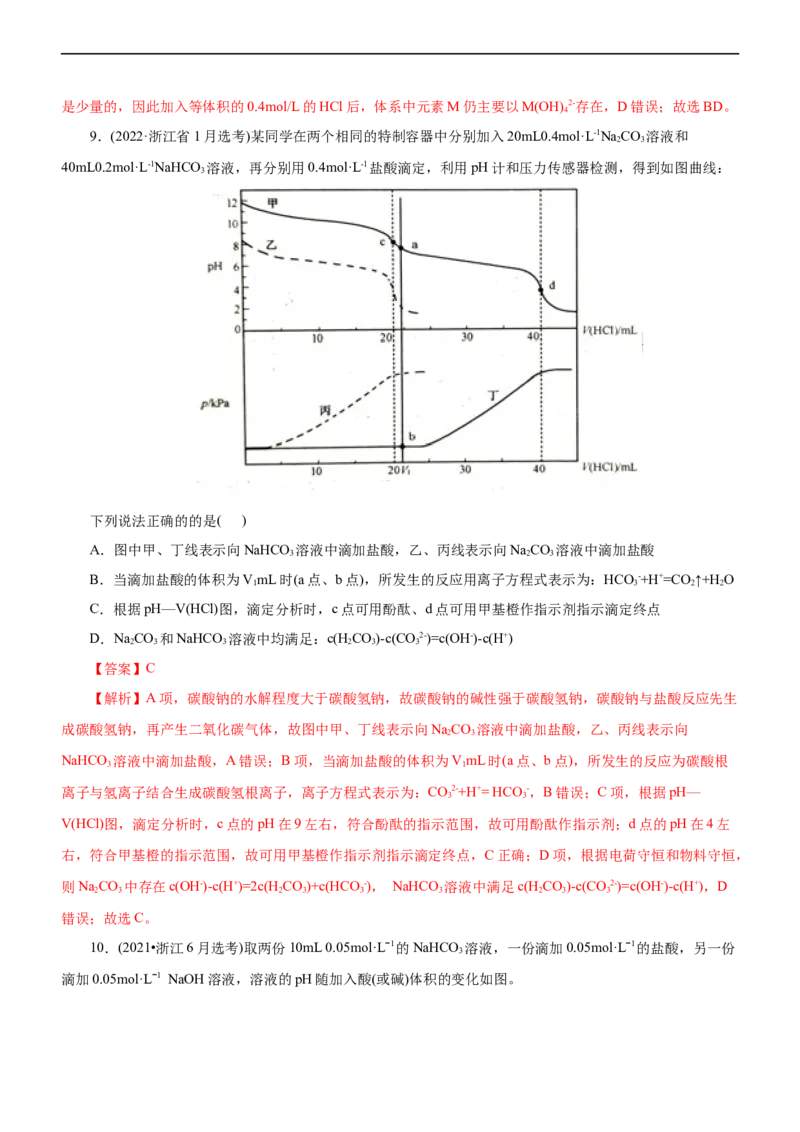
9.(2022·浙江省1月选考)某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1NaCO 溶液和
2 3
40mL0.2mol·L-1NaHCO 溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
3
下列说法正确的的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐酸
3 2 3
B.当滴加盐酸的体积为VmL时(a点、b点),所发生的反应用离子方程式表示为:HCO -+H+=CO ↑+H O
1 3 2 2
C.根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点
D.NaCO 和NaHCO 溶液中均满足:c(HCO)-c(CO2-)=c(OH-)-c(H+)
2 3 3 2 3 3
【答案】C
【解析】A项,碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,碳酸钠与盐酸反应先生
成碳酸氢钠,再产生二氧化碳气体,故图中甲、丁线表示向NaCO 溶液中滴加盐酸,乙、丙线表示向
2 3
NaHCO 溶液中滴加盐酸,A错误;B项,当滴加盐酸的体积为VmL时(a点、b点),所发生的反应为碳酸根
3 1
离子与氢离子结合生成碳酸氢根离子,离子方程式表示为:CO2-+H+= HCO -,B错误;C项,根据pH—
3 3
V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,故可用酚酞作指示剂;d点的pH在4左
右,符合甲基橙的指示范围,故可用甲基橙作指示剂指示滴定终点,C正确;D项,根据电荷守恒和物料守恒,
则NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO-), NaHCO 溶液中满足c(HCO)-c(CO2-)=c(OH-)-c(H+),D
2 3 2 3 3 3 2 3 3
错误;故选C。
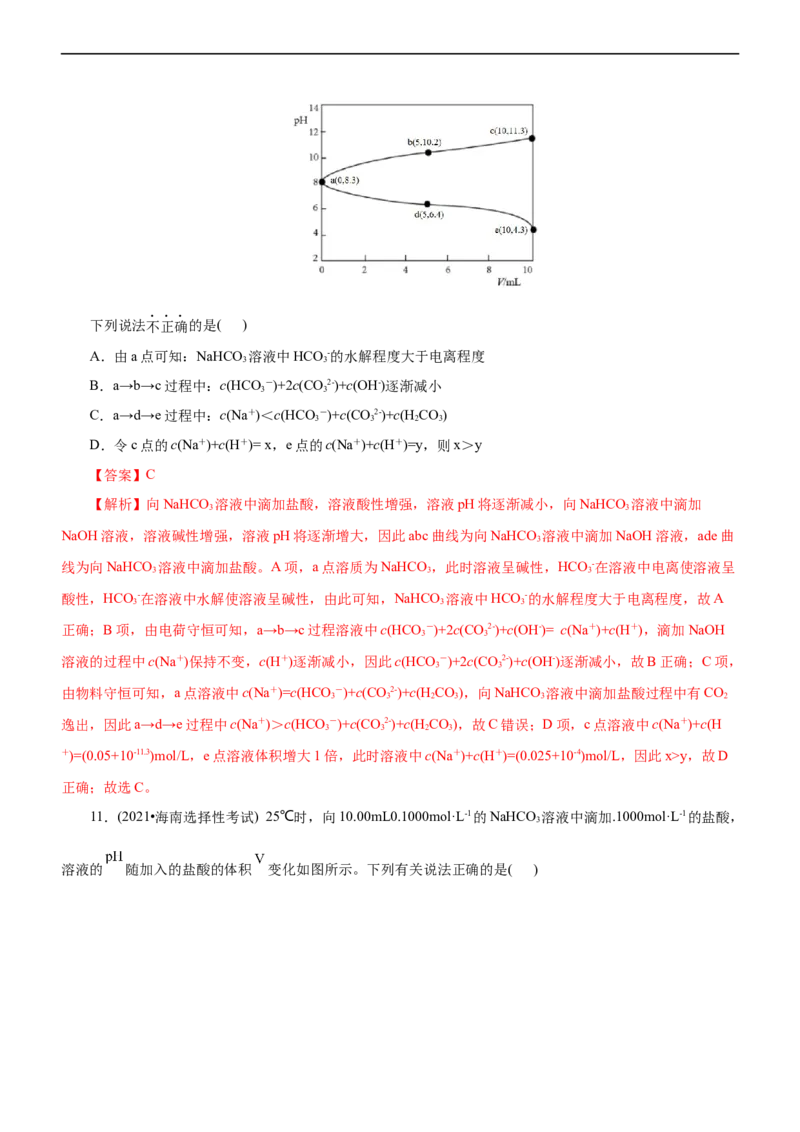
10.(2021•浙江6月选考)取两份10mL 0.05mol·Lˉ1的NaHCO 溶液,一份滴加0.05mol·Lˉ1的盐酸,另一份
3
滴加0.05mol·Lˉ1 NaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图。下列说法不正确的是( )
A.由a点可知:NaHCO 溶液中HCO -的水解程度大于电离程度
3 3
B.a→b→c过程中:c(HCO -)+2c(CO2-)+c(OH-)逐渐减小
3 3
C.a→d→e过程中:c(Na+)<c(HCO -)+c(CO2-)+c(H CO)
3 3 2 3
D.令c点的c(Na+)+c(H+)= x,e点的c(Na+)+c(H+)=y,则x>y
【答案】C
【解析】向NaHCO 溶液中滴加盐酸,溶液酸性增强,溶液pH将逐渐减小,向NaHCO 溶液中滴加
3 3
NaOH溶液,溶液碱性增强,溶液pH将逐渐增大,因此abc曲线为向NaHCO 溶液中滴加NaOH溶液,ade曲
3
线为向NaHCO 溶液中滴加盐酸。A项,a点溶质为NaHCO ,此时溶液呈碱性,HCO -在溶液中电离使溶液呈
3 3 3
酸性,HCO -在溶液中水解使溶液呈碱性,由此可知,NaHCO 溶液中HCO -的水解程度大于电离程度,故A
3 3 3
正确;B项,由电荷守恒可知,a→b→c过程溶液中c(HCO -)+2c(CO2-)+c(OH-)= c(Na+)+c(H+),滴加NaOH
3 3
溶液的过程中c(Na+)保持不变,c(H+)逐渐减小,因此c(HCO -)+2c(CO2-)+c(OH-)逐渐减小,故B正确;C项,
3 3
由物料守恒可知,a点溶液中c(Na+)=c(HCO -)+c(CO2-)+c(H CO),向NaHCO 溶液中滴加盐酸过程中有CO
3 3 2 3 3 2
逸出,因此a→d→e过程中c(Na+)>c(HCO -)+c(CO2-)+c(H CO),故C错误;D项,c点溶液中c(Na+)+c(H
3 3 2 3
+)=(0.05+10-11.3)mol/L,e点溶液体积增大1倍,此时溶液中c(Na+)+c(H+)=(0.025+10-4)mol/L,因此x>y,故D
正确;故选C。
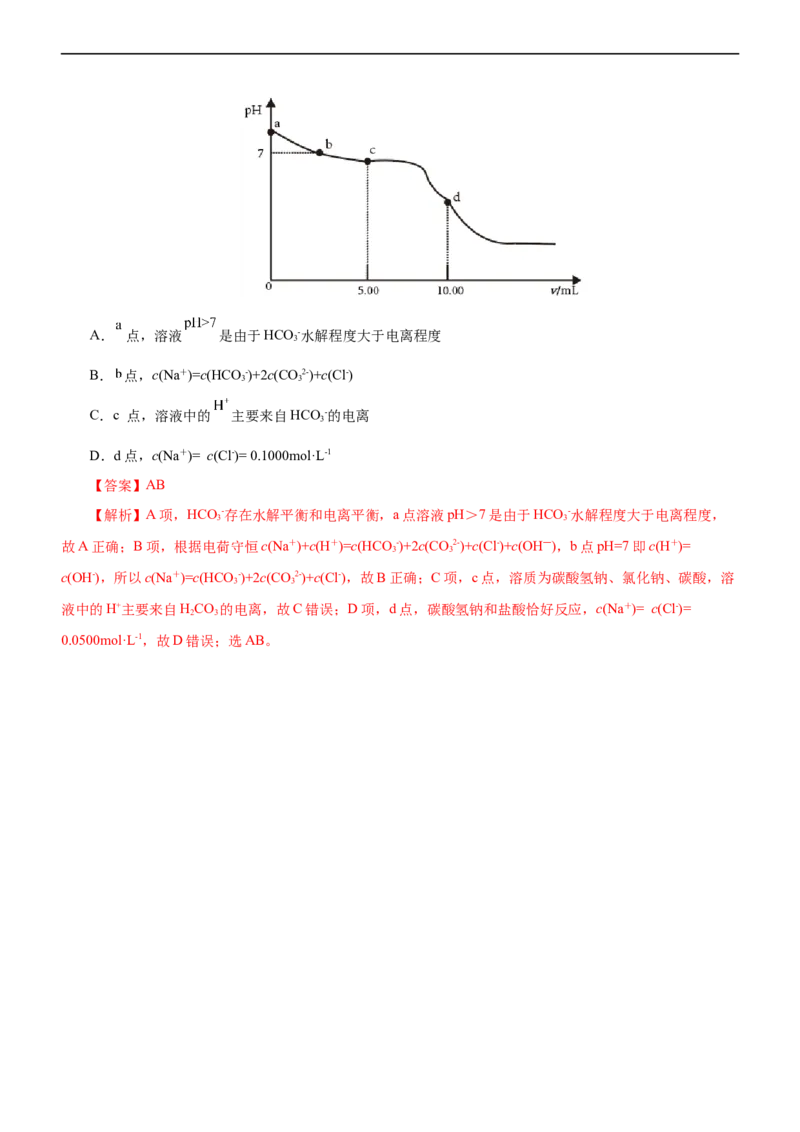
11.(2021•海南选择性考试) 25℃时,向10.00mL0.1000mol·L-1的NaHCO 溶液中滴加.1000mol·L-1的盐酸,
3
溶液的 随加入的盐酸的体积 变化如图所示。下列有关说法正确的是( )A. 点,溶液 是由于HCO -水解程度大于电离程度
3
B. 点,c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-)
3 3
C.c 点,溶液中的 主要来自HCO -的电离
3
D.d点,c(Na+)= c(Cl-)= 0.1000mol·L-1
【答案】AB
【解析】A项,HCO -存在水解平衡和电离平衡,a点溶液pH>7是由于HCO -水解程度大于电离程度,
3 3
故A正确;B项,根据电荷守恒c(Na+)+c(H+)=c(HCO -)+2c(CO2-)+c(Cl-)+c(OH―),b点pH=7即c(H+)=
3 3
c(OH-),所以c(Na+)=c(HCO -)+2c(CO2-)+c(Cl-),故B正确;C项,c点,溶质为碳酸氢钠、氯化钠、碳酸,溶
3 3
液中的H+主要来自HCO 的电离,故C错误;D项,d点,碳酸氢钠和盐酸恰好反应,c(Na+)= c(Cl-)=
2 3
0.0500mol·L-1,故D错误;选AB。