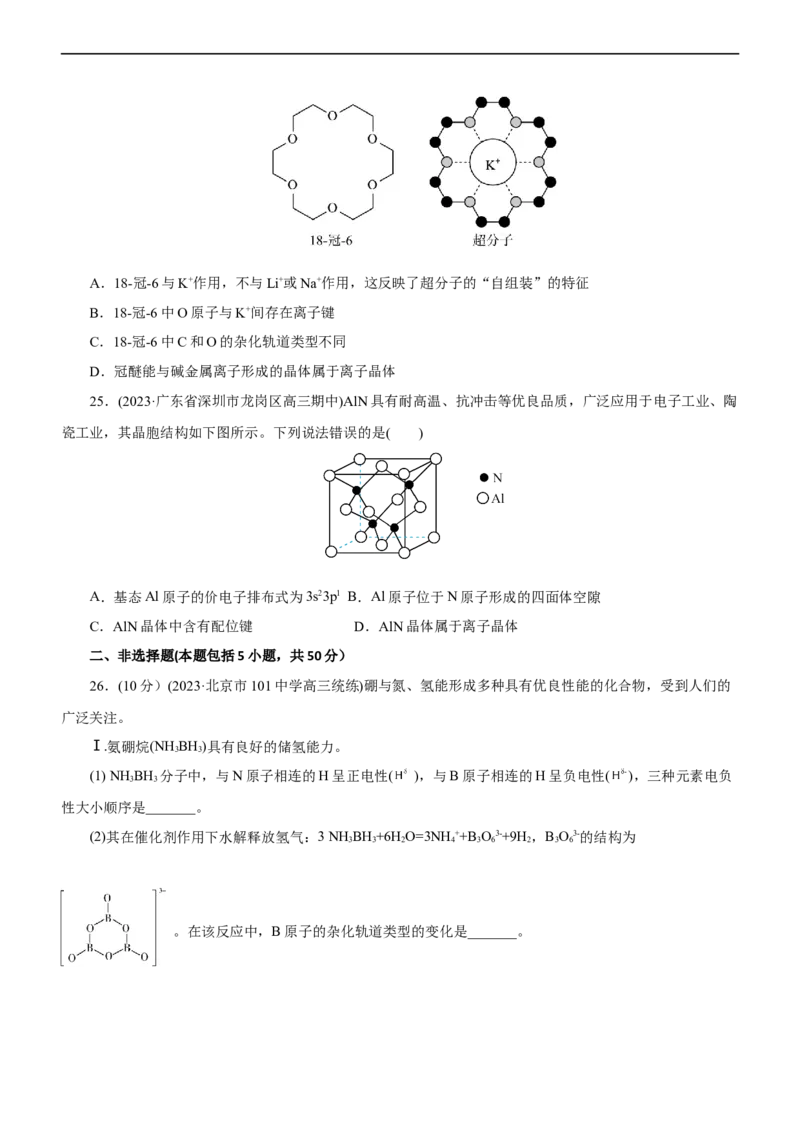
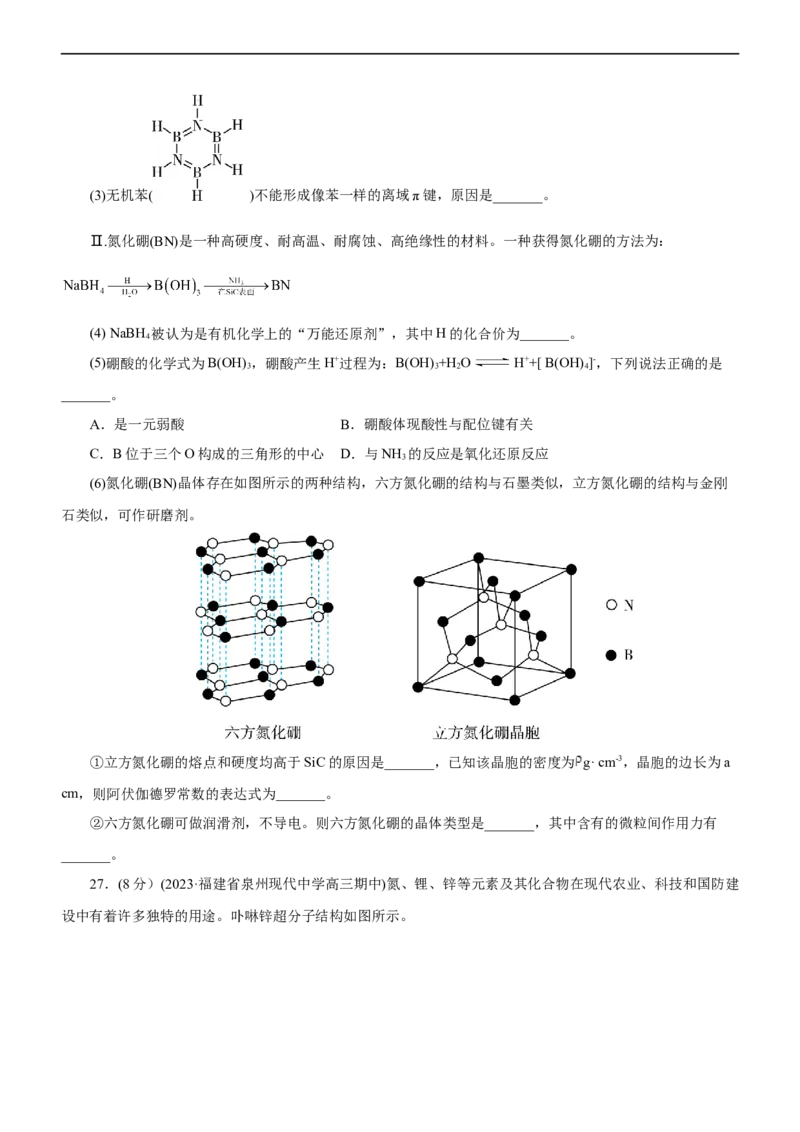
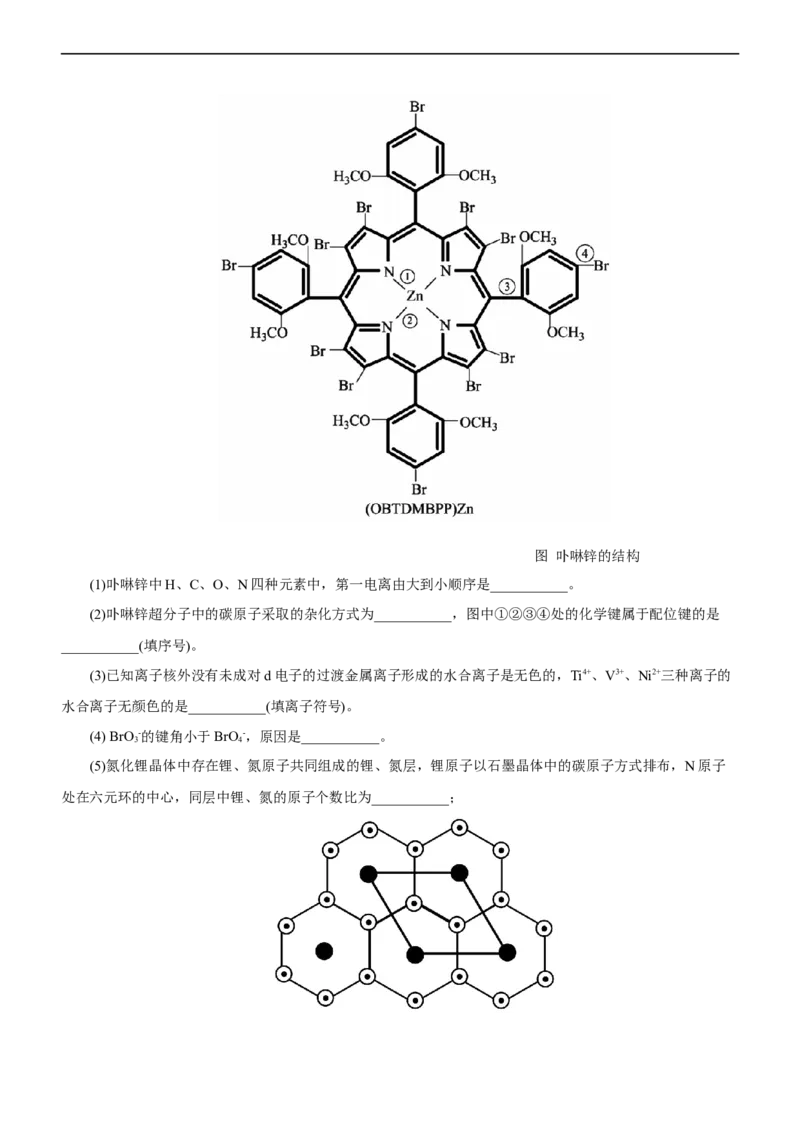
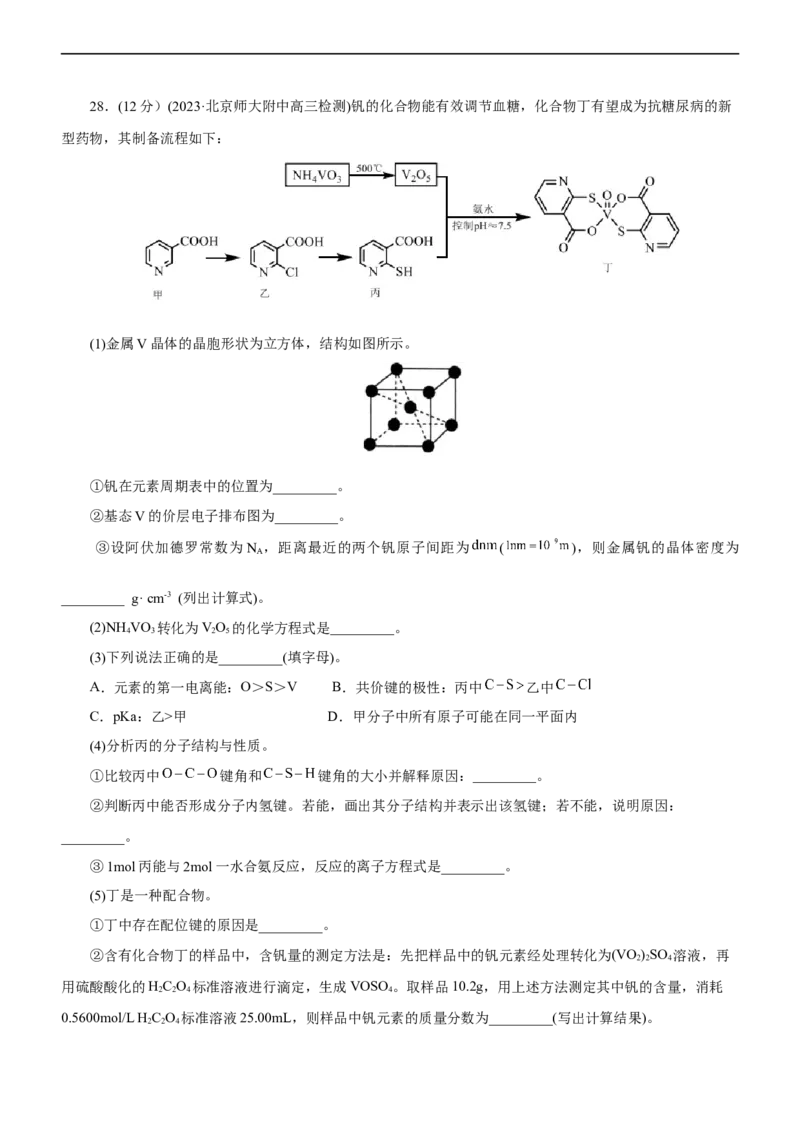
文档内容
专题 15 物质结构与性质
一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)
1.(2023·黑龙江省绥化市第九中学高三质检)已知在一定条件下,SO 也能体现其氧化性,例如:
2
2HS+SO=3S+2H O,下列化学用语使用正确的是( )
2 2 2
A.SO 的VSEPR模型:
2
B. HS-电离的离子方程式:HS-+H2O HS+OH-
2
C.基态硫原子 轨道的电子云轮廓图:
D.基态氧原子最外层电子的轨道表示式:
2.(2023·江苏省南京市江宁区高三期中)尿素CO(NH) 是一种高效化肥,也是一种化工原料。反应
2 2
CO+2NH CO(NH)+H O可用于尿素的制备。下列有关说法不正确的是( )
2 3 2 2 2
A.NH 与CO(NH) 均为极性分子
3 2 2
B.NH 分子的电子式为
2 4
C.NH 的键角大于HO的键角
3 2
D.尿素分子σ键和π键的数目之比为6∶1
3.(2023·广东省深圳市龙岗区高三期中)拉希法制备肼(NH)的主要反应为NaClO+2NH = NaCl+N H+H O
2 4 3 2 4 2
。下列表示反应中相关微粒的化学用语正确的是( )
A.基态氧原子的轨道表示式:
B.中子数为18的氯原子:C.NH 的空间填充模型:
3
D.NH 的电子式:
2 4
4.(2023·北京师大附中高三统测)下列化学用语或图示表达不正确的是( )
A.AsO 3-的空间结构模型:
4
B.反-2-丁烯的分子结构模型:
C.基态铬原子的价层电子排布式:3d54s1
D.过氧化钠的电子式:
5.(2023·山东省济宁市兖州区教学研究室高三期中)连二亚硝酸是一种重要的还原剂,可由亚硝酸和羟胺
反应制备,其反应的化学方程式为:HONO+HNOH = HON=NOH+H O。下列说法错误的是( )
2 2
A.亚硝酸根离子为V形结构 B.羟胺是极性分子
C.1个 中有6个 键 D.连二亚硝酸可能易溶于水
6.(2023·广东省四校高三联考)下列符号表征或说法正确的是( )
A.葡萄糖的实验式:C H O
6 12 6
B.Fe、Co、Ni位于元素周期表p区
C.BH-、CH、NH +空间结构均为正四面体
4 4 4
D.金刚石的晶胞:
7.(2023·山东省临沂市高三期中)亚铁氰化钾属于欧盟批准使用的食品添加剂,受热易分解:3K[Fe(CN) ]
4 6
12KCN+Fe C+2(CN) ↑+N ↑+C,下列关于该反应说法错误的是( )
3 2 2
A.基态Fe2+的价层电子排布式为3d6
B.N 和(CN) 均为非极性分子
2 2
C.(CN) 分子中σ键和π键数目比为3:4
2
D.配合物K[Fe(CN) ]中配位原子是氮原子
4 68.(2023·广东省名校联盟高三大联考)氢氰酸是酸性极弱的一种酸,其结构式为H-C≡N,下列有关
的说法错误的是( )
A.碳原子为 杂化 B.是V形分子
C. 键、 键数目相等 D.所含化学键均是极性键
9.(2023·辽宁省沈阳二中高三期中)下列有关描述及化学用语的表示方法正确的是( )
A.As原子的简化电子排布式为[Ar]3s23p3
B.KCI形成过程:
C.基态Mg原子的核外电子排布图为
D.Se在周期中属于p区元素,Zn属于ds区元素
10.(2023·甘肃省西北师大附中高三期中)下列元素或化合物的性质变化顺序正确的是( )
A.第一电离能:Cl>S>P> Si
B.分子的极性:
C.价层电子对互斥模型中, 键电子对数不计入中心原子的价层电子对数
D.第四周期元素中,锰原子价电子层中未成对电子数最多
11.(2023·江苏省高三第二次大联考)下列关于NO -、NO -和[Fe(NO)(HO) ]SO 的说法正确的是( )
2 3 2 5 4
A.NO -中氮原子轨道采用sp杂化 B.NO -的空间构型为三角锥形
2 3
C.配合物[Fe(NO)(HO) ]SO 中有2种配体 D.1mol[Fe(NO)(HO) ]2+中含有6molσ键
2 5 4 2 5
12.(2023·辽宁省抚顺市六校协作体高三期中)在酸性或者接近中性的条件下, 易发生歧化反应,将
CO 通入KMnO 溶液中,其反应为3KMnO +2CO =2KMnO +MnO+2K CO。下列有关说法错误的是( )
2 2 4 2 4 2 4 2 2 3
A.CO2-的空间结构为三角锥形
3
B.CO 中心原子的杂化方式是sp
2
C.基态钾原子的价电子排布式:4s1
D.基态Mn2+的价电子轨道表示式:
13.(2022·天津市滨海新区塘沽第一中学高三期中)磷酸亚铁锂(LiFePO )可作锂离子电池的正极材料。工业
4
上以FeCl 、NH H PO 、LiCl和苯胺( )等为原料制备磷酸亚铁锂。下列说法错误的是( )
3 4 2 4
A.苯胺中氮原子的杂化方式是sp3B.NH +和PO 3-的空间结构相同
4 4
C.1mol苯胺分子中含有9molσ键
D.LiC1、苯胺和甲苯的熔点由高到低的顺序是LiCl>苯胺>甲苯
14.(2023·河北省石家庄精英中学高三第三次考试)下列说法正确的是( )
A. σ键和π键比例为7:1
B.SO 空间结构为三角锥形
3
C.配合物铁氰化钾K[Fe(CN) ]中几种元素电离能由大到小的顺序是N>C>K>Fe
3 6
D.CO 分子中C和O原子之间的σ键是由C原子的sp杂化轨道与O原子的2p轨道重叠形成
2
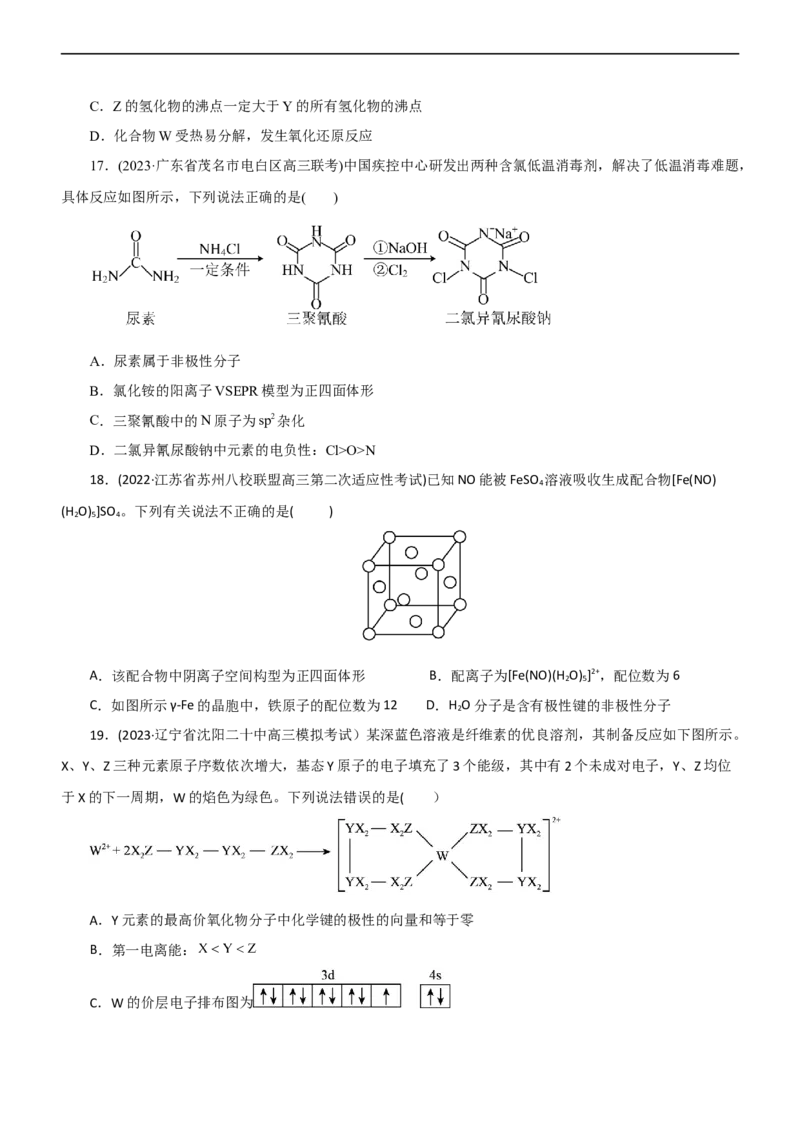
15.(2023·重庆南开中学高三检测)W、X、Y、Z为是四种原子序数依次增大的短周期元素,这四种元素
组成的化学式为XWYZ的物质在有机合成中具有较高的应用价值。X元素的族序数是周期数的两倍,Y元素
2 5
的电离能如下表所示,Z原子得到一个电子后核外电子排布变为与稀有气体电子排布相同。下列说法正确的是
( )
I I I I
1 2 3 4
A.电负性:
B.原子半径:
C.在XWYZ中,所有原子均满足八电子稳定结构
2 5
D.电解Y和Z组成的二元化合物的水溶液可得到Y和Z的单质
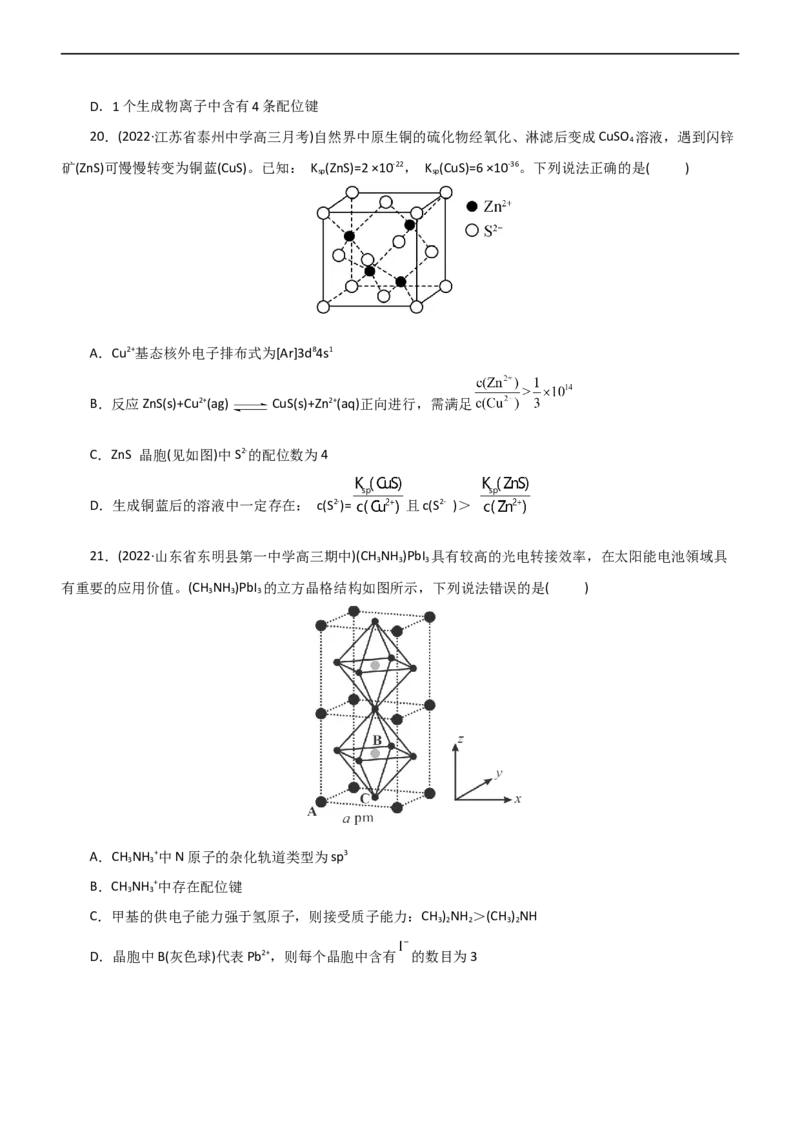
16.(2023·重庆市拔尖强基联合高三检测)物质W常用作食品添加剂,其组成元素均为短周期主族元素,
各元素原子半径与原子序数的关系如图所示,元素N的单质在常温下为气体。下列说法正确的是( )
A.W中Y原子的杂化方式为sp3
B.常温下N的单质与NaOH溶液反应,其中一种产物的水溶液呈碱性,有漂白性C.Z的氢化物的沸点一定大于Y的所有氢化物的沸点
D.化合物W受热易分解,发生氧化还原反应
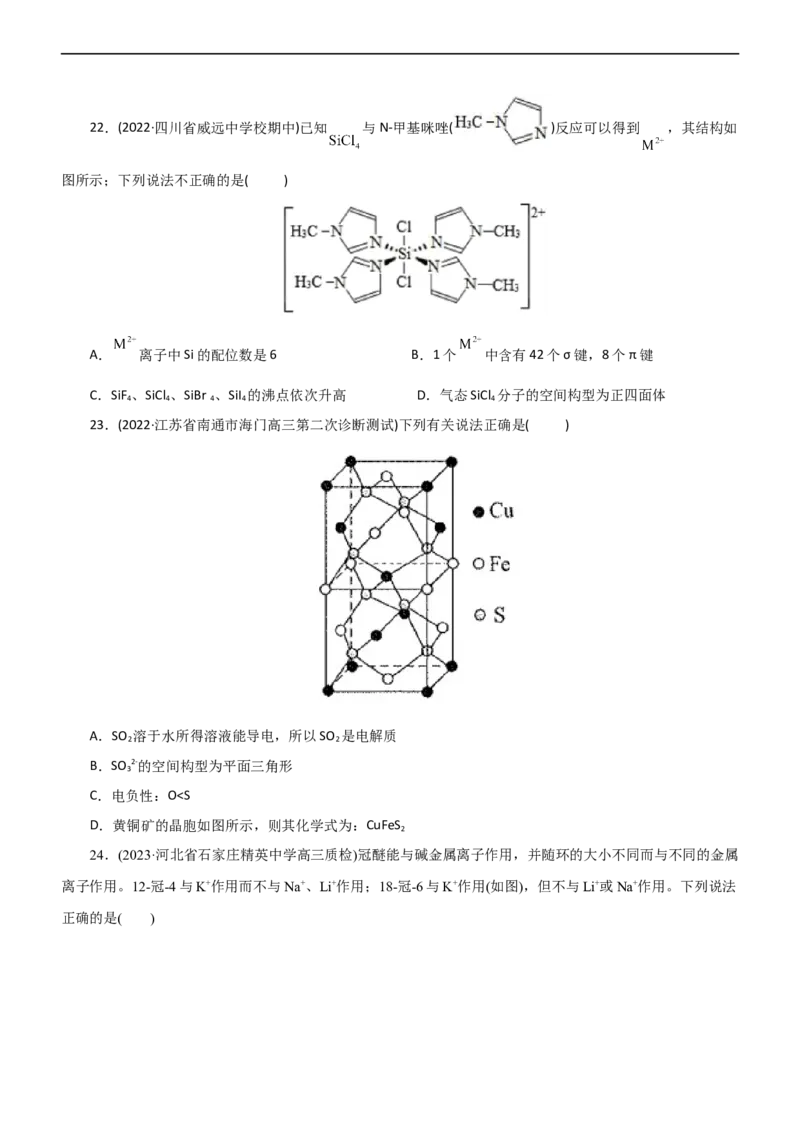
17.(2023·广东省茂名市电白区高三联考)中国疾控中心研发出两种含氯低温消毒剂,解决了低温消毒难题,
具体反应如图所示,下列说法正确的是( )
A.尿素属于非极性分子
B.氯化铵的阳离子VSEPR模型为正四面体形
C.三聚氰酸中的N原子为sp2杂化
D.二氯异氰尿酸钠中元素的电负性:Cl>O>N
18.(2022·江苏省苏州八校联盟高三第二次适应性考试)已知NO能被FeSO 溶液吸收生成配合物[Fe(NO)
4
(H O) ]SO 。下列有关说法不正确的是( )
2 5 4
A.该配合物中阴离子空间构型为正四面体形 B.配离子为[Fe(NO)(H O) ]2+,配位数为6
2 5
C.如图所示γ-Fe的晶胞中,铁原子的配位数为12 D.H O分子是含有极性键的非极性分子
2
19.(2023·辽宁省沈阳二十中高三模拟考试)某深蓝色溶液是纤维素的优良溶剂,其制备反应如下图所示。
X、Y、Z三种元素原子序数依次增大,基态Y原子的电子填充了3个能级,其中有2个未成对电子,Y、Z均位
于X的下一周期,W的焰色为绿色。下列说法错误的是( )
A.Y元素的最高价氧化物分子中化学键的极性的向量和等于零
B.第一电离能:
C.W的价层电子排布图为D.1个生成物离子中含有4条配位键
20.(2022·江苏省泰州中学高三月考)自然界中原生铜的硫化物经氧化、淋滤后变成CuSO 溶液,遇到闪锌
4
矿(ZnS)可慢慢转变为铜蓝(CuS)。已知: K (ZnS)=2 ×10-22, K (CuS)=6 ×10-36。下列说法正确的是( )
sp sp
A.Cu2+基态核外电子排布式为[Ar]3d84s1
B.反应ZnS(s)+Cu2+(ag) CuS(s)+Zn2+(aq)正向进行,需满足
C.ZnS 晶胞(见如图)中S2-的配位数为4
D.生成铜蓝后的溶液中一定存在: c(S2-)= 且c(S2- )>
21.(2022·山东省东明县第一中学高三期中)(CH NH )PbI 具有较高的光电转接效率,在太阳能电池領域具
3 3 3
有重要的应用价值。(CH NH )PbI 的立方晶格结构如图所示,下列说法错误的是( )
3 3 3
A.CH NH +中N原子的杂化轨道类型为sp3
3 3
B.CH NH +中存在配位键
3 3
C.甲基的供电子能力强于氢原子,则接受质子能力:CH ) NH >(CH ) NH
3 2 2 3 2
D.晶胞中B(灰色球)代表Pb2+,则每个晶胞中含有 的数目为322.(2022·四川省威远中学校期中)已知 与N-甲基咪唑( )反应可以得到 ,其结构如
图所示;下列说法不正确的是( )
A. 离子中Si的配位数是6 B.1个 中含有42个σ键,8个π键
C.SiF 、SiCl 、SiBr 、SiI 的沸点依次升高 D.气态SiCl 分子的空间构型为正四面体
4 4 4 4 4
23.(2022·江苏省南通市海门高三第二次诊断测试)下列有关说法正确是( )
A.SO 溶于水所得溶液能导电,所以SO 是电解质
2 2
B.SO 2-的空间构型为平面三角形
3
C.电负性:O甲 D.甲分子中所有原子可能在同一平面内
(4)分析丙的分子结构与性质。
①比较丙中 键角和 键角的大小并解释原因:_________。
②判断丙中能否形成分子内氢键。若能,画出其分子结构并表示出该氢键;若不能,说明原因:
_________。
③1mol丙能与2mol一水合氨反应,反应的离子方程式是_________。
(5)丁是一种配合物。
①丁中存在配位键的原因是_________。
②含有化合物丁的样品中,含钒量的测定方法是:先把样品中的钒元素经处理转化为(VO )SO 溶液,再
2 2 4
用硫酸酸化的HC O 标准溶液进行滴定,生成VOSO。取样品10.2g,用上述方法测定其中钒的含量,消耗
2 2 4 4
0.5600mol/L H C O 标准溶液25.00mL,则样品中钒元素的质量分数为_________(写出计算结果)。
2 2 429.(10分)(2023·湖湘名校教育联合体五市十校教研教改共同体高三第三次大联考)2022年珠海航展成功
举办,歼20战机和C919国产大飞机等大国重器悉数亮相,世界瞩目。金属材料和复合材料在航空航天工业中
具有重要的应用。回答下列问题:
(1)金属铼(Re)是生产航空发动机叶片必不可少的材料。NH ReO 在高温下用H 还原可制得金属铼,反应
4 4 2
的化学方程式为_____。
(2)硬铝中含Mg、Si等合金元素,因其密度小、强度高且耐腐蚀,常用于制造飞机的外壳。
①基态Al原子核外电子的空间运动状态有____种。
②Mg、Al、Si的第一电离能由大到小的顺序为____。
③AlCl 易与Cl-形成配离子AlCl -,AlCl -的空间构型为____,其中Al的杂化轨道类型为____。写出与
3 4 4
AlCl -原子总数和价电子总数均相等的一种等电子体的分子式____。
4
(3)以SiC为连续基体的碳陶瓷是一种复合材料,可用于制造歼20的刹车片。
①SiC的熔点比晶体Si____(填“高”或“低”),原因是____。
②某碳族元素参与形成的三元化合物晶胞示意图如图,该化合物的化学式为____。
30.(10分)(2023·山东省青岛市四区县高三期中)硼、铝、镓、铟等第IIIA族元素及其化合物在材料化学、
工业生产和生活中具有广泛的应用。回答下列问题:
(1)基态镓原子核外价电子的轨道表示式为_______;同周期主族元素基态原子与其具有相同数目未成对电
子的有_______。
(2)氨硼烷(NH BH)是目前最具潜力的储氢材料之一。
3 3
①氨硼烷晶体中B原子的杂化方式为________。
②氨硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“N-H…H-B”表示。以下物质之间可能形成双氢键的是_______(填序号)。
a.N H 和AlH b.C H 和C H c.B H 和HCN
2 4 3 3 6 2 6 2 6
(3)氟化铝常用作非铁金属的熔剂,可由氯化铝与氢氟酸、氨水作用制得。从氟化铝熔点(1090℃)到氯化铝
熔点(192.6℃)下降幅度近900℃的原因是_______。
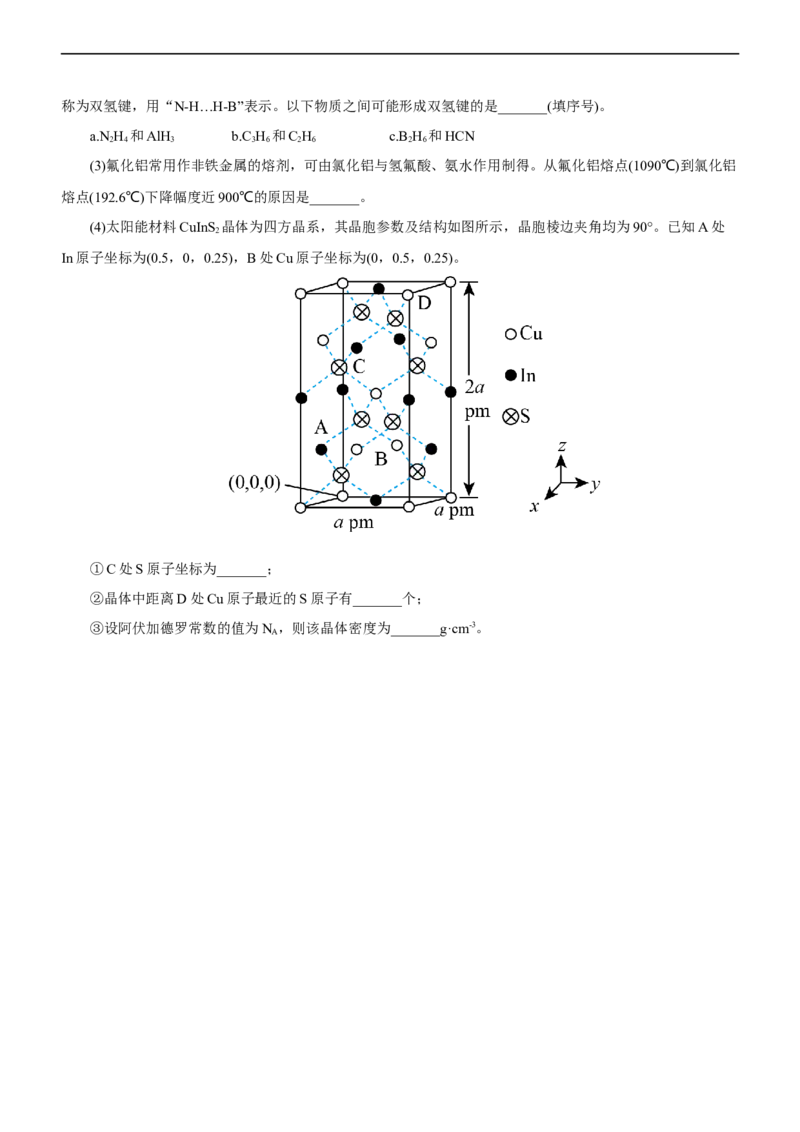
(4)太阳能材料CuInS 晶体为四方晶系,其晶胞参数及结构如图所示,晶胞棱边夹角均为90°。已知A处
2
In原子坐标为(0.5,0,0.25),B处Cu原子坐标为(0,0.5,0.25)。
①C处S原子坐标为_______;
②晶体中距离D处Cu原子最近的S原子有_______个;
③设阿伏加德罗常数的值为N ,则该晶体密度为_______g·cm-3。
A