文档内容
专题 27 化学平衡状态 化学平衡的移动
(建议完成时间:45分钟 实际完成时间:_______分钟)
目 录
考点一 化学平衡状态
考点二 化学平衡的移动
考点一 化学平衡状态
1.(2023·上海青浦·统考二模)在一个2L的密闭容器中,发生反应: 2SO (g) 2SO (g)+ O (g) — Q
3 2 2
(Q>0),其中SO 的物质的量随时间变化如图所示,下列判断错误的是
3
A.0~8min内v(SO )=0.025mol/(L·min)
3
B.8min时,v逆(SO )=2v正(O )
2 2
C.8min时,容器内压强保持不变
D.若8min时将容器压缩为1L,n(SO )的变化如图中a
3
【答案】D
【解析】A、0~8 min内v(SO )= =0.025mol/(L•min),选项A正确;B、8min时,n(SO )不
3 3
再变化,说明反应已达平衡,v逆(SO )= v正(SO )=2v正(O ),选项B正确;C、8min时,n(SO )不再变化,
2 2 2 3
说明各组分浓度不再变化,容器内压强保持不变,选项C正确;D、若8min时压缩容器体积时,平衡向气
体体积减小的逆向移动,但纵坐标是指物质的量,不是浓度,SO 的变化曲线应为逐变不可突变,选项D
3
错误;答案选D。
2.(2023·河北·校联考一模)工业上,利用氨气还原二氧化氮的技术已经成熟。250℃时,在1L恒容密闭
容器中通入 氨气和 二氧化氮,发生反应: ,测
得容器中压强随时间变化情况如下:
反应时间
0 10 20 30 50 60 70
总压
10 10.50 10.60 10.70 10.80 11.00 11.00
1
原创精品资源学科网独家享有版权,侵权必究!下列说法不正确的是
A.单位时间内断裂 键,同时断裂 键即达到平衡状态
B.在 内,二氧化氮的化学反应速率是
C.达到化学平衡时,氮气的体积分数是30%
D. 的活化能小于 的活化能
【答案】C
【解析】A.单位时间内断裂 键,即消耗 氨气,同时断裂 键,即消耗
,说明正逆反应速率相同,即达到平衡状态,选项A正确;B.利用容器体积不变,温度不变,压强
比等于气体的物质的量之比, 时,设转化的NO 的物质的量为x,根据三段式有:
2
则有 ,解得x=0.42mol,二氧化氮的化学反应速率是 =
,选项B正确;C.根据表格中的数据,可以看出在 时,化学反应达到平衡,设
N 的物质的量为y,利用三段式可知:
2
则有 ,解得y=0.98mol,气体总物质的量为 =7.7mol,氮气的体积分
数约为 =12.7%,选项C错误;D.由于 是放热反应,逆
反应是吸热反应,正反应的活化能小于逆反应的活化能,选项D正确;答案选C。
3.(2023秋·云南昆明·高三昆明市官渡区第二中学校考开学考试)已知密闭容器中发生反应
,下列说法正确的是
A.当容器内压强保持不变时,表明反应已经达到平衡
B.改变某一条件,若再次达到v(X)=v(Y),则反应达到平衡
C.达到平衡时,X与Y的物质的量之比一定是1:1
D.若保持容器体积不变,升温后体系内气体平均相对分子质量增大【答案】D
【解析】A.该反应为气体体积不变的反应,压强始终不变,不能判断平衡状态,故A错误;B.平衡时
不同物质的正逆反应速率之比等于化学计量数之比,不能由v(X)=v(Y)判断是否达到平衡,故B错误;
C.起始量未知,转化率未知,则平衡时X、Y的物质的量比不确定,故C错误;D.焓变为负,升高温度
平衡逆向移动,气体的物质的量不变、质量增大,则平均相对分子质量增大,故D正确;故答案为D。
4.(2023秋·湖南长沙·高三长沙市明德中学校考开学考试)T ℃时,向某恒温恒容密闭容器中充入等物质
的量的CH(g)和CO(g),发生二氧化碳重整甲烷反应:CH(g)+CO(g) 2CO(g)+2H(g),测得体系中
4 2 4 2 2
CH(g)和CO(g)的物质的量浓度随时间变化如图所示,下列说法错误的是
4
A.点B的坐标为(5, )
B.反应进行到5 min时,2v (CH)<v (CO)
正 4 逆
C.CO(g)的平衡转化率约为33.3%
2
D.T ℃时,该反应的平衡常数为
【答案】B
【解析】A.根据图象可知:在5 min时CH(g)的浓度减少0.25 mol/L,则根据物质反应转化关系可知:反
4
应产生CO的浓度为0.50 mol/L,故B点的坐标为(5, ),A正确;B.反应进行到5 min时,CH(g)的浓
4
度还在减小,说明反应正向进行,v (CH)>v (CH),由于v (CO)=2v (CH),所以2v (CH)>v
正 4 逆 4 逆 逆 4 正 4 逆
(CO),B错误;C.平衡时CH(g)的浓度与CO(g)浓度相等,等于 ,开始时CO(g)的浓度为1.00
4 2 2
mol/L,故CO(g)的平衡转化率为: ,C正确;D.根据图象可知:在温度为T ℃时,
2
c(CH)=c(CO)=c(CO)=c(H )= ,则根据平衡常数的含义可知K= ,D正确;故合理
4 2 2
选项是B。
5.(2023春·北京海淀·高三校考开学考试)二氧化碳到淀粉的人工合成第一步为用无机催化剂将二氧化碳
还原为甲醇,反应方程式为3H(g)+CO (g) CHOH(g)+H O(g)。一定温度下,恒容密闭容器中按照投
2 2 3 2料比 =3充入H 与CO,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CHOH),在
2 2 3
T=250℃下的x(CHOH)~p、在p=5×105Pa下的x(CHOH)~T如图所示。下列说法不正确的是
3 3
A.当体系中c(CHOH)与c(H)比值不变,可说明此时该反应达到平衡状态
3 2
B.曲线b表示的是压强相同时,温度升高该反应逆向移动,说明正反应放热
C.在原p=5×105Pa,210℃的条件下,向该恒容密闭容器中继续通入3molH 与1molCO ,达到新的平衡后,
2 2
x(CHOH)<0.10
3
D.当x(CHOH)=0.10时,反应条件可能为p=5×105Pa,210℃或p=9×105Pa,250℃
3
【答案】C
【解析】A.初始投料为 和 ,所以平衡前 浓度减小, 浓度增大,所以当 与
比值不变时说明反应达到平衡状态,故A正确;B.该反应为体积减小的反应,增大压强,平衡正
向移动,故曲线b为等压条件下,温度升高, 减小,说明平衡逆向移动, ,故B正确;
C.在 ,210℃的条件下,向该密闭体系中继续通入 与 ,可以理解为先在另一个
容器中达到平衡,x(CHOH)=0.10,再压缩到一个容器中,平衡正向移动,达到新的平衡后,
3
,故C错误;D.由图和信息T=250℃下的x(CHOH)~p、在p=5×105Pa下的x(CHOH)
3 3
~T可知:满足平衡时 的条件有: ,210℃或 ,250℃,故D正确;综
上所述,答案为C。
6.(2023秋·云南昆明·高三昆明市官渡区第二中学校考开学考试)一定条件下2A(g)+2B(g) 3C(g)
+D(g),达到平衡的标志是
A.单位时间生成2nmolA,同时消耗nmolD B.容器内的压强不随时间变化而变化
C.容器内混合气密度不随时间而变化 D.单位时间内生成nmolB,同时生成1.5nmolC
【答案】D
【解析】A.无论反应是否达到平衡状态,每生成2nmolA,同时消耗nmolD,所以不能判断该反应是否达
到平衡状态,故A错误;B.反应前后气体的物质的量不发生变化,一定条件下压强自始至终不变化,压强不变不能说明到达平衡,故B错误;C.反应前后气体的体积、质量均不变,所以混合气体的密度也不
变,不能说明反应达到平衡状态,故C错误;D.单位时间内生成n mol B,必然消耗1.5nmolC,而又同时
生成1.5n mol C,所以正逆反应速率相等,反应达到平衡状态,故D正确;故选:D。
7.(2023秋·云南曲靖·高三宣威市第三中学校考开学考试)一定温度下,在2 L的密闭容器中,X、Y、Z
三种气体的物质的量随时间变化的曲线如图所示。下列描述正确的是
A.反应在0~10 s内,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应在0~10 s内,X的物质的量浓度减少了0.79 mol·L-1
C.反应进行到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)=Z(g)
【答案】C
【解析】A.反应开始到10s,用Z表示的反应速率为 ,A错误;B.X初始物
质的量为1.2mol,到10s物质的量为0.41mol,物质的量减少了0.79mol,浓度减小了0.395mol/L,B错误;
C.Y初始物质的量为1mol,到10s剩余0.21mol,转化了0.79mol,转化率为79%,C正确;D.X、Y物
质的量减小,Z物质的量增大,说明X、Y为反应物,Z为生成物,达到平衡时Z物质的量变化量
Δn(X)=0.79mol,Δn(Y)=0.79mol,Δn(Z)=1.58mol,故X、Y、Z化学计量数之比为1:1:2,D错误;故选
C。
8.(2023秋·河北·高三校联考开学考试)在恒温恒容条件下,向容积为1L的密闭容器中充入一定量的
SO (g),发生下列反应: 。温度为T时,部分实验数据如表所示:
3
0 50 100 150
4.00 2.50 2.00 2.00
下列说法错误的是
A.前50s内 的平均生成速率为
B.容器内密度不再改变说明反应已达平衡
C.150s时,向容器中继续通入 、 、 ,则此时反应将逆向进行
D.其他条件不变,若将恒容改为恒压,则平衡时 的转化率增大
【答案】B【解析】A.由题干表格数据可知,前50s内SO (g)的平均消耗速率为: = ,
3
根据反应速率之比等于化学计量数之比,故前50s内SO (g)的平均生成速率为 ,A正确;
2
B.已知反应过程中气体的质量不变,容器的体积不变,即反应过程中溶液内密度始终保持不变,故容器
内密度不再改变不能说明反应已达平衡,B错误;C.由题干表格数据可知,达到化学平衡时c(SO )=
3
c(SO )=2.00mol/L,c(O)=1.00mol/L,此时化学平衡常数K= = =1,150s时,向容器中继
2 2
续通入2molSO 、2molSO 、1molO ,则此时Qc= = =2>K,故反应将逆向进行,
3 2 2
C正确;D.其他条件不变,若将恒容改为恒压,随着反应的进行容器的体积增大,相当于减小压强,平
衡正向移动,则平衡时SO 的转化率增大,D正确;故答案为:B。
3
9.(2023·河北秦皇岛·昌黎一中校考模拟预测)在T℃时,向一个3L的密闭容器中通入4mol 、amol
,发生反应: 。此时 的平衡转化率为60%。下列说法错误
的是
A.当混合气体的平均摩尔质量不变时,反应达到平衡
B.当 时,反应达到平衡
C.反应过程中分离出 ,正反应速率增大
D.平衡时,若 的转化率为60%,则a=5
【答案】C
【解析】A.由质量守恒定律可知,反应前后气体的质量相等,该反应为气体体积增大的反应,反应中混
合气体的平均摩尔质量减小,则混合气体的平均摩尔质量不变说明正逆反应速率相等,反应已达到平衡,
故A正确;B.由化学反应速率之比等于化学计量数之比可知, 说明正逆反应速
率相等,反应已达到平衡,故B正确;C.反应过程中分离出水蒸气,生成物的浓度减小,正、逆反应速
率均减小,故C错误;D.平衡时反应物氨气和氧气的转化率相等说明起始通入的氨气和氧气的物质的量
比等于化学计量数比,由起始氨气为4mol,则通入的氧气一定为5mol,则a=5,故D正确;故选C。
10.(2023秋·广东湛江·高三湛江市第二中学校联考开学考试)在Fe O 的催化作用下,向200℃的恒温恒
2 3
容密闭容器中充入1molCH 和2molNO ,发生反应CH(g)+2NO (g) CO(g)+N(g)+2HO(g),反应过程
4 2 4 2 2 2 2
及能量变化示意图如图所示。下列说法正确的是
A.容器内气体的密度不再发生变化时,该反应达到平衡状态B.反应一段时间后(未达平衡),Fe O 会远远多于Fe O
3 4 2 3
C.起始条件相同,其他条件不变,仅改为绝热密闭容器,CH 和NO 的转化率降低
4 2
D.使用更高效的催化剂能提高该反应平衡时的转化率
【答案】C
【解析】A.容器为恒容密闭容器,气体质量在反应过程中理论上是不变的,根据 ,反应过程中密
度一直保持不变,故密度不发生变化不能说明该反应达到平衡状态,A错误;B.根据题干能量变化图,
反应i的活化能比反应的大,反应ii速率较快,不会有大量Fe O 剩余,B错误;C.根据能量变化图,总
3 4
反应正向为放热反应,绝热密闭容器中反应开始后温度会升高,导致平衡逆向移动,反应物转化率降低,
C正确;D.催化剂只能提高反应速率,不能改变平衡转化率,D错误;故选C。
考点二 化学平衡的移动
1.(2023·湖南长沙·长郡中学校考一模)用活性炭还原 可防止空气污染,其反应原理为
。在密闭容器中, 和足量C发生上述反应,维持温度不变,
反应相同时间内不同密闭容器中测得 百分含量的变化如图所示,下列说法错误的是
A.F点可能已达到平衡
B.G点的 小于E点的
C.E、G两点的平衡常数相等,但体系中 的物质的量不相等
D.在恒温恒容下,向E点体系中充入一定量的 ,达到平衡时, 的百分含量不可能与F点相等
【答案】C
【分析】化学平衡是化学反应的最大限度,由图可知,F点氮气的百分含量最大,所以F点反应达到平衡;
容器体积减小,气体压强增大,该反应是气体体积增大的反应,增大压强,平衡向逆反应方向移动,氮气
的百分含量减小,则G点反应未达到平衡、E点反应达到平衡。
【解析】A.由分析可知,E、F点反应均达到平衡,G点反应未达到平衡,故A正确;B.由分析可知,
G点反应未达到平衡、E点反应达到平衡,由图可知,G点压强小于E点,则G点的v 小于E点的v ,
逆 正
故B正确;C.由图可知,E、G两点的N 的百分含量相等,由方程式可知,N 和NO 的的百分含量之比
2 2 2
始终为1:2,化学平衡常数是温度函数,温度不变,平衡常数不变,则E、G两点的平衡常数相等,N 的
2
百分含量相同,则体系中NO 的百分含量相等,物质的量相等,故C错误;D.在恒温恒容下,向E点平
2
衡体系中充入一定量的NO ,向正反应方向移动,N 的百分含量增大,故D正确;故选C。
2 2
2.(2023·江苏·统考二模)用草酸二甲酯( )和氢气为原料制备乙二醇的反应原理如下:在2MPa条件下,将氢气和草酸二甲酯体积比(氢酯比)为80:1的混合气体以一定流速通过装有催化剂的反
应管,草酸二甲酯的转化率、产物的选择性与温度的关系如图所示。
产物的选择性
下列说法正确的是
A.曲线I表示乙二醇的选择性随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在190~195℃温度范围,随着温度升高,出口处乙醇酸甲酯的量不断减小
D.其他条件不变,在190~210℃温度范围,随着温度升高,出口处甲醇和乙二醇的物质的量之比[
]减小
【答案】D
【解析】A.当曲线乙醇酸甲酯选择性为50%时,曲线Ⅱ对应的选择性恰好为50%,而乙二醇的选择性此
时应为50%,故曲线Ⅱ表示乙二醇的选择性随温度的变化,故A错误;B.两个反应△H均小于0,即两
反应均为放热反应,当升高温度时,平衡向逆反应方向移动,草酸二甲酯的平衡转化率减小,故B错误;
C.由图可知,在190-195摄氏度温度范围,随着温度升高,草酸二甲酯的转化率升高,乙醇酸甲酯的选择
性几乎不变,故出口乙醇酸甲酯的量会不断增多,故C错误;D.在190-210摄氏度温度范围,随着温度
升高,由图可知,草酸二甲酯的转化率不断增大,乙二醇的选择性不断增大,出口处甲醇和乙二醇的物质
的量之比减小,故D正确;故选D。
3.(2023·辽宁沈阳·东北育才学校校考模拟预测)在催化剂作用下,向容积为1L的容器中加入1molX和
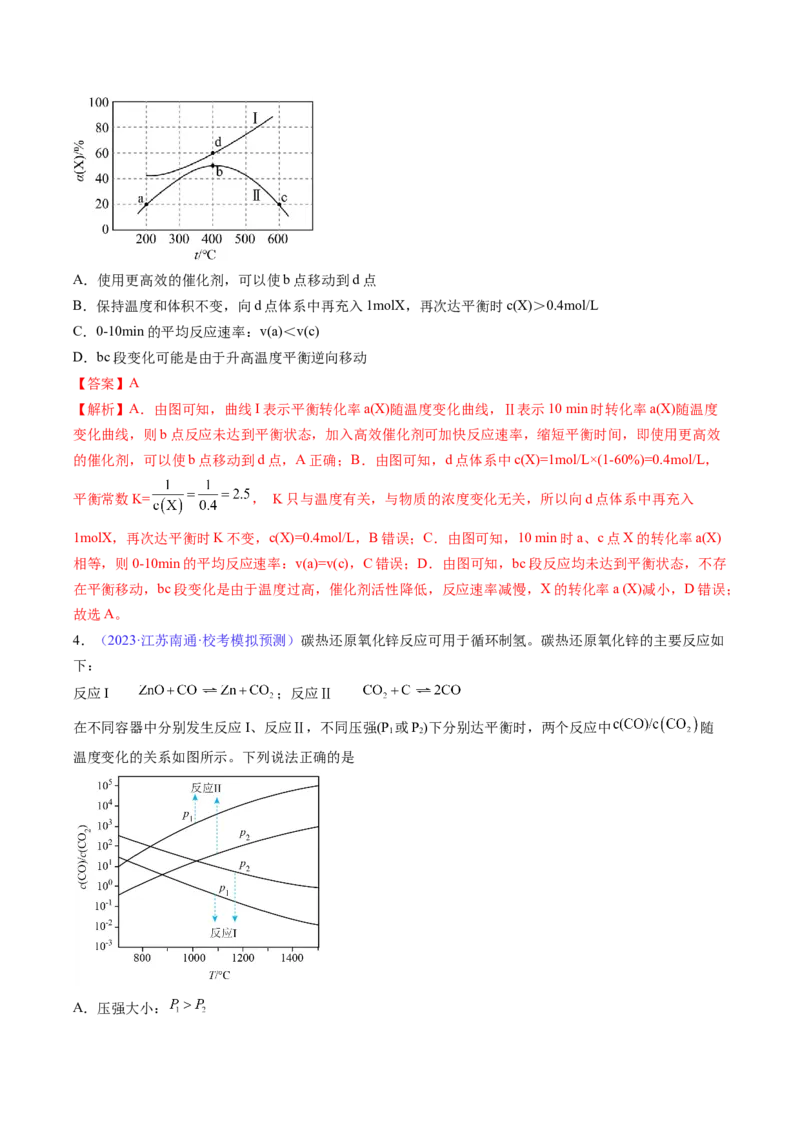
3molY,发生反应:X(g)+2Y(s) 2Z(s),平衡时和反应10min时X的转化率α(X)随温度的变化分别如
曲线I、Ⅱ所示。下列说法正确的是A.使用更高效的催化剂,可以使b点移动到d点
B.保持温度和体积不变,向d点体系中再充入1molX,再次达平衡时c(X)>0.4mol/L
C.0-10min的平均反应速率:v(a)<v(c)
D.bc段变化可能是由于升高温度平衡逆向移动
【答案】A
【解析】A.由图可知,曲线I表示平衡转化率a(X)随温度变化曲线,Ⅱ表示10 min时转化率a(X)随温度
变化曲线,则b点反应未达到平衡状态,加入高效催化剂可加快反应速率,缩短平衡时间,即使用更高效
的催化剂,可以使b点移动到d点,A正确;B.由图可知,d点体系中c(X)=1mol/L×(1-60%)=0.4mol/L,
平衡常数K= , K只与温度有关,与物质的浓度变化无关,所以向d点体系中再充入
1molX,再次达平衡时K不变,c(X)=0.4mol/L,B错误;C.由图可知,10 min时a、c点X的转化率a(X)
相等,则0-10min的平均反应速率:v(a)=v(c),C错误;D.由图可知,bc段反应均未达到平衡状态,不存
在平衡移动,bc段变化是由于温度过高,催化剂活性降低,反应速率减慢,X的转化率a (X)减小,D错误;
故选A。
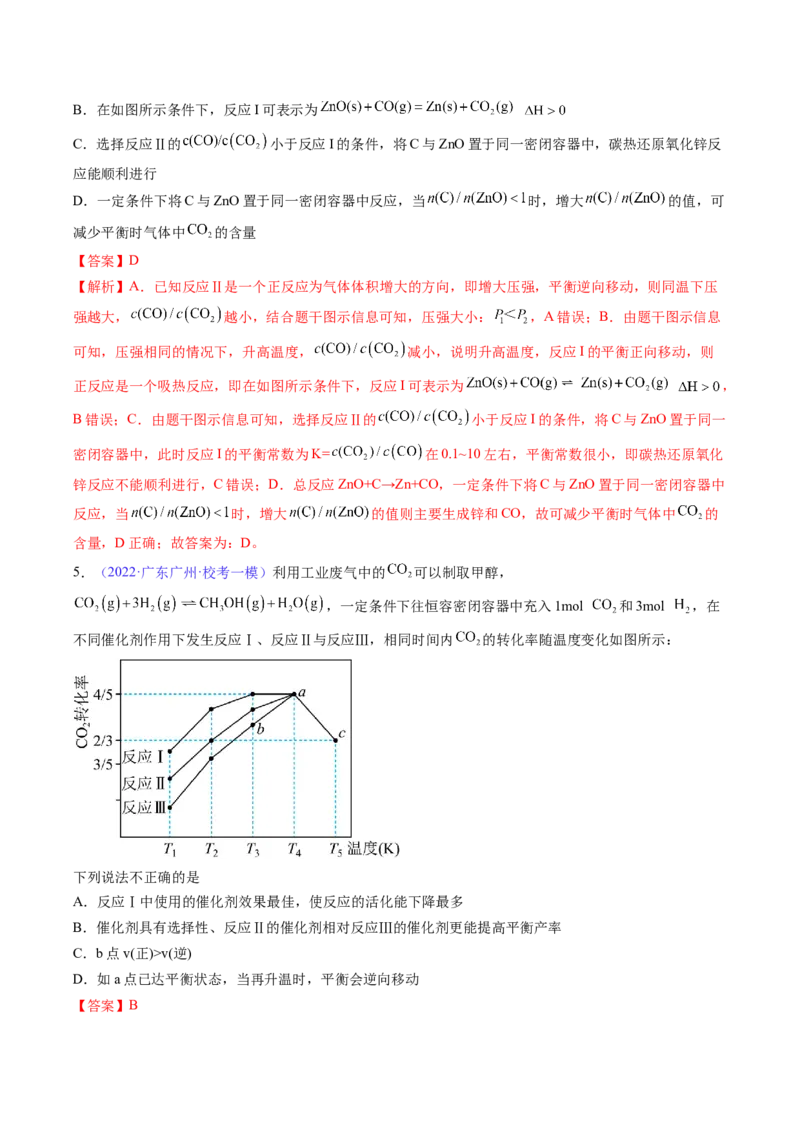
4.(2023·江苏南通·校考模拟预测)碳热还原氧化锌反应可用于循环制氢。碳热还原氧化锌的主要反应如
下:
反应I ;反应Ⅱ
在不同容器中分别发生反应I、反应Ⅱ,不同压强(P 或P)下分别达平衡时,两个反应中 随
1 2
温度变化的关系如图所示。下列说法正确的是
A.压强大小:B.在如图所示条件下,反应I可表示为
C.选择反应Ⅱ的 小于反应I的条件,将C与ZnO置于同一密闭容器中,碳热还原氧化锌反
应能顺利进行
D.一定条件下将C与ZnO置于同一密闭容器中反应,当 时,增大 的值,可
减少平衡时气体中 的含量
【答案】D
【解析】A.已知反应Ⅱ是一个正反应为气体体积增大的方向,即增大压强,平衡逆向移动,则同温下压
强越大, 越小,结合题干图示信息可知,压强大小: ,A错误;B.由题干图示信息
可知,压强相同的情况下,升高温度, 减小,说明升高温度,反应I的平衡正向移动,则
正反应是一个吸热反应,即在如图所示条件下,反应I可表示为 ,
B错误;C.由题干图示信息可知,选择反应Ⅱ的 小于反应I的条件,将C与ZnO置于同一
密闭容器中,此时反应I的平衡常数为K= 在0.1~10左右,平衡常数很小,即碳热还原氧化
锌反应不能顺利进行,C错误;D.总反应ZnO+C→Zn+CO,一定条件下将C与ZnO置于同一密闭容器中
反应,当 时,增大 的值则主要生成锌和CO,故可减少平衡时气体中 的
含量,D正确;故答案为:D。
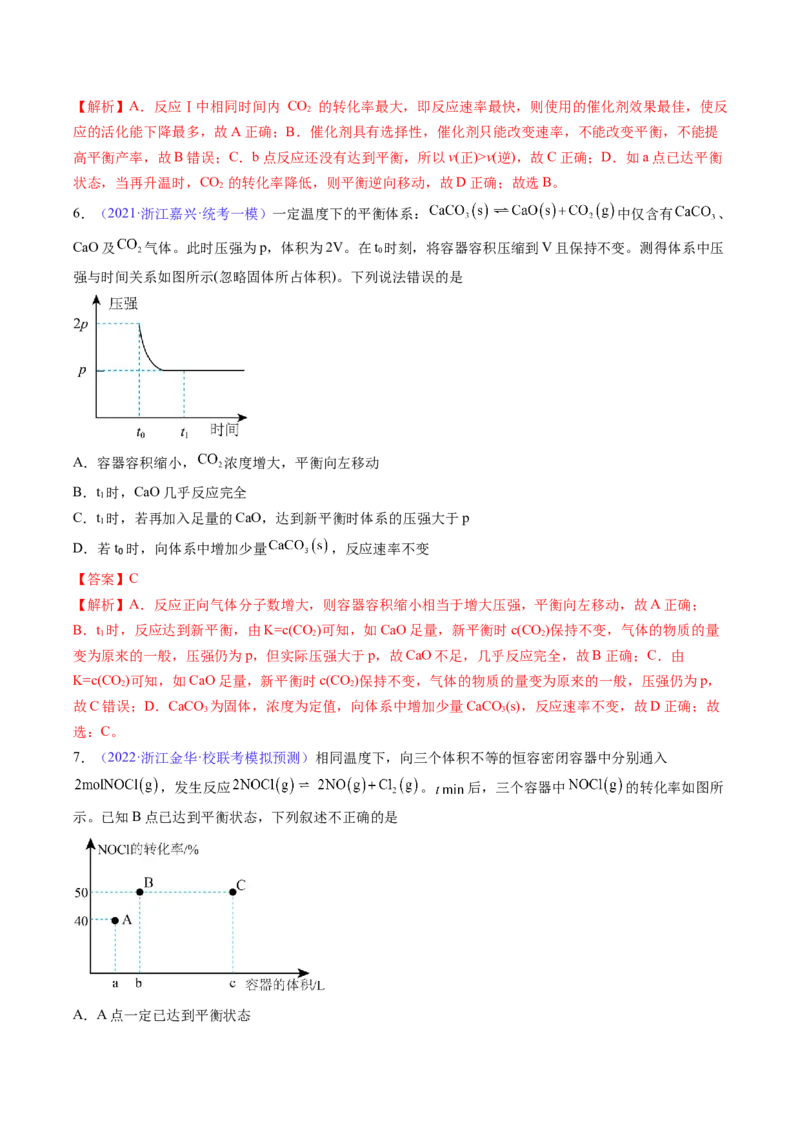
5.(2022·广东广州·校考一模)利用工业废气中的 可以制取甲醇,
,一定条件下往恒容密闭容器中充入1mol 和3mol ,在
不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内 的转化率随温度变化如图所示:
下列说法不正确的是
A.反应Ⅰ中使用的催化剂效果最佳,使反应的活化能下降最多
B.催化剂具有选择性、反应Ⅱ的催化剂相对反应Ⅲ的催化剂更能提高平衡产率
C.b点v(正)>v(逆)
D.如a点已达平衡状态,当再升温时,平衡会逆向移动
【答案】B【解析】A.反应Ⅰ中相同时间内 CO 的转化率最大,即反应速率最快,则使用的催化剂效果最佳,使反
2
应的活化能下降最多,故A正确;B.催化剂具有选择性,催化剂只能改变速率,不能改变平衡,不能提
高平衡产率,故B错误;C.b点反应还没有达到平衡,所以v(正)>v(逆),故C正确;D.如a点已达平衡
状态,当再升温时,CO 的转化率降低,则平衡逆向移动,故D正确;故选B。
2
6.(2021·浙江嘉兴·统考一模)一定温度下的平衡体系: 中仅含有 、
CaO及 气体。此时压强为p,体积为2V。在t 时刻,将容器容积压缩到V且保持不变。测得体系中压
0
强与时间关系如图所示(忽略固体所占体积)。下列说法错误的是
A.容器容积缩小, 浓度增大,平衡向左移动
B.t 时,CaO几乎反应完全
1
C.t 时,若再加入足量的CaO,达到新平衡时体系的压强大于p
1
D.若t₀时,向体系中增加少量 ,反应速率不变
【答案】C
【解析】A.反应正向气体分子数增大,则容器容积缩小相当于增大压强,平衡向左移动,故A正确;
B.t 时,反应达到新平衡,由K=c(CO)可知,如CaO足量,新平衡时c(CO)保持不变,气体的物质的量
1 2 2
变为原来的一般,压强仍为p,但实际压强大于p,故CaO不足,几乎反应完全,故B正确;C.由
K=c(CO)可知,如CaO足量,新平衡时c(CO)保持不变,气体的物质的量变为原来的一般,压强仍为p,
2 2
故C错误;D.CaCO 为固体,浓度为定值,向体系中增加少量CaCO (s),反应速率不变,故D正确;故
3 3
选:C。
7.(2022·浙江金华·校联考模拟预测)相同温度下,向三个体积不等的恒容密闭容器中分别通入
,发生反应 。 后,三个容器中 的转化率如图所
示。已知B点已达到平衡状态,下列叙述不正确的是
A.A点一定已达到平衡状态B.容器体积
C.B点对应容器中,再通入 和 ,平衡正向移动
D.当三个容器都达到平衡状态时,体积为 的容器中NOCl转化率最高
【答案】C
【解析】A.a容器体积小,压强大,反应速率比b容器快,B点已达到平衡状态,所以A点一定已达到平
衡状态,故A正确;B. A、B两点均达到平衡状态,
A点
B点
温度相同,平衡常数相等,所以 ;则 ,故B正确;C.B点
对应容器中,再通入 和 ,Q= =K,平衡不移动,故C错误;D.增
大容器体积,减小压强,平衡正向移动,NOCl转化率增大,当三个容器都达到平衡状态时,体积为 的
容器中NOCl转化率最高,故D正确;选C。
8.(2023·辽宁大连·大连八中校考模拟预测)工业上利用 和 制备 ,相关化学键的键能如
下表所示:
键
键能
745 436 462.8 413.4 351
已知:①温度为 时,
②实验测得: , , 、 为速率常数。
下列说法错误的是
A.反应
B. 时,密闭容器充入浓度均为1mol/L的 、 ,反应至平衡,则 体积分数为C. 时,
D.若温度为 时, ,则
【答案】D
【解析】A.焓变=反应物总键能-生成物总键能,反应
,故A正确;B. 时,密闭容器充入浓
度均为1mol/L的 、 ,反应至平衡,
,x=0.5,则 体积分数 ,故B正确;C. 时, ,反应达到平
衡 = , ,故C正确;D.正反应放热,
升高温度平衡常数减小,若温度为 时, ,则 ,即平衡常数增大,则 ,
故D错误;选D。
9.(2023·浙江·浙江省杭州第二中学校联考二模)已知 在瞬间即可达成化学平
衡。NO 和NO 混合气体体积由V压缩至 时,相关数据变化如下表。根据表中数据得出若干结论,下
2 2 4
列结论不正确的是
温度/L 气体的总压强/Pa NO 的物质的量浓度/ mol·L-1
2
298 1.28×10-2
311 2.80×10-2
A.体积由V压缩至 时,NO 的物质的量减少
2
B.正反应和逆反应的活化能均较低
C.体积缩小后混合气体的颜色加深
D.其它条件不变,温度升高,该反应正向移动
【答案】A
【解析】A.体积为VL时,NO 的物质的量为1.28×10-2mol/L×VL=1.28×10-2Vmol,体积为 时,NO 的物
2 2质的量为2.80×10-2mol/L× L=1.40×10-2Vmol,NO 的物质的量增大,A不正确;B.由于该反应在瞬间即
2
可达成化学平衡,所以正反应和逆反应的活化能均较低,B正确;C.体积缩小后,NO 的浓度增大,则混
2
合气体的颜色加深,C正确;D.由于该反应为吸热反应,则其它条件不变,温度升高,该反应正向移动,
D正确;故选A。
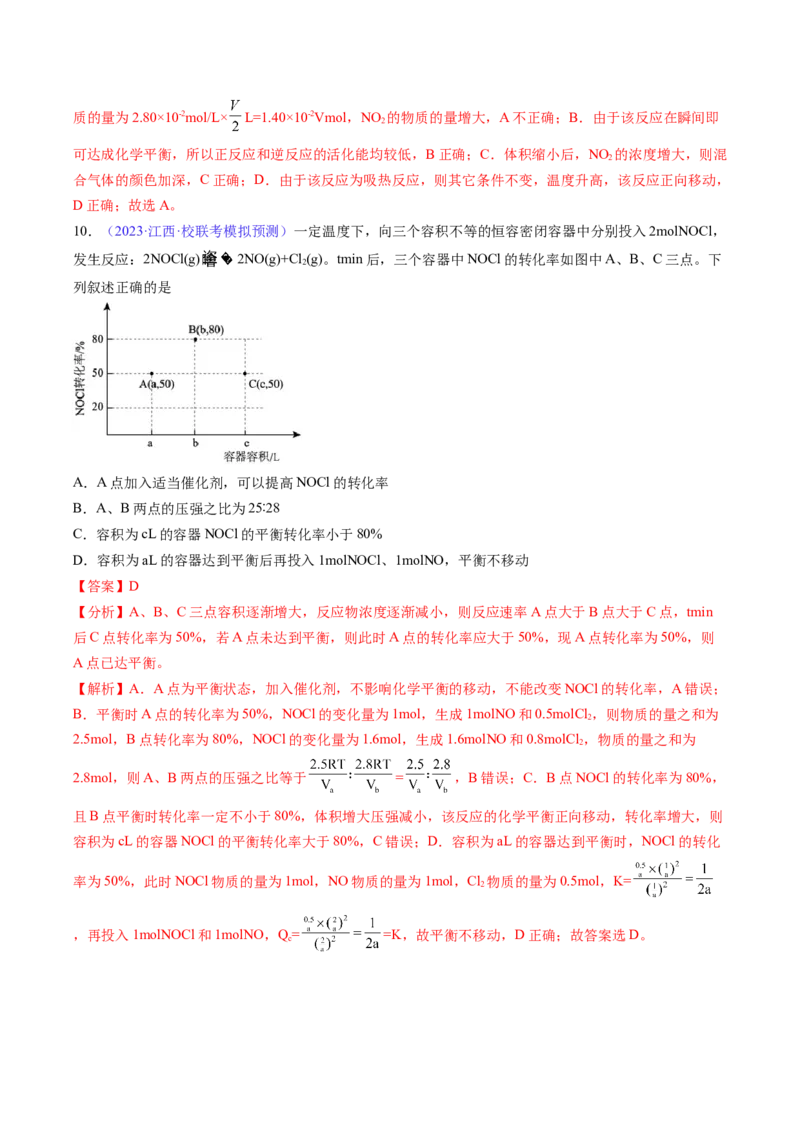
10.(2023·江西·校联考模拟预测)一定温度下,向三个容积不等的恒容密闭容器中分别投入2molNOCl,
发生反应:2NOCl(g) 2NO(g)+Cl (g)。tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下
2
列叙述正确的是
A.A点加入适当催化剂,可以提高NOCl的转化率
B.A、B两点的压强之比为25∶28
C.容积为cL的容器NOCl的平衡转化率小于80%
D.容积为aL的容器达到平衡后再投入1molNOCl、1molNO,平衡不移动
【答案】D
【分析】A、B、C三点容积逐渐增大,反应物浓度逐渐减小,则反应速率A点大于B点大于C点,tmin
后C点转化率为50%,若A点未达到平衡,则此时A点的转化率应大于50%,现A点转化率为50%,则
A点已达平衡。
【解析】A.A点为平衡状态,加入催化剂,不影响化学平衡的移动,不能改变NOCl的转化率,A错误;
B.平衡时A点的转化率为50%,NOCl的变化量为1mol,生成1molNO和0.5molCl ,则物质的量之和为
2
2.5mol,B点转化率为80%,NOCl的变化量为1.6mol,生成1.6molNO和0.8molCl ,物质的量之和为
2
2.8mol,则A、B两点的压强之比等于 = ,B错误;C.B点NOCl的转化率为80%,
且B点平衡时转化率一定不小于80%,体积增大压强减小,该反应的化学平衡正向移动,转化率增大,则
容积为cL的容器NOCl的平衡转化率大于80%,C错误;D.容积为aL的容器达到平衡时,NOCl的转化
率为50%,此时NOCl物质的量为1mol,NO物质的量为1mol,Cl 物质的量为0.5mol,K=
2
,再投入1molNOCl和1molNO,Q= =K,故平衡不移动,D正确;故答案选D。
c