文档内容
合格演练测评(二)
(化学计量在实验中的应用)
姓名: 班级: 正确率:
题号 1 2 3 4 5 6 7 8 9 10
答案
题号 11 12 13 14 15 16 17 18 19 20
答案
一、单项选择题
1.物质的量的单位是( )
A.mol B.g·mol-1
C.mol·L-1 D.mol·L-1·s-1
解析:物质的量的单位是mol,答案选A。
答案:A
2.标准状况下,64 g O 所占体积约为( )
2
A.44.8 L B.22.4 L
C.11.2 L D.5.6 L
解析:标准状况下,62 g O 的物质的量是64 g÷32 g·mol-1=2 mol,所占体积约为2 mol×22.4
2
L·mol-1=44.8 L,答案选A。
答案:A
3.CaCO 的摩尔质量为100 g·mol-1。将5.0 g CaCO 固体完全溶于稀盐酸后,再用蒸馏水稀释成100
3 3
mL溶液。该溶液中Ca2+的物质的量浓度为( )
A.5.0 mol·L-1 B.0.10 mol·L-1
C.1.0 mol·L-1 D.0.50 mol·L-1
解析:n(CaCO)=5.0 g÷100 g·mol-1=0.05 mol,碳酸钙和稀盐酸反应方程式为 CaCO +
3 3
2HCl===CaCl+HO+CO↑,根据钙原子守恒得n(CaCO)=n(Ca2+)=0.05 mol,钙离子的物质的量浓度c=
2 2 2 3
n÷V=0.05 mol÷0.1 L=0.50 mol·L-1。答案:D
4.标准状况下,32 g CH 所占体积约为( )
4
A.44.8 L B.22.4 L
C.11.2 L D.5.6 L
解析:标准状况下,32 g CH 的物质的量是32 g÷16 g·mol-1=2 mol,所占体积约为2 mol×22.4
4
L·mol-1=44.8 L,答案选A。
答案:A
5.22.4 L CH 气体中含有的分子数为( )
4
A.6.02×1023 B.44.8
C.3.01×1023 D.22.4
解析:标准状况下,22.4 L CH 气体的物质的量是22.4 L÷22.4 L·mol-1=1 mol,其中含有的分子
4
数为6.02×1023,A正确。
答案:A
6.精确配制250 mL一定物质的量浓度的NaOH溶液,下列实验操作正确的是( )
A.选择仪器时,使用500 mL容量瓶
B.将称量好的氢氧化钠固体放入容量瓶中,加入少量水溶解
C.在烧杯中溶解氢氧化钠后,立即将所得溶液注入容量瓶中
D.将烧杯中的氢氧化钠溶液注入未经干燥的洁净容量瓶中
解析:A项,应选用250 mL容量瓶。B项,容量瓶不能用作溶解的仪器,应在烧杯中溶解。C项,应将溶
解NaOH后的溶液恢复到室温后再向容量瓶中转移。D项,容量瓶未干燥对所配溶液浓度无影响,正确。
答案:D
7.实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl
的质量分别是( )
A.950 mL,111.2 g B.500 mL,117 g
C.1 000 mL,117 g D.任意规格,111.2 g
解析:没有950 mL的容量瓶,只能选1 000 mL的容量瓶,含NaCl 2 mol,质量为117 g。
答案:C8.用N 表示阿伏加德罗常数的值,下列说法错误的是( )
A
A.标准状况下,22.4 L H 中含有氢分子的个数为2N
2 A
B.24 g Mg变为Mg2+时失去的电子数为2N
A
C.常温常压下,32 g O 和O 的混合气体中含有氧原子的个数为2N
2 3 A
D.1 L 1 mol·L-1 NaCl溶液中含有钠离子的个数为N
A
答案:A
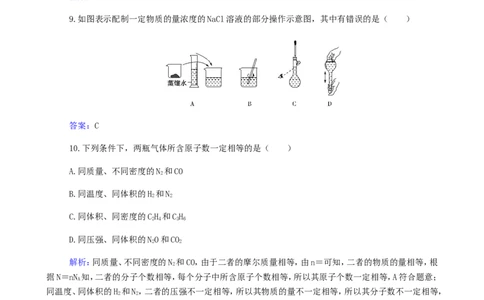
9.如图表示配制一定物质的量浓度的NaCl溶液的部分操作示意图,其中有错误的是( )
答案:C
10.下列条件下,两瓶气体所含原子数一定相等的是( )
A.同质量、不同密度的N 和CO
2
B.同温度、同体积的H 和N
2 2
C.同体积、同密度的CH 和CH
2 4 3 6
D.同压强、同体积的NO和CO
2 2
解析:同质量、不同密度的N 和CO,由于二者的摩尔质量相等,由n=可知,二者的物质的量相等,根
2
据N=nN 知,二者的分子个数相等,每个分子中所含原子个数相等,所以其原子个数一定相等,A符合题意;
A
同温度、同体积的H 和N,二者的压强不一定相等,所以其物质的量不一定相等,所以其分子数不一定相等,
2 2
则其原子个数不一定相等,B不符合题意;同体积、同密度的CH 和CH,二者的质量相等,但二者的摩尔质
2 4 3 6
量不相等,所以其物质的量不等,每个分子中所含原子个数不相等,所以其原子个数一定不相等,C不符合
题意;同压强、同体积的NO和CO,由于温度未知,所以无法判断两者的物质的量大小,D不符合题意。
2 2
答案:A
11.有一种气体的质量是14.2 g,体积是4.48 L(标准状况),该气体的摩尔质量是( )
A.28.4 B.28.4 g·mol-1
C.71 D.71 g·mol-1答案:D
12.下列叙述正确的是( )
A.1 mol任何气体的体积一定是22.4 L
B.同温、同压下两种气体分子数相同,则它们所占体积也相同
C.在标准状况下,体积为22.4 L的任何物质都是1 mol
D.在非标准状况下,1 mol任何气体的体积不可能为22.4 L
解析:气体摩尔体积的大小与外界条件(温度、压强)有关,A错误;气体摩尔体积概念的适用范围是气
体,C错误;在非标准状况下,气体摩尔体积也有可能是22.4 L·mol-1,D错误。
答案:B
13.下列有关1 mol NaOH的说法中,正确的是( )
A.NaOH的摩尔质量为40 g
B.1 mol NaOH 的质量为40 g·mol-1
C.标准状况下,1 mol NaOH 所占的体积为22.4 L
D.将1 mol NaOH溶于水配成100 mL溶液,则溶液中溶质的物质的量浓度为10 mol·L-1
答案:D
14.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.16 g氧气含有0.5N 个氧原子
A
B.22.4 L氧气含有N 个氧分子
A
C.标准状况下,22.4 L水中含有N 个水分子
A
D.N 个氮分子的质量为28 g
A
答案:D
15.下列各组物质中,所含氯原子(包含氯离子)个数最多的是( )
A.448 mL(标准状况)Cl
2
B.0.5 mol HCl
C.13.35 g AlCl
3D.1 L 0.5 mol·L-1 MgCl 溶液
2
答案:D
16.下列说法正确的是(N 表示阿伏加德罗常数的值)( )
A
A.在常温、常压下,11.2 L CH 含有的分子数为0.5N
4 A
B.常温、常压下,0.5 mol氦气含有的原子数为N
A
C.32 g氧气所含电子数目为16N
A
D.同温同压下,相同体积的任何气体单质所含的原子数目都为N
A
解析:A中,标准状况下才合理,错;B中,0.5 mol He含原子数为0.5N,错;C中,32 g O 为1 mol,有
A 2
2 mol O原子,O原子核外电子数为8,所以32 g O 含有电子数为2×8 mol=16 mol,即16N,对;D中,不
2 A
同气体单质所含原子数不一定相同,错。
答案:C
17.将0.1 mol NaOH固体溶解在100 mL水中,再稀释成1 L,所得溶液的物质的量浓度是( )
A.0.01 mol·L-1 B.0.1 mol·L-1
C.1 mol·L-1 D.10 mol·L-1
答案:B
18.已知6.02×1023个X气体分子的质量为64 g,则X气体的摩尔质量是( )
A.16 g B.32 g
C.64 g·mol-1 D.32 g·mol-1
解析:本题考查以物质的量为中心的有关物理量的换算。因n=,6.02×1023个X气体分子的物质的量
为1 mol;又因n=,M===64 g·mol-1。
答案:C
19.下列溶液中的Cl-浓度与100 mL 1 mol·L-1 MgCl 溶液中的Cl-浓度相等的是( )
2
A.150 mL 1 mol·L-1 NaCl溶液
B.75 mL 0.5 mol·L-1 CaCl 溶液
2
C.150 mL 2 mol·L-1 KCl溶液
D.75 mL 1 mol·L-1 AlCl 溶液
3解析:物质的量浓度与体积无关,100 mL 1 mol·L-1MgCl 溶液中的Cl-浓度为2 mol·L-1。
2
答案:C
20.关于1.5 mol NH 的说法错误的是( )
3
A.在标准状况下体积约为33.6 L
B.所含的分子数目约为9.03×1023
C.摩尔质量为17 g·mol-1
D.溶于水制成0.5 L溶液时物质的量浓度为1.5 mol·L-1
解析:NH 溶于水会生成NH·HO,若NH 溶于水不考虑化学反应,c(NH)=1.5 mol÷0.5 L=3
3 3 2 3 3
mol·L-1,故D错误。
答案:D
二、非选择题
21.标准状况下,1.7 g NH 和 L HS含有相同的氢原子数。
3 2
答案:3.36
22.2 mol SO 和3 mol SO 其分子数之比为 ;相同状况下(均为气体)体积之比为
3 2
;氧原子数之比为 。
答案:2∶3 2∶3 1∶1
23.欲用98%的浓硫酸(ρ=1.84 g·cm-3)配制浓度为0.25 mol·L-1的稀硫酸1 000 mL。请回答下
列问题:
(1)所需浓硫酸的体积约为 mL。
(2)如果实验室有15 mL、20 mL、50 mL的量筒,应选用 mL的量筒。
( 3 ) 将 浓 硫 酸 沿 烧 杯 内 壁 慢 慢 注 入 盛 水 的 烧 杯 中 , 并 不 断 搅 拌 的 目 的 是
________________________________________________,
若搅拌过程中有液体溅出,会使浓度 (填“偏高”“偏低”或“无影响”)。
(4)烧杯中液体在转入容量瓶前应 ;洗涤烧杯和玻璃棒2~3次,洗涤液也要转入容
量瓶,否则会使浓度 (填“偏高”“偏低”或“无影响”)。
(5)定容时必须使溶液凹液面的最低处与刻度线相切,若俯视会使浓度 (填“偏高”“偏
低”或“无影响”,下同);仰视则使浓度 。答案:(1)13.6 (2)15 (3)迅速散热,防止液体飞溅 偏低 (4)冷却至室温 偏低
(5)偏高 偏低