文档内容
专题七 有机化合物结构和性质
必备知识 解读
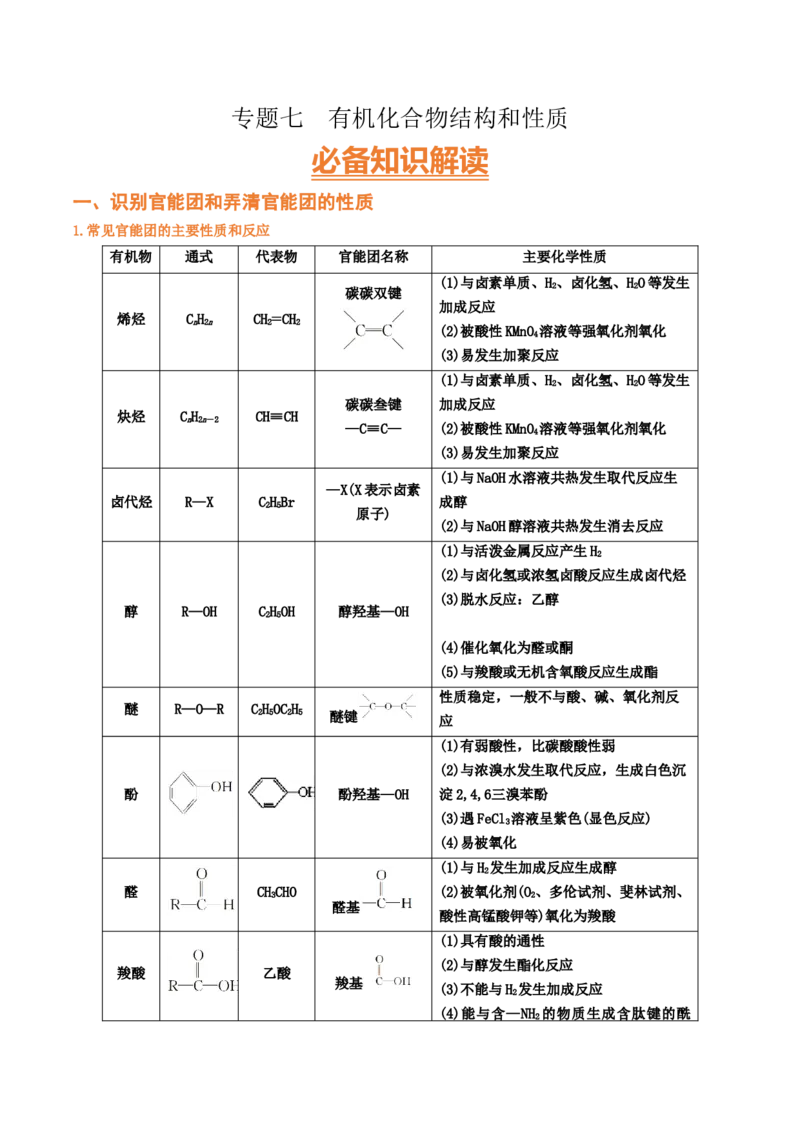
一、识别官能团和弄清官能团的性质
1.常见官能团的主要性质和反应
有机物 通式 代表物 官能团名称 主要化学性质
(1)与卤素单质、H、卤化氢、HO等发生
2 2
碳碳双键
加成反应
烯烃 CH CH=CH
n 2n 2 2
(2)被酸性KMnO 溶液等强氧化剂氧化
4
(3)易发生加聚反应
(1)与卤素单质、H、卤化氢、HO等发生
2 2
碳碳叁键 加成反应
炔烃 CH CH≡CH
n 2n-2
—C≡C— (2)被酸性KMnO 溶液等强氧化剂氧化
4
(3)易发生加聚反应
(1)与NaOH水溶液共热发生取代反应生
—X(X表示卤素
卤代烃 R—X CHBr 成醇
2 5
原子)
(2)与NaOH醇溶液共热发生消去反应
(1)与活泼金属反应产生H
2
(2)与卤化氢或浓氢卤酸反应生成卤代烃
(3)脱水反应:乙醇
醇 R—OH CHOH 醇羟基—OH
2 5
(4)催化氧化为醛或酮
(5)与羧酸或无机含氧酸反应生成酯
性质稳定,一般不与酸、碱、氧化剂反
醚 R—O—R CHOCH
2 5 2 5 醚键
应
(1)有弱酸性,比碳酸酸性弱
(2)与浓溴水发生取代反应,生成白色沉
酚 酚羟基—OH 淀2,4,6三溴苯酚
(3)遇FeCl 溶液呈紫色(显色反应)
3
(4)易被氧化
(1)与H 发生加成反应生成醇
2
醛 CHCHO (2)被氧化剂(O、多伦试剂、斐林试剂、
3 2
醛基
酸性高锰酸钾等)氧化为羧酸
(1)具有酸的通性
(2)与醇发生酯化反应
羧酸 乙酸
羧基
(3)不能与H 发生加成反应
2
(4)能与含—NH 的物质生成含肽键的酰
2胺
(5)与羧基脱水形成酸酐
(1)发生水解反应生成羧酸和醇
酯 乙酸乙酯
酯基 (2)可发生醇解反应生成新酯和新醇
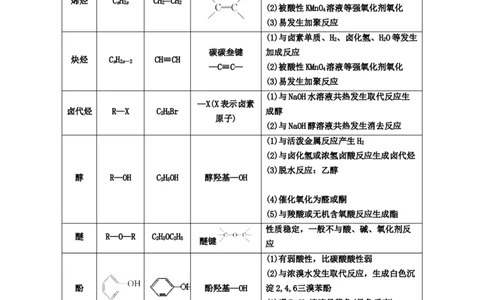
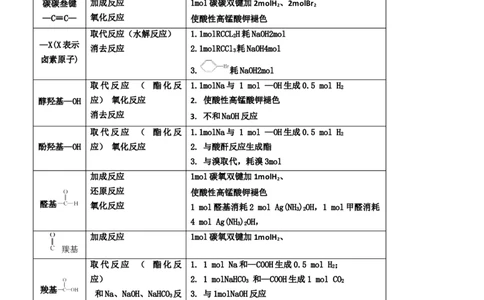
2、重要官能团的反应类型
官能团 反应类型 反应说明
碳碳双键 加成反应 1mol碳碳双键加1molH 、1molBr
2 2
氧化反应 使酸性高锰酸钾褪色
碳碳叁键 加成反应 1mol碳碳双键加2molH 、2molBr
2 2
—C≡C— 氧化反应 使酸性高锰酸钾褪色
取代反应(水解反应) 1.1molRCCLH耗NaOH2mol
2
—X(X表示
消去反应 2.1molRCCl 耗NaOH4mol
3
卤素原子)
3. 耗NaOH2mol
取代反应 ( 酯化反 1.1molNa与 1 mol —OH生成0.5 mol H
2
醇羟基—OH 应) 氧化反应 2. 使酸性高锰酸钾褪色
消去反应 3. 不和NaOH反应
取代反应 ( 酯化反 1.1molNa与 1 mol —OH生成0.5 mol H
2
酚羟基—OH 应) 氧化反应 2. 与酸酐反应生成酯
3. 与溴取代,耗溴3mol
加成反应 1mol碳氧双键加1molH 、
2
还原反应 使酸性高锰酸钾褪色
醛基 氧化反应 1 mol醛基消耗2 mol Ag(NH)OH,1 mol甲醛消耗
3 2
4 mol Ag(NH)OH,
3 2
加成反应 1mol碳氧双键加1molH 、
2
羰基
取代反应 ( 酯化反 1. 1 mol Na和—COOH生成0.5 mol H;
2
应) 2. 1 molNaHCO 和—COOH生成1 mol CO
3 2
羧基
和Na、NaOH、NaHCO 反 3. 与1molNaOH反应
3
应
酯基 取代反应 ( 水解反 1mol酯耗1molNaOH
应)
1mol 耗2molNaOH
和NaOH反应
二、空间构型、核磁共振氢谱锋的面积和手性碳原子个数
1.空间构型:
碳原子 共线点 共面点2点共线,3点以上不共线 3点共面,4点以上不共面
饱和碳原子
碳碳双键 2点共线,3点以上不共线 6点共面
碳碳三键—C≡C— 4点共线 4点共面
4点共线 12点共面
苯环
3点不共线 3点共面
2.核磁共振氢谱:
核磁共振氢谱锋的面积面积比:一般是:3或3的倍数,2或2的倍数,1或1的倍数。
3.手性碳原子个数:手性碳原子是不对称碳原子,碳原子上连接的四个原子或原子团都不相同。
应考能力 解 密
一.判断同分异构种数
1.巧用不饱和度记住常见有机物的官能团异构
1、不饱和度
(1)概念:不饱和度又称缺氢指数,即有机物分子中的氢原子与和它碳原子数相等的链状烷烃相比较,每
减少2个氢原子,则有机物的不饱和度增加1,用Ω表示
(2)有机化合物(CHO)分子不饱和度的计算公式为:
x y z
(3)在计算不饱和度时,若有机化合物分子中含有卤素原子,可将其视为氢原子;若含有氧原子,则不予
考虑;若含有氮原子,就在氢原子总数中加上氮原子数
(4)几种常见结构的不饱和度
官能团或结构 C==C C==O 环 C C 苯环
不饱和度 1 1 1 2 4
常见有机物的官能团异构
通式 不饱和度 常见类别异构体
CH 0 无类别异构体
n 2n+2
碳碳双键CH 1 单烯烃、环烷烃
n 2n
碳碳三键CH 2 单炔烃、二烯烃、环烯烃、二环烃
n 2n-2
羟基醚键CH
n 2n+ 0 饱和一元醇、饱和一元醚
O
2饱和一元醛、饱和一元酮、烯醇、烯醚、环醇、环
醛酮CH O 1
n 2n
醚
羧 酸CH O 1 饱和一元羧酸、饱和一元酯、羟醛、羟酮
n 2n 2
CH ON 1 氨基酸、硝基烷
n 2n+1 2
苯CH 4 含苯环
n 2n-6
(5)不饱和度相同、碳、氧原子数相同、杂原子数相同的物质是同分异构体。
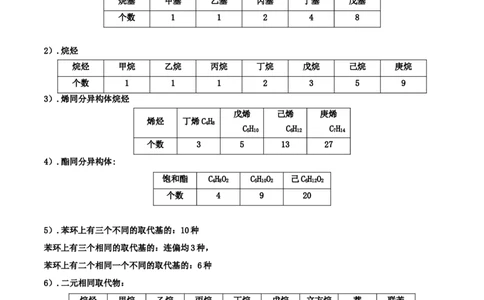
2.记住常见同分异构体的数目
1).烷基
烷基 甲基 乙基 丙基 丁基 戊基
个数 1 1 2 4 8
2).烷烃
烷烃 甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷
个数 1 1 1 2 3 5 9
3).烯同分异构体烷烃
戊烯 己烯 庚烯
烯烃 丁烯CH
4 8
CH CH CH
5 10 6 12 7 14
个数 3 5 13 27
4).酯同分异构体:
饱和酯 CHO CH O 己CH O
4 8 2 5 10 2 6 12 2
个数 4 9 20
5).苯环上有三个不同的取代基的:10种
苯环上有三个相同的取代基的:连偏均3种,
苯环上有二个相同一个不同的取代基的:6种
6).二元相同取代物:
烷烃 甲烷 乙烷 丙烷 丁烷 戊烷 立方烷 萘 联苯
个数 1 2 4 9 21 3 10 12
7).二元不同的取代基:
烷烃 甲烷 乙烷 丙烷 丁烷 戊烷 立方烷 萘 联苯
个数 1 2 5 12 31 3 14 21
二、记准几个定量关系
1.1 mol醛基消耗2 mol Ag(NH)OH生成2 mol Ag单质、1 mol HO、3 mol NH;1 mol甲醛消耗4 mol
3 2 2 3
Ag(NH)OH,生成4 mol Ag单质、
3 2
2.1 mol醛基消耗2 mol Cu(OH) 生成1 mol CuO沉淀、2 mol HO;1 mol甲醛消耗4 mol Cu(OH),生成
2 2 2 22 mol CuO沉淀
2
3.消耗H 的物质的量
2
官能团 —C≡C—
耗H 1 2 3 1 0 0 0
2
4.消耗NaOH的物质的量
1)1mol单醇、酚、酸、酯耗NaOH1mol
2)1mol 、 耗NaOH2mol
3)1molRCCLH耗NaOH2mol
2
4) 1molRCCl 耗NaOH4mol
3
5.消耗Br 的物质的量
2
官能团 —C≡C—
反应类型 加成 加成 取代反应 取代反应
耗Br 1 2 邻、对位3 对位被占,邻2
2
三、有机物的溶解性和熔沸点的比较
1.常温下含有 小于或等于 4 个 碳原子的烃为气态,随碳原子数的增多,逐渐过渡到液态、固态
2.烷烃随碳原子数的增多,分子量增大,沸点逐渐升高;同分异构体中,支链越多,沸点越低
3.羧酸、醇、胺类、胺基酸等有机物分子间可以形成氢键,熔沸点比同碳其它有机物高
4.羧酸、醇、胺类、胺基酸等有机物与水分子间可以形成氢键,比同碳其它有机物易溶于水
5.含有-OH、-CHO、-COOH、-NH 等亲水基的有机物,含碳少的化合物易溶于水,随着碳原子数增多,溶解
2
度变小。
6.含X-、R-、R-COO-R等憎水基的都不溶于水。
高考实例剖析
高频考点 1 分子组成 和结构
1. 分子式的正误判断
2. 分子中共面、共线原子和手性碳原子的判断
3. 同分异构体、同系物的判断
4. 一氯代物种数判断
【高考实例】
1.(2022·全国乙卷)一种实现二氧化碳固定及再利用的反应如下:下列叙述正确的是
A.化合物1分子中的所有原子共平面 B.化合物1与乙醇互为同系物
C.化合物2分子中含有羟基和酯基 D.化合物2可以发生开环聚合反应
【答案】D
【解析】A项:化合物1分子中还有亚甲基结构,其中心碳原子采用sp3杂化方式,所以所有原子不可能共
平面,A错误;
B项:结构相似,分子上相差n个CH 的有机物互为同系物,上述化合物1为环氧乙烷,属于醚类,乙醇属
2
于醇类,与乙醇结构不相似,不是同系物,B错误;
C项:根据上述化合物2的分子结构可知,分子中含酯基,不含羟基,C错误;
D项:化合物2分子可发生开环聚合形成高分子化合物 ,D正确;
答案选D。
【考点演练】
1.(2022·全国甲卷)辅酶 具有预防动脉硬化的功效,其结构简式如下。下列有关辅酶 的说法正确
的是
A.分子式为
B.分子中含有14个甲基
C.分子中的四个氧原子不在同一平面
D.可发生加成反应,不能发生取代反应
【答案】B【解析】A项:由该物质的结构简式可知,其分子式为C H O ,A错误;
59 90 4
B项:由该物质的结构简式可知,键线式端点代表甲基,10个重复基团的最后一个连接H原子的碳是甲基,
故分子中含有1+1+1+10+1=14个甲基,B正确;
C项:双键碳以及与其相连的四个原子共面,羰基碳采取sp2杂化,羰基碳原子和与其相连的氧原子及另外
两个原子共面,因此分子中的四个氧原子在同一平面上,C错误;
D项:分子中有碳碳双键,能发生加成反应,分子中含有甲基,能发生取代反应,D错误;
答案选B。
2.(2022·河南商丘·三模)长时间看电子显示屏幕,会对眼睛有一定的伤害。人眼的视色素中含有视黄醛,
而与视黄醛结构相似的维生素A常作为保健药物。下列有关叙述正确的是
A.视黄醛的分子式为C H O
20 26
B.视黄醛与乙醛(CH CHO)互为同系物
3
C.一定条件下,维生素A可被氧化生成视黄醛
D.视黄醛和维生素A互为同分异构体
【答案】C
【解析】A项:由结构简式可知,视黄醛的分子式为C H O,故A错误;
20 28
B项:由结构简式可知,视黄醛分子与乙醛分子中含有的官能团种类不同,不是同类物质,所以不可能互
为同系物,故B错误;
C项:由结构简式可知,维生素A中含有—CH OH能被氧化转化为—CHO,则一定条件下,维生素A可被氧
2
化生成视黄醛,故C正确;
D项:由结构简式可知,视黄醛和维生素A的分子式不同,不可能互称同分异构体,故D错误;
故选C。
高频考点 2 有机物的分类官能团的反应
1. 有机物种类判断:何种有机物,有何种官能团,是否高分子
2. 与H 加成,耗多少mol
2
3. 与Br 反应,耗多少mol
2
4. 耗NaOH多少mol5. 耗NaHCO 多少mol
3
6. 能否使酸性高锰酸钾褪色
7. 与Na反应产生多少molH
2
8. 能发生的反应类型的判断:如取代,加成,消去、氧化等
【高考实例】
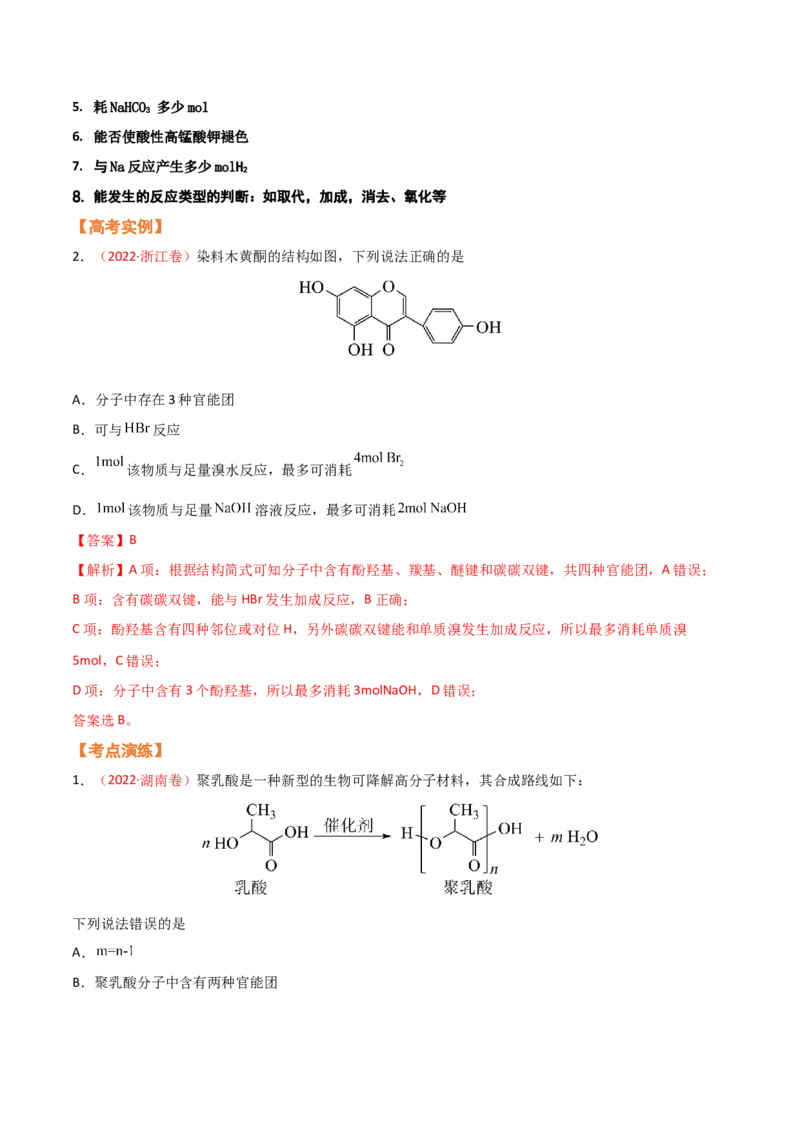
2.(2022·浙江卷)染料木黄酮的结构如图,下列说法正确的是
A.分子中存在3种官能团
B.可与 反应
C. 该物质与足量溴水反应,最多可消耗
D. 该物质与足量 溶液反应,最多可消耗
【答案】B
【解析】A项:根据结构简式可知分子中含有酚羟基、羰基、醚键和碳碳双键,共四种官能团,A错误;
B项:含有碳碳双键,能与HBr发生加成反应,B正确;
C项:酚羟基含有四种邻位或对位H,另外碳碳双键能和单质溴发生加成反应,所以最多消耗单质溴
5mol,C错误;
D项:分子中含有3个酚羟基,所以最多消耗3molNaOH,D错误;
答案选B。
【考点演练】
1.(2022·湖南卷)聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是
A.
B.聚乳酸分子中含有两种官能团C. 乳酸与足量的 反应生成
D.两分子乳酸反应能够生成含六元环的分子
【答案】B
【解析】A项:根据氧原子数目守恒可得:3n=2n+1+m,则m=n-1,A正确;
B项:聚乳酸分子中含有三种官能团,分别是羟基、羧基、酯基,B错误;
C项:1个乳酸分子中含有1个羟基和1个羧基,则1mol乳酸和足量的Na反应生成1mol H ,C正确;
2
D项:1个乳酸分子中含有1个羟基和1个羧基,则两分子乳酸可以缩合产生含六元环的分子(
),D正确;
故选B。
2.(2022·山西太原·二模)2021年诺贝尔化学奖授予Benjamin List、David W.C.MacMillan,以奖励他们
“对于有机小分子不对称催化的重要贡献”。脯氨酸( )催化分子内的羟醛缩合反应:
下列说法不正确的是
A.脯氨酸能与Y发生取代反应
B.X和Y互为同分异构体,且Y能发生消去反应
C.X中所有碳原子处于同一平面
D.1mol脯氨酸与足量NaHCO 反应,生成44gCO
3 2
【答案】C
【解析】A项:脯氨酸含有羧基,Y中含有羟基,两者能发生酯化反应(取代反应),故A正确;
B项:X和Y分子式相同,结构不同,互为同分异构体,Y分子中羟基的邻位碳原子上含有氢原子,能发生消去反应,故B正确;
C项:如图所示 ,X中用“*”标记的碳原子为饱和碳原子,与之相连的碳原子不可能处于
同一平面,因此X中所有碳原子不可能共面,故C错误;
D项:1mol脯氨酸含有1mol羧基,与足量NaHCO 反应,生成1molCO ,质量为1mol×44g/mol=44g,故D
3 2
正确;
答案选C。