文档内容
多平衡体系中的规范解答题(A)
1.(8分)精脱硫技术主要用于煤气中羰基硫(COS)和二硫化碳(CS )的转化。回答下列问题:
2
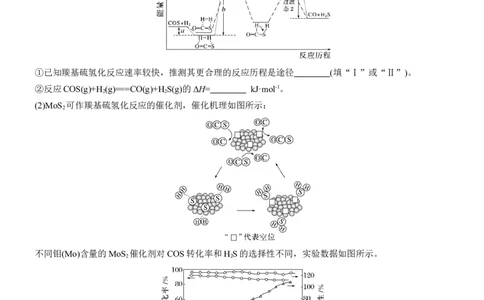
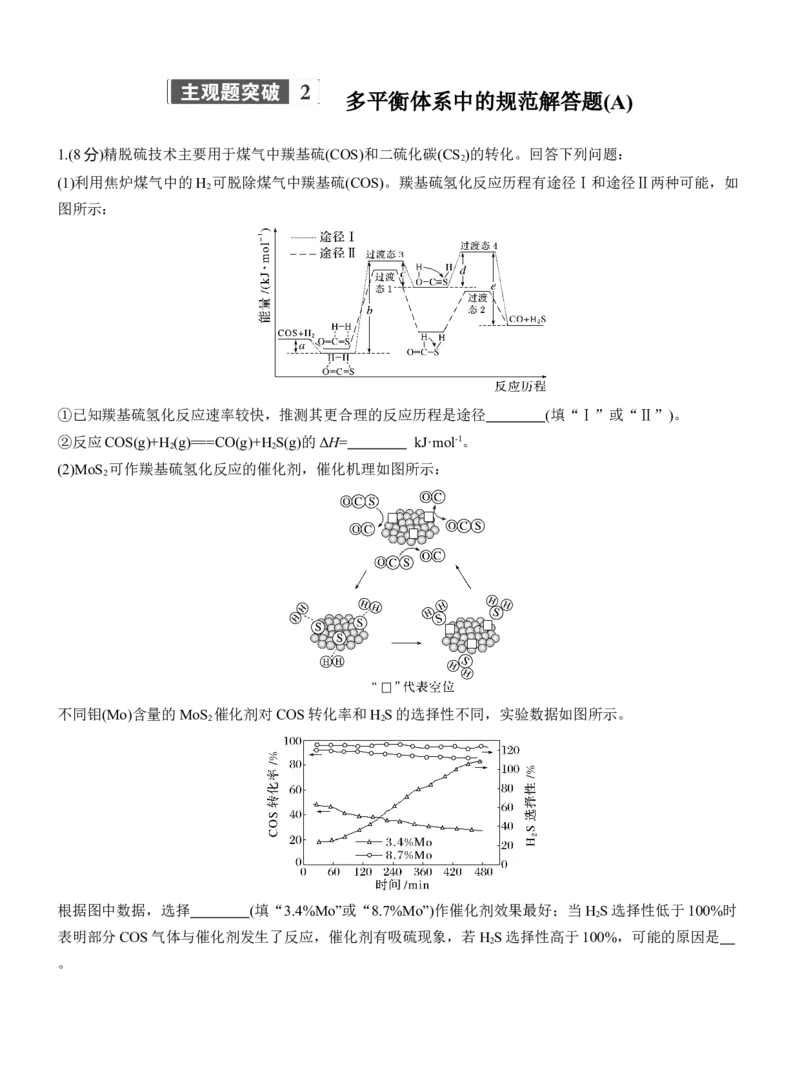
(1)利用焦炉煤气中的H 可脱除煤气中羰基硫(COS)。羰基硫氢化反应历程有途径Ⅰ和途径Ⅱ两种可能,如
2
图所示:
①已知羰基硫氢化反应速率较快,推测其更合理的反应历程是途径 (填“Ⅰ”或“Ⅱ”)。
②反应COS(g)+H (g)===CO(g)+H S(g)的ΔH= kJ·mol-1。
2 2
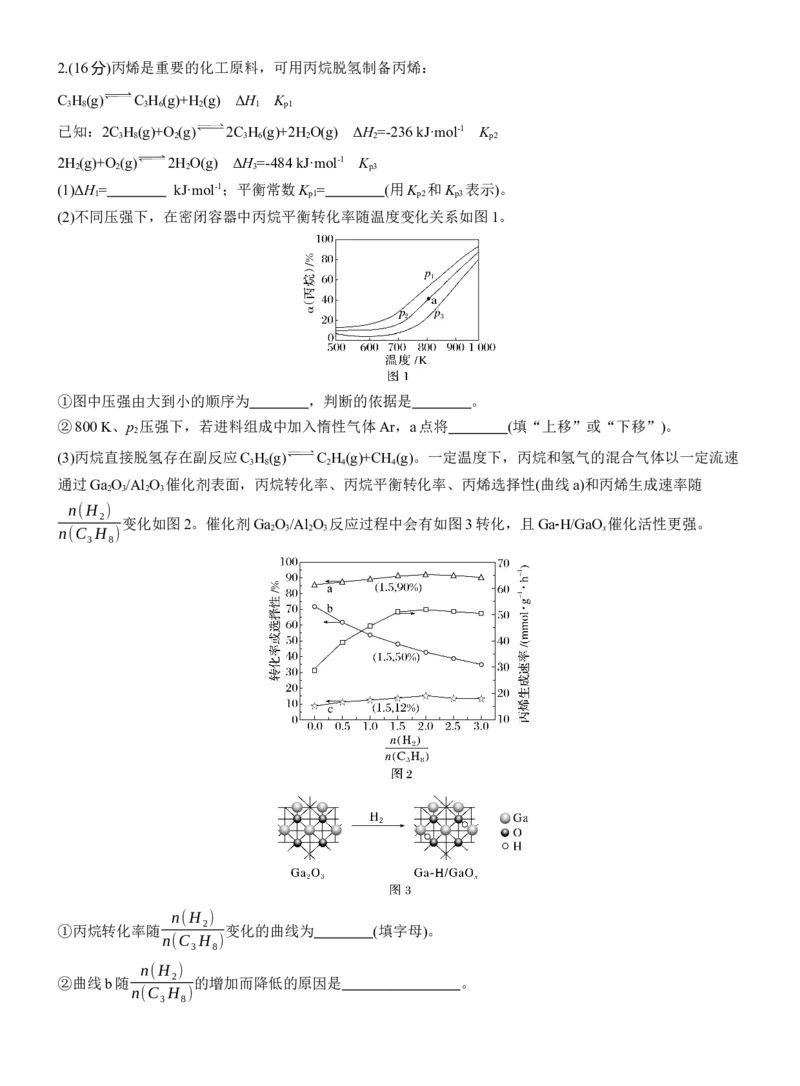
(2)MoS 可作羰基硫氢化反应的催化剂,催化机理如图所示:
2
不同钼(Mo)含量的MoS 催化剂对COS转化率和H S的选择性不同,实验数据如图所示。
2 2
根据图中数据,选择 (填“3.4%Mo”或“8.7%Mo”)作催化剂效果最好;当H S选择性低于100%时
2
表明部分COS气体与催化剂发生了反应,催化剂有吸硫现象,若H S选择性高于100%,可能的原因是
2
。2.(16分)丙烯是重要的化工原料,可用丙烷脱氢制备丙烯:
C H (g) C H (g)+H (g) ΔH K
3 8 3 6 2 1 p1
已知:2C H (g)+O (g) 2C H (g)+2H O(g) ΔH =-236 kJ·mol-1 K
3 8 2 3 6 2 2 p2
2H (g)+O (g) 2H O(g) ΔH =-484 kJ·mol-1 K
2 2 2 3 p3
(1)ΔH = kJ·mol-1;平衡常数K = (用K 和K 表示)。
1 p1 p2 p3
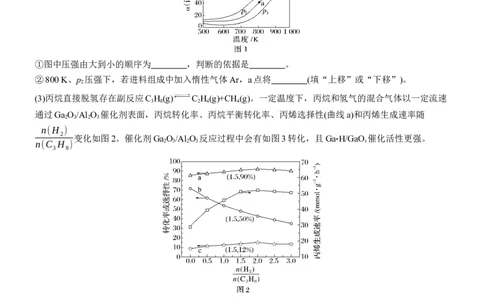
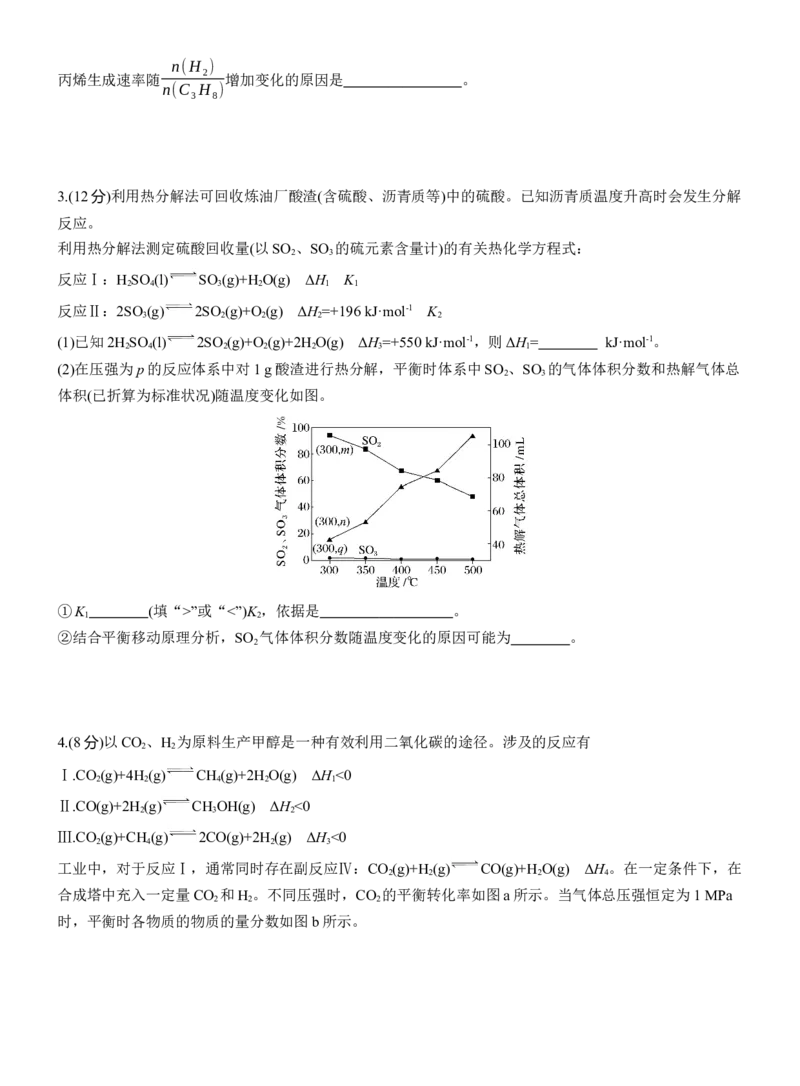
(2)不同压强下,在密闭容器中丙烷平衡转化率随温度变化关系如图1。
①图中压强由大到小的顺序为 ,判断的依据是 。
②800 K、p 压强下,若进料组成中加入惰性气体Ar,a点将 (填“上移”或“下移”)。
2
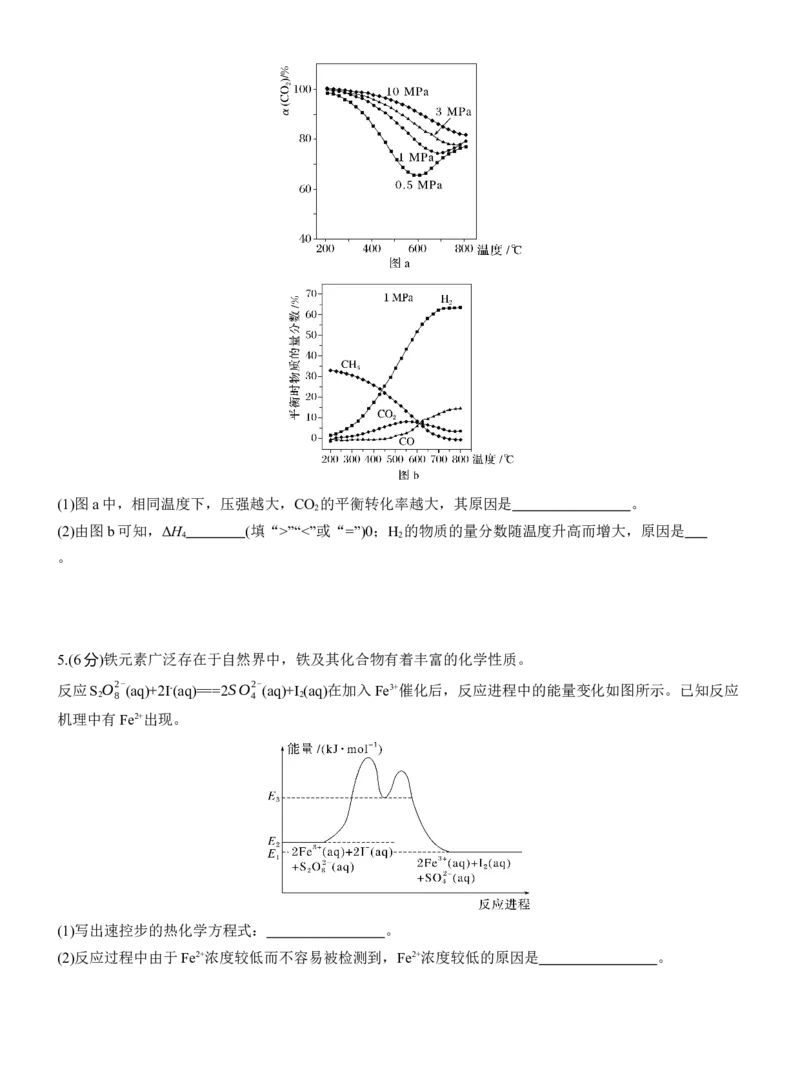
(3)丙烷直接脱氢存在副反应C H (g) C H (g)+CH (g)。一定温度下,丙烷和氢气的混合气体以一定流速
3 8 2 4 4
通过Ga O /Al O 催化剂表面,丙烷转化率、丙烷平衡转化率、丙烯选择性(曲线a)和丙烯生成速率随
2 3 2 3
n(H )
2
n(C H )
变化如图2。催化剂Ga
2
O
3
/Al
2
O
3
反应过程中会有如图3转化,且Ga⁃H/GaO
x
催化活性更强。
3 8
n(H )
2
①丙烷转化率随 变化的曲线为 (填字母)。
n(C H )
3 8
n(H )
②曲线b随 2 的增加而降低的原因是 。
n(C H )
3 8n(H )
2
丙烯生成速率随 增加变化的原因是 。
n(C H )
3 8
3.(12分)利用热分解法可回收炼油厂酸渣(含硫酸、沥青质等)中的硫酸。已知沥青质温度升高时会发生分解
反应。
利用热分解法测定硫酸回收量(以SO 、SO 的硫元素含量计)的有关热化学方程式:
2 3
反应Ⅰ:H SO (l) SO (g)+H O(g) ΔH K
2 4 3 2 1 1
反应Ⅱ:2SO (g) 2SO (g)+O (g) ΔH =+196 kJ·mol-1 K
3 2 2 2 2
(1)已知2H SO (l) 2SO (g)+O (g)+2H O(g) ΔH =+550 kJ·mol-1,则ΔH = kJ·mol-1。
2 4 2 2 2 3 1
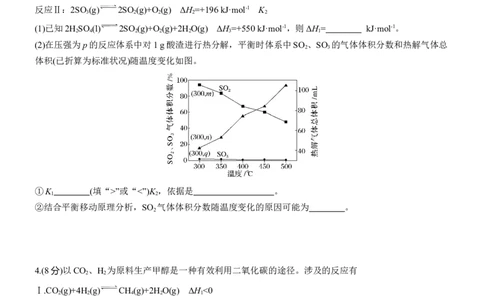
(2)在压强为p的反应体系中对1 g酸渣进行热分解,平衡时体系中SO 、SO 的气体体积分数和热解气体总
2 3
体积(已折算为标准状况)随温度变化如图。
①K (填“>”或“<”)K ,依据是 。
1 2
②结合平衡移动原理分析,SO 气体体积分数随温度变化的原因可能为 。
2
4.(8分)以CO 、H 为原料生产甲醇是一种有效利用二氧化碳的途径。涉及的反应有
2 2
Ⅰ.CO (g)+4H (g) CH (g)+2H O(g) ΔH <0
2 2 4 2 1
Ⅱ.CO(g)+2H (g) CH OH(g) ΔH <0
2 3 2
Ⅲ.CO (g)+CH (g) 2CO(g)+2H (g) ΔH <0
2 4 2 3
工业中,对于反应Ⅰ,通常同时存在副反应Ⅳ:CO (g)+H (g) CO(g)+H O(g) ΔH 。在一定条件下,在
2 2 2 4
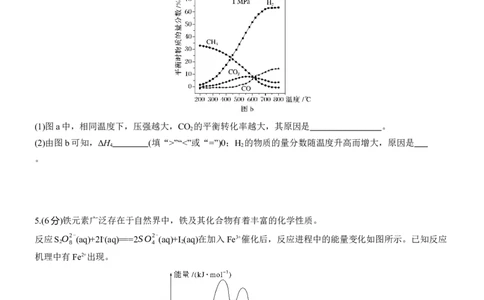
合成塔中充入一定量CO 和H 。不同压强时,CO 的平衡转化率如图a所示。当气体总压强恒定为1 MPa
2 2 2
时,平衡时各物质的物质的量分数如图b所示。(1)图a中,相同温度下,压强越大,CO 的平衡转化率越大,其原因是 。
2
(2)由图b可知,ΔH (填“>”“<”或“=”)0;H 的物质的量分数随温度升高而增大,原因是
4 2
。
5.(6分)铁元素广泛存在于自然界中,铁及其化合物有着丰富的化学性质。
反应S O2- (aq)+2I-(aq)===2SO2- (aq)+I (aq)在加入Fe3+催化后,反应进程中的能量变化如图所示。已知反应
2 8 4 2
机理中有Fe2+出现。
(1)写出速控步的热化学方程式: 。
(2)反应过程中由于Fe2+浓度较低而不容易被检测到,Fe2+浓度较低的原因是 。多平衡体系中的规范解答题(B)
1.(15分)丁烯是一种重要的化工原料,可由丁烷催化脱氢制备:C H (g) C H (g)+H (g) ΔH=+123
4 10 4 8 2
kJ·mol-1。
回答下列问题:
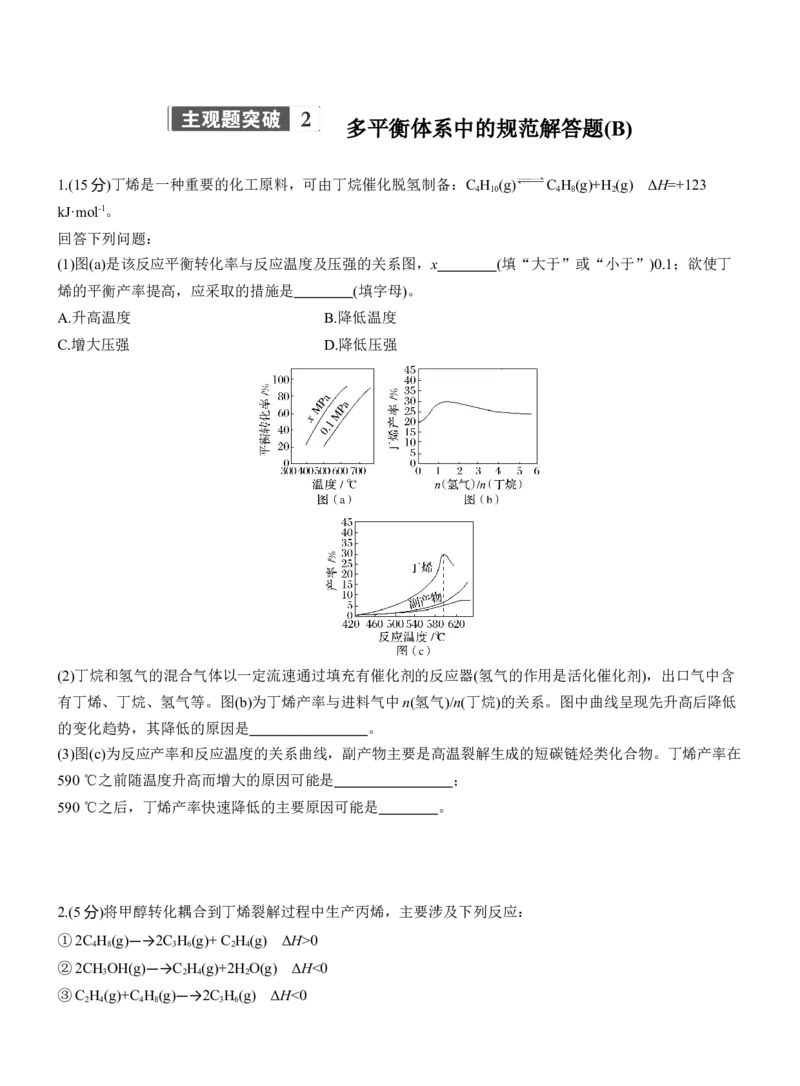
(1)图(a)是该反应平衡转化率与反应温度及压强的关系图,x (填“大于”或“小于”)0.1;欲使丁
烯的平衡产率提高,应采取的措施是 (填字母)。
A.升高温度 B.降低温度
C.增大压强 D.降低压强
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含
有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低
的变化趋势,其降低的原因是 。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在
590 ℃之前随温度升高而增大的原因可能是 ;
590 ℃之后,丁烯产率快速降低的主要原因可能是 。
2.(5分)将甲醇转化耦合到丁烯裂解过程中生产丙烯,主要涉及下列反应:
①2C H (g)―→2C H (g)+ C H (g) ΔH>0
4 8 3 6 2 4
②2CH OH(g)―→C H (g)+2H O(g) ΔH<0
3 2 4 2
③C H (g)+C H (g)―→2C H (g) ΔH<0
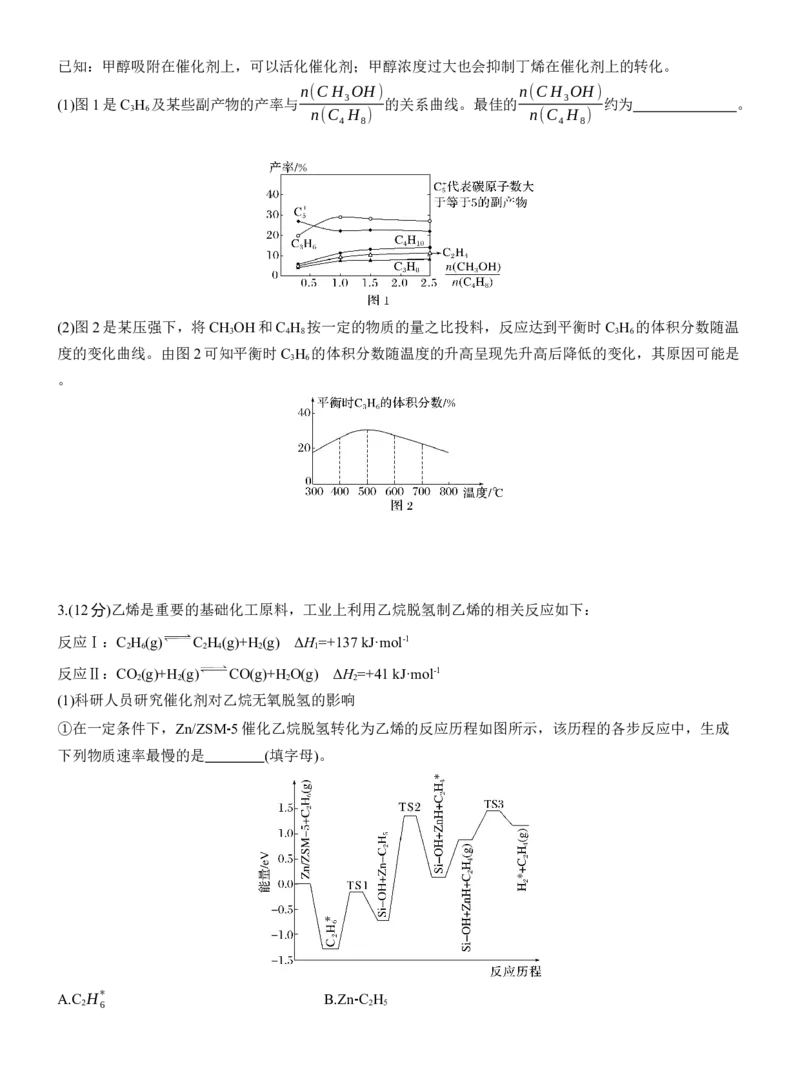
2 4 4 8 3 6已知:甲醇吸附在催化剂上,可以活化催化剂;甲醇浓度过大也会抑制丁烯在催化剂上的转化。
n(CH OH) n(CH OH)
(1)图1是C H 及某些副产物的产率与 3 的关系曲线。最佳的 3 约为 。
3 6 n(C H ) n(C H )
4 8 4 8
(2)图2是某压强下,将CH OH和C H 按一定的物质的量之比投料,反应达到平衡时C H 的体积分数随温
3 4 8 3 6
度的变化曲线。由图2可知平衡时C H 的体积分数随温度的升高呈现先升高后降低的变化,其原因可能是
3 6
。
3.(12分)乙烯是重要的基础化工原料,工业上利用乙烷脱氢制乙烯的相关反应如下:
反应Ⅰ:C H (g) C H (g)+H (g) ΔH =+137 kJ·mol-1
2 6 2 4 2 1
反应Ⅱ:CO (g)+H (g) CO(g)+H O(g) ΔH =+41 kJ·mol-1
2 2 2 2
(1)科研人员研究催化剂对乙烷无氧脱氢的影响
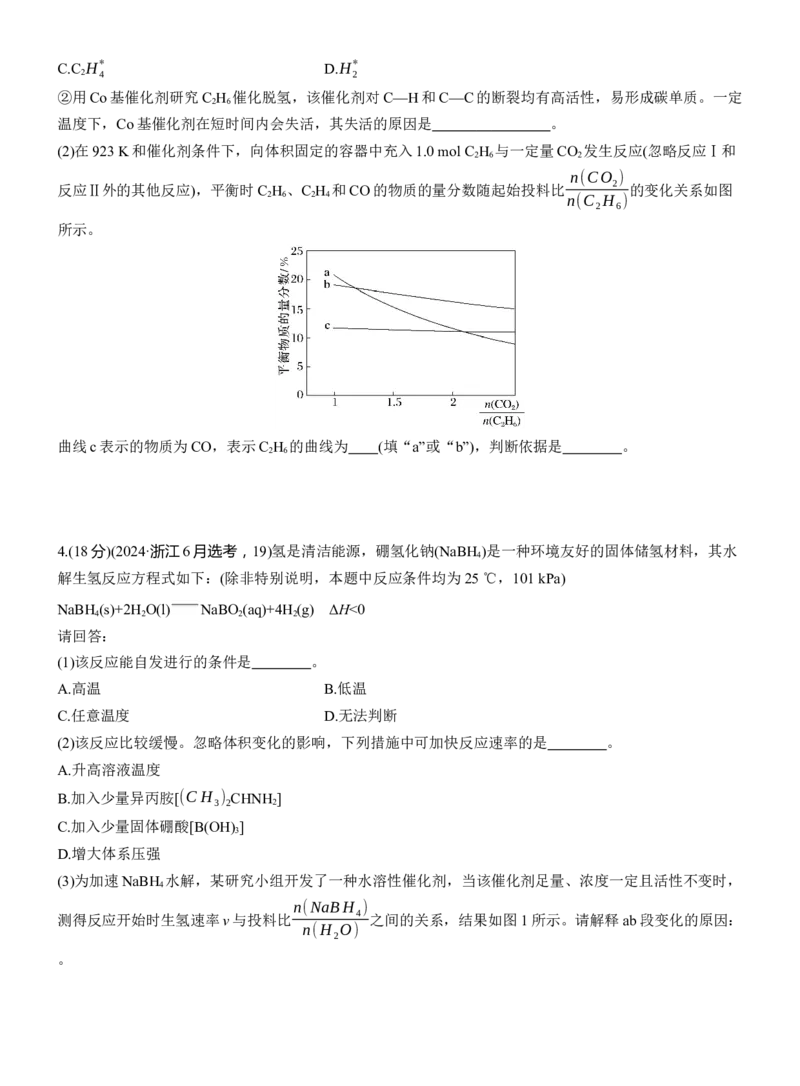
①在一定条件下,Zn/ZSM⁃5催化乙烷脱氢转化为乙烯的反应历程如图所示,该历程的各步反应中,生成
下列物质速率最慢的是 (填字母)。
A.C
2
H
6
* B.Zn⁃C
2
H
5C.C
H* D.H*
2 4 2
②用Co基催化剂研究C H 催化脱氢,该催化剂对C—H和C—C的断裂均有高活性,易形成碳单质。一定
2 6
温度下,Co基催化剂在短时间内会失活,其失活的原因是 。
(2)在923 K和催化剂条件下,向体积固定的容器中充入1.0 mol C H 与一定量CO 发生反应(忽略反应Ⅰ和
2 6 2
n(CO )
反应Ⅱ外的其他反应),平衡时C H 、C H 和CO的物质的量分数随起始投料比 2 的变化关系如图
2 6 2 4 n(C H )
2 6
所示。
曲线c表示的物质为CO,表示C H 的曲线为 (填“a”或“b”),判断依据是 。
2 6
4.(18分)(2024·浙江6月选考,19)氢是清洁能源,硼氢化钠(NaBH )是一种环境友好的固体储氢材料,其水
4
解生氢反应方程式如下:(除非特别说明,本题中反应条件均为25 ℃,101 kPa)
NaBH (s)+2H O(l) NaBO (aq)+4H (g) ΔH<0
4 2 2 2
请回答:
(1)该反应能自发进行的条件是 。
A.高温 B.低温
C.任意温度 D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是 。
A.升高溶液温度
B.加入少量异丙胺[(CH ) CHNH ]
3 2 2
C.加入少量固体硼酸[B(OH) ]
3
D.增大体系压强
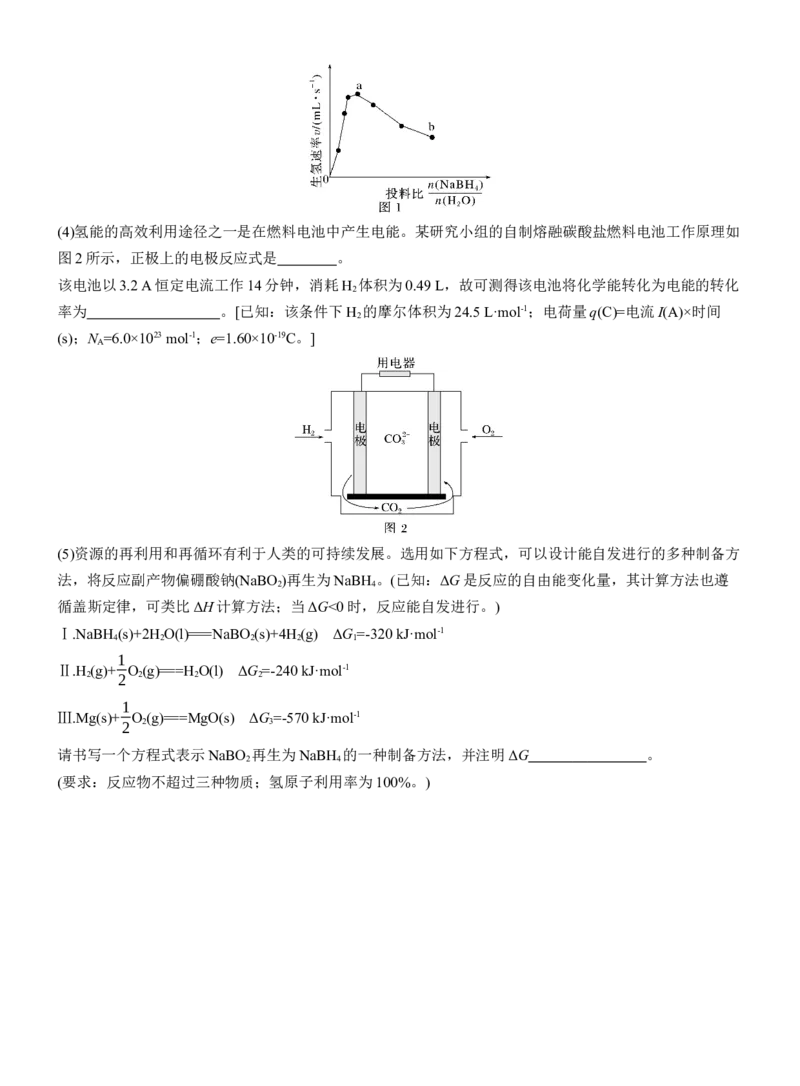
(3)为加速NaBH 水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,
4
n(NaBH )
测得反应开始时生氢速率v与投料比 4 之间的关系,结果如图1所示。请解释ab段变化的原因:
n(H O)
2
。(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如
图2所示,正极上的电极反应式是 。
该电池以3.2 A恒定电流工作14分钟,消耗H 体积为0.49 L,故可测得该电池将化学能转化为电能的转化
2
率为 。[已知:该条件下H 的摩尔体积为24.5 L·mol-1;电荷量q(C)=电流I(A)×时间
2
(s);N =6.0×1023 mol-1;e=1.60×10-19C。]
A
(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方
法,将反应副产物偏硼酸钠(NaBO )再生为NaBH 。(已知:ΔG是反应的自由能变化量,其计算方法也遵
2 4
循盖斯定律,可类比ΔH计算方法;当ΔG<0时,反应能自发进行。)
Ⅰ.NaBH (s)+2H O(l)===NaBO (s)+4H (g) ΔG =-320 kJ·mol-1
4 2 2 2 1
1
Ⅱ.H (g)+ O (g)===H O(l) ΔG =-240 kJ·mol-1
2 2 2 2 2
1
Ⅲ.Mg(s)+ O (g)===MgO(s) ΔG =-570 kJ·mol-1
2 2 3
请书写一个方程式表示NaBO 再生为NaBH 的一种制备方法,并注明ΔG 。
2 4
(要求:反应物不超过三种物质;氢原子利用率为100%。)答案精析
A
1.(1)①Ⅱ ②b-a-c+d-e (2)8.7%Mo 催化剂本身在反应过程中有失硫现象
解析 (1)①反应的活化能越大,反应速率越慢,由图可知,途径Ⅰ的活化能大于途径Ⅱ,所以反应速率较
快的羰基硫氢化的反应历程是途径Ⅱ。
√K
2.(1)+124 p2 (2)①p >p >p 反应为气体分子数增大的反应,增大压强,平衡向左移动,丙烷的平
3 2 1
K
p3
衡转化率减小 ②上移 (3)①c ②随着H 的含量增大,平衡向左移动,丙烷平衡转化率降低 H 活化了
2 2
催化剂
Ⅱ-Ⅲ ΔH -ΔH
解析 (1)将3个反应依次记为反应Ⅰ、Ⅱ、Ⅲ,由盖斯定律可知反应Ⅰ= ,ΔH = 2 3=
2 1 2
(-236 kJ·mol-1 )-(-484 kJ·mol-1 ) √K
=+124 kJ·mol-1;则K = p2 。(2)①该反应为正向气体分子数增
p1
2 K
p3
大的反应,当温度一定时,增大压强,平衡逆向移动,丙烷的转化率减小,则压强p >p >p 。②800 K、p
3 2 1 2
压强下,若进料组成中加入惰性气体Ar,原气体的分压减小,则平衡正向移动,丙烷的转化率增大,a点
n(H )
将上移。(3)①已知曲线a为丙烯选择性,随 2 增加丙烯的选择性基本不变,则丙烷转化率几乎没有
n(C H )
3 8
起伏,故曲线c为丙烷转化率。
3.(1)+177 (2)①< 平衡时SO 的体积分数远小于SO
3 2
②温度升高,反应Ⅱ平衡正向移动程度小于酸渣中沥青质分解程度
(+550)-(+196)
解析 (1)依题意知,已知反应=反应Ⅰ×2+反应Ⅱ,故ΔH =2ΔH +ΔH ,故ΔH =
3 1 2 1 2
kJ·mol-1=+177 kJ·mol-1。
4.(1)增大压强,反应Ⅳ平衡不移动,反应Ⅰ平衡向正反应方向移动 (2)> 反应Ⅰ放热,反应Ⅳ吸热,温
度升高时,反应Ⅰ平衡向左移动增加的H 的量大于反应Ⅳ平衡向右移动减少的H 的量
2 2
解析 (1)②根据反应Ⅰ、Ⅳ可知只有反应Ⅳ生成CO,根据图b可知CO平衡时的物质的量分数随着温度
的升高而增大,说明该反应吸热,ΔH >0。
4
5.(1)2Fe3+(aq)+2I-(aq)===I (aq)+2Fe2+(aq) ΔH=+(E -E ) kJ·mol-1 (2)第一步基元反应活化能较高为慢反应,
2 3 2
第二步基元反应活化能较低为快反应。第一步反应产生的Fe2+很快被第二步反应消耗,故Fe2+浓度较小
解析 (1)根据S
O2- (aq)+2I-(aq)===2SO2-
(aq)+I (aq)结合图像,可得两步反应为2Fe3+(aq)+2I-(aq)===I (aq)
2 8 4 2 2
+2Fe2+(aq);2Fe2+(aq)+S
O2- (aq)===2Fe3+(aq)+2SO2-
(aq);活化能最大的一步为速控步,由图可知,速控步
2 8 4
热化学方程式为2Fe3+(aq)+2I-(aq)===I (aq)+2Fe2+(aq) ΔH=+(E -E )kJ·mol-1。
2 3 2
B1.(1)小于 AD
n(氢气)
(2)氢气是产物之一,随着 的增大,该平衡向逆反应方向移动
n(丁烷)
(3)升高温度,反应速率加快,生成的丁烯会增多,同时由于反应是吸热反应,升高温度,平衡向正反应方
向移动 丁烯高温裂解生成短碳链烃类化合物
解析 (1)由图(a)可以看出,温度相同时,压强由0.1 MPa变化到x MPa,丁烷的转化率增大,即平衡正向
移动,所以x<0.1。由于正反应为吸热反应,所以温度升高时,平衡正向移动,丁烯的平衡产率增大,因
此A正确、B错误;反应正向进行时体积增大,加压时平衡逆向移动,丁烯的平衡产率减小,因此C错误、
n(氢气)
D正确。(2)反应初期,H 可以活化催化剂,进料气中 较小,丁烷浓度大,反应向正反应方向进
2 n(丁烷)
n(氢气)
行的程度大,丁烯产率升高;随着进料气中 增大,原料中过量的H 会使平衡逆向移动,所以丁
n(丁烷) 2
烯产率下降。
2.(1)1.0 (2)300~500 ℃时,丁烯裂解(反应①)为主要反应,是吸热反应,升高温度,平衡正向移动,使
C H 的体积分数增大;温度高于500 ℃时,反应②③为主要反应,是放热反应,升高温度,平衡逆向移动,
3 6
使C H 的体积分数降低,同时温度升高易发生副反应,C H 可能转化为C H 、C H 、C H
、C+
等,使
3 6 3 6 2 4 3 8 4 10 5
C H 的体积分数降低
3 6
n(CO )
3.(1)①C ②积碳在其表面快速沉积使其失活 (2)a 2 比值增大,乙烷转化率增大,其物质的量
n(C H )
2 6
分数变化比CO和C H 要大
2 4
n(NaBH )
4.(1)C (2)AC (3)随着投料比 4 增大,NaBH 的水解转化率降低 (4)O +4e-+2CO ===2CO2-
n(H O) 4 2 2 3
2
70%
(5)NaBO (s)+2H (g)+2Mg(s)===NaBH (s)+2MgO(s) ΔG=-340 kJ·mol-1
2 2 4
解析 (1)反应NaBH (s)+2H O(l)===NaBO (aq)+4H (g) ΔH<0,ΔS>0,由ΔG=ΔH-TΔS可知,任意温度下,
4 2 2 2
该反应均能自发进行。(2)升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,A符合题意;
硼氢化钠与水反应的实质是利用其强还原性来还原水中的氢离子,异丙胺[(CH ) CHNH ]呈碱性,使水中
3 2 2
氢离子的浓度减小,化学反应速率降低,B不符合题意;硼酸[B(OH) ]呈弱酸性,加入少量固体硼酸,水
3
中氢离子的浓度增大,化学反应速率加快,C符合题意;增大体系压强,忽略体积变化,测气体浓度不变,
化学反应速率不变,D不符合题意。(4)根据题干信息,该燃料电池中H 为负极,O 为正极,熔融碳酸盐
2 2
为电解质,故正极的电极反应式为O +4e-+2CO
===2CO2-
,该条件下,0.49 L H 的物质的量为
2 2 3 2
0.49 L
=0.02 mol,工作时,H 失去电子:H -2e-===2H+,所带电荷量:2×0.02×6.0×1023×1.60×10-19
24.5 L·mol-1 2 2
2 688 C
C=3 840 C,工作电荷量:3.2×14×60 C=2 688 C,则该电池将化学能转化为电能的转化率:
3 840 C
×100%=70%。(5)结合题干信息,要使得氢原子利用率为100%,可由(2×反应Ⅲ)-(2×反应Ⅱ+反应Ⅰ)得NaBO (s)+2H (g)+2Mg(s)===NaBH (s)+2MgO(s) ΔG=2ΔG -(2ΔG +ΔG )=2×(-570 kJ·mol-1)-[2×(-240
2 2 4 3 2 1
kJ·mol-1)+(-320 kJ·mol-1)]=-340 kJ·mol-1。