文档内容
电化学装置图的综合分析
(选择题1~5题,每小题3分,6~12题,每小题5分,共50分)
1.某锂离子电池其原理如图所示,下列说法不正确的是( )
A.隔膜为阳离子交换膜
B.放电时,A极发生反应为I-
+2e-===3I-
3
C.充放电过程中,只有一种元素化合价发生变化
D.用此电池电解(惰性电极)足量AgNO 溶液,当有1 mol离子穿过隔膜时,产生气体分子数目为0.25N
3 A
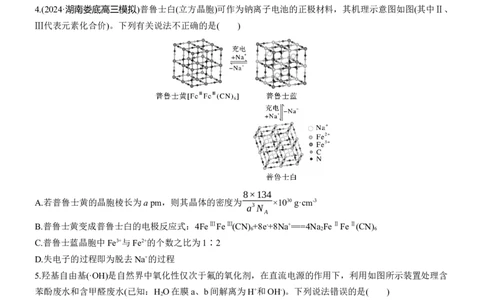
2.(2024·河南省创新联盟模拟)科学家开发的一种宽温域的锂离子电池,其工作原理如图所示。
下列叙述错误的是( )
A.X极电势高于Y极电势
B.放电时,X极电极反应式为Li V (PO ) -2e-+2Li+===Li V (PO )
3 2 4 3 5 2 4 3
C.充电时,电极Y与电源负极连接
D.充电时,每生成1.4 g Li时理论上转移电子数约为1.204×1023
3.(2024·长沙高三新高考适应性考试)氧化铋(Bi O )作为镍/铋电池的负极材料,因其理论容量高、易制备而
2 3
受到广泛关注。如图为该电池的示意图,下列说法正确的是( )A.放电时,OH-从电极a移向电极b
B.充电时,电子从电源负极→电极a→电极b→电源正极
C.放电时,总反应为Bi O +3H O+6NiO===6NiOOH+2Bi
2 3 2
D.充电时,电路转移9.03×1024个电子,阳极质量增加255 g
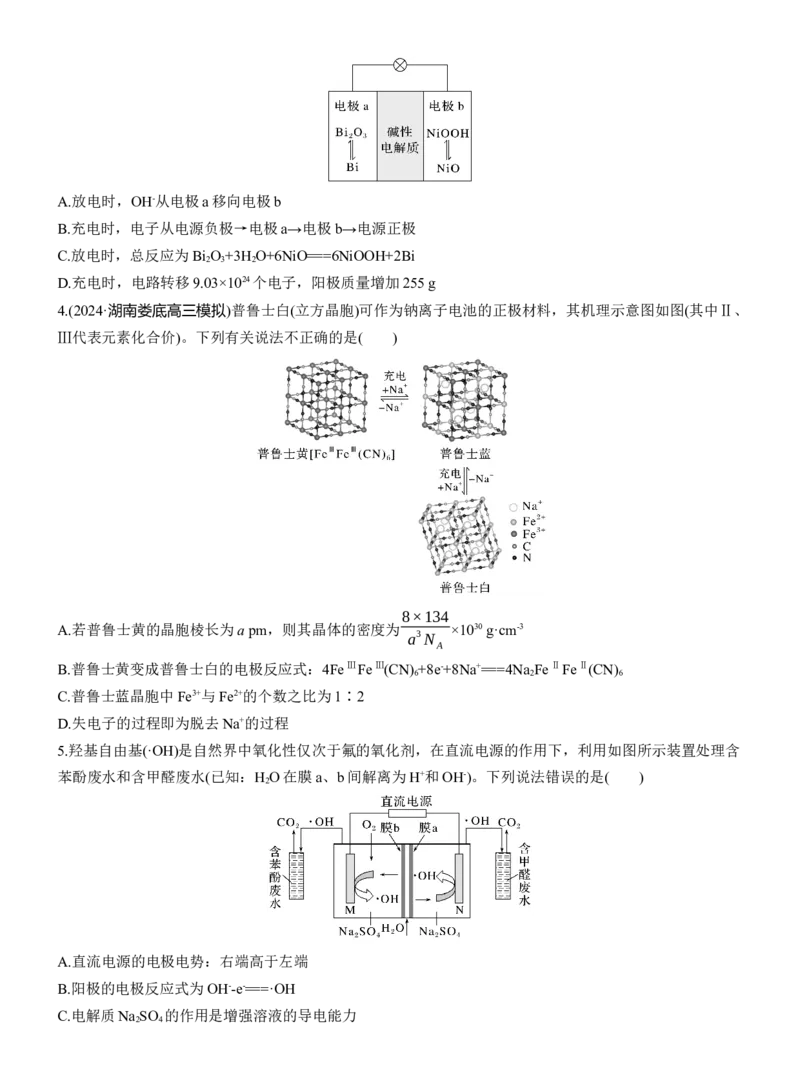
4.(2024·湖南娄底高三模拟)普鲁士白(立方晶胞)可作为钠离子电池的正极材料,其机理示意图如图(其中Ⅱ、
Ⅲ代表元素化合价)。下列有关说法不正确的是( )
8×134
A.若普鲁士黄的晶胞棱长为a pm,则其晶体的密度为 ×1030 g·cm-3
a3N
A
B.普鲁士黄变成普鲁士白的电极反应式:4FeⅢFeⅢ(CN) +8e-+8Na+===4Na FeⅡFeⅡ(CN)
6 2 6
C.普鲁士蓝晶胞中Fe3+与Fe2+的个数之比为1∶2
D.失电子的过程即为脱去Na+的过程
5.羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂,在直流电源的作用下,利用如图所示装置处理含
苯酚废水和含甲醛废水(已知:H O在膜a、b间解离为H+和OH-)。下列说法错误的是( )
2
A.直流电源的电极电势:右端高于左端
B.阳极的电极反应式为OH--e-===·OH
C.电解质Na SO 的作用是增强溶液的导电能力
2 4D.每处理9.4 g苯酚,理论上有2.8 mol OH-透过膜b
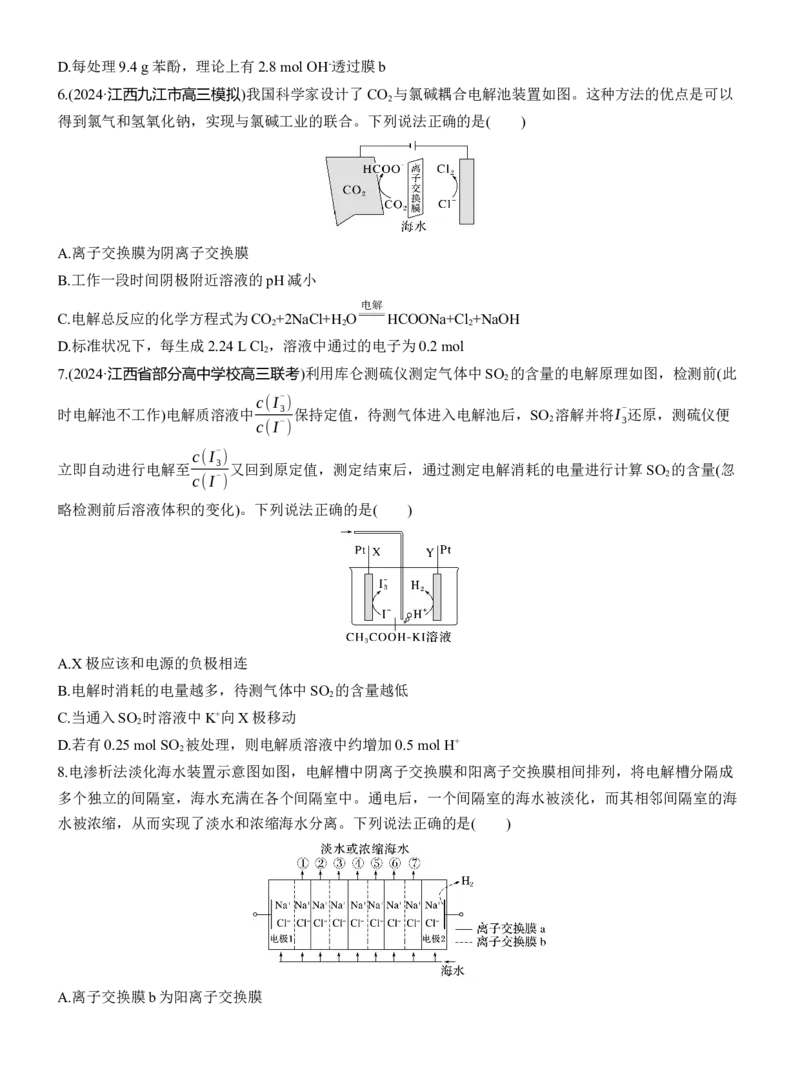
6.(2024·江西九江市高三模拟)我国科学家设计了CO 与氯碱耦合电解池装置如图。这种方法的优点是可以
2
得到氯气和氢氧化钠,实现与氯碱工业的联合。下列说法正确的是( )
A.离子交换膜为阴离子交换膜
B.工作一段时间阴极附近溶液的pH减小
C.电解总反应的化学方程式为CO +2NaCl+H O HCOONa+Cl +NaOH
2 2 2
D.标准状况下,每生成2.24 L Cl ,溶液中通过的电子为0.2 mol
2
7.(2024·江西省部分高中学校高三联考)利用库仑测硫仪测定气体中SO 的含量的电解原理如图,检测前(此
2
c(I-
)
时电解池不工作)电解质溶液中 3 保持定值,待测气体进入电解池后,SO 溶解并将I- 还原,测硫仪便
c(I-
)
2 3
c(I-
)
立即自动进行电解至 3 又回到原定值,测定结束后,通过测定电解消耗的电量进行计算SO 的含量(忽
c(I-
)
2
略检测前后溶液体积的变化)。下列说法正确的是( )
A.X极应该和电源的负极相连
B.电解时消耗的电量越多,待测气体中SO 的含量越低
2
C.当通入SO 时溶液中K+向X极移动
2
D.若有0.25 mol SO 被处理,则电解质溶液中约增加0.5 mol H+
2
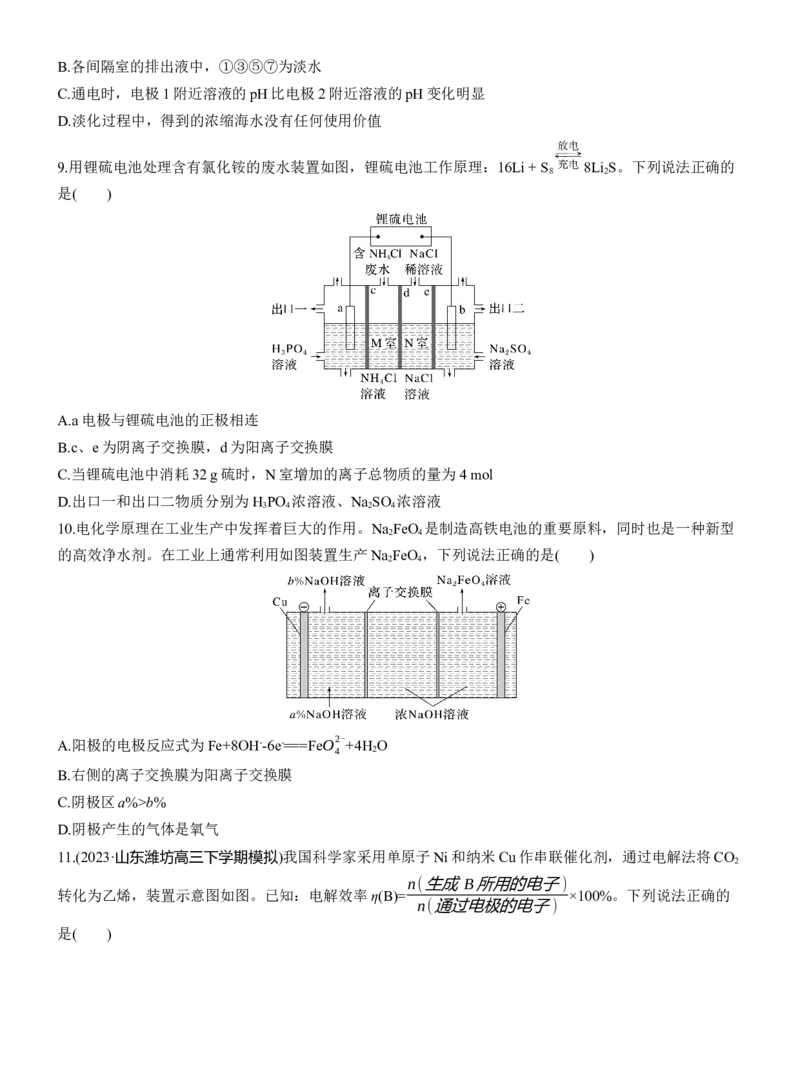
8.电渗析法淡化海水装置示意图如图,电解槽中阴离子交换膜和阳离子交换膜相间排列,将电解槽分隔成
多个独立的间隔室,海水充满在各个间隔室中。通电后,一个间隔室的海水被淡化,而其相邻间隔室的海
水被浓缩,从而实现了淡水和浓缩海水分离。下列说法正确的是( )
A.离子交换膜b为阳离子交换膜B.各间隔室的排出液中,①③⑤⑦为淡水
C.通电时,电极1附近溶液的pH比电极2附近溶液的pH变化明显
D.淡化过程中,得到的浓缩海水没有任何使用价值
9.用锂硫电池处理含有氯化铵的废水装置如图,锂硫电池工作原理:16Li + S 8Li S。下列说法正确的
8 2
是( )
A.a电极与锂硫电池的正极相连
B.c、e为阴离子交换膜,d为阳离子交换膜
C.当锂硫电池中消耗32 g硫时,N室增加的离子总物质的量为4 mol
D.出口一和出口二物质分别为H PO 浓溶液、Na SO 浓溶液
3 4 2 4
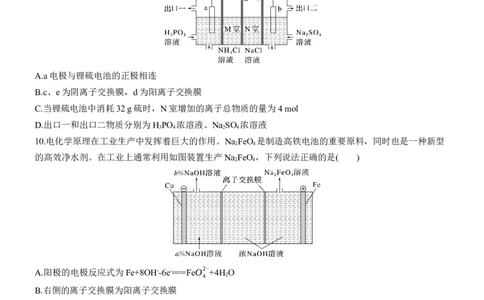
10.电化学原理在工业生产中发挥着巨大的作用。Na FeO 是制造高铁电池的重要原料,同时也是一种新型
2 4
的高效净水剂。在工业上通常利用如图装置生产Na FeO ,下列说法正确的是( )
2 4
A.阳极的电极反应式为Fe+8OH--6e-===FeO2-
+4H O
4 2
B.右侧的离子交换膜为阳离子交换膜
C.阴极区a%>b%
D.阴极产生的气体是氧气
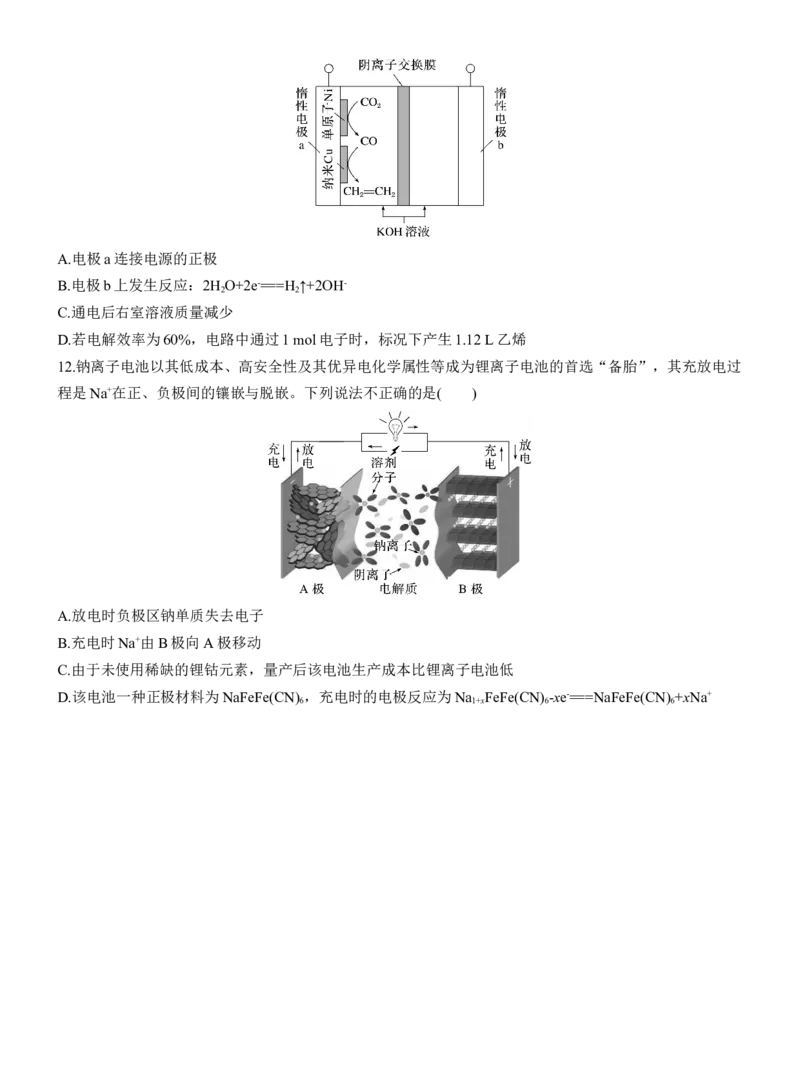
11.(2023·山东潍坊高三下学期模拟)我国科学家采用单原子Ni和纳米Cu作串联催化剂,通过电解法将CO
2
n(生成B所用的电子)
转化为乙烯,装置示意图如图。已知:电解效率η(B)= ×100%。下列说法正确的
n(通过电极的电子)
是( )A.电极a连接电源的正极
B.电极b上发生反应:2H O+2e-===H ↑+2OH-
2 2
C.通电后右室溶液质量减少
D.若电解效率为60%,电路中通过1 mol电子时,标况下产生1.12 L乙烯
12.钠离子电池以其低成本、高安全性及其优异电化学属性等成为锂离子电池的首选“备胎”,其充放电过
程是Na+在正、负极间的镶嵌与脱嵌。下列说法不正确的是( )
A.放电时负极区钠单质失去电子
B.充电时Na+由B极向A极移动
C.由于未使用稀缺的锂钴元素,量产后该电池生产成本比锂离子电池低
D.该电池一种正极材料为NaFeFe(CN) ,充电时的电极反应为Na FeFe(CN) -xe-===NaFeFe(CN) +xNa+
6 1+x 6 6答案精析
1.C [放电时B极为负极,S失去电子,发生氧化反应,释放出的锂离子移向正极,所以隔膜为阳离子交
换膜,A正确;放电时,A极为正极,发生还原反应,电极反应式为I-
+2e-===3I-,B正确;充放电过程中,
3
C元素和I元素的化合价均发生变化,C错误;用此电池电解(惰性电极)足量AgNO 溶液,阳极发生
3
2H O-4e-===O ↑+4H+,阴极发生4Ag++4e-===4Ag,当有1 mol离子穿过隔膜时(转移电子1 mol),产生氧
2 2
气0.25 mol,分子数目为0.25N ,D正确。]
A
2.B [放电时,电极X为正极,电极Y为负极,电池中正极电势高于负极电势,电势:电极X高于电极
Y,A项正确;放电时,X极是正极,得电子,发生还原反应,电极反应式为Li V (PO ) +2e-
3 2 4 3
+2Li+===Li V (PO ) ,B项错误;充电时,电极Y为阴极,阴极与电源负极连接,C项正确;阴极反应式为
5 2 4 3
1.4 g
Li++e-===Li,n(Li)= =0.2 mol,转移n(e-)=0.2 mol,转移电子数目约为1.204×1023,D项正确。]
7 g·mol-1
3.D [放电时,OH-从电极b移向电极a,故A错误;充电时,电子从电源负极→电极a,电极b→电源正
极,电子不经过电解质溶液,故B错误;放电时,电极a为负极,电极反应式为2Bi-6e-+6OH-
===Bi O +3H O,电极b为正极,电极反应式为NiOOH+e-===NiO+OH-,总反应式为
2 3 2
6NiOOH+2Bi===Bi O +3H O+6NiO,故C错误;充电时,电极b为阳极,电极反应式为NiO+OH--e-
2 3 2
===NiOOH,电路转移9.03×1024个电子,即15 mol电子,根据原子守恒可知,阳极增加的质量为15 mol
OH-的质量,即15 mol×17 g·mol-1=255 g,故D正确。]
4×56×2+26×24 8×134
4.C [普鲁士黄晶胞中含有4个FeⅢFeⅢ(CN) ,故该晶体的密度为 g·cm-3=
6 (a×10-10 ) 3×N a3N
A A
×1030g·cm-3,故A正确;由图可知,1个普鲁士黄晶胞变成普鲁士白晶胞迁移钠离子个数为8,故电极反应
式为4FeⅢFeⅢ(CN) +8e-+8Na+===4Na FeⅡFeⅡ(CN) ,故B正确;普鲁士黄晶胞中Fe3+个数为8,普鲁士蓝
6 2 6
晶胞中含有4个Na+,说明发生反应Fe3++e-===Fe2+,故普鲁士蓝晶胞中Fe3+与Fe2+的个数之比为1∶1,故
C错误;根据机理图可看出,失电子的过程即为脱去Na+的过程,故D正确。]
5.D [M电极通入O ,发生反应生成·OH,反应式为O +2e-+2H+===2·OH,M作阴极,N为阳极,反应式
2 2
为OH--e-===·OH,据此作答。M作阴极,连接的直流电源左端为负极,N为阳极,连接的直流电源右端为
正极,正极电势高于负极,即右端高于左端,故A正确;加入电解质Na SO ,溶解后自由移动的离子增多,
2 4
但不影响电极反应,可以增强溶液的导电能力,故C正确;苯酚与·OH反应生成CO 的化学方程式为
2
+28·OH 6CO ↑+17H O,则每处理9.4 g即0.1 mol苯酚,理论上有2.8 mol OH-透过膜a,故D错
2 2
误。]6.C [由图示可知,阴极的电极反应式为CO +2e-+H O===HCOO-+OH-,阳极的电极反应式为2Cl--2e-
2 2
===Cl ↑,由此分析回答。阴极区生成OH-,Na+从阳极区通过离子交换膜进入阴极区,所以该离子交换膜
2
为阳离子交换膜,A错误;工作一段时间阴极产生OH-,阴极附近溶液pH变大,B错误;电子不能通过溶
液,D错误。]
7.D
[由图可知,测硫仪工作时,左侧铂电极为电解池的阳极,I-在阳极失去电子发生氧化反应生成I-
,电
3
极反应式:3I--2e-===I- ,反应生成的I-
与SO
反应生成I-、SO2-
和H+,反应的离子方程式为SO
+I-
3 3 2 4 2 3
+2H O===3I-+SO2- +4H+,右侧铂电极为阴极,溶液中的氢离子在阴极得到电子发生还原反应生成氢气。根
2 4
据分析,左侧铂电极为电解池的阳极,应与电源正极相连,A错误;由题干知电解时消耗的电量越多,被
还原的I-
越多,待测气体中SO 的含量越高,B错误;电解池中阳离子向阴极移动,即溶液中K+向Y极移
3 2
c(I-
)
动,C错误;SO
溶解并将I-
还原,测硫仪便立即自动进行电解至
3
又回到原定值,根据装置中得失电
2 3 c(I-
)
子守恒可知,有0.25 mol SO 被处理,则电解质溶液中约增加0.5 mol H+,D正确。]
2
8.B [A项,由图分析可知,电极1为电解池的阳极,氯离子放电生成氯气,电极反应为2Cl--2e-
===Cl ↑,电极2为阴极,溶液中H O放电生成氢气,电极反应为2H O+2e-===H ↑+2OH-,离子交换膜a
2 2 2 2
是阳离子交换膜,离子交换膜b是阴离子交换膜,错误;B项,结合阴、阳离子的移向可知,各间隔室的
排出液中,①③⑤⑦为淡水,正确;C项,由上述电极反应式知电极2附近溶液的pH比电极1附近溶液的
pH变化明显,错误;D项,淡化过程中,得到的浓缩海水可以提取氯化钠、镁、溴等,有使用价值,错
误。]
9.C [电池放电时,Li电极失去电子变为Li+,发生氧化反应,则Li为负极,硫为正极,电极反应为
S +16e-===8S2-,N室氯化钠浓度变大,故b极区钠离子向N室移动,M室氯离子向N室移动,e为阳离子
8
交换膜,d为阴离子交换膜,b为阳极,电极反应式为2H O-4e-===O ↑+4H+,故出口二物质为硫酸。a为
2 2
阴极,电极反应式为2H++2e-===H ↑,铵根离子从M室向左侧迁移,c为阳离子交换膜,据此分析。由分
2
析可知,a为阴极,与锂硫电池的负极相连,A错误;根据正极电极反应式可知,消耗32 g硫转移2 mol
电子,有2 mol钠离子和2 mol氯离子向N室移动,N室增加的离子总物质的量为4 mol,C正确;出口一
和出口二物质分别为磷酸铵、硫酸,D错误。]
10.A
[由图所示,Fe为阳极,故发生氧化反应生成FeO2- ,电极反应式为Fe+8OH--6e-===FeO2-
+4H O,A
4 4 2
正确;阳极反应消耗阴离子,中间室中的氢氧根离子向右侧阳极移动,故右侧离子交换膜为阴离子交换膜,
B错误;阴极区水被电解产生H 和OH-,中间室中的Na+向左侧阴极移动,NaOH浓度变大,a%