文档内容
专题讲座(二)阿伏加德罗常数的突破
1.设N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.1 mol CH =CH 分子中含有的共价键数为6N
2 2 A
B.500 mL 0.5 mol·L−1的NaCl溶液中微粒数大于0.5N
A
C.30 g HCHO与CHCOOH混合物中含C原子数为N
3 A
D.2.3 g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N 之间
2 A A
2.设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.7.8 g的NaS和NaO 的混合物中含有阴、阳离子总数为0.3 N
2 2 2 A
B.常温常压下,22.4 LCO 中含有N 个CO 分子
2 A 2
C.1.0 L 1.0 mol·L-1的NaClO水溶液中含有的氧原子数为N
A
D.常温常压下,18 g羟基(-O2H)中所含的中子数为8 N
A
3. 为阿伏加德罗常数的值。下列说法正确的是
A. 含有的中子数为
B. 溶液中含有的 数为
C. 与 在密闭容器中充分反应后的分子数为
D. 和 (均为标准状况)在光照下充分反应后的分子数为
4.N 是阿伏加德罗常数的值。下列关于含氮物质的说法错误的是
A
A.通常状况下,10.8gN O 中含有的电子数目为5.4N
2 5 A
B.足量铜和1molHNO 反应生成Cu(NO ) 时转移电子数为2N
3 3 2 A
C.1L1mol·L-1NaNO 溶液中NO 和HNO 粒子数目之和为N
2 2 A
D.1molN 和4molH 在密闭容器中反应生成NH 分子数目小于2N
2 2 3 A
5.若用N 表示阿伏加德罗常数的值,下列叙述错误的是
A
A.142g Na SO 和NaHPO 的固体混合物中所含阴、阳离子的总数目为3N
2 4 2 4 A
B.锌与某浓度的浓硫酸反应,生成SO 和H 的混合气体22.4 L(标准状况),锌失去电子数目为2N
2 2 A
C.标准状况下,22.4L甲烷和乙烯混合物中含碳氢共价键数目为4N
A
D.0.1mol•L﹣1的CHCOONH 溶液显中性,1L该溶液中含CHCOO-数等于0.1N
3 4 3 A6. 是阿伏加德罗常数的值。下列说法正确的是
A.标准状态下,11.2L 分子中所含的O原子数为1.5
B.32.5g 水解形成的 胶体粒子数为0.2
C.10g质量分数为46%的乙醇水溶液中含有的氢原子数为1.2
D.工业上将1mol 和3mol 在一定条件下反应转移的电子数为6
7.用 表示阿伏加德罗常数的值。下列说法正确的是
A. 中含有的原子数为
B. 溶液含有的 个数为
C.标准状况下, 和 的混合气体中分子数为
D. 与 盐酸充分反应,转移电子数为
8.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.2.24LCl 与足量HO反应转移的电子数为0.1N
2 2 A
B.9.2g甲苯与丙三醇的混合液中所含的氢原子数目为0.8N
A
C.29gC HO分子中含σ键数目为0.45N
3 6 A
D.0.1mol/L的CHCOOH溶液中CHCOOH数目小于0.1N
3 3 A
9.近日,中科院上海高研院在二氧化碳电催化转化研究中取得重要进展。通过调控 的孔道结构
和表面活性位构型,成功实现了 直接转化生成乙醇。用 表示阿伏加德罗常数的值,下列说法正确
的是A.标准状况下, 中所含电子的数目为4
B. 时, 所含共价键的数目为8
C. 乙醇和 乙酸发生酯化反应,最多可生成0.1 乙酸乙酯
D. 电催化过程中,每生成 乙醇,转移电子的数目为
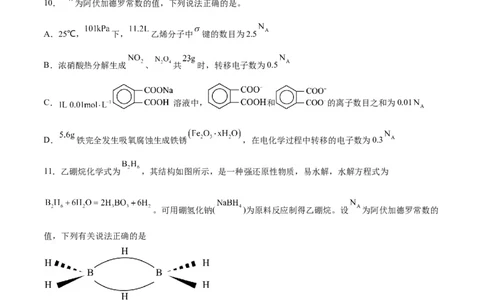
10. 为阿伏加德罗常数的值,下列说法正确的是。
A.25℃, 下, 乙烯分子中 键的数目为2.5
B.浓硝酸热分解生成 、 共 时,转移电子数为0.5
C. 溶液中, 和 的离子数目之和为0.01
D. 铁完全发生吸氧腐蚀生成铁锈 ,在电化学过程中转移的电子数为0.3
11.乙硼烷化学式为 ,其结构如图所示,是一种强还原性物质,易水解,水解方程式为
。可用硼氢化钠( )为原料反应制得乙硼烷。设 为阿伏加德罗常数的
值,下列有关说法正确的是
A.1mol 中含有的共用电子对数目为
B.2.8g 完全水解,转移的电子数目为1.2
C. 可与甲醇反应生成D.能用 和稀硫酸反应制备
12.设 为阿伏加德罗常数的值,下列叙述正确的是
A. 中含有的配位键数为22N
A
B.铬晶胞如图所示, 铬能切割成如图晶胞的数目为N
A
C. 参与氧化还原反应时,转移的电子数一定为2N
A
D. 溶液中含有的 数为0.1N
A
13.设N 为阿伏加德罗常数的值,下列有关叙述正确的是
A
A.31g白磷(P )中含有磷原子数为N
4 A
B. 中含有的中子数为6N
A
C.标准状况下,2.24L苯完全燃烧生成的CO 分子数为0.6N
2 A
D.1molNa O 与足量的水反应转移电子数为2N
2 2 A
14.设 为阿伏加德罗常数的值,下列有关叙述正确的是
A. 溶液中阴离子的数目为
B. 含有共价键的数目为
C. 个 分子中共用电子对的数目为
D. 与足量 反应,生成 和 的混合物,钠失去的电子数为
15. 为阿伏加德罗常数的值。下列说法正确的是A.1 L 0.1 mol/L乙醇溶液中存在的共价键总数为0.8
B.5 g 和 的混合物发生热核聚变反应: ,净产生的中子( )数为
C.1 L 1 mol/L的 溶液中通入适量氨气后呈中性,此时溶液中 的数目为
D.将0.1 mol 完全溶于水中,所得到溶液中 、 、HClO、ClO的粒子数之和为0.2
16. 为阿伏加德罗常数,下列说法正确的是
A.1L 的 溶液中 离子数为
B.11.2L乙烷和丙烯的混合气体中所含碳氢键数为
C.0.1L 的 溶液中,含有的 数目可能为
D.常温下,5.6g铁与 的硝酸反应,铁失去的电子数为
17.甲酸甲酯常用作杀菌剂、熏蒸剂和烟草处理剂,可由甲酸和甲醇反应制得。N 为阿伏加德罗常数的
A
值。下列有关说法正确的是
A.pH=3的甲酸溶液中氢离子数目为1×10-3N
A
B.0.5 mol甲酸甲酯中含有sp3杂化的原子数目为N
A
C.50g质量分数为64%的甲醇水溶液中含有σ键数目为5N
A
D.甲醇燃料电池中,每消耗22.4L(标准状况)甲醇,转移电子数目为6N
A
18.设 为阿伏加德罗常数的值。下列说法正确的是
A. 石墨中含有的 键电子数为
B. 的 溶液中含有的阴离子总数为
C. 羟基和 中含有的质子数均为
D. 的浓硫酸与足量铜反应转移的电子数为
19.设N 为阿伏加德罗常数的值。下列说法正确的是
AA.24g乙烯和丙烯的混合气体中p-pσ键数目为2N
A
B.1L1mol/L氯化铵溶液中NH 和H+数目之和为N
A
C.2molNO与1molO 在密闭容器中充分反应后的分子数为2N
2 A
D.标准状况下,11.2LCH 与22.4LCl 反应后分子总数为1.5N
4 2 A
20.金粉溶于过氧化氢-浓盐酸可以安全环保的制备氯金酸( ),其化学方程式为:
。设 为阿伏加德罗常数的值,下列说法正确的是
A.消耗1molAu,反应转移的电子数为
B.消耗2molHCl生成的 分子数为
C.消耗85g ,产物中形成的配位键数目为
D.2mol液态水中含有的氢键数目为