文档内容
专题讲座(四) 常见气体的实验室制备、净化和收集
第一部分:高考真题感悟
1.(2022·广东·高考真题)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气
处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
【答案】D
【解析】A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸干燥,A
2
装置能达到实验目的,故A不符合题意;B.氯气的密度大于空气,用向上排空气法收集,B装置能收集
氯气,故B不符合题意;C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白
性,故C不符合题意;D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目
的,故D符合题意;答案选D。
2.(2021·海南·高考真题)用如图装置制取干燥的气体(a、b表示加入的试剂),能实现的是
选
气体 a b
项
A 稀
溶
B
液
C 浓 铁片
D 浓氨水
【答案】B
【解析】A. 与浓硫酸反应,故不能用浓硫酸干燥,故A错误;B.发生反应2HO 2HO+O,
2 2 2 2
浓硫酸干燥氧气,故B正确;C.铁片和浓硝酸常温下发生钝化,故不能制取二氧化氮气体,故C错误;D.氨气与浓硫酸反应,故不能用浓硫酸干燥氨气,故D错误;故选B。
3.(2021·全国乙卷,8)在实验室采用如图装置制备气体,合理的是( )
选项 化学试剂 制备气体
A Ca(OH)+NHCl NH
2 4 3
B MnO+HCl(浓) Cl
2 2
C MnO+KClO O
2 3 2
D NaCl+HSO(浓) HCl
2 4
【答案】C
【解析】氨气的密度比空气小,不能用向上排空气法收集,故 A错误;二氧化锰与浓盐酸共热制备氯气为固液
加热反应,不能选用固固加热装置,故 B错误;二氧化锰和氯酸钾共热制备氧气为固固加热的反应,氧气的密
度大于空气,可选用向上排空气法收集,故 C正确;氯化钠与浓硫酸共热制备为固液加热反应,不能选用固固
加热装置,故D错误。
4.(2020·江苏,5)实验室以CaCO 为原料,制备CO 并获得CaCl·6HO晶体。下列图示装置和原理不能达到实
3 2 2 2
验目的的是( )
【答案】D
【解析】A对,碳酸钙与稀盐酸反应可制备CO,且为固液常温型反应,装置也正确;B对,CO 密度比空气大,
2 2
可以用向上排空气法收集;C对,分离固体与液体,可采用过滤的方法;D错,CaCl·6HO晶体可以通过蒸发
2 2
浓缩、冷却结晶、过滤的方法制得,采用蒸发结晶法易导致CaCl·6HO失去结晶水。
2 2
5.(2017·全国卷Ⅰ,10)实验室用H 还原WO 制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没
2 3
食子酸溶液用于吸收少量氧气)。下列说法正确的是( )
A.①②③中依次盛装KMnO 溶液、浓HSO、焦性没食子酸溶液
4 2 4
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
【答案】B
【解析】A项,气体从溶液中逸出易带出水蒸气,所以浓硫酸应放在③中,错误;B项,先通H 以排出空气,
2
加热前应先检验H 的纯度,正确;C项,若先停止通H,空气中的氧气有可能重新将W氧化,应先停止加热,
2 2
再关闭活塞K,错误;D项,MnO 和浓盐酸反应制氯气需要加热,不能用启普发生器制备,错误。
2
第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(每小题只有一个正确选项,共12*5分)
1.(2022·山东泰安·一模)关于下列各实验装置及药品的叙述中,正确的是
A.装置①可用于实验室制取少量
B.可用从左侧加水的方法检验装置②的气密性
C.利用装置③验证铁的析氢腐蚀
D.装置④随关随停制氨气
【答案】A
【解析】A.二氧化锰催化过氧化氢制氧气为固液不加热反应,装置①可用于实验室制取少量 ,A正确;
B.右侧为敞口体系,不能检验装置②的气密性,B错误;C.铁的析氢腐蚀需要较强的酸性环境,C错误;
D.碱石灰中氢氧化钠溶于水、氧化钙和水生成粉末状氢氧化钙,隔板不起作用,D错误;故选A。
2.(2022·北京延庆·一模)实验室制备下列气体所选试剂、制备装置及收集方法均正确的是
气体 试剂 制备装置 收集方法A NH NH Cl a e
3 4
B Cl MnO +浓盐酸 b d
2 2
C NO Cu+浓HNO b f
2 3
D CH=CH C HOH+浓HSO c f
2 2 2 5 2 4
【答案】D
【解析】A.制备氨气应选用氯化铵和氢氧化钙固体,只用氯化铵无法制得氨气,A错误;B.浓盐酸与二
氧化锰需要加热才能反应生成氯气,制备装置应选用c,B错误;C.NO 会和水反应,不能用排水法收集,
2
C错误;D.乙醇与浓硫酸共热至170℃发生消去反应制取乙烯,所以制备装置选c,乙烯难溶于水,可以
用排水法收集,D正确;综上所述答案为D。
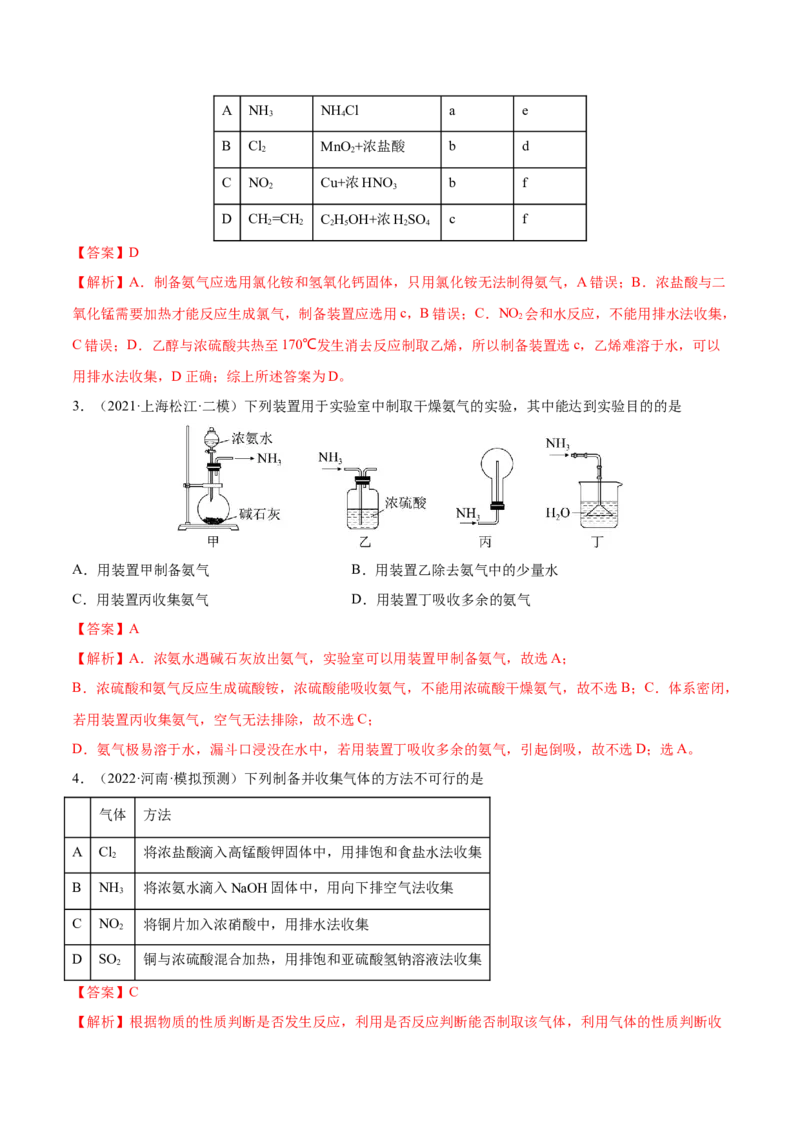
3.(2021·上海松江·二模)下列装置用于实验室中制取干燥氨气的实验,其中能达到实验目的的是
A.用装置甲制备氨气 B.用装置乙除去氨气中的少量水
C.用装置丙收集氨气 D.用装置丁吸收多余的氨气
【答案】A
【解析】A.浓氨水遇碱石灰放出氨气,实验室可以用装置甲制备氨气,故选A;
B.浓硫酸和氨气反应生成硫酸铵,浓硫酸能吸收氨气,不能用浓硫酸干燥氨气,故不选B;C.体系密闭,
若用装置丙收集氨气,空气无法排除,故不选C;
D.氨气极易溶于水,漏斗口浸没在水中,若用装置丁吸收多余的氨气,引起倒吸,故不选D;选A。
4.(2022·河南·模拟预测)下列制备并收集气体的方法不可行的是
气体 方法
A Cl 将浓盐酸滴入高锰酸钾固体中,用排饱和食盐水法收集
2
B NH 将浓氨水滴入NaOH固体中,用向下排空气法收集
3
C NO 将铜片加入浓硝酸中,用排水法收集
2
D SO 铜与浓硫酸混合加热,用排饱和亚硫酸氢钠溶液法收集
2
【答案】C
【解析】根据物质的性质判断是否发生反应,利用是否反应判断能否制取该气体,利用气体的性质判断收集的方法,不溶于水的气体可以利用排空气法,不与溶液反应的气体可以用排液法进行收集;A.浓盐酸
具有还原性,高锰酸钾具有强氧化性,两者发生氧化还原反应,可以生成氯气,而氯气在饱和食盐水中的
溶解度比较低,故可以排饱和食盐水收集,故A不符合题意;B.氢氧化钠溶于水放热,且导致溶液中氢
氧根离子浓度增大,导致氨气放出,因为氨气的密度比空气小,可以用向下排空气法收集,故B不符合题
意;C.二氧化氮与水会发生反应,故不能用排水法收集二氧化氮,故C符合题意;D.铜与浓硫酸发生
氧化还原反应生成二氧化硫,二氧化硫在亚硫酸氢钠溶液中溶解度比较小,故可以利用排饱和亚硫酸氢钠
溶液收集,故D不符合题意;故选答案C。
5.(2022·贵州铜仁·二模)用如图所示装置制备并收集气体,其中合理的是
选
反应物 制备的气体
项
A 稀盐酸+石灰石 CO
2
B 浓盐酸+MnO Cl
2 2
HNO (稀) +铜
C 3 NO
片
D HSO (稀) +Zn H
2 4 2
【答案】A
【解析】A.稀盐酸和石灰石反应为固体和液体反应,二氧化碳的密度大于空气,故用长管进短管处的连
接方式,故A正确;B.浓盐酸和二氧化锰反应制备氯气需要加热,故B错误;C.一氧化氮气体易于氧
气反应且密度与空气接近,故不能用排空气法收集,故C错误;D.氢气的密度小于空气,应该短管进长
管出,故D错误;故选A。
6.(2022·浙江绍兴·模拟预测)下列实验操作不正确的是
A.洗气 B.干燥气体 C.用水吸收NH D.排空气法收集H
3 2【答案】D
【解析】A.洗气气体从长导管进入液体中,短导管出,A正确;B.气体从导管处进入碱石灰中,经干燥
后从另一头出,B正确;C.氨气极易溶于水,图示装置可有效防止倒吸,C正确;D,收集H 应该用排水
2
集气法或者向下排空气法,图示装置错误,D错误;故答案选D。
7.(2022·上海上海·二模)实验室制取乙烯并验证其化学性质,下列装置正确的是
A.制备乙烯 B.除去杂质 C.验证加成反应 D.收集乙烯
【答案】C
【解析】A.用乙醇与浓硫酸混合液加热170℃,乙醇发生消去反应制备乙烯,要使用温度计测量溶液的温
度,因此温度计的水银球要在溶液的液面以下,A错误;B.用NaOH溶液除去制取乙烯的杂质SO 、CO
2 2
时,导气管应该是长进短出,导气管连接顺序反了,B错误;C.乙烯若与Br 发生加成反应,产生反应产
2
生1,2-二溴乙烷会溶解在四氯化碳中,使溶液橙色褪去,因此可以证明乙烯发生了加成反应,C正确;D.
乙烯与空气密度非常接近,气体容易与空气混合,导致不能收集到纯净气体,因此不能使用排空气方法收
集,应该使用排水方法收集,D错误;故合理选项是C。
8.(2022·广西广西·模拟预测)碳酰氯(COCl )俗名光气,熔点为-118°C,沸点为8.2°C,遇水迅速水解。
2
生成氯化氢。光气可由氯仿(CHCl )和氧气在光照条件下合成。下列说法错误的是
3A.装置丁中发生反应的化学方程式为2CHCl +O 2COCl + 2HCl
3 2 2
B.装置丙的主要作用是吸收尾气中的氯化氢
C.丁中冰水混合物的作用是降温,防止COCl 挥发
2
D.装置的连接顺序(装置可重复使用)应为c→a→b→e→f→a→b →d
【答案】D
【解析】光气可由氯仿(CHCl )和氧气在光照条件下合成,且光气遇水迅速水解,由实验装置可知,乙装置
3
制备氧气,然后经甲干燥氧气,在装置丁中合成光气,丁后面需连接干燥装置防止水进入丁中,最后连接
丙装置吸收尾气。A.装置丁中氯仿和氧气在光照条件下合成光气,反应的化学方程式为2CHCl +O
3 2
2COCl + 2HCl,故A正确;B.装置丁中生成氯化氢,氯化氢极易溶于水,倒扣的漏斗可防止倒吸,则装
2
置丙的主要作用是吸收尾气中的氯化氢,故B正确;C.COCl 的沸点为8.2°C,沸点较低易挥发,则冰水
2
混合物的作用是降温,防止COCl 挥发,故C正确;D.由上述分析可知,乙装置制备氧气,然后经甲干
2
燥氧气,在装置丁中合成光气,丁后面需连接干燥装置防止水进入丁中,最后连接丙装置吸收尾气,则装
置的连接顺序为c→b→a→e→f→b→a→d,故D错误;答案选D。
9.(2022·湖北·华中师大一附中模拟预测)化学是以实验为基础的自然科学。下列实验操作规范且能达到
实验目的的是
A.利用图甲制备SO 气体
2
B.利用图乙制备干燥的NO
2
C.利用图丙制备乙酸乙酯
D.利用图丁装置制备、干燥、收集氨
【答案】C
【解析】A.铜与浓硫酸反应需要加热,此装置没有加热仪器,故A错误;B.冷的浓硝酸与铁反应会发
生钝化,不能用来制备二氧化氮气体,故B错误;C.饱和碳酸钠溶液可中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度,使用干燥管可防止倒吸,故C正确;D.生石灰溶于水放热且与水反应生产氢氧化钙增大
氢氧根离子浓度,促使氨水产生氨气,氨用碱石灰来干燥,用向下排空气的方法可以收集氨,但需要将导
管伸入试管底部,故D错误;故选C。
10.(2022·江苏南通·模拟预测)NaClO是家用消毒液的有效成分,可通过Cl 与NaOH反应制得。NaClO
2
能与CO 反应生成HClO。常温下ClO 为黄绿色有毒气体,易溶于水。ClO 体积分数大于10%或其水溶液
2 2 2
在温度过高时可能发生爆炸,与碱反应生成ClO 和ClO 等。实验室制备ClO 的反应原理为
2
2KClO+H C O+H SO =2ClO ↑+2CO ↑+K SO +2H O。实验室用如图所示方法制备ClO 水溶液,下列说法
3 2 2 4 2 4 2 2 2 4 2 2
不正确的是
A.KClO 发生氧化反应 B.反应过程中需持续通入N
3 2
C.乙装置应置于冰水浴中 D.丙装置用于吸收ClO 尾气
2
【答案】A
【解析】甲装置用来制备ClO ,反应原理为题中所给化学方程式,其中KClO 作为氧化剂,草酸作为还原
2 3
剂。产生的ClO 进入乙装置中用水吸收得到其水溶液,丙装置的作用是吸收ClO ,防止污染空气。A.根
2 2
据分析,KClO 作为氧化剂,发生还原反应,A错误;B.ClO 体积分数大于10%时可能发生爆炸,所以
3 2
需要持续通入氮气稀释ClO ,B正确;C.ClO 水溶液在温度过高时可能发生爆炸,乙装置应在冰水浴中,
2 2
C正确;D.根据分析,丙装置用于吸收ClO 尾气,D正确;故选A。
2
11.(2022·重庆市育才中学模拟预测)下列实验装置能达到实验目的的是
A B C D
制备并收集NH 3 除去H 2 S中混 除去Cl 2 中的 收集干燥的NO 2 气体有的少量水蒸
HCl
气
【答案】A
【解析】A.浓氨水滴入CaO中,CaO与水反应放热,使氨气的溶解度降低,从而制得NH ,氨气的密度
3
比空气小,用向下排空气法收集,试管口塞一团棉花,以防止氨气与空气发生对应,尽快地收集到纯净的
NH ,A正确;B.HS具有较强的还原性,能被浓硫酸氧化,不能用浓硫酸干燥,B不正确;C.Cl 难溶
3 2 2
于饱和食盐水,HCl易溶于饱和食盐水,使用洗气法除去Cl 中混有的HCl时,导管应左长右短,C不正确;
2
D.NO 的密度比空气大,使用排空气法收集时,导管应左长右短,D不正确;故选A。
2
12.(2021·湖南·模拟预测)亚硝酰氯(ClNO)是有机物合成中的重要试剂,遇水反应生成一种氢化物和两
种氧化物。某学习小组用Cl 和NO利用如图所示装置制备亚硝酰氯(ClNO),下列说法正确的是
2
A.X装置可以随开随用,随关随停
B.Y装置中的药品可以换成浓硫酸
C.装入药品打开K 后,应先打开K 再打开K
2 1 3
D.若无装置Y,则Z中可能发生反应的化学方程式为2ClNO+HO=2HCl+NO↑+NO↑
2 2 3
【答案】A
【解析】A.X装置打开K,铜丝与硝酸接触反应生成的NO被排出。关闭K,NO不溶于稀硝酸,将液
1 1
面压到铜丝下方,反应停止,A项符合题意;B.Y装置中的药品若换成浓硫酸,则无法除去X中可能产
生的NO 等杂质,且U形管装置承装的干燥剂应为固体,B项不符合题意;C.实验时应先通入氯气赶走
2
装置内的空气,防止NO被氧化为NO ,C项不符合题意;D.方程式未配平,N元素不守恒,D项不符合
2
题意;故正确选项为A。
二、主观题(共3小题,共40分)
13.(2022·陕西·西北工业大学附属中学模拟预测)(13分)二氯化钒(VCl )有强还原性和吸湿性,熔点
2
为425℃、沸点为900℃,是制备多种医药、催化剂、含钒化合物的中间体。某学习小组在实验室制备
VCl 并进行相关探究。回答下列问题:
2(1)小组同学通过VCl 分解制备VCl 。
3 2
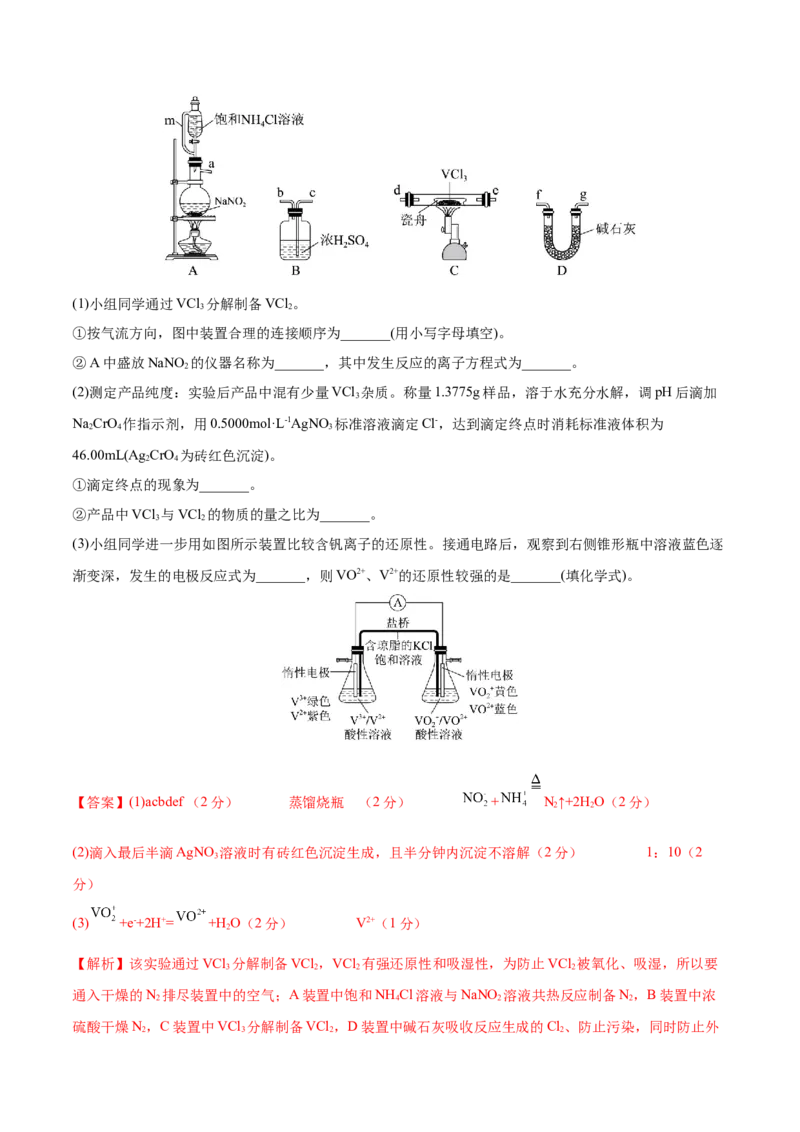
①按气流方向,图中装置合理的连接顺序为_______(用小写字母填空)。
②A中盛放NaNO 的仪器名称为_______,其中发生反应的离子方程式为_______。
2
(2)测定产品纯度:实验后产品中混有少量VCl 杂质。称量1.3775g样品,溶于水充分水解,调pH后滴加
3
NaCrO 作指示剂,用0.5000mol·L-1AgNO 标准溶液滴定Cl-,达到滴定终点时消耗标准液体积为
2 4 3
46.00mL(Ag CrO 为砖红色沉淀)。
2 4
①滴定终点的现象为_______。
②产品中VCl 与VCl 的物质的量之比为_______。
3 2
(3)小组同学进一步用如图所示装置比较含钒离子的还原性。接通电路后,观察到右侧锥形瓶中溶液蓝色逐
渐变深,发生的电极反应式为_______,则VO2+、V2+的还原性较强的是_______(填化学式)。
【答案】(1)acbdef (2分) 蒸馏烧瓶 (2分) + N↑+2H O(2分)
2 2
(2)滴入最后半滴AgNO 溶液时有砖红色沉淀生成,且半分钟内沉淀不溶解(2分) 1:10(2
3
分)
(3) +e-+2H+= +H O(2分) V2+(1分)
2
【解析】该实验通过VCl 分解制备VCl ,VCl 有强还原性和吸湿性,为防止VCl 被氧化、吸湿,所以要
3 2 2 2
通入干燥的N 排尽装置中的空气;A装置中饱和NH Cl溶液与NaNO 溶液共热反应制备N,B装置中浓
2 4 2 2
硫酸干燥N,C装置中VCl 分解制备VCl ,D装置中碱石灰吸收反应生成的Cl、防止污染,同时防止外
2 3 2 2界空气进入C装置中;据此作答。
(1)①根据分析,按气流方向,图中装置的合理顺序为acbdef;答案为:acbdef。
②根据A中盛放NaNO 溶液的仪器特点可知,其名称为蒸馏烧瓶;其中发生的反应为NH Cl与NaNO 共
2 4 2
热反应生成N、NaCl和水,反应的离子方程式为 + N↑+2H O;答案为:蒸馏烧瓶; +
2 2 2
N↑+2H O。
2 2
(2)①该滴定实验的原理为Ag++Cl-=AgCl↓,当Cl-完全反应,再滴入半滴AgNO 标准溶液,AgNO 与指示
3 3
剂NaCrO 作用产生砖红色沉淀,故滴定终点的现象为:滴入最后半滴AgNO 溶液时有砖红色沉淀生成,
2 4 3
且半分钟内沉淀不溶解;答案为:滴入最后半滴AgNO 溶液时有砖红色沉淀生成,且半分钟内沉淀不溶解。
3
②根据滴定的原理,2n(VCl )+3n(VCl )=n(AgNO)=0.5000mol/L×0.046L,122g/moln(VCl )+157.5g/
2 3 3 2
moln(VCl )=1.3775g,解得n(VCl )=0.01mol、n(VCl )=0.001mol,产品中VCl 与VCl 物质的量之比为
3 2 3 3 2
0.001mol:0.01mol=1:10;答案为:1:10。
(3)接通电路后,右侧锥形瓶中溶液蓝色逐渐变深, 得电子被还原成VO2+,右侧为正极,电极反应式
为 +e-+2H+= +H O;左侧发生失电子的氧化反应,左侧为负极,电极反应式为V2+-e-=V3+;总反应
2
为V2++ +2H+=V3++VO2++H O,V2+为还原剂,VO2+为还原产物。根据还原剂的还原性强于还原产物的
2
还原性,VO2+、V2+的还原性较强的是V2+;答案为: +e-+2H+= +H O;V2+。
2
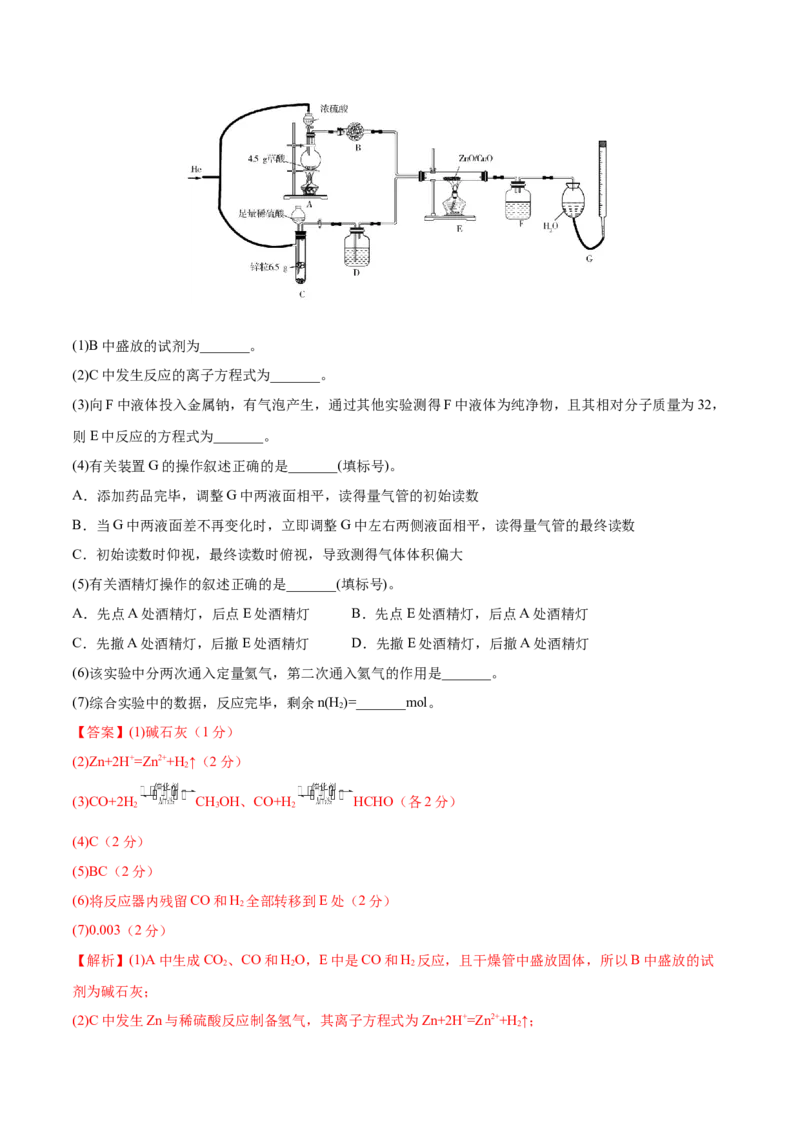
14.(2022·重庆·模拟预测)(15分)某同学在实验室采用下列装置探究CO和H 的转化,并检验部分产
2
物。已知草酸(HOOC−COOH)在浓硫酸存在时加热分解为CO、CO和HO,E中的ZnO/CuO仅作催化剂,
2 2
实验完毕,F中收集到纯净液体1.536 g,G中收集到的气体体积为89.6 mL(折算成标准状况,不包括通入
的氦气)。请回答下列问题:(1)B中盛放的试剂为_______。
(2)C中发生反应的离子方程式为_______。
(3)向F中液体投入金属钠,有气泡产生,通过其他实验测得F中液体为纯净物,且其相对分子质量为32,
则E中反应的方程式为_______。
(4)有关装置G的操作叙述正确的是_______(填标号)。
A.添加药品完毕,调整G中两液面相平,读得量气管的初始读数
B.当G中两液面差不再变化时,立即调整G中左右两侧液面相平,读得量气管的最终读数
C.初始读数时仰视,最终读数时俯视,导致测得气体体积偏大
(5)有关酒精灯操作的叙述正确的是_______(填标号)。
A.先点A处酒精灯,后点E处酒精灯 B.先点E处酒精灯,后点A处酒精灯
C.先撤A处酒精灯,后撤E处酒精灯 D.先撤E处酒精灯,后撤A处酒精灯
(6)该实验中分两次通入定量氦气,第二次通入氦气的作用是_______。
(7)综合实验中的数据,反应完毕,剩余n(H )=_______mol。
2
【答案】(1)碱石灰(1分)
(2)Zn+2H+=Zn2++H ↑(2分)
2
(3)CO+2H CHOH、CO+H HCHO(各2分)
2 3 2
(4)C(2分)
(5)BC(2分)
(6)将反应器内残留CO和H 全部转移到E处(2分)
2
(7)0.003(2分)
【解析】(1)A中生成CO、CO和HO,E中是CO和H 反应,且干燥管中盛放固体,所以B中盛放的试
2 2 2
剂为碱石灰;
(2)C中发生Zn与稀硫酸反应制备氢气,其离子方程式为Zn+2H+=Zn2++H ↑;
2(3)向F中液体投入钠块,有气泡产生,且相对分子质量为32,则该物质是甲醇,所以E中反应的化学方程
式为CO+2H CHOH,根据实验数据,初始n(CO)=0.05 mol,初始n(H )=0.1 mol,生成
2 3 2
n(CHOH)=0.048 mol,剩余CO和H 共0.004 mol,如果CO和H 反应只生成CHOH,应该剩余CO和H
3 2 2 3 2
共0.006 mol,减少的0.002 mol气体是发生了CO+H HCHO,且产物甲醛极易溶于水,故答案为:
2
CO+2H CHOH;CO+H HCHO;
2 3 2
(4)A.添加药品完毕,调整G中两液面相平之前,应该先通入氦气赶走反应装置内的空气,避免发生爆炸,
故A错误;B.当G中两液面差不再变化时,应该等气体恢复到室温时,再调整G中两液面相平,读得量
气管的最终读数,故B错误;C.初始读数时仰视,最终读数时俯视,在量气管上的高度差变高,导致测
得气体体积偏大,故C正确;故选C;
(5)有关酒精灯操作的叙述,先点E处的酒精灯,让过来的CO和H 立即反应,后撤E处的酒精灯,因为第
2
二次通氦气的目的是将反应器残留的CO和H 赶到E处反应,不能没有加热条件,因此正确的是BC;
2
(6)该实验中分两次通入定量氦气,第二次通入氦气的作用是将反应器残留的CO和H 赶到E处反应,否则
2
定量实验测定的数据不准确;
(7)综合实验中的数据,CO+2H CHOH,生成甲醇0.048 mol,CO+H HCHO,生成甲醛
2 3 2
0.001 mol,所以反应完毕,剩余n(H )为0.003mol。
2
15.(2022·天津·模拟预测)(12分)SO 和焦亚硫酸钠(Na SO)可用作食品添加剂。回答下列问题:
2 2 2 5
(1)实验室用HSO 和NaHSO 制取SO 的化学方程式为_______。欲净化与收集SO ,选择必要装置,按气
2 4 3 2 2
流方向连接顺序为_______(填仪器接口的字母编号)。
(2)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
已知:2NaHSO NaSO+H O。
3 2 2 5 2
试剂:稀盐酸、稀HSO 、稀HNO、BaCl 溶液、酸性KMnO 溶液、HO 溶液
2 4 3 2 4 2 2
实验编
实验步骤 现象 结论
号I 取少量样品,加入除氧蒸馏水 固体完全溶解得到无色溶液 /
II 取实验I的溶液,_______ _______ 样品已氧化变质
III 另取实验I的溶液,_______ _______ 样品未完全氧化变质
(3)某小组利用下列装置测定空气中SO 的含量。
2
已知该反应的化学方程式为:SO +I +2H O=HSO +2HI。若空气流速为a m3·min-1,当观察到_______时,
2 2 2 2 4
结束计时,测定耗时t min。假定样品中的SO 可被溶液充分吸收,该空气样品中SO 的含量是
2 2
_______mg·m-3。
【答案】(1) HSO +2NaHSO =Na SO +2H O+2SO ↑ (2分) baefgh(2分)
2 4 3 2 4 2 2
(2) 向其中加入足量稀盐酸,振荡、静置,然后滴加BaCl 溶液 (2分) 出现白色沉淀(1
2
分) 酸性KMnO 溶液(1分) 溶液褪色(1分)
4
(3)蓝色变为无色(1分) (2分)
【解析】HSO 和NaHSO 发生复分解反应制取SO ,装置连接顺序按照制取气体、净化、收集,尾气处理
2 4 3 2
连接。在检验物质成分时,若样品已经变质,则溶液中含有 ,可根据BaSO 是白色既不溶于水也不溶
4
于酸的性质检验;若样品为完全变质,则溶液中含有 ,该物质具有还原性,能够被酸性KMnO 溶液
4
氧化而使溶液褪色,据此判断。在测定空气中SO 的含量时,可根据方程式SO +I +2H O=HSO +2HI中物
2 2 2 2 2 4
质转化关系,n(SO )=n(I),结合m=n·M计算SO 的质量,再结合空气的流速及通气时间计算该空气样品中
2 2 2
SO 的含量。
2
(1)实验室用HSO 和NaHSO 发生复分解反应制取SO ,该反应的化学方程式为:
2 4 3 2
HSO +2NaHSO =Na SO +2H O+2SO ↑;
2 4 3 2 4 2 2
实验室用上述方法制取的SO 中含有水蒸气,可浓硫酸吸收,导气管长进短出。然后根据SO 气体的密度
2 2
比空气大,用向上排空气的方法收集,多余气体用碱石灰吸收,故装置按气流方向连接顺序为baefgh;(2)II.取少量实验I的溶液,溶于足量稀盐酸,振荡、静置,滴加BaCl 溶液,若出现沉淀,则样品已氧化
2
变质;
III.另取实验I的溶液,向其中加入酸性KMnO 溶液,充分振荡,若观察到酸性KMnO 溶液褪色,说明
4 4
溶液中含有焦亚硫酸钠,即样品未完全氧化变质;
(3)在100 mL0.1000 mol/L碘溶液中含有溶质I 的物质的量n(I)=0.1000 mol/L×0.1 L=0.0100 mol,含有SO
2 2 2
的空气不断通入碘水中,发生反应:SO +I +2H O=HSO +2HI,当碘水中I 恰好消耗完全时,含有淀粉的
2 2 2 2 4 2
I 溶液蓝色消失,此时停止通入空气,达到滴定终点,根据物质转化关系可知:n(SO )=n(I)=0.0100 mol,
2 2 2
m(SO )=0.0100 mol×64 g/mol=0.6400 g=640 mg,通入空气的体积V=a m3·min-1×t min=at m3,故该空气样品
2
中SO 的含量是: 。
2