文档内容
主题七 化学实验测试(一)
(考试时间:75 分钟 试卷满分:100 分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 Na-23 K-39 Cr-52 Mn-55
第Ⅰ卷(选择题 共 45 分)
一、选择题(本题共 15 个小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符合
题目要求的)
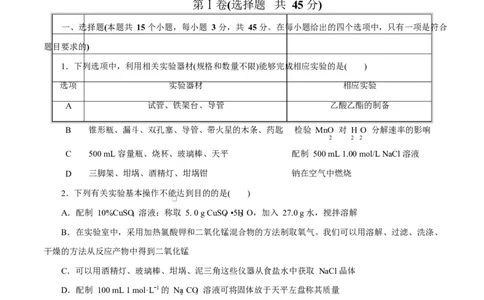
1.下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是( )
选项 实验器材 相应实验
A 试管、铁架台、导管 乙酸乙酯的制备
B 锥形瓶、漏斗、双孔塞、导管、带火星的木条、药匙 检验 MnO 对 H O 分解速率的影响
2 2 2
C 500 mL 容量瓶、烧杯、玻璃棒、天平 配制 500 mL 1.00 mol/L NaCl 溶液
D 三脚架、坩埚、酒精灯、坩埚钳 钠在空气中燃烧
2.下列有关实验基本操作不能达到目的的是( )
A.配制 10%CuSO 溶液:称取 5. 0 g CuSO •5H O,加入 27.0 g 水,搅拌溶解
4 4 2
B.在实验室中,采用加热氯酸钾和二氧化锰混合物的方法制取氧气。我们可以用溶解、过滤、洗涤、
干燥的方法从反应产物中得到二氧化锰
C.可以用酒精灯、玻璃棒、坩埚、泥三角这些仪器从食盐水中获取 NaCl 晶体
D.配制 100 mL 1 mol·Lˉ1 的 Na CO 溶液可将固体放于天平左盘称其质量
2 3
3.下列有关实验的说法正确的是( )
A.为了防止 KMnO 溶液对磨砂处氧化,须用碱式滴定管量取 20.00mL 该溶液
4
B.当振荡分液漏斗中的混合溶液时,须用一只手压住分液漏斗的玻璃塞,另一只手握住旋塞,将分液漏斗倒转过来,用
力振荡
C.做“钠与水的反应”实验时,切取绿豆大小的金属钠,用滤纸吸干其表面的煤油,放入烧杯中,滴入
两滴酚酞溶液,再加入少量水,然后观察并记录实验现象
D.在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起
始温度,充分反应后再读出并记录反应体系的最高温度
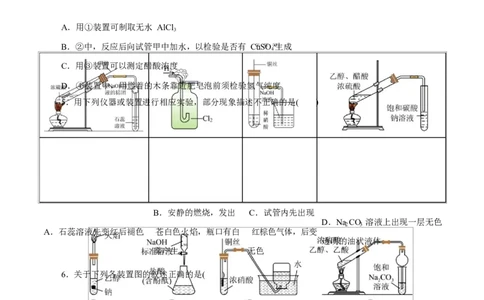
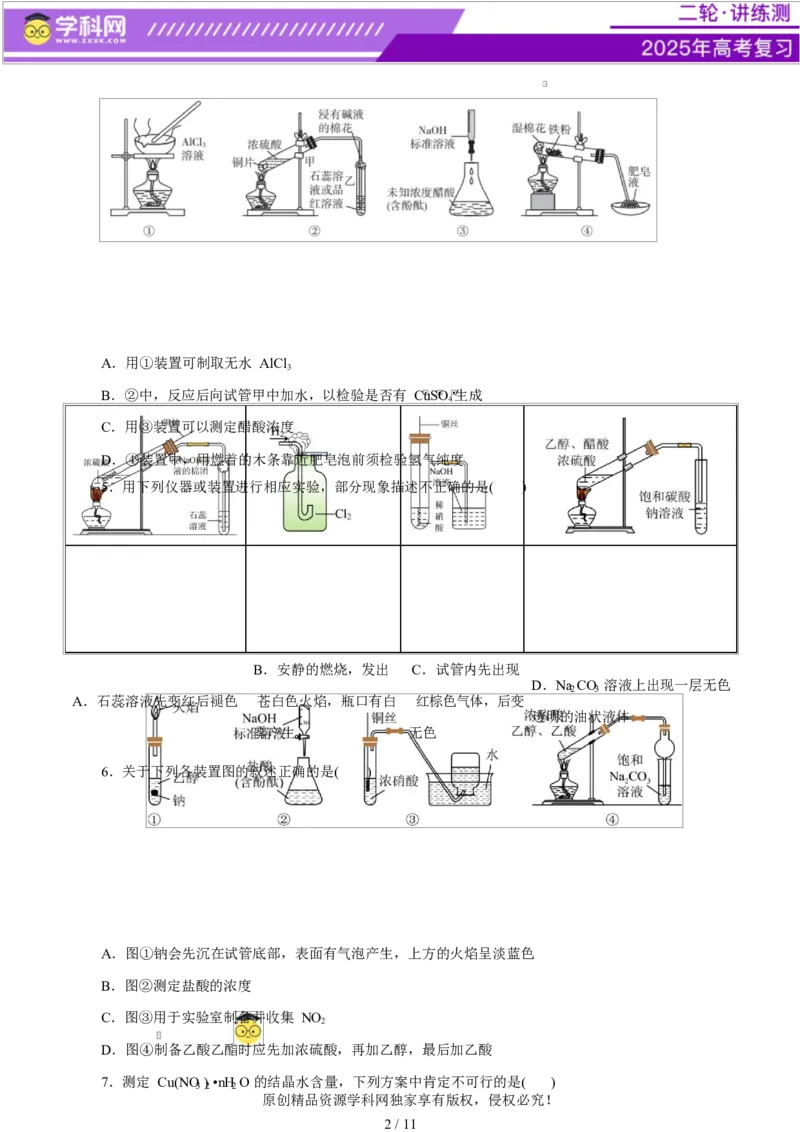
4.下列关于实验操作说法正确的是( )
原创精品资源学科网1独 / 1家1享有版权,侵权必究!A.用①装置可制取无水 AlCl
3
B.②中,反应后向试管甲中加水,以检验是否有 CuSO 生成
4
C.用③装置可以测定醋酸浓度
D.④装置中,用燃着的木条靠近肥皂泡前须检验氢气纯度
5.用下列仪器或装置进行相应实验,部分现象描述不正确的是( )
B.安静的燃烧,发出 C.试管内先出现
D.Na CO 溶液上出现一层无色
2 3
A.石蕊溶液先变红后褪色 苍白色火焰,瓶口有白 红棕色气体,后变
透明的油状液体
雾产生 无色
6.关于下列各装置图的叙述正确的是( )
A.图①钠会先沉在试管底部,表面有气泡产生,上方的火焰呈淡蓝色
B.图②测定盐酸的浓度
C.图③用于实验室制备并收集 NO
2
D.图④制备乙酸乙酯时应先加浓硫酸,再加乙醇,最后加乙酸
7.测定 Cu(NO ) •nH O 的结晶水含量,下列方案中肯定不可行的是( )
3 2 2
原创精品资源学科网独家享有版权,侵权必究!
2 / 11A.称量样品→加热→冷却→称量 CuO
B.称量样品→加热→冷却→称量 Cu(NO )
3 2
C.称量样品→加热→用已知质量的无水氯化钙吸收水蒸气并称量
D.称量样品→加 NaOH→过滤→加热→冷却→称量 CuO
8.下列各实验的原理、操作、现象和结论均完全正确的是
A.证明某红棕色气体是溴蒸气还是 NO ,可用 AgNO 溶液检验,观察是否有沉淀生成
2 3
B.将点燃的镁条迅速投入到集满 CO 的集气瓶中,观察到镁条在集气瓶底部继续燃烧
2
C.实验室用氢氧化钠标准溶液滴定未知浓度的醋酸溶液时,选用甲基橙做指示剂
D.向盛有 5mL 苯酚溶液的试管中滴入 2~3 滴稀溴水,边加边振荡,立即观察到有白色沉淀生成
9.根据下列化学实验事实得出的结论一定正确的是( )
A.向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解。结论:该溶液
中有 SO2-4
B.向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润的蓝色石蕊试纸变红。结论:该溶
液中有 NH+4
C.向 1 mL 浓度均为 0.05 mol·L-1 的 NaCl、NaI 混合溶液中滴加 2 滴 0.01 mol·L-1 的 AgNO 溶液,
3
振荡,沉淀呈黄色。结论:K (AgCl)>K (AgI)
sp sp
D.向 1 mL 1%的 NaOH 溶液中加入 2 mL 2%的 CuSO 溶液,振荡后再加入 0.05 mL 有机物 X,加热
4
后
未出现红色沉淀。结论:X 中不含有醛基
10.对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定含有 CO2-
3
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有 SO 2-
4
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有 NH 4+
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有 Ba2+
11.实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去)
下列说法正确的是( )
原创精品资源学科网3独 / 1家1享有版权,侵权必究!A.玻璃纤维的作用是防止 E 装置中液体倒吸入 D 装置中
B.E 装置中液体用于吸收多余的氯气和氯化氢
C.要使 B 装置中产生氯气,应先加热圆底烧瓶,再滴加浓盐酸
D.实验中加热的先后顺序为先加热硬质玻璃管 D,再加热圆底烧瓶 B
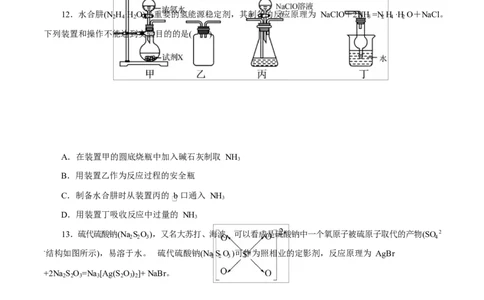
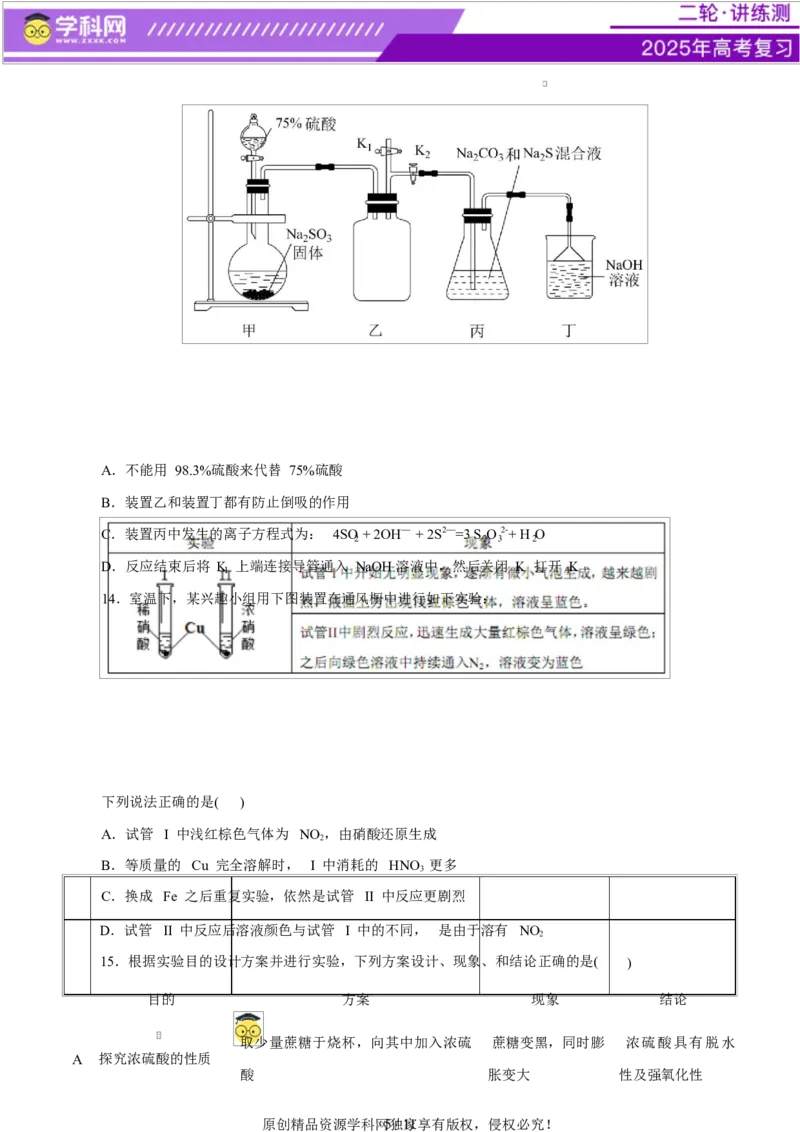
12.水合肼(N H ·H O)是重要的氢能源稳定剂,其制备的反应原理为 NaClO+2NH =N H ·H O+NaCl。
2 4 2 3 2 4 2
下列装置和操作不能达到实验目的的是( )
A.在装置甲的圆底烧瓶中加入碱石灰制取 NH
3
B.用装置乙作为反应过程的安全瓶
C.制备水合肼时从装置丙的 b 口通入 NH
3
D.用装置丁吸收反应中过量的 NH
3
13.硫代硫酸钠(Na S O ),又名大苏打、海波,可以看成是硫酸钠中一个氧原子被硫原子取代的产物(SO 2
2 2 3 4
-结构如图所示),易溶于水。 硫代硫酸钠(Na S O )可作为照相业的定影剂,反应原理为 AgBr
2 2 3
+2Na S O =Na [Ag(S O ) ]+ NaBr。
2 2 3 3 2 3 2
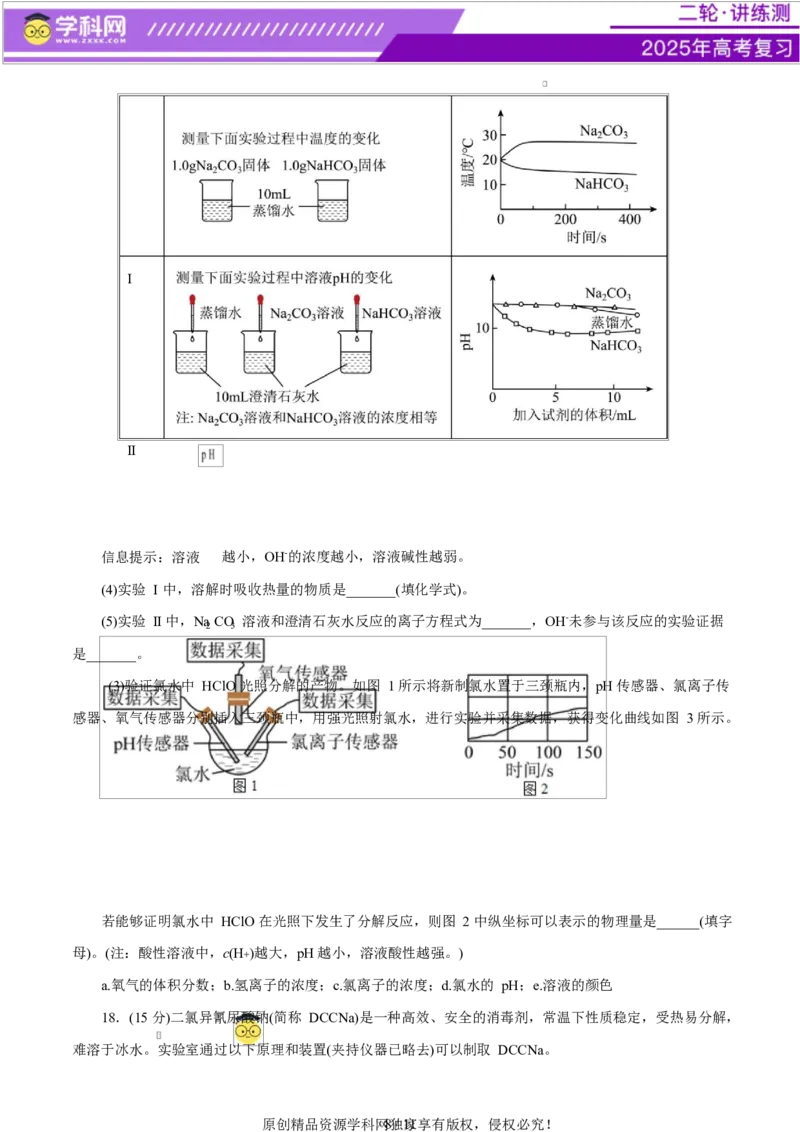
下图是实验室模拟工业制备 Na S O 的装置示意图,下列说法不正确的是( )
2 2 3
原创精品资源学科网4独 / 1家1享有版权,侵权必究!A.不能用 98.3%硫酸来代替 75%硫酸
B.装置乙和装置丁都有防止倒吸的作用
C.装置丙中发生的离子方程式为: 4SO + 2OH— + 2S2—=3 S O 2-+ H O
2 2 3 2
D.反应结束后将 K 上端连接导管通入 NaOH 溶液中,然后关闭 K 打开 K
1 2 1
14.室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
下列说法正确的是( )
A.试管 I 中浅红棕色气体为 NO ,由硝酸还原生成
2
B.等质量的 Cu 完全溶解时, I 中消耗的 HNO 更多
3
C.换成 Fe 之后重复实验,依然是试管 II 中反应更剧烈
D.试管 II 中反应后溶液颜色与试管 I 中的不同, 是由于溶有 NO
2
15.根据实验目的设计方案并进行实验,下列方案设计、现象、和结论正确的是( )
目的 方案 现象 结论
取少量蔗糖于烧杯,向其中加入浓硫 蔗糖变黑,同时膨 浓硫酸具有脱水
A 探究浓硫酸的性质
酸 胀变大 性及强氧化性
原创精品资源学科网5独 / 1家1享有版权,侵权必究!取相同的 Na S O 和 H SO 分别在冷
2 2 3 2 4
探究温度对化学反 热水组产生气泡的 高温可以加快反
B 水 和 热 水 中 存 放 , 一 段 时 间
应速率的影响 后 将 速率快 应速率
Na S O 和 H SO 混合
2 2 3 2 4
比 较 相 同 浓 度 的 用洁净干燥的玻璃棒蘸取同浓度
的 CuSO 溶液对应的 CuSO 溶液的酸性
4 4
C CuSO 和 MgSO 溶 CuSO 和 MgSO 溶液,滴在 pH 试纸
4 4 4 4
pH 更小 更强
液的酸碱性 上,并与标准比色卡对比
将集满臭氧的两支试管分别用铁架台 倒置在盛有水的烧 臭 氧 是 极 性
分
D 探究臭氧的极性 固定并倒置在盛有水和 CCl 的两个烧 杯中的试管液面上 子,在极性溶剂中
4
杯中 升较高 溶解度大
第 II 卷(非选择题 共 55
分)
二、填空题(本题共 4 小题,共 55 分)
16.(13 分)FeCl 在工业上常作催化剂和刻蚀剂。实验室中,先合成 SOCl ,再与 FeCl ·6H O 反应制备
3 2 3 2
无水 FeCl,所用装置如下图所示(加热及夹持仪器略)。
3
已知:①SO +PCl POCl + SOCl ;
2 5
3 2
②SOCl 的熔点为-101℃,沸点为 75.6℃,易水解;POCl 沸点为 105℃。
2 3
回答下列问题:
(1)仪器乙的名称是 。
(2)写出一个 FeCl 作催化剂的化学方程式 。
3
(3)按气体的流向将装置连接起来:
a→h→( )→( )→( )→d→( )→( )→( )→j
(4)下列说法正确的是_______。
原创精品资源学科网6独 / 1家1享有版权,侵权必究!A.打开 K 前,需打开 K 和将三通阀调至
1 2
B.丙装置中盛放的是无水氯化钙
C.乙中盛放的是 98%的浓硫酸
D.实验过程中需要将温度计水银球调至三颈烧瓶的瓶口处
(5)制得的 FeCl 可以用来制备铁强化盐。市售铁强化盐中铁含量测定:
3
已知:a.铁强化盐含有 NaCl、KIO 、NaFeY,其中 n(KIO ):n(NaFeY)=1:50
3 3
b.I +2S O 2-=S O 2-+2I-
2 2 3 4 6
c.NaFeY 能溶解在稀硫酸中,其中的铁元素会完全转化为 Fe3+
称取 mg 样品,加稀硫酸溶解后配成 100mL 溶液。取出 10.00mL,加入稍过量的 KI 溶液,充分反应后,
滴入淀粉溶液,cmol·L-1 Na S O 标准液滴定,重复操作 2~3 次,消耗 Na S O 标准液平均值为 VmL。
2 2 3 2 2 3
①若用移液管取出 10.00mL 所配溶液,从移液管中将其放出的操作是 。
②样品中铁元素的质量分数为 。
17.(14 分)现代传感信息技术在化学实验中有广泛的应用.某兴趣小组用传感技术开展研究。
(1)利用压强传感器和 CO 传感器设计了如图甲、乙两个实验装置,甲的注射器中装有过量的 NaOH 溶
2
液,乙的注射器中装有等体积的水,实验时将两装置注射器中的液体全部推入烧瓶中,试验后,得到了压
强随时间变化的曲线(如图丙)
①设计实验乙的目的是_______。
②图丙中曲线_______(选填“I”或“II”)表示 CO 和 NaOH 溶液的反应,写出该反应的离子反应方程
2
式
_______。
③两烧瓶中的压强在开始阶段均增大的原因是_______。
(2)为进一步探究 Na CO 和 NaHCO 的性质,利用传感器继续做如下实验:
2 3 3
编号 实验操作 实验数据
原创精品资源学科网7独 / 1家1享有版权,侵权必究!I
II
信息提示:溶液 越小,OH-的浓度越小,溶液碱性越弱。
(4)实验 I 中,溶解时吸收热量的物质是_______(填化学式)。
(5)实验 II 中,Na CO 溶液和澄清石灰水反应的离子方程式为_______,OH-未参与该反应的实验证据
2 3
是_______。
(3)验证氯水中 HClO 光照分解的产物。如图 1 所示将新制氯水置于三颈瓶内,pH 传感器、氯离子传
感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得变化曲线如图 3 所示。
若能够证明氯水中 HClO 在光照下发生了分解反应,则图 2 中纵坐标可以表示的物理量是______(填字
母)。(注:酸性溶液中,c(H+)越大,pH 越小,溶液酸性越强。)
a.氧气的体积分数;b.氢离子的浓度;c.氯离子的浓度;d.氯水的 pH;e.溶液的颜色
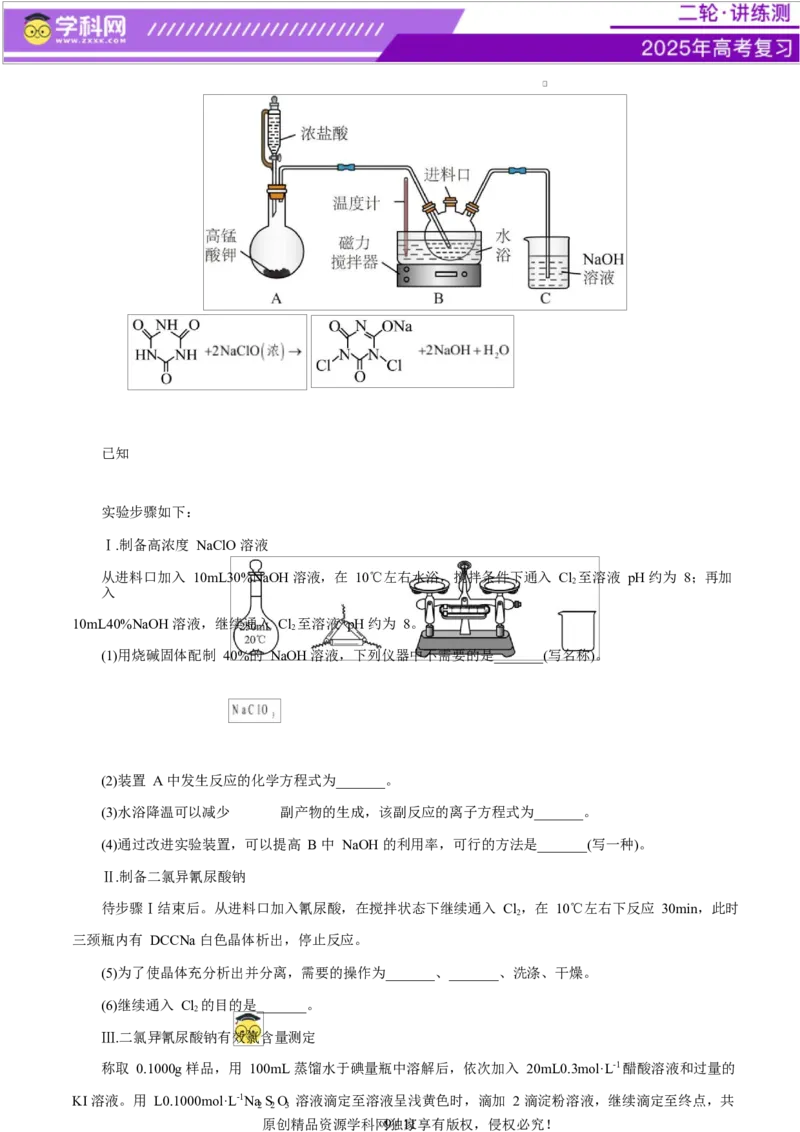
18.(15 分)二氯异氰尿酸钠(简称 DCCNa)是一种高效、安全的消毒剂,常温下性质稳定,受热易分解,
难溶于冰水。实验室通过以下原理和装置(夹持仪器已略去)可以制取 DCCNa。
原创精品资源学科网8独 / 1家1享有版权,侵权必究!已知
实验步骤如下:
Ⅰ.制备高浓度 NaClO 溶液
从进料口加入 10mL30%NaOH 溶液,在 10℃左右水浴,搅拌条件下通入 Cl 至溶液 pH 约为 8;再加
2
入
10mL40%NaOH 溶液,继续通入 Cl 至溶液 pH 约为 8。
2
(1)用烧碱固体配制 40%的 NaOH 溶液,下列仪器中不需要的是_______(写名称)。
(2)装置 A 中发生反应的化学方程式为_______。
(3)水浴降温可以减少 副产物的生成,该副反应的离子方程式为_______。
(4)通过改进实验装置,可以提高 B 中 NaOH 的利用率,可行的方法是_______(写一种)。
Ⅱ.制备二氯异氰尿酸钠
待步骤Ⅰ结束后。从进料口加入氰尿酸,在搅拌状态下继续通入 Cl,在 10℃左右下反应 30min,此时
2
三颈瓶内有 DCCNa 白色晶体析出,停止反应。
(5)为了使晶体充分析出并分离,需要的操作为_______、_______、洗涤、干燥。
(6)继续通入 Cl 的目的是_______。
2
Ⅲ.二氯异氰尿酸钠有效氯含量测定
称取 0.1000g 样品,用 100mL 蒸馏水于碘量瓶中溶解后,依次加入 20mL0.3mol·L-1 醋酸溶液和过量的
KI 溶液。用 L0.1000mol·L-1Na S O 溶液滴定至溶液呈浅黄色时,滴加 2 滴淀粉溶液,继续滴定至终点,共
2 2 3
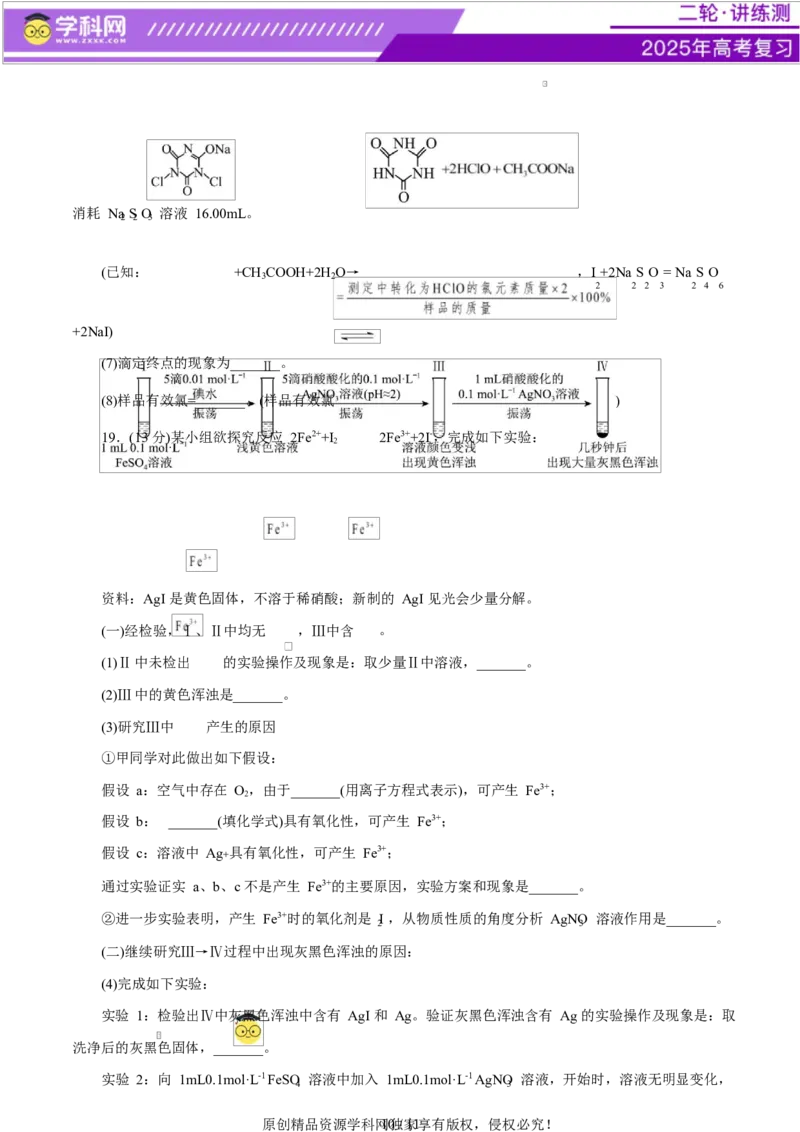
原创精品资源学科网9独 / 1家1享有版权,侵权必究!消耗 Na S O 溶液 16.00mL。
2 2 3
(已知: +CH COOH+2H O→ ,I +2Na S O = Na S O
3 2
2 2 2 3 2 4 6
+2NaI)
(7)滴定终点的现象为_______。
(8)样品有效氯=_______。(样品有效氯 )
19.(13 分)某小组欲探究反应 2Fe2++I 2Fe3++2I-,完成如下实验:
2
资料:AgI 是黄色固体,不溶于稀硝酸;新制的 AgI 见光会少量分解。
(一)经检验,Ⅰ、Ⅱ中均无 ,Ⅲ中含 。
(1)Ⅱ中未检出 的实验操作及现象是:取少量Ⅱ中溶液,_______。
(2)Ⅲ中的黄色浑浊是_______。
(3)研究Ⅲ中 产生的原因
①甲同学对此做出如下假设:
假设 a:空气中存在 O,由于_______(用离子方程式表示),可产生 Fe3+;
2
假设 b: _______(填化学式)具有氧化性,可产生 Fe3+;
假设 c:溶液中 Ag+ 具有氧化性,可产生 Fe3+;
通过实验证实 a、b、c 不是产生 Fe3+的主要原因,实验方案和现象是_______。
②进一步实验表明,产生 Fe3+时的氧化剂是 I ,从物质性质的角度分析 AgNO 溶液作用是_______。
2 3
(二)继续研究Ⅲ→Ⅳ过程中出现灰黑色浑浊的原因:
(4)完成如下实验:
实验 1:检验出Ⅳ中灰黑色浑浊中含有 AgI 和 Ag。验证灰黑色浑浊含有 Ag 的实验操作及现象是:取
洗净后的灰黑色固体,_______。
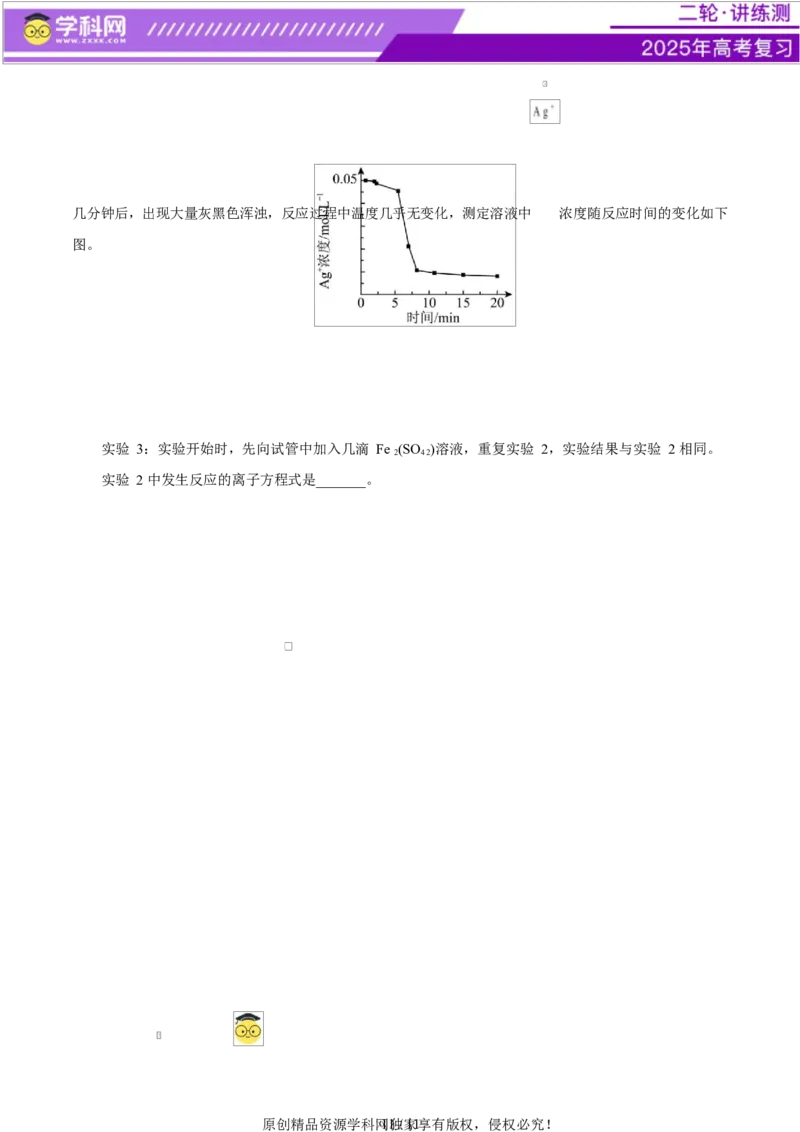
实验 2:向 1mL0.1mol·L-1 FeSO 溶液中加入 1mL0.1mol·L-1 AgNO 溶液,开始时,溶液无明显变化,
4 3
原创精品资源学科网10独 / 家11享有版权,侵权必究!几分钟后,出现大量灰黑色浑浊,反应过程中温度几乎无变化,测定溶液中 浓度随反应时间的变化如下
图。
实验 3:实验开始时,先向试管中加入几滴 Fe (SO )溶液,重复实验 2,实验结果与实验 2 相同。
2 4 2
实验 2 中发生反应的离子方程式是_______。
原创精品资源学科网11独 / 家11享有版权,侵权必究!