文档内容
2010 年全国初中化学素质和实验能力竞赛
湖北赛区初赛试题
说明:
1.本试卷共8页,包括第Ⅰ卷和第Ⅱ卷,第Ⅰ卷为选择题,共40分;第Ⅱ卷为非选择题,共60
分,全卷满分100分。
2.可能用到的相对原子质量:
H—1 C—12 N—14 O—16 S—32 Cl—35.5 Na—23 Al—27
K—39 Ca—40 Mn—55 Fe——56 Cu—64 Zn—65 Ag—108 Ba—137
3.考试时间:120分钟
第Ⅰ卷(选择题,共40分)
一、选择题(本题包括20个小题,每小题2分,共40分。每小题有1个或2个选项符合题意。
若有两个答案的错1 个不得分,漏选1个扣1 分。)
1.古诗词是古人为我们留下的宝贵精神财富。下列诗句中只涉及物理变化的是
A.野火烧不尽,春风吹又生 B.春蚕到死丝方尽,蜡炬成灰泪始干
C.只要功夫深,铁杵磨成针 D.爆竹声中一岁除,春风送暖入屠苏
2.实验室使用大理石和盐酸反应制取的CO 是不纯净的,为证明该气体中含有多种物质,所
2
用的试剂及使用顺序正确的是
A.无水硫酸铜、硝酸银溶液、石灰水 B.浓硫酸、氢氧化钠溶液、石灰水
C.硝酸银溶液、石灰水、无水硫酸铜 D.氯化钙、石蕊试液、水
3.由石灰石、水、苏打为原料制取烧碱的过程中,未发生的化学反应类型是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
4.下列实验中所选用的仪器或操作合理的是
A.用托盘天平称量5.85g氯化钠晶体 B.用酸式滴定管量取25.00mL酸性高锰酸钾
C.用湿润pH试纸测定某HSO 溶液的pH D.用瓷坩埚(含有二氧化硅)灼烧碳酸钠晶体
2 4
5.“绿色绿色是将反应物全部转化为期望的产物,使原子的利用率达到100%,以昼减少有害
物质生成的化学工艺理念。下列符合“绿色化学”要求的是
A.湿法冶铜:Fe+CuSO=FeSO+Cu
4 4
B.高炉炼铁:FeO+3CO=2Fe+3CO
2 3 2
△
C.制氧气:2KMnO KMnO+MnO+O↑
4 2 4 2 2
D.用乙烯(CH)为原料制取乙二醇(CHO):CH+HO→CHO
2 4 2 6 2 2 4 2 2 2 6 2
6.下列说法中,你认为科学的是
A. 臭氧在一定条件下能转化为有毒气体B.多吃腌制食品能防癌
C.生理盐水含食盐的量越高越好 D.活性炭可以制作冰箱的除味剂
7.同学们在做实验时发现,将镁条放入某CuCl 溶液中,镁条表面有气泡产生。对于这一“异
2
常现象”产生原因,同学们设计了以下探究方案进行讨论。其中没有意义的是
A.甲同学推测该气体可能是H,于是收集气体并检测该气体
2
B.乙同学猜想该CuCl 溶液呈酸性,并用PH试纸检测
2
C.丙同学用锌粒与该CuCl 溶液反应,观察是否有气泡产生
2
D.丁同学用镁粉与该CuCl 溶液反应,观察产生气泡的快慢
2
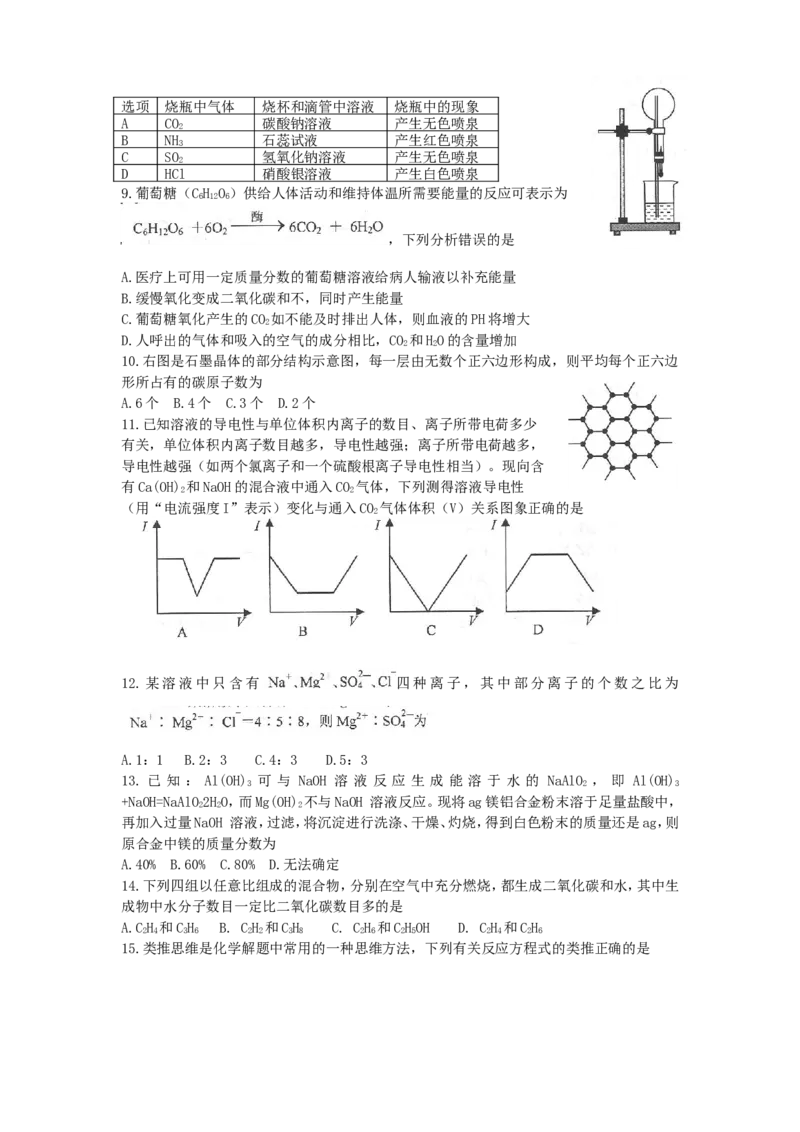
8.右图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液,挤压滴管的胶头,
下列与实验事实不相符的是选项 烧瓶中气体 烧杯和滴管中溶液 烧瓶中的现象
A CO 碳酸钠溶液 产生无色喷泉
2
B NH 石蕊试液 产生红色喷泉
3
C SO 氢氧化钠溶液 产生无色喷泉
2
D HCl 硝酸银溶液 产生白色喷泉
9.葡萄糖(CH O)供给人体活动和维持体温所需要能量的反应可表示为
6 12 6
,下列分析错误的是
A.医疗上可用一定质量分数的葡萄糖溶液给病人输液以补充能量
B.缓慢氧化变成二氧化碳和不,同时产生能量
C.葡萄糖氧化产生的CO 如不能及时排出人体,则血液的PH将增大
2
D.人呼出的气体和吸入的空气的成分相比,CO 和HO的含量增加
2 2
10.右图是石墨晶体的部分结构示意图,每一层由无数个正六边形构成,则平均每个正六边
形所占有的碳原子数为
A.6个 B.4个 C.3个 D.2个
11.已知溶液的导电性与单位体积内离子的数目、离子所带电荷多少
有关,单位体积内离子数目越多,导电性越强;离子所带电荷越多,
导电性越强(如两个氯离子和一个硫酸根离子导电性相当)。现向含
有Ca(OH) 和NaOH的混合液中通入CO 气体,下列测得溶液导电性
2 2
(用“电流强度I”表示)变化与通入CO 气体体积(V)关系图象正确的是
2
12.某溶液中只含有 四种离子,其中部分离子的个数之比为
A.1:1 B.2:3 C.4:3 D.5:3
13. 已 知 : Al(OH) 可 与 NaOH 溶 液 反 应 生 成 能 溶 于 水 的 NaAlO , 即 Al(OH)
3 2 3
+NaOH=NaAlO2HO,而Mg(OH) 不与NaOH 溶液反应。现将ag镁铝合金粉末溶于足量盐酸中,
2 2 2
再加入过量NaOH 溶液,过滤,将沉淀进行洗涤、干燥、灼烧,得到白色粉末的质量还是ag,则
原合金中镁的质量分数为
A.40% B.60% C.80% D.无法确定
14.下列四组以任意比组成的混合物,分别在空气中充分燃烧,都生成二氧化碳和水,其中生
成物中水分子数目一定比二氧化碳数目多的是
A.CH 和CH B. CH 和CH C. CH 和CHOH D. CH 和CH
2 4 3 6 2 2 3 8 2 6 2 5 2 4 2 6
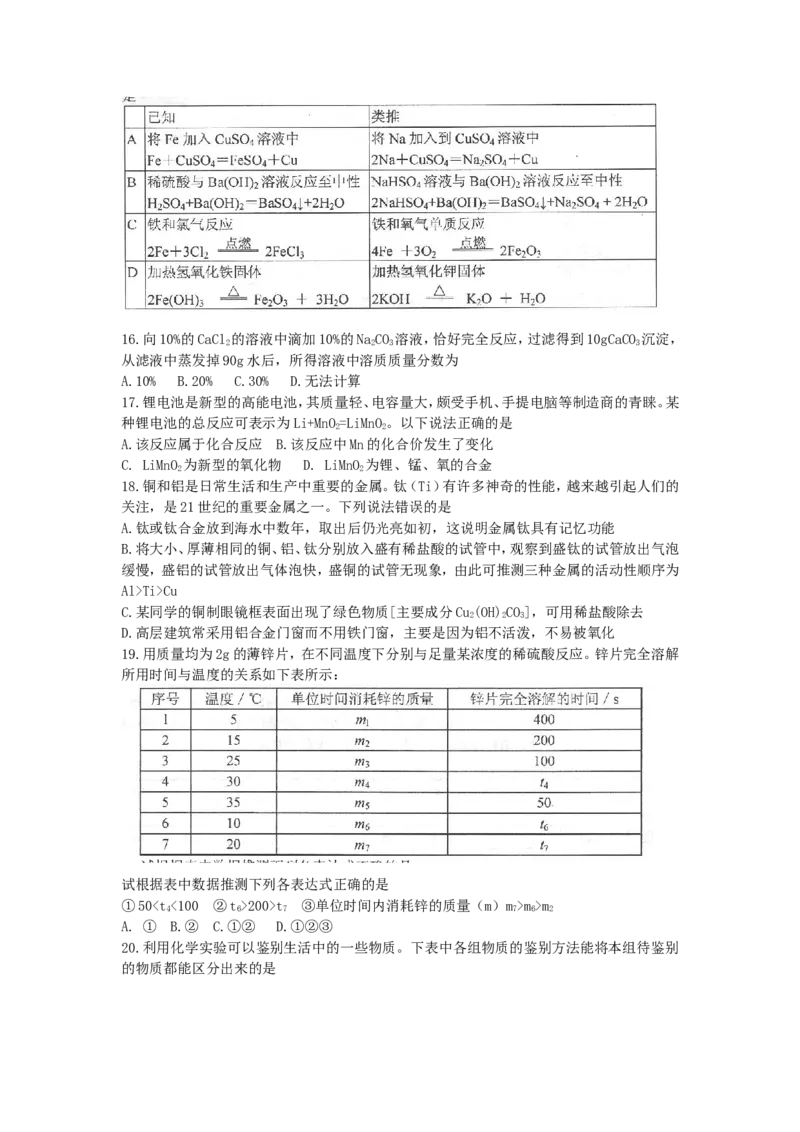
15.类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是16.向10%的CaCl 的溶液中滴加10%的NaCO 溶液,恰好完全反应,过滤得到10gCaCO 沉淀,
2 2 3 3
从滤液中蒸发掉90g水后,所得溶液中溶质质量分数为
A.10% B.20% C.30% D.无法计算
17.锂电池是新型的高能电池,其质量轻、电容量大,颇受手机、手提电脑等制造商的青睐。某
种锂电池的总反应可表示为Li+MnO=LiMnO。以下说法正确的是
2 2
A.该反应属于化合反应 B.该反应中Mn的化合价发生了变化
C. LiMnO 为新型的氧化物 D. LiMnO 为锂、锰、氧的合金
2 2
18.铜和铝是日常生活和生产中重要的金属。钛(Ti)有许多神奇的性能,越来越引起人们的
关注,是21世纪的重要金属之一。下列说法错误的是
A.钛或钛合金放到海水中数年,取出后仍光亮如初,这说明金属钛具有记忆功能
B.将大小、厚薄相同的铜、铝、钛分别放入盛有稀盐酸的试管中,观察到盛钛的试管放出气泡
缓慢,盛铝的试管放出气体泡快,盛铜的试管无现象,由此可推测三种金属的活动性顺序为
Al>Ti>Cu
C.某同学的铜制眼镜框表面出现了绿色物质[主要成分Cu(OH)CO],可用稀盐酸除去
2 2 3
D.高层建筑常采用铝合金门窗而不用铁门窗,主要是因为铝不活泼,不易被氧化
19.用质量均为2g的薄锌片,在不同温度下分别与足量某浓度的稀硫酸反应。锌片完全溶解
所用时间与温度的关系如下表所示:
试根据表中数据推测下列各表达式正确的是
①50200>t ③单位时间内消耗锌的质量(m)m>m>m
4 6 7 7 6 2
A. ① B.② C.①② D.①②③
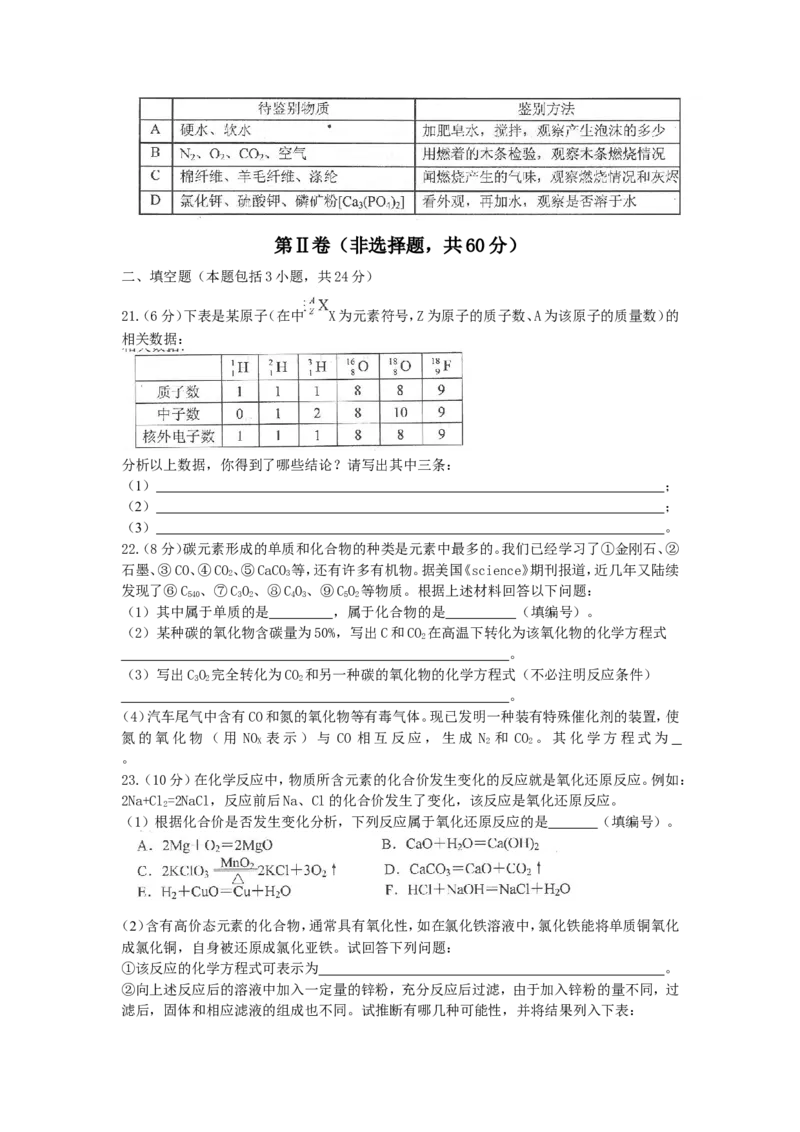
20.利用化学实验可以鉴别生活中的一些物质。下表中各组物质的鉴别方法能将本组待鉴别
的物质都能区分出来的是第Ⅱ卷(非选择题,共60分)
二、填空题(本题包括3小题,共24分)
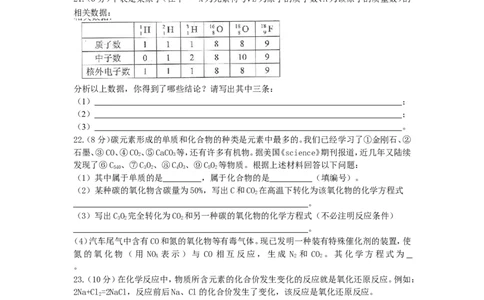
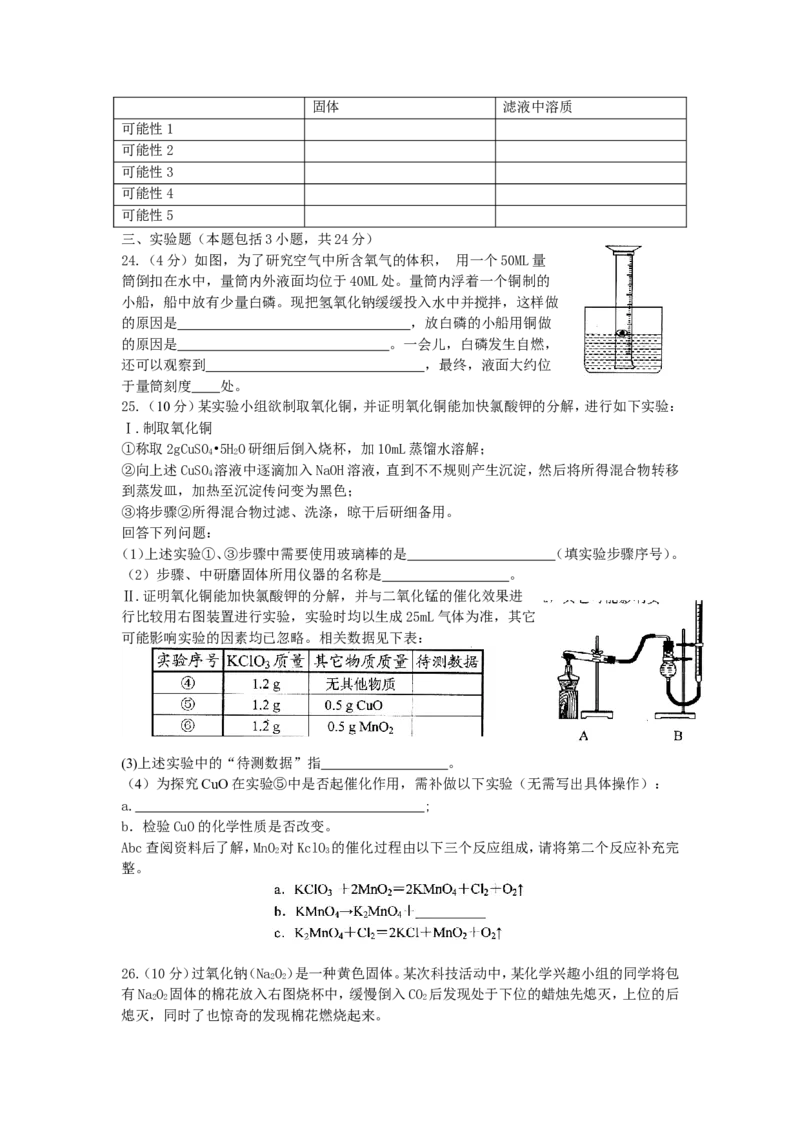
21.(6分)下表是某原子(在中 X为元素符号,Z为原子的质子数、A为该原子的质量数)的
相关数据:
分析以上数据,你得到了哪些结论?请写出其中三条:
(1) ;
(2) ;
(3) 。
22.(8分)碳元素形成的单质和化合物的种类是元素中最多的。我们已经学习了①金刚石、②
石墨、③CO、④CO、⑤CaCO 等,还有许多有机物。据美国《science》期刊报道,近几年又陆续
2 3
发现了⑥C 、⑦CO、⑧CO、⑨CO 等物质。根据上述材料回答以下问题:
540 3 2 4 3 5 2
(1)其中属于单质的是 ,属于化合物的是 (填编号)。
(2)某种碳的氧化物含碳量为50%,写出C和CO 在高温下转化为该氧化物的化学方程式
2
。
(3)写出CO 完全转化为CO 和另一种碳的氧化物的化学方程式(不必注明反应条件)
3 2 2
。
(4)汽车尾气中含有CO和氮的氧化物等有毒气体。现已发明一种装有特殊催化剂的装置,使
氮的氧化物(用 NO 表示)与 CO 相互反应,生成 N 和 CO 。其化学方程式为
X 2 2
。
23.(10分)在化学反应中,物质所含元素的化合价发生变化的反应就是氧化还原反应。例如:
2Na+Cl=2NaCl,反应前后Na、Cl的化合价发生了变化,该反应是氧化还原反应。
2
(1)根据化合价是否发生变化分析,下列反应属于氧化还原反应的是 (填编号)。
(2)含有高价态元素的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化
成氯化铜,自身被还原成氯化亚铁。试回答下列问题:
①该反应的化学方程式可表示为 。
②向上述反应后的溶液中加入一定量的锌粉,充分反应后过滤,由于加入锌粉的量不同,过
滤后,固体和相应滤液的组成也不同。试推断有哪几种可能性,并将结果列入下表:固体 滤液中溶质
可能性1
可能性2
可能性3
可能性4
可能性5
三、实验题(本题包括3小题,共24分)
24.(4分)如图,为了研究空气中所含氧气的体积, 用一个50ML量
筒倒扣在水中,量筒内外液面均位于40ML处。量筒内浮着一个铜制的
小船,船中放有少量白磷。现把氢氧化钠缓缓投入水中并搅拌,这样做
的原因是 ,放白磷的小船用铜做
的原因是 。一会儿,白磷发生自燃,
还可以观察到 ,最终,液面大约位
于量筒刻度 处。
25.( 10分)某实验小组欲制取氧化铜,并证明氧化铜能加快氯酸钾的分解,进行如下实验:
Ⅰ.制取氧化铜
①称取2gCuSO•5HO研细后倒入烧杯,加10mL蒸馏水溶解;
4 2
②向上述CuSO 溶液中逐滴加入NaOH溶液,直到不不规则产生沉淀,然后将所得混合物转移
4
到蒸发皿,加热至沉淀传问变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用。
回答下列问题:
(1)上述实验①、③步骤中需要使用玻璃棒的是 (填实验步骤序号)。
(2)步骤、中研磨固体所用仪器的名称是 。
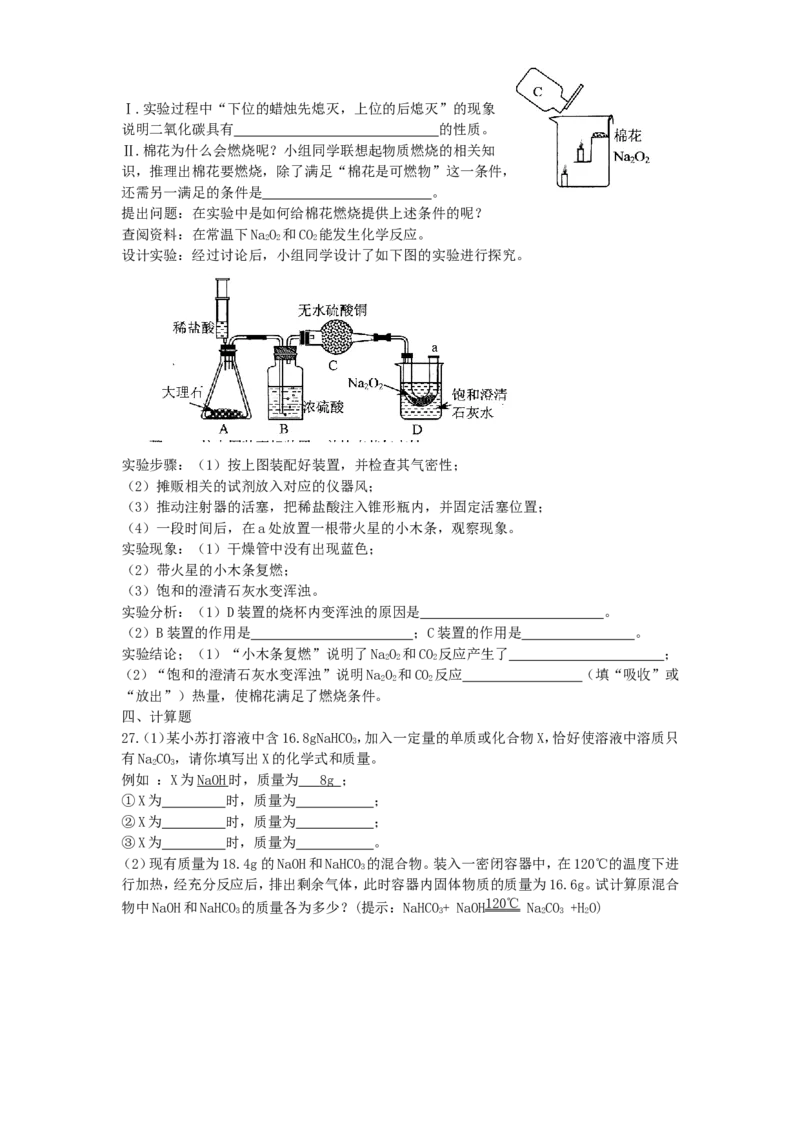
Ⅱ.证明氧化铜能加快氯酸钾的分解,并与二氧化锰的催化效果进
行比较用右图装置进行实验,实验时均以生成25mL气体为准,其它
可能影响实验的因素均已忽略。相关数据见下表:
(3)上述实验中的“待测数据”指 。
(4)为探究CuO在实验⑤中是否起催化作用,需补做以下实验(无需写出具体操作):
a. ;
b.检验CuO的化学性质是否改变。
Abc查阅资料后了解,MnO 对KclO 的催化过程由以下三个反应组成,请将第二个反应补充完
2 3
整。
26.(10分)过氧化钠(NaO)是一种黄色固体。某次科技活动中,某化学兴趣小组的同学将包
2 2
有NaO 固体的棉花放入右图烧杯中,缓慢倒入CO 后发现处于下位的蜡烛先熄灭,上位的后
2 2 2
熄灭,同时了也惊奇的发现棉花燃烧起来。Ⅰ.实验过程中“下位的蜡烛先熄灭,上位的后熄灭”的现象
说明二氧化碳具有 的性质。
Ⅱ.棉花为什么会燃烧呢?小组同学联想起物质燃烧的相关知
识,推理出棉花要燃烧,除了满足“棉花是可燃物”这一条件,
还需另一满足的条件是 。
提出问题:在实验中是如何给棉花燃烧提供上述条件的呢?
查阅资料:在常温下NaO 和CO 能发生化学反应。
2 2 2
设计实验:经过讨论后,小组同学设计了如下图的实验进行探究。
实验步骤:(1)按上图装配好装置,并检查其气密性;
(2)摊贩相关的试剂放入对应的仪器风;
(3)推动注射器的活塞,把稀盐酸注入锥形瓶内,并固定活塞位置;
(4)一段时间后,在a处放置一根带火星的小木条,观察现象。
实验现象:(1)干燥管中没有出现蓝色;
(2)带火星的小木条复燃;
(3)饱和的澄清石灰水变浑浊。
实验分析:(1)D装置的烧杯内变浑浊的原因是 。
(2)B装置的作用是 ;C装置的作用是 。
实验结论;(1)“小木条复燃”说明了NaO 和CO 反应产生了 ;
2 2 2
(2)“饱和的澄清石灰水变浑浊”说明NaO 和CO 反应 (填“吸收”或
2 2 2
“放出”)热量,使棉花满足了燃烧条件。
四、计算题
27.(1)某小苏打溶液中含16.8gNaHCO,加入一定量的单质或化合物X,恰好使溶液中溶质只
3
有NaCO,请你填写出X的化学式和质量。
2 3
例如 :X为NaOH 时,质量为 8 g ;
①X为 时,质量为 ;
②X为 时,质量为 ;
③X为 时,质量为 。
(2)现有质量为18.4g的NaOH和NaHCO 的混合物。装入一密闭容器中,在120℃的温度下进
3
行加热,经充分反应后,排出剩余气体,此时容器内固体物质的质量为16.6g。试计算原混合
120℃
物中NaOH和NaHCO 的质量各为多少?(提示:NaHCO+ NaOH NaCO +HO)
3 3 2 3 2