文档内容
2009 年广东省中山市初中化学竞赛
初赛试题
说明:1.全卷共6页。考试时间90分钟,满分100分。
2.答卷前,务必用黑色字迹的钢笔或签字笔将自己的考生号和姓名填写在答题卡
上,并用2B铅笔将试室号和座位号填涂在答题卡对应的位置上。
3.请将选择题的答案用2B铅笔在答题卡上对应题目的答案标号涂黑;如需改动,
用橡皮擦擦干净后,再选涂其他答案。
4.非选择题必须用黑色字迹的钢笔或签字笔在答题卡上指定区域作答;如需改动,
先在原来的答案上划一横线,然后在旁边空位处重新写。不准使用铅笔和涂改液。
5.相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Si-28 Cl-35.5 Ca-40
Ag-108
一、选择题(本题有14小题,每题2分,共28分。每小题只有一个选项符合题意)
1.下列自然现象的过程一定为化学变化的是
A.温室效应 B.云雾消失 C.冰川融化 D.形成酸雨
2.金星大气层存在一种二氧化三碳的气体(C O),则C O 不属于
3 2 3 2
A.混合物 B.纯净物 C.化合物 D.氧化物
3.用分子的观点对下列常见现象的解释,错误的是
A.花香四溢——分子在不停运动 B.热胀冷缩——分子的大小随温度变化而改变
C.酒精挥发——分子间距增大 D.氢气和氧气反应生成水——分子发生了变化
4.下图所示实验操作错误的是
A. 称量NaOH B. CO 性质检验 C. 添加酒精 D. 制取CO 并验满
2 2
5.用一种试剂鉴别盐酸、氯化钠和氢氧化钙三种溶液,应选用下列的
A.稀硫酸 B.氯化钡 C.碳酸钠 D.氢氧化钾
6.下列情况不会造成室内空气污染的是
A.吸烟产生的一氧化碳、尼古丁等物质 B.水烧开时产生的大量水蒸气
C.装修木板释放出的甲醛、苯等物质 D.大理石放出的放射性气体——氡
7.现有HSO 、NaOH、CuO、NaCO 四种物质,分别与其他某种物质反应都有同一种物质X
2 4 2 3
生成,则X的化学式可能是
A.HO B.CO C.NaCl D.BaSO
2 2 4
8.根据你所学过的化学知识分析,下列说法错误的是
A.腌制的酸菜含有少量亚硝酸盐 B.区分硬水和软水的方法是加肥皂水
C.将pH试纸直接浸入溶液中测溶液pH D.碳酸氢铵化肥一定要密封于阴暗处保存
9.将质量相等、化合价相同的甲乙两块金属,分别放入溶质质量分数相同的足量稀硫酸中,生成氢气的质量m
与反应时间t的关系如右图所示。则下列分析正确的是
A.甲比乙活泼 B.产生的H 乙比甲多
2
C.相对原子质量甲大于乙 D.在t 时:甲、乙均完全反应
2
10.“绿色化学”要求物质回收或循环利用,反应物原子利用率为100%、且全部转化为产物,
“三废”必须先处理再排放。下列做法或反应符合“绿色化学”要求的是
A.焚烧塑料以消除“白色污染” B.深埋含镉、汞的废旧电池
C.C 3 H 4 +2H 2 +2CO 催 化 剂 C 5 H 8 O 2 D.2KMnO 4 ==△=K 2 MnO 4 +MnO 2 +O 2 ↑
11.用数轴表示某些化 学知识直观、简明、易记。下列数轴表示错误的是
A.银、铜、铁的金属活动性强弱:
B.硫及其化合物与化合价的关系:
C.根据铁的含碳量,将其分成生铁和钢:
D.物质形成溶液的pH:
12.日常生活的下列放热现象中,与其他三种有本质区别的一种是
A.燃烧 B.电熨斗通电发热 C.生石灰与水混合放热 D.锌与硫酸反应放热
13.除去下列物质中的杂质(括号内物质为杂质)的方法错误的是
A.N(O)——通过灼热的铜网
2 2
B.Fe(Fe O)——过量稀盐酸、过滤
2 3
C.H(水蒸气)——通过浓硫酸的洗气瓶
2
D.NaOH溶液(NaCO)——适量Ca(OH) 溶液,过滤
2 3 2
14.以下对某一主题知识进行的归纳,正确的一组是
A.健康常识 B.安全常识
人体缺铁——易患贫血病 不明洞穴探险——先做灯火实验
人体缺锌——易患佝偻病 家中石油气泄漏――立即打开排气扇
C. 性质与用途 D. 物质分类
石墨能导电——作电极 常见的碱——熟石灰、烧碱、纯碱
活性炭有吸附性——作冰箱除臭剂 常见的干燥剂——浓硫酸、生石灰、碱石灰
二、填空题(本题有5小题,共22分)
15.(4分)农业上经常要配制一定浓度的食盐水溶液来选种,配制的步骤是计算、
、溶解,需要用到的仪器有天平、药匙、烧杯、玻棒、 ,其中玻棒的作用是
。
16.(3分)A、B两种物质的溶解度曲线如右图。则:
在t℃时,物质的溶解度B ______ A (填:大于、小于、
2
等于);当B溶液中含有少量A时,可用____________法提纯B;在t℃时,一定量的A物质的饱和溶液蒸发掉10g水,可得到mg A晶体(不含结晶水),
2
那么该温度时A的溶解度为__________g。
17.(3分)右下图形象地表示了某化学反应,其中 表示氢原子, 表示氧原子,该反应
的化学方程式为: ,
反应类型为 。
18.(6分)请用化学知识回答:
(1)化石燃料通常是指煤、 、天然气;用石灰浆粉刷墙壁后的室内放置一燃烧的煤
炉,可使墙壁迅速硬化,同时墙壁上会出现一些水珠,其原因是(用化学方程式表示)
。
(2)如果煤炭长期密实地堆积,可能会因 导致温度升高而自燃;当大量堆积
的煤发生燃烧时,灭火的最好方法是 (写一种)。
(3)汽车的尾气管中装有金属铂、钯的合金网,目的是将汽油燃烧时产生的有害气体CO、
NO转变为CO 和N,那么这些金属在反应中起的作用是 。
2 2
19.(6分)右下图为“太平梳打饼干”的 “营养说明书”的一部分,请回答:
(1)有些青少年不爱吃蔬菜、水果,影响生长发育, 太平梳打饼营养成份(100g)
能量:2031kJ 蛋白质:8.2g
这主要是由于摄入______(填序号)不足而引起的:
脂肪:20g 碳水化合物:65.2g
A.维生素、B.油脂、C.蛋白质。 钙: 320mg 铁:4.8mg ………
(2)“太平梳打饼干”中所含的钙、铁是指
_________(填:单质、原子、元素),这种饼干有咸味是因为它加入了___________(填名称)。
(3)每100g这种饼干含量最多的营养物质是 ;制作这种饼干过程中常加入膨
松剂NaHCO ,它与发酵面团中的酸反应产生 气体使饼干酥松;正常情况下,成人每
3
日摄入的脂肪不超过60g,则每日成人食用该梳打饼最多不应超过__________g。
三.(本题有2小题,共16分)
20.(8分)铝在我们的工业和日常生活中随处可见:厨房里的铝锅铝勺,包糖果、香烟的
铝箔;制造门窗框架的是硬铝(含少量铜、镁、硅)等。请回答:
(1)地壳中铝的含量居所有元素的第 位;利用铝的延展性将其拉成细丝、压成
薄片;利用铝的 性用做电线、电缆;利用硬铝合金的质轻、 和强度好用其制造
火箭、飞机、轮船的外壳。
(2)铝制品耐用是因为表面有一层致密的氧化铝保护膜,该保护膜中铝的化合价为
;铝元素摄入过多会引起“老年痴呆症”,请对生活中减少铝元素的摄入提一条合理建议
。
(3)铁路工人在野外焊接钢轨时,点燃铝粉与三氧化二铁的混合物,在高温下发生置换
反应生成氧化铝和 ;氮化铝(AlN)因耐高温、抗冲击、导热性好,被广泛用于大规模
集成电路生产、陶瓷工业等,工业上是用氧化铝、氮气、单质碳在一定条件下反应生成AlN和
CO,该反应的化学方程式为: 。
21.(8分)老师在做镁条在空气中燃烧。细心的同学发现,燃烧后的生成物除了白色粉末状固体以外,还有少量淡黄色固体。同学们查资料知道氧化镁与水只是微量反应,于是他们
对淡黄白色固体进行了如下的探究:
请回答下列的问题:
(1)镁在空气中燃烧的现象有: 、有白色的烟、 、有淡黄白色固体
生成;镁与氧气反应的化学方程式为: 。
(2)由操作③的现象说明该气体是 (填化学式)。经查阅资料了解到:这种气体
是镁燃烧产物中的淡黄色固体MgN 与水反应生成氢氧化镁时生成的,其化学方程式为:
3 2
。
(3)操作⑤包含的具体操作名称是:蒸发浓缩、降温 。
四、(本题有2小题,共22分)
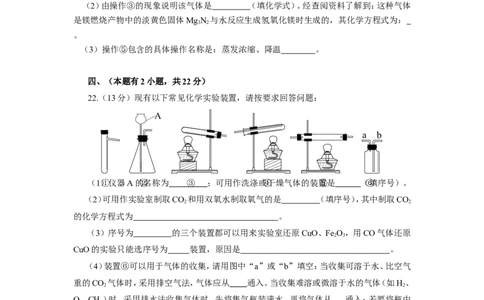
22.(13分)现有以下常见化学实验装置,请按要求回答问题:
A
a b
(1)①仪 器 A 的 ②名 称 为 ③ ; 可 用 作 洗 涤 或 ④干 燥 气 体 的 装 置⑤是 ( ⑥填序号)。
(2)可用作实验室制取CO 和用双氧水制取氧气的是 (填序号),其中制取CO
2 2
的化学方程式为 。
(3)序号为 的三个装置都可以用来实验室还原CuO、Fe O,用CO气体还原
2 3
CuO的实验只能选序号为 装置,原因是 。
(4)装置⑥可以用于气体的收集,请用图中“a”或“b”填空:当收集可溶于水、比空气
重的CO 气体时,采用排空气法,气体应从 通入。当收集难溶或微溶于水的气体(如H、
2 2
O、CH)时,采用排水法收集气体时,先将集气瓶装满水,再将气体从 通入;若要将瓶中
2 4
气体导出,应将水从 充入。
23.(9分)水田或池塘里常常不时地冒出一些气泡,几位同学决心弄清这种气泡的成分。
请你与他们一起完成如下的探究:
【猜想】Ⅰ. 这种气体含有CO; Ⅱ.这种气体含有CH。
2 4
【实验和结论】
(1)在水田中一位同学用木棍搅拌瘀泥,另一位同学将装满水的集气瓶倒置于水中的气
泡上方接收气体,如此重复几次后集满了2瓶气体。这种集气方法属于 。(2)将一集气瓶的玻片移开少许,向瓶中加入澄清石灰水,盖好玻片反复振荡,发现澄清
石灰水变浑浊,说明“猜想Ⅰ” (填:成立、不成立);然后移开玻片,立即
用燃着的火柴靠近瓶口,剩余气体噗的一声燃烧起来,一位同学就认为“猜想Ⅱ”成立,燃
烧的化学方程式为 ; 另几位同学认为此现象
不能说明CH 的存在,原因是 。
4
(3)为了验证这种可燃性气体含有碳和氢,他们把另一瓶气体装配为如右图所示的装置,
旋开活塞放水到集气瓶中,经验纯后用燃着的火柴靠近导管口,气
体燃烧起来,紧接着的操作、现象和判断是:①用内壁涂有澄清石灰
水的小烧杯罩于火焰上方,如果杯底变浑浊,说明该气体中含碳;②
。
干燥管中的碱石灰(CaO+固体 NaOH)所起的作用是
。
【拓展】如果要进一步确证这种含有C和H的可燃性气体就是CH,还应该进行
4
。
五、(本题有2小题,共12分)
24.(5分)美国“9.11”恐怖事件给纽约市带来了一场严重的环境灾难——“石棉污
染”,世贸大厦中的装修材料石棉纤维若被人体吸入易患肺癌。已知石棉是硅酸盐矿物,某
种石棉的化学式可表示为:CaMgSi O (OH) 。请计算回答:
2 5 x 22 2
(1)该石棉是由 种元素组成的。 (2)钙元素和镁元素质量比是 。
(3)硅的化合价为+4价,则这种石棉的化学式中的x= ;其中硅的质量分数为
(精确到0.1%)。
25.(7分)右下图是某种加钙食盐标签的一部分,请仔细阅读后回答以下问题:
(1)包装标签上 元素被称为“智力
配料表:氯化钠、食用碳酸钙、碘酸钾
之花”,可预防甲状腺肿大。
净含量:500.0g
(2)若已知该食盐中钙元素的质量分数
成分表:氯化钠≥?%
为1%,则食盐中碳酸钙的质量分数为 。 钙(以Ca计)0.5%~1.3%
(3)由于标签上氯化钠的含量已模糊不清, 碘(以I计,20.0~50.0)mg/㎏
为了测定食盐中氯化钠的含量,某同学取100 .0g
样品加水溶解过滤后,加入足量的硝酸银,生成了白色的氯化银沉淀220.8g。试计算该食盐
中氯化钠的质量分数(精确到0.1%)。2009年中山市初中化学竞赛初赛试题参考答案及评分标准
一、选择题(本题包括14小题,每小题2分,共28分)
1.D 2.A 3.B 4.A 5.C 6.B 7.A 8.C 9.D 10.C 11.D 12.B 13.B 14.C
以下化学方程式若为2分,则未配平扣1分、无反应条件扣1分、该方程扣完为止。
二、填空题(本题有5小题,共22分)
15.(4分)称量(1分) 量筒(1分) 搅拌(1分)、加速溶解(1分)
16.(3分)小于 蒸发溶剂 10m
17.(3分)2HO M n O 22H O + O↑ (2分) 分解反应(1分)
2 2 2 2
18.(6分)
(1)(3分)石油(1分) Ca(OH) + CO = CaCO ↓ + H O(2分)
2 2 3 2
(2)(2分)缓慢氧化(1分) 用沙或石棉等方法隔绝空气(合理均给分,1分。注:若
用水或用泡末灭火器浇灭,会产生水煤气:H+CO)
2
(3)(1分)催化剂(或催化作用)
19.(6分)
(1)(1分)A (2)(2分)元素 食盐(或氯化钠)(3)(3分)碳水化合物(或糖类) 二氧化碳(或CO) 300
2
三、(本题有2小题,共16分)
20.(8分)
(1)(3分)3(1分) 导电(1分) 硬度(1分)
(2)(2分) +3 (1分) 少用铝制餐具,或少吃用铝制易拉罐装的饮料、或少有铝箔
包装食品等(合
理均给分,1分)
(3)(3分) Fe (或铁,1分) Al O+ N + 3C 一 定 条2件AlN+3CO(2分)
2 3 2
21.(8分)
(1)(4分)发出耀眼的白光(1分) 放出大量的热(1分) 2Mg + O 2M点g燃O( 2
2
分)
(2)(3分)NH (1分) MgN + 6HO = 3Mg(OH) + 2NH ↑(2分)
3 3 2 2 2 3
(3)(1分)结晶
四、(本题有2小题,共22分)
22.(13分)
(1)(2分)长颈漏斗(1分) ⑥(1分)
(2)(4分)①②(2分) CaCO +2HCl==CaCl+CO ↑+H O(2分,若写为NaCO、
3 2 2 2 2 3
NaHCO 的反应且
3
正确给1分)
(3)(4分)③④⑤(选对2个给1分,3个全对给2分) ⑤(1分) 可以将尾气在导
管末端点燃,
以防止空气污染(1分)
(4)(3分)b a b
23.(9分)
【实验和结论】
(1)(1分)排水集气法
(2)(4分)成立(1分) CH
4
+2O 2点==燃==CO
2
+2H
2
O(2分) 能然烧的气体不一定是
CH[或没有检验可燃
4
性气体中的C和H的存在,合理表述均给分。1分]
(3)(3分)②用干冷(或用无水粘胶粘有硫酸铜的)烧杯罩于火焰上方(1分),如果烧杯
内壁出现水雾(或
无水硫酸铜由白色变为蓝色),则说明这种气体含有氢(1分) 吸收原气体中的
CO 和水蒸汽(1分)
2
【拓展】(1分)定量测定气体中碳和氢的质量 [或先用烧碱或生石灰吸收气体中的CO,
2然后用干燥剂干燥
气体后测气体的密度。或并将气体燃烧后生成的气体分别用浓硫酸、用碱石灰吸收,
再称量浓硫酸和碱石灰的增加的质量,计算。1分]
五、(本题有2小题,共12分)
24.(5分) 5(1分) 2 : 3(1分) 8(2分) 27.7%(1分)
25.(7分)
(1)碘(1分)
(2)(2分)2.5%(1%÷40%)
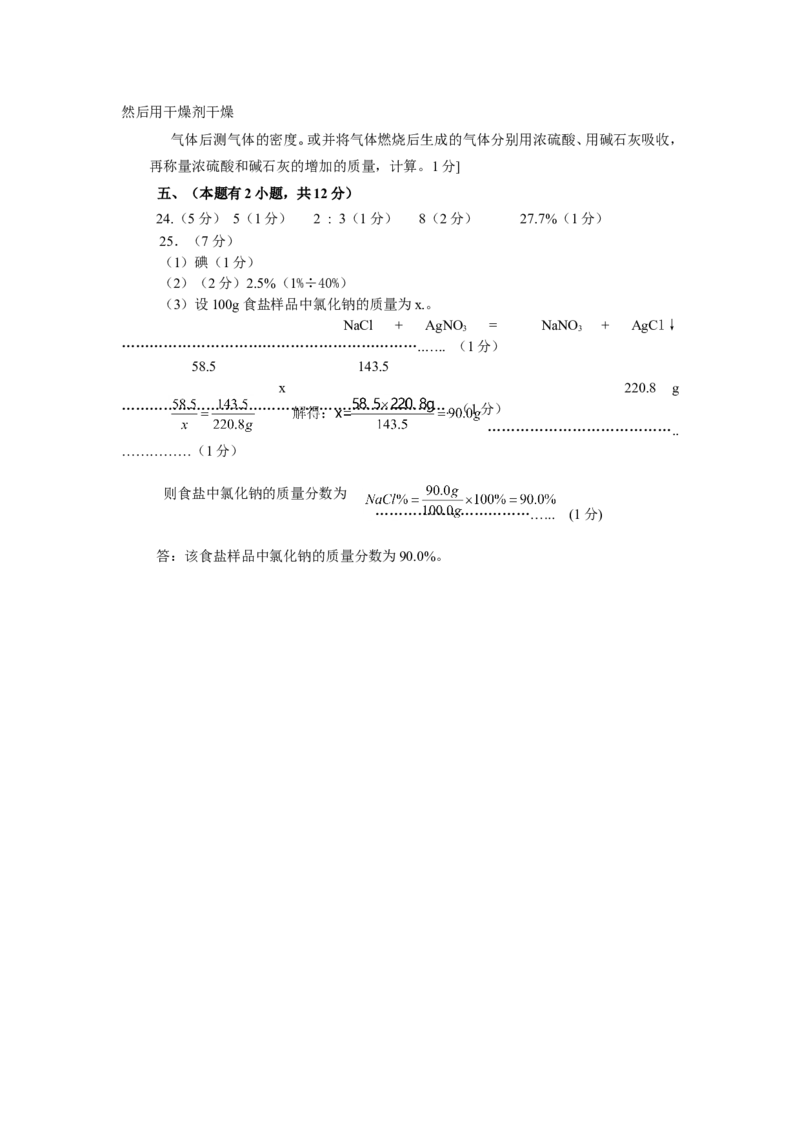
(3)设100g食盐样品中氯化钠的质量为x.。
NaCl + AgNO = NaNO + AgCl↓
3 3
………………………………………………………..….. (1分)
58.5 143.5
x 220.8 g
……………………………………………………………. (1分)
…………………………………..
……………(1分)
则食盐中氯化钠的质量分数为
…………………………….….. (1分)
答:该食盐样品中氯化钠的质量分数为90.0%。