文档内容
2010年海南省初中化学竞赛初赛试题
(本试卷满分100分,考试时间90分钟)
题号 一 二 三 四 五 总分
得分
评卷人
相对原子质量:H:1 C:12 O:16 Na:23 Al:27 Ca:40 Fe:56 Zn:65
一、选择题(每小题只有一个正确选项,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案序号
题号 11 12 13 14 15 16 17 18 19 20
答案序号
1.下列有关“化学之最”的叙述中正确的是:
A.最简单的有机物是乙酸 B.化学变化中最小的粒子是原子
C.地壳中含量最多的元素是硅 D.最硬的金属是铁
2.2009年12月,联合国气候变化大会在丹麦首都哥本哈根召开,进一步推动了各国实施
“节能减排”计划。下列造成地球温暖化的气体中,影响最大的是:
A、臭氧 B、氧化亚氮 C、一氧化碳 D、二氧化碳
3.下图为身边常见物质的pH。据此判断下列说法中正确的:
物质 厕所清洁剂 苹果 橘子 酱油 牛奶 牙膏 肥皂 草木灰 稀氨水
pH 2 3 3.5 4.5 6.5 8 10 11 11.5
A.蚊虫叮咬后,可涂稀氨水减轻疼痛
B.胃酸过多的病人应多食橘子、苹果
C.牙膏的碱性比草木灰的碱性更强
D.刨芋头时,皮肤沾上芋头皮会奇痒难忍(芋皮上含有一种碱性的物质——皂角素),
可选肥皂水涂抹止痒。
4.加勒比岛国海地当地时间2010年1月12日下午发生里氏7.3级地震,造成重大的人员伤
亡。在灾区,为防止疾病传染,河水需处理后方可饮用。常用的处理方法有:①加热煮沸,②过
滤,③投药消毒,④自然沉降。较合理的顺序为
A.③②④① B.③①④② C.④②③① D.④①③②
5.文卡特拉曼·拉马克里希南等三位科学家因“对核糖体结构和功能的研究”而共同获得
2009年诺贝尔化学奖。核糖体是进行蛋白质合成的重要细胞器,蛋白质是一类非常复杂的化
合物,由碳、氢、氧、氮、硫等元素组成,蛋白质在酸、碱或酶的作用下能发生水解反应生成氨
基酸,氨基酸分子中含有氨基(—NH ,具有碱的性质)和羧基(—COOH,具有酸的性质)。氨基
2
酸分子具有的性质是:
A.只能与硫酸反应,不能与氢氧化钠反应
B.只能与氢氧化钠反应,不能与硫酸反应
C.既能与硫酸反应,又能与氢氧化钠反应
D.既不能与硫酸反应,又不能与氢氧化钠反应
6.右图为元素周期表第四周期的局部。据此判断
下列说法中正确的是:
A.锗元素的元素符号为SeB.砷元素的原子序数为33
C.镓元素的相对原子质量为31
D.它们都属于金属元素
7.将56g不纯的铁粉与足量的稀盐酸反应,生成2g氢气。下列有关铁粉的说法正确的是:
A.铁中含有碳 B.铁表面有铁锈 C.铁中含有碳和锌 D.铁中含有碳和铝
8.长期使用的氢氧化钠会部分变质生成碳酸钠。为了鉴定其是否变质,某学习小组的同学设
计了以下四种方案。其中合理的是:
A.取试样溶于水,滴加足量稀盐酸,观察是否产生气体
B.取试样溶于水,滴加少量酚酞试液,观察是否变红
C.取试样溶于水,滴加硫酸铜溶液,观察是否产生沉淀
D.取试样溶于水,滴加氯化镁溶液,观察是否产生沉淀
9.已知KNO 在不同温度下的溶解度如下表:
3
温度/℃ 0 10 20 30 40 50 60
溶解度/g 13.3 20.9 31.6 45.8 63.9 85.5 110
下列说法不正确的是:
A. 在20℃时,KNO 的溶解度为31.6 g
3
B. 在10℃时,将25 g KNO 加入75 g 水中,充分搅拌,可得25%的KNO 溶液
3 3
C. KNO 的溶解度随温度的升高而增大
3
D. 60℃时,KNO 饱和溶液中溶质与溶剂的质量之比为11∶10
3
10.某同学利用右图装置测定空气中氧气的含量,红磷燃烧后恢复到室
温,打开弹簧夹发现进入广口瓶中的水的高度不足广口瓶容积的1/5。
造成这一现象的原因不可能是:
A.实验时,将木炭代替红磷
B.实验中所取的红磷不足,瓶中氧气未反应完
C.插入燃烧匙太慢,塞紧瓶塞之前,瓶内已有部分空气受热逸出
D.实验时,没有将弹簧夹夹紧
11.我省有辽阔的海岸线、充足的海水资源。人们常把海水引入盐田,经过风吹日晒使海水中
的水分蒸发获得粗盐。在此过程中:
A.溶剂的质量不变 B.氯化钠的质量不变
C.氯化钠的质量分数始终不变 D.氯化钠的质量分数变小
12.实验室里保存下列试剂,对其保存的方法和理由的描述均不正确的是:
编号 试剂 保存方法 理由
A 固体氢氧化钠 保存在带橡皮塞的细口瓶中 防止与空气接触被氧化
B 浓硝酸 保存在密闭的棕色瓶中 浓硝酸见光容易分解
C 碳酸钠晶体 保存在干燥密封的广口瓶中 防止风化而碎裂成粉末
D 白磷 保存在水中 白磷在空气中易自燃
13.航天员在太空的饮用水是小分子团水,它显弱碱性,具有饮用量少、在人体内储留时间长、
排放量少的特点。下列关于小分子团水的说法中正确的是
A.小分子团水的化学性质被改变了
B.常温下该水的pH等于7
C.小分子团水中分子间没有间隙
D.小分子团水的部分物理性质与普通水有所不同14.复习物质分类时,小红对部分物质归纳如下。其中不正确的是:
A.海水和酸雨都属于混合物 B.冰和干冰都属于氧化物
C.生石灰和熟石灰都属于碱 D.酒精和淀粉都属于有机物
15.根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见下图)。将试管浸
入烧杯或从中取出,可以控制反应的进行。下列气体的制取宜使用该装置的是:
A.用碳酸钙(块状)与稀硫酸制二氧化碳
B.用碳酸钙(块状)与稀盐酸制二氧化碳
C. 用铁粉与稀硫酸制氢气
D.用二氧化锰(粉末)与双氧水制氧气
16.经测定,由甲酸(HCOOH)、乙醛(CHCHO)和丙酮
3
(CHCOCH )组成的混合物中,氢元素的质量分数为X%,则该混合物中氧元素的质量分数
3 3
为:
A.6X% B.1-2X% C.1-7X% D.2X%
17. 为了探究Fe、Cu、Ag三种金属的活动性顺序,某兴趣小组设计了下图所示的四组实验方
案,你认为不可行的是:
A .
B .
C .
D .
18. 综
合利用海水提取镁的主要反应有:
①CaCO = CaO + CO↑ ②CaO + HO = Ca(OH) ③MgCl + Ca(OH) = Mg(OH) ↓+
3 2 2 2 2 2 2
CaCl ④Mg (OH) + 2HCl = MgCl + 2HO ⑤MgCl = Mg + Cl↑
2 2 2 2 2 2
其中属于复分解反应的是:
A.①②⑤ B.②③④ C.①⑤ D.③④
19.下列“家庭小实验”不能达到预期目的的是
A. 用过滤法使硬水转化成软水
B. 用食醋区别小苏打和食盐
C. 用洁厕精(含有盐酸)除去铁锈
D. 用食醋、石灰水验证蛋壳中含有碳酸盐
20.实验室中浓硫酸的商标如右图所示。据此判断下列说法不正确的是:
硫酸
A.该硫酸的纯度超过工业纯浓硫酸
B.配制100mL溶质质量分数为19.6%的稀硫酸,需要这种浓硫酸
化学纯(CP)
500mL 约920g
20mL
化学式HSO
C. 稀释浓硫酸时,应将其沿器壁缓慢倒入水中,并不断搅拌 2 4
相对分子质量:98.00
D.配制100g溶质质量分数为19.6%的稀硫酸,需要这种浓硫酸
密度1.84g/mL
20g
质量分数为98%
二、填空题(每空2分,共24分)
质量分数为36.5%
21.生活之中处处都有碳元素的踪影。请用含碳元素的物质的化学符号填写下列空白。
(1)沼气的主要成分 ;(2)祥云火炬的燃料 ;
(3)治疗胃酸过多症的药物的主要成分 。22. 1803年10月,在曼彻斯特的文学和哲学学会的一次集会上,英国科学家道尔顿讲述了他
的原子论,主要论点如下:
(1)一切元素都由不可再分的微粒构成,这种微粒叫做原子。原子在一切化学变化中都保持
它的不可再分性。
(2)同一元素的原子,各方面的性质,特别是重量,都完全相同;不同元素的原子重量不同。
原子的相对重量(原子量)是每一种元素的特征性质。
(3)不同元素的原子是以简单的整数比相化合。
请利用所学知识判断,道尔顿的上述论点中有哪些错误。
。
23.汽车的安全气囊内有叠氮化钠(NaN )或硝酸铵(NH NO )等物质。当汽车在高速行驶中
3 4 3
受到猛烈撞击时,这些物质会迅速发生分解反应,产生大量气体,充满气囊。
(1)其中,叠氮化钠分解产生氮气和固态钠。请写出叠氮化钠分解的化学方程式
。
(2)硝酸铵是常用氮肥,从安全角度考虑,存放和使用化学硝酸铵时应注意的问题有
。
24.锌、碘是人体必须的微量元素,在国际上
食品名称:锌强化营养盐
锌被誉为“生命之花”、碘被誉为“智力元
配料表:精制盐、葡萄糖酸锌、碘酸钾
素”。 锌含量(以Zn计):(125±15)毫克/千克
某品牌食盐使用说明的部分内容如右图所示。 碘含量(以I计):(35±15)毫克/千克
生产日期:见盒内合格证
请回答下列问题:
保质期:壹年
(1)人体缺锌会导致 等
疾病。
(2)葡萄糖酸锌的化学式为C H O Zn(相对分子质量为455)。计算其中锌的质量分数为
12 22 14
。
(3)1kg该品牌食盐中葡萄糖酸锌的含量为 g。
25.下图是王老师在“燃烧和灭火”一节中做的两个关于燃烧的条件的实验装置:
甲 乙
请回答:(1)写出白磷燃烧的化学方程式 ;
(2)与甲装置相比,乙装置的优点是: ;
三、简答题(10分)26.宋时,江西上饶有一苦泉,当地人用铁锅熬苦泉的水获得胆矾,结果发现铁锅用久了变成
了铜锅。其中包含什么化学道理?
27.过滤实验时,过滤后,所得到的水仍然浑浊。请说出可能的原因。
四、实验题(18分)
28.为了探究氢氧化钠溶液与盐酸反应的实质,小林设计了以下两种方案。
方案1、向盛有氢氧化钠溶液的试管中滴加几滴酚酞试液,溶液变红;再向其中逐滴加入稀盐
酸,红色变浅,最终退去。证明盐酸与氢氧化钠反应了。
方案2、先向盛有盐酸的试管中滴加氢氧化钠溶液,再向其中滴加硝酸银溶液,如果有白色沉
淀产生,则说明生成了氯化钠,证明盐酸与氢氧化钠反应了。
(1)请判断上述两种方案的可行性,并说明原因。
。
(2)请你设计另一种方案,证明氢氧化钠溶液与盐酸的确反应了。
。
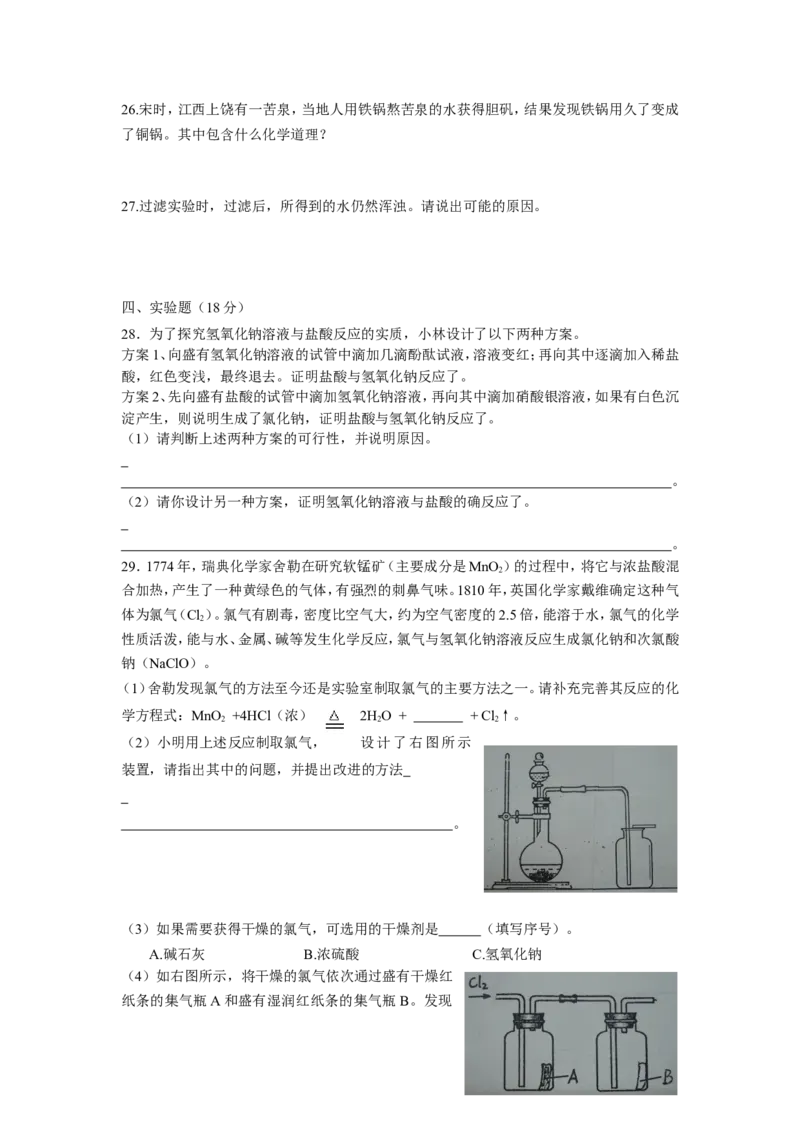
29.1774年,瑞典化学家舍勒在研究软锰矿(主要成分是MnO )的过程中,将它与浓盐酸混
2
合加热,产生了一种黄绿色的气体,有强烈的刺鼻气味。1810年,英国化学家戴维确定这种气
体为氯气(Cl)。氯气有剧毒,密度比空气大,约为空气密度的2.5倍,能溶于水,氯气的化学
2
性质活泼,能与水、金属、碱等发生化学反应,氯气与氢氧化钠溶液反应生成氯化钠和次氯酸
钠(NaClO)。
(1)舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请补充完善其反应的化
学方程式:MnO +4HCl(浓) 2HO + + Cl↑。
2 2 2
(2)小明用上述反应制取氯气, 设计了右图所示
装置,请指出其中的问题,并提出改进的方法
。
(3)如果需要获得干燥的氯气,可选用的干燥剂是 (填写序号)。
A.碱石灰 B.浓硫酸 C.氢氧化钠
(4)如右图所示,将干燥的氯气依次通过盛有干燥红
纸条的集气瓶A和盛有湿润红纸条的集气瓶B。发现量 生
成
沉
淀
的
质
/g
瓶A中的红纸没有变化,而瓶B中的红纸退色了。
据此,你能获得什么结论?
你能推断使红纸退色的物质可能是 ;
理由是 。
五、计算题(8分)
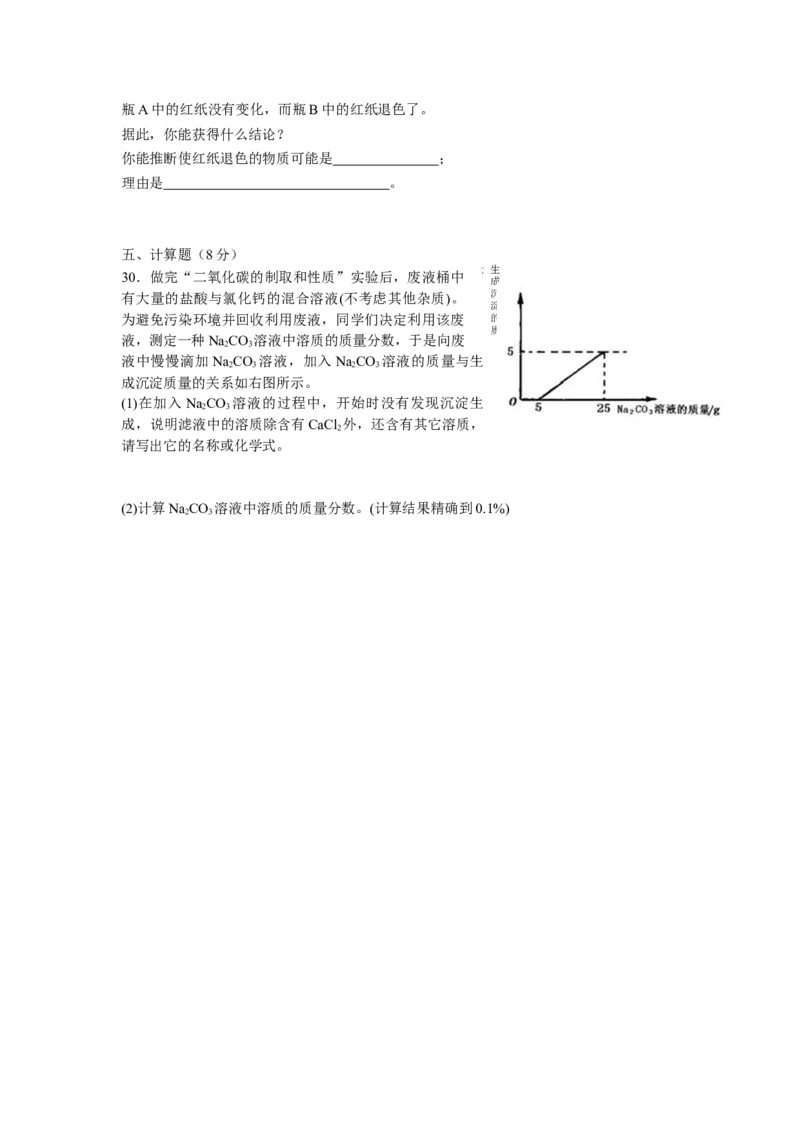
30.做完“二氧化碳的制取和性质”实验后,废液桶中
有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。
为避免污染环境并回收利用废液,同学们决定利用该废
液,测定一种NaCO 溶液中溶质的质量分数,于是向废
2 3
液中慢慢滴加NaCO 溶液,加入NaCO 溶液的质量与生
2 3 2 3
成沉淀质量的关系如右图所示。
(1)在加入NaCO 溶液的过程中,开始时没有发现沉淀生
2 3
成,说明滤液中的溶质除含有CaCl 外,还含有其它溶质,
2
请写出它的名称或化学式。
(2)计算NaCO 溶液中溶质的质量分数。(计算结果精确到0.1%)
2 32010 年海南省初中化学竞赛初赛试题答案
一、选择题(每小题只有一个正确选项,每小题2分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案序号 B D A C C B D A B C
题号 11 12 13 14 15 16 17 18 19 20
答案序号 B A D C B C C D A B
二、填空题(每空2分,共24分)
21.(1)CH (2)CH (3)NaHCO 、Na CO 、MgCO 、Al(OH) 等
4 3 8 3 2 3 3 3
22.原子并非构成物质的唯一微粒;同种元素的原子,其质量可能不同。
23.(1)2NaN =2Na+3N↑ (2)不能与易燃物质混在一起;避免受到撞击(或结块时,不能
3 2
用铁锤砸碎。)
24.(1)缺锌会引起食欲不振,生长迟缓,发育不良等。
(2)14.3% (3)0.87
25.(1)4P + 5O = 2P O (2)乙装置在密闭环境中进行,避免了PO 对空气的污染。
2 2 5 2 5
三、简答题(每题5分,共10分)
26.水中含有硫酸铜溶液,硫酸铜溶液与铁锅反应生成了铜,覆盖在铁锅表面。
27.(1)倒进漏斗中的水的水面比滤纸过滤器的过缘高。(2)玻璃棒靠的地方比滤纸过滤器
的边缘高。(3)滤纸破损。(4)仪器不干净等。
四、实验题(第28题8分,第29题10分,共18分)
28.(1)方案1可行;方案不可行,因为盐酸也会与硝酸银溶液反应生成氯化银白色沉淀。
(2)用2支试管分别盛少量盐酸,向其中一支试管中加入足量铁粉,有气泡产生;向另一支试
管滴加氢氧化钠溶液,再加铁粉,没有气泡产生。说明盐酸与氢氧化钠反应了。
将盐酸分成两份,向其中一份中加入碳酸钙粉末,有气泡产生;向另一份盐酸中滴加足
量氢氧化钠溶液,充分反应后,再加碳酸钙粉末,若无气泡产生,表明氢氧化钠溶液与盐酸反
应了。(其它合理答案均可)
29.(1)MnCl (2)二氧化锰与浓盐酸反应的条件是加热,应将圆底烧瓶置于酒精
2
灯上加热;氯气有毒,应增加尾气吸收装置。
(3)B (4)氯气与水反应的生成物;干燥的氯气不能使红纸退色,仅有水也不能使红
纸退色,B瓶中既有氯气又有水。
五、计算题(8分)
30.(1)HCl或盐酸 (2) 26.5%