文档内容
2010 年黄高优录考试选拔赛试卷 10
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24
S—32 Cl—35.5 K—39 Ca—40 Cu—64 I—127
一、选择题(本题包括15个小题,每小题2分,共30分。每小题有1个或2个选项符合题意。
若有两个答案的错1个不得分,漏选1个扣1分。请将答案填在下表相应的空格内。)
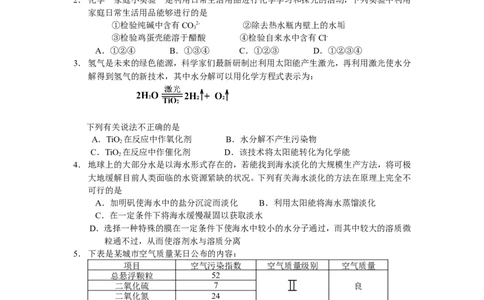
1.列说法中,你认为不科学的是
A.用含碘食盐可预防甲状腺肿大 B.使用含氟牙膏可预防龋齿
C.绿色食品是指不含任何化学物质的食品
D.光导纤维是以二氧化硅为主要原料制成的高性能通讯材料
2.化学“家庭小实验”是利用日常生活用品进行化学学习和探究的活动,下列实验中利用
家庭日常生活用品能够进行的是
①检验纯碱中含有CO2- ②除去热水瓶内壁上的水垢
3
③检验鸡蛋壳能溶于醋酸 ④检验自来水中含有Cl-
A.①②④ B.①③④ C.①②③ D.①②③④
3.氢气是未来的绿色能源,科学家们最新研制出利用太阳能产生激光,再利用激光使水分
解得到氢气的新技术,其中水分解可以用化学方程式表示为:
下列有关说法不正确的是
A.TiO 在反应中作氧化剂 B.水分解不产生污染物
2
C.TiO 在反应中作催化剂 D.该技术将太阳能转化为化学能
2
4.地球上的大部分水是以海水形式存在的,若能找到海水淡化的大规模生产方法,将可极
大地缓解目前人类面临的水资源紧缺的状况。下列有关海水淡化的方法在原理上完全不
可行的是
A.加明矾使海水中的盐分沉淀而淡化 B.利用太阳能将海水蒸馏淡化
C.在一定条件下将海水缓慢凝固以获取淡水
D.选择一种特殊的膜在一定条件下使海水中较小的水分子通过,而其中较大的溶质微
粒通不过,从而使溶剂水与溶质分离
5.下表是某城市空气质量某日公布的内容:
项目 空气污染指数 空气质量级别 空气质量
总悬浮颗粒 52
二氧化硫 7 良
二氧化氮 24
下列情况对表中三个空气质量指标不会产生影响的是
A.用柴油作燃料 B.焚烧垃圾
C.汽车排放的尾气 D.用天然气作燃料
6.英国泰晤士河曾是世界上最脏的河流之一。由于执行了严格的污水排放制度、重建了水道
体系和用专门船只向河水里输送某种气体等措施,河水水质已得到显著的改善。这里的
“某种气体”是指
A.氢气 B.氯气 C.氧气 D.二氧化碳
7.十九世纪初,法国科学家库图瓦正在家中做实验,一只猫把盛装海藻灰溶液和硫酸溶液的
瓶子都碰翻了,他看到了一个奇异的现象:打翻在地的混合液里产生了一种紫色蒸气,气
味十分难闻、呛鼻,而且紫色蒸气遇冷物体后变为紫黑色闪者金属光泽的晶体。库图瓦又做了许多实验,终于弄明白这种气体是一种新发现的元素,这种元素是
A.碘 B.碳 C.铜 D.汞
8.2004年4月22日是第35个“世界地球日”,其主题是“善待地球——科学发展”。下列
行为中不符合这一主题的是
A.用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.大量开采地下水,以满足社会对水的需求
C.不使用对大气臭氧层起破坏作用的氟里昂
D.节约能源,提高能源的利用率
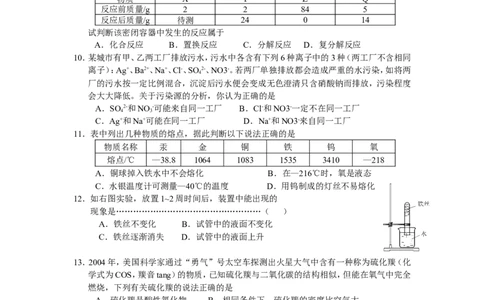
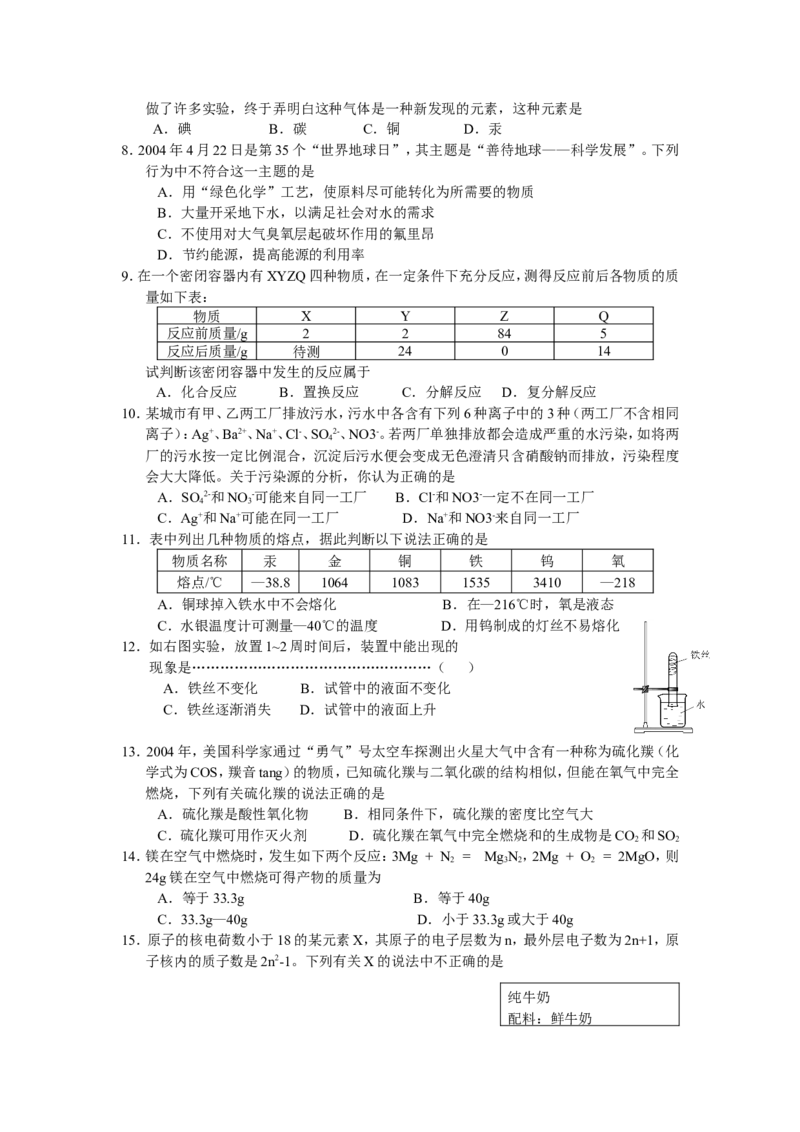
9.在一个密闭容器内有XYZQ四种物质,在一定条件下充分反应,测得反应前后各物质的质
量如下表:
物质 X Y Z Q
反应前质量/g 2 2 84 5
反应后质量/g 待测 24 0 14
试判断该密闭容器中发生的反应属于
A.化合反应 B.置换反应 C.分解反应 D.复分解反应
10.某城市有甲、乙两工厂排放污水,污水中各含有下列6种离子中的3种(两工厂不含相同
离子):Ag+、Ba2+、Na+、Cl-、SO 2-、NO3-。若两厂单独排放都会造成严重的水污染,如将两
4
厂的污水按一定比例混合,沉淀后污水便会变成无色澄清只含硝酸钠而排放,污染程度
会大大降低。关于污染源的分析,你认为正确的是
A.SO 2-和NO -可能来自同一工厂 B.Cl-和NO3-一定不在同一工厂
4 3
C.Ag+和Na+可能在同一工厂 D.Na+和NO3-来自同一工厂
11.表中列出几种物质的熔点,据此判断以下说法正确的是
物质名称 汞 金 铜 铁 钨 氧
熔点/℃ —38.8 1064 1083 1535 3410 —218
A.铜球掉入铁水中不会熔化 B.在—216℃时,氧是液态
C.水银温度计可测量—40℃的温度 D.用钨制成的灯丝不易熔化
12.如右图实验,放置1~2周时间后,装置中能出现的
现象是……………………………………………( )
A.铁丝不变化 B.试管中的液面不变化
C.铁丝逐渐消失 D.试管中的液面上升
13.2004年,美国科学家通过“勇气”号太空车探测出火星大气中含有一种称为硫化羰(化
学式为COS,羰音tang)的物质,已知硫化羰与二氧化碳的结构相似,但能在氧气中完全
燃烧,下列有关硫化羰的说法正确的是
A.硫化羰是酸性氧化物 B.相同条件下,硫化羰的密度比空气大
C.硫化羰可用作灭火剂 D.硫化羰在氧气中完全燃烧和的生成物是CO 和SO
2 2
14.镁在空气中燃烧时,发生如下两个反应:3Mg + N = MgN,2Mg + O = 2MgO,则
2 3 2 2
24g镁在空气中燃烧可得产物的质量为
A.等于33.3g B.等于40g
C.33.3g—40g D.小于33.3g或大于40g
15.原子的核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原
子核内的质子数是2n2-1。下列有关X的说法中不正确的是
纯牛奶
配料:鲜牛奶保质期:8个月
净含量:250mL/盒
营养成分(每 100mL 内
含):
钙≥0.11g
A.X能形成化学式为X(OH) 的碱
3
脂肪≥3.3g
B.X可能形成化学式为KXO 的含氧酸钾盐
3
蛋白质≥2.9g
C.X原子的最外层电子数和核电荷数肯定为奇数
D.X能与某些金属元素形成化合物
二、填空题(本题包括7小题,共38分。)
16.(4分)人体中的钙元素主要存在于骨骼和牙齿中,
以羟基磷酸钙晶体[Ca (PO4) (OH)]形式存在,其相对分子质量为502。牛奶含钙丰富又易被
5 3
吸收,且牛奶中钙和磷比例合适,是健骨的理想食品。右图是某乳业公司纯牛奶包装标签的
部分说明。请仔细阅读后回答下列问题:
⑴羟基磷酸钙中钙元素的质量分数 (保留到0.1%)
⑵成人每天至少需要0.6g钙,且这些钙有90%来自牛奶,则一个人每天要喝 盒这种牛
奶。
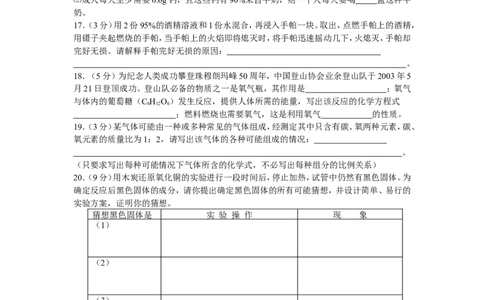
17.(3分)用2份95%的酒精溶液和1份水混合,再浸入手帕一块。取出,点燃手帕上的酒精,
用镊子夹起燃烧的手帕,当手帕上的火焰即将熄灭时,将手帕迅速摇动几下,火熄灭,手帕却
完好无损。请解释手帕完好无损的原因:
。
18.(5分)为纪念人类成功攀登珠穆朗玛峰50周年,中国登山协会业余登山队于2003年5
月21日登顶成功。登山队必备的物质之一是氧气瓶,其作用是 ;氧气
与体内的葡萄糖(C H O)发生反应,提供人体所需的能量,写出该反应的化学方程式
6 12 6
;燃料燃烧也需要氧气,这是利用氧气 的性质。
19.(3分)某气体可能由一种或多种常见的气体组成,经测定其中只含有碳、氧两种元素,碳、
氧元素的质量比为1:2,请写出该气体的各种可能组成的情况:
。
(只要求写出每种可能情况下气体所含的化学式,不必写出每种组分的比例关系)
20.(9分)用木炭还原氧化铜的实验进行一段时间后,停止加热,试管中仍然有黑色固体。为
确定反应后黑色固体的成分,请你提出确定黑色固体的所有可能猜想,并设计简单、易行的
实验方案,证明你的猜想。
猜想黑色固体是 实 验 操 作 现 象
(1)
(2)
(3)
21.(8分)若从HSO 、NaCO、NaSO 、NaCl、NaNO 、Cu(NO )、HNO 七种溶液中取出其中
2 4 2 3 2 4 3 3 2 3
的两种,进行混合及有关实验,所观察到的现象记录如下表。试根据各步实验和现象先进行
分步推断,再推断所取的两种溶液的可能组合。
步骤 实 验 操 作 实 验 现 象 推 断(或结论)
(1) 混合溶液无色、澄清 混合液中肯定不含Cu(NO )
3 2
混合液肯定不是下列组合:
将取出的两种溶液混
合 无明显现象(2) 用PH试纸测定混合
测定结果:PH=2
液的PH
(3) 向混合液中滴入足量
有白色沉淀出现
Ba(NO ) 溶液
3 2
(4) 向上述过滤所得滤液
无明显现象
中滴加AgNO 溶液
3
①
混合溶液的可能组合(写出溶质的化学式,有几组写 ②
几组) ③
④
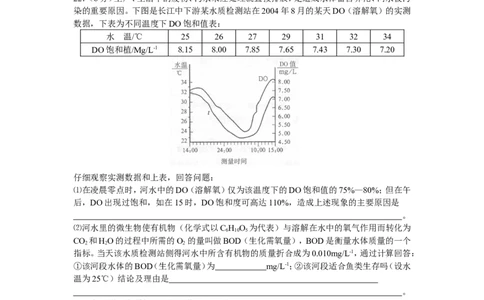
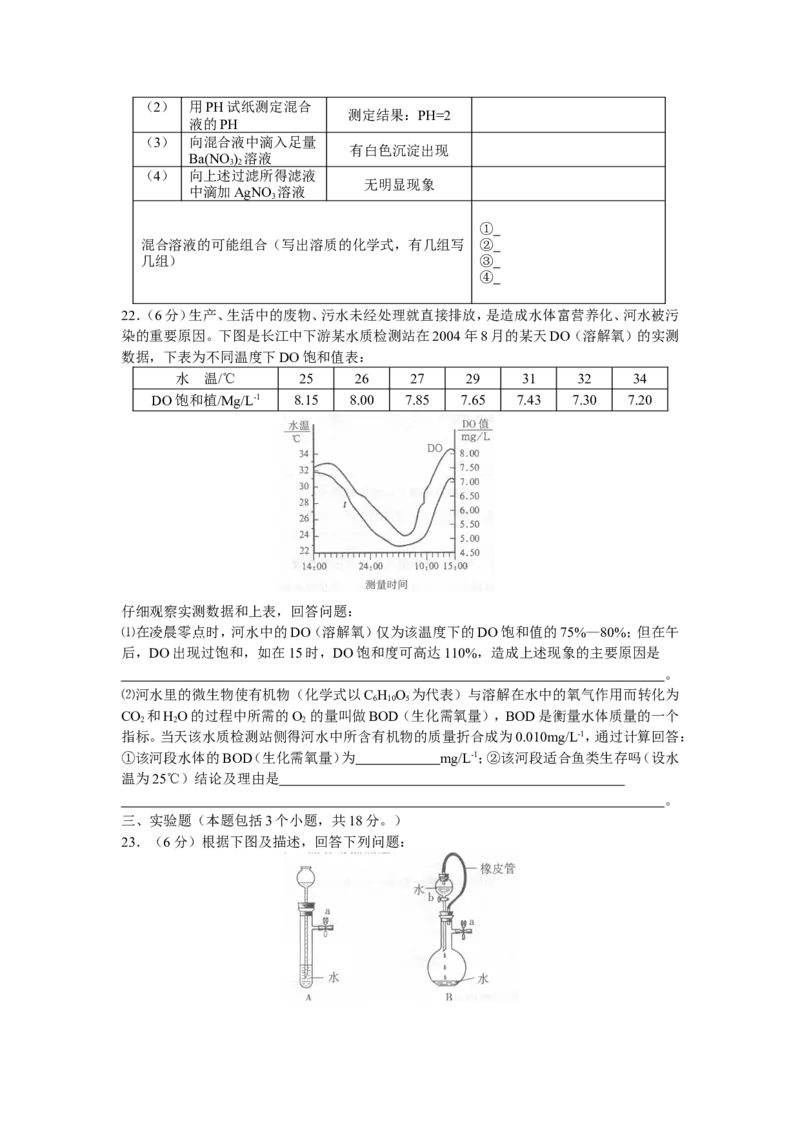
22.(6分)生产、生活中的废物、污水未经处理就直接排放,是造成水体富营养化、河水被污
染的重要原因。下图是长江中下游某水质检测站在2004年8月的某天DO(溶解氧)的实测
数据,下表为不同温度下DO饱和值表:
水 温/℃ 25 26 27 29 31 32 34
DO饱和植/Mg/L-1 8.15 8.00 7.85 7.65 7.43 7.30 7.20
仔细观察实测数据和上表,回答问题:
⑴在凌晨零点时,河水中的DO(溶解氧)仅为该温度下的DO饱和值的75%—80%;但在午
后,DO出现过饱和,如在15时,DO饱和度可高达110%,造成上述现象的主要原因是
。
⑵河水里的微生物使有机物(化学式以C H O 为代表)与溶解在水中的氧气作用而转化为
6 10 5
CO 和HO的过程中所需的O 的量叫做BOD(生化需氧量),BOD是衡量水体质量的一个
2 2 2
指标。当天该水质检测站侧得河水中所含有机物的质量折合成为0.010mg/L-1,通过计算回答:
①该河段水体的BOD(生化需氧量)为 mg/L-1;②该河段适合鱼类生存吗(设水
温为25℃)结论及理由是
。
三、实验题(本题包括3个小题,共18分。)
23.(6分)根据下图及描述,回答下列问题:⑴关闭图A装置中的弹簧夹a后,从长颈漏斗向试管口注入一定量的水,静置后如图所示。
试判断:A装置是否漏气?(填“漏气”、“不漏气”、“无法确定”) 。判断理由:
。
⑵关闭图B装置中的弹簧夹a后,开启分液漏斗的活塞b,水不断往下滴,直至全部流入烧瓶。
试判断:A装置是否漏气?(填“漏气”、“不漏气”、“无法确定”) 。判断理由:
。
24.(7分)⑴根据初中化学知识,硫酸铜溶液与氢氧化钠溶液反应可得到蓝色沉淀,进一步
将沉淀加热可生成黑色物质,请写出有关反应的化学方程式
① ②
⑵小明做了这个实验。他在试管中到入2mLCuSO 溶液,再加入一定量NaOH溶液,结果得
4
到的沉淀并不是蓝色的,而是浅绿色的;将此浊液加热至沸腾,观察不到有分解变黑生成
CuO的迹象,这是为什么呢?小明通过查找资料得知,该浅绿色沉淀物有可能是溶解度及小
的碱式硫酸铜,其化学式为Cu (OH) SO
4 6 4
①请帮助小明写出生成浅绿色沉淀的有关反应的化学方程式
。
②请帮助小明设计一个实验,证明该浅绿色沉淀中含有硫酸根。
。
25.(5分)小明按右图装好了实验装置(两胶头滴管中的稀盐酸浓度和体积都相等),实验时,
同时完全捏扁两滴管的胶头,并观察实验现象。
⑴小明实验的目的是: 。
⑵装置中长玻璃导管的作用是: ;
红墨水的作用是: 。
⑶你估计两根玻璃导管中的实验现象是 ;
理由是 。
四、计算题(本题包括2小题,共14分。)
26.(8分)闪电是一种自然现象,据估计地球上年平均发生31万余次闪电。每当电闪雷鸣之
时,空气中发生的一种反应为N + O == 2NO。已知32g氧气和足量的氮气化合成一氧化
2 2
氮时要吸收180kJ的能量,假设某次闪电的能量为1.50ⅹ107kJ,其中1/1000的能量用于这
一反应,求:⑴此次闪电所产生的NO的质量是多少千克?
⑵此次闪电的生成物相当于多少千克尿素[CO(NH)]的含氮量?
2
27.(6分)糖类(按C H O 计,相对分子质量为180)发酵生成乙醇反应的化学方程式为
6 12 6
C H O = 2C HOH + 2CO,问多少质量分数的糖类溶液发酵能得到1º的酒?(1º酒是指:
6 12 6 2 5 2
1体积乙醇和99体积水的混合溶液。水和乙醇的密度分别为 1.0g/cm3和0.8g/cm3)(答案只
要求小数点后一位数字)
答案
一、选择题:
题号 1 2 3 4 5 6 7 8 9 1O 1l 12 13 14 15
-
答案 C C A A D C A B C B BD D BD C A
二、填空题: (本题包括7个小题,共38分)1 6.(4分)(每空2分)
(1)39.8%, (2)2
17.(3分)酒精燃烧释热,使部分酒精挥发(1分)(减少了燃烧释放的热量);
使水蒸发消耗并带走热量(1分);使手帕达不到着火点。 (1分)18. (5分)供给呼吸 CH 0+60=6C0+6H0 支持燃烧
6 12 6 2 2 2
(分别为1、3、1分)19. (3分)CO、CO:CO、0:CO、02、CO2, (各1分)
2 2
20. (9分) (每空1分)
猜想黑色固体是 实验操作 现象
(1}氧化铜 取少量黑色固体放入试管中,黑色固体全部溶解,溶液变成蓝
加入足量的稀硫酸,振荡 色,试管底部有少量红色固体
(2)木炭 取少量黑色固体放入试管中.无明显现象
加入足量的稀硫酸,振荡
(3)木炭和氧化铜取少量黑色固体放入试管中,黑色固体部分溶解,溶液变成蓝
的混合物 加入足量的稀硫酸,振荡 色,试管底部有少量红色固体
21. (8分) (每空1分)
步骤 实验操作 实验现象 推断(或结论)
(1) 将取出的两种溶液混合 混合溶液无色、澄 混合液中肯定不含:Cu(N0)
3 2
清
无明显现象 混合溶液肯定不是下列组合:HS0 与
2 4
NaC0 或 HN0 与NaC0
2 3 3 2 3
(2) 用pH试纸测定混合溶 测定结果:pH=2 溶液呈酸性,所以一定有酸 性物质
液的pH 存在,如H2S04或 HN03
(3) 向混合溶液中滴入足 有白色溶液出现 H2S04或Na 2S04(或H2S04
量Ba(N03)2溶液 和Na2S04同时共存)
(4) 向上述溶液过滤所的 滤 无明显现象 不含NaCl
液中滴加AgN03溶液
混合溶液的可能组合(写出溶 ①HN03 H2g04 ②HN03 Na 2S04 ③H2804 Na2S04
质的化学式,有几组写几组) ④H2SO4 NaN03
22.(6分) (每空2分)
(1)水温升高,DO饱和值下降:光照增强,水生植物光合作用加强,产氧 量增加 (2
分)
(2)①11.85 mg-L-1 (2分)
②不适合鱼类生存。因为25℃饱和DO值为8.15 mg.L-1,小于BOD的
11.85 mg.L-1,会造成鱼类缺氧 (2分)
三、实验题: (本题包括3个小题,共18分)
23. (6分)
(1) 不漏气(1分) 由于不漏气,加水后试管内气体体积减小,导致压
强增大,长颈漏斗内的水面高出试管内的水面。 (2分)
(2)无法确定(1分)由于分液漏斗和烧瓶间有橡皮管相连,使分液漏斗
中液面上方和烧瓶中液面上方的压强相同,无论装置是否漏气,都不
影响分液漏斗中的水滴入烧瓶。 (2分)
24. (7 分) (1)CuSO +2NaOH=Cu(OH)↓+NaS0(1 分) Cu(OH) =CuO+HO
4 2 2 4 2 2
(1分)(2)① 4CUS0+6NaOH=Cu(OH)S0 ↓+3NaS0(2分)
4 4 6 4 2 4
②将浅绿色的浊液过滤,并把得到的绿色沉淀用蒸馏水多次洗涤,至洗涤液中用BaCl
2
溶液检验不出S02-后,用稀盐酸溶解绿色沉淀,此时再用BaCl 溶液检验,溶解液中有大量白
4 2
色BaS0 生成,表示浅绿色沉淀中有S02-。 (2分)
4 4
25. (5分)
(1)比较粉末状和块状的碳酸钙和同浓度、同体积盐酸反应的速率的大小。(1分)
(2)相同的液体体积变化在细长的玻璃导管中造成的液面高度变化大,便于 观察: (1
分)
使导管中的液柱呈现红色,便于观察导管中液面高度的变化。 (1分)
(3)两装置中导管内的液面均上升,装置A中导管内液面的上升速度比装置B的快(1分):
等质量的粉末状碳酸钙与盐酸的接触面积比块状碳酸钙的大,反应速率快,单位时间内产生
的气体多,压上的液柱高度增高。(1分)
四、计算题: (本题包括2个小题,共14分)26. (8分)
解: (1)设生成NO的质量为x