文档内容
2008 年“天原杯”初中化学竞赛
广东省初赛试题
说明:
1、本试题分两部分,总分130分,考试时间为120分钟。
2、答题前,考生必须将自己所在的学校、班级、姓名、座号写在密封线内。
3、相对原子质量: H—1 C—12 O—16 S—32 Ca—40 Fe—56 Cu—64
Zn—65 Al—27 Mg—24 K—39 I—127
题号 一 二 三 四 五 六 七 八 总分
分数
第一部分 (共100分)
一、选择题(共计14小题,每小题2分,共28分,每小题只有一个选项符合题意)
1.下列自然界中的变化,没有新物质生成的是 ( )
A.食物腐烂 C.光合作用 B.钢铁生锈 D.露水蒸发
2.元素在自然界里分布并不均匀,如智利富藏铜矿、澳大利亚多铁矿、我国山东富含
黄金,但从在整个地壳含量来看,最丰富的金属元素是( )
A. Fe B. Si C. O D. Al
3.下列试剂瓶标签上的化学式书写错误的是( )
4 . 下列各组物质按照单质、氧化物、混合物的顺序排列的是 ( )
A.水银 水 糖水 B.石墨 熟石灰 生石灰
C.氮气 氧气 空气 D.冰 干冰 冰醋酸
5.下列实验操作错误的是 ( )
A.倾倒液体 B.装入固体粉末 C.加热液体 D.读取液体体积
6.下列操作或现象与分子对应的特性不一致的选项是( )
选项 操作或现象 分子的特性
A 25m3的石油气在加压装入容积为0.024m3的钢瓶中 分子间有间隔
号考
名姓
级班
校学
密
封
线
内
不
得
答
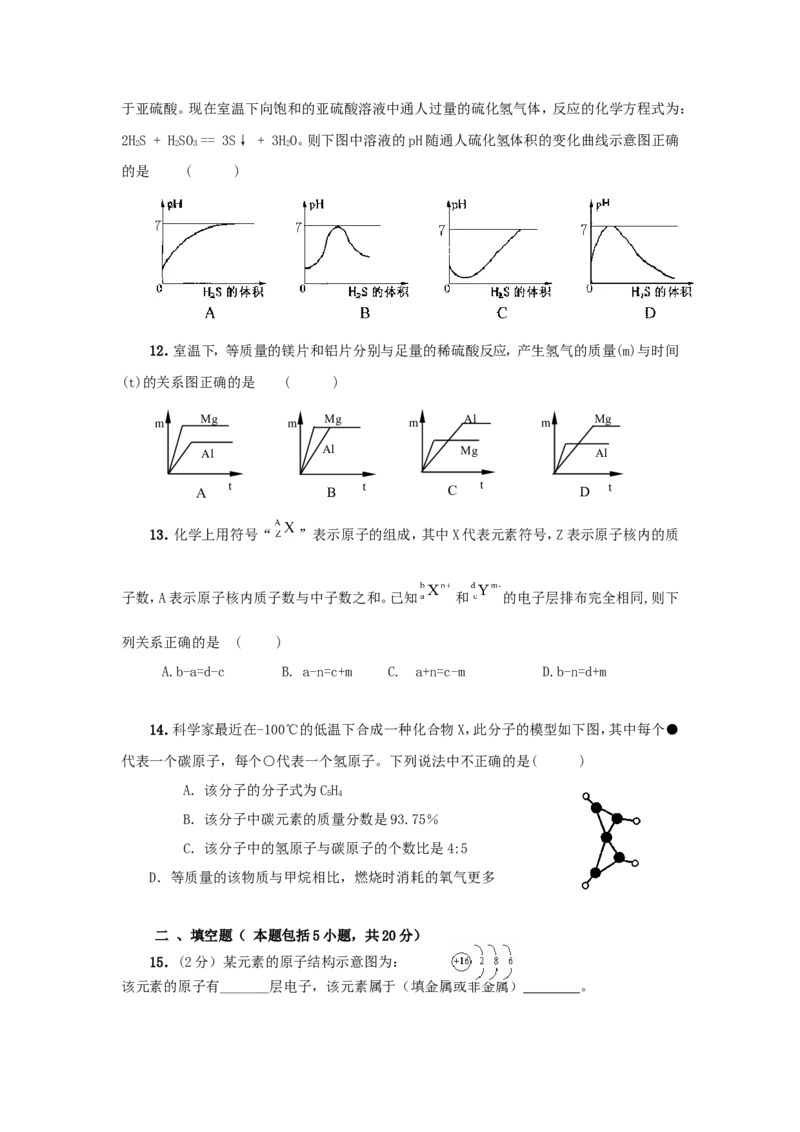
题B 经过加油站常闻到汽油的气味 分子是运动的
C 100mL氧气和100mL氮气混合在一起,体积小于200mL 分子的质量非常小
D 加热氧化汞可得到金属汞和氧气 分子是可以再分的
7.在物质混合、反应等过程中,会存在“1+1≠2”的现象。通常情况下,下列各种混合或
反应过程中,“1+1”不等于“2”的是( )
A. 1g酒精和1g水混合后的总质量
B. 1g金属锌和1g稀盐酸反应后溶液的质量
C. 温度一定时1g饱和硝酸钾溶液中加入1g硝酸钾后,所得溶液的质量
D. 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量
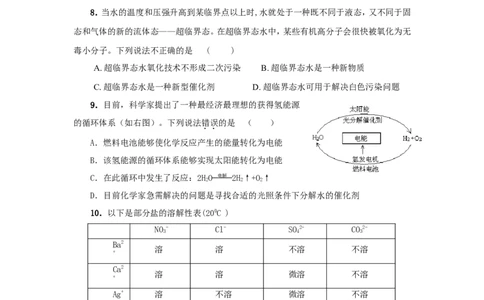
8.当水的温度和压强升高到某临界点以上时,水就处于一种既不同于液态,又不同于固
态和气体的新的流体态——超临界态。在超临界态水中,某些有机高分子会很快被氧化为无
毒小分子。下列说法不正确的是 ( )
A. 超临界态水氧化技术不形成二次污染 B. 超临界态水是一种新物质
C. 超临界态水是一种新型催化剂 D. 超临界态水可用于解决白色污染问题
9.目前,科学家提出了一种最经济最理想的获得氢能源
的循环体系(如右图)。下列说法错误的是 ( )
A.燃料电池能够使化学反应产生的能量转化为电能
B.该氢能源的循环体系能够实现太阳能转化为电能
C.在此循环中发生了反应:2HO 电解 2H↑+O↑
2 2 2
D.目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂
10.以下是部分盐的溶解性表(200C )
NO- Cl- SO2- CO2-
3 4 3
Ba2
溶 溶 不溶 不溶
+
Ca2
溶 溶 微溶 不溶
+
Ag+ 溶 不溶 微溶 不溶
根据以上信息无法获得的启示是 ( )
A、实验室不用大理石与硫酸来制二氧化碳,因为硫酸钙是微溶的
B 、硝酸盐都能溶解在水中
C 、Ba2+ 和SO2-不能共同存在一杯溶液中
4
D、碳酸钡是一种有毒的盐
11.二氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(HSO )。硫化氢(HS)是
2 3 2
一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。已知相同的条件下,氢硫酸的酸性弱于亚硫酸。现在室温下向饱和的亚硫酸溶液中通人过量的硫化氢气体,反应的化学方程式为:
2HS + HSO == 3S↓ + 3HO。则下图中溶液的pH随通人硫化氢体积的变化曲线示意图正确
2 2 3 2
的是 ( )
12.室温下,等质量的镁片和铝片分别与足量的稀硫酸反应,产生氢气的质量(m)与时间
(t)的关系图正确的是 ( )
Mg Mg Al Mg
m m m m
Al Al Mg Al
A t B t C t D t
13.化学上用符号“ ”表示原子的组成,其中X代表元素符号,Z表示原子核内的质
子数,A表示原子核内质子数与中子数之和。已知 和 的电子层排布完全相同,则下
列关系正确的是 ( )
A.b-a=d-c B. a-n=c+m C. a+n=c-m D.b-n=d+m
14.科学家最近在-100℃的低温下合成一种化合物X,此分子的模型如下图,其中每个●
代表一个碳原子,每个○代表一个氢原子。下列说法中不正确的是( )
A.该分子的分子式为CH
5 4
B.该分子中碳元素的质量分数是93.75%
C.该分子中的氢原子与碳原子的个数比是4:5
D.等质量的该物质与甲烷相比,燃烧时消耗的氧气更多
二 、填空题( 本题包括5小题,共20分)
15.(2分)某元素的原子结构示意图为:
该元素的原子有_______层电子,该元素属于(填金属或非金属) 。16.( 4分)物质的用途与物质的性质密切相关。某同学根据此规律进行归纳、整理,请
你帮助他补充填空:
物质 性质 → 用途 物质 性质 → 用途
石墨 导电性 → ① 氢气 ③ →填充升空气球
盐酸 酸性 → ② 一氧化碳 ④ →冶炼金属
17.(4分)沼气(主要成分甲烷)是当今已开发和使用的最洁净的气体燃料之一,使用沼
气是解决农村能源不足问题的重要途径。
(1)写出甲烷燃烧的化学方程式 。
(2)沼气中除含有甲烷外,还含有二氧化碳及少量的氢气、氮气、硫化氢、一氧化碳、水
蒸气等。沼气略带臭味,你认为臭味可能来自_______________气体。
(3)从安全方面考虑,使用沼气时一定要防止沼气中混入________________。
18.(5分) 置换反应是化学反应的基本类型之一。
⑴ 金属与盐溶液之间的置换反应,一般是活动性较强的金属可把活动性较弱的金属
从其盐溶液中置换出来。如铜和硝酸银溶液的化学方程式为__________________________。
⑵ 非金属单质也具有类似金属与盐溶液之间的置换反应的规律,即活动性较强的非
金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:
, , 由此可判断:
①S、Cl、I、Br 非金属活动性由强到弱顺序是___________________________。
2 2 2
②下列化学方程式书写错误的是______________________。
A. B.
C. D.
19.(5分) 某同学欲配置40g质量分数为9%的氯化钠溶液,全部操作过程如下图所示,
看图回答下列问题:
(1) 称量时,应称取 g 食盐;把水的密度近似地看作1g/mL,则须量取
mL水。如果有10mL、50mL和100mL的量筒,最好选取 mL的量筒。
(2)实验中使用玻璃棒的目的是 。
(3)如果所配得的溶液溶质的质量分数比小于9%,你认为可能的原因有(写一条):
。
三、简答题( 本题包括2小题 ,共15分 )
20. (8分)温室效应被列为21世纪人类面临的最大威胁之一,二氧化碳是大气中的主
要温室气体。为了减缓二氧化碳使全球变暖的趋势,有科学家设想:将排放到空气中的二氧化碳压缩使其液化,然后将其压入到冰冷的深海中。但也有科学家担心海水中富含二氧化碳
后酸度会增加,可能会杀死一些海洋生物,甚至会溶解掉部分海床,从而造成灾难性的后果。
(1)为减少二氧化碳这种温室气体的排放,我们可以采取的措施有:
、 。(两种即可)
(2)二氧化碳气体转变为液体时将会 能量(填“释放”或“消耗”);
(3) 二氧化碳使海水酸度增加的原理用化学方程式表示为:
;
(4)二氧化碳在深海中的溶解度比在通常状况下的水中的溶解度 ,理由是
。
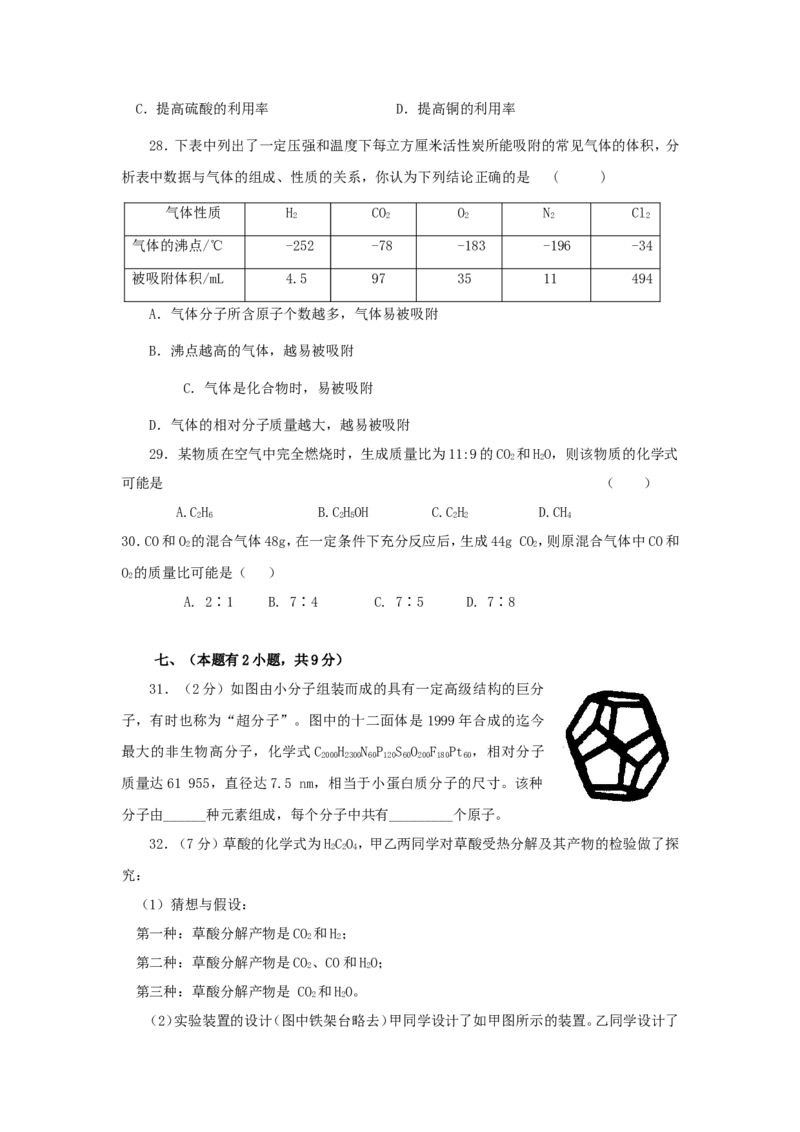
21.( 7分) 已知A、B是常见的碱,甲、乙是常见的盐,C是一种常见的无色无味的气体。
这几种物质间的转化关系如图所示。请回答:
(1):下列物质的化学式:A 、B 、甲 ;
(2)写出甲与A反应的化学方程式 ;
该反应的基本类型属于 ;
(3)若要测定B溶液酸碱度的大小,应选择(填序号) 。
①pH试纸 ②石蕊试液 ③酚酞试液
四、实验题(本题包括2小题 ,共23分 )
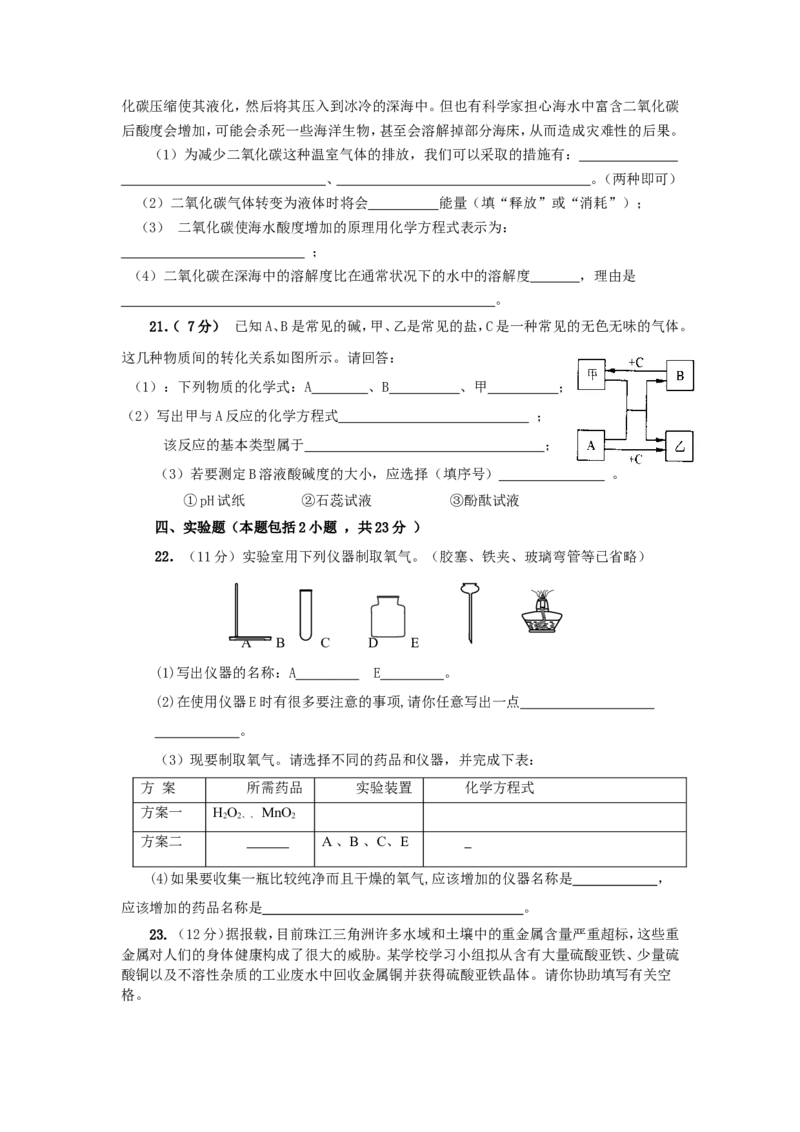
22.(11分)实验室用下列仪器制取氧气。(胶塞、铁夹、玻璃弯管等已省略)
A B C D E
(1)写出仪器的名称:A E 。
(2)在使用仪器E时有很多要注意的事项,请你任意写出一点
。
(3)现要制取氧气。请选择不同的药品和仪器,并完成下表:
方 案 所需药品 实验装置 化学方程式
方案一 HO MnO
2 2、、 2
方案二 A 、B 、C、E
(4)如果要收集一瓶比较纯净而且干燥的氧气,应该增加的仪器名称是 ,
应该增加的药品名称是 。
23. (12分)据报载,目前珠江三角洲许多水域和土壤中的重金属含量严重超标,这些重
金属对人们的身体健康构成了很大的威胁。某学校学习小组拟从含有大量硫酸亚铁、少量硫
酸铜以及不溶性杂质的工业废水中回收金属铜并获得硫酸亚铁晶体。请你协助填写有关空
格。(1)操作步骤和目的如下:
操 作 步 骤 目 的
①将废水过滤 ①
②向滤液中加入过量铁粉 ②
③ ③将Cu和过量的铁粉与FeSO 溶液分离
4
④在过滤后的固体混合物中加入过量稀硫酸 ④
⑤将反应后的混合物过滤 ⑤
⑥ ⑥得到硫酸亚铁晶体
(2)写出步骤②和步骤④的化学方程式: 、 。
(3)步骤②中,加入的铁粉刚好反应完后,继续加入的铁粉对最后得到的铜和硫酸亚铁晶
体质量的影响分别是(填增大、减小或不变):铜的质量 ;硫酸亚铁晶体质量
。
五、计算题( 本题包括2小题 ,共14分 )
24 . (7分)下图是某厂生产的加钙碘盐包装袋商标的部分内容。请仔细阅读后回答以
下问题:
(1)人体缺乏钙元素易引发的疾病是 (填代码) 配料表:氯化钠、食用碳酸钙、
A.夜盲症 B.甲状腺肿大 C.佝偻病 D.坏血病 碘酸钾
(2)碘酸钾(化学式为KIO)中碘元素的质量分数是多少? 净含量:500g
3
成份表:氯化钠≥88%
钙含量:0.5%~1.3%
(3)一袋该食盐中KIO 3 的质量最多是多少? 碘含量:40~50mg/Kg
25.(7分)原煤中含有硫元素,在燃烧过程中产生的二氧化硫会造成大气的污染。某煤场
向原煤中加入适量的生石灰制成供居民采暖用的“环保煤”,以减少二氧化硫的排放,消弱
二氧化硫对空气的污染。燃烧时生石灰吸收二氧化硫的化学方程式为:
。请回答下列问题:
(1)m值是______________________;(2)若煤厂一次共加入含氧化钙80%的生石灰1400 t,则理论上最多可吸收二氧化硫多
少吨?
第二部分(共30分)
六、选择题(本题有5小题,每小题3分,共15分。每小题有1或2个选项符合题意。若
有两个答案的选1 个而且正确的得1分,凡是有错误的不得分。)
26.印制电路板时常用氯化铁溶液作为“腐蚀液”,发生的反应为:2FeCl+Cu=2FeCl+
3 2
CuCl,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现
2
的是( )
A.烧杯中有铜无铁 B.烧杯中有铁无铜
C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
27.铜与浓硫酸共热的条件下可以发生化学反应 Cu + 2HSO = CuSO + SO↑ +
2 4 4 2
2HO,但是在工业上制取硫酸铜不是直接利用浓硫酸与铜反应,而是将铜屑在空气中加热氧
2
化,然后浸入稀硫酸中反应过滤,并反复加热和浸入操作,你认为这样的优点是( )
A.节约能源 B.不产生污染大气的二氧化硫C.提高硫酸的利用率 D.提高铜的利用率
28.下表中列出了一定压强和温度下每立方厘米活性炭所能吸附的常见气体的体积,分
析表中数据与气体的组成、性质的关系,你认为下列结论正确的是 ( )
气体性质 H CO O N Cl
2 2 2 2 2
气体的沸点/℃ -252 -78 -183 -196 -34
被吸附体积/mL 4.5 97 35 11 494
A.气体分子所含原子个数越多,气体易被吸附
B.沸点越高的气体,越易被吸附
C.气体是化合物时,易被吸附
D.气体的相对分子质量越大,越易被吸附
29.某物质在空气中完全燃烧时,生成质量比为11:9的CO 和HO,则该物质的化学式
2 2
可能是 ( )
A.CH B.CHOH C.CH D.CH
2 6 2 5 2 2 4
30.CO和O 的混合气体48g,在一定条件下充分反应后,生成44g CO,则原混合气体中CO和
2 2
O 的质量比可能是( )
2
A. 2∶1 B. 7∶4 C. 7∶5 D. 7∶8
七、(本题有2小题,共9分)
31.(2分)如图由小分子组装而成的具有一定高级结构的巨分
子,有时也称为“超分子”。图中的十二面体是1999年合成的迄今
最大的非生物高分子,化学式C H N P S O F Pt ,相对分子
2000 2300 60 120 60 200 180 60
质量达61 955,直径达7.5 nm,相当于小蛋白质分子的尺寸。该种
分子由______种元素组成,每个分子中共有_________个原子。
32.(7分)草酸的化学式为HCO,甲乙两同学对草酸受热分解及其产物的检验做了探
2 2 4
究:
(1)猜想与假设:
第一种:草酸分解产物是CO 和H;
2 2
第二种:草酸分解产物是CO、CO和HO;
2 2
第三种:草酸分解产物是 CO 和HO。
2 2
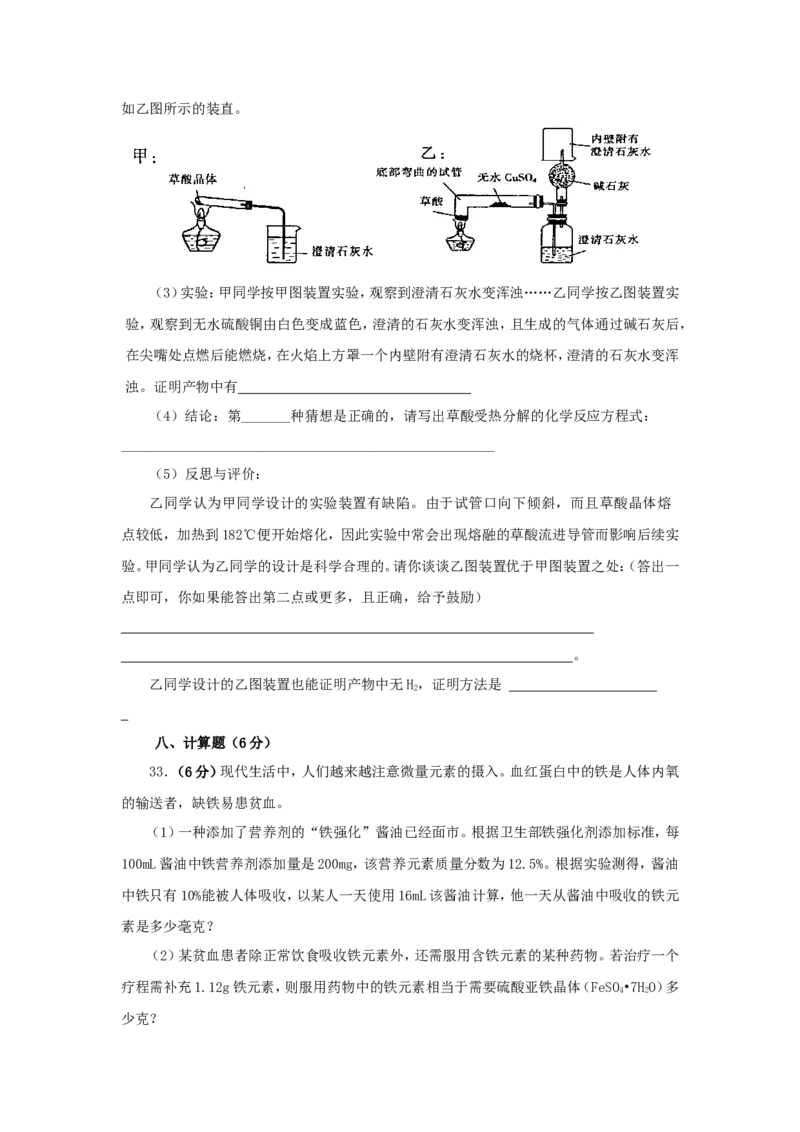
(2)实验装置的设计(图中铁架台略去)甲同学设计了如甲图所示的装置。乙同学设计了如乙图所示的装直。
(3)实验:甲同学按甲图装置实验,观察到澄清石灰水变浑浊……乙同学按乙图装置实
验,观察到无水硫酸铜由白色变成蓝色,澄清的石灰水变浑浊,且生成的气体通过碱石灰后,
在尖嘴处点燃后能燃烧,在火焰上方罩一个内壁附有澄清石灰水的烧杯,澄清的石灰水变浑
浊。证明产物中有
(4)结论:第_______种猜想是正确的,请写出草酸受热分解的化学反应方程式:
_____________________________________________________
(5)反思与评价:
乙同学认为甲同学设计的实验装置有缺陷。由于试管口向下倾斜,而且草酸晶体熔
点较低,加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实
验。甲同学认为乙同学的设计是科学合理的。请你谈谈乙图装置优于甲图装置之处:(答出一
点即可,你如果能答出第二点或更多,且正确,给予鼓励)
。
乙同学设计的乙图装置也能证明产物中无H,证明方法是
2
八、计算题(6分)
33.(6分)现代生活中,人们越来越注意微量元素的摄入。血红蛋白中的铁是人体内氧
的输送者,缺铁易患贫血。
(1)一种添加了营养剂的“铁强化”酱油已经面市。根据卫生部铁强化剂添加标准,每
100mL酱油中铁营养剂添加量是200mg,该营养元素质量分数为12.5%。根据实验测得,酱油
中铁只有10%能被人体吸收,以某人一天使用16mL该酱油计算,他一天从酱油中吸收的铁元
素是多少毫克?
(2)某贫血患者除正常饮食吸收铁元素外,还需服用含铁元素的某种药物。若治疗一个
疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁晶体(FeSO•7HO)多
4 2
少克?2008年“天原杯”广东省初中化学竞赛初赛试题答案
第一部分((共100分)
一 、 选择题(本题包括14小题,本大题共28分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D D C A C C B B C D B C B D
二 、填空题( 本题包括5小题,共20分)
15.(2分)3;非金属
16.( 4分)电极;除铁锈 ; 密度最小;还原性
17.(4分)CH+2O CO+2HO;硫化氢;空气(或氧气)
4 2 2 2
18.(5分) ⑵ ①Cl>Br>I>S ② B
2 2 2
19.(5分) 4.5 45.5 50 加速溶解 取水时视线俯视;称量固体时左码右物三、简答题( 本题包括2小题 ,共15分 )
20. (8分)(1).开发新能源;减少矿石燃料的使用或提高燃料的利用率。
2释放; 3、CO+HO=HCO; 4大;深海中压强大,温度低。
2 2 2 3
21.( 7分) Ca(OH); NaOH; NaCO NaCO + Ca(OH) === CaCO↓+ 2NaOH
2 3 3 3 3 2 3
复分解反应; ①
四、 实验题(本题包括2小题 ,共23分 )
22.(11分) (1)铁架台;酒精灯
(2)酒精不能超过酒精灯容积的2/3;用酒精灯外焰加热等(或其他合理答案)
MnO
2、
(3)ABCD或CD 2HO ===== 2HO + O↑
2 2 2 2
(4)水槽;碱石灰(或生石灰、烧碱、浓硫酸等)
23.(1)
① ① 除去不溶性杂质
② ②与硫酸铜完全反应
③过滤 ③
④ ④除去过量的铁
⑤ ⑤得到硫酸亚铁溶液和铜
⑥将滤液蒸发结晶 ⑥
(2) Fe + CuSO === FeSO + Cu Fe+ HSO =H↑+ Fe SO
4 4 2 4 2 2 4
(3)不变;增大
24 .(共7分)(1)C (1分)
(2)59.3% (3分)
(3)42.2mg (3分)
25.(1)(2分) 所以
(2)(2分)解:设理论是最多吸收二氧化硫的质量为x。
112 128
1400t×80% x
第二部分(共30分)
六、选择题(本题有5小题,每小题3分,共15分)
题号 26 27 28 29 30
答案 B BC BD D AC
七、(本题有2小题,共9分)
31. (共2分) 8 4980
32.(共7分)(3)、CO、CO、HO。(1分)
2 2
(4)第二种(1分) HCOComCO↑+CO↑+HO (2分)
2 2 4bin 2 2
(5)底部弯曲的试管避免了熔化的草酸晶体流进导管 (1分)(或乙同学设计的装置
可同时证明 CO、CO、HO的存在;或乙同学的设计在验证了CO存在的同时又解决了CO
2 2
的污染问题)
证明方法:在干燥管的尖嘴处点燃干燥后导出的气体、并在火焰上方罩一个冷而干燥的小烧杯,烧杯内壁无水雾。 (2分)
八、(6分)
33.(6分)⑴ (3分)设16mL该酱油中含铁元素质量为x
由题意得:100mL∶(200mg ×12 .5%)=16mL∶x
解得:x= 4mg
∴此人一天从酱油中吸收的铁元素质量为4mg×10%=0.4 mg
⑵ (3分)设需要硫酸亚铁晶体(FeSO·7HO)晶体质量为y
4 2
Fe ~ FeSO·7HO
4 2
56 278
1.12g y
56∶1.12 g = 278∶y
解得y = 5.56g
答:⑴0.4 mg; ⑵5.56g