文档内容
绝密★启用前
2025 年高考考前信息必刷卷 01
化 学
考情速递
高考·新动向:
1.跨学科融合:化学与物理、生物、环境科学等学科的交叉融合将成为命题趋势。例如,化学反应与能
量转化、化学物质与生态环境的关系等。
2.贴近生活与科技前沿:命题将更多结合生活实际和科技发展,如新能源材料、环境保护、医药合成
等,体现化学学科的社会价值。
高考·新考法:
1. 情境化命题:试题将设置真实或模拟的情境,要求学生从情境中提取信息并解决问题。例如,以工业
生产流程、实验探究过程或环境保护问题为背景,考查学生对知识的迁移能力。
2.信息提取与整合能力:试题可能提供图表、数据或文献资料,要求学生从中提取关键信息并进行分
析。例如,根据反应速率曲线推断反应机理,或利用物质结构数据推测其性质。
高考·新情境:
1. 工业生产与工艺流程:以工业生产为背景,考查学生对化学反应原理、物质分离与提纯、资源综合利
用的理解。例如,硫酸工业、合成氨工艺、金属冶炼等。
2.医药与生命科学:结合医药合成、生物化学等领域的知识,考查学生对有机化学、物质结构与性质的
理解。例如,药物分子的设计与合成、酶催化反应等。
命题·大预测:
1. 化学反应原理
命题形式:结合工业生产流程(如合成氨、硫酸工业)或新能源开发(如燃料电池、锂电池),考查
学生对反应原理的理解与应用。
创新考法:通过图表、数据或实验现象,要求学生分析反应条件对平衡或速率的影响。
2.有机化学
命题形式:结合医药合成、农药开发或环境保护,考查学生对有机反应机理的理解与合成路线的设计
能力。
创新考法:提供未知有机物的结构或反应路径,要求学生推断其性质或设计合成路线。
(考试时间:建议50分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。可能用到的相对原子质量:H 1 C 12 N 14 O 16 P 31 S 32 K 39
第 I 卷 选择题(共 42 分)
一、选择题:本题共7小题,每题6分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1.巴黎奥运会精彩纷呈,化学在其中扮演着重要的角色。下列说法不正确的是
A.奥运奖牌铜牌采用青铜材料,青铜的熔点低于铜
B.奥运火炬以丙烷为燃料,丙烷与丙醇均属于烃类物质
C.跑鞋鞋底材料采用轻质、耐磨的聚氨酯,聚氨酯是一种高分子材料
D.水上运动中心屋顶覆盖太阳能电池板,它能将太阳能转化为电能
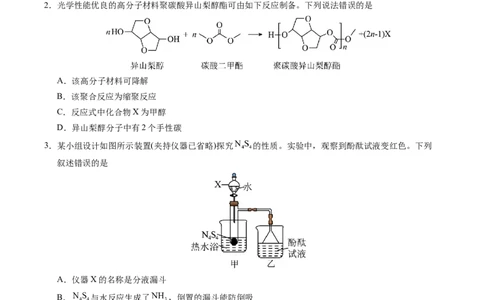
2.光学性能优良的高分子材料聚碳酸异山梨醇酯可由如下反应制备。下列说法错误的是
A.该高分子材料可降解
B.该聚合反应为缩聚反应
C.反应式中化合物X为甲醇
D.异山梨醇分子中有2个手性碳
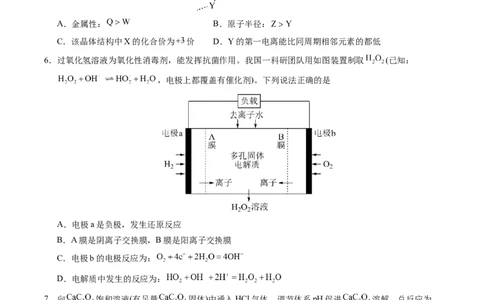
3.某小组设计如图所示装置(夹持仪器已省略)探究 的性质。实验中,观察到酚酞试液变红色。下列
叙述错误的是
A.仪器X的名称是分液漏斗
B. 与水反应生成了 ,倒置的漏斗能防倒吸
C.其他条件不变,撤去热水浴,酚酞试液变色会加快
D.若有 生成,向试管中加盐酸会产生浅黄色沉淀
4.宏观辨识与微观探析是化学学科核心素养之一、下列实验对应离子方程式书写正确的是
A.饱和 溶液中通入过量 :
B.向 中滴加少量 溶液:
C.向 溶液中通入少量 气体:D.过量铁粉加入稀硝酸中:
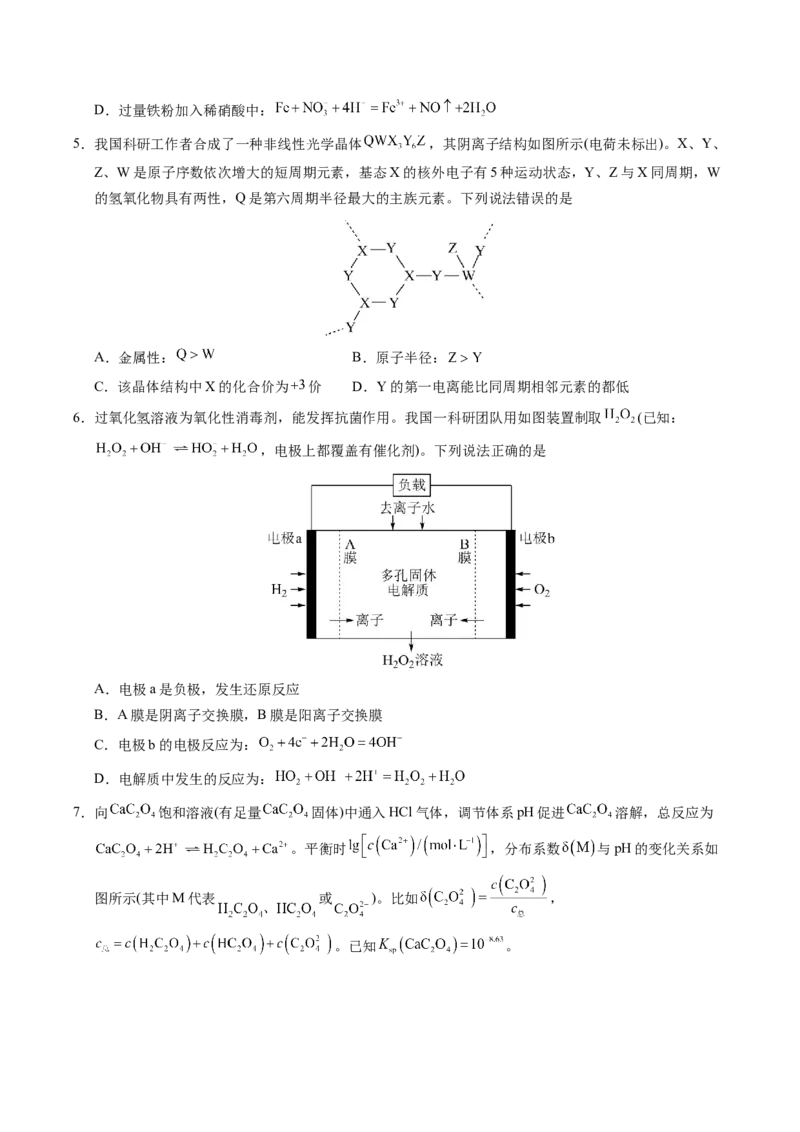
5.我国科研工作者合成了一种非线性光学晶体 ,其阴离子结构如图所示(电荷未标出)。X、Y、
Z、W是原子序数依次增大的短周期元素,基态X的核外电子有5种运动状态,Y、Z与X同周期,W
的氢氧化物具有两性,Q是第六周期半径最大的主族元素。下列说法错误的是
A.金属性: B.原子半径:
C.该晶体结构中X的化合价为 价 D.Y的第一电离能比同周期相邻元素的都低
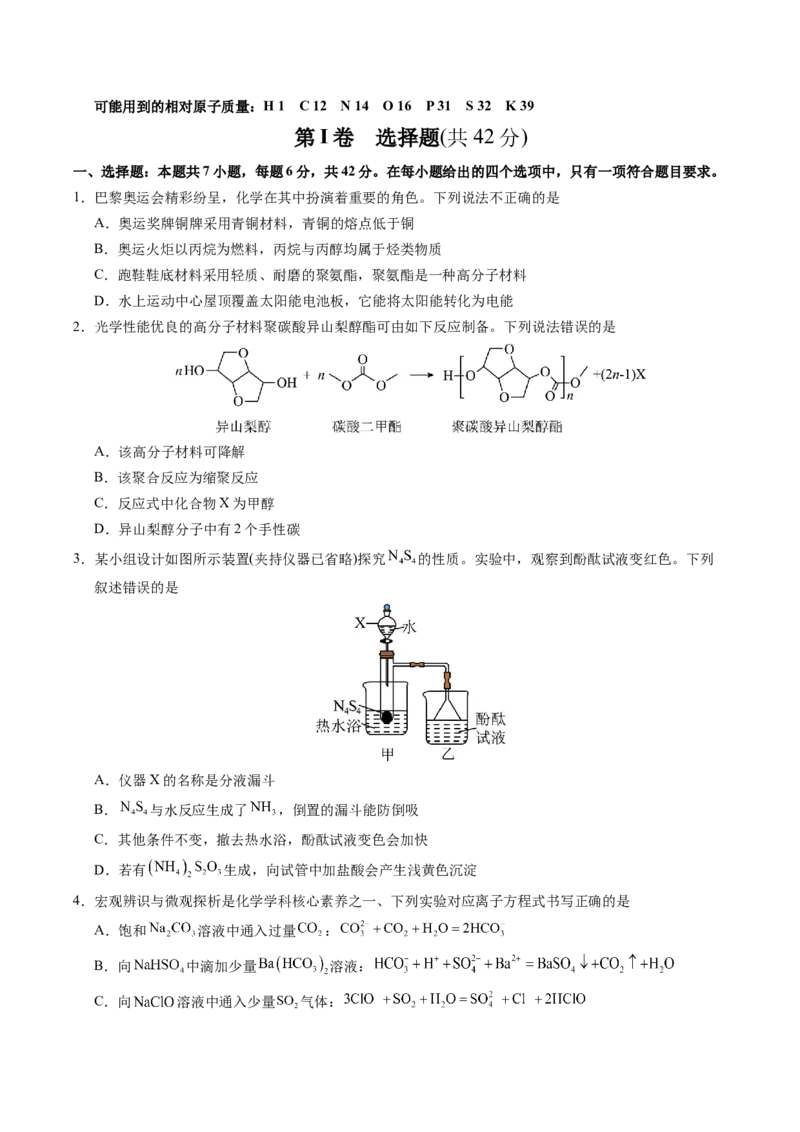
6.过氧化氢溶液为氧化性消毒剂,能发挥抗菌作用。我国一科研团队用如图装置制取 (已知:
,电极上都覆盖有催化剂)。下列说法正确的是
A.电极a是负极,发生还原反应
B.A膜是阴离子交换膜,B膜是阳离子交换膜
C.电极b的电极反应为:
D.电解质中发生的反应为:
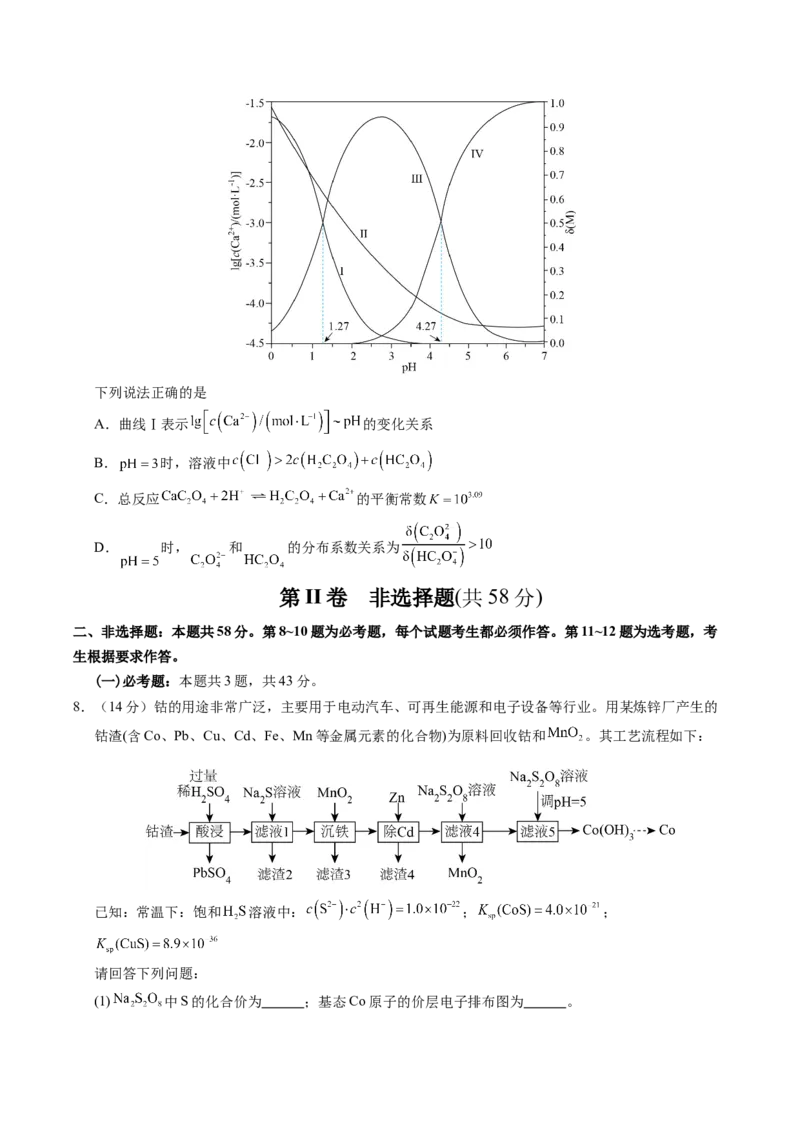
7.向 饱和溶液(有足量 固体)中通入HCl气体,调节体系pH促进 溶解,总反应为
。平衡时 ,分布系数 与pH的变化关系如
图所示(其中M代表 或 )。比如 ,
。已知 。下列说法正确的是
A.曲线Ⅰ表示 的变化关系
B. 时,溶液中
C.总反应 的平衡常数
D. 时, 和 的分布系数关系为
第 II 卷 非选择题(共 58 分)
二、非选择题:本题共58分。第8~10题为必考题,每个试题考生都必须作答。第11~12题为选考题,考
生根据要求作答。
(一)必考题:本题共3题,共43分。
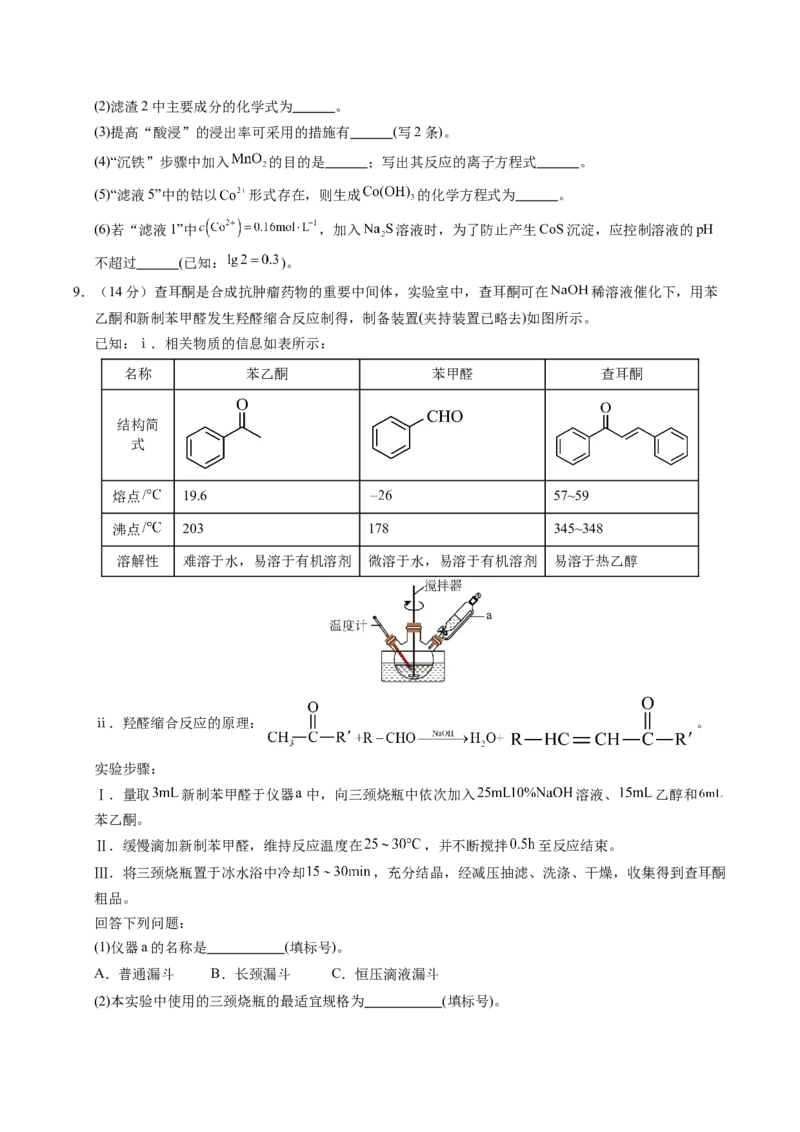
8.(14分)钴的用途非常广泛,主要用于电动汽车、可再生能源和电子设备等行业。用某炼锌厂产生的
钴渣(含Co、Pb、Cu、Cd、Fe、Mn等金属元素的化合物)为原料回收钴和 。其工艺流程如下:
已知:常温下:饱和 溶液中: ; ;
请回答下列问题:
(1) 中S的化合价为 ;基态Co原子的价层电子排布图为 。(2)滤渣2中主要成分的化学式为 。
(3)提高“酸浸”的浸出率可采用的措施有 (写2条)。
(4)“沉铁”步骤中加入 的目的是 ;写出其反应的离子方程式 。
(5)“滤液5”中的钴以 形式存在,则生成 的化学方程式为 。
(6)若“滤液1”中 ,加入 溶液时,为了防止产生CoS沉淀,应控制溶液的pH
不超过 (已知: )。
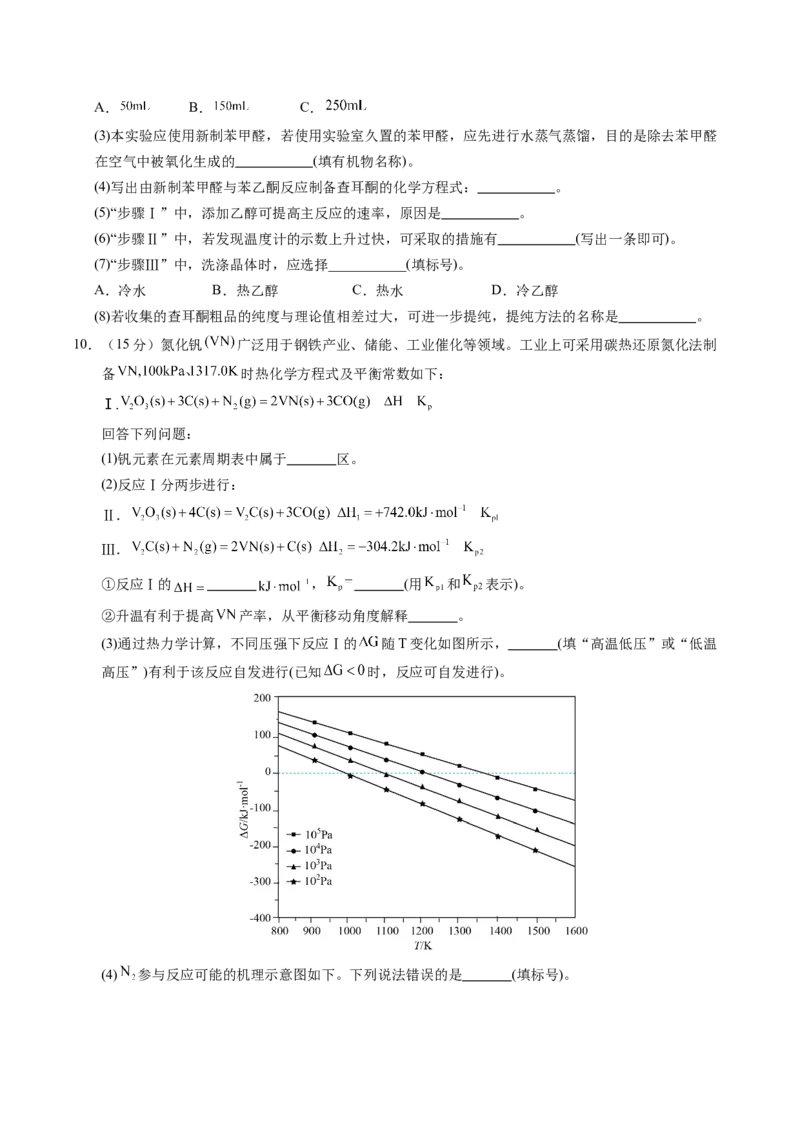
9.(14分)查耳酮是合成抗肿瘤药物的重要中间体,实验室中,查耳酮可在 稀溶液催化下,用苯
乙酮和新制苯甲醛发生羟醛缩合反应制得,制备装置(夹持装置已略去)如图所示。
已知:ⅰ.相关物质的信息如表所示:
名称 苯乙酮 苯甲醛 查耳酮
结构简
式
熔点 19.6 57~59
沸点 203 178 345~348
溶解性 难溶于水,易溶于有机溶剂 微溶于水,易溶于有机溶剂 易溶于热乙醇
ⅱ.羟醛缩合反应的原理: 。
实验步骤:
Ⅰ.量取 新制苯甲醛于仪器 中,向三颈烧瓶中依次加入 溶液、 乙醇和
苯乙酮。
Ⅱ.缓慢滴加新制苯甲醛,维持反应温度在 ,并不断搅拌 至反应结束。
Ⅲ.将三颈烧瓶置于冰水浴中冷却 ,充分结晶,经减压抽滤、洗涤、干燥,收集得到查耳酮
粗品。
回答下列问题:
(1)仪器a的名称是 (填标号)。
A.普通漏斗 B.长颈漏斗 C.恒压滴液漏斗
(2)本实验中使用的三颈烧瓶的最适宜规格为 (填标号)。A. B. C.
(3)本实验应使用新制苯甲醛,若使用实验室久置的苯甲醛,应先进行水蒸气蒸馏,目的是除去苯甲醛
在空气中被氧化生成的 (填有机物名称)。
(4)写出由新制苯甲醛与苯乙酮反应制备查耳酮的化学方程式: 。
(5)“步骤Ⅰ”中,添加乙醇可提高主反应的速率,原因是 。
(6)“步骤Ⅱ”中,若发现温度计的示数上升过快,可采取的措施有 (写出一条即可)。
(7)“步骤Ⅲ”中,洗涤晶体时,应选择___________(填标号)。
A.冷水 B.热乙醇 C.热水 D.冷乙醇
(8)若收集的查耳酮粗品的纯度与理论值相差过大,可进一步提纯,提纯方法的名称是 。
10.(15分)氮化钒 广泛用于钢铁产业、储能、工业催化等领域。工业上可采用碳热还原氮化法制
备 时热化学方程式及平衡常数如下:
Ⅰ.
回答下列问题:
(1)钒元素在元素周期表中属于 区。
(2)反应Ⅰ分两步进行:
Ⅱ.
Ⅲ.
①反应Ⅰ的 , (用 和 表示)。
②升温有利于提高 产率,从平衡移动角度解释 。
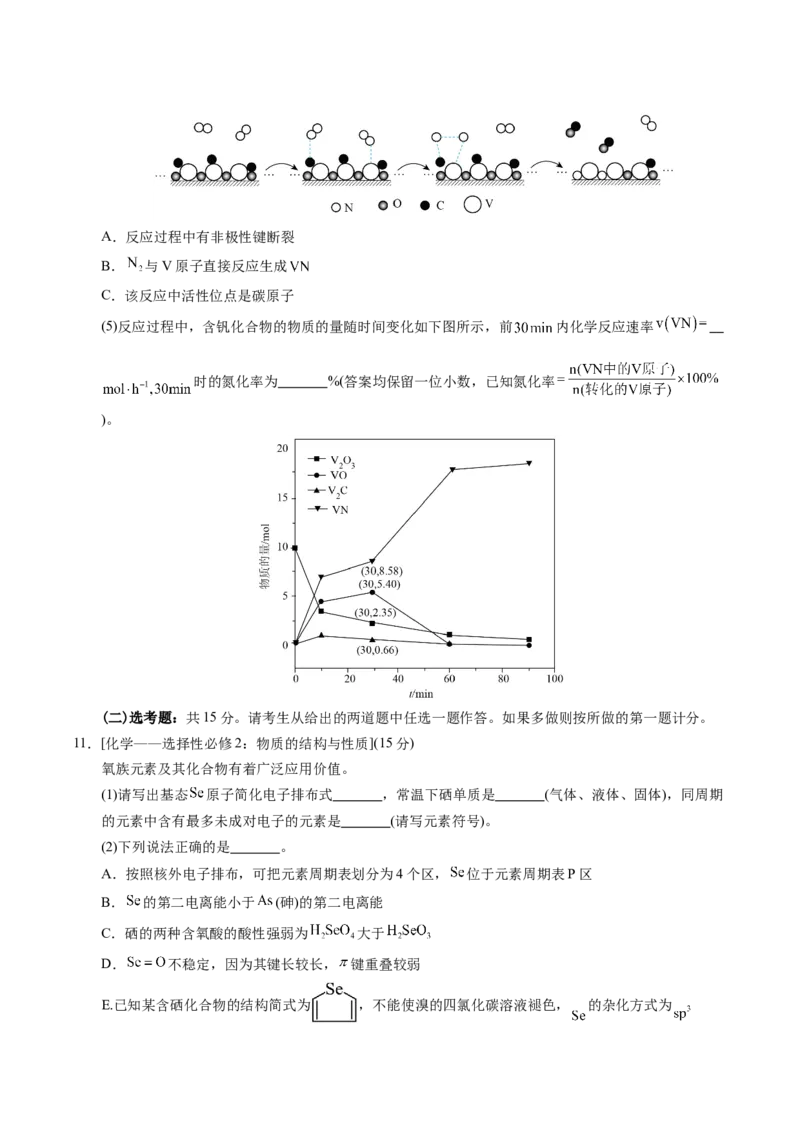
(3)通过热力学计算,不同压强下反应Ⅰ的 随T变化如图所示, (填“高温低压”或“低温
高压”)有利于该反应自发进行(已知 时,反应可自发进行)。
(4) 参与反应可能的机理示意图如下。下列说法错误的是 (填标号)。A.反应过程中有非极性键断裂
B. 与V原子直接反应生成
C.该反应中活性位点是碳原子
(5)反应过程中,含钒化合物的物质的量随时间变化如下图所示,前 内化学反应速率
时的氮化率为 %(答案均保留一位小数,已知氮化率
)。
(二)选考题:共15分。请考生从给出的两道题中任选一题作答。如果多做则按所做的第一题计分。
11.[化学——选择性必修2:物质的结构与性质](15分)
氧族元素及其化合物有着广泛应用价值。
(1)请写出基态 原子简化电子排布式 ,常温下硒单质是 (气体、液体、固体),同周期
的元素中含有最多未成对电子的元素是 (请写元素符号)。
(2)下列说法正确的是 。
A.按照核外电子排布,可把元素周期表划分为4个区, 位于元素周期表P区
B. 的第二电离能小于 (砷)的第二电离能
C.硒的两种含氧酸的酸性强弱为 大于
D. 不稳定,因为其键长较长, 键重叠较弱
E.已知某含硒化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色, 的杂化方式为(3)人体代谢甲硒醇( )后可增加抗癌活性,下表中有机物沸点不同的原因 。
有机物 甲醇 甲硫醇( ) 甲硒醇
沸点/℃ 64.7 5.95 25.05
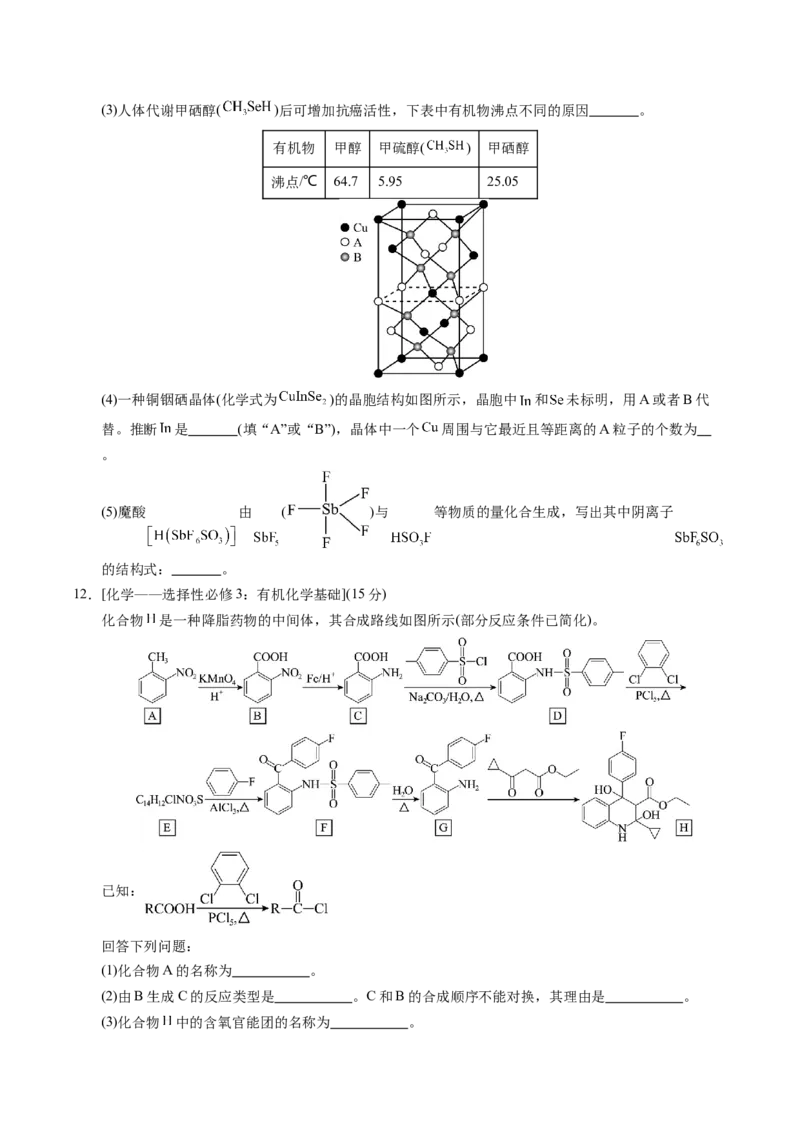
(4)一种铜铟硒晶体(化学式为 )的晶胞结构如图所示,晶胞中 和 未标明,用A或者B代
替。推断 是 (填“A”或“B”),晶体中一个 周围与它最近且等距离的A粒子的个数为
。
(5)魔酸 由 ( )与 等物质的量化合生成,写出其中阴离子
的结构式: 。
12.[化学——选择性必修3:有机化学基础](15分)
化合物 是一种降脂药物的中间体,其合成路线如图所示(部分反应条件已简化)。
已知:
回答下列问题:
(1)化合物A的名称为 。
(2)由B生成C的反应类型是 。C和B的合成顺序不能对换,其理由是 。
(3)化合物 中的含氧官能团的名称为 。(4)C转化为D的过程中加入 的作用是 。
(5)E的结构简式为 。
(6)C的同分异构体有多种,同时满足下列两个条件的有 种,其中核磁共振氢谱有5组
峰,且峰的面积之比为 的同分异构体的结构简式为 。
①与 溶液能发生显色反应 ②能发生银镜反应