文档内容
绝密★启用前
2025 年高考考前信息必刷卷 04(浙江专用)
化 学
考情速递
高考·新动向:部分考生认为化学简单到离谱,甚至觉得不需要动脑子就能做对题目,这些考生平日里
知识积累扎实,在这次考试中做题得心应手。然而,对于那些化学基础稍薄弱或者对新题型预估不足
的考生,情况则不太乐观。新的大题题型打乱了他们的解题节奏,在考场上花费大量时间理解题意和
摸索解题思路,导致时间紧张。
高考·新考法:非选择题由原来的5道精简为4道。在分值分配上,第一大题16分,第二大题12分,
第三大题12分,第四大题12分。这种变化对考生的知识综合运用能力和思维转换能力提出了更高要求。
例如物质结构和无机流程融合成了16分的第一道大题,考生不仅要熟知物质结构的微观奥秘,还要能
将其与宏观的无机流程顺畅对接,增加了答题的难度和对知识综合运用的要求。题型布局打乱,一直
以来考生习惯的大题数量和出题套路被彻底打破,出题人改变了原有的题型布局。这种变化让考生失
去了熟悉题型带来的优势,需要在考场上重新适应新的题型结构,增加了考试的挑战性。
命题·大预测:在2025浙江化学第二次考试中,难度比首考略有增加。物质分类可能会给出一些特殊的
新材料或者新型化合物,要求依据物质分类的基础定义和特殊情况进行判断。在反应分类中,可能会
出现一些新的化学反应类型组合或者特殊反应条件下的反应分类。随着新能源的发展,2025年的化学
情景可能更多涉及新能源相关化学知识。例如在氢能的利用方面。在环境方面,可能会涉及到新型的
环境治理化学方法或者污染物检测的化学原理。
(考试时间:90分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 F-19 Na-23 Mg-24 Al-27 S-32
Cl-35.5 K-39 Ca-40 V-51 Cr-52 Mn-55 Fe-56 Cu-64 Zn-65 Br-80 I-127 Ag-108 Te
-128 Ba-137 Hg-201 Bi-209
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有一项是符合题
目要求的,不选、多选、错选均不得分)
1.下列物质一定属于极性分子的是( )
A.BF B.C HF C.C HO D.二氯苯
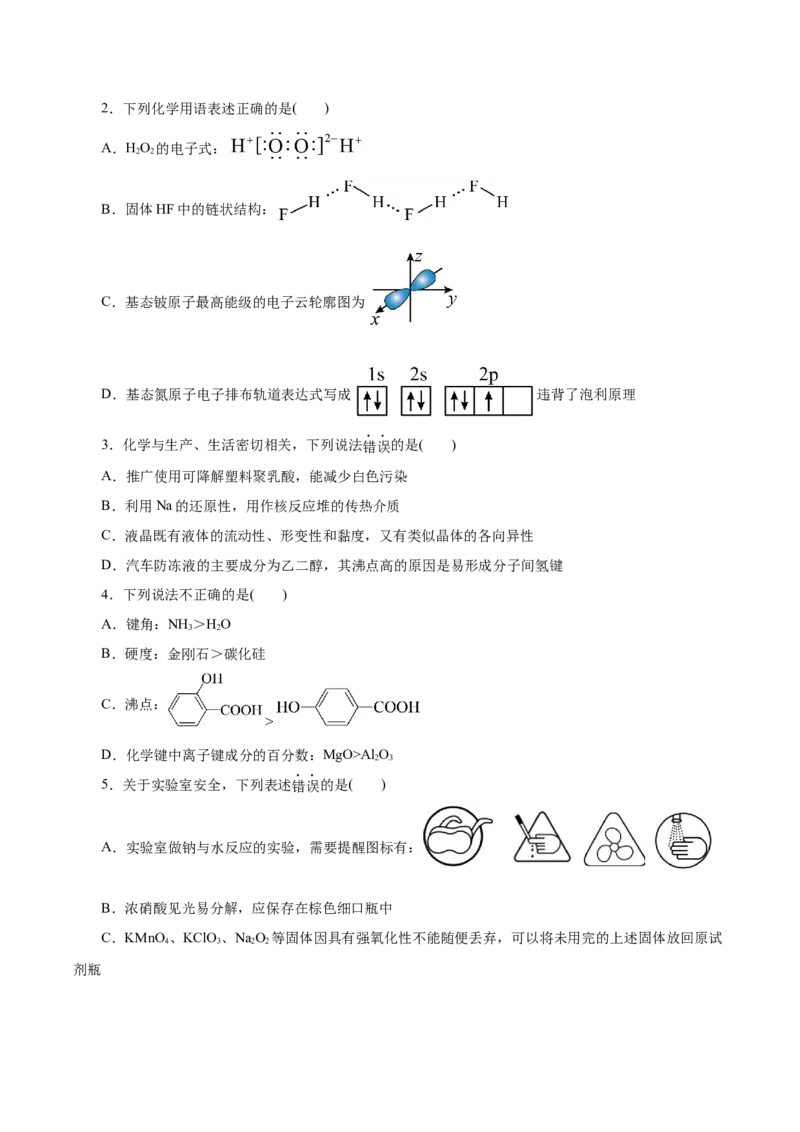
3 2 2 2 2 42.下列化学用语表述正确的是( )
A.HO 的电子式:
2 2
B.固体HF中的链状结构:
C.基态铍原子最高能级的电子云轮廓图为
D.基态氮原子电子排布轨道表达式写成 违背了泡利原理
3.化学与生产、生活密切相关,下列说法错误的是( )
A.推广使用可降解塑料聚乳酸,能减少白色污染
B.利用Na的还原性,用作核反应堆的传热介质
C.液晶既有液体的流动性、形变性和黏度,又有类似晶体的各向异性
D.汽车防冻液的主要成分为乙二醇,其沸点高的原因是易形成分子间氢键
4.下列说法不正确的是( )
A.键角:NH >HO
3 2
B.硬度:金刚石>碳化硅
C.沸点:
D.化学键中离子键成分的百分数:MgO>Al O
2 3
5.关于实验室安全,下列表述错误的是( )
A.实验室做钠与水反应的实验,需要提醒图标有:
B.浓硝酸见光易分解,应保存在棕色细口瓶中
C.KMnO 、KClO、NaO 等固体因具有强氧化性不能随便丢弃,可以将未用完的上述固体放回原试
4 3 2 2
剂瓶D.盛放浓硫酸试剂瓶的储物柜上应张贴的标识:
6.电解法合成己二腈[NC(CH )CN]的反应为:CH=CHCN+HO→NC(CH )CN+X(未配平),下列说法
2 4 2 2 2 4
不正确的是( )
A.X表示O
2
B.NC(CH )CN分子中C原子有2种杂化方式
2 4
C.每1molCH =CHCN参与反应,转移的电子数为2N
2 A
D.该反应中氧化剂与还原剂的物质的量之比为2:1
7.结构决定性质,性质决定用途。下列事实解释错误的是( )
事实 解释
A 甘油是黏稠液体 甘油分子间的氢键较强
B 王水溶解铂 浓盐酸增强了浓硝酸的氧化性
C 冰的密度小于干冰 冰晶体中水分子的空间利用率相对较低
D 石墨能导电 未杂化的p轨道重叠使电子可在整个碳原子平面内运动
8.下列离子方程式书写正确的是( )
A.FeCl 溶液中通入过量HS气体:Fe2++H S= FeS↓+2H+
2 2 2
B.向H18O中加入NaO:2NaO+2H 18O=4Na++4OH-+18O↑
2 2 2 2 2 2 2
C.向碳酸氢铵溶液中加入足量石灰水:NH ++Ca2++HCO-=CaCO ↓+ NH ·H O+HO
4 3 3 3 2 2
D.向FeI 溶液中通入足量Cl:2Fe2++2I-+2Cl=2Fe3++I+4Cl-
2 2 2 2
9.某医药中间体Z的合成路线如下,有关物质说法错误的是( )
A.物质X、Y、Z分子中原子杂化类型有sp2、sp3
B.反应Ⅰ和Ⅱ的反应类型均属于取代反应
C.若将 替换X发生反应Ⅰ,所得产物中可能含有
D.物质Z与HO的加成产物只有1种结构(不考虑立体异构)
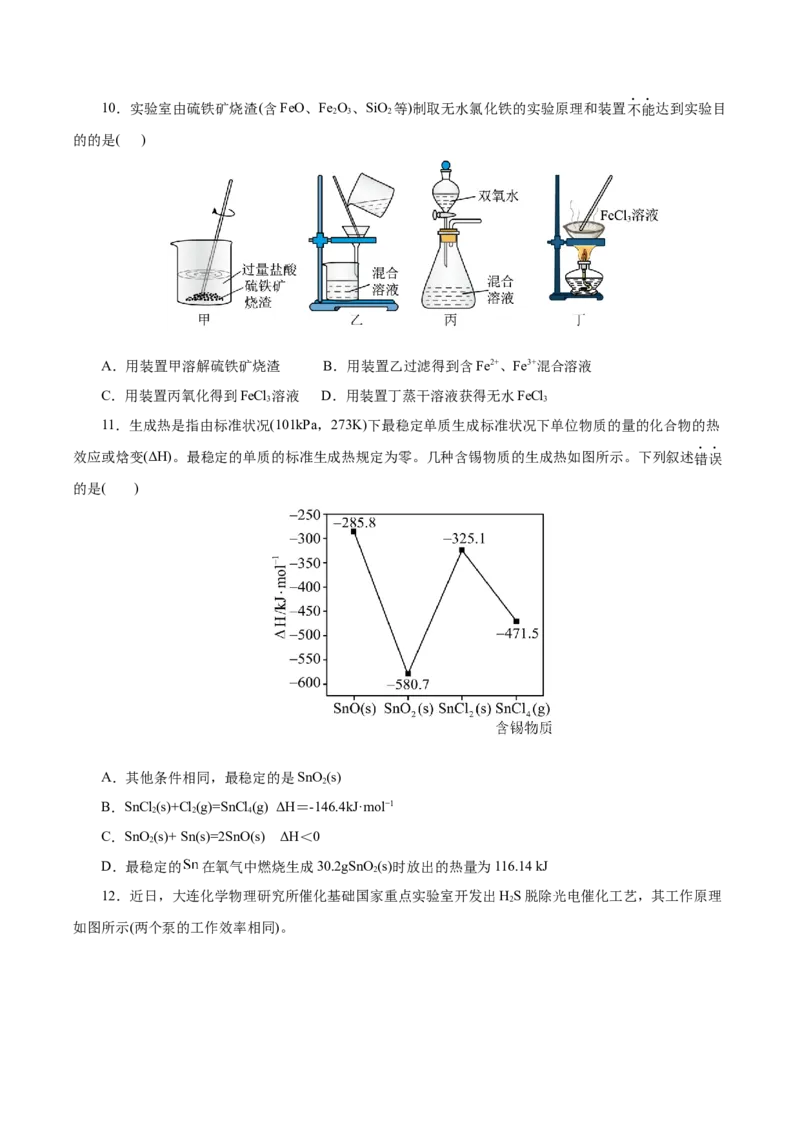
210.实验室由硫铁矿烧渣(含FeO、Fe O 、SiO 等)制取无水氯化铁的实验原理和装置不能达到实验目
2 3 2
的的是( )
A.用装置甲溶解硫铁矿烧渣 B.用装置乙过滤得到含Fe2+、Fe3+混合溶液
C.用装置丙氧化得到FeCl 溶液 D.用装置丁蒸干溶液获得无水FeCl
3 3
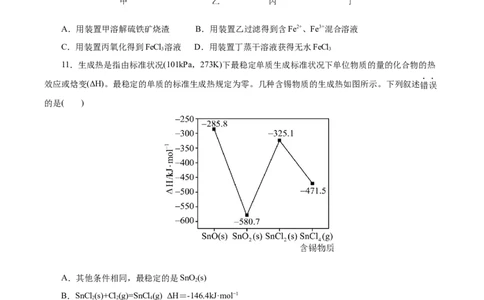
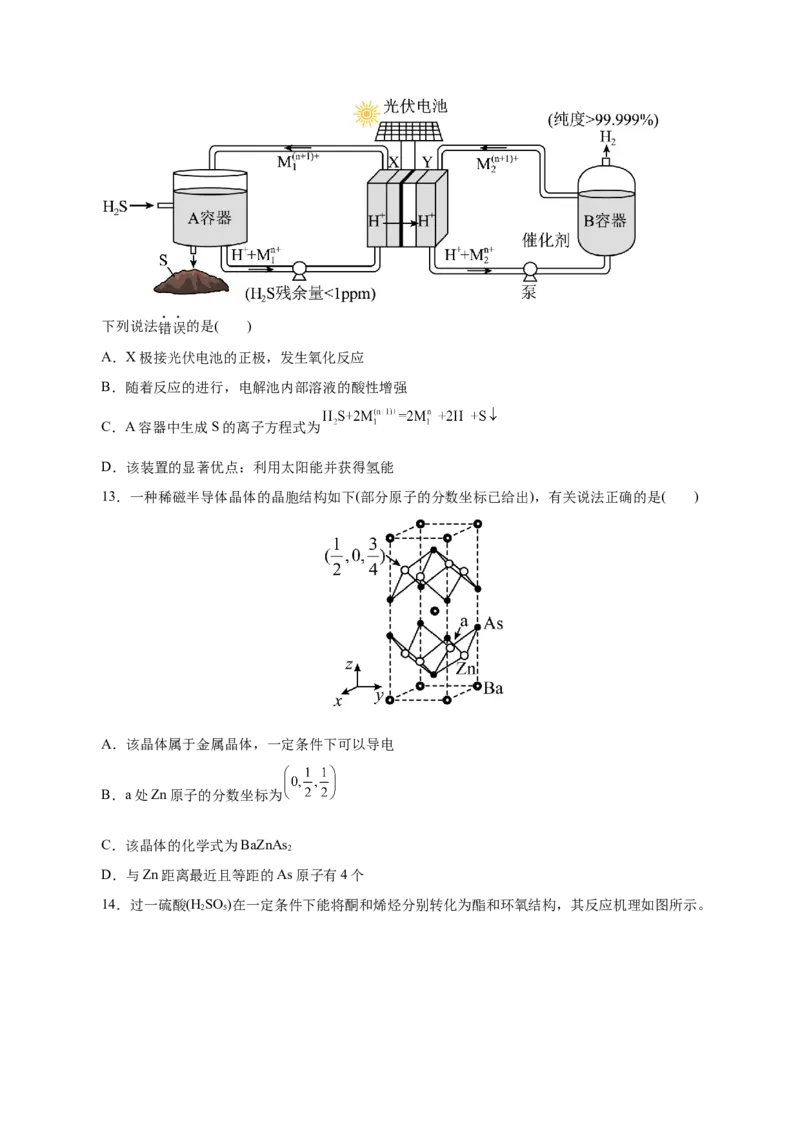
11.生成热是指由标准状况(101kPa,273K)下最稳定单质生成标准状况下单位物质的量的化合物的热
效应或焓变(ΔH)。最稳定的单质的标准生成热规定为零。几种含锡物质的生成热如图所示。下列叙述错误
的是( )
A.其他条件相同,最稳定的是SnO(s)
2
B.SnCl(s)+Cl(g)=SnCl(g) ΔH=-146.4kJ·mol−1
2 2 4
C.SnO(s)+ Sn(s)=2SnO(s) ΔH<0
2
D.最稳定的 在氧气中燃烧生成30.2gSnO(s)时放出的热量为116.14 kJ
2
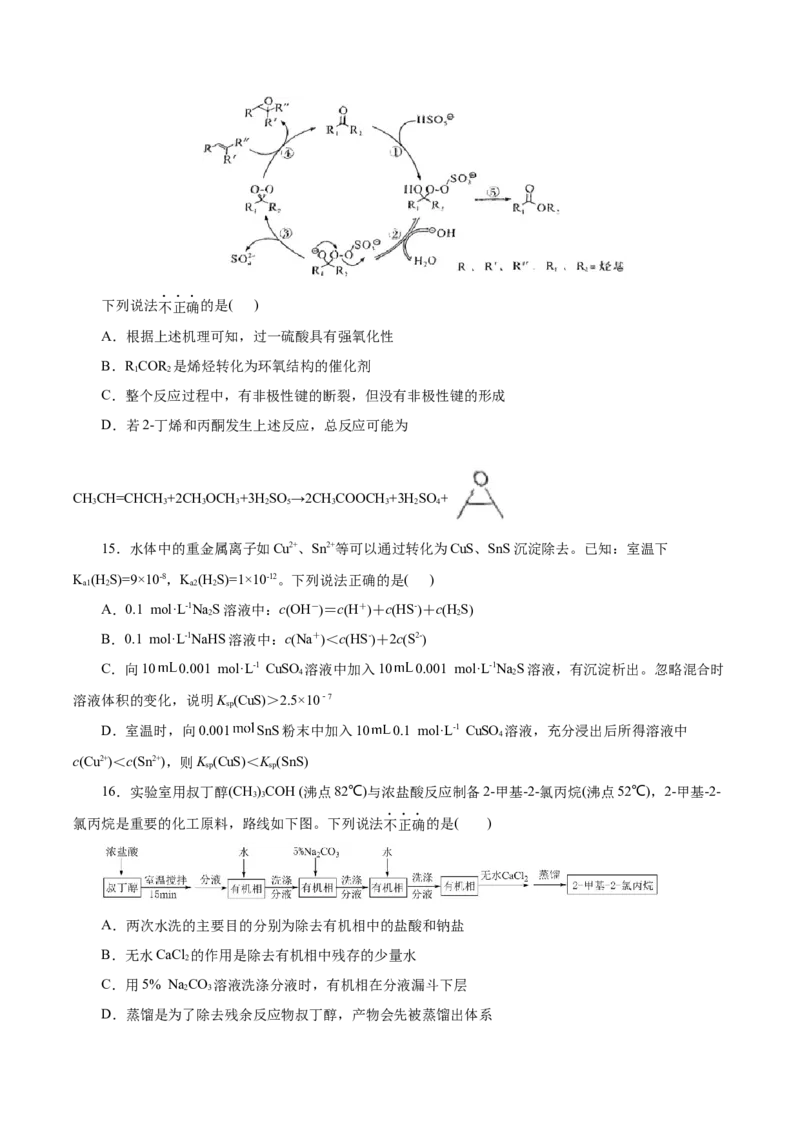
12.近日,大连化学物理研究所催化基础国家重点实验室开发出HS脱除光电催化工艺,其工作原理
2
如图所示(两个泵的工作效率相同)。下列说法错误的是( )
A.X极接光伏电池的正极,发生氧化反应
B.随着反应的进行,电解池内部溶液的酸性增强
C.A容器中生成S的离子方程式为
D.该装置的显著优点:利用太阳能并获得氢能
13.一种稀磁半导体晶体的晶胞结构如下(部分原子的分数坐标已给出),有关说法正确的是( )
A.该晶体属于金属晶体,一定条件下可以导电
B.a处Zn原子的分数坐标为
C.该晶体的化学式为BaZnAs
2
D.与Zn距离最近且等距的As原子有4个
14.过一硫酸(H SO )在一定条件下能将酮和烯烃分别转化为酯和环氧结构,其反应机理如图所示。
2 5下列说法不正确的是( )
A.根据上述机理可知,过一硫酸具有强氧化性
B.R COR 是烯烃转化为环氧结构的催化剂
1 2
C.整个反应过程中,有非极性键的断裂,但没有非极性键的形成
D.若2-丁烯和丙酮发生上述反应,总反应可能为
CHCH=CHCH +2CH OCH +3H SO →2CHCOOCH +3H SO +
3 3 3 3 2 5 3 3 2 4
15.水体中的重金属离子如Cu2+、Sn2+等可以通过转化为CuS、SnS沉淀除去。已知:室温下
K (H S)=9×10-8,K (H S)=1×10-12。下列说法正确的是( )
a1 2 a2 2
A.0.1 mol·L-1NaS溶液中:cOH-=cH++cHS-+cHS
2 2
B.0.1 mol·L-1NaHS溶液中:cNa+<cHS-+2cS2-
C.向10 0.001 mol·L-1 CuSO 溶液中加入10 0.001 mol·L-1NaS溶液,有沉淀析出。忽略混合时
4 2
溶液体积的变化,说明K (CuS)>2.5×10-7
sp
D.室温时,向0.001 SnS粉末中加入10 0.1 mol·L-1 CuSO 溶液,充分浸出后所得溶液中
4
c(Cu2+)<c(Sn2+),则K (CuS)<K (SnS)
sp sp
16.实验室用叔丁醇(CH)COH (沸点82℃)与浓盐酸反应制备2-甲基-2-氯丙烷(沸点52℃),2-甲基-2-
3 3
氯丙烷是重要的化工原料,路线如下图。下列说法不正确的是( )
A.两次水洗的主要目的分别为除去有机相中的盐酸和钠盐
B.无水CaCl 的作用是除去有机相中残存的少量水
2
C.用5% NaCO 溶液洗涤分液时,有机相在分液漏斗下层
2 3
D.蒸馏是为了除去残余反应物叔丁醇,产物会先被蒸馏出体系二、非选择题(本大题共4小题,共52分)
17.(16分)锂是相对质量最小的金属,锂及其化合物在有机合成、电池等领域应用广泛。回答下列问
题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为 、 (填标号)
A. B.
C. D.
(2)LiAlH 是有机合成中常用的还原剂,LiAlH 中的阴离子空间构型是 ,中心原子的杂化
4 4
形式为 ,LiAlH 中存在 (填标号)
4
A.离子键 B.σ键 C.π键 D.氢键
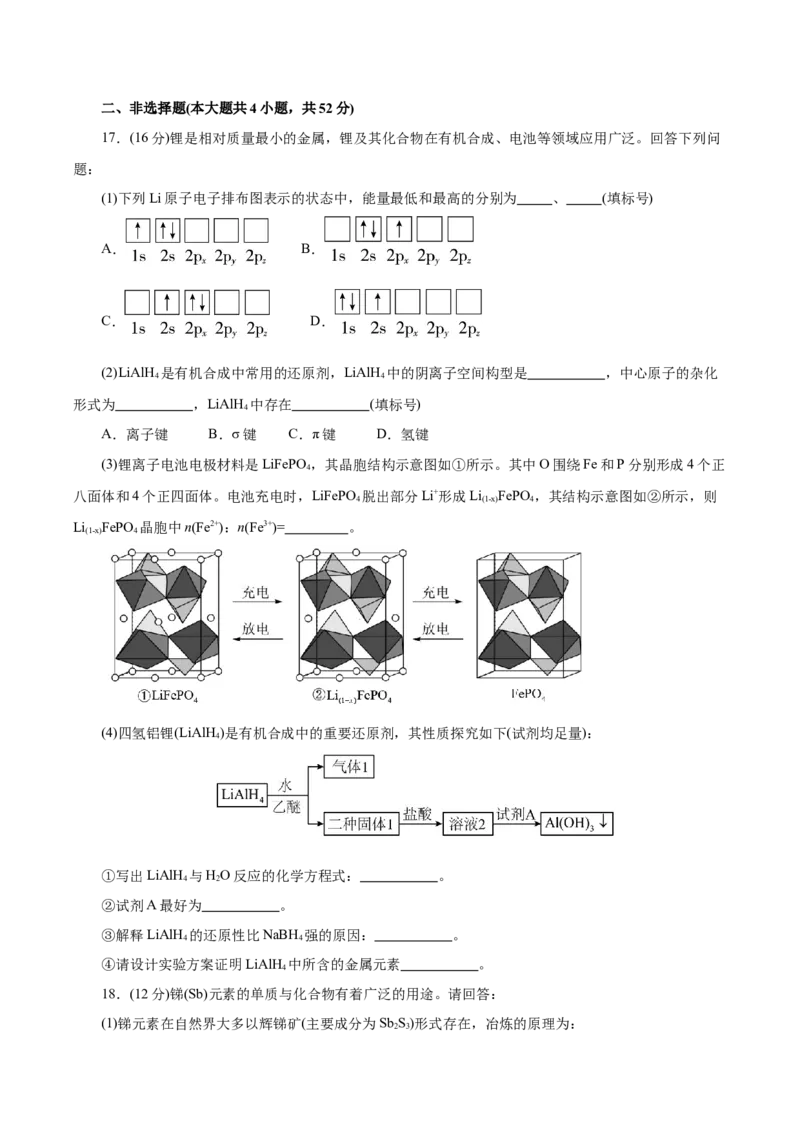
(3)锂离子电池电极材料是LiFePO ,其晶胞结构示意图如①所示。其中O围绕Fe和P分别形成4个正
4
八面体和4个正四面体。电池充电时,LiFePO 脱出部分Li+形成Li FePO ,其结构示意图如②所示,则
4 (1-x) 4
Li FePO 晶胞中n(Fe2+):n(Fe3+)= 。
(1-x) 4
(4)四氢铝锂(LiAlH )是有机合成中的重要还原剂,其性质探究如下(试剂均足量):
4
①写出LiAlH 与HO反应的化学方程式: 。
4 2
②试剂A最好为 。
③解释LiAlH 的还原性比NaBH 强的原因: 。
4 4
④请设计实验方案证明LiAlH 中所含的金属元素 。
4
18.(12分)锑(Sb)元素的单质与化合物有着广泛的用途。请回答:
(1)锑元素在自然界大多以辉锑矿(主要成分为Sb S)形式存在,冶炼的原理为:
2 3反应:Sb S(s)+3ZnO(s)+3C(s)=2Sb(s)+3ZnS(s)+3CO(g) ∆H
2 3
已知该反应在400℃以上才能自发进行,∆H 0(填“<”“>”或“=”)。
(2)Sb3+的水解方程式为2SbCl+3H O Sb O+6HCl,下列叙述正确的是 。
3 2 2 3
A.配制氯化锑溶液时先用浓盐酸溶解溶质
B.在较高温度下配制氯化锑溶液
C.氯化锑溶液中加入少量氨水制备氧化锑
D.配制成较浓的氯化锑溶液有利于得到氧化锑固体
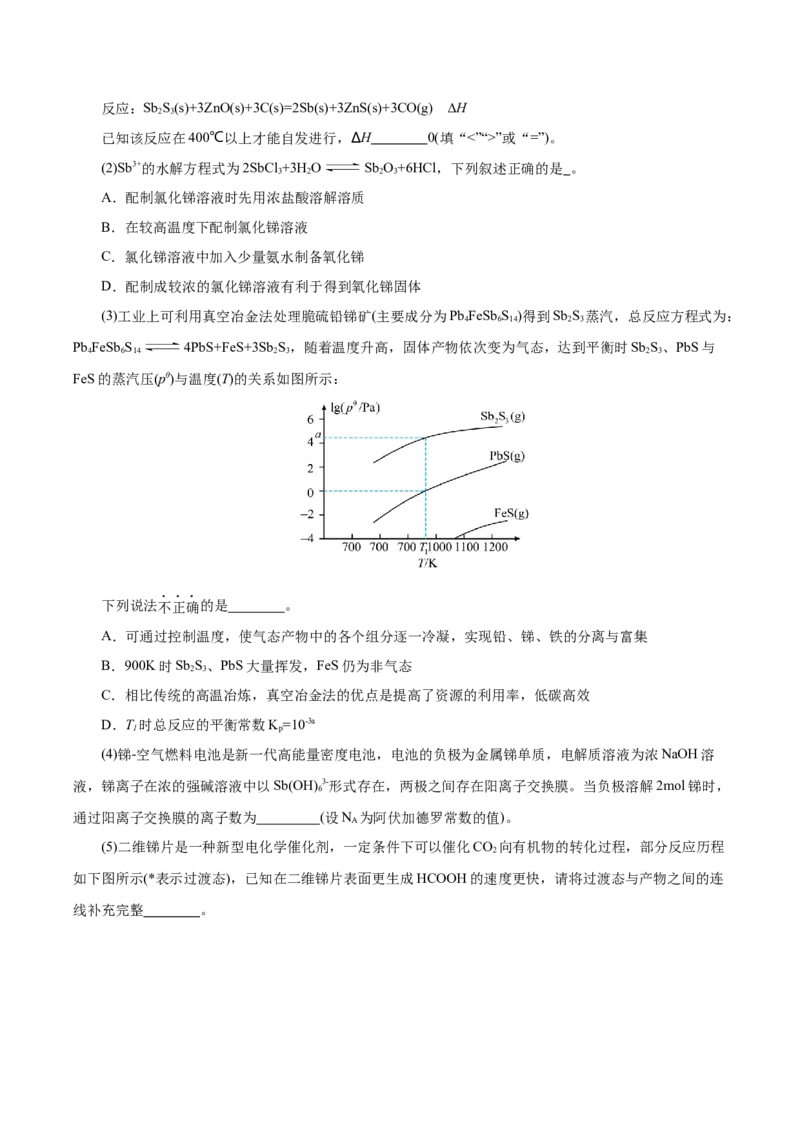
(3)工业上可利用真空冶金法处理脆硫铅锑矿(主要成分为Pb FeSb S )得到Sb S 蒸汽,总反应方程式为:
4 6 14 2 3
Pb FeSb S 4PbS+FeS+3Sb S,随着温度升高,固体产物依次变为气态,达到平衡时Sb S、PbS与
4 6 14 2 3 2 3
FeS的蒸汽压(pθ)与温度(T)的关系如图所示:
下列说法不正确的是 。
A.可通过控制温度,使气态产物中的各个组分逐一冷凝,实现铅、锑、铁的分离与富集
B.900K时Sb S、PbS大量挥发,FeS仍为非气态
2 3
C.相比传统的高温冶炼,真空冶金法的优点是提高了资源的利用率,低碳高效
D.T 时总反应的平衡常数K=10-3a
1 p
(4)锑-空气燃料电池是新一代高能量密度电池,电池的负极为金属锑单质,电解质溶液为浓NaOH溶
液,锑离子在浓的强碱溶液中以Sb(OH)3-形式存在,两极之间存在阳离子交换膜。当负极溶解2mol锑时,
6
通过阳离子交换膜的离子数为 (设N 为阿伏加德罗常数的值)。
A
(5)二维锑片是一种新型电化学催化剂,一定条件下可以催化CO 向有机物的转化过程,部分反应历程
2
如下图所示(*表示过渡态),已知在二维锑片表面更生成HCOOH的速度更快,请将过渡态与产物之间的连
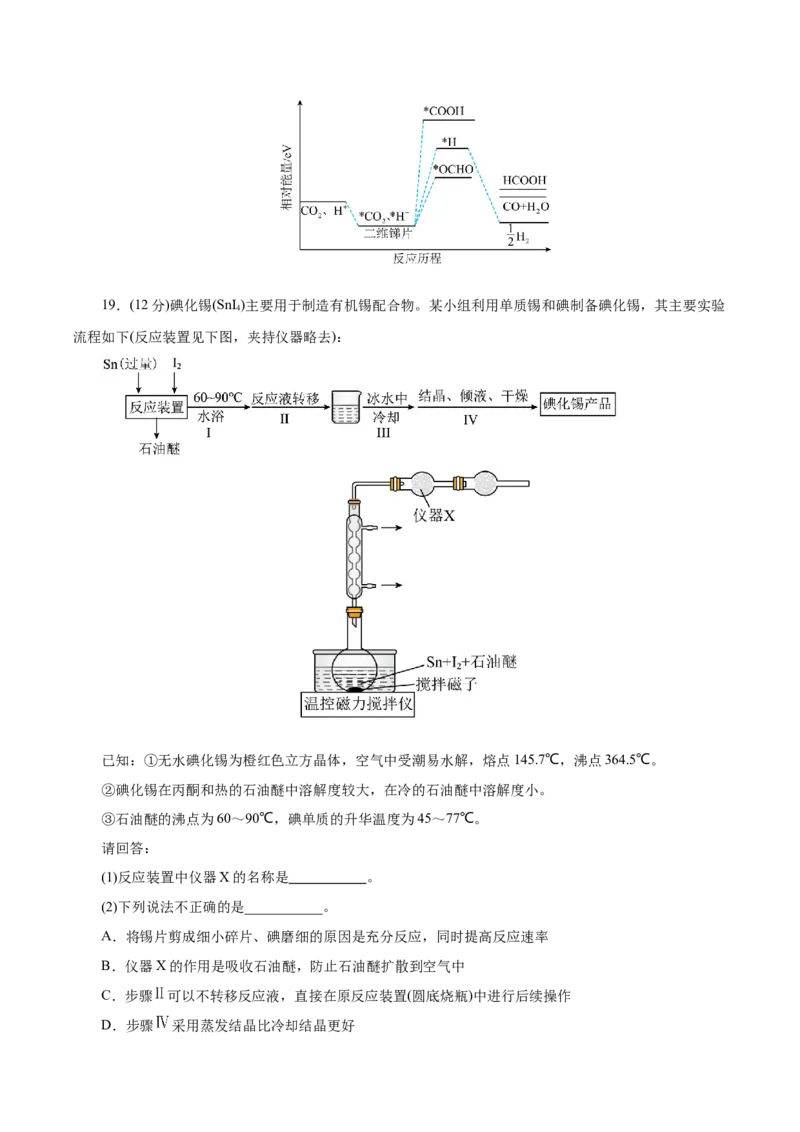
线补充完整 。19.(12分)碘化锡(SnI )主要用于制造有机锡配合物。某小组利用单质锡和碘制备碘化锡,其主要实验
4
流程如下(反应装置见下图,夹持仪器略去):
已知:①无水碘化锡为橙红色立方晶体,空气中受潮易水解,熔点145.7℃,沸点364.5℃。
②碘化锡在丙酮和热的石油醚中溶解度较大,在冷的石油醚中溶解度小。
③石油醚的沸点为60~90℃,碘单质的升华温度为45~77℃。
请回答:
(1)反应装置中仪器X的名称是 。
(2)下列说法不正确的是___________。
A.将锡片剪成细小碎片、碘磨细的原因是充分反应,同时提高反应速率
B.仪器X的作用是吸收石油醚,防止石油醚扩散到空气中
C.步骤 可以不转移反应液,直接在原反应装置(圆底烧瓶)中进行后续操作
D.步骤 采用蒸发结晶比冷却结晶更好(3)反应装置中,为使紫色碘蒸气上升不高于冷凝管的中间部位,可采取的措施是 ;判断
“反应装置”中的反应已完全的实验现象是 。
(4)步骤 ,圆底烧瓶中还附着四碘化锡晶体,处理的方法是 。
(5)产品中的杂质可以进一步采用重结晶法提纯。请从下列选项中选择最佳选项并进行排序。
取碘化锡样品放入烧杯中→___________→___________→___________
a.加入适量的热水
b.加入适量的热的石油醚
c.用冷水浴冷却结晶
d.趁热过滤
e.加入适量的冷的石油醚
(6)该小组对制备的碘化锡产品进行性质和组成上的研究。
①取适量的产品溶解在2mL丙酮中配成溶液,再加入1ml蒸馏水,产生白色无定型沉淀,写出反应的
化学方程式 。
②本实验可以通过测定某些物理量来确定碘化锡的化学式,需测定的物理量有 。
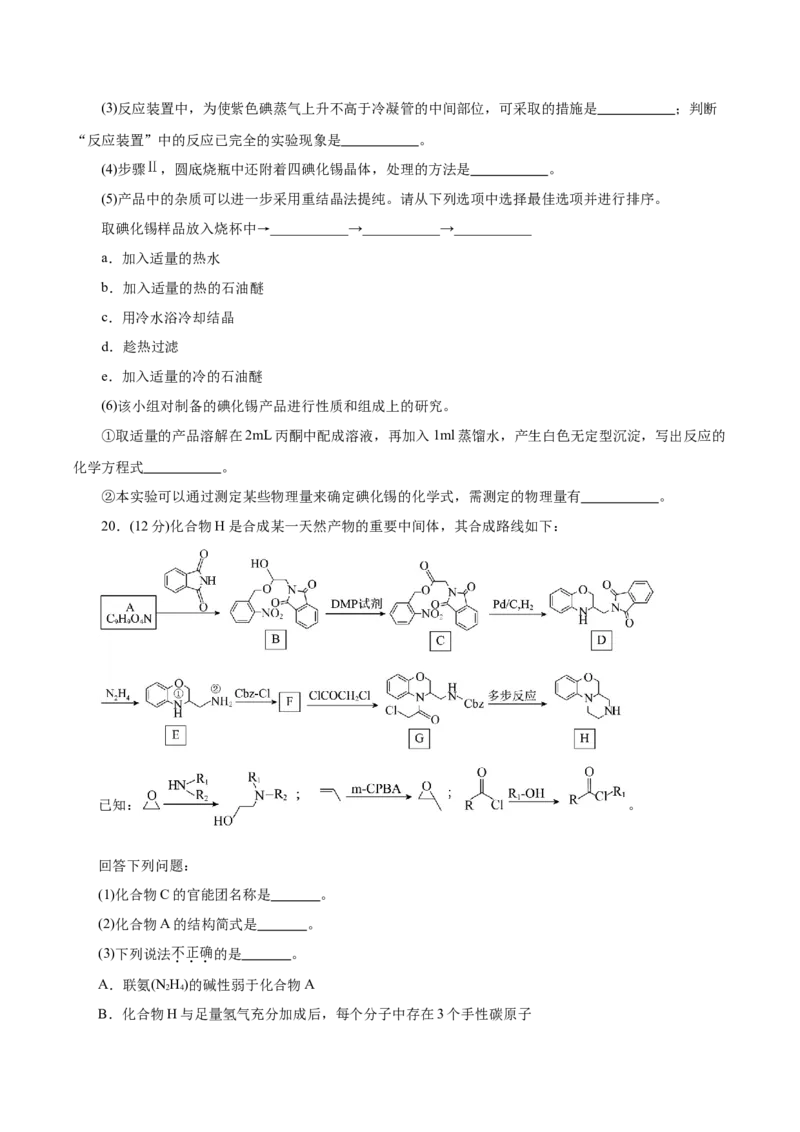
20.(12分)化合物H是合成某一天然产物的重要中间体,其合成路线如下:
已知: 。
回答下列问题:
(1)化合物C的官能团名称是 。
(2)化合物A的结构简式是 。
(3)下列说法不正确的是 。
A.联氨(N H)的碱性弱于化合物A
2 4
B.化合物H与足量氢气充分加成后,每个分子中存在3个手性碳原子C.化合物B→C的转化过程中, 试剂作氧化剂
D.化合物E中,氨基的反应活性:
E.化合物E→F的转化过程中, 试剂起到保护氨基的作用
(4)化合物D→E的转化过程中两种产物均含两个六元环,写出转化的化学方程式 。
(5)有机物X( )是一种医药中间体,设计以苯乙烯( )和光气(COCl)为原料
2
合成有机物X的路线(用流程图表示,无机试剂任选) 。
(6)写出4种同时符合下列条件的化合物E的同分异构体的结构简式 。
① 谱和R谱检测表明:分子中共有5种氢原子;
②除了苯环外无其他环,环上含三个取代基团,且可以发生银镜反应