文档内容
高三化学试卷参考答案
!#$!!解析"本题主要考查化学与科技知识#侧重考查学生对基础知识的认知能力$水体富营养化与含磷废水
的排放有关!%项错误"青铜是铜的合金!硬度比纯铜大!&项错误"’()纤维属于合成纤维!*项错误#
+#*!!解析"本题主要考查化学用语的基础知识#侧重考查学生对基础知识的认知能力$氯化铵分子中,原
子不是-电子稳定结构!*项错误#
.#%!!解析"本题主要考查传统文化中的化学知识#侧重考查学生对基础知识的认知能力$$紫烟%是形容瀑
布在红日的照射下!幻化成一片紫色的云霞!%项错误#
"#$!!解析"本题主要考查氨气的制备和收集实验#侧重考查学生对基础知识的应用能力$实验室用生石灰和
浓氨水反应制取氨气是固液不加热型!%项不符合题意"’/ 为酸性氧化物!不能干燥氨气!&项不符合题
+ 0
意"验满应用湿润的红色石蕊试纸!*项不符合题意#
0#*!!解析"本题主要考查有机物的性质#侧重考查学生对基础知识的理解能力$!123该有机物最多能与
+!123, 发生加成反应!*项错误#
+
4#&!!解析"本题主要考查铜及其化合物的性质#侧重考查学生对基础知识的理解能力$5为正二价的铜盐!
加入浓氢氧化钠!不会形成$6&/,’胶体!&项错误#
+
7#&!!解析"本题主要考查对离子方程式的书写正误的判断#侧重考查学生分析和解决问题的能力$
89&/,’
+
难溶于水!%项错误"加入过量铁粉!产物为亚铁离子!$项错误"!&$3
+
’:;#+123!;#!123$3
+
先
氧化;#+123<=+>!然后;#!123$3氧化;#+123&?@!正确的离子方程式为+<=+>>+&?@>+$3"""+<=.>
+ +
>&?>"$3@!*项错误#
+
-#%!!解析"本题主要考查阿伏加德罗常数的知识#侧重考查学生分析和解决问题的能力$磷酸溶液中还存
在磷酸分子!&项错误";#!123由$, 和$,/,组成的混合气体在氧气中完全燃烧时!消耗的/ 分子
+ " + 0 +
数为;#."
%
!$项错误"阳极的电极反应式为+$3@@+=@"""$3 +#!产生;#!123$3
+
时!转移;#+123电子!*
项错误#
A#$!!解析"本题主要考查含氮物质的转化#侧重考查学生分析和解决问题的能力$由图示可知!过程!为
酶!
B/@ 在酶!的作用下转化为B/和,/!反应的离子方程式为B/@>+,>>=@"""B/>,/!生成
+ + + +
!123B/!C过程转移!123=@"过程"为B/和B,
"
> 在酶+的作用下发生氧化还原反应生成,
+
/和
酶+
B, !反应的离子方程式为+,>>.=@>B/>B,> """,/>B, !消耗!123B/!D过程转移
+ " " + + "
.123=@"过程#为B
+
,
"
转化为B
+
和",>("=@!反应的离子方程式为B
+
,
"
"""B
+
>",>>"=@!则过程
!$#的总反应为B/
+
@>B,
"
> """B +#>+,
+
/#因产物是B
+
!不是氮的固定!%项错误"生物酶不能改变
反应的焓变!&项错误"整个过程中没有离子键的形成!*项错误#
!;#%!!解析"本题主要考查元素周期律的相关知识#侧重考查学生分析和解决问题的能力$由已知可以推
出)8为,!E为$!F为B!G为H#,B/ 和,H/ 均为弱酸!&项错误"B, 分子间能形成氢键!沸点较
+ + . .
高!但碳的氢化物的种类有很多!$项错误"该分子中还含有B*B非极性键!*项错误#
!!#$!!解析"本题主要考查实验设计与探究#侧重考查学生对实验装置的应用和分析能力$高锰酸钾溶液会
与盐酸发生氧化还原反应而褪色!%项不符合题意"实验%说明溶液中不含<=.>!但不能说明固体中没有
三价铁!也可能溶于盐酸时!过量的铁单质把三价铁还原了!&项不符合题意"实验&说明溶液中含有<=+>!
实验%说明溶液中不含<=.>!而铁与水蒸气能生成三价铁!所以可以推知反应后的固体中有铁粉剩余!$项
!高三化学"参考答案!第!!!!!页#共"页$% "!"#!$%&"
书书书符合题意"灰绿色的沉淀是<=&/,’转化为<=&/,’的中间产物!*项不符合题意#
+ .
!+#&!!解析"本题主要考查碳酸锂的制备流程#侧重考查学生分析和解决化学问题的能力$$萃取%和$反萃
取%应在分液漏斗中进行!&项错误#
!.#*!!解析"本题主要考查电解池的相关知识#侧重考查学生分析和解决问题的能力$&电极的电极反应式
为+,
+
/@"=@"""/ +#>",>!质子交换膜中有""
%
个,>通过!外电路中有"123=@转移!产生!123
/!标准状况下体积为++#"I!*项错误#
+
!"#*!!解析"本题主要考查酸的稀释#侧重考查学生对图像的分析能力$,J
!
溶液稀释至体积为原本的!;;
倍!K,由.变为0!,J
!
是强酸"而,J
+
溶液稀释至体积为原本的!;;倍!K,增大值小于+!,J
+
是弱酸#
!L!;@.
起始K,:.!#&,>’:!L!;@.123+I@!#,J
+
$%,>>J
+
!!:
;#!@!;@.
L!;;M&!M!*项错误#
!0#&!’恒压滴液漏斗&!分’"D&!分’
&+’溶液上方不再有明显油珠&或其他合理答案!+分’"受热均匀!容易控制温度&!分’
&.’8N/&!分’".&+分’
+
&"’不能&!分’"醋酸是弱酸!无法将溶液调至强酸性&或其他合理答案!+分’
&0’A7#4M&+分’"偏高&!分’
!解析"本题主要考查实验设计与探究#考查学生对实验装置的应用和分析能力$
&!’根据仪器的构造知!仪器E为恒压滴液漏斗"冷凝管的进水口为C#
&+’由于甲苯不溶于水!而苯甲酸在水中能溶解!因此当三颈烧瓶中溶液不分层!说明甲苯已完全反应"油浴
加热的优点是受热均匀!容易控制温度#
&.’由题给信息可知!反应后溶液呈碱性!且有二氧化锰生成!所以发生的反应为甲苯和高锰酸钾溶液反应
生成苯甲酸钾(二氧化锰(氢氧化钾和水#
&0’根据盐酸与氢氧化钠反应时!参加反应的溶质的物质的量之比为!O!可知!与苯甲酸反应的!&BC/,’
:-L!;@"123!所以苯甲酸的纯度为A7#4M"滴定过程中!滴定管起始有气泡!滴定终点时气泡消失!读数
得出消耗盐酸的体积偏大!则与苯甲酸反应的BC/,溶液体积偏小!所以测得样品中苯甲酸的纯度偏高#
!4#&!’<=&/,’&+分’
.
&+’,/&或/ 或/!+分’
+ + + .
&.’’&!分’"细菌中蛋白质变性!活性降低&或水解程度增大!+分’
&"’$6<=H>"<=.>"""0<=+>>$6+>>+H&+分’
+
&0’碱&!分’";#+&+分’
&4’"#;L!;@7&+分’
!解析"本题主要考查以黄铜矿粉制备$6H= 的工艺流程#考查学生对元素化合物的理解能力和综合运用
. +
能力$
&0’根据电荷守恒)+#&H=H/+@’>#&,H=H/@’>#&/,@’:#&BC>’>#&,>’!得+#&H=H/+@’>#&,H=H/@’
. . . .
>#&/,@’@#&,>’:#&BC>’:;#+123+I@!#
#,-$6&B,’.+>/+#+&/,@’
&4’$:
#"&B
.
,
"
+,/’
:$稳L$
PK
:"#;L!;@7#
. +
!7#&!’’@.A7.#A&+分’
&&*&+分’
&+’’温度&!分’"正反应是吸热反应!平衡后升高温度!平衡向正方向移动!$/的体积分数增大&或若%表
!高三化学"参考答案!第!!!!+页#共"页$% "!"#!$%&"示压强!随着压强的增大!$/的体积分数将减小!+分’
&’&+分’
%;#04+0&+分’
&.’$CQ+&+分’"$CQ+直线斜率变化值较小&或直线$CQ+斜率绝对值较小或直线$CQ+较$C!平缓’!活化能
较小!催化效能较高&+分’
!解析"本题主要考查化学反应原理#考查学生对化学反应原理的理解能力和综合运用知识的能力$
&!’’根据盖斯定律!’>&得目标反应#
&平衡常数只与温度有关!温度不变!平衡常数不变!&项错误"改变体积时!平衡发生了移动!固体质量改
变!*项错误#
.&
&+’%8点$/体积分数为0;M#起始B
+
浓度为!123+I@!!设变化浓度为&!有
!>+&
L!;;M:0;M!&
:;#+0123+I@!#平衡时!#&B’:;#70123+I@!!#&$/’:;#70123+I@!#
+
! !
&.’温度从’ 升高至’ 时)(3N)@(3N):@*& @ ’!两边取绝对值!得出结论是升高相同的温度!
! + ! + C’ ’
! +
速率常数变化值越大!活化能越大#$CQ!作用下直线斜率较大!速率常数变化值较大!活化能较大!即$CQ+
催化效率较高#
!-#&!’PK+(PK.&+分’"+O!&!分’
&+’B’/’$&!分’"B的+K轨道为半充满状态!/的+K轨道上有"个电子!失去!个电子所需能量更小!故
第一电离能B’/!又因为同周期!从左往右!原子半径减小!第一电离能增大!故第一电离能B’/’$&+分’
&.’’&!分’"两分子的中心原子均采取PK.杂化!而B,
.
中B原子含一对孤电子对!,
+
/中/原子含两个
孤电子对!孤电子对之间的斥力大于孤电子对与成键电子对之间的斥力!故键角B, .’,
+
/&+分’
&"’(&!分’
&0’’&;!!!!’&!分’
+LA4L!;.;
&槡++&+分’" &+分’
"+.
%
!解析"本题主要考查物质结构与性质#考查学生对物质结构的理解能力和综合运用知识的能力$
&!’有机物中双键碳为PK+杂化!单键碳为PK.杂化#(()键的存在规律)单键均为!个2键!双键中含!个
(键和!个)键!注意$和,之间的(键#
&+’同一周期元素中!元素的第一电离能随着原子序数的增大而呈增大趋势!但氮原子的半充满状态比较稳
定!故第一电离能B’/’$#
&.’水分子和氨气分子都是四面体结构!在水分子中占据四面体四个角的是+对电子和+个氢原子!在氨气
分子中占据四面体四个角的是!对电子和.个氢原子!由于电子对之间的斥力大于电子对与氢原子之间的
斥力!所以水分子键角小于氨气键角#
&"’烷基为推电子基!氯原子为吸电子基!吸电子基使羧基的氢氧键极性增强!电离程度增大!酸性增强!推
电子基反之#
!A#&!’+@甲基丙烯&!分’"羟基(羧基&+分’
&+’&?&3’&或液溴’!<=&?&或<=’&+分’
+ .
&.’酯化反应&或取代反应!!分’
!高三化学"参考答案!第!!!!.页#共"页$% "!"#!$%&"** **
&"))’ **++>$,
.
$3- % - 3 - $3 , . ))**++ >,$3&+分’
&?
**++
&0’!+&+分’" ))**++ ++ &+分’
,/
/""/,
/, &? 89&?
++ ++ ++ ++
&4’ -- , - &? , -- 8 , 9 -- $/ , + &.分’
催化剂 乙醚
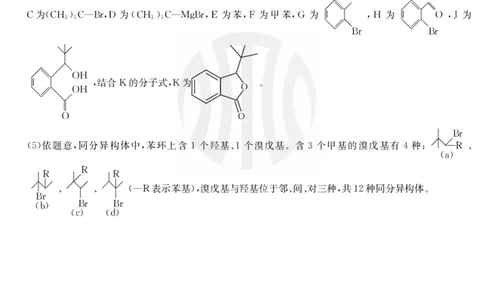
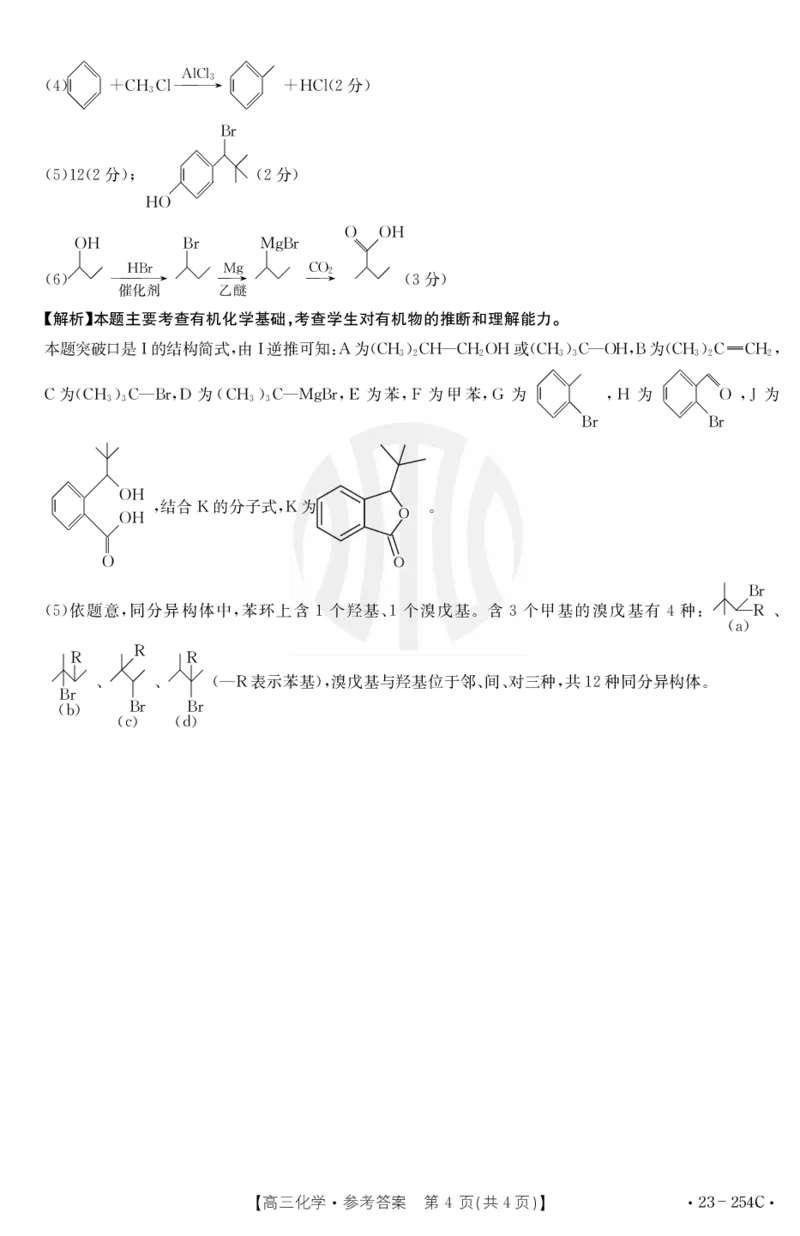
!解析"本题主要考查有机化学基础#考查学生对有机物的推断和理解能力$
本题突破口是R的结构简式!由R逆推可知)%为&$,’$,*$,/,或&$,’$*/,!&为&$,’$""$,!
.+ + .. .+ +
** **""
$为&$,
.
’
.
$*&?!*为&$,
.
’
.
$*89&?!(为苯!<为甲苯!S为))**++ !, 为))**++ / !T为
&? &?
++
++
**
/,
))**++ !结合U的分子式!U为 #
/,
..
/
++ &?
&0’依题意!同分异构体中!苯环上含!个羟基(!个溴戊基#含.个甲基的溴戊基有"种)++--J (
&C’
J
++J ++ ++J
++++
( (
++
&*J表示苯基’!溴戊基与羟基位于邻(间(对三种!共!+种同分异构体#
&? ++ ++
&D’ &? &?
&5’ &V’
!高三化学"参考答案!第!!!!"页#共"页$% "!"#!$%&"