文档内容
河北省“五个一”名校联盟 2023 届高三年级摸底考试
化学试卷
命题单位:石家庄市第一中学
(满分:100分,测试时间:75分钟)
可能用到的相对原子质量:H 1 O 16 S 32 Cu 64
第 I 卷(选择题,共 43 分)
一、选择题:本题共9小题,每小题3分,共27分,在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.化学与生产、生活密切相关,下列叙述错误的是
A.绿色化学要求从源头上消除或减少生产活动对环境的污染
B.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
C.可溶性的铝盐和铁盐可用作净水剂
D.从海水中提取物质都必须通过化学反应才能实现
2.下列叙述正确的是
A.中子数为10的氧原子:10O B. Cl-的结构示意图:
8
C.HClO的结构式为:H-O-Cl D.NH 的电子式:
3
3.下列说法不正确的是
A.钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
B.油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应
C.除去干燥CO 中混有的少量SO ,可将混合气体依次通过盛有酸性KMnO 溶液、
2 2 4
浓硫酸的洗气瓶
D.“中和滴定”实验中,锥形瓶用蒸馏水洗涤后即可使用,滴定管用蒸馏水洗涤后,
需经润洗方可使用
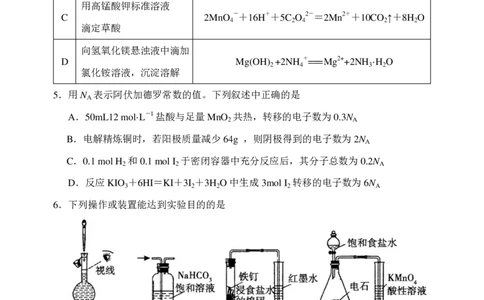
化学试卷 第1页 (共9页)4.下列离子方程式能用来解释相应实验操作或者现象的是
实验现象 离子方程式
向沸水中滴加饱和氯化铁
A Fe3++3H O== △ === Fe(OH) ↓+3H+
2 3
溶液,得到氢氧化铁胶体
向硫酸铜溶液中加入
B Cu2++2NH ·H O=Cu(OH) ↓+2NH +
3 2 2 4
过量氨水
用高锰酸钾标准溶液
C 2MnO -+16H++5C O 2-=2Mn2++10CO ↑+8H O
4 2 4 2 2
滴定草酸
向氢氧化镁悬浊液中滴加
D Mg(OH) +2NH +=== Mg2++2NH ·H O
2 4 3 2
氯化铵溶液,沉淀溶解
5.用N 表示阿伏加德罗常数的值。下列叙述中正确的是
A
A.50mL12 mol·L-1盐酸与足量MnO 共热,转移的电子数为0.3N
2 A
B.电解精炼铜时,若阳极质量减少64g ,则阴极得到的电子数为2N
A
C.0.1 mol H 和0.1 mol I 于密闭容器中充分反应后,其分子总数为0.2N
2 2 A
D.反应KIO +6HI=KI+3I +3H O中生成3mol I 转移的电子数为6N
3 2 2 2 A
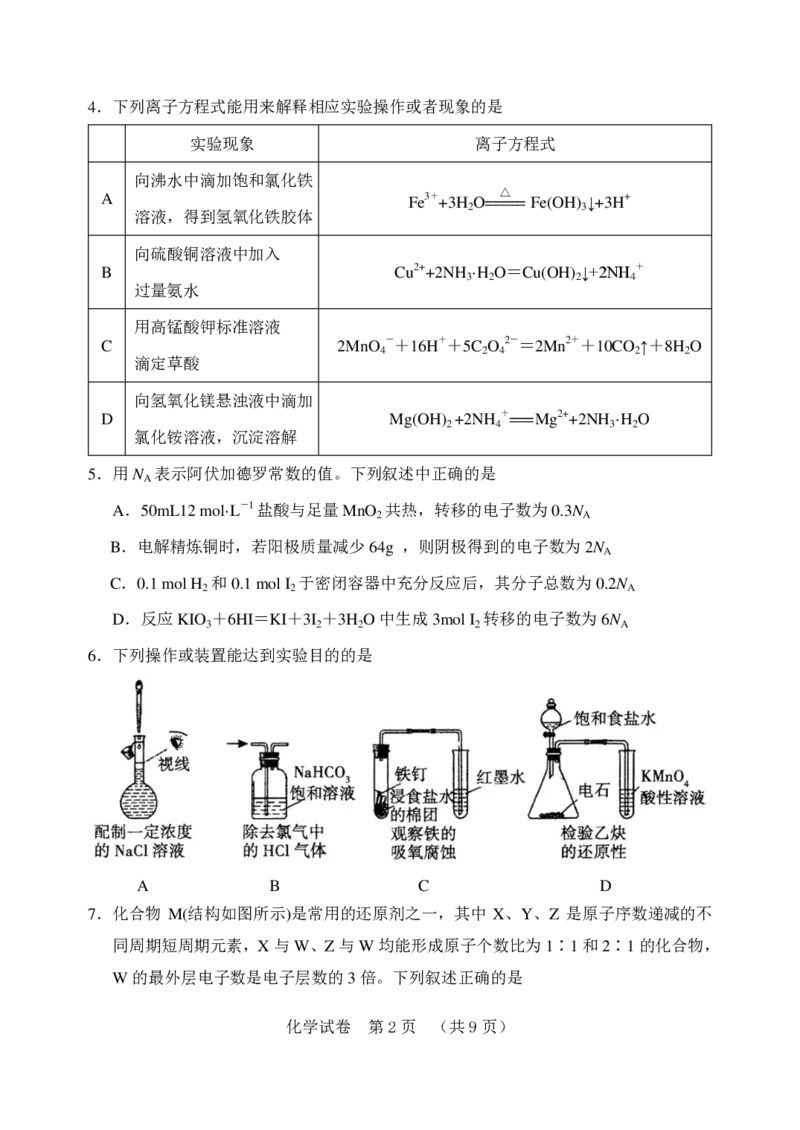
6.下列操作或装置能达到实验目的的是
A B C D
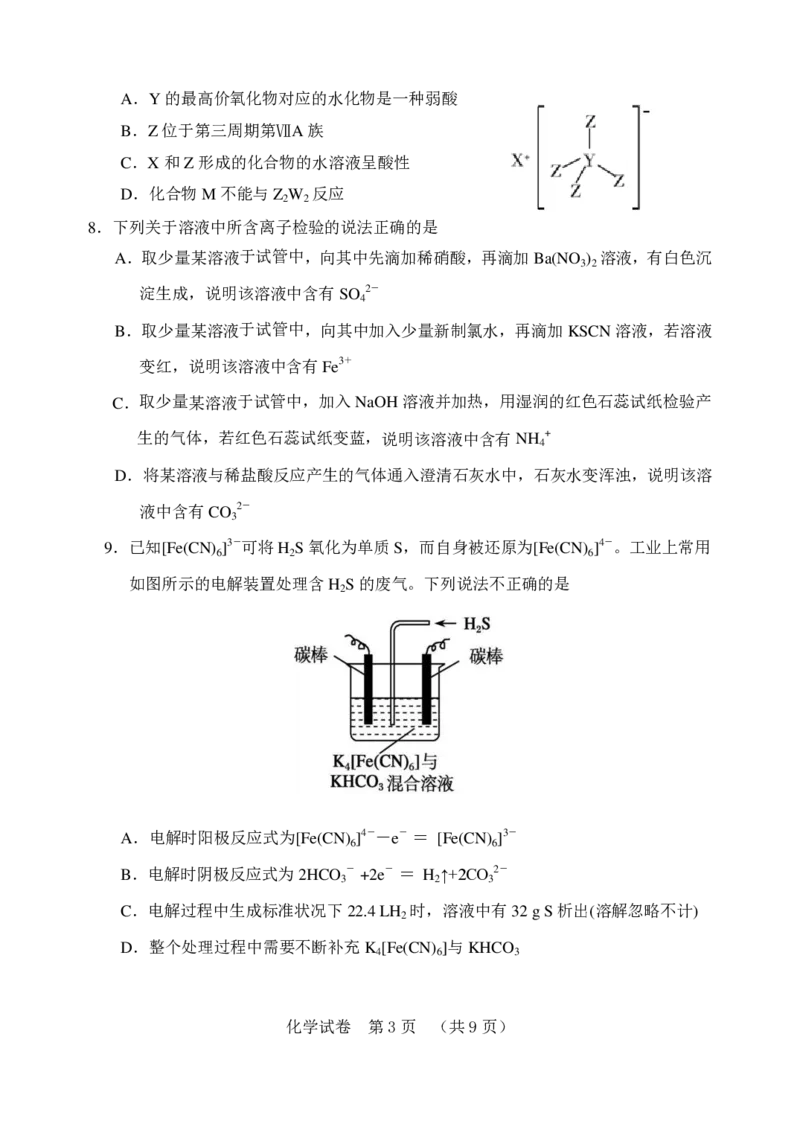
7.化合物 M(结构如图所示)是常用的还原剂之一,其中 X、Y、Z 是原子序数递减的不
同周期短周期元素,X与W、Z与W均能形成原子个数比为1∶1和2∶1的化合物,
W的最外层电子数是电子层数的3倍。下列叙述正确的是
化学试卷 第2页 (共9页)A.Y的最高价氧化物对应的水化物是一种弱酸
B.Z位于第三周期第ⅦA族
C.X和Z形成的化合物的水溶液呈酸性
D.化合物M不能与Z W 反应
2 2
8.下列关于溶液中所含离子检验的说法正确的是
A.取少量某溶液于试管中,向其中先滴加稀硝酸,再滴加Ba(NO ) 溶液,有白色沉
3 2
淀生成,说明该溶液中含有SO 2-
4
B.取少量某溶液于试管中,向其中加入少量新制氯水,再滴加KSCN溶液,若溶液
变红,说明该溶液中含有Fe3+
C.取少量某溶液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产
生的气体,若红色石蕊试纸变蓝,说明该溶液中含有NH +
4
D.将某溶液与稀盐酸反应产生的气体通入澄清石灰水中,石灰水变浑浊,说明该溶
液中含有CO 2-
3
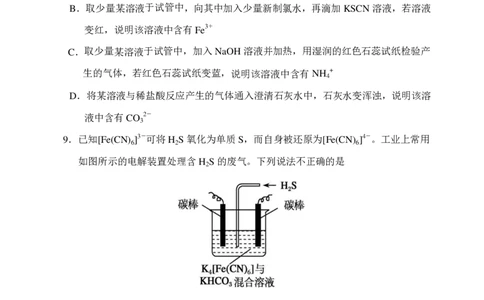
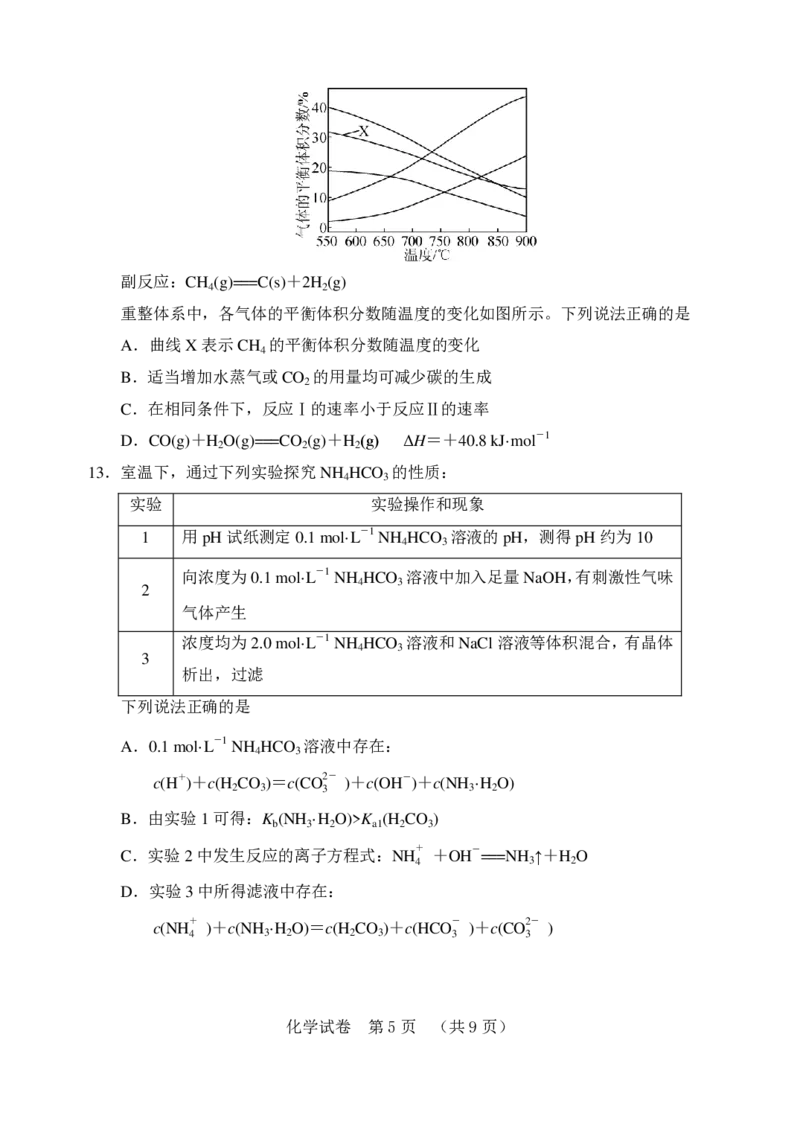
9.已知[Fe(CN) ]3-可将H S氧化为单质S,而自身被还原为[Fe(CN) ]4-。工业上常用
6 2 6
如图所示的电解装置处理含H S的废气。下列说法不正确的是
2
A.电解时阳极反应式为[Fe(CN) ]4--e- = [Fe(CN) ]3-
6 6
B.电解时阴极反应式为2HCO - +2e- = H ↑+2CO 2-
3 2 3
C.电解过程中生成标准状况下22.4 LH 时,溶液中有32 g S析出(溶解忽略不计)
2
D.整个处理过程中需要不断补充K [Fe(CN) ]与KHCO
4 6 3
化学试卷 第3页 (共9页)二、不定项选择题:本题共4小题,每小题4分,共16分,在每小题给出的四个选项中,
有一项或两项符合题目要求。若正确答案只包括一个选项,多选时,该小题得 0 分;若
正确答案包括两个选项,只选一个且正确的得 2分,选两个且都正确的得 4 分,但只要
选错一个,该小题得0分。
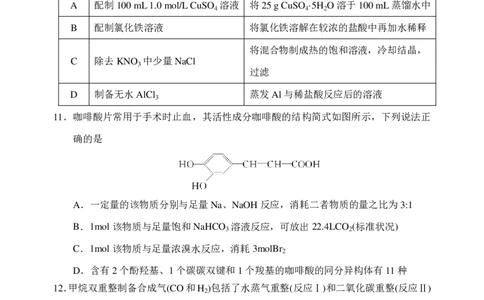
10.下列操作不能达到目的的是
选项 目的 操作
A 配制100 mL 1.0 mol/L CuSO 溶液 将25 g CuSO ·5H O溶于100 mL蒸馏水中
4 4 2
B 配制氯化铁溶液 将氯化铁溶解在较浓的盐酸中再加水稀释
将混合物制成热的饱和溶液,冷却结晶,
C 除去KNO 中少量NaCl
3
过滤
D 制备无水AlCl 蒸发Al与稀盐酸反应后的溶液
3
11.咖啡酸片常用于手术时止血,其活性成分咖啡酸的结构简式如图所示,下列说法正
确的是
A.一定量的该物质分别与足量Na、NaOH反应,消耗二者物质的量之比为3:1
B.1mol该物质与足量饱和NaHCO 溶液反应,可放出22.4LCO (标准状况)
3 2
C.1mol该物质与足量浓溴水反应,消耗3molBr
2
D.含有2个酚羟基、1个碳碳双键和1个羧基的咖啡酸的同分异构体有11种
12.甲烷双重整制备合成气(CO和H )包括了水蒸气重整(反应Ⅰ)和二氧化碳重整(反应Ⅱ)
2
两个反应。在p=3.2×106 Pa下,向密闭容器中按n(CH )∶n(H O)∶n(CO )=5∶4∶2
4 2 2
通入混合气,发生反应:(E 表示反应中基元反应的最大活化能)
a
反应Ⅰ: CH (g)+H O(g)===CO(g)+3H (g) ΔH =+206.2 kJ·mol-1
4 2 2 1
E =240.1 kJ·mol-1
a1
反应Ⅱ: CH (g)+CO (g)===2CO(g)+2H (g) ΔH =+247.0 kJ·mol-1
4 2 2 2
E =577.6 kJ·mol-1
a2
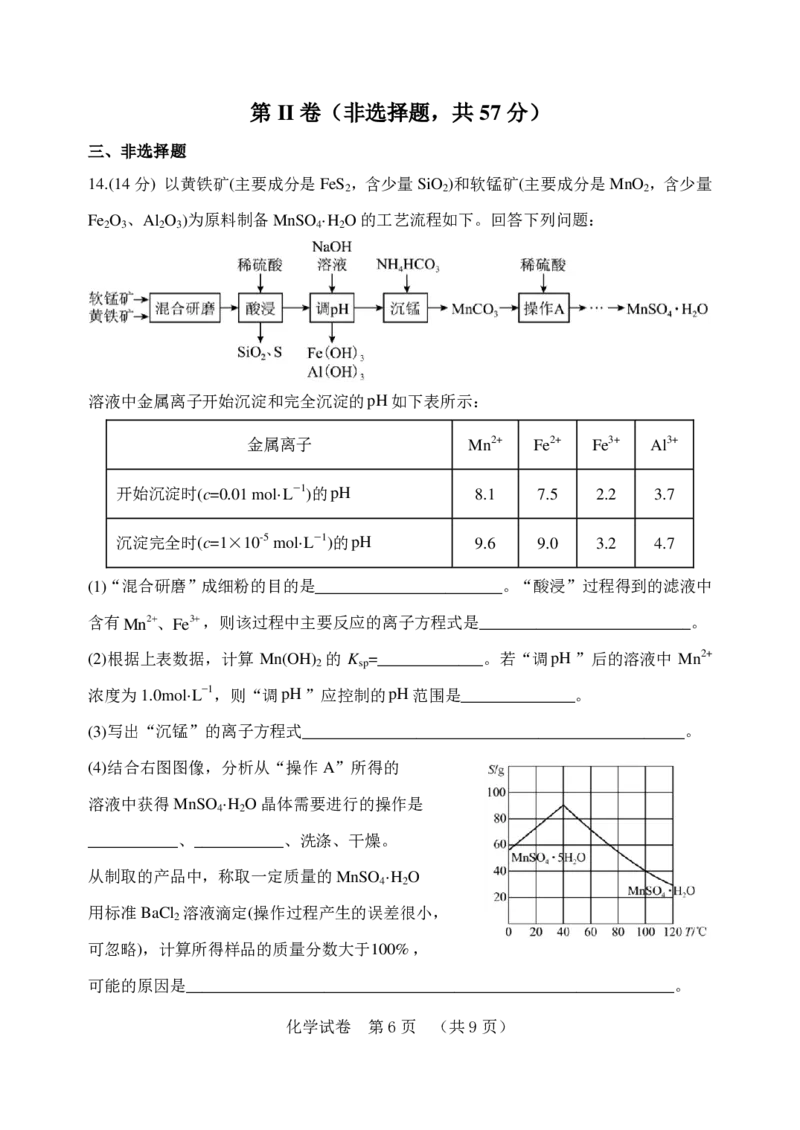
化学试卷 第4页 (共9页)副反应:CH (g)===C(s)+2H (g)
4 2
重整体系中,各气体的平衡体积分数随温度的变化如图所示。下列说法正确的是
A.曲线X表示CH 的平衡体积分数随温度的变化
4
B.适当增加水蒸气或CO 的用量均可减少碳的生成
2
C.在相同条件下,反应Ⅰ的速率小于反应Ⅱ的速率
D.CO(g)+H O(g)===CO (g)+H (g) ΔH=+40.8 kJ·mol-1
2 2 2
13.室温下,通过下列实验探究NH HCO 的性质:
4 3
实验 实验操作和现象
1 用pH试纸测定0.1 mol·L-1 NH HCO 溶液的pH,测得pH约为10
4 3
向浓度为0.1 mol·L-1 NH HCO 溶液中加入足量NaOH,有刺激性气味
4 3
2
气体产生
浓度均为2.0 mol·L-1 NH HCO 溶液和NaCl溶液等体积混合,有晶体
4 3
3
析出,过滤
下列说法正确的是
A.0.1 mol·L-1 NH HCO 溶液中存在:
4 3
c(H+)+c(H CO )=c(CO 2- )+c(OH-)+c(NH ·H O)
2 3 3 3 2
B.由实验1可得:K (NH ·H O)>K (H CO )
b 3 2 a1 2 3
C.实验2中发生反应的离子方程式:NH+ +OH-===NH ↑+H O
4 3 2
D.实验3中所得滤液中存在:
c(NH+ )+c(NH ·H O)=c(H CO )+c(HCO- )+c(CO 2- )
4 3 2 2 3 3 3
化学试卷 第5页 (共9页)第 II 卷(非选择题,共 57 分)
三、非选择题
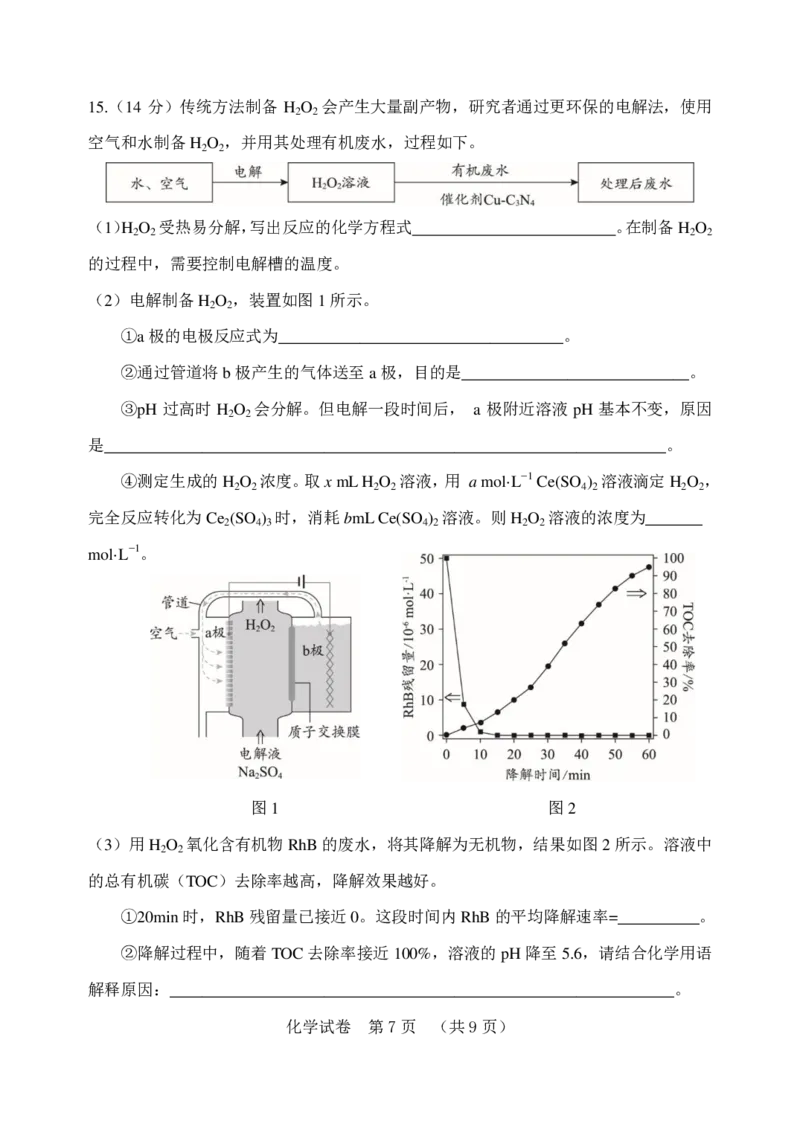
14.(14分) 以黄铁矿(主要成分是FeS ,含少量SiO )和软锰矿(主要成分是MnO ,含少量
2 2 2
Fe O 、Al O )为原料制备MnSO ·H O的工艺流程如下。回答下列问题:
2 3 2 3 4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Mn2+ Fe2+ Fe3+ Al3+
开始沉淀时(c=0.01 mol·L-1)的pH 8.1 7.5 2.2 3.7
沉淀完全时(c=1×10-5 mol·L-1)的pH 9.6 9.0 3.2 4.7
(1)“混合研磨”成细粉的目的是_______________________。“酸浸”过程得到的滤液中
含有Mn2、Fe3,则该过程中主要反应的离子方程式是__________________________。
(2)根据上表数据,计算 Mn(OH) 的 K =_____________。若“调pH”后的溶液中 Mn2+
2 sp
浓度为1.0mol·L−1,则“调pH”应控制的pH范围是______________。
(3)写出“沉锰”的离子方程式_______________________________________________。
(4)结合右图图像,分析从“操作A”所得的
溶液中获得MnSO ·H O晶体需要进行的操作是
4 2
___________、___________、洗涤、干燥。
从制取的产品中,称取一定质量的MnSO ·H O
4 2
用标准BaCl 溶液滴定(操作过程产生的误差很小,
2
可忽略),计算所得样品的质量分数大于100%,
可能的原因是____________________________________________________________。
化学试卷 第6页 (共9页)15.(14 分)传统方法制备 H O 会产生大量副产物,研究者通过更环保的电解法,使用
2 2
空气和水制备H O ,并用其处理有机废水,过程如下。
2 2
(1)H O 受热易分解,写出反应的化学方程式 。在制备H O
2 2 2 2
的过程中,需要控制电解槽的温度。
(2)电解制备H O ,装置如图1所示。
2 2
①a极的电极反应式为___________________________________。
②通过管道将b极产生的气体送至a极,目的是____________________________。
③pH 过高时 H O 会分解。但电解一段时间后, a 极附近溶液 pH 基本不变,原因
2 2
是_____________________________________________________________________。
④测定生成的H O 浓度。取x mL H O 溶液,用 a mol·L−1 Ce(SO ) 溶液滴定H O ,
2 2 2 2 4 2 2 2
完全反应转化为Ce (SO ) 时,消耗bmL Ce(SO ) 溶液。则H O 溶液的浓度为_______
2 4 3 4 2 2 2
mol·L−1。
图1 图2
(3)用H O 氧化含有机物RhB的废水,将其降解为无机物,结果如图2所示。溶液中
2 2
的总有机碳(TOC)去除率越高,降解效果越好。
①20min时,RhB残留量已接近0。这段时间内RhB的平均降解速率=__________。
②降解过程中,随着TOC去除率接近100%,溶液的pH降至5.6,请结合化学用语
解释原因:______________________________________________________________。
化学试卷 第7页 (共9页)16.(14分)中国科学家在国际上首次实现了CO 到淀粉的合成,不依赖植物光合作用,
2
原料只需CO 、H 和电,相关成果发表在《科学》上。回答下列问题:
2 2
(1)CO 的空间结构为 形,其中C原子的杂化方式为 。
2
(2)淀粉遇碘变蓝。单质碘易溶于KI溶液,原因是
(用离子方程式表示)。
H
O O
2 1
(3)淀粉在一定条件下可水解成葡萄糖( ),葡萄糖分
CH CH CH CH C C H
2 2 1 1
OH OH OH OH H
子中键角 ∠H C O ∠C C O (填“>”、“<”或“=”)。
1 1 1 1 2 2
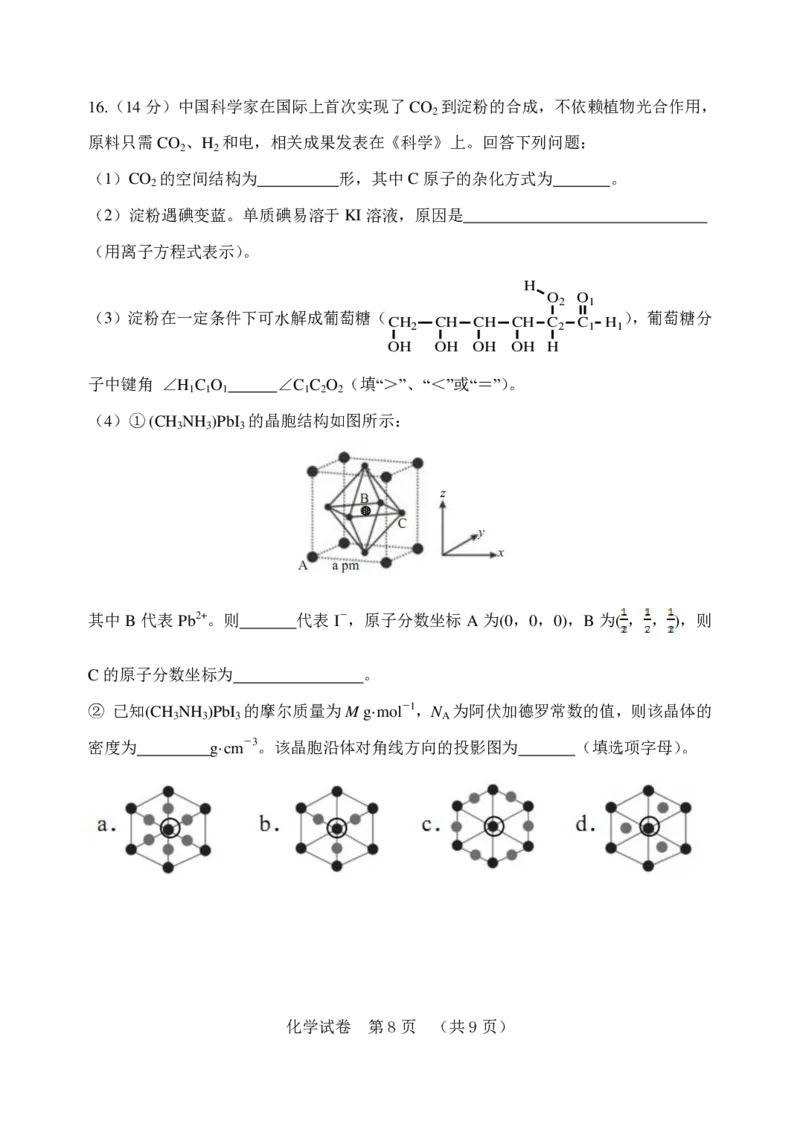
(4)① (CH NH )PbI 的晶胞结构如图所示:
3 3 3
其中B 代表Pb2+。则 代表 I-,原子分数坐标 A 为(0,0,0),B 为( , , ),则
C的原子分数坐标为 。
② 已知(CH NH )PbI 的摩尔质量为M g·mol-1,N 为阿伏加德罗常数的值,则该晶体的
3 3 3 A
密度为 g·cm-3。该晶胞沿体对角线方向的投影图为 (填选项字母)。
化学试卷 第8页 (共9页)17.(15分)
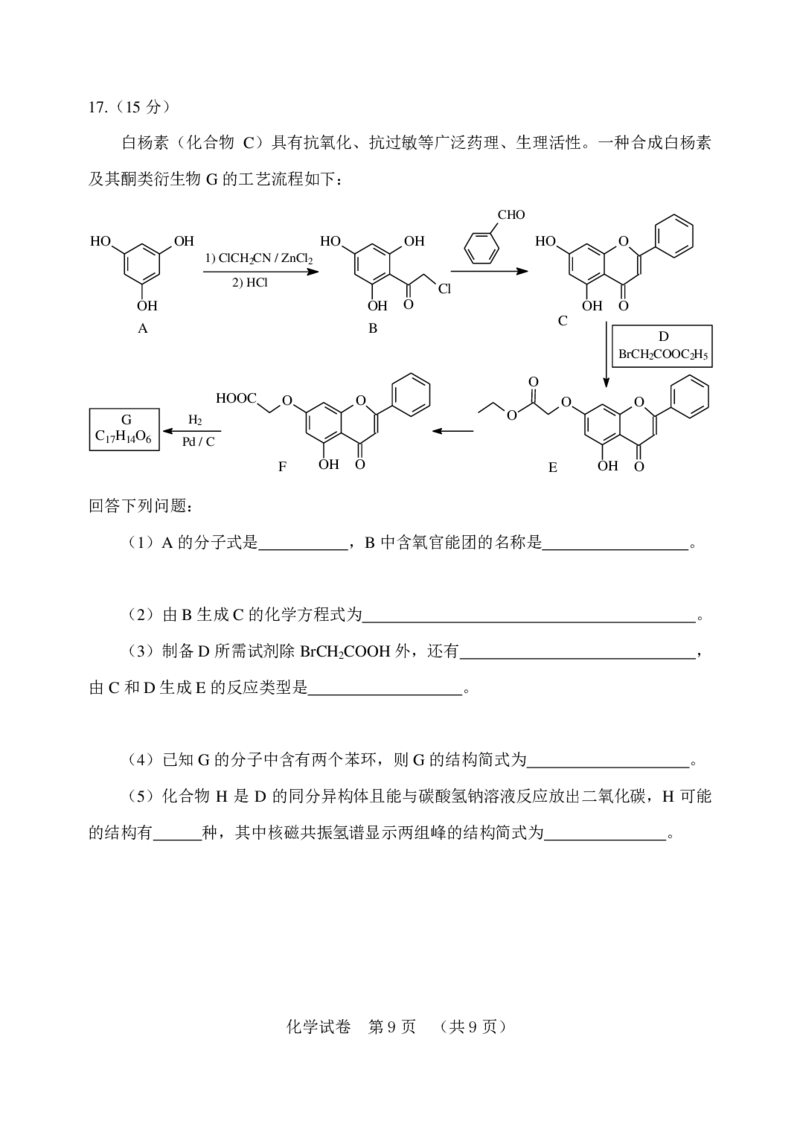
白杨素(化合物 C)具有抗氧化、抗过敏等广泛药理、生理活性。一种合成白杨素
及其酮类衍生物G的工艺流程如下:
CHO
HO OH HO OH HO O
1) ClCH2CN / ZnCl2
2) HCl
Cl
OH OH O OH O
C
A B
D
BrCH2COOC2H5
O
HOOC O O O O
G H2 O
C H O
17 14 6 Pd / C
F OH O E OH O
回答下列问题:
(1)A的分子式是 ,B中含氧官能团的名称是 。
(2)由B生成C的化学方程式为 。
(3)制备D所需试剂除BrCH COOH外,还有 ,
2
由C和D生成E的反应类型是 。
(4)已知G的分子中含有两个苯环,则G的结构简式为 。
(5)化合物 H 是 D 的同分异构体且能与碳酸氢钠溶液反应放出二氧化碳,H 可能
的结构有 种,其中核磁共振氢谱显示两组峰的结构简式为 。
化学试卷 第9页 (共9页)