文档内容
天津市耀华中学 2023 届高三年级第三次月考
化学试卷
本试卷分为第I卷(选择题)和第II卷(非选择题)两部分,共100分,考试时间60分钟。第I卷
1至5页,第II卷6至10页。
答卷前,考生务必将姓名、班级、考号填在答题卡上。答卷时,考生务必将答案涂写在答题
卡上,答在试卷上的无效。考试结束后,将答题卡交回。
祝各位考生考试顺利!
第I卷(共36分)
注意事项:
1.每题选出答案后,用铅笔将答题卡对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,
再选涂其他答案标号。
2.本卷共12题,每题3分,共36分。在每题给出的四个选项中,只有一项是最符合题目要求
的。
以下数据可供解题时参考:
相对原子质量:H-1 C-12 O-16 Na-23 Al-27 Cl-35.5 Co-59
1. 发任意球时,足球裁判会在球场喷少量液体做标记,该液体迅速形成白色泡沫并很快消失。该液体的组
成:80%水、17%液态丁烷、2%植物油及1%表面活性剂,液体形成泡沫有表面活性剂的作用,还因为
A. 丁烷变成气体 B. 植物油变成固体 C. 水变成气体 D. 水变成固体
【答案】A
【解析】
【详解】常温下丁烷为气态烃,由液体的组成和性质可知,在球场喷少量液体做标记时,喷出的液体中的
液态丁烷迅速变成气体使表面活性剂形成泡沫,故选A。
2. 设N 为阿伏加德罗常数的值。由电化学固氮得到的AlN转化为 的反应为:
A
,下列说法不正确的是
A. 固氮过程中,每生成1mol AlN转移的电子数目为3N
A
B. 室温下,pH为13的NaOH溶液中OH-数目为0.1N
A
C. 标准状况下,1.12LNH 中含有的电子数目为0.5N
3 A
D. 11.8g 中含有的共价键数目为0.8N
A【答案】B
【解析】
【详解】A.固氮过程中,Al与N 反应生成AlN,电子转移的数目为3e-,则每生成1mol AlN转移的电子
2
数目为3N ,A正确;
A
B.pH为13的NaOH溶液的体积未知,无法计算溶液中所含OH-的数目,B不正确;
C.标准状况下,1.12LNH 的物质的量为0.05mol,每个NH 分子中含有10个电子,则1.12LNH 含有的电
3 3 3
子数目为0.5N ,C正确;
A
D.11.8g 的物质的量为 ,每个 中含有8个共价键,则含
有的共价键数目为0.8N ,D正确;
A
故选B。
3. 高中化学《化学反应原理》模块从不同的视角对化学反应进行了探究、分析,以下观点中不正确的是
A. 难溶电解质在水中达到溶解平衡时,再加入难溶电解质,溶液中各离子浓度不变
B. 将 加入水中并加热使其转化为
C. 乙烯聚合为聚乙烯的反应是熵减的过程,却能够自发进行,可知该反应的
D. 溶液显碱性 原的因:
【答案】D
【解析】
【详解】A.难溶电解质在水中达到溶解平衡时,再加入难溶电解质,溶液仍处于饱和状态,溶液中各离
子浓度不变,A正确;
B.将 加入水中,钛离子水解生成氢氧化钛和挥发性酸盐酸,故加热氢氧化钛最终会使其转化为
,B正确;
C.熵变、焓变都是影响反应自发的因素,乙烯聚合为聚乙烯的反应是熵减的过程,却能够自发进行,可
知该反应的 ,C正确;
D. 溶液显碱性的原因是碳酸氢根离子水解生成氢氧根离子: ,
D错误;
故选D。
4. 下列说法正确的是A. 镁在空气中燃烧可生成氧化镁和氮化镁
B. 浓HSO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
C. 加热NaI与浓HPO 混合物可制备HI,说明HPO 比HI酸性强
3 4 3 4
D. 向浓HNO 中插入红热的炭,产生红棕色气体,说明炭可与浓HNO 反应生成NO
3 3 2
【答案】A
【解析】
【详解】A.镁非常活泼,在空气中燃烧可和氮气、氧气反应,生成氧化镁和氮化镁,A正确;
B.浓HSO 能吸收糖类化合物中的水分并使其炭化,是其脱水性的体现,B错误;
2 4
C.浓HPO 为难挥发性酸,加热NaI与浓HPO 混合物可制备HI,是难挥发性酸制取挥发性酸,C错误;
3 4 3 4
D.向浓HNO 中插入红热的炭,产生红棕色气体,也可能是硝酸受热分解生成二氧化氮气体,D错误。
3
故选A。
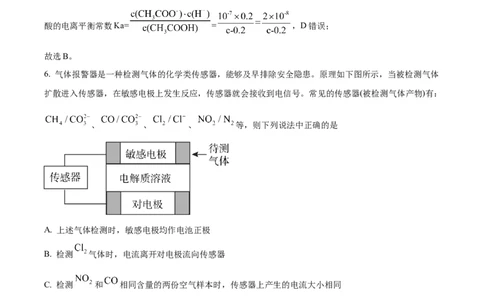
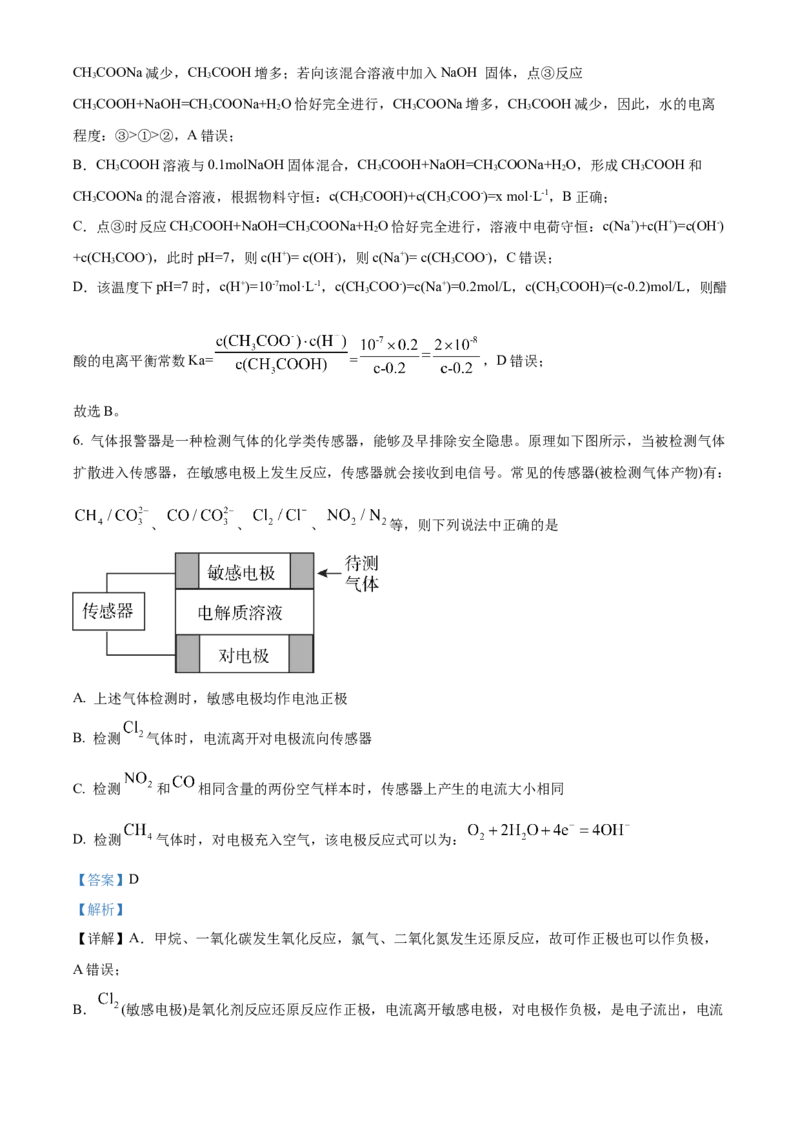
5. 25℃时,将1.0Lx mol ·L-1 CHCOOH溶液与0. 1 mol NaOH固体混合,使之充分反应。然后向该混合溶
3
液中通入HCl气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的物质的量的变
化如图所示。下列叙述正确的是
A. 水的电离程度:①>②>③
B. 点②对应的混合溶液中:c(CHCOOH)+c(CH COO-)=x mol·L-1
3 3
C. 点③对应的混合溶液中:c(Na+)> c(CHCOO-)
3
D. 该温度下,CHCOOH的电离平衡常数K=
3 a
【答案】B
【解析】
【详解】A.CHCOOH溶液与0.1molNaOH固体混合,CHCOOH+NaOH=CH COONa+H O,形成
3 3 3 2
CHCOOH和CHCOONa的混合溶液,其中CHCOONa的水解促进水的电离,CHCOOH的电离抑制水的
3 3 3 3
电离。若向该混合溶液中通入HCl,点②反应CHCOONa+HCl=CH COOH+NaCl恰好完全发生,
3 3CHCOONa减少,CHCOOH增多;若向该混合溶液中加入NaOH 固体,点③反应
3 3
CHCOOH+NaOH=CH COONa+H O恰好完全进行,CHCOONa增多,CHCOOH减少,因此,水的电离
3 3 2 3 3
程度:③>①>②,A错误;
B.CHCOOH溶液与0.1molNaOH固体混合,CHCOOH+NaOH=CH COONa+H O,形成CHCOOH和
3 3 3 2 3
CHCOONa的混合溶液,根据物料守恒:c(CHCOOH)+c(CH COO-)=x mol·L-1,B正确;
3 3 3
C.点③时反应CHCOOH+NaOH=CH COONa+H O恰好完全进行,溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)
3 3 2
+c(CH COO-),此时pH=7,则c(H+)= c(OH-),则c(Na+)= c(CHCOO-),C错误;
3 3
D.该温度下pH=7时,c(H+)=10-7mol·L-1,c(CHCOO-)=c(Na+)=0.2mol/L,c(CHCOOH)=(c-0.2)mol/L,则醋
3 3
酸的电离平衡常数Ka= = ,D错误;
故选B。
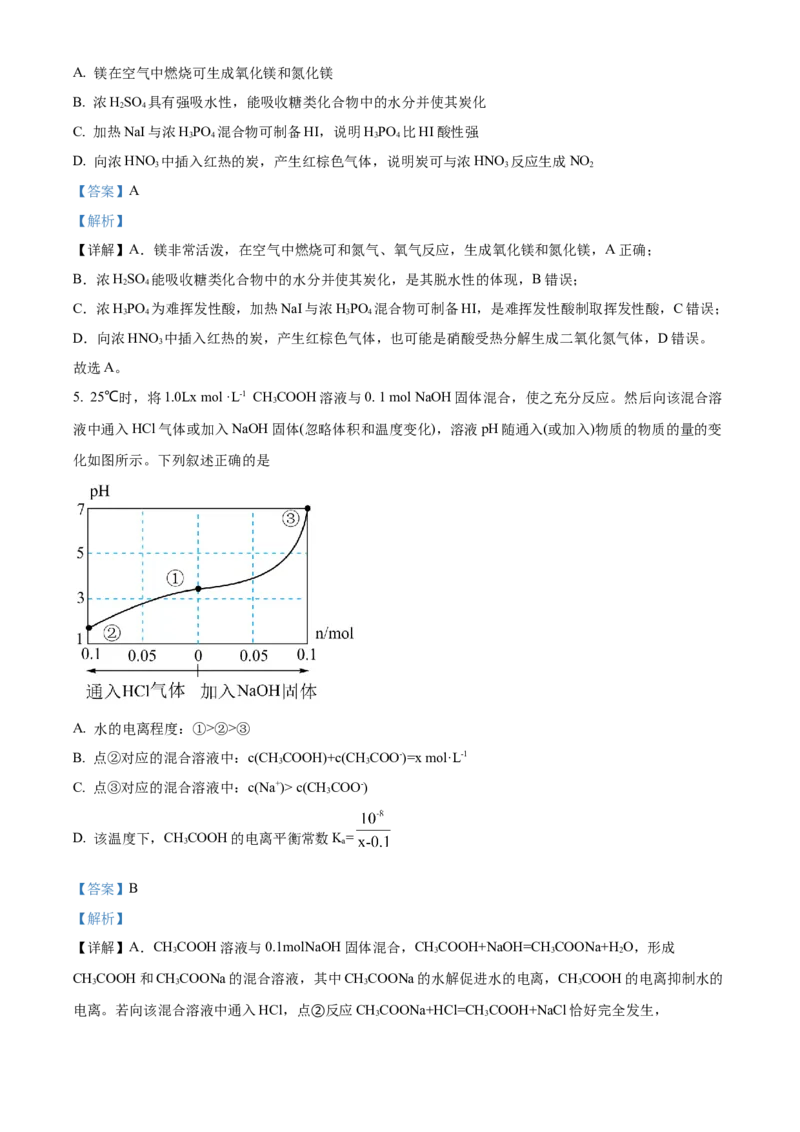
6. 气体报警器是一种检测气体的化学类传感器,能够及早排除安全隐患。原理如下图所示,当被检测气体
扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。常见的传感器(被检测气体产物)有:
、 、 、 等,则下列说法中正确的是
A. 上述气体检测时,敏感电极均作电池正极
B. 检测 气体时,电流离开对电极流向传感器
C. 检测 和 相同含量的两份空气样本时,传感器上产生的电流大小相同
D. 检测 气体时,对电极充入空气,该电极反应式可以为:
【答案】D
【解析】
【详解】A.甲烷、一氧化碳发生氧化反应,氯气、二氧化氮发生还原反应,故可作正极也可以作负极,
A错误;
B. (敏感电极)是氧化剂反应还原反应作正极,电流离开敏感电极,对电极作负极,是电子流出,电流流入,B错误;
C.电流大小由转移电子大小决定, 由+4变为0价转移4个电子, 由+2价变为+4价转移2个电
子,相同量气体转移电子不同,则电流不同,C错误;
D. 氧化产物为 说明电解质为碱性,对电极为正极,电极反应式可以为:
,D正确;
故选D。
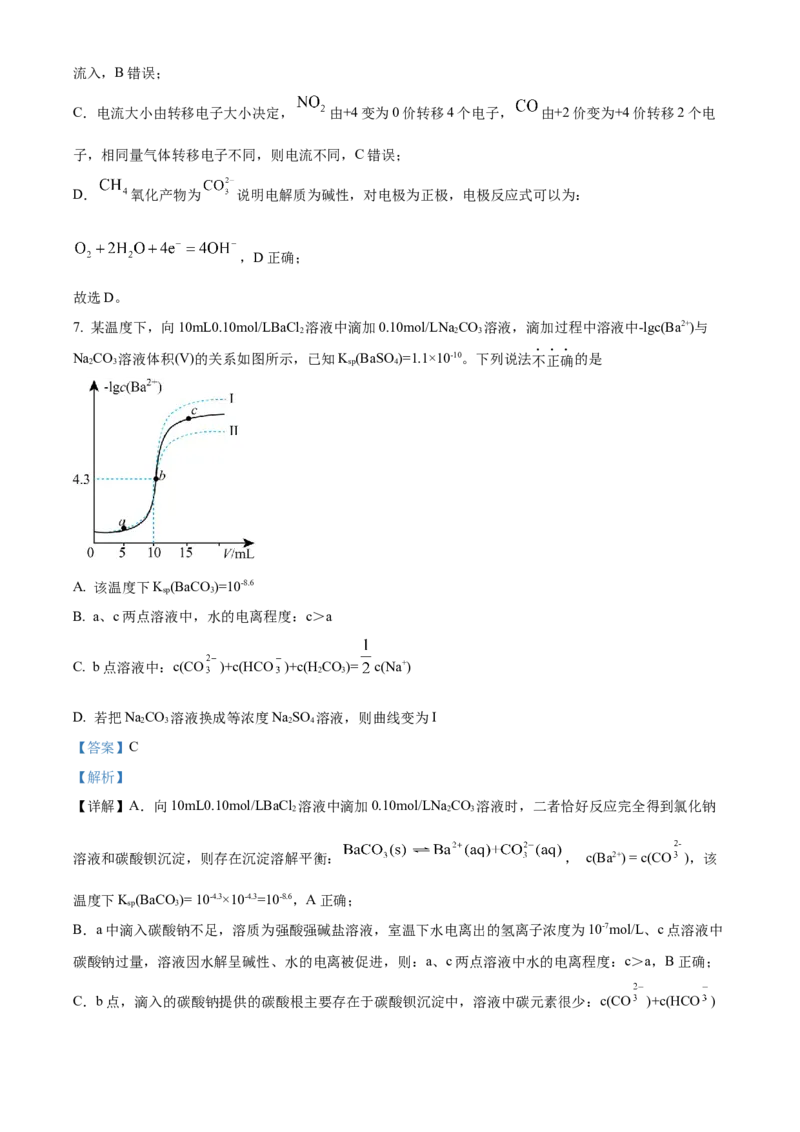
7. 某温度下,向10mL0.10mol/LBaCl 溶液中滴加0.10mol/LNa CO 溶液,滴加过程中溶液中-lgc(Ba2+)与
2 2 3
NaCO 溶液体积(V)的关系如图所示,已知K (BaSO)=1.1×10-10。下列说法不正确的是
2 3 sp 4
A. 该温度下K (BaCO)=10-8.6
sp 3
B. a、c两点溶液中,水的电离程度:c>a
C. b点溶液中:c(CO )+c(HCO )+c(H CO)= c(Na+)
2 3
D. 若把NaCO 溶液换成等浓度NaSO 溶液,则曲线变为I
2 3 2 4
【答案】C
【解析】
【详解】A.向10mL0.10mol/LBaCl 溶液中滴加0.10mol/LNa CO 溶液时,二者恰好反应完全得到氯化钠
2 2 3
溶液和碳酸钡沉淀,则存在沉淀溶解平衡: , c(Ba2+) = c(CO ),该
温度下K (BaCO)= 10-4.3×10-4.3=10-8.6,A正确;
sp 3
B.a中滴入碳酸钠不足,溶质为强酸强碱盐溶液,室温下水电离出的氢离子浓度为10-7mol/L、c点溶液中
碳酸钠过量,溶液因水解呈碱性、水的电离被促进,则:a、c两点溶液中水的电离程度:c>a,B正确;
C.b点,滴入的碳酸钠提供的碳酸根主要存在于碳酸钡沉淀中,溶液中碳元素很少:c(CO )+c(HCO )+c(H CO)< c(Na+),C不正确;
2 3
D. 若把NaCO 溶液换成等浓度NaSO 溶液:向10mL0.10mol/LBaCl 溶液中滴加0.10mol/L Na SO 溶液
2 3 2 4 2 2 4
时,二者恰好反应完全得到氯化钠溶液和硫酸钡沉淀,则存在沉淀溶解平衡:
, c(Ba2+) = c(SO ),该温度下K (BaSO)= 1.1×10-10,则c(Ba2+) =
sp 4
c(SO )= , >4.3,则曲线变为I,D正确;
答案选C。
8. 在直流电源作用下,双极膜中间层中的HO解离为H+和OH-,利用双极膜电解池产生强氧化性的羟基
2
自由基(•OH),处理含苯酚废水和含SO 的烟气的工作原理如图所示。下列说法错误的是
2
A. 电势:N电极>M电极
B. 阴极电极反应式为O+2e-+2H+=2•OH
2
C. 每处理9.4g苯酚,理论上有2.8molH+透过膜a
D. 若•OH只与苯酚和SO 反应,则参加反应的苯酚和SO 物质的量之比为1:14
2 2
【答案】C
【解析】
【分析】双极膜中间层中的HO解离为H+和OH-,M极上O 得电子与H+反应生成羟基自由基(•OH),说明
2 2
M极为阴极,连接电源的负极,M极上产生的羟基自由基将苯酚氧化生成CO;N极为阳极,HO解离产
2 2
生的OH-失电子产生羟基自由基,羟基自由基将SO 氧化为硫酸根离子。
2
的
【详解】A.M极上O 得电子生成羟基自由基(•OH),说明M极为阴极,连接电源 负极,N极为阳极,
2故电势:N电极>M电极,选项A正确;
B.M为阴极,阴极上O 得电子生成羟基自由基(•OH),电极反应式为O+2e-+2H+=2•OH,选项B正确;
2 2
C.每mol苯酚转化为CO,转移电子28mol,每处理9.4g苯酚(即0.1mol),理论上有2.8mol电子转移,
2
则有2.8molH+透过膜b,选项C错误;
D.若•OH只与苯酚和SO 反应,转移电子数之比为28:2,则参加反应的苯酚和SO 物质的量之比为1:
2 2
14,选项D正确;
答案选C。
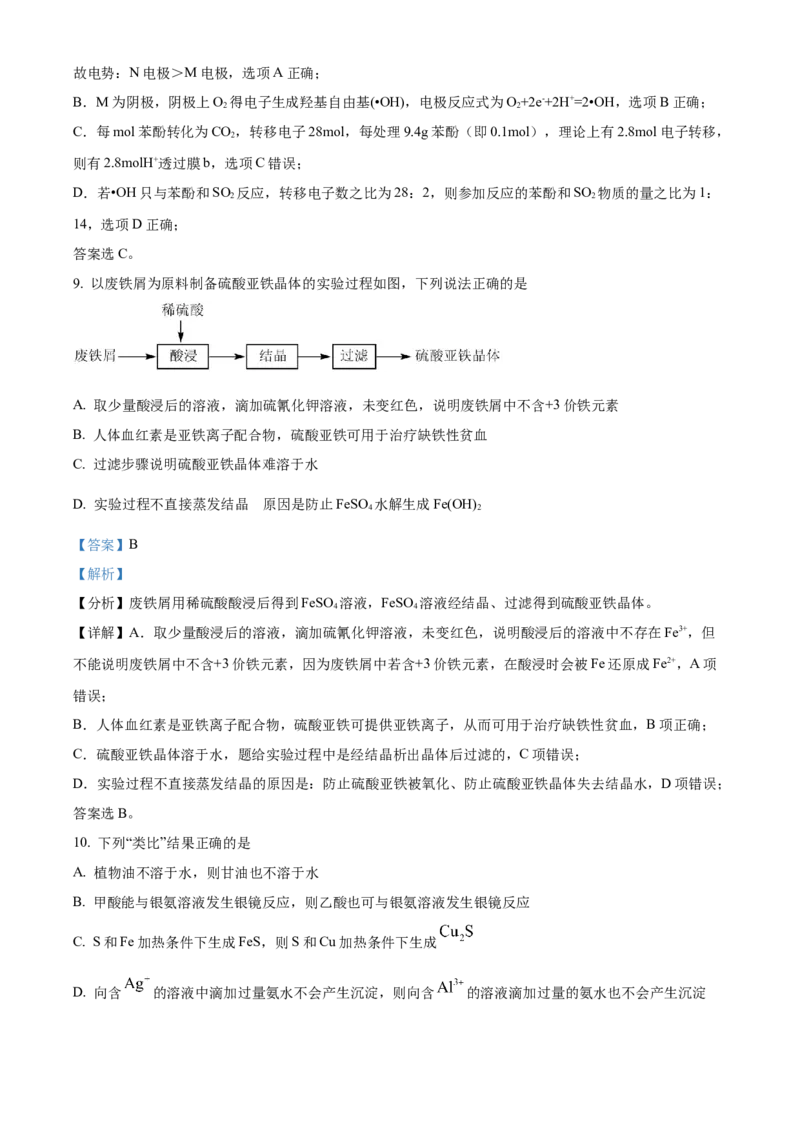
9. 以废铁屑为原料制备硫酸亚铁晶体的实验过程如图,下列说法正确的是
A. 取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明废铁屑中不含+3价铁元素
B. 人体血红素是亚铁离子配合物,硫酸亚铁可用于治疗缺铁性贫血
C. 过滤步骤说明硫酸亚铁晶体难溶于水
的
D. 实验过程不直接蒸发结晶 原因是防止FeSO 水解生成Fe(OH)
4 2
【答案】B
【解析】
【分析】废铁屑用稀硫酸酸浸后得到FeSO 溶液,FeSO 溶液经结晶、过滤得到硫酸亚铁晶体。
4 4
【详解】A.取少量酸浸后的溶液,滴加硫氰化钾溶液,未变红色,说明酸浸后的溶液中不存在Fe3+,但
不能说明废铁屑中不含+3价铁元素,因为废铁屑中若含+3价铁元素,在酸浸时会被Fe还原成Fe2+,A项
错误;
B.人体血红素是亚铁离子配合物,硫酸亚铁可提供亚铁离子,从而可用于治疗缺铁性贫血,B项正确;
C.硫酸亚铁晶体溶于水,题给实验过程中是经结晶析出晶体后过滤的,C项错误;
D.实验过程不直接蒸发结晶的原因是:防止硫酸亚铁被氧化、防止硫酸亚铁晶体失去结晶水,D项错误;
答案选B。
10. 下列“类比”结果正确的是
A. 植物油不溶于水,则甘油也不溶于水
B. 甲酸能与银氨溶液发生银镜反应,则乙酸也可与银氨溶液发生银镜反应
C. S和Fe加热条件下生成FeS,则S和Cu加热条件下生成
D. 向含 的溶液中滴加过量氨水不会产生沉淀,则向含 的溶液滴加过量的氨水也不会产生沉淀【答案】C
【解析】
【详解】A.甘油为丙三醇,能与水混溶,A错误;
B.甲酸中有醛基,故能发生银镜反应,乙酸中无醛基,不能发生银镜反应,B错误;
C.硫的氧化性较弱,与变价金属反应只能生成低价态化合物,故与铁反应生成硫化亚铁,与铜反应生成
硫化亚铜,C正确;
D. 向银离子的溶液中加入过量的氨水生成银氨溶液,不会产生沉淀,但向含有铝离子的溶液中加入过量
的氨水只能生成氢氧化铝沉淀,D错误;
故选C。
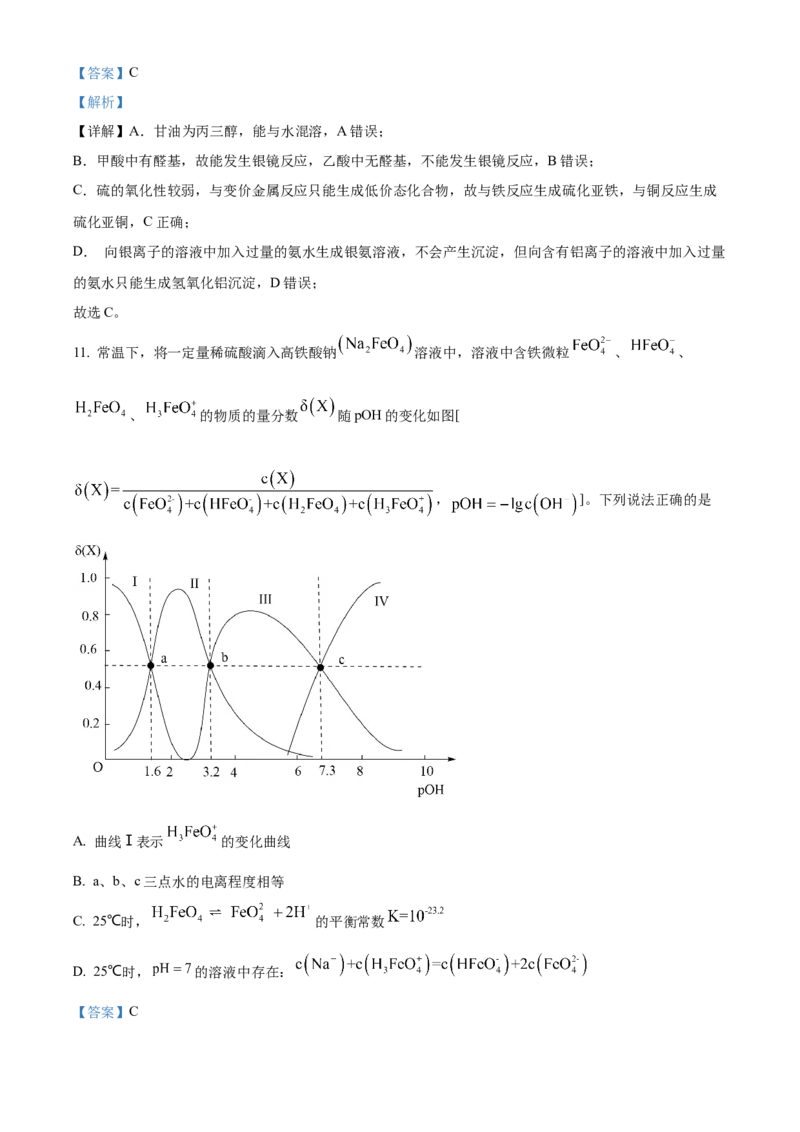
11. 常温下,将一定量稀硫酸滴入高铁酸钠 溶液中,溶液中含铁微粒 、 、
、 的物质的量分数 随pOH的变化如图[
, ]。下列说法正确的是
A. 曲线Ⅰ表示 的变化曲线
B. a、b、c三点水的电离程度相等
C. 25℃时, 的平衡常数
D. 25℃时, 的溶液中存在:
【答案】C【解析】
【分析】稀硫酸逐滴滴入高铁酸钠 溶液中,溶液pOH不断增大,OH-的浓度不断减小,H+的
浓度不断增大,则 的物质的量分数减小,之后 的物质的量分数先增大后减小,然后
的物质的量分数先增大后减小,最后 的物质的量分数增大,故曲线I表示 的变化
曲线,曲线II表示 的变化曲线,曲线III表示 的变化曲线,曲线IV表示 的变化曲
线。
【详解】A.据分析知,曲线Ⅰ表示 的变化曲线,A错误;
B.a、b、c三点溶液中微粒成分不同,溶液pOH不同,对水的电离影响程度不同,则水的电离程度不相
等,B错误;
C.由a点可知, ,所以 的 ,同理可推
知 的 ,所以 的平衡常数
,C正确;
D.根据电荷守恒得, ,
的溶液中 ,所以 ,D
错误;
故选C。
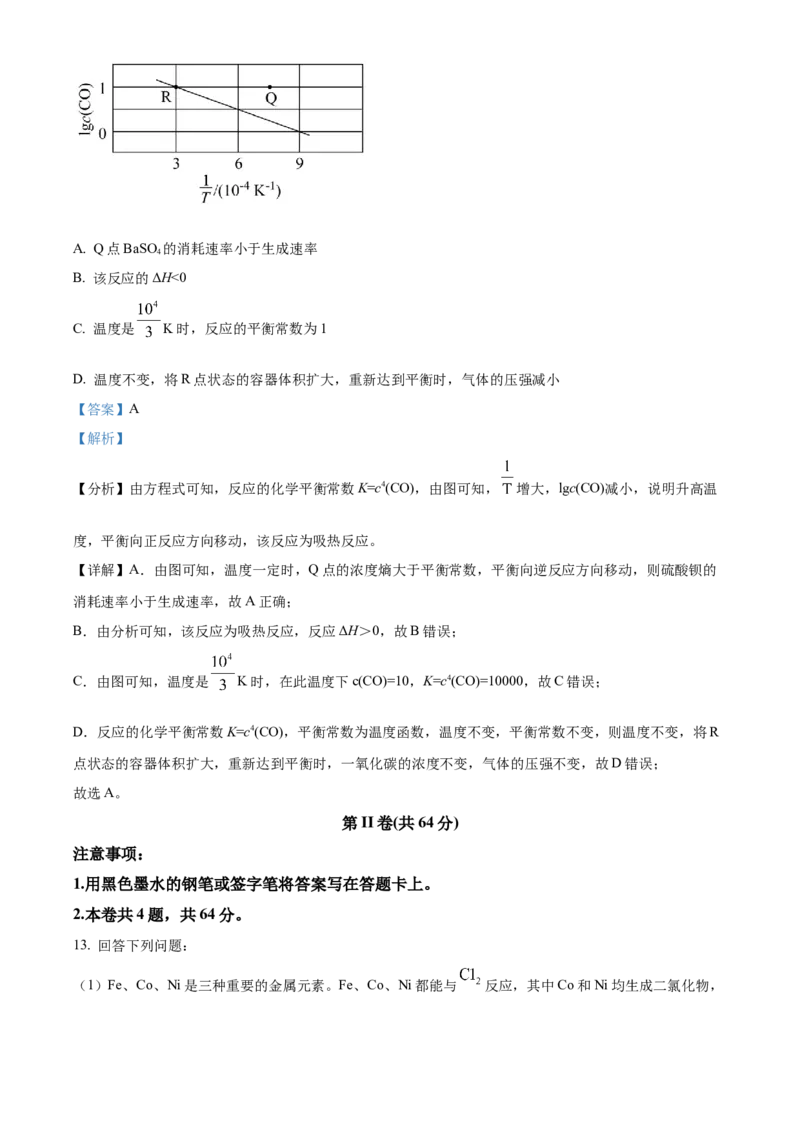
12. 在一定温度下,BaSO 和C在一密闭容器中进行反应:BaSO(s)+4C(s) BaS(s)+4CO(g),CO的平
4 4
衡浓度(mol/L)的对数lgc(CO)与温度的倒数 的关系如图所示,下列说法中正确的是A. Q点BaSO 的消耗速率小于生成速率
4
B. 该反应的ΔH<0
C. 温度是 K时,反应的平衡常数为1
D. 温度不变,将R点状态的容器体积扩大,重新达到平衡时,气体的压强减小
【答案】A
【解析】
【分析】由方程式可知,反应的化学平衡常数K=c4(CO),由图可知, 增大,lgc(CO)减小,说明升高温
度,平衡向正反应方向移动,该反应为吸热反应。
【详解】A.由图可知,温度一定时,Q点的浓度熵大于平衡常数,平衡向逆反应方向移动,则硫酸钡的
消耗速率小于生成速率,故A正确;
B.由分析可知,该反应为吸热反应,反应ΔH>0,故B错误;
C.由图可知,温度是 K时,在此温度下c(CO)=10,K=c4(CO)=10000,故C错误;
D.反应的化学平衡常数K=c4(CO),平衡常数为温度函数,温度不变,平衡常数不变,则温度不变,将R
点状态的容器体积扩大,重新达到平衡时,一氧化碳的浓度不变,气体的压强不变,故D错误;
故选A。
第II卷(共64分)
注意事项:
1.用黑色墨水的钢笔或签字笔将答案写在答题卡上。
2.本卷共4题,共64分。
13. 回答下列问题:
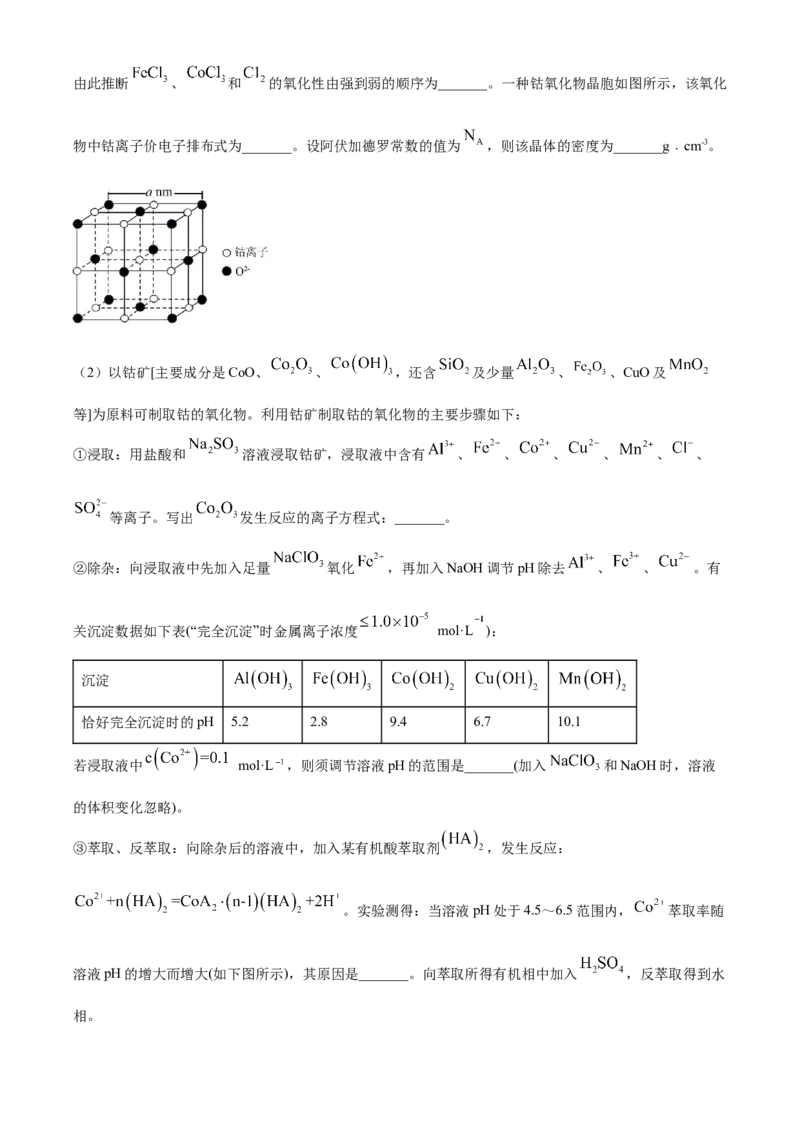
(1)Fe、Co、Ni是三种重要的金属元素。Fe、Co、Ni都能与 反应,其中Co和Ni均生成二氯化物,由此推断 、 和 的氧化性由强到弱的顺序为_______。一种钴氧化物晶胞如图所示,该氧化
物中钴离子价电子排布式为_______。设阿伏加德罗常数的值为 ,则该晶体的密度为_______g﹒cm-3。
(2)以钴矿[主要成分是CoO、 、 ,还含 及少量 、 、CuO及
等]为原料可制取钴的氧化物。利用钴矿制取钴的氧化物的主要步骤如下:
①浸取:用盐酸和 溶液浸取钴矿,浸取液中含有 、 、 、 、 、 、
等离子。写出 发生反应的离子方程式:_______。
②除杂:向浸取液中先加入足量 氧化 ,再加入NaOH调节pH除去 、 、 。有
关沉淀数据如下表(“完全沉淀”时金属离子浓度 mol·L ):
沉淀
恰好完全沉淀时的pH 5.2 2.8 9.4 6.7 10.1
若浸取液中 mol·L ,则须调节溶液pH的范围是_______(加入 和NaOH时,溶液
的体积变化忽略)。
③萃取、反萃取:向除杂后的溶液中,加入某有机酸萃取剂 ,发生反应:
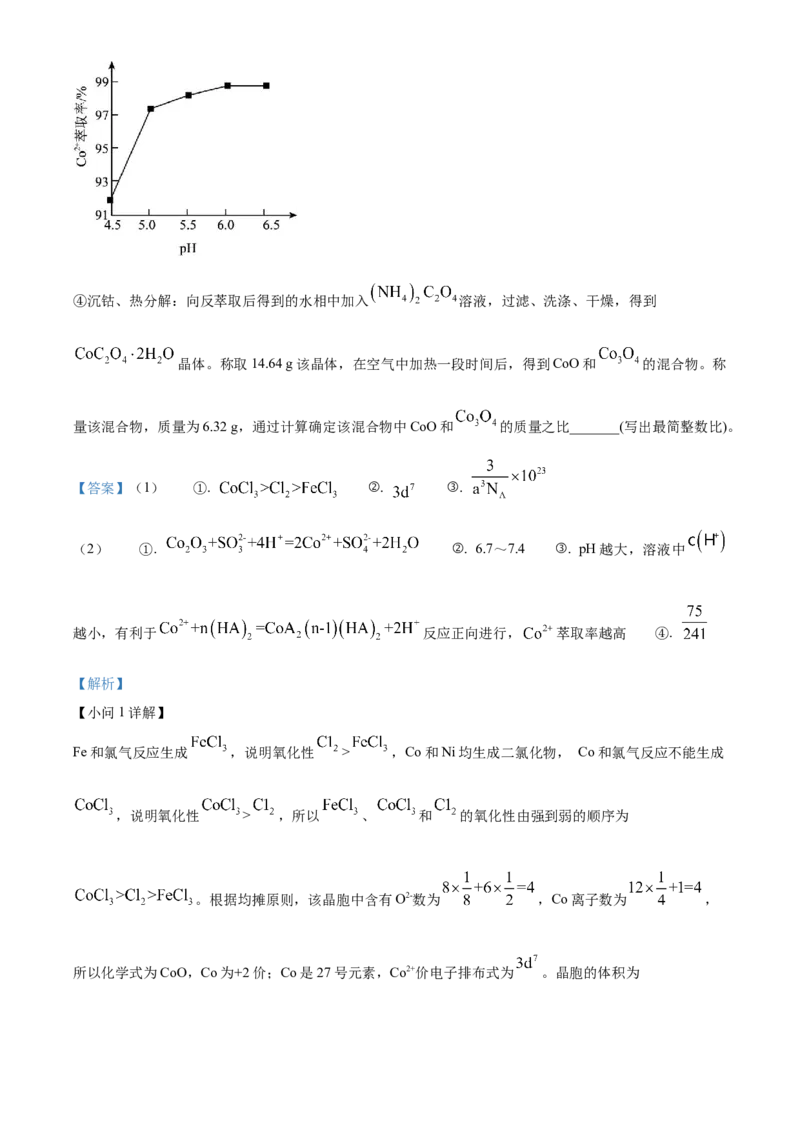
。实验测得:当溶液pH处于4.5~6.5范围内, 萃取率随
溶液pH的增大而增大(如下图所示),其原因是_______。向萃取所得有机相中加入 ,反萃取得到水
相。④沉钴、热分解:向反萃取后得到的水相中加入 溶液,过滤、洗涤、干燥,得到
晶体。称取14.64 g该晶体,在空气中加热一段时间后,得到CoO和 的混合物。称
量该混合物,质量为6.32 g,通过计算确定该混合物中CoO和 的质量之比_______(写出最简整数比)。
【答案】(1) ①. ②. ③.
(2) ①. ②. 6.7~7.4 ③. pH越大,溶液中
越小,有利于 反应正向进行, 萃取率越高 ④.
【解析】
【小问1详解】
Fe和氯气反应生成 ,说明氧化性 > ,Co和Ni均生成二氯化物, Co和氯气反应不能生成
,说明氧化性 > ,所以 、 和 的氧化性由强到弱的顺序为
。根据均摊原则,该晶胞中含有O2-数为 ,Co离子数为 ,
所以化学式为CoO,Co为+2价;Co是27号元素,Co2+价电子排布式为 。晶胞的体积为,设阿伏加德罗常数的值为 ,则该晶体的密度为
g﹒cm-3。
【小问2详解】
①浸取液中含有 ,说明 被 还原为 , 被氧化为 , 与 发生
反应的离子方程式为 。
② 完全沉淀的pH=9.4,则Ksp[ ]= ;若浸取液中
mol·L ,为防止 生成Co(OH) 沉淀,c(OH-)的最大值为 mol·L
2
,则 开始沉淀的pH=7.4,所以须调节溶液pH的范围是6.7~7.4。
③pH越大,溶液中 越小,有利于 反应正向进行,
萃取率越高。
④14.64 g 的物质的量为14.64g÷183g/mol=0.08mol。设CoO和 的物质的量分别为
xmol、ymol。 ,x=0.02、y=0.02,该混合物中CoO和 的质量之比
。
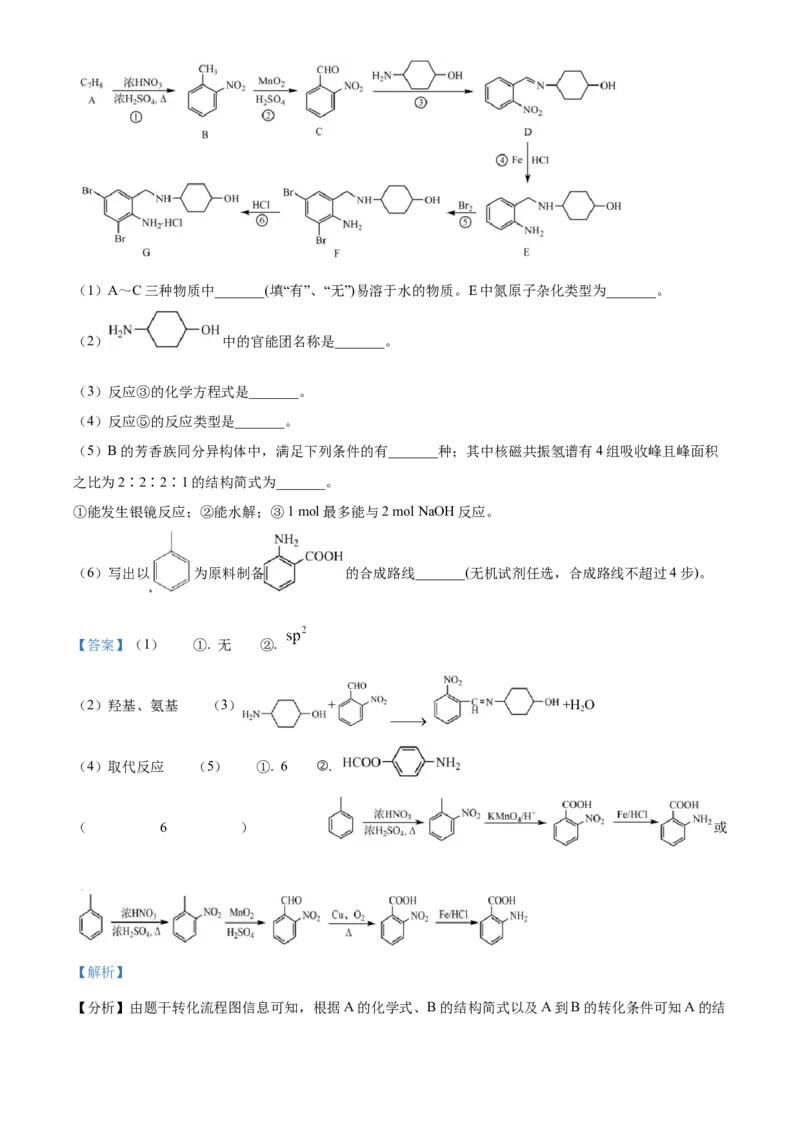
14. 氨溴索(G)是β-内酰胺类的抗生素,可以治疗多种细菌感染。一种合成路线如下:(1)A~C三种物质中_______(填“有”、“无”)易溶于水的物质。E中氮原子杂化类型为_______。
(2) 中的官能团名称是_______。
(3)反应③的化学方程式是_______。
(4)反应⑤的反应类型是_______。
(5)B的芳香族同分异构体中,满足下列条件的有_______种;其中核磁共振氢谱有4组吸收峰且峰面积
之比为2∶2∶2∶1的结构简式为_______。
①能发生银镜反应;②能水解;③1 mol最多能与2 mol NaOH反应。
(6)写出以 为原料制备 的合成路线_______(无机试剂任选,合成路线不超过4步)。
【答案】(1) ①. 无 ②.
(2)羟基、氨基 (3) + +H O
2
(4)取代反应 (5) ①. 6 ②.
( 6 ) 或
【解析】
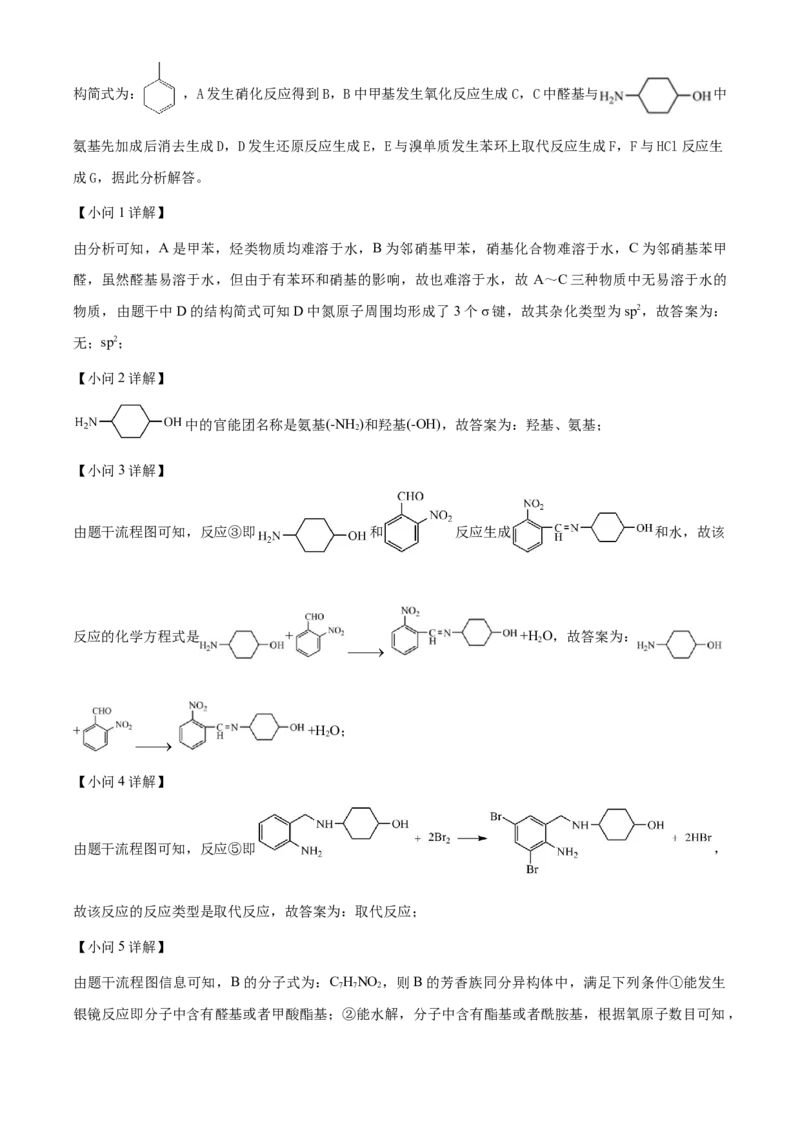
【分析】由题干转化流程图信息可知,根据A的化学式、B的结构简式以及A到B的转化条件可知A的结构简式为: ,A发生硝化反应得到B,B中甲基发生氧化反应生成C,C中醛基与 中
氨基先加成后消去生成D,D发生还原反应生成E,E与溴单质发生苯环上取代反应生成F,F与HCl反应生
成G,据此分析解答。
【小问1详解】
由分析可知,A是甲苯,烃类物质均难溶于水,B为邻硝基甲苯,硝基化合物难溶于水,C为邻硝基苯甲
醛,虽然醛基易溶于水,但由于有苯环和硝基的影响,故也难溶于水,故 A~C三种物质中无易溶于水的
物质,由题干中D的结构简式可知D中氮原子周围均形成了3个σ键,故其杂化类型为sp2,故答案为:
无;sp2;
【小问2详解】
中的官能团名称是氨基(-NH )和羟基(-OH),故答案为:羟基、氨基;
2
【小问3详解】
由题干流程图可知,反应③即 和 反应生成 和水,故该
反应的化学方程式是 + +H O,故答案为:
2
+ +H O;
2
【小问4详解】
由题干流程图可知,反应⑤即 ,
故该反应的反应类型是取代反应,故答案为:取代反应;
【小问5详解】
由题干流程图信息可知,B的分子式为:C HNO ,则B的芳香族同分异构体中,满足下列条件①能发生
7 7 2
银镜反应即分子中含有醛基或者甲酸酯基;②能水解,分子中含有酯基或者酰胺基,根据氧原子数目可知,分子中含有甲酸酯基或者甲酰胺基;③1mol最多能与2mol NaOH反应说明分子中含有甲酸酚酯基,则符
合条件的同分异构体为苯环上连:-OOCH和NH 、或者-CH 和-NHCHO两种组合,每组又有邻间对三种
2 3
位置关系,故共有2×3=6种;其中核磁共振氢谱有4组吸收峰且峰面积之比为2∶2∶2∶1的结构简式为
,故答案为:6; ;
【小问6详解】
由题干流程图可知,根据A到B,B到C的流程信息可知,由以 为原料制备 ,由于-CH
3
为邻位上的定位基团,故可以先由 在浓硫酸和浓硝酸作用下发生硝化反应生成 ,由于由
于-NH 也易被氧化,故需先将 转化为 ,在将 转化为 ,故可
2
以确定合成路线为: 或
,故答案为: 或
15. 六氨合氯化镁(MgCl •6NH)具有极好的可逆吸、放氨特性,是一种优良的储氨材料。某研究小组以
2 3MgCl •6H O为原料在实验室制备MgCl •6NH,并测定所得产品中氯的含量
2 2 2 3
(一)制备MgCl •6NH
2 3
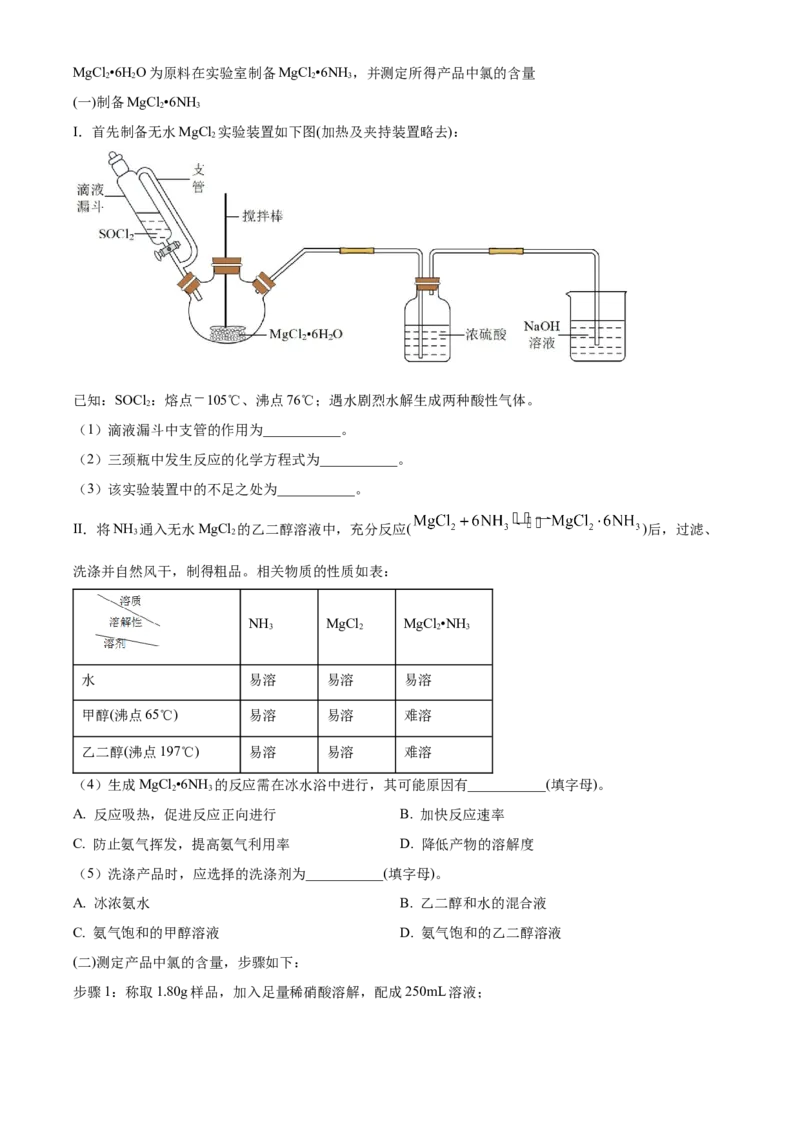
I.首先制备无水MgCl 实验装置如下图(加热及夹持装置略去):
2
已知:SOCl :熔点 105℃、沸点76℃;遇水剧烈水解生成两种酸性气体。
2
(1)滴液漏斗中支管的作用为___________。
(2)三颈瓶中发生反应的化学方程式为___________。
(3)该实验装置中的不足之处为___________。
II.将NH 通入无水MgCl 的乙二醇溶液中,充分反应( )后,过滤、
3 2
洗涤并自然风干,制得粗品。相关物质的性质如表:
NH MgCl MgCl •NH
3 2 2 3
水 易溶 易溶 易溶
甲醇(沸点65℃) 易溶 易溶 难溶
乙二醇(沸点197℃) 易溶 易溶 难溶
(4)生成MgCl •6NH 的反应需在冰水浴中进行,其可能原因有___________(填字母)。
2 3
A. 反应吸热,促进反应正向进行 B. 加快反应速率
C. 防止氨气挥发,提高氨气利用率 D. 降低产物的溶解度
(5)洗涤产品时,应选择的洗涤剂为___________(填字母)。
A. 冰浓氨水 B. 乙二醇和水的混合液
C. 氨气饱和的甲醇溶液 D. 氨气饱和的乙二醇溶液
(二)测定产品中氯的含量,步骤如下:
步骤1:称取1.80g样品,加入足量稀硝酸溶解,配成250mL溶液;步骤2:取25.00mL待测液于锥形瓶中,以KCrO 为指示剂,用0.20 的AgNO 标准液滴定溶液中
2 4 3
,记录消耗标准液的体积;
步骤3:重复步骤2操作2~3次,平均消耗标准液10.00 mL。
(6)步骒1中,用稀硝酸溶解样品的目的为___________。
(7)该品中氯的质量分数为___________(保留小数点后2位);该实验值与理论值(36.04%)有偏差,造成该
偏差的可能原因是(已知滴定操作均正确)___________。
【答案】(1)平衡压强,以使液体顺利流下
(2)
(3)缺少防倒吸措施(合理即可) (4)CD (5)C
(6)将 转化为 ,防止滴定时与 反应
(7) ①. 39.44% ②. 样品中含有 或晶体称量时已有部分氨气逸出
【解析】
【分析】先用 反应制备无水 ,然后将NH
3
通入无水MgCl 的乙二醇溶液中,发生反应 ,MgCl •6NH 难溶于乙
2 2 3
二醇,过滤出MgCl •6NH 沉淀,用氨气饱和的甲醇溶液洗涤、自然风干,制得MgCl •6NH 粗品。
2 3 2 3
【小问1详解】
滴液漏斗中支管能平衡三口烧瓶和滴液漏斗的压强,使滴液漏斗中的液体顺利流入三口烧瓶内;
【小问2详解】
三颈瓶中MgCl •6H O和SOCl 发生反应生成无水MgCl 、SO 、HCl,反应的化学方程式为
2 2 2 2 2
;
【小问3详解】
二氧化硫、氯化氢易溶于氢氧化钠溶液,易引起倒吸,该实验装置中的不足之处为缺少防倒吸措施;
【小问4详解】
A.反应吸热,降低温度,平衡逆向移动,不利于反应正向进行,故不选A;
B.降低温度,反应速率减慢,故不选B;
C.降低温度,氨气溶解度增大,反应在冰水浴中进行,可以防止氨气挥发,提高氨气利用率,故选C;D.温度越低,MgCl •6NH 的溶解度越小,反应在冰水浴中进行,可以降低产物的溶解度,有利于产物析
2 3
出,故选D;
选CD。
【小问5详解】
A.MgCl •6NH 易溶于水,不能用冰浓氨水洗涤MgCl •6NH,故不选A;
2 3 2 3
B.MgCl •6NH 易溶于水,不能用乙二醇和水的混合液洗涤MgCl •6NH,故不选B;
2 3 2 3
C.MgCl •6NH 难溶于甲醇,甲醇易挥发,可以用氨气饱和的甲醇溶液洗涤MgCl •6NH,故选C;
2 3 2 3
D.MgCl •6NH 难溶于乙二醇溶液,乙二醇难挥发,不能用氨气饱和的甲醇溶液洗涤MgCl •6NH,故不
2 3 2 3
选D;
选C。
【小问6详解】
和 能形成 ,用稀硝酸溶解样品,将 转化为 ,防止滴定时 与
反应;
【小问7详解】
用0.20 的AgNO 标准液滴定25.00mL溶液中 ,平均消耗标准液10.00 mL,根据Ag++Cl-
3
=AgCl,n(Cl-)= n(Ag+)=0.2mol/L×0.01L=0.002mol,该品中氯的质量分数为
;该实验值比理论值(36.04%)偏大,说明NH 含量少,
3
造成该偏差的可能原因是样品中含有 或晶体称量时已有部分氨气逸出。
16. 处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物 的反应为 。在 作用下该反
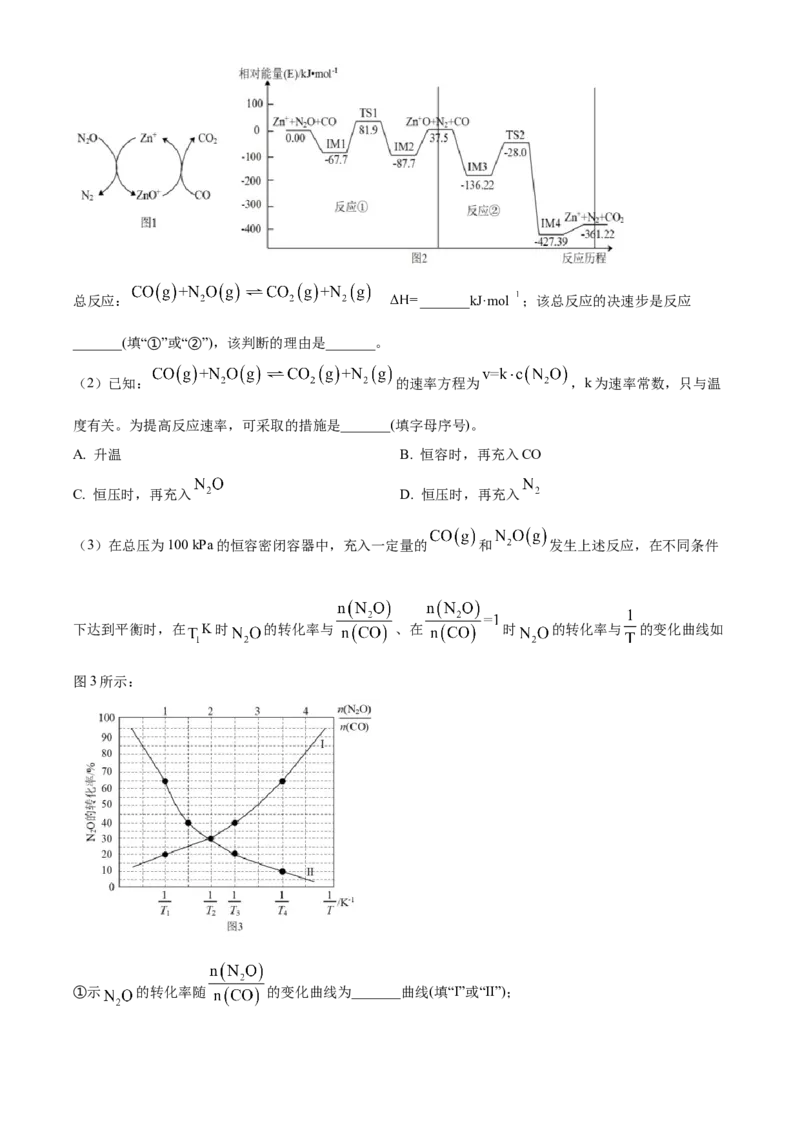
应的具体过程如图1所示,反应过程中能量变化情况如图2所示。总反应: _______kJ·mol ;该总反应的决速步是反应
_______(填“①”或“②”),该判断的理由是_______。
(2)已知: 的速率方程为 ,k为速率常数,只与温
度有关。为提高反应速率,可采取的措施是_______(填字母序号)。
A. 升温 B. 恒容时,再充入CO
C. 恒压时,再充入 D. 恒压时,再充入
(3)在总压为100 kPa的恒容密闭容器中,充入一定量的 和 发生上述反应,在不同条件
下达到平衡时,在 K时 的转化率与 、在 时 的转化率与 的变化曲线如
图3所示:
①示 的转化率随 的变化曲线为_______曲线(填“I”或“II”);② _______ (填“>”或“<”)。
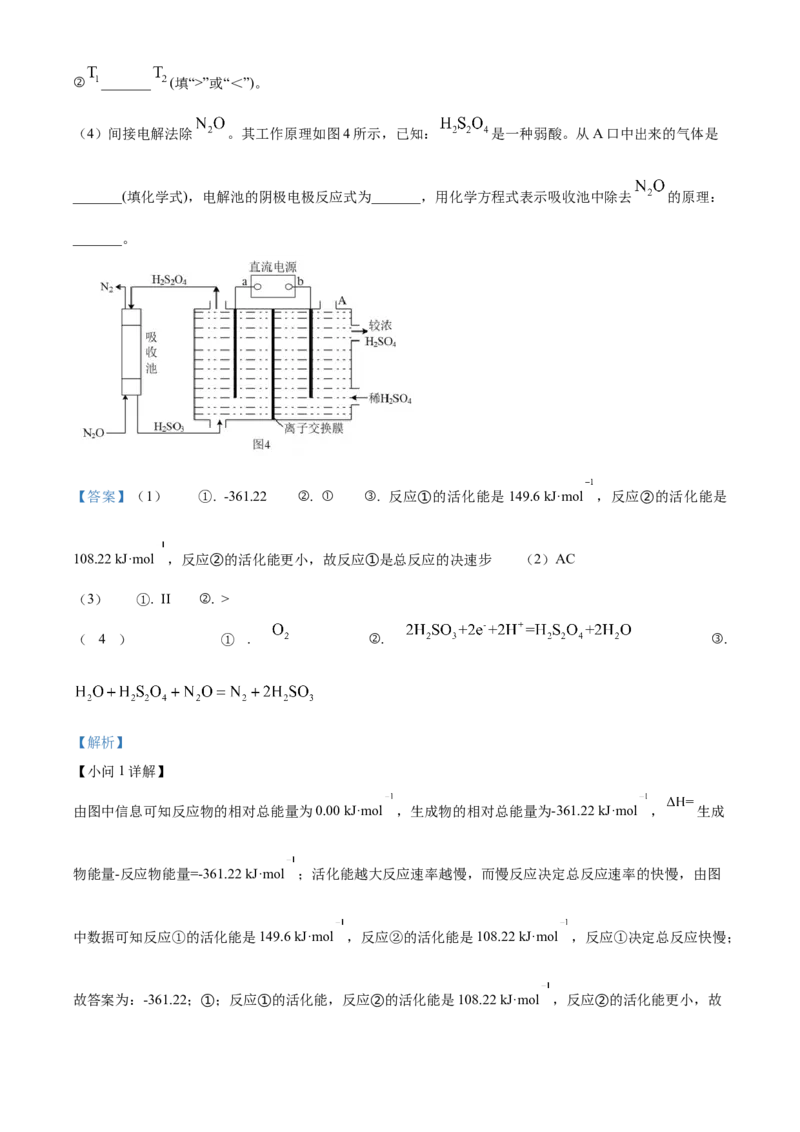
(4)间接电解法除 。其工作原理如图4所示,已知: 是一种弱酸。从A口中出来的气体是
_______(填化学式),电解池的阴极电极反应式为_______,用化学方程式表示吸收池中除去 的原理:
_______。
【答案】(1) ①. -361.22 ②. ① ③. 反应①的活化能是149.6 kJ·mol ,反应②的活化能是
108.22 kJ·mol ,反应②的活化能更小,故反应①是总反应的决速步 (2)AC
(3) ①. II ②. >
( 4 ) ① . ②. ③.
【解析】
【小问1详解】
由图中信息可知反应物的相对总能量为0.00 kJ·mol ,生成物的相对总能量为-361.22 kJ·mol , 生成
物能量-反应物能量=-361.22 kJ·mol ;活化能越大反应速率越慢,而慢反应决定总反应速率的快慢,由图
中数据可知反应①的活化能是149.6 kJ·mol ,反应②的活化能是108.22 kJ·mol ,反应①决定总反应快慢;
故答案为:-361.22;①;反应①的活化能,反应②的活化能是108.22 kJ·mol ,反应②的活化能更小,故反应①是总反应的决速步;
【小问2详解】
的
由速率方程可知,此反应 速率与温度和c( N O)有关,
2
A.升温,k增大,速率加快,A正确;
B.恒容时,再充入CO,c(NO)不变,速率不变,B错误;
2
C.恒压时,再充入NO,c(NO)增大,速率增大,C正确;
2 2
D.恒压时,再充入N,c(NO)减小,速率减慢,D错误;
2 2
故答案为:AC;
【小问3详解】
的变化越大,NO的转化率越小,故曲线II表示NO的转化率随 的变化;
2 2
②曲线I表示NO的转化率随 的变化,由于 ,则 越大,NO的转化率越大,故T>T;
2 2 1 2
故答案为:II;>;
【小问4详解】
由图可知,电解池的阳极电极反应式为 ,故从A口中出来的气体是O,电解池的
2
阴极电极反应式为 ,由装置图可知吸收池中除去NO的原理是
2
。故答案为:O; ;
2
;