文档内容
《化学反应速率与化学平衡》单元测试(培优提升)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分) 对于水煤气转换反应 ,下列条件的改变,能增大活
化分子百分数的是
A.降低温度 B.增大反应物浓度
C.恒容条件下,充入稀有气体 D.使用催化剂
2.(本题3分) 某温度下,浓度都是 的两种气体 和 ,在密闭容器中反应生成Z,反应2min后,
测得参加反应的 为 ,用 变化表示的反应速率 ,生成的
,则该反应方程式为
A. B.
C. D.
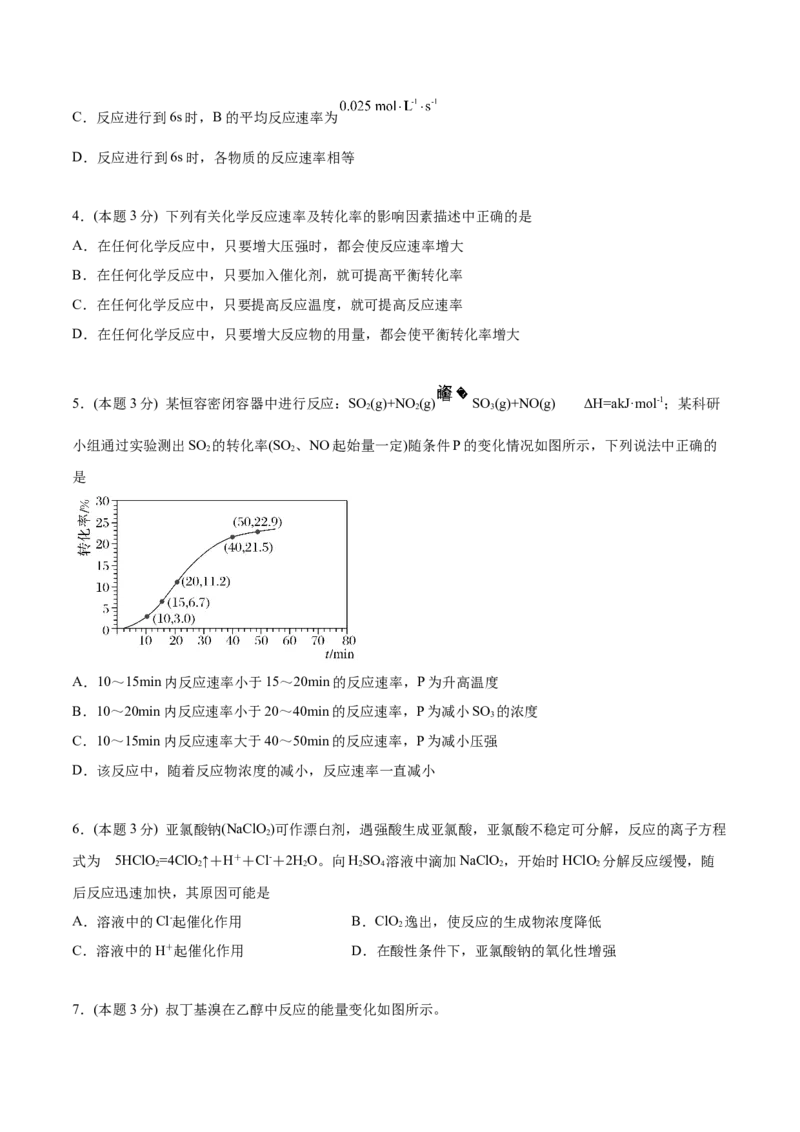
3.(本题3分) 一定温度下,向容积为4L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质
的量变化如图所示,下列对反应的推断合理的是
A.该反应的化学方程式为
B.反应进行到1s时,C.反应进行到6s时,B的平均反应速率为
D.反应进行到6s时,各物质的反应速率相等
4.(本题3分) 下列有关化学反应速率及转化率的影响因素描述中正确的是
A.在任何化学反应中,只要增大压强时,都会使反应速率增大
B.在任何化学反应中,只要加入催化剂,就可提高平衡转化率
C.在任何化学反应中,只要提高反应温度,就可提高反应速率
D.在任何化学反应中,只要增大反应物的用量,都会使平衡转化率增大
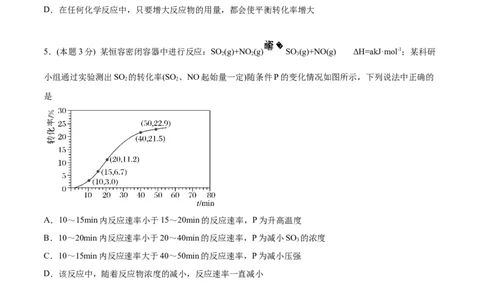
5.(本题3分) 某恒容密闭容器中进行反应:SO (g)+NO (g) SO (g)+NO(g) ΔH=akJ·mol-1;某科研
2 2 3
小组通过实验测出SO 的转化率(SO 、NO起始量一定)随条件P的变化情况如图所示,下列说法中正确的
2 2
是
A.10~15min内反应速率小于15~20min的反应速率,P为升高温度
B.10~20min内反应速率小于20~40min的反应速率,P为减小SO 的浓度
3
C.10~15min内反应速率大于40~50min的反应速率,P为减小压强
D.该反应中,随着反应物浓度的减小,反应速率一直减小
6.(本题3分) 亚氯酸钠(NaClO)可作漂白剂,遇强酸生成亚氯酸,亚氯酸不稳定可分解,反应的离子方程
2
式为 5HClO=4ClO ↑+H++Cl-+2HO。向HSO 溶液中滴加NaClO,开始时HClO 分解反应缓慢,随
2 2 2 2 4 2 2
后反应迅速加快,其原因可能是
A.溶液中的Cl-起催化作用 B.ClO 逸出,使反应的生成物浓度降低
2
C.溶液中的H+起催化作用 D.在酸性条件下,亚氯酸钠的氧化性增强
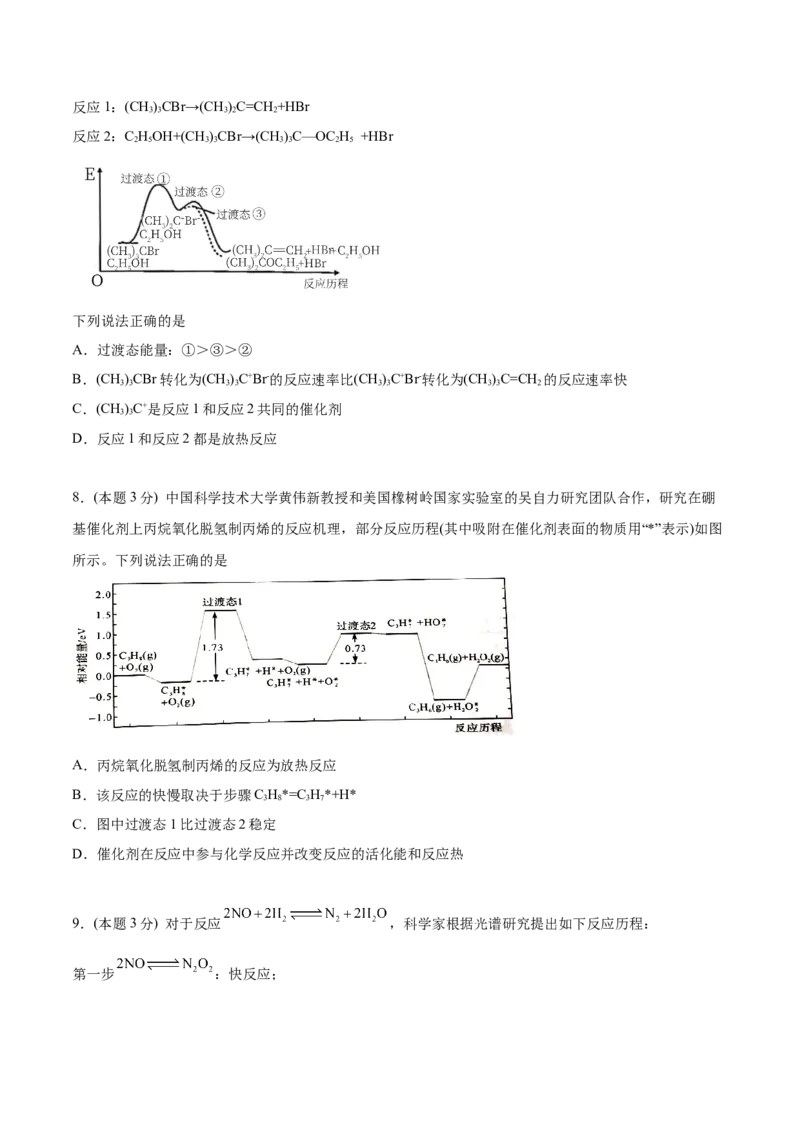
7.(本题3分) 叔丁基溴在乙醇中反应的能量变化如图所示。反应1:(CH)CBr→(CH)C=CH +HBr
3 3 3 2 2
反应2:C HOH+(CH )CBr→(CH)C—OC H +HBr
2 5 3 3 3 3 2 5
下列说法正确的是
A.过渡态能量:①>③>②
B.(CH)CBr转化为(CH)C+Br-的反应速率比(CH)C+Br-转化为(CH)C=CH 的反应速率快
3 3 3 3 3 3 3 3 2
C.(CH)C+是反应1和反应2共同的催化剂
3 3
D.反应1和反应2都是放热反应
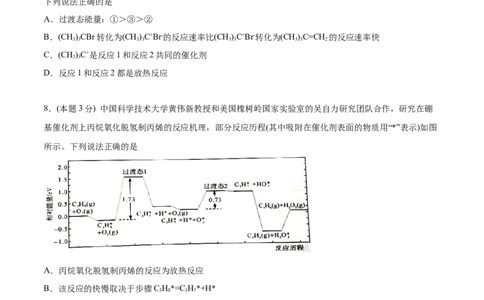
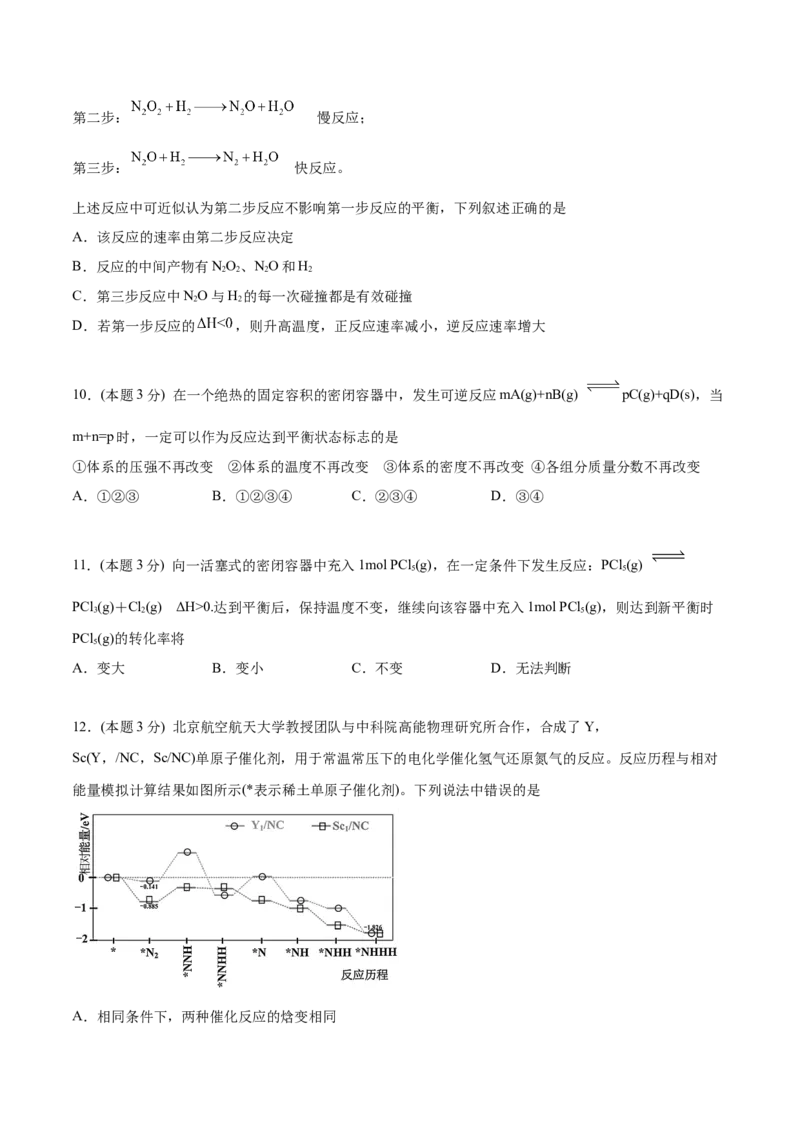
8.(本题3分) 中国科学技术大学黄伟新教授和美国橡树岭国家实验室的吴自力研究团队合作,研究在硼
基催化剂上丙烷氧化脱氢制丙烯的反应机理,部分反应历程(其中吸附在催化剂表面的物质用“*”表示)如图
所示。下列说法正确的是
A.丙烷氧化脱氢制丙烯的反应为放热反应
B.该反应的快慢取决于步骤C H*=C H*+H*
3 8 3 7
C.图中过渡态1比过渡态2稳定
D.催化剂在反应中参与化学反应并改变反应的活化能和反应热
9.(本题3分) 对于反应 ,科学家根据光谱研究提出如下反应历程:
第一步 :快反应;第二步: 慢反应;
第三步: 快反应。
上述反应中可近似认为第二步反应不影响第一步反应的平衡,下列叙述正确的是
A.该反应的速率由第二步反应决定
B.反应的中间产物有NO、NO和H
2 2 2 2
C.第三步反应中NO与H 的每一次碰撞都是有效碰撞
2 2
D.若第一步反应的 ,则升高温度,正反应速率减小,逆反应速率增大
10.(本题3分) 在一个绝热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g) pC(g)+qD(s),当
m+n=p时,一定可以作为反应达到平衡状态标志的是
①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再改变 ④各组分质量分数不再改变
A.①②③ B.①②③④ C.②③④ D.③④
11.(本题3分) 向一活塞式的密闭容器中充入1mol PCl (g),在一定条件下发生反应:PCl (g)
5 5
PCl (g)+Cl(g) ΔH>0.达到平衡后,保持温度不变,继续向该容器中充入1mol PCl (g),则达到新平衡时
3 2 5
PCl (g)的转化率将
5
A.变大 B.变小 C.不变 D.无法判断
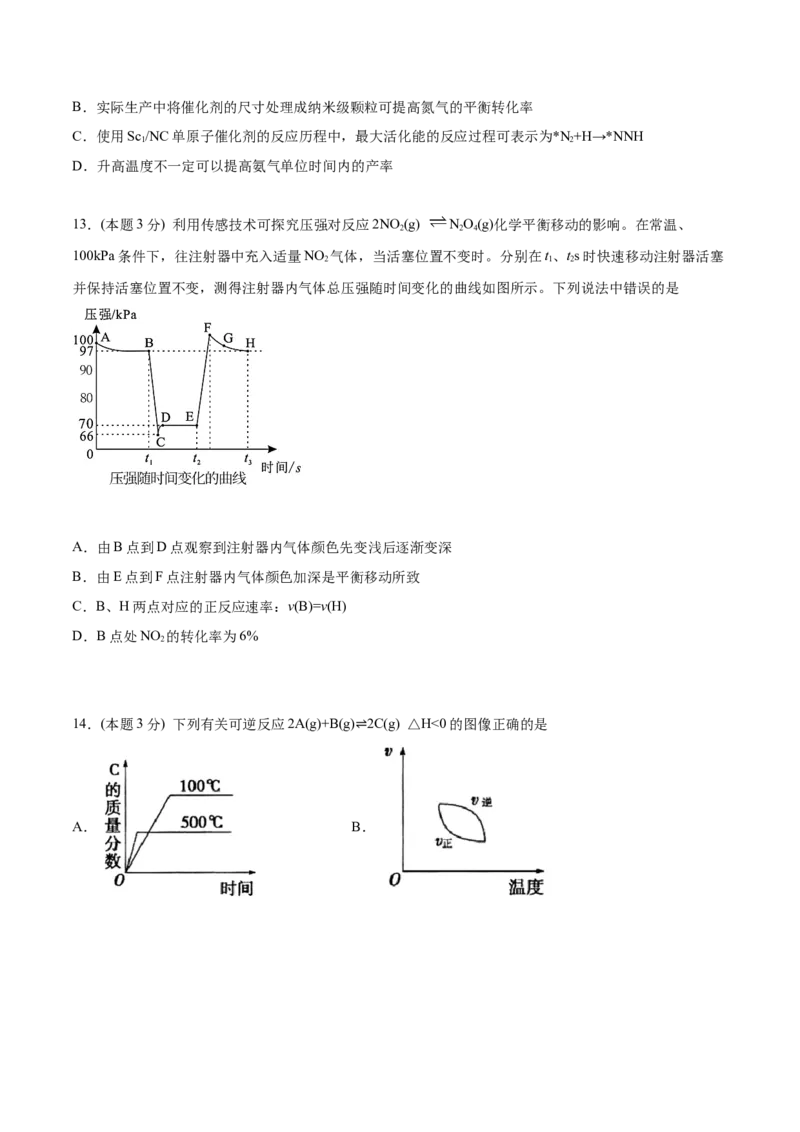
12.(本题3分) 北京航空航天大学教授团队与中科院高能物理研究所合作,合成了Y,
Sc(Y,/NC,Sc/NC)单原子催化剂,用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对
能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法中错误的是
A.相同条件下,两种催化反应的焓变相同B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氮气的平衡转化率
C.使用Sc /NC单原子催化剂的反应历程中,最大活化能的反应过程可表示为*N+H→*NNH
1 2
D.升高温度不一定可以提高氨气单位时间内的产率
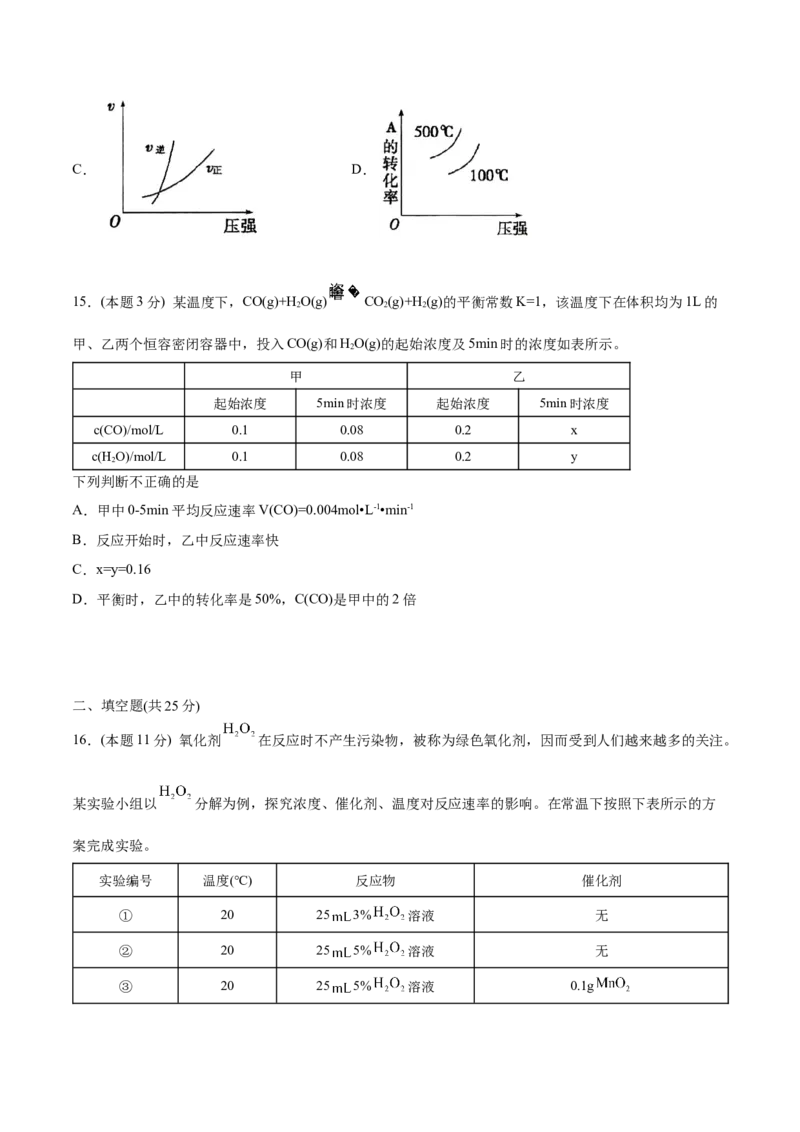
13.(本题3分) 利用传感技术可探究压强对反应2NO (g) NO(g)化学平衡移动的影响。在常温、
2 2 4
100kPa条件下,往注射器中充入适量NO 气体,当活塞位置不变时。分别在t、ts时快速移动注射器活塞
2 1 2
并保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图所示。下列说法中错误的是
A.由B点到D点观察到注射器内气体颜色先变浅后逐渐变深
B.由E点到F点注射器内气体颜色加深是平衡移动所致
C.B、H两点对应的正反应速率:v(B)=v(H)
D.B点处NO 的转化率为6%
2
14.(本题3分) 下列有关可逆反应2A(g)+B(g) 2C(g) △H<0的图像正确的是
⇌
A. B.C. D.
15.(本题3分) 某温度下,CO(g)+HO(g) CO(g)+H(g)的平衡常数K=1,该温度下在体积均为1L的
2 2 2
甲、乙两个恒容密闭容器中,投入CO(g)和HO(g)的起始浓度及5min时的浓度如表所示。
2
甲 乙
起始浓度 5min时浓度 起始浓度 5min时浓度
c(CO)/mol/L 0.1 0.08 0.2 x
c(HO)/mol/L 0.1 0.08 0.2 y
2
下列判断不正确的是
A.甲中0-5min平均反应速率V(CO)=0.004mol•L-1•min-1
B.反应开始时,乙中反应速率快
C.x=y=0.16
D.平衡时,乙中的转化率是50%,C(CO)是甲中的2倍
二、填空题(共25分)
16.(本题11分) 氧化剂 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。
某实验小组以 分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方
案完成实验。
实验编号 温度(℃) 反应物 催化剂
① 20 25 3% 溶液 无
② 20 25 5% 溶液 无
③ 20 25 5% 溶液 0.1g④ 20 25 5% 溶液 1~2滴1 溶液
⑤ 30 25 5% 溶液 0.1g
(1)实验①和②的目的是___________。同学甲在进行实验①和②时并没有观察到明显现象。资料显示,通
常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是___________(写出一种即可)。
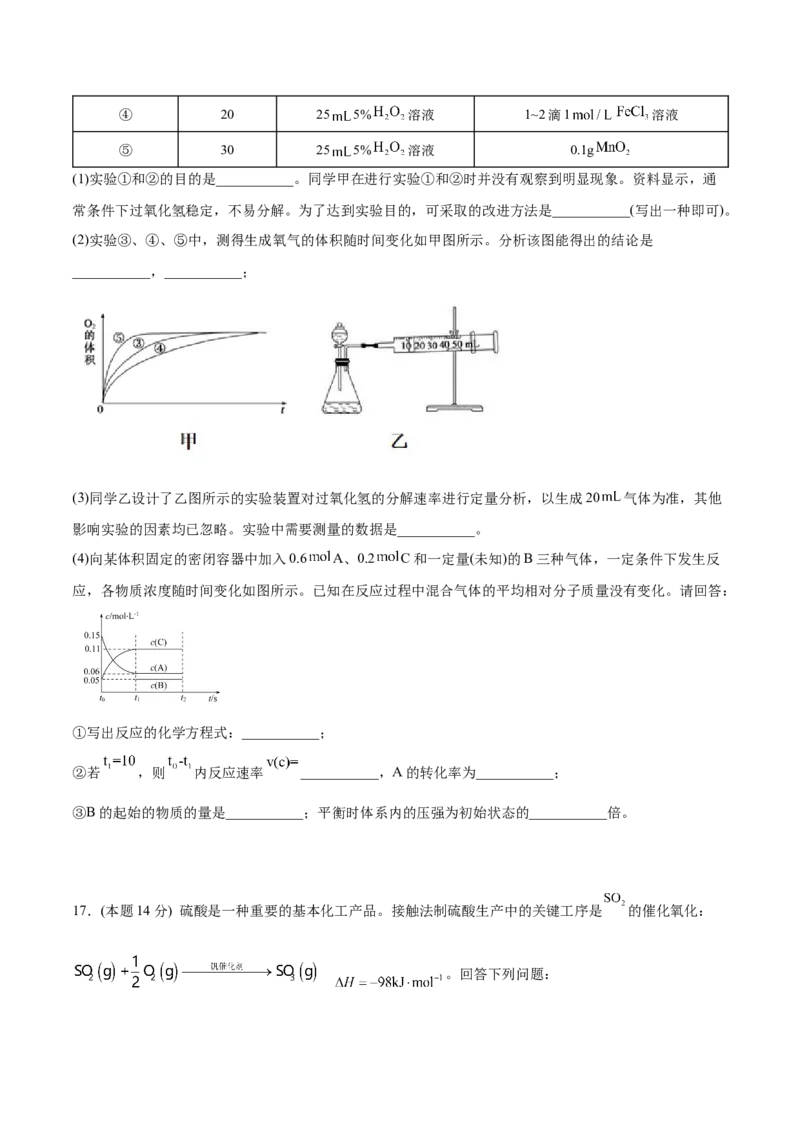
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。分析该图能得出的结论是
___________,___________;
(3)同学乙设计了乙图所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20 气体为准,其他
影响实验的因素均已忽略。实验中需要测量的数据是___________。
(4)向某体积固定的密闭容器中加入0.6 A、0.2 C和一定量(未知)的B三种气体,一定条件下发生反
应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①写出反应的化学方程式:___________;
②若 ,则 内反应速率 ___________,A的转化率为___________;
③B的起始的物质的量是___________;平衡时体系内的压强为初始状态的___________倍。
17.(本题14分) 硫酸是一种重要的基本化工产品。接触法制硫酸生产中的关键工序是 的催化氧化:
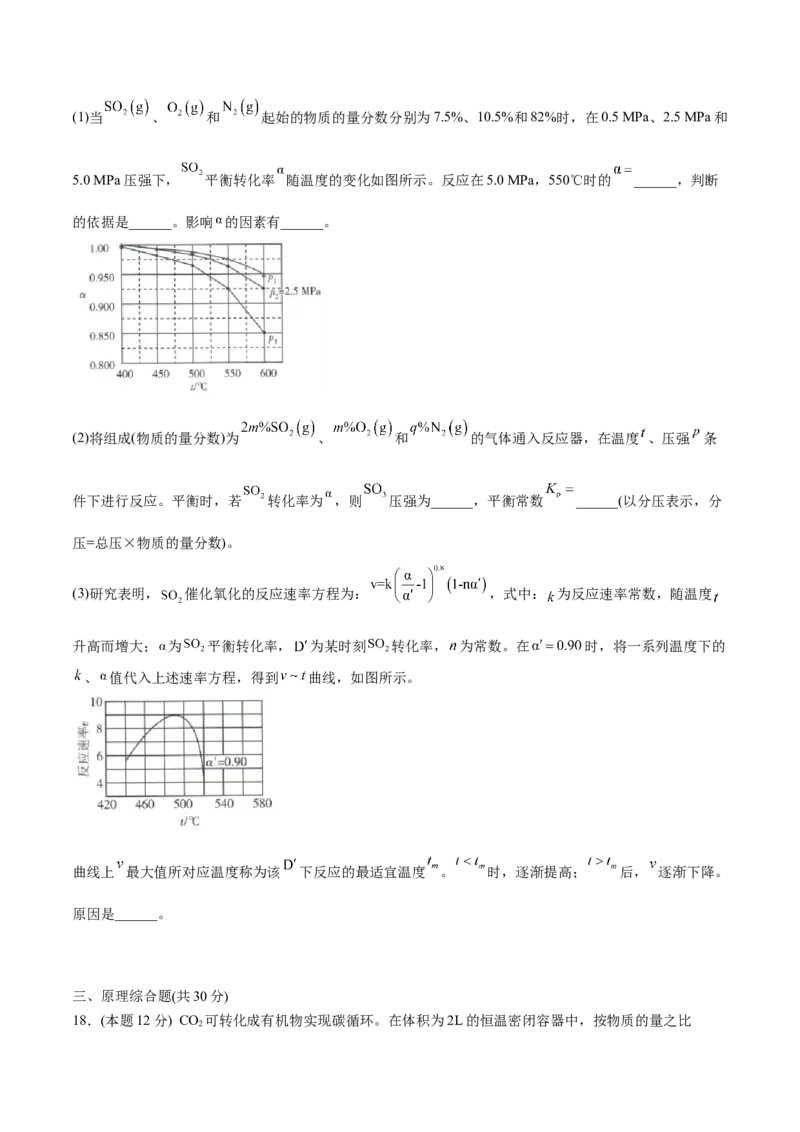
。回答下列问题:(1)当 、 和 起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5 MPa、2.5 MPa和
5.0 MPa压强下, 平衡转化率 随温度的变化如图所示。反应在5.0 MPa,550℃时的 ______,判断
的依据是______。影响 的因素有______。
(2)将组成(物质的量分数)为 、 和 的气体通入反应器,在温度 、压强 条
件下进行反应。平衡时,若 转化率为 ,则 压强为______,平衡常数 ______(以分压表示,分
压=总压×物质的量分数)。
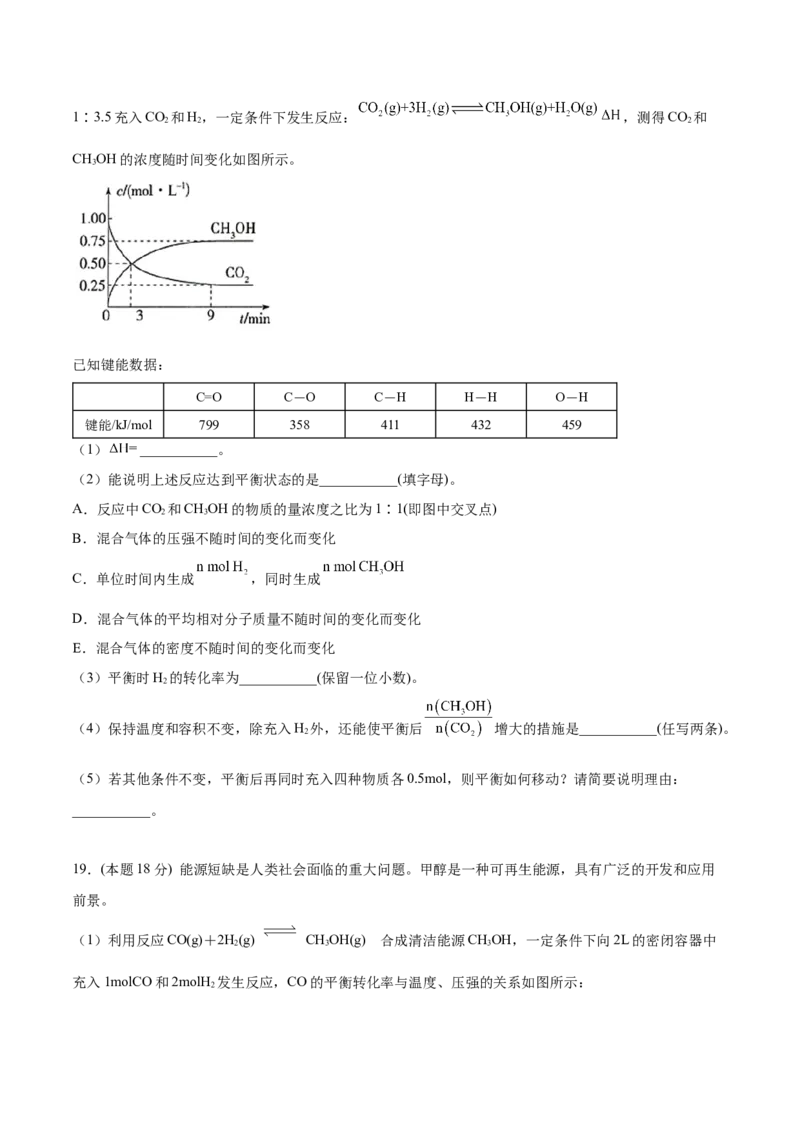
(3)研究表明, 催化氧化的反应速率方程为: ,式中: 为反应速率常数,随温度
升高而增大; 为 平衡转化率, 为某时刻 转化率, 为常数。在 时,将一系列温度下的
、 值代入上述速率方程,得到 曲线,如图所示。
曲线上 最大值所对应温度称为该 下反应的最适宜温度 。 时,逐渐提高; 后, 逐渐下降。
原因是______。
三、原理综合题(共30分)
18.(本题12分) CO 可转化成有机物实现碳循环。在体积为2L的恒温密闭容器中,按物质的量之比
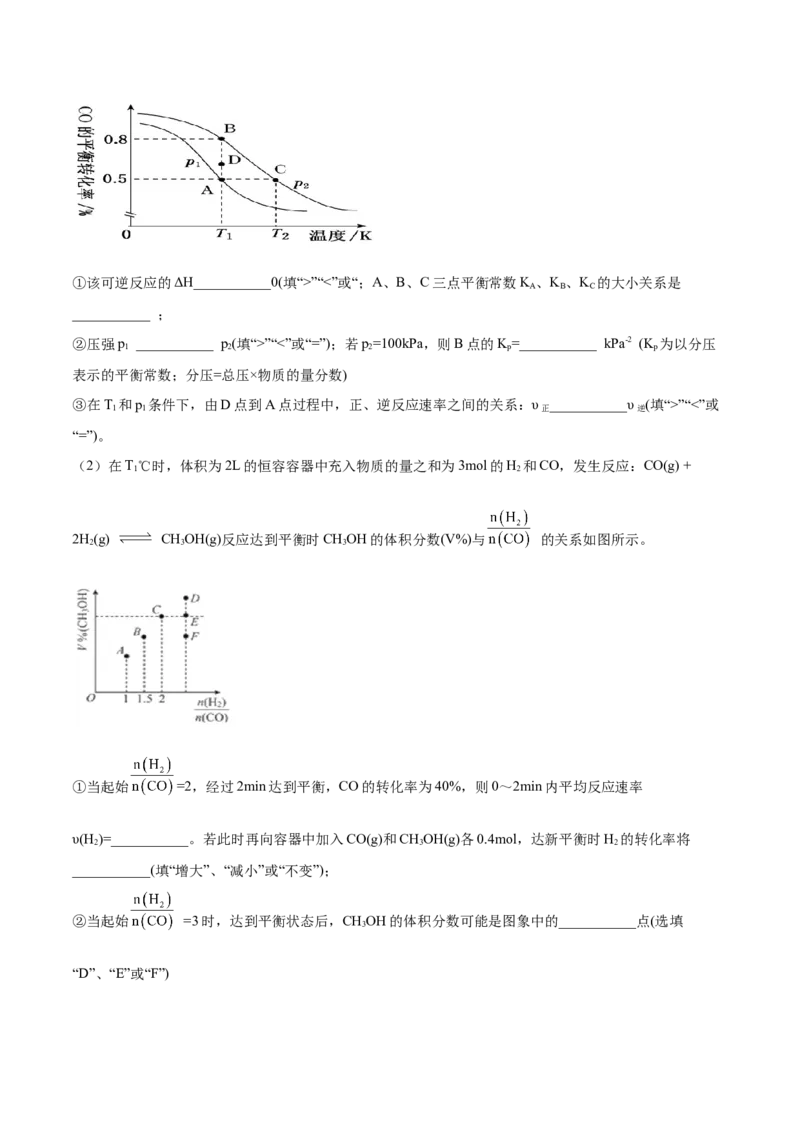
21∶3.5充入CO 和H,一定条件下发生反应: ,测得CO 和
2 2 2
CHOH的浓度随时间变化如图所示。
3
已知键能数据:
C=O C-O C-H H-H O-H
键能/kJ/mol 799 358 411 432 459
(1) ___________。
(2)能说明上述反应达到平衡状态的是___________(填字母)。
A.反应中CO 和CHOH的物质的量浓度之比为1∶1(即图中交叉点)
2 3
B.混合气体的压强不随时间的变化而变化
C.单位时间内生成 ,同时生成
D.混合气体的平均相对分子质量不随时间的变化而变化
E.混合气体的密度不随时间的变化而变化
(3)平衡时H 的转化率为___________(保留一位小数)。
2
(4)保持温度和容积不变,除充入H 外,还能使平衡后 增大的措施是___________(任写两条)。
2
(5)若其他条件不变,平衡后再同时充入四种物质各0.5mol,则平衡如何移动?请简要说明理由:
___________。
19.(本题18分) 能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用
前景。
(1)利用反应CO(g)+2H(g) CHOH(g) 合成清洁能源CHOH,一定条件下向2L的密闭容器中
2 3 3
充入1molCO和2molH 发生反应,CO的平衡转化率与温度、压强的关系如图所示:
2①该可逆反应的ΔH___________0(填“>”“<”或“;A、B、C三点平衡常数K 、K 、K 的大小关系是
A B C
___________ ;
②压强p ___________ p (填“>”“<”或“=”);若p=100kPa,则B点的K=___________ kPa-2 (K 为以分压
1 2 2 p p
表示的平衡常数;分压=总压×物质的量分数)
③在T 和p 条件下,由D点到A点过程中,正、逆反应速率之间的关系:υ ___________υ (填“>”“<”或
1 1 正 逆
“=”)。
(2)在T℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H 和CO,发生反应:CO(g) +
1 2
2H(g) CHOH(g)反应达到平衡时CHOH的体积分数(V%)与 的关系如图所示。
2 3 3
①当起始 =2,经过2min达到平衡,CO的转化率为40%,则0~2min内平均反应速率
υ(H )=___________。若此时再向容器中加入CO(g)和CHOH(g)各0.4mol,达新平衡时H 的转化率将
2 3 2
___________(填“增大”、“减小”或“不变”);
②当起始 =3时,达到平衡状态后,CHOH的体积分数可能是图象中的___________点(选填
3
“D”、“E”或“F”)倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育