文档内容
教材无机实验
(一)配制一定物质的量浓度的溶液
1.主要仪器
固体溶解配制溶液:托盘天平、烧杯、
{
玻璃棒、容量瓶、胶头滴管
溶液稀释配制溶液:量筒、烧杯、玻璃棒、
容量瓶、胶头滴管
2.注意事项
(1)容量瓶:只有一个刻度线,只能配制瓶上规定容积的溶液,若配制480 mL溶液应用500 mL容量瓶。
(2)写所用仪器时,容量瓶必须注明规格。
(3)容量瓶使用之前必须查漏。
n m
3.误差分析依据:c = B= B 。
B V M V
B
4.命题角度:一是仪器的缺失与选择,二是实验误差分析。
(二)酸碱中和滴定实验
实验说明:
(1)实验操作
①滴定前的准备工作。滴定管:查漏→水洗→润洗→装液→赶气泡→调液面→记录初始读数;
锥形瓶:水洗→装液→滴加指示剂。
②滴定。左手控制滴定管,右手不停摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。
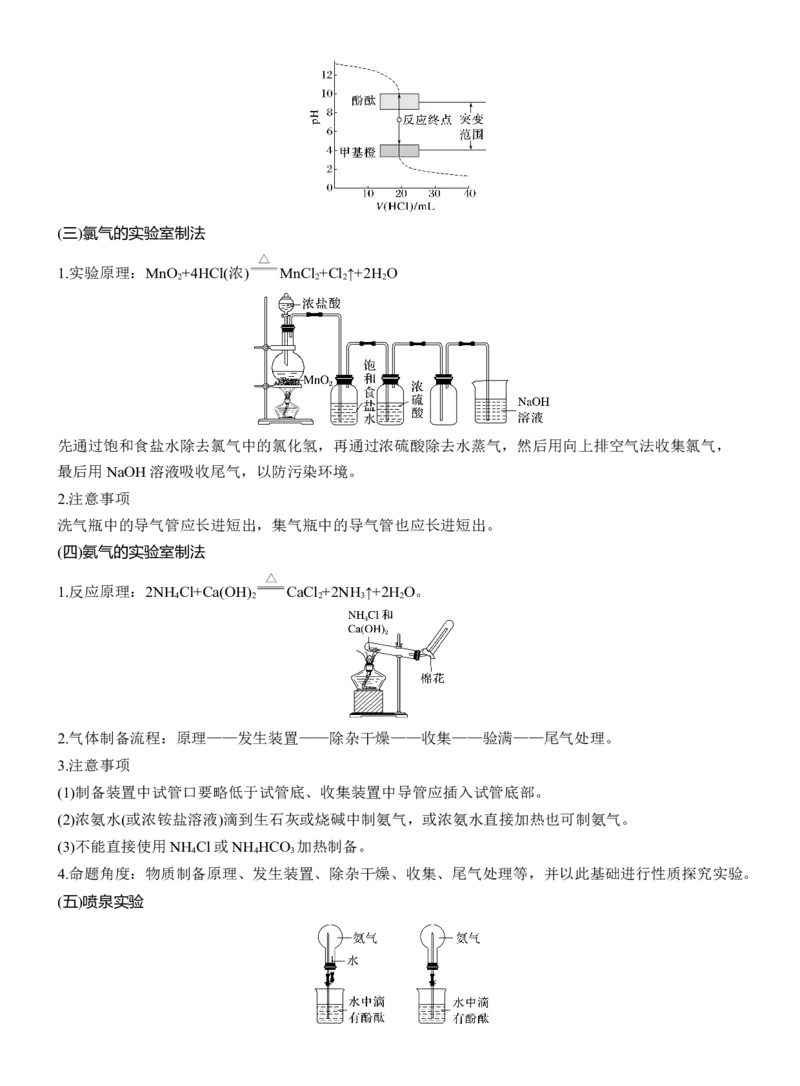
(2)滴定曲线是以酸碱中和滴定过程中滴加酸(或碱)的量为横坐标,以溶液 pH 为纵坐标绘出的一条溶
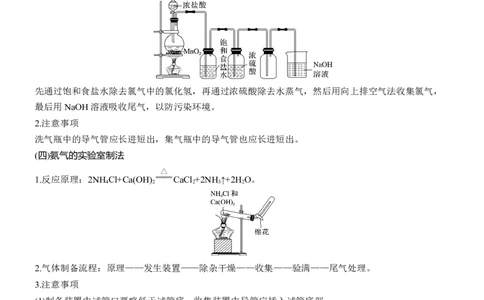
液 pH 随酸(或碱)的滴加量而变化的曲线。如图。(三)氯气的实验室制法
1.实验原理:MnO +4HCl(浓) MnCl +Cl ↑+2H O
2 2 2 2
先通过饱和食盐水除去氯气中的氯化氢,再通过浓硫酸除去水蒸气,然后用向上排空气法收集氯气,
最后用NaOH溶液吸收尾气,以防污染环境。
2.注意事项
洗气瓶中的导气管应长进短出,集气瓶中的导气管也应长进短出。
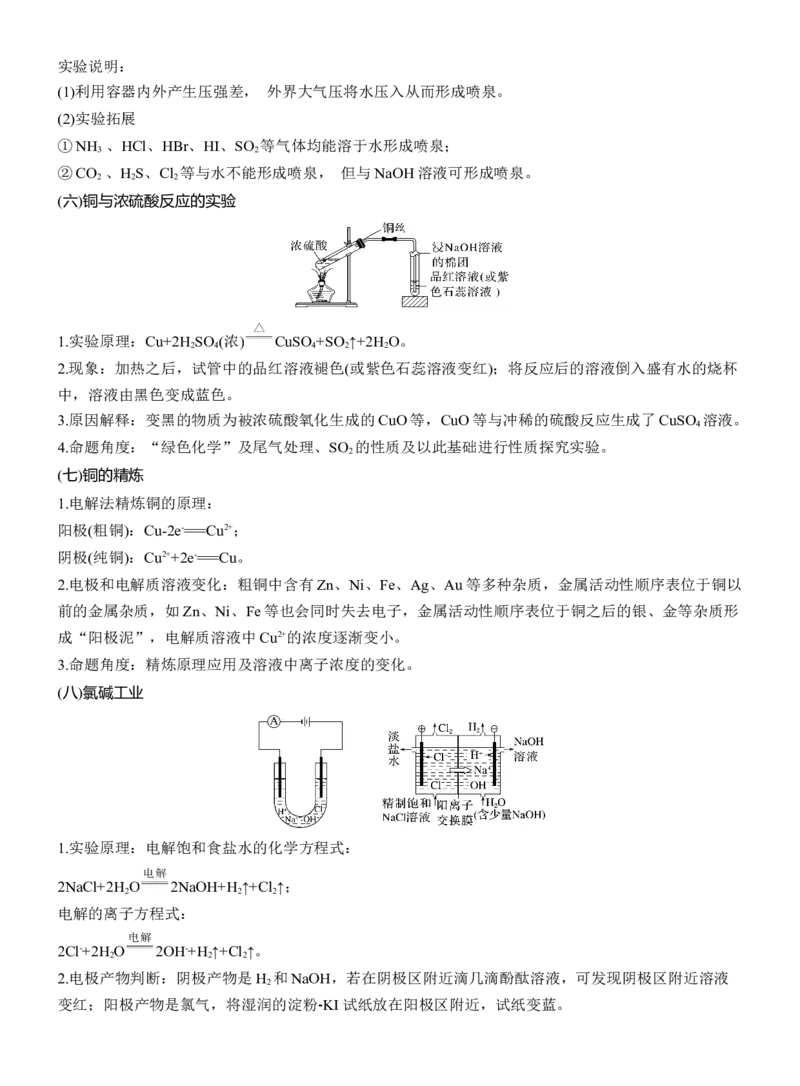
(四)氨气的实验室制法
1.反应原理:2NH Cl+Ca(OH) CaCl +2NH ↑+2H O。
4 2 2 3 2
2.气体制备流程:原理——发生装置——除杂干燥——收集——验满——尾气处理。
3.注意事项
(1)制备装置中试管口要略低于试管底、收集装置中导管应插入试管底部。
(2)浓氨水(或浓铵盐溶液)滴到生石灰或烧碱中制氨气,或浓氨水直接加热也可制氨气。
(3)不能直接使用NH Cl或NH HCO 加热制备。
4 4 3
4.命题角度:物质制备原理、发生装置、除杂干燥、收集、尾气处理等,并以此基础进行性质探究实验。
(五)喷泉实验实验说明:
(1)利用容器内外产生压强差, 外界大气压将水压入从而形成喷泉。
(2)实验拓展
①NH 、HCl、HBr、HI、SO 等气体均能溶于水形成喷泉;
3 2
②CO 、H S、Cl 等与水不能形成喷泉, 但与NaOH溶液可形成喷泉。
2 2 2
(六)铜与浓硫酸反应的实验
1.实验原理:Cu+2H SO (浓) CuSO +SO ↑+2H O。
2 4 4 2 2
2.现象:加热之后,试管中的品红溶液褪色(或紫色石蕊溶液变红);将反应后的溶液倒入盛有水的烧杯
中,溶液由黑色变成蓝色。
3.原因解释:变黑的物质为被浓硫酸氧化生成的CuO等,CuO等与冲稀的硫酸反应生成了CuSO 溶液。
4
4.命题角度:“绿色化学”及尾气处理、SO 的性质及以此基础进行性质探究实验。
2
(七)铜的精炼
1.电解法精炼铜的原理:
阳极(粗铜):Cu-2e-===Cu2+;
阴极(纯铜):Cu2++2e-===Cu。
2.电极和电解质溶液变化:粗铜中含有Zn、Ni、Fe、Ag、Au等多种杂质,金属活动性顺序表位于铜以
前的金属杂质,如Zn、Ni、Fe等也会同时失去电子,金属活动性顺序表位于铜之后的银、金等杂质形
成“阳极泥”,电解质溶液中Cu2+的浓度逐渐变小。
3.命题角度:精炼原理应用及溶液中离子浓度的变化。
(八)氯碱工业
1.实验原理:电解饱和食盐水的化学方程式:
2NaCl+2H O 2NaOH+H ↑+Cl ↑;
2 2 2
电解的离子方程式:
2Cl-+2H O 2OH-+H ↑+Cl ↑。
2 2 2
2.电极产物判断:阴极产物是H 和NaOH,若在阴极区附近滴几滴酚酞溶液,可发现阴极区附近溶液
2
变红;阳极产物是氯气,将湿润的淀粉 ⁃KI试纸放在阳极区附近,试纸变蓝。3.命题角度
(1)两极上析出产物的判断、产物的性质及相关电解原理。
(2)离子交换膜的原理和使用。