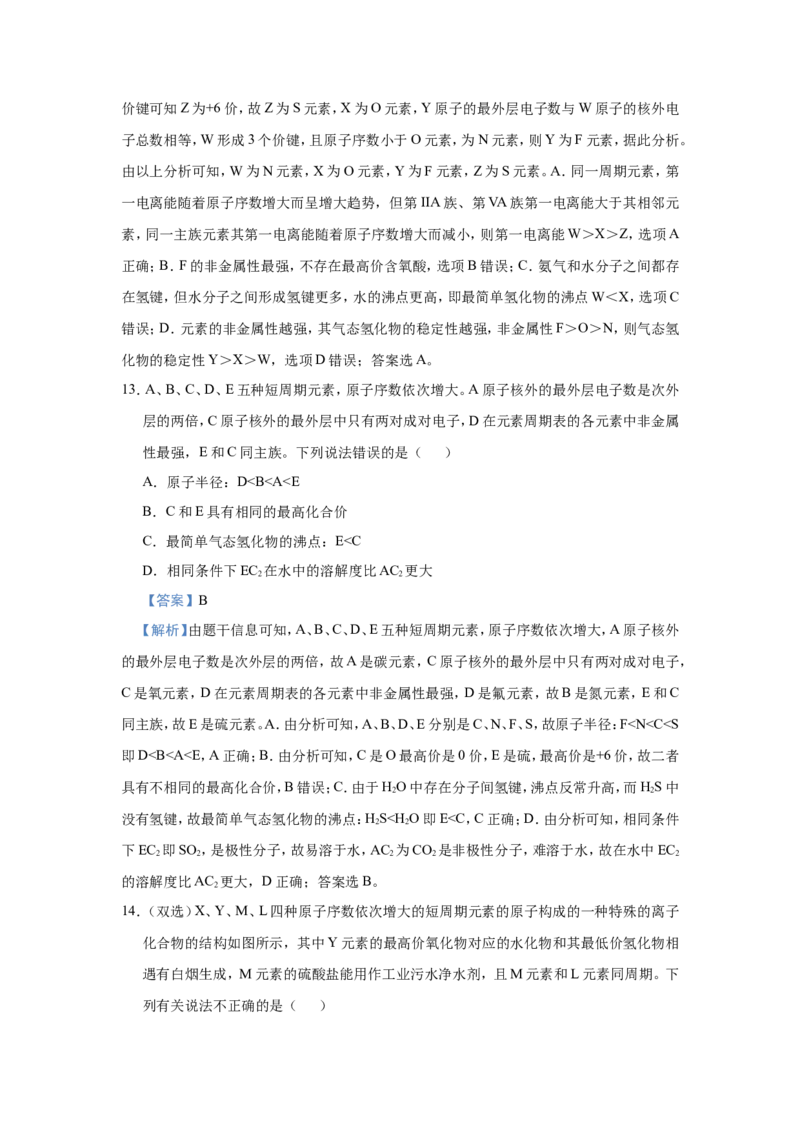文档内容
(新高考)小题必练7:原子结构与元素
性质、元素周期律的关系
原子结构和元素周期律师每年必考的重点内容,纵观近几年高考试题,主要是以元素及
其化合物知识为载体,用物质结构理论,将解释现象、定性推理、规律总结、简单计算相结合。
全方位,多层次地考查写生综合分析能力、逻辑推理能力及知识迁移应用能力。在选择题中
主要考查同位素概念、元素周期表位构性的关系,多涉及原子半径,电离能,电负性,最高价
氧化物水化物的酸碱性比较,化学键类型的判断等。
1.【2020年山东卷】短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子的电子总
数是其最高能级电子数的2倍,Z可与X形成淡黄色化合物ZX,Y、W最外层电子数相
2 2
同。下列说法正确的是( )
A.第一电离能:W>X>Y>Z B.简单离子的还原性:Y>X>W
C.简单离子的半径:W>X>Y>Z D.氢化物水溶液的酸性:Y>W
【答案】C
【解析】依据题意给出信息能推断得到X为O元素,Y为F元素,Z为Na元素,W为Cl元
素。A.同一周期从左向右第一电离能总趋势为逐渐增大,同一主族从上到下第一电离能逐渐
减小,故四种元素中第一电离能从大到小的顺序为F>O>Cl>Na,A错误;B.单质的氧化性
越强,简单离子的还原性越弱,O、F、Cl三种元素中F 的氧化性最强O 的氧化性最弱,故简
2 2
单离子的还原性O2−>Cl−>F−,B错误;C.电子层数越多简单离子半径越大,相同结构的离子,
原子序数越大半径越小,故四种元素中离子半径从大到小的顺序为Cl−>O2−>F−>Na+,C正
确;D.F元素的非金属性强于Cl元素,则形成氢化物后F原子束缚H原子的能力强于Cl原
子,在水溶液中HF不容易发生电离,故HCl的酸性强于HF,D错误;故选C。
【点睛】主要抓住元素周期律来解答此题,离子半径大小的比较时,首先核外电子层数的
大小,如若核外电子排布相同时,再看原子序数的大小,原子序数越大,半径越小。
2.【2020年天津卷】短周期元素X、Y、Z、W的原子序数依次增大。用表中信息判断下列说法
正确的是( )元素 X Y Z W
最高价氧化物的水化物 HZO
3 4
0.1mol∙L−1溶液对应的pH(25℃) 1.00 13.00 1.57 0.70
A.元素电负性:ZH-S,因此HO的沸点高于HS
2 2
B.相对分子质量HS>HO,因此HS比HO稳定
2 2 2 2
C.HO与SO 均为V形结构,因此中心原子的杂化方式相同
2 2D.得电子的能力O>S,因此O的电负性强于S
【答案】D
【解析】A.HO的沸点高于HS是因为水中含有氢键,与键能无关,故A错误;B.HS、
2 2 2
HO的稳定性与键能强弱有关,与相对分子质量无关,故B错误;C.HO为V型,是sp3杂化,
2 2
SO 为平面三角形,是sp2杂化,因此中心原子的杂化方式不同,故C错误;D.氧的原子半径
2
小于硫,因此得电子的能力O>S,所以O的电负性强于S,故D正确;故选D。
【点睛】对于气体分子的熔沸点比较,与分子间的作用力有关,相对分子质量越大,分子间
的作用力越大,熔沸点越大,还要注意有些物质中含有氢键,氢键的影响大于分子间的作用
力,故遇见氢键的情况,要仔细应对。
2.(双选)已知元素周期表中1~18号元素中的四种元素的简单离子W3+、X+、Y2-、Z-都具有
相同的电子层结构,下列判断正确的是( )
A.元素的第一电离能:X>W B.离子的还原性:Y2->Z-
C.氢化物的稳定性:HYX>Y B.元素的简单气态氧化物的热稳定性:X>Y
C.熔点:MY >MW D.Z、M的最高价氧化物对应水化物的碱性:Z>M
2 2
【答案】D
【解析】主族元素W、M、X、Y、Z的原子序数依次增大,且原子序数均不超过20,W元素
的电负性是周期表所有元素中最强的,则W为F元素;M的价电子数等于其最内层电子数,
则M为Mg元素;X的最高正价为+6价,则X为S元素;Z的原子半径是前20号主族元素中
最大的,则Z为K元素,由原子序数依次增大可知,Y为Cl元素。A.电子层结构相同的离子,
核电荷数越大,离子半径越小,钾离子、硫离子和氯离子的电子层结构相同,则简单离子半径:
X>Y>Z,故A错误;B.同周期元素,从左到右非金属性依次增强,氢化物的稳定性依次增
强,硫元素和氯元素同周期,则氯化氢的稳定性强于硫化氢,故B错误;C.离子晶体的晶格
能越大,熔点越高,氯化镁和氟化镁都是离子晶体,氟离子的离子半径小于氯离子,则氟化镁
的晶格能大于氯化镁,熔点高于氯化镁,故C错误;D.元素的金属性越强,最高价氧化物对
应水化物的碱性越强,钾元素的金属性强于镁元素,则氢氧化钾的碱性强于氢氧化镁,故D
正确;故选D。
11.已知基态X原子的3p轨道上有3个未成对电子,基态Y原子的2p轨道上有2个未成对
电子,Z元素可以形成负价离子,且三种元素的原子序数之和等于32。下列说法不正确的
是( )A.Y元素原子的电子排布图为
B.X位于元素周期表中第三周期VA族
C.电负性:Z>Y> X
D.第一电离能:XO>P,即Z>Y>X,故C正确;D.同周期自左至
右第一电离能成增大趋势,同主族元素自上而下第一电离能减小,所以第一电离能PY,B错误;C.L元素
原子的最外层电子数为7,等于Y元素的核电荷数,C正确;D.含YX的盐溶液即铵盐溶液,
和NaOH溶液混合不一定会产生大量有刺激性气味的气体即氨气,一般需要在浓氢氧化钠
加热条件下进行,D错误;答案为BD。