文档内容
专题 一
化学用语 物质的量
××
命 题 趋 势
1.了解原子结构示意图、分子式、结构式和结构简式的表示方法。
2.了解物质的量及其单位摩尔(mol)、摩尔质量、气体摩尔体积、物质的量浓度和阿伏加德罗常数的
含义。
3.根据物质的量与微粒(分子、原子、离子等)数目、气体摩尔体积(标准状况)之间的相互关系进行
相关计算。
4.了解溶液浓度的表示方法,理解溶液中溶质的质量分数和物质的量浓度的概念,并进行相关计算。
5.掌握配制一定溶质质量分数的溶液和物质的量浓度溶液的方法。
新课标全国卷命题强调知识的综合性,往往通过阿伏加德罗常数将化学基本概念、基本原理、以及元素
化合物知识与化学计量联系起来,从物质状态、物质组成、化学键、气体摩尔体积、弱电解质的电离、盐类
水解、以及氧化还原反应中电子的转移等角度设计问题。
Ⅰ.客观题
(1)考查“常数”:结合阿伏加德罗常数,以物质的组成、电解质溶液、氧化还原反应等为载体,考查摩
尔质量、气体摩尔体积、溶液浓度、电子转移数目等的简单计算。
(2)考查“实验”:结合一定物质的量浓度溶液的配制,考查仪器使用、基本操作和误差分析。
(3)考查“化学用语”:化学式、分子式、电子式、结构简式、结构示意图的判断。
Ⅱ.主观题(考查“计算”)
(1)与氧化还原反应、化学反应与能量、反应速率、平衡常数等相结合考查物质的量、物质的量浓度的相
关计算。
(2)渗透于化学工艺流程题或综合实验题中,考查物质的量浓度的相关计算。
(3)在综合题中,考查常用的化学用语及方程式的书写。
考 点 清 单
一、常用化学用语
1.常用的七种图式示例
(1)化学式:NaO、NH SO、SiO
2 4 4 2(2)分子式:C H、NH
2 4 3
(3)最简式(实验式):CH、CHO
2 2
(4)电子式HOOH 、Na+[OO]2-Na+
(5)结构式:
(6)结构简式:CHCHOH
3 2
(7)原子结构示意图:
二、常用化学计量——物质的量
1.与物质的量相关的重要定律
阿伏伽德罗定律:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。
注意:(1)使用范围:气体
(2)使用条件:同温、同压、同体积
(3)特例:标准状况下的气体摩尔体积(V =22.4L/mol)
m
质量守恒定律:参加反应的各物质质量总和等于反应后生成物的质量总和(或反应前后各原子的种类及个
数相同)。此定律是书写化学方程式及进行计算的依据。
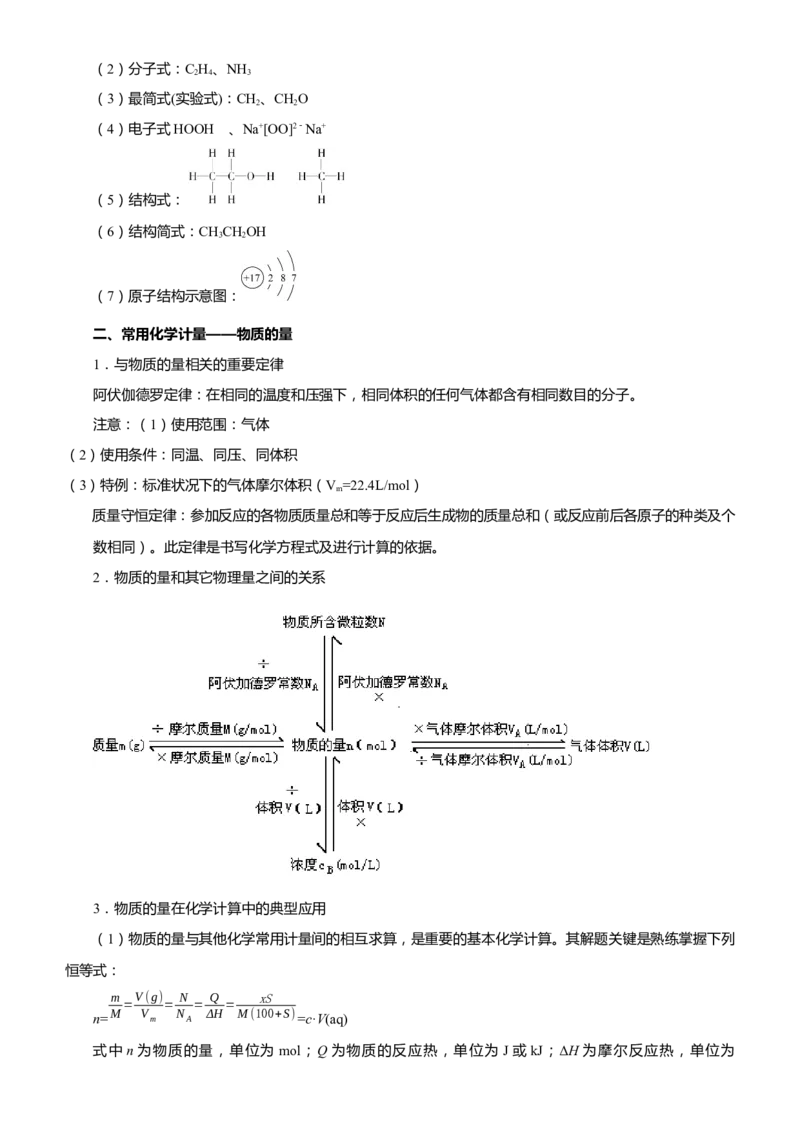
2.物质的量和其它物理量之间的关系
3.物质的量在化学计算中的典型应用
(1)物质的量与其他化学常用计量间的相互求算,是重要的基本化学计算。其解题关键是熟练掌握下列
恒等式:
m V(g) N Q xS
= = = =
n=
M V
m
N
A
ΔH M(100+S)=c·V(aq)
式中 n为物质的量,单位为 mol;Q为物质的反应热,单位为 J或kJ;ΔH为摩尔反应热,单位为kJ·mol−1;V(aq)为溶液体积,单位为L;x为饱和溶液的质量,单位为g;S为溶解度,单位为g。
(2)c、w%、ρ之间的计算关系
1000ρω%
c=
M
①计算关系:
②使用范围:同一种溶液的质量分数与物质的量浓度之间的换算
(3)有关气体定律的计算
①气体摩尔体积的计算
VL
对标准状况下的气体有n=
22.4L⋅mol−1
。
②确定气体的分子组成
一般思路是:根据阿伏加德罗定律,由体积比推导出粒子、分子个数比,再根据质量守恒定律确定化学
式。如2体积气体A 与1体积气体B 恰好完全反应生成2体积AB,由阿伏加德罗定律可知:气体的分子数
x y 2
之比等于其体积比,即A∶B ∶A B=2∶1∶2,所以两气体反应物为双原子分子,即A 和B 。
x y 2 2 2
③气体的相对分子质量的计算方法
a.已知标准状况下气体密度ρ,M=ρ·22.4 L·mol−1,M=M g·mol−1。
r
M m
A A
=
M m
b.根据阿伏加德罗定律计算: B B (同T、p、V)。精 题 集 训
(70分钟)
经典训练题
1.研究物质可从微观辨析角度认识,下列说法不正确的是( )
A.二氧化硅的分子式为SiO B.甲酸的结构式为
2
C.氯化铵的电子式为 D.核内中子数为21的K表示为 K
2.2018年11月13日第26届国际计量大会对国际单位制进行修改。规定1mol任何粒子的粒子数叫做阿伏加
德罗常数,符号为N 。若定义阿伏加德罗常数数值为B,下列有关说法正确的是( )
A
A.实验室用MnO 和浓盐酸制取氯气反应中,每生成0.1B个氯气,消耗还原剂为0.4B
2
B.0.1B个Fe加热时消耗3.36L氯气
C.78g NaO 中含有的阴离子数为B
2 2
D.1L 0.5mol/L HNO 溶液中含有的氧原子数为1.5B
3
3.设N 为阿伏加德罗常数的数值,下列说法正确的是( )
A
A.0.1mol/L的CuCl 溶液中,Cu2+数目为0.1N
2 A
B.标准状況下,2.24L乙醇分子中含有羟基(-OH)的数目为0.1N
A
C.电解精炼铜时,若阴极得到电子数为2N 个,则阳极质量减少64g
A
D.密闭容器中,2mol SO 和1mol O 催化反应生成SO 分子总数小于2N
2 2 3 A
4.在标准状况下,将22.4L HCl完全溶于1L水中(水的密度近似为1g/mL),溶液的密度为ρ g/cm3(ρ>
1),溶液的体积为VmL,溶质的质量分数为w,溶质的物质的量浓度为c mol/L。下列叙述中正确的是
( )
①w= ×100% ②c=1mol·L−1 ③向上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w ④
向上述溶液中再加入VmL水后,所得溶液的质量分数小于0.5w
A.①②③ B.①③④ C.①③ D.①④
5.甲酸钙[Ca(HCOO) ]广泛用于食品工业生产。实验室制取甲酸钙方法之一是将氢氧化钙和甲醛溶液依次加
2
入质量分数为30%~70%的过氧化氢溶液中。下列说法错误的是( )
A.参加反应的氧化剂与还原剂的物质的量之比为1∶1
B.每生成26g甲酸钙,反应转移的电子数为0.4N
A
C.该反应中被还原的元素只有OD.氧化性:HO>Ca(HCOO)
2 2 2
6.(双选)向13.6g由Cu和Cu O组成的混合物中加入一定浓度的稀硝酸250mL,当固体物质完全溶解后生
2
成Cu(NO ) 和NO气体。在所得溶液中加入1.0L 0.5mol/L NaOH溶液,生成沉淀质量为19.6g,此时溶液
3 2
呈中性且金属离子已完全沉淀。下列说法正确的是( )
A.原固体混合物中Cu与Cu O的物质的量之比为2∶1
2
B.原稀硝酸中HNO 的物质的量浓度为1.3mol/L
3
C.产生的标准状况下的NO体积为2.24L
D.Cu、Cu O与硝酸反应后剩余HNO 为0.4mol
2 3
高频易错题
1.用N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.所含共价键数目均为0.4N 的白磷( )和甲烷的物质的量相等
A
B.向FeI 溶液中通入适量Cl,当有1mol Fe2+被氧化时,反应转移的电子数为3N
2 2 A
C.通入了1mol Cl 的新制氯水中,HClO、Cl−、ClO−粒子数目之和为2N
2 A
D.常温下,向1L 0.1mol·L−1醋酸钠溶液中加入醋酸至中性,则溶液中CHCOO−的数目为0.1N
3 A
2.下列化学用语正确的是( )
A.中子数为18的氯原子: Cl B.CO 分子的电子式:
2
C.顺-2-丁烯的结构简式: D.铝离子的结构示意图:
3.(双选)用N 表示阿伏加德罗常数,下列叙述正确的是( )
A
A.标准状况下,18g HO含有的分子数为N
2 A
B.常温常压下,16g O 和O 的混合气体中氧原子的数目为N
2 3 A
C.通常状况下,N 个CO 分子占有的体积为22.4L
A 2
D.物质的量浓度为0.5mol/L的MgCl 溶液中,含有Cl−个数为N
2 A
4.Cu(NO ) 受热分解的方程式为2Cu(NO )=2CuO+4NO ↑+O ↑,将所得气体充满一干燥烧瓶(标准状况),再
3 2 3 2 2 2
将烧瓶倒置于水中,过较长时间后,烧瓶中溶液的物质的量浓度可能为(假设烧瓶中的溶质不扩散到外面)
( )
A.1/28mol/L B.1/14mol/L C.0mol/L D.1/22.4mol/L
5.(双选)设N 为阿伏加德罗常数的值,下列说法不正确的是( )
A
A.2.3g金属钠与氧气完全反应生成NaO与NaO 混合物,转移的电子数目为0.1N
2 2 2 A
B.1.6g O 和O 混合气体中所含的分子数目为0.1N
2 3 AC.1L 0.1mol/L CuCl 溶液中Cu2+的数目小于0.1N
2 A
D.标准状况下,11.2L SO 完全溶于水后配成的稀溶液中所含SO的数目为0.5N
3 A
精准预测题
1.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1mol NH F晶体中含有的共价键数目为3N
4 A
B.CH 和C H 混合气体2.24L(标准状况)完全燃烧,则消耗O 分子数目为0.25N
4 2 4 2 A
C.向100mL 0.10mol·L−1 FeCl 溶液中加入足量Cu粉充分反应,转移电子数目为0.01N
3 A
D.0.1mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目为0.1N
3 3 2 3 2 3 A
2.SCl 在工业生产中有着广泛的用途。已知:12SCl +16H O=S+24HCl+4H SO ,下列叙述正确的是( )
2 2 2 8 2 4
A.S2−和Cl−的结构示意图都可以表示为
B.SCl 的电子式是
2
C.水的比例模型是
D.S 中硫原子最外层均满足8电子稳定结构,其结构式可表示为S﹣S﹣S﹣S﹣S﹣S﹣S﹣S
8
3.(双选)工业上,可将Cl 通入石灰乳中制备漂白粉,发生反应:2Cl+2Ca(OH) =CaCl +Ca(ClO) +2HO。
2 2 2 2 2 2
用N 表示阿伏加德罗常数的值,下列说法不正确的是( )
A
A.22.4L Cl 中含有2N 个氯原子
2 A
B.反应中每生成1.8g HO就会转移0.1N 电子
2 A
C.0.1mol∙L−1的Ca(ClO) 溶液中ClO−的数目为0.2N
2 A
D.常温下,1L pH=12的Ca(OH) 溶液中OH−的数目为0.01N
2 A
4.同温同压,不同体积的密闭容器中分别有相同质量的甲、乙两种气体,且甲的密度大于乙的密度。下列分
析正确的是( )
A.物质的量:甲>乙 B.分子数:甲<乙
C.摩尔体积:甲<乙 D.摩尔质量:甲<乙
5.磷有多种同素异形体,其中白磷和黑磷(每一个层由曲折的磷原子链组成)的结构如图所示,设N 为阿伏
A
加德罗常数的值。下列说法不正确的是( )A.3.1g 31P中含有的中子数为1.6N
A
B.31g白磷与31g黑磷中含有的P—P键数目均为1.5N
A
C.12.4g白磷与0.6mol H 在密闭容器中充分反应,生成的PH 分子数为0.4N
2 3 A
D.6.82g白磷发生反应: ,转移的电子数为0.6N
A
6.某同学购买了一瓶“84消毒液”,包装说明如下:
请根据以上信息和相关知识判断,下列分析不正确的是( )
A.该“84消毒液”的物质的量浓度约为4.0mol·L−1
B.一瓶该“84消毒液”敞口放置一段时间后浓度会变小
C.取100mL该“84消毒液”稀释100倍消毒,稀释后溶液中c(Na+)约为0.04mol·L−1
D.参阅该“84消毒液”的配方,欲用NaClO固体配制含25% NaClO的消毒液480mL,需要称量的
NaClO固体质量为143g
7.将一定量的锌与100mL 18.5mol/L浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6 L(标准状况)。将
反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol/L,则下列叙述中错误的是( )
A.反应中共转移电子3mol
B.反应中共消耗锌97.5g
C.相同条件下气体A中SO 与H 的体积比为1∶4
2 2
D.气体A不能使溴水退色
8.设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.2.0g重水(D 16O)和14ND 的混合物中含有的电子数为N
2 3 A
B.1mol Fe(CO) 中的σ键数为5N
5 A
C.一定量铁粉溶于1.0L 0.4mol/L的稀硝酸溶液中,当生成2.24L NO气体时,溶液中的氮原子数为0.3N
A
D.卤素性质相似,标况下,体积分别为1.12L的HCl和HF中所含分子数都约是0.05N
A9.设N 为阿伏加德罗常数的值。已知反应:NaS+(x-1)S=Na S(x≤5),下列说法正确的是( )
A 2 2 x
A.1mol S2−所含电子数为8N B.1mol/L Na S溶液中,S2−的数目为N
A 2 A
C.7.8g Na S固体所含离子数为0.3N D.1mol Na S最多溶解S原子的数目为5N
2 A 2 A
10.碱式碳酸铝镁[MgAl (OH)(CO)·xH O]常用作塑料阻燃剂。
a b c 3 d 2
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和_________。
(2)MgAl (OH)(CO)·xH O中a、b、c、d的代数关系式为_________________。
a b c 3 d 2
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO 0.560L(已换算成标准状况下)。②另取一定量
2
样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如
右图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)。
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH−)∶n(CO)(写出计算过程)________。
11.卫生部发出公告,禁止在面粉生产中添加过氧化钙(CaO)等食品添加剂。过氧化钙(CaO)是一种安全无毒
2 2
物质,带有结晶水,通常还含有CaO,过氧化钙(CaO)与过氧化钠(Na O)性质相似,都会与HO和酸反
2 2 2 2
应。
(1)下列对于过氧化钙(CaO)的叙述错误的是______。
2
A.CaO 具有氧化性,对面粉可能具有增白作用
2
B.CaO 中阴阳离子的个数比为1∶1
2
C.CaO 和水反应时,每产生1mol O 转移电子4mol
2 2
D.CaO 和CO 反应的化学方程式为:2CaO+2CO =2CaCO +O
2 2 2 2 3 2
(2)写出过氧化钙(CaO)与盐酸反应的离子方程式______________________。
2
(3)某化学学习小组为测定过氧化钙样品(含有CaO杂质)中过氧化钙的结晶水的数目,做如下实验:
实验一:称取5.42g过氧化钙样品,灼热时发生如下反应:2[CaO·xH O]=2CaO+O ↑+2xH O,得到O
2 2 2 2 2在标准状况下体积为672mL。
实验二:另取同一样品5.42g,溶于适量稀盐酸中,然后加入足量的NaCO 溶液,将溶液中Ca2+全部转化
2 3
为CaCO 沉淀,得到干燥的CaCO 7.0g。
3 3
①5.42g过氧化钙样品中CaO 的物质的量为______。
2
②该样品中CaO·xH O的x值为______。
2 2
12.硫代硫酸钠晶体(Na SO∙5H O)又名大苏打、海波,易溶于水,难溶于乙醇,在中性或碱性溶液中较稳
2 2 3 2
定,酸性溶液中产生浑浊,广泛应用于日常生产生活中。某小组设计了如下实验装置制备NaSO(夹持仪
2 2 3
器略),总反应为2NaS+Na CO+4SO=3Na SO+CO 。回答下列问题:
2 2 3 2 2 2 3 2
(1)烧瓶B中制备SO 的化学方程式为_______。
2
(2)当pH计读数接近7.0时,应立即停止通SO 的原因_______(用离子方程式表示),具体操作是_______。
2
(3)准确称取1.4g产品,加入20mL刚煮沸并冷却过的蒸馏水,使其完全溶解,以淀粉作指示剂,用
0.1000mol∙L−1标准碘的水溶液滴定。已知:2SO+I (aq)=S O(无色)+2I−(aq)。
2 2 4
①标准碘的水溶液应盛放在_______(填“酸式”或“碱式”)滴定管中。
②第一次滴定开始和结束时,滴定管中的液面如图所示,则第一次消耗标准碘的水溶液的体积为
_______mL。
③重复上述操作三次,记录另两次数据如下表,则产品中NaSO∙5H O的质量分数为_______%(保留1位
2 2 3 2
小数)。
滴定次数 滴定前刻度/mL 滴定前刻度/mL
第二次 1.56 30.30
第三次 0.22 26.34参 考 答 案
经典训练题
1.【答案】A
【解析】A.SiO 由原子构成,不存在SiO 分子,A错误;B.甲酸中存在H原子和羧基,甲酸的结构式
2 2
为 ,B正确;C.氯化铵有铵根离子和氯离子构成,氯化铵的电子式为 ,C正确;D.
中子数为21的K原子的质量数为19+21=40,因此这种K原子的原子符号为 K,D正确;故答案选A。
2.【答案】C
【解析】A.MnO 和浓盐酸制取氯气的化学方程式为MnO +4HCl(浓)====MnCl +2H O+Cl ↑,由反应可
2 2 2 2 2
知,反应物HCl表现还原性和酸性,每生成1mol氯气,消耗还原剂为2mol,则每生成0.1B个氯气,消耗还
原剂为0.2B,故A错误;B.铁和氯气加热时反应生成氯化铁,1molFe消耗1.5mol氯气,则0.1B个Fe加热
时消耗标况下3.36L氯气,由于没有指明是在标况下,故B错误;C.78gNaO 的物质的量为n=
2 2
=1mol,NaO 中含Na+、O,则1mol Na O 中含阴离子数为B,故C正确;D.1L 0.5mol/L HNO 溶液中含
2 2 2 2 3
HNO 的物质的量为0.5mol/L 1L=0.5mol,1个硝酸分子中含有3个氧原子,0.5mol HNO 中含有的氧原子数
3 3
为1.5B,但水分子中也含有氧原子,故D错误;答案选C。
3.【答案】D
【解析】A.溶液体积不明确,故溶液中的铜离子的个数无法计算,故A错误;B.标况下乙醇为液态,
故不能根据气体摩尔体积来计算其物质的量和羟基数,故B错误;C.电解精炼铜时,粗铜为阳极,含有杂
质锌、铁、镍、金、银等杂质,当阴极得到电子数为2N 个故时,无法确定阳极减少的质量,故C错误;
A
D.该反应为可逆反应,无法进行到底,则生成的分子总数小于2N ,故D正确;故选D。
A
4.【答案】C
【解析】根据c= 可得w= ×100%,故①正确;36.5g HCl的物质的量为1mol,1mol氯化氢溶
解在1L水中,所得溶液体积不是1L,浓度不是1mol/L,故②错误;③盐酸的密度大于水的密度,则加入等
体积的水后,由于水的质量小于原盐酸的质量,根据质量分数公式可知混合液的总质量小于原先的 2倍,则
混合液中溶质的质量分数大于原溶液的 1半,即大于0.5w,故③正确、④错误;所以正确的为①③,故选C。
5.【答案】B
【解析】将氢氧化钙和甲醛溶液依次加入质量分数为 30%∼70%的过氧化氢溶液中,生成Ca(HCOO) 和
2
HO,其反应的方程式为:Ca(OH) +2HCHO+2H O=Ca(HCOO) +4H O。A.根据氢氧化钙和甲醛溶液反应的
2 2 2 2 2 2
化学方程式Ca(OH) +2HCHO+2H O=Ca(HCOO) +4H O可知,甲醛中碳元素的化合价为0价,生成物甲酸钙
2 2 2 2 2
中碳元素的化合价为+2价,两个碳原子的化合价升高,甲醛作还原剂;过氧化氢中氧元素的化合价从-1价降
低到-2价,四个氧原子的化合价降低,作氧化剂,参加反应的氧化剂与还原剂的系数都为 2,故物质的量之
比 为 1∶1 , 故 A 不 符 合 题 意 ; B . 根 据 氢 氧 化 钙 和 甲 醛 溶 液 反 应 的 化 学 方 程 式
Ca(OH) +2HCHO+2H O=Ca(HCOO)
2 2 2 2
+4H O可知,由A项分析,每生成1mol甲酸钙转移的电子数为4mol,每生成26g甲酸钙,即甲酸钙的物质
2
的量n= = =0.2mol,反应转移的电子数为0.8N ,故B符合题意;C.根据A项分析,该反应中
A
过氧化氢中氧元素的化合价降低,被还原的元素只有O,故C不符合题意;D.根据A项分析,HO 是氧化
2 2
剂,Ca(HCOO) 是氧化产物,氧化剂的氧化性大于氧化产物,氧化性:HO >Ca(HCOO) ,故D不符合题
2 2 2 2
意;答案选B。
6.【答案】AC
【解析】A.向所得溶液中加入0.5mol/L的NaOH溶液1L,溶液呈中性,金属离子已完全沉淀,此时溶
液中溶质为NaNO ,n(NaNO )=n(NaOH)=0.5mol/L×1L=0.5mol,沉淀为Cu(OH) ,质量为19.6g,其物质的量
3 3 2
为:19.6g÷98g/mol=0.2mol,根据铜元素守恒有n(Cu)+2n(Cu O)=n[Cu(OH) ]。设Cu和Cu O的物质的量分别
2 2 2
为 xmol、ymol,根据二者质量有 64x+144y=13.6,根据铜元素守恒有 x+2y=0.2,联立方程解得 x=0.1,
y=0.05,则:n(Cu)∶n(Cu O)=0.1mol∶0.05mol=2∶1,故 A 正确;B.根据 N 元素守恒可知 n(HNO)=n(NO)
2 3
+n(NaNO ),根据电子转移守恒可知:3n(NO)=2n(Cu)+2n(Cu O),所以3n(NO)=2×0.1mol+2×0.05mol,解得
3 2
n(NO)=0.1mol , 根 据 Na 元 素 可 知 n(NaNO )=n(NaOH)=0.5mol/L×1L=0.5mol , 所 以 n(HNO)=n(NO)
3 3
+n(NaNO )=0.1mol+0.5mol=
3
0.6mol,所以原硝酸溶液的浓度为:0.6mol÷0.25L=2.4mol/L,故 B 错误;C.由 B 中计算可知
n(NO)=0.1mol,标准状况下,即NO的体积为0.1mol×22.4L/mol=2.24L,故C正确;D.反应后的溶液中加入
氢氧化钠溶液,氢氧化钠与硝酸铜反应,剩余的氢氧化钠与硝酸反应,最后为硝酸钠溶液,根据氮元素守恒
可 知 反 应 后 溶 液 中 知 n (HNO)+2n[[Cu(NO )]=n(NaNO ) , 所 以 n (HNO)=n(NaNO )-
剩 余 3 3 2 3 剩 余 3 3
2n[[Cu(NO )]=0.5mol-2×0.2mol=0.1mol,故D错误;故选:AC。
3 2
高频易错题
1.【答案】D【解析】A.白磷分子内有6个共价键、甲烷分子内有4个共价键,故所含共价键数目均为0.4N 的白磷(
A
)和甲烷的物质的量不相等,A错误;B.碘离子的还原性大于亚铁离子,向FeI 溶液中通入适量Cl ,
2 2
碘离子先被氧化,当有1mol Fe2+被氧化时,已有I−被氧化,但不知道碘离子的物质的量,故无法计算转移的
电子数,B错误;C.通入了1mol Cl 的新制氯水中,氯气和水的反应是可逆反应,氯水中还有氯气存在,
2
则HClO、Cl−、ClO−粒子数目之和小于2N ,C错误;D.常温下,向1L 0.1mol·L−1醋酸钠溶液中加入醋酸至
A
中 性 , 则 , 根 据 核 电 荷 数 可 知 :
,则溶液中CHCOO−的数目等于钠离子的数目,为0.1N ,D正确;答案选D。
3 A
2.【答案】C
【解析】A.中子数为18的氯原子的质量数(A)=质子数(Z)+中子数(N)=17+18=35,该核素的符号为 ,
故A错误;B.CO 是共价化合物,C原子与每个O原子形成两对共用电子对,其结构式为O=C=O,其电子
2
式为 ,故B错误;C.顺—2—丁烯,主链为丁烯,碳碳双键在2号C,两个甲基位于双键的同
侧,结构简式为 ,故C正确;D.铝的原子序数为13,核内13个质子,核外13个电子,铝原子
失去最外层的三个电子即形成了铝离子,质子数不变,核外只有10个电子,铝离子的结构示意图为 ,
故D错误;答案为C。
3.【答案】AB
【解析】A.标准状况下,18g HO的物质的量为1mol,故18g HO含有的分子数为N ,故A正确;
2 2 A
B.O 和O 的最简式均为O,16g O的物质的量为1mol,故16g O 和O 的混合气体中氧原子的数目为N ,
2 3 2 3 A
故B正确;C.通常状况下,气体的摩尔体积不一定为22.4L/mol,根据V=nV 可知1mol CO 分子所占体积不
m 2
一定为22.4L,故C错误;D.根据n=cV可知,该条件没有给出溶液的体积V的具体数值,所以不能计算
Cl−的物质的量,故D错误;故选AB。
4.【答案】A
【解析】因Cu(NO ) 受热分解产生的NO 和O 体积比为4∶1,恰好完全反应:4NO +O +H O=4HNO ,反
3 2 2 2 2 2 2 3
应完后试管内没有气体,试管中完全充满水,溶质为HNO ,设烧瓶体积为VL,则HNO 溶液的体积也是
3 3VL,n(HNO)=n(NO )= ,c(HNO )= ,故A正确。故选A。
3 2 3
5.【答案】BD
【解析】A.2.3g金属钠与氧气完全反应生成NaO与NaO 混合物,按得失电子数相等,0.1mol钠失去
2 2 2
0.1mol电子,转移的电子数目为0.1N ,A项正确;B.1.6g O 和O 混合气体中含有0.1N 个氧原子,所含的
A 2 3 A
分子数目无法确定,B项错误;C.铜离子在溶液中会发生水解,1L 0.1mol/L CuCl 溶液中Cu2+的数目少于
2
0.1N ,C项正确;D.标准状况下,SO 为固体,1.2L SO 完全溶于水后配成的稀溶液中所含SO的数目远大
A 3 3
于0.5N ,D项错误;答案选BD。
A
精准预测题
1.【答案】C
【解析】A.NH F结构中只有铵根中含有4个共价键,则lmol NH F晶体中含有的共价键数目为4N ,A
4 4 A
错误;B.CH 和C H 混合气体2.24L(标准状况)的物质的量是0.1mol,由于1mol CH 和C H 分别完全燃烧消
4 2 4 4 2 4
耗氧气的物质的量分别是2mol、3mol,则0.1mol混合气体完全燃烧消耗氧气的分子数目应该介于0.2N 和
A
0.3N 之间,B错误;C.l00mL 0.10mol/L FeCl 溶液中铁离子的物质的量是0.01mol,加入足量Cu粉充分反
A 3
应,铁离子被还原为亚铁离子,则转移电子数目为0.01N ,C正确;D.乙酸和乙醇的酯化反应是可逆反
A
应,则0.1mol CH COOH与足量CHCHOH充分反应生成的CHCOOCH CH 分子数目小于0.1N ,D错误;
3 3 2 3 2 3 A
答案选C。
2.【答案】B
【解析】A.硫离子其核电荷数为16,核外电子总数为18,用 表示,氯原子获得1个电子形成氯
离子,Cl−离子的结构示意图为: ,A错误;B.SCl 分子中S原子和两个Cl原子共用两对电子,每
2
个Cl原子和S原子共用一对电子,这样所有原子都达到稳定结构,则SCl 的电子式为 ,B正确;
2
C.O原子的半径大于H原子,因此HO分子的比例模型是 ,C错误;D.S 中硫原子最外层均满足8
2 8
电子稳定结构,其结构式的球棍模型可表示为: ,D错误;答案选B。
3.【答案】AC【解析】A.不清楚温度和压强,因此22.4L Cl 气体的物质的量无法计算,故A错误;B.根据反应方程
2
式转移2mol电子生成2mol水即36g,因此反应中每生成 1.8g HO就会转移0.1N 电子,故B正确;C.
2 A
0.1mol∙L−1的Ca(ClO) 溶液,体积未知,因此ClO-的数目无法计算,故C错误;D.常温下,1L pH=12的
2
Ca(OH) 溶液中c(OH−)=0.01mol∙L−1,因此1L Ca(OH) 溶液中n(OH−)=0.01mol,OH−的数目为0.01N ,故D正
2 2 A
确。综上所述,答案为AC。
4.【答案】B
【解析】因为ρ(甲)>ρ(乙),且两者质量相同,结合 ,知V(甲)M(乙)。A.由分析知M(甲)>M(乙),结合n= ,推得
n(甲)M(乙),D错误;故答案选B。
5.【答案】C
【解析】A.1 个 31P 原子中含有 31-15=16 个中子,则 3.1g 31P 中含有的中子数为
=1.6N ,A正确;B.白磷和黑磷分子中,每个P原子平均形成1.5个P-P键,则31g白磷与31g黑磷中含有
A
的P-P键数目均为 =1.5N ,B正确;C.12.4g白磷物质的量为 =0.1mol,与0.6mol
A
H 在密闭容器中发生反应P+6H 4PH ,则充分反应生成的PH 分子数小于0.4N ,C不正确;D.6.82g
2 4 2 3 3 A
白磷的物质的量为 =0.055mol,反应 中,电
子转移的数目为 24×(5-0)e−=120e−,则 0.055mol P 参加反应时转移的电子数为
4
=0.6N ,D正确;故选C。
A
6.【答案】D
【解析】A.该“84消毒液”的物质的量浓为c= = =4.0mol·L−1,故A正确;
B.一瓶该“84消毒液”敞口放置一段时间后,由于其易吸收空气中的 CO 变质而浓度变小,故B正确;
2C.稀释后的溶液中c(Na+)等于其原物质的量浓度4.0mol·L−1的1/10,约为0.04mol·L−1,故C正确;D.应选
取500 mL的容量瓶进行配制,所以需要NaClO的质量为0.5L×4.0mol·L−1×74.5g·mol-1=149g,故D不正确。
故选D。
7.【答案】D
【解析】锌与浓硫酸发生 Zn+2H SO =ZnSO +SO↑+2H O,随着反应的进行,硫酸浓度降低,发生:
2 4 4 2 2
Zn+H SO =ZnSO +H ↑,生成气体为SO 和H 的混合物,物质的量为 =1.5mol,剩余硫酸的物质
2 4 4 2 2 2
的量为:n(H SO ) = ×1L×0.1mol/L=0.05mol,消耗硫酸的物质的量为n(H SO ) =0.1L×18.5mol/L-0.05mol=
2 4 剩 2 4 消耗
1.8mol。A.共生成1.5mol气体,根据方程式可知无论生成SO 还是生成H ,每生成一分子气体转移2个电
2 2
子,所以反应中共转移电子3mol,故A正确;B.根据方程式可知消耗的锌与反应生成的气体的物质的量相
同,所以消耗 1.5mol 锌,质量为 1.5mol65g/mol=97.5g,故 B 正确;C.根据方程式可知 n(H
2
SO
4
)
消耗
=n(H )+2n(SO )=1.8mol,且n(H )+n(SO )=1.5mol,解得n(SO )=0.3mol,n(H )=1.2mol,所以相同条件下气体
2 2 2 2 2 2
A中SO 与H 的体积比为1∶4,故C正确;D.气体A中含有二氧化硫,可以还原溴单质,使溴水褪色,故D
2 2
错误;综上所述答案为D。
8.【答案】A
【解析】A.D16O和14ND 的摩尔质量均为20g/mol,则2.0g重水(D 16O)和14ND 的混合物的物质的量为
2 3 2 3
0.1mol,又1个D16O含有电子数为10个,1个14ND 含有的电子数也为10个,则0.1mol该混合物中含有的
2 3
电子数为N ,故A正确;B.Fe(CO) 中CO与Fe形成5个σ键,每个CO中有1个σ键,则1mol Fe(CO) 中
A 5 5
的σ键数为10N ,故B错误;C.生成2.24L NO气体,没有指明是否标况,无法计算,故C错误;D.标况
A
下,HF不是气体,所含分子数不是0.05N ,故D错误;故选A。
A
9.【答案】C
【解析】A.S2−原子核外有18个电子,则1mol S2−所含电子数为18N ,A说法错误;B.NaS为强碱弱酸
A 2
盐,在溶液中S2−发生水解反应,导致S2−浓度减小且未给定溶液的体积,无法计算S2−的数目,B说法错误;
C.NaS的摩尔质量为 78g/mol,7.8g Na S固体即 0.1mol,含有 0.2mol Na+和0.1mol S2−,共含离子数为
2 2
0.3N ,C说法正确;D.根据方程式可知,1mol Na S最多溶解S原子的数目为4N ,D说法错误;答案为
A 2 A
C。
10.【答案】(1)生成的产物具有阻燃作用
(2)2a+3b=c+2d
(3)3∶5(过程见解析)
【解析】(1)碱式碳酸铝镁[MgAl (OH)(CO)·xH O]受热分解最终生成MgO、Al O ,MgO、Al O 的熔点
a b c 3 d 2 2 3 2 3较高且都不燃烧,所以有阻燃作用,故答案为生成的产物具有阻燃作用;(2)化合物中各元素化合价的代数和
为 0,所以 2a+3b+c+4d=(c+3d)×2,所以得 2a+3b=c+2d,故答案为 2a+3b=c+2d;(3)n(CO )=
2
=2.50×10−2
mol,m(CO )=2.50×10−2mol×44g/mol=1.10g,在270℃~600℃之间,失去结晶水后的样品进一步受热分解生
2
成 CO 、HO,m(CO )+m(H O)=3.390g×(0.7345-0.3702)=1.235g,m(HO)=1.235g-1.10g=0.135g,n(H O)=
2 2 2 2 2 2
=
7.50×10−3mol,再根据氢原子守恒得n(OH−)=2n(HO)=1.50×10−2mol,根据C原子守恒得n(CO)=n(CO )=2.50
2 2
×10−2mol , 所 以 n(OH−)∶n(CO)=1.50×10−2mol∶2.50×10−2mol=3∶5 , 答 : 碱 式 碳 酸 铝 镁 样 品 中 的
n(OH−)∶n(CO)=3∶5。
11.【答案】(1)C
(2)2CaO+4H+=2Ca2++2H O+O↑
2 2 2
(3)0.06mol
【解析】(1)A.CaO 具有氧化性,因此对面粉可能具有增白作用,A正确;B.CaO 是由钙离子和过氧根
2 2
离子组成的离子化合物,其中阴阳离子的个数比为 1∶1,B 正确;C.CaO 和水反应的方程式为
2
2CaO+2H O=2Ca(OH) +O ,过氧化钙既是氧化剂也是还原剂,氧元素化合价从-1价升高到0价,每产生
2 2 2 2
1mol O 转移电子2mol,C错误;D.根据过氧化钠和二氧化碳的反应可类推CaO 和CO 反应的化学方程式
2 2 2
为:2CaO+2CO =2CaCO +O ,D正确;答案选C;(2)根据过氧化钠和盐酸的反应可类推过氧化钙(CaO)与盐
2 2 3 2 2
酸反应的离子方程式2CaO+4H+=2Ca2++2H O+O↑。(3)①得到O 在标准状况下体积为672mL,氧气的物质
2 2 2 2
的量=0.672L÷22.4L/mol=0.03mol,根据方程式2[CaO·xH O]=2CaO+O ↑+2xH O可知,5.42 g过氧化钙样品
2 2 2 2
中CaO 的物质的量为0.03mol×2=0.06mol;②7g碳酸钙的物质的量是7g÷100g/mol=0.07mol,根据钙离子守
2
恒样品中杂质CaO的物质的量是0.07mol-0.06mol=0.01mol,质量是0.01mol×56g/mol=0.56g,所以结晶水的质
量=5.42g-0.56g-0.06mol×72g/mol=0.54g,其物质的量为0.54g÷18g/mol=0.03mol,故0.06x=0.03,则x= 。
12.【答案】(1)HSO +Na SO =SO↑+H O+Na SO
2 4 2 3 2 2 2 4
(2)SO+2H+=S↓+SO ↑+H O 关闭K、K,打开K
2 2 2 1 2 3
(3)酸式 26.10 92.5
【解析】烧瓶B中HSO 与NaSO 反应制备SO ,硫代硫酸钠晶体在中性或碱性溶液中较稳定,在酸性
2 4 2 3 2
溶液中,反应:SO+2H+=S↓+SO ↑+H O产生浑浊,故当pH计读数接近7.0时,应立即停止通SO 。测定
2 2 2 2
NaSO∙5H O的质量分数时,应作平行试验,重复二到三次,数据误差较大则舍去,其余取平均消耗标准液
2 2 3 2体积,结合关系式求算;(1)烧瓶B中HSO 与NaSO 反应制备SO ,化学方程式为HSO +Na SO =SO↑+H O
2 4 2 3 2 2 4 2 3 2 2
+Na SO 。(2)硫代硫酸钠晶体在中性或碱性溶液中较稳定,在酸性溶液中产生浑浊,反应的离子方程式为:
2 4
SO+2H+=S↓+SO ↑+H O,故当pH计读数接近7.0时,应立即停止通SO ,具体操作是关闭K 、K ,打开
2 2 2 2 1 2
K 。(3)①碘具有氧化性,为防止其氧化碱式滴定管的橡皮管,标准碘的水溶液应盛放在酸式滴定管内;②由
3
图可知,起始读数为0.00mL,终点读数为26.10mL,故第一次消耗碘的标准溶液的体积为26.10mL;③重复
上述操作三次,第二次数据误差较大,舍去,则平均消耗标准液体积为(26.10mL+26.12mL)÷2=26.11mL,根
据反应有: , ,则产品中
NaSO∙5H O的质量分数为 。
2 2 3 2