文档内容
绝密 ★ 启用前
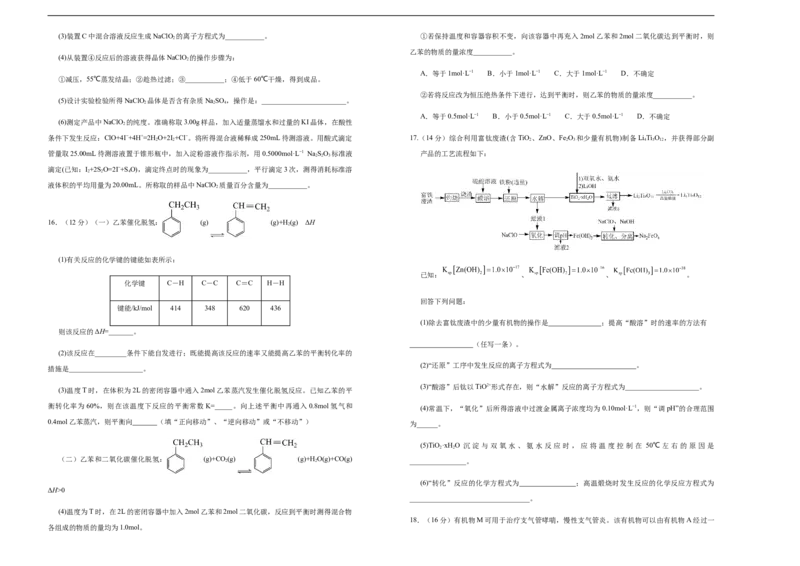
3.化合物甲(H BNH )可由无机苯(分子式为B NH ,结构式为 )通过反应制得:
2021 年普通高等学校招生全国统一考试 3 3 3 3 6
班级
姓名
化 学
。下列叙述错误的是
准考证号
注意事项:
考场号 A.B NH 为非极性分子
3 3 6
此卷只
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己
装订座不位密号封 B.CH、CO 分子空间构型分别是:正四面体形、直线形
4 2
的姓名、考生号填写在答题卡上。
C.第一电离能大小为:N>O>C>B
2.回答第Ⅰ卷时,选出每小题的答案后,用铅笔把答题卡上对应题目的答案标号涂黑,
如需改动,用橡皮擦干净后,再选涂其他答案标号。写在试卷上无效。
D.化合物甲和无机苯分子中B的杂化类型相同
3.回答第Ⅱ卷时,将答案填写在答题卡上,写在试卷上无效。
4.下列物质性质与用途对应关系正确的是
4.考试结束,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cu 64
性质 用途
A SO 具有氧化性 漂白纸浆
2
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
B NaHCO 溶液呈弱碱性 中和过多的胃酸
3
合题目要求的。
刻制铜制电路板时作为“腐蚀
1.中华优秀传统文化博大精深、源远流长,王翰《凉州词》中写道“葡萄美酒夜光杯,欲饮琵琶 C FeCl 溶液呈酸性
3 液”
马上催···”。夜光杯的主要成分为3MgO·4SiO ·H O,古代制作琵琶的主要原料为木料或竹料、
2 2
丝线等,下列说法错误的是 D HF具有弱酸性 刻蚀玻璃
A.由蚕丝搓纺而成的丝线的主要成分为蛋白质 5.下列反应的离子方程式书写正确的是
B.葡萄酒中通常含有微量SO ,SO 既可以杀菌又能防止营养成分被氧化
2 2
A.1mol 的溶液与4mol NaOH的溶液混合:
C.夜光杯属硅酸盐产品,难溶于水,不耐酸碱侵蚀
B.用稀硝酸洗涤试管内壁的银镜:Ag+4H++NO=Ag++NO↑+2HO
2
D.制作琵琶的竹料放入饱和NaSiO 溶液中充分浸透后沥干可起到防火的作用
2 3
2.下列关于化学用语的表述正确的是 C.苯甲酸与过量 溶液反应:2 +CO→2 +CO ↑+H O
2 2
A.中子数为143的U原子: B.HN-CN分子中含3个σ键
2 D.NaSO(焦亚硫酸钠)与稀硫酸反应放出SO :SO+2H+=2SO↑+H O
2 2 5 2 2 2 2
6.下列有关实验装置的说法中错误的是
C.Fe2+的原子结构示意图: D.BF 的电子式:
3D.Y简单气态氢化物的沸点大于W简单气态氢化物的沸点
9.废气的污染成为世界各国关注的焦点,科技团队研究发现利用工业尾气中硫化物与氮氧化物可
以制取NaSO 和NH NO 。
2 2 4 4 3
A.图1装置可用于检验氯化铵受热分解生成的两种气体
B.图2装置中反应一段时间后,试管中固体变为黑色
C.图3装置可测量Cu与浓硝酸反应产生气体的体积
有关该流程下列说法错误的是
D.图4装置可用于实验室制备Fe(OH)
2
A.该流程中可以循环使用的物质是Ce4+
7.某科研小组采用铜基催化剂(Cua+,其中a=0或者1),CO 多步加氢合成甲醇,其合成反应历
2
程如下。下列说法中正确的是 B.装置Ⅱ中若生成1.204×1023个H+,则消耗18g水
C.装置Ⅲ中得到0.3mol SO时,若用乙醇燃料电池进行电解时,理论上要消耗0.05mol乙醇
2
D.装置Ⅳ获得粗产品NH NO 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等
4 3
10.下列装置图或曲线图与对应的叙述不相符的是
A.催化剂Cua+是加氢反应的活性中心,能提高H 的转化率
2
B.该过程中只得到甲醇一种产物
C.能通过调控反应条件获得甲醛(HCHO)等有机物
D.该催化过程中同时有极性共价键、非极性共价键的断裂和形成 A.图1:用0.1mol/L NaOH溶液分别滴定相同物质的量浓度、相同体积的盐酸和醋酸,其中实
线表示的是滴定盐酸的曲线
8.短周期主族元素M、W、X、Y、Z原子序数依次增大,W、X的简单离子具有相同的电子层结
构,X的原子半径是短周期主族元素原子中最大的,M的气态氢化物和最高价氧化物对应的水 B.图2:酸性KMnO 溶液颜色会逐渐变浅乃至褪去
4
化物反应生成一种盐,W与Y同主族,Y的氢化物为具有臭鸡蛋气味的气体。下列说法正确的
C.图3:用0.1mol/L CHCOOH溶液滴定20mL 0.1mol/L NaOH溶液的滴定曲线,当pH=7时:
3
是
c(Na+)=c(CH COO−)>c(OH−)=c(H+)
3
A.Z的氧化物的水化物的酸性比Y的强
D.图4:表示N(g)+3H(g) 2NH (g)的v 随时间变化曲线,由图知t 时刻可能减小了容器
2 2 3 逆 1
B.W与其他四种元素均可形成至少两种二元化合物 内的压强
C.简单离子半径:W<X<Z 12.下列根据实验操作和实验现象得出的结论正确的是选项 实验操作 实现现象 结论
向久置的NaSO 溶液中加入足量 出现白色沉淀,加入稀 久置的NaSO
A 2 3 2 3
BaCl 溶液,再加入足量稀硝酸 硝酸后沉淀不溶解 溶液已全部变质
2
取1mL 20%蔗糖溶液,加入少量稀硫
B 酸,水浴加热后,取少量溶液,加入 未有砖红色沉淀生成 蔗糖未水解
几滴新制Cu(OH) 悬浊液,加热
2
常温下用pH计测定浓度均为 酸性:
pH:NaClO溶液
C 0.1mol·L−1的NaClO溶液和NaHCO 3 >NaHCO 溶液 A.将0.2mol·L−1 CH 3 COOH溶液和0.1mol·L−1 NaOH溶液等体积混合,则反应后的混合液中:
溶液的pH 3 HCO>HClO
2 3
2c(OH−)+c(CH COO−)=2c(H+)+c(CH COOH)
3 3
向KNO 和KOH混合溶液中加入铝粉 NO离子被还原
D 3 试纸变为蓝色
并加热,管口放湿润的红色石蕊试纸 为NH B.a点时,c(Na+)>c(HF)>c(H+)>c(OH−)
3
13.在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为 C.常温下,0.1mol/L NaF溶液的pH小于0.1mol/L CH COONa溶液的pH
3
反应Ⅰ:CO 2 (g)+4H 2 (g)=CH 4 (g)+2H 2 O(g) ΔH 1 =-164.7kJ/mol K 1 D.向0.1mol·L−1 HF溶液中加入等体积的 0.1mol·L−1 NaOH溶液后所得的混合溶液中 c(H+)
+c(HF)
反应Ⅱ:CO(g)+H(g)=CO(g)+HO(g) ΔH=41.2kJ/mol K
2 2 2 2 2
=c(OH−)
反应Ⅲ:2CO(g)+2H(g)=CO (g)+CH (g) ΔH=-247.1kJ/mol K
2 2 4 3 3
二、非选择题:共58分。
向恒压、密闭容器中通入1mol CO 和4mol H ,平衡时CH 、CO、CO 的物质的量随温度的变
2 2 4 2
化如图所示。下列说法不正确的是 15.(16分)亚氯酸钠(NaClO)是重要漂白剂,某化学实验小组设计如下实验探究亚氯酸钠的制备
2
与性质。
A.图中曲线B表示CO的物质的量随温度的变化
B.反应Ⅲ的平衡常数K=
3
已知:①NaClO 饱和溶液在低于38℃时析出NaClO·3H O,高于38℃时析出无水NaClO ,温
2 2 2 2
度高于60℃时,NaClO 分解为NaClO 和NaCl。
2 3
C.提高CO 转化为CH 的转化率,需要研发在低温区高效的催化剂
2 4
回答下列问题:
D.CO(g)+3H(g)=CH (g)+HO(g)的ΔH=-205.9kJ/mol
2 4 2
(1)仪器a的名称是___________,仪器b的作用是______。
14.常温下,将NaOH溶液分别加到HF溶液、CHCOOH溶液中,两混合溶液中离子浓度与pH的
3
(2)A装置中发生的主要反应的化学方程式为___________
变化关系如图所示,已知pK=-lgK,下列有关叙述错误的是
a a(3)装置C中混合溶液反应生成NaClO 的离子方程式为___________。 ①若保持温度和容器容积不变,向该容器中再充入2mol乙苯和2mol二氧化碳达到平衡时,则
2
乙苯的物质的量浓度___________。
(4)从装置④反应后的溶液获得晶体NaClO 的操作步骤为:
2
A.等于1mol·L−1 B.小于1mol·L−1 C.大于1mol·L−1 D.不确定
①减压,55℃蒸发结晶;②趁热过滤;③___________;④低于60℃干燥,得到成品。
②若将反应改为恒压绝热条件下进行,达到平衡时,则乙苯的物质的量浓度___________。
(5)设计实验检验所得NaClO 晶体是否含有杂质NaSO ,操作是:________________________。
2 2 4
A.等于0.5mol·L−1 B.小于0.5mol·L−1 C.大于0.5mol·L−1 D.不确定
(6)测定产品中NaClO 的纯度。准确称取3.00g样品,加入适量蒸馏水和过量的KI晶体,在酸性
2
条件下发生反应:ClO+4I−+4H+=2H O+2I +Cl−。将所得混合液稀释成250mL待测溶液。用酸式滴定 17.(14分)综合利用富钛废渣(含TiO 、ZnO、Fe O 和少量有机物)制备LiTiO ,并获得部分副
2 2 2 2 3 4 5 12
管量取25.00mL待测溶液置于锥形瓶中,加入淀粉溶液作指示剂,用0.5000mol·L−1 Na SO 标准液 产品的工艺流程如下:
2 2 3
滴定(已知:I+2S O=2I−+S O),滴定终点时的现象为___________,平行滴定3次,测得消耗标准溶
2 2 4
液体积的平均用量为20.00mL。所称取的样品中NaClO 质量百分含量为___________。
2
16.(12分)(一)乙苯催化脱氢: (g) (g)+H(g) ΔH
2
(1)有关反应的化学键的键能如表所示:
已知: 、 、 。
化学键 C-H C-C C=C H-H
回答下列问题:
键能/kJ/mol 414 348 620 436
(1)除去富钛废渣中的少量有机物的操作是 ;提高“酸溶”时的速率的方法有
则该反应的ΔH=_______。
(任写一条)。
(2)该反应在_________条件下能自发进行;既能提高该反应的速率又能提高乙苯的平衡转化率的
(2)“还原”工序中发生反应的离子方程式为 。
措施是_____________________。
(3)“酸溶”后钛以TiO2+形式存在,则“水解”反应的离子方程式为_____________________。
(3)温度T时,在体积为2L的密闭容器中通入2mol乙苯蒸汽发生催化脱氢反应。已知乙苯的平
衡转化率为60%,则在该温度下反应的平衡常数K=_____。向上述平衡中再通入0.8mol氢气和 (4)常温下,“氧化”后所得溶液中过渡金属离子浓度均为 0.10mol·L−1,则“调pH”的合理范围
0.4mol乙苯蒸汽,则平衡向 (填“正向移动”、“逆向移动”或“不移动”)
为______。
(5)TiO ·xH O 沉淀与双氧水、氨水反应时,应将 温度控制在 50℃左右的原因是
2 2
(二)乙苯和二氧化碳催化脱氢: (g)+CO (g) (g)+HO(g)+CO(g)
2 2 ________________。
(6)“转化”反应的化学方程式为 ;高温煅烧时发生反应的化学反应方程式为
ΔH>0
__________________________________。
(4)温度为T时,在2L的密闭容器中加入2mol乙苯和2mol二氧化碳,反应到平衡时测得混合物
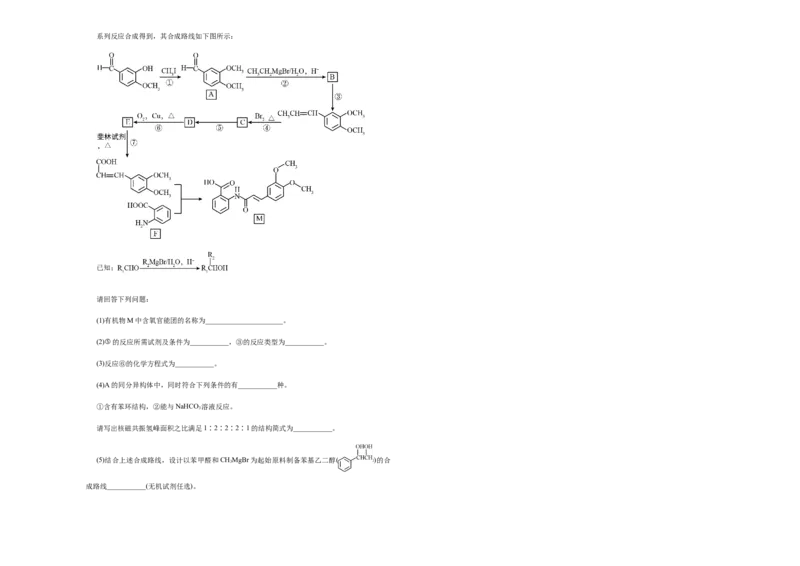
18.(16分)有机物M可用于治疗支气管哮喘,慢性支气管炎。该有机物可以由有机物A经过一
各组成的物质的量均为1.0mol。系列反应合成得到,其合成路线如下图所示:
已知;
请回答下列问题:
(1)有机物M中含氧官能团的名称为______________________。
(2)⑤的反应所需试剂及条件为___________,③的反应类型为___________。
(3)反应⑥的化学方程式为___________。
(4)A的同分异构体中,同时符合下列条件的有___________种。
①含有苯环结构,②能与NaHCO 溶液反应。
3
请写出核磁共振氢峰面积之比满足1∶2∶2∶2∶1的结构简式为___________。
(5)结合上述合成路线,设计以苯甲醛和CHMgBr为起始原料制备苯基乙二醇( )的合
3
成路线___________(无机试剂任选)。