文档内容
6.周期表中“位—构—性”的关系及分析
1.(2024·浙江6月卷)元素X、Y、Z、M分布在三个短周期中,其中Y和Z原子序数相差2,Z的最外
层电子数为内层的3倍,Y和M同族,下列说法错误的是 ( )
A.键角:YX+ >YX-
3 3
B.极性:Y X>X Z
2 2 2 2
C.单质熔点:Y>M
D.热稳定性:YX>MX
4 4
2.(2024·吉林省吉林地区三模)A、B、C、D、E是五种原子序数依次递增的短周期元素。已知:A的
一种同位素可以用于测定文物的年代;基态C原子含3对成对电子;D在同周期金属元素中第一电离
能最大;基态E原子的3p轨道中含有自旋方向不同且数目之比为3∶1的电子。下列说法正确的是(
)
A.简单离子的离子半径:BR>Z
B.元素电负性:XY>W
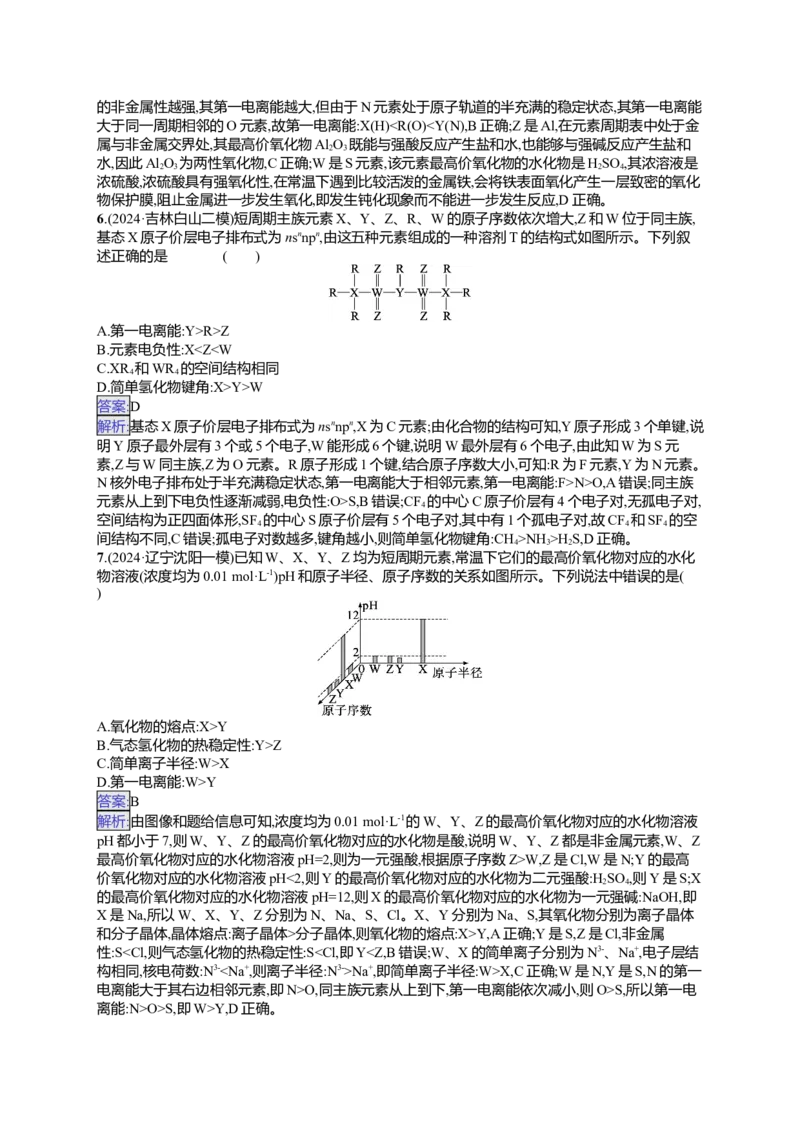
7.(2024·辽宁沈阳一模)已知W、X、Y、Z均为短周期元素,常温下它们的最高价氧化物对应的水化
物溶液(浓度均为0.01 mol·L-1)pH和原子半径、原子序数的关系如图所示。下列说法中错误的是(
)
A.氧化物的熔点:X>Y
B.气态氢化物的热稳定性:Y>Z
C.简单离子半径:W>X
D.第一电离能:W>Y
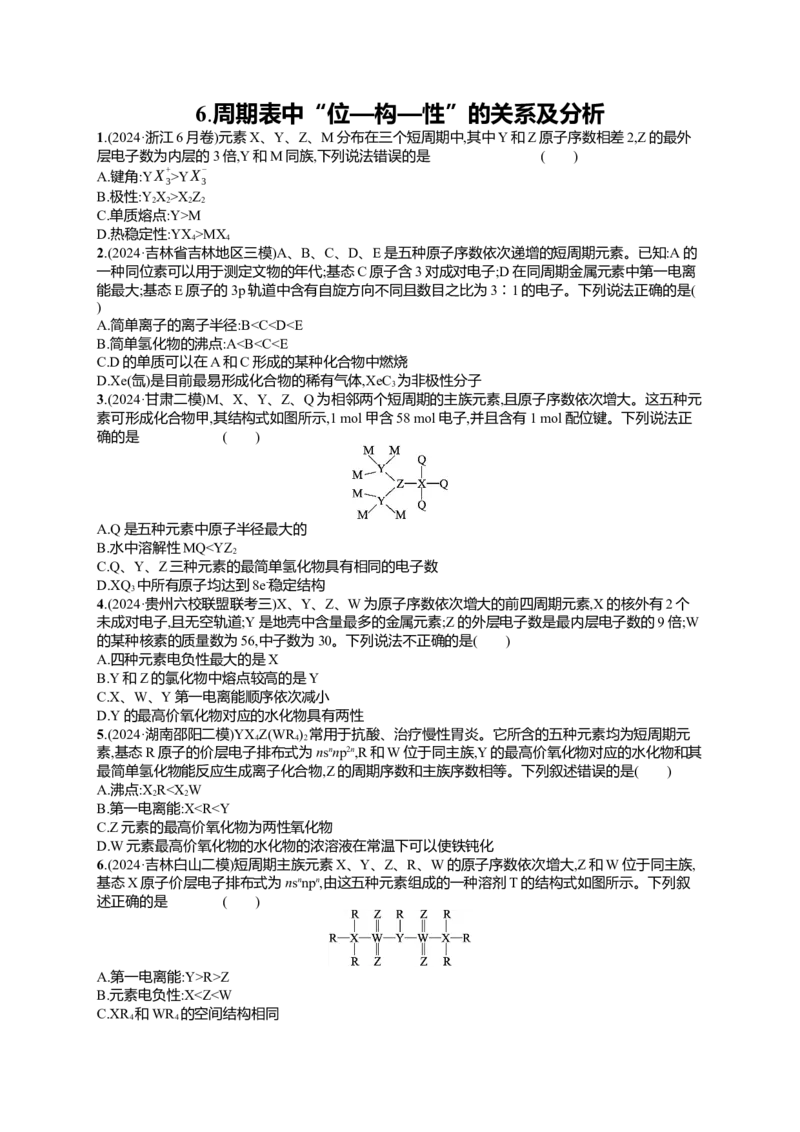
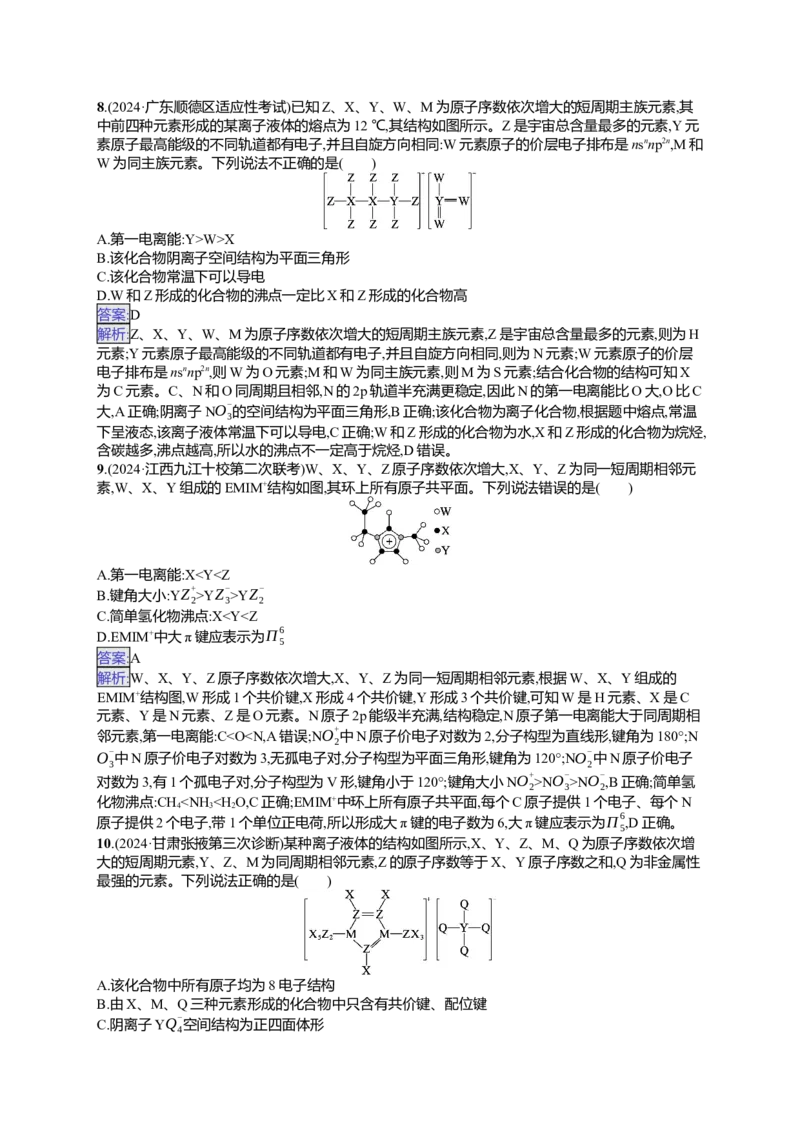
8.(2024·广东顺德区适应性考试)已知Z、X、Y、W、M为原子序数依次增大的短周期主族元素,其
中前四种元素形成的某离子液体的熔点为12 ℃,其结构如图所示。Z是宇宙总含量最多的元素,Y元
素原子最高能级的不同轨道都有电子,并且自旋方向相同:W元素原子的价层电子排布是nsnnp2n,M和
W为同主族元素。下列说法不正确的是( )
A.第一电离能:Y>W>X
B.该化合物阴离子空间结构为平面三角形
C.该化合物常温下可以导电
D.W和Z形成的化合物的沸点一定比X和Z形成的化合物高
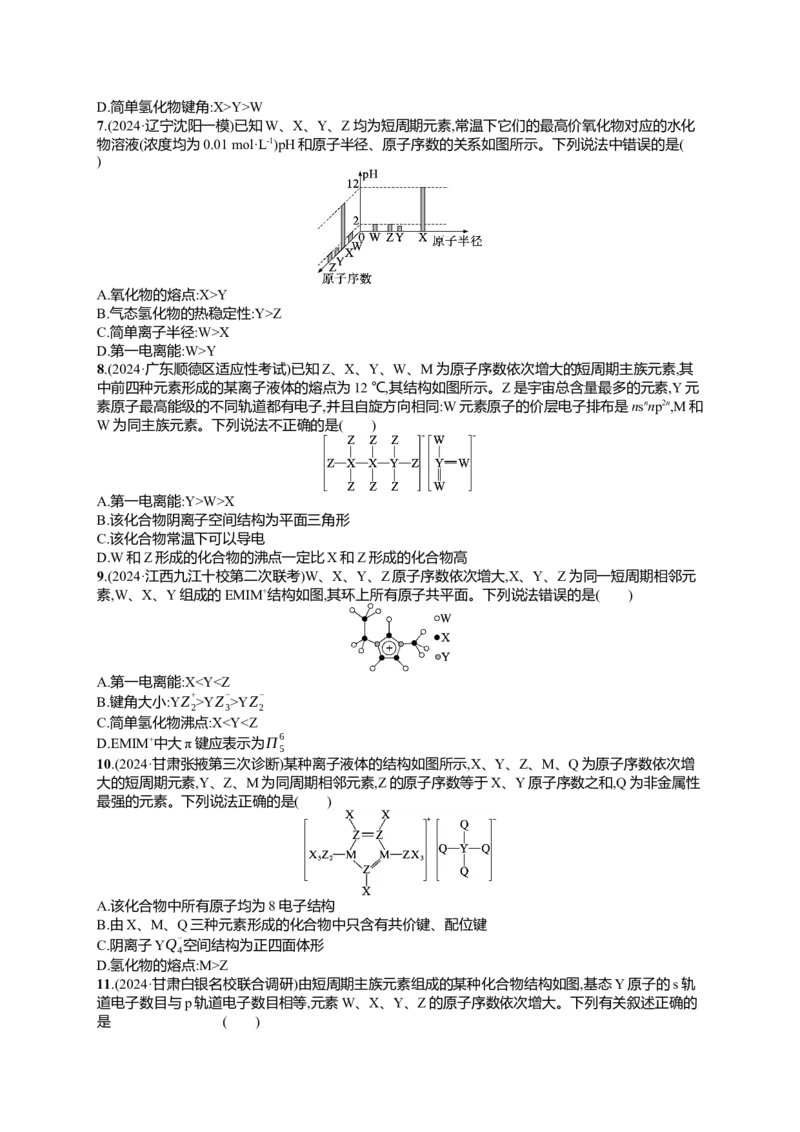
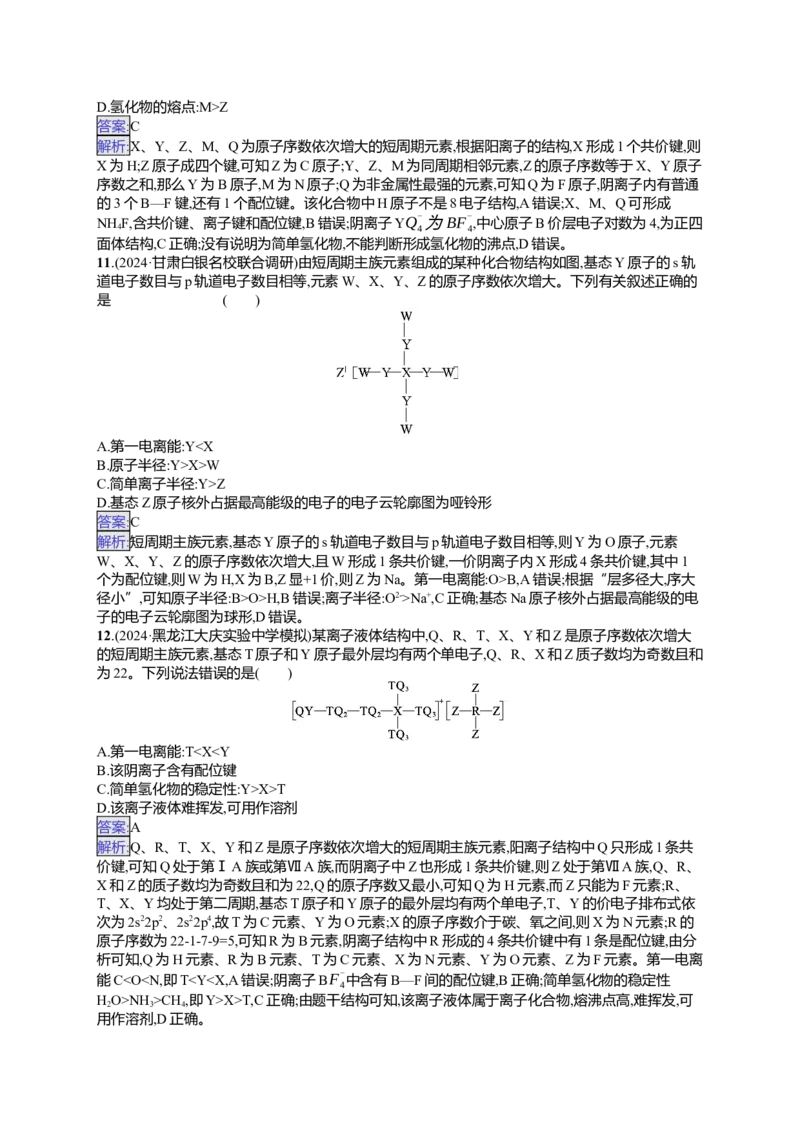
9.(2024·江西九江十校第二次联考)W、X、Y、Z原子序数依次增大,X、Y、Z为同一短周期相邻元
素,W、X、Y组成的EMIM+结构如图,其环上所有原子共平面。下列说法错误的是( )
A.第一电离能:XYZ- >YZ-
2 3 2
C.简单氢化物沸点:XZ
11.(2024·甘肃白银名校联合调研)由短周期主族元素组成的某种化合物结构如图,基态Y原子的s轨
道电子数目与p轨道电子数目相等,元素W、X、Y、Z的原子序数依次增大。下列有关叙述正确的
是 ( )A.第一电离能:YX>W
C.简单离子半径:Y>Z
D.基态Z原子核外占据最高能级的电子的电子云轮廓图为哑铃形
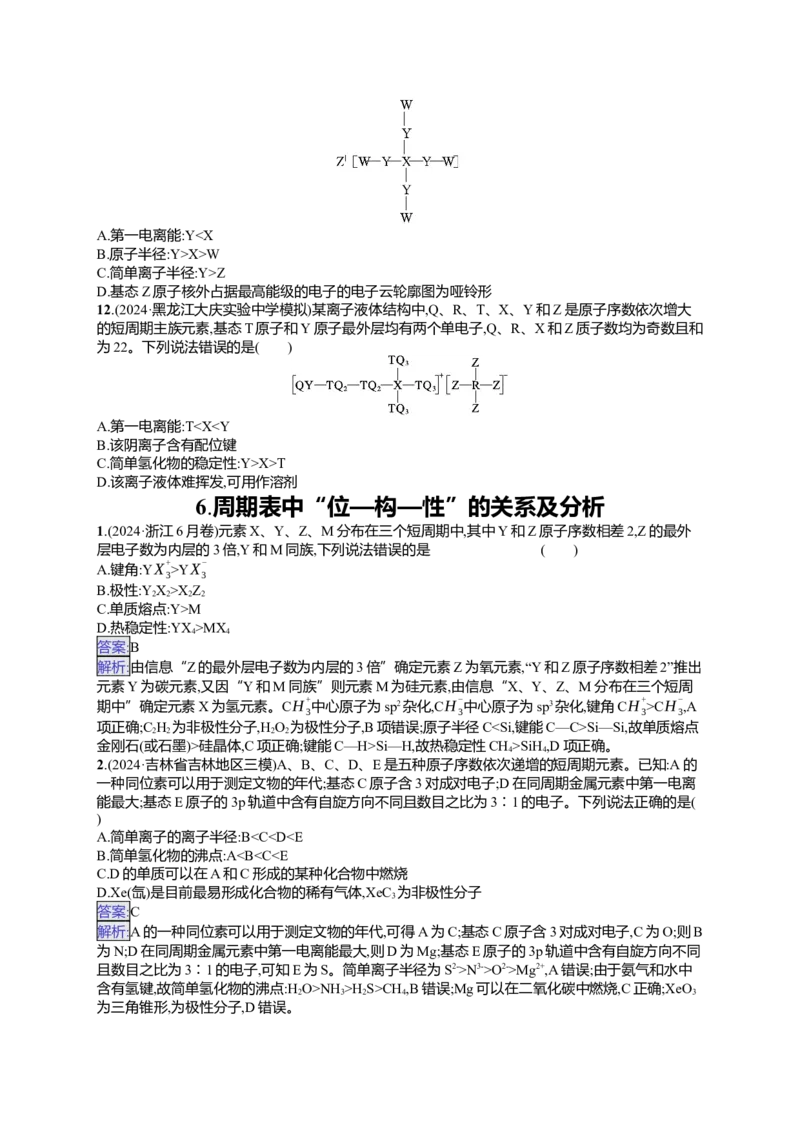
12.(2024·黑龙江大庆实验中学模拟)某离子液体结构中,Q、R、T、X、Y和Z是原子序数依次增大
的短周期主族元素,基态T原子和Y原子最外层均有两个单电子,Q、R、X和Z质子数均为奇数且和
为22。下列说法错误的是( )
A.第一电离能:TX>T
D.该离子液体难挥发,可用作溶剂
6.周期表中“位—构—性”的关系及分析
1.(2024·浙江6月卷)元素X、Y、Z、M分布在三个短周期中,其中Y和Z原子序数相差2,Z的最外
层电子数为内层的3倍,Y和M同族,下列说法错误的是 ( )
A.键角:YX+ >YX-
3 3
B.极性:Y X>X Z
2 2 2 2
C.单质熔点:Y>M
D.热稳定性:YX>MX
4 4
答案:B
解析:由信息“Z的最外层电子数为内层的3倍”确定元素Z为氧元素,“Y和Z原子序数相差2”推出
元素Y为碳元素,又因“Y和M同族”则元素M为硅元素,由信息“X、Y、Z、M分布在三个短周
期中”确定元素X为氢元素。CH+ 中心原子为sp2杂化,CH- 中心原子为sp3杂化,键角CH+ >CH-
,A
3 3 3 3
项正确;C H 为非极性分子,H O 为极性分子,B项错误;原子半径CSi—Si,故单质熔点
2 2 2 2
金刚石(或石墨)>硅晶体,C项正确;键能C—H>Si—H,故热稳定性CH>SiH ,D项正确。
4 4
2.(2024·吉林省吉林地区三模)A、B、C、D、E是五种原子序数依次递增的短周期元素。已知:A的
一种同位素可以用于测定文物的年代;基态C原子含3对成对电子;D在同周期金属元素中第一电离
能最大;基态E原子的3p轨道中含有自旋方向不同且数目之比为3∶1的电子。下列说法正确的是(
)
A.简单离子的离子半径:BN3->O2->Mg2+,A错误;由于氨气和水中
含有氢键,故简单氢化物的沸点:H O>NH >H S>CH,B错误;Mg可以在二氧化碳中燃烧,C正确;XeO
2 3 2 4 3
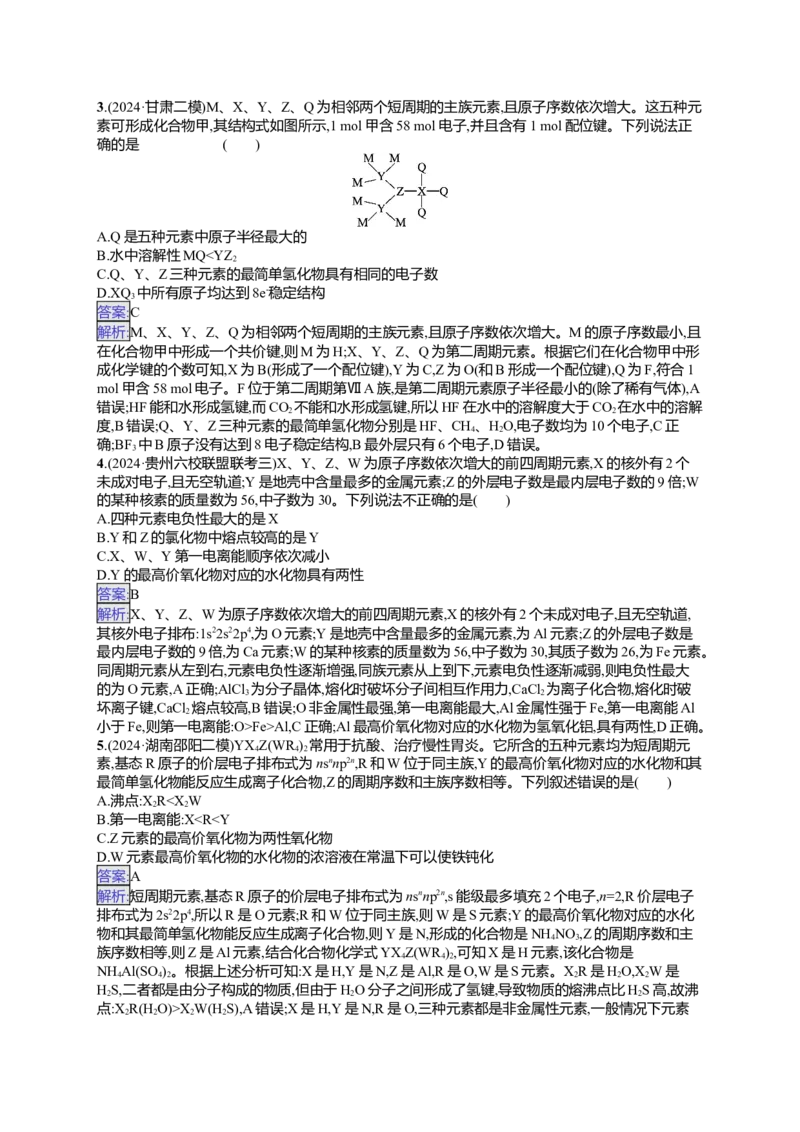
为三角锥形,为极性分子,D错误。3.(2024·甘肃二模)M、X、Y、Z、Q为相邻两个短周期的主族元素,且原子序数依次增大。这五种元
素可形成化合物甲,其结构式如图所示,1 mol甲含58 mol电子,并且含有1 mol配位键。下列说法正
确的是 ( )
A.Q是五种元素中原子半径最大的
B.水中溶解性MQFe>Al,C正确;Al最高价氧化物对应的水化物为氢氧化铝,具有两性,D正确。
5.(2024·湖南邵阳二模)YX Z(WR ) 常用于抗酸、治疗慢性胃炎。它所含的五种元素均为短周期元
4 4 2
素,基态R原子的价层电子排布式为nsnnp2n,R和W位于同主族,Y的最高价氧化物对应的水化物和其
最简单氢化物能反应生成离子化合物,Z的周期序数和主族序数相等。下列叙述错误的是( )
A.沸点:X RXW(HS),A错误;X是H,Y是N,R是O,三种元素都是非金属性元素,一般情况下元素
2 2 2 2的非金属性越强,其第一电离能越大,但由于N元素处于原子轨道的半充满的稳定状态,其第一电离能
大于同一周期相邻的O元素,故第一电离能:X(H)R>Z
B.元素电负性:XY>W
答案:D
解析:基态X原子价层电子排布式为nsnnpn,X为C元素;由化合物的结构可知,Y原子形成3个单键,说
明Y原子最外层有3个或5个电子,W能形成6个键,说明W最外层有6个电子,由此知W为S元
素,Z与W同主族,Z为O元素。R原子形成1个键,结合原子序数大小,可知:R为F元素,Y为N元素。
N核外电子排布处于半充满稳定状态,第一电离能大于相邻元素,第一电离能:F>N>O,A错误;同主族
元素从上到下电负性逐渐减弱,电负性:O>S,B错误;CF 的中心C原子价层有4个电子对,无孤电子对,
4
空间结构为正四面体形,SF 的中心S原子价层有5个电子对,其中有1个孤电子对,故CF 和SF 的空
4 4 4
间结构不同,C错误;孤电子对数越多,键角越小,则简单氢化物键角:CH >NH>H S,D正确。
4 3 2
7.(2024·辽宁沈阳一模)已知W、X、Y、Z均为短周期元素,常温下它们的最高价氧化物对应的水化
物溶液(浓度均为0.01 mol·L-1)pH和原子半径、原子序数的关系如图所示。下列说法中错误的是(
)
A.氧化物的熔点:X>Y
B.气态氢化物的热稳定性:Y>Z
C.简单离子半径:W>X
D.第一电离能:W>Y
答案:B
解析:由图像和题给信息可知,浓度均为0.01 mol·L-1的W、Y、Z的最高价氧化物对应的水化物溶液
pH都小于7,则W、Y、Z的最高价氧化物对应的水化物是酸,说明W、Y、Z都是非金属元素,W、Z
最高价氧化物对应的水化物溶液pH=2,则为一元强酸,根据原子序数Z>W,Z是Cl,W是N;Y的最高
价氧化物对应的水化物溶液pH<2,则Y的最高价氧化物对应的水化物为二元强酸:H SO ,则Y是S;X
2 4
的最高价氧化物对应的水化物溶液pH=12,则X的最高价氧化物对应的水化物为一元强碱:NaOH,即
X是Na,所以W、X、Y、Z分别为N、Na、S、Cl。X、Y分别为Na、S,其氧化物分别为离子晶体
和分子晶体,晶体熔点:离子晶体>分子晶体,则氧化物的熔点:X>Y,A正确;Y是S,Z是Cl,非金属
性:SNa+,即简单离子半径:W>X,C正确;W是N,Y是S,N的第一
电离能大于其右边相邻元素,即N>O,同主族元素从上到下,第一电离能依次减小,则O>S,所以第一电
离能:N>O>S,即W>Y,D正确。8.(2024·广东顺德区适应性考试)已知Z、X、Y、W、M为原子序数依次增大的短周期主族元素,其
中前四种元素形成的某离子液体的熔点为12 ℃,其结构如图所示。Z是宇宙总含量最多的元素,Y元
素原子最高能级的不同轨道都有电子,并且自旋方向相同:W元素原子的价层电子排布是nsnnp2n,M和
W为同主族元素。下列说法不正确的是( )
A.第一电离能:Y>W>X
B.该化合物阴离子空间结构为平面三角形
C.该化合物常温下可以导电
D.W和Z形成的化合物的沸点一定比X和Z形成的化合物高
答案:D
解析:Z、X、Y、W、M为原子序数依次增大的短周期主族元素,Z是宇宙总含量最多的元素,则为H
元素;Y元素原子最高能级的不同轨道都有电子,并且自旋方向相同,则为N元素;W元素原子的价层
电子排布是nsnnp2n,则W为O元素;M和W为同主族元素,则M为S元素;结合化合物的结构可知X
为C元素。C、N和O同周期且相邻,N的2p轨道半充满更稳定,因此N的第一电离能比O大,O比C
大,A正确;阴离子NO-
的空间结构为平面三角形,B正确;该化合物为离子化合物,根据题中熔点,常温
3
下呈液态,该离子液体常温下可以导电,C正确;W和Z形成的化合物为水,X和Z形成的化合物为烷烃,
含碳越多,沸点越高,所以水的沸点不一定高于烷烃,D错误。
9.(2024·江西九江十校第二次联考)W、X、Y、Z原子序数依次增大,X、Y、Z为同一短周期相邻元
素,W、X、Y组成的EMIM+结构如图,其环上所有原子共平面。下列说法错误的是( )
A.第一电离能:XYZ- >YZ-
2 3 2
C.简单氢化物沸点:XNO- >NO-
,B正确;简单氢
2 3 2
化物沸点:CH Z
答案:C
解析:X、Y、Z、M、Q为原子序数依次增大的短周期元素,根据阳离子的结构,X形成1个共价键,则
X为H;Z原子成四个键,可知Z为C原子;Y、Z、M为同周期相邻元素,Z的原子序数等于X、Y原子
序数之和,那么Y为B原子,M为N原子;Q为非金属性最强的元素,可知Q为F原子,阴离子内有普通
的3个B—F键,还有1个配位键。该化合物中H原子不是8电子结构,A错误;X、M、Q可形成
NH
F,含共价键、离子键和配位键,B错误;阴离子YQ- 为BF-
,中心原子B价层电子对数为4,为正四
4 4 4
面体结构,C正确;没有说明为简单氢化物,不能判断形成氢化物的沸点,D错误。
11.(2024·甘肃白银名校联合调研)由短周期主族元素组成的某种化合物结构如图,基态Y原子的s轨
道电子数目与p轨道电子数目相等,元素W、X、Y、Z的原子序数依次增大。下列有关叙述正确的
是 ( )
A.第一电离能:YX>W
C.简单离子半径:Y>Z
D.基态Z原子核外占据最高能级的电子的电子云轮廓图为哑铃形
答案:C
解析:短周期主族元素,基态Y原子的s轨道电子数目与p轨道电子数目相等,则Y为O原子,元素
W、X、Y、Z的原子序数依次增大,且W形成1条共价键,一价阴离子内X形成4条共价键,其中1
个为配位键,则W为H,X为B,Z显+1价,则Z为Na。第一电离能:O>B,A错误;根据“层多径大,序大
径小”,可知原子半径:B>O>H,B错误;离子半径:O2->Na+,C正确;基态Na原子核外占据最高能级的电
子的电子云轮廓图为球形,D错误。
12.(2024·黑龙江大庆实验中学模拟)某离子液体结构中,Q、R、T、X、Y和Z是原子序数依次增大
的短周期主族元素,基态T原子和Y原子最外层均有两个单电子,Q、R、X和Z质子数均为奇数且和
为22。下列说法错误的是( )
A.第一电离能:TX>T
D.该离子液体难挥发,可用作溶剂
答案:A
解析:Q、R、T、X、Y和Z是原子序数依次增大的短周期主族元素,阳离子结构中Q只形成1条共
价键,可知Q处于第ⅠA族或第ⅦA族,而阴离子中Z也形成1条共价键,则Z处于第ⅦA族,Q、R、
X和Z的质子数均为奇数且和为22,Q的原子序数又最小,可知Q为H元素,而Z只能为F元素;R、
T、X、Y均处于第二周期,基态T原子和Y原子的最外层均有两个单电子,T、Y的价电子排布式依
次为2s22p2、2s22p4,故T为C元素、Y为O元素;X的原子序数介于碳、氧之间,则X为N元素;R的
原子序数为22-1-7-9=5,可知R为B元素,阴离子结构中R形成的4条共价键中有1条是配位键,由分
析可知,Q为H元素、R为B元素、T为C元素、X为N元素、Y为O元素、Z为F元素。第一电离
能CNH >CH ,即Y>X>T,C正确;由题干结构可知,该离子液体属于离子化合物,熔沸点高,难挥发,可
2 3 4
用作溶剂,D正确。