文档内容
第 3 讲 氧化还原反应的概念和规律
[复习目标] 1.了解氧化还原反应的概念。2.会用“单、双线桥”分析电子转移的方向和数
目。3.掌握氧化性、还原性强弱的比较及价态规律的应用。
考点一 氧化还原反应及相关概念
1.氧化还原反应
(1)判断依据:反应前后有元素的化合价发生变化。
(2)本质:电子转移(得失或偏移)。
2.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
3.氧化还原反应电子转移的表示方法
(1)双线桥法
表示反应前后同一元素由反应物转化为反应产物时电子转移的情况。
(2)单线桥法
表示反应过程中不同元素原子间的电子转移情况。
[应用举例]
(1)分别用双线桥法、单线桥法标出MnO 与浓盐酸在加热条件下反应的电子转移的方向和数
2
目,并指出氧化剂、还原剂、氧化产物、还原产物。答案
(2)上述反应若产生1 mol Cl 时,转移电子数目为__________,被氧化的HCl的物质的量是
2
________ mol。
答案 2N (或1.204×1024) 2
A
分析氧化还原反应,走好关键第一步——正确标出元素的化合价。
请标出下列陌生物质中指定元素的化合价:
LiNH:N - 3 ,LiNH:N - 3 ,NH:N - 2 ,
2 2 2 4
NaSO:S + 2 ,SO:S + 6 、O - 1 、- 2 ,
2 2 3 2
C O:C + 3 ,HCN:C + 2 、N - 3 ,BH:B + 3 、H - 1 ,
2
CuH:Cu + 1 、H - 1 ,MnO(OH):Mn + 3 ,
FePO :Fe + 3 ,CrO:Cr + 6 ,KFeO:Fe + 6 ,
4 2 4
LiFePO :Fe + 2 ,CuFeS:Fe + 2 。
4 2
4.常见的氧化剂和还原剂
(1)常见的氧化剂
常见的氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见的还原剂
常见的还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离
子、某些非金属单质及其氢化物等。如:金属氢化物(如NaH等)、NaBH 也是重要的还原剂。
4
(3)元素化合价处于中间价态的物质既可以作氧化剂,又可以作还原剂。如:
其中:Fe2+、SO主要表现还原性,HO 主要表现氧化性。
2 2
5.氧化还原反应与四种基本反应类型的关系
分析下列四个化学反应:
A.2Na+2HO===2NaOH+H↑
2 2
B.2HClO=====2HCl+O↑
2
C.4NH +5O=====4NO+6HO
3 2 2
D.4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
其中属于区域“1”的是________(填字母,下同),属于区域“2”的是________,属于区域
“3”的是______,属于区域“4”的是________。
答案 D B C A
1.某元素从游离态变为化合态,则该元素一定被还原( )
2.有单质参加或生成的化学反应不一定是氧化还原反应( )
3.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( )
4.向0.01 mol·L-1硫酸酸化的KMnO 溶液中滴加0.1 mol·L-1 HO 溶液,溶液褪色,则
4 2 2
HO 具有氧化性( )
2 2
5.反应2NaO +2HO===4NaOH+O↑与反应Cl +HOHCl+HClO均为水作还原剂的
2 2 2 2 2 2
氧化还原反应( )
6. ( )
答案 1.× 2.√ 3.× 4.× 5.× 6.×1.(2022·浙江6月选考,10)关于反应NaSO+HSO ===NaSO +S↓+SO ↑+HO,下列
2 2 3 2 4 2 4 2 2
说法正确的是( )
A.HSO 发生还原反应
2 4
B.NaSO 既是氧化剂又是还原剂
2 2 3
C.氧化产物与还原产物的物质的量之比为2∶1
D.1 mol Na SO 发生反应,转移4 mol电子
2 2 3
答案 B
解析 该反应的本质是硫代硫酸根离子在酸性条件下发生歧化反应生成硫和二氧化硫,化合
价发生变化的只有S元素,硫酸的作用是提供酸性环境。HSO 中所含元素的化合价均未发
2 4
生变化,A说法不正确;NaSO 中S元素的平均化合价为+2,其发生歧化反应生成S(0价)
2 2 3
和SO (+4价),故其既是氧化剂又是还原剂,B说法正确;该反应的氧化产物是SO ,还原
2 2
产物为S,氧化产物与还原产物的物质的量之比为 1∶1,C说法不正确;根据NaSO 中S
2 2 3
元素的化合价变化情况可知,1 mol Na SO 发生反应,转移2 mol电子,D说法不正确。
2 2 3
2.已知过二硫酸分子中含有一个过氧键(—O—O—),过二硫酸钾(K SO)与MnSO 反应的
2 2 8 4
化学方程式为5KSO+2MnSO +8HO===2KMnO +8HSO +4KSO 。
2 2 8 4 2 4 2 4 2 4
(1)被还原的元素是________。
(2)氧化产物是________。
(3)氧化剂和还原剂的物质的量之比是______________________________________________。
(4)若反应消耗3.6 g H O时,反应中转移电子数为________(用N 表示阿伏加德罗常数的值)。
2 A
答案 (1)氧 (2)KMnO (3)5∶2 (4)0.25N
4 A
3.已知NaBH 与水反应的化学方程式为NaBH +2HO===NaBO +4H↑。
4 4 2 2 2
(1)氧化剂为________,还原剂为________。
(2)用“单线桥”标出电子转移的方向和数目:
________________________________________________________________________,
其中氧化产物与还原产物的质量比为______________________________________________。
(3)若生成标准状况下4.48 L H ,则转移电子的物质的量为________。
2
答案 (1)H O NaBH
2 4
(2) 1∶1
(3)0.2 mol考点二 氧化性、还原性的强弱及影响因素
1.氧化性是指得电子的性质(或能力);还原性是指失电子的性质(或能力)。
2.氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
如:Na-e-===Na+,Al-3e-===Al3+,根据金属活动性顺序可知,Na比Al活泼,更易失
去电子,所以Na的还原性比Al强。
3.物质的还原性、氧化性强弱还与反应环境的许多因素有关,如温度、浓度、酸性。一般
浓度越大,物质的氧化性或还原性越强;酸性增强时,氧化剂的氧化性增强。
一、比较物质氧化性或还原性的强弱
1.试比较下列单质或离子的氧化性。
①Cl、Br 、I、S;
2 2 2
②H+、Cu2+、Zn2+、Na+。
答案 ①Cl>Br >I >S
2 2 2
②Na+Fe>Cu>Ag ②Br-Cl->OH->SO
3.根据反应:MnO +4HCl(浓)=====MnCl +Cl↑+2HO,2KMnO +16HCl(浓)===2KCl+
2 2 2 2 4
2MnCl +5Cl↑+8HO,可判断氧化性:KMnO >MnO 。
2 2 2 4 2
4.下列各组物质:
①Cu与HNO 溶液 ②Cu与FeCl 溶液 ③Zn与HSO 溶液 ④Fe与FeCl 溶液
3 3 2 4 3
⑤Cl 与NaOH溶液 ⑥Fe与HNO 溶液 ⑦Fe与HSO 溶液 ⑧Na与O
2 3 2 4 2
(1)由于浓度不同而发生不同氧化还原反应的是____________(填序号,下同)。
(2)由于温度不同而发生不同氧化还原反应的是_____________________________________。
(3)氧化还原反应不受浓度、温度影响的是___________________________________________。
答案 (1)①③⑥⑦ (2)⑤⑥⑦⑧ (3)②④
解析 ⑥Fe和浓HNO 常温下钝化,加热继续反应;Fe和稀HNO 反应,HNO 被还原成
3 3 3
NO。⑦Fe和浓HSO 常温下钝化,加热继续反应;Fe和稀HSO 反应生成FeSO 和H。
2 4 2 4 4 2
5.铊(Tl)盐与氰化钾(KCN)被列为A级危险品。已知下列反应在一定条件下能够发生:①Tl3
++2Ag===Tl++2Ag+,②Ag++Fe2+===Ag+Fe3+,③Fe+2Fe3+===3Fe2+。则Fe2+、Ag+ 、 Tl3 + 的 氧 化 性 由 强 到 弱 的 顺 序 是
___________________________________________________。
答案 Tl3+>Ag+>Fe2+
二、实验探究物质氧化性或还原性的强弱
6.验证氧化性强弱:Cl>Br >I ,设计如下实验(已知:稀溴水呈黄色,浓溴水呈红棕色,
2 2 2
碘水呈棕黄色;忽略氧气的影响)。下列说法不正确的是( )
实验① 实验② 实验③ 实验④
溶液变为浅黄绿色 溶液变为黄色 溶液变为棕黄色 溶液变为蓝色
A.实验①设计目的:排除实验②③④水稀释的影响
B.实验②发生反应为2Br-+Cl===Br +2Cl-
2 2
C.实验③的现象可以证明氧化性:Cl>I
2 2
D.实验④能证明氧化性:Br >I
2 2
答案 D
解析 实验①是将氯水加入蒸馏水将其稀释,后续实验都是在溶液中进行的,这样可以排除
实验②③④水稀释的影响,故A正确;溶液变为黄色是因为产生溴单质,说明氯气可以将
溴单质置换出来,发生的反应为2Br-+Cl===Br +2Cl-,故B正确;溶液变为棕黄色是因
2 2
为产生碘单质,说明氯气可以将碘单质置换出来,发生的反应为 2I-+Cl===I +2Cl-,可
2 2
以证明氧化性:Cl>I ,故C正确;②反应后的黄色溶液是含有溴单质的溶液,但是不能排
2 2
除含有氯单质,加入淀粉碘化钾溶液会变蓝,证明产生了碘单质,可能是氯气或是溴单质置
换出了碘单质,不能证明氧化性:Br >I ,故D错误。
2 2
(1)利用化学反应比较物质氧化性或还原性的强弱,关键是分析出氧化剂、还原剂以及对应
的还原产物和氧化产物。
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
(2)利用某些实验手段,证明物质具有氧化性或还原性时,①选择的化学反应有明显的实验
现象;②要注意控制单一变量。1.(2023·全国乙卷,7)下列应用中涉及到氧化还原反应的是( )
A.使用明矾对水进行净化
B.雪天道路上撒盐融雪
C.暖贴中的铁粉遇空气放热
D.荧光指示牌被照发光
答案 C
解析 明矾水解生成氢氧化铝胶体,能吸附水中的悬浮颗粒并沉降使水变得澄清,没有涉及
到氧化还原反应,A不符合题意;雪遇到盐而熔点降低并熔化,未发生化学反应,B不符合
题意;使用暖贴时,铁粉与空气中的O 发生氧化还原反应,C符合题意;荧光指示牌被照
2
发光,是因为光被指示牌反射,D不符合题意。
2.(2023·浙江1月选考,6)关于反应2NH OH+4Fe3+===NO↑+4Fe2++4H++HO,下列
2 2 2
说法正确的是( )
A.生成1 mol N O,转移4 mol电子
2
B.HO是还原产物
2
C.NH OH既是氧化剂又是还原剂
2
D.若设计成原电池,Fe2+为负极产物
答案 A
解析 由方程式可知,反应生成1 mol一氧化二氮,转移4 mol电子,故A正确;该反应中
H、O元素化合价不变,HO既不是氧化产物,也不是还原产物,还原产物为 Fe2+,故B错
2
误;由方程式可知,反应中氮元素的化合价升高被氧化,NH OH是反应的还原剂,铁元素
2
的化合价降低被还原,铁离子是反应的氧化剂,故C错误;由方程式可知,反应中铁元素
的化合价降低被还原,铁离子是反应的氧化剂,若设计成原电池,铁离子在正极得到电子发
生还原反应生成亚铁离子,亚铁离子为正极产物,故D错误。
3.下列判断不正确的是________(填字母)。
A.Na-的还原性比Na的强(2021·湖北,13B)
B.硫代碳酸钠(Na CS)常用于处理废水中的重金属离子,不能被氧化(2022·湖北,8A)
2 3
C.在稀HSO 中加入少量Cu O(s),溶液由无色变为蓝色并有红色固体生成,反应中Cu O
2 4 2 2
既作氧化剂又作还原剂(2021·海南,14D)
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
(2021·河北,10D)
答案 BD
解析 A正确,Na-的半径比Na的大,Na-中原子核对最外层电子的吸引力小,失电子能力
增强;B错误,NaCS 中硫元素为-2价,还原性比较强,能被氧化;C正确,发生歧化反
2 3
应:Cu O+2H+===Cu2++Cu+HO;D错误,铜与浓硝酸反应比与稀硝酸反应剧烈,故浓
2 2
硝酸的氧化性大于稀硝酸。4.[2020·天津,13(3)节选]Fe、Co、Ni能与Cl 反应,其中Co和Ni均生成二氯化物,由此
2
推断FeCl 、CoCl 和Cl 的氧化性由强到弱的顺序为____________________。
3 3 2
答案 CoCl >Cl>FeCl
3 2 3
解析 由Fe与Cl 反应生成FeCl 可知,氧化性:Cl >Fe3+;由Co和Cl 反应只生成CoCl
2 3 2 2 2
可知,氧化性:Co3+>Cl 。综上分析,FeCl 、CoCl 和Cl 三者氧化性由强到弱的顺序为
2 3 3 2
CoCl >Cl>FeCl 。
3 2 3
课时精练
1.(2023·烟台模拟)中华传统文化中富含化学知识,下列叙述与氧化还原反应无关的是(
)
A.熬胆矾铁釡,久之亦化为铜
B.千锤万凿出深山,烈火焚烧若等闲
C.落红不是无情物,化作春泥更护花
D.有舶上铁丝日久起销
答案 B
解析 “熬胆矾铁釜,久之亦化为铜”是指Fe与CuSO 溶液的置换反应,涉及氧化还原反
4
应,A项不符合题意;“千锤万凿出深山,烈火焚烧若等闲”是指石灰石的煅烧,不涉及氧
化还原反应,B项符合题意;“落红不是无情物,化作春泥更护花”是指有机物的腐败过程,
涉及氧化还原反应,C项不符合题意;“有舶上铁丝日久起销”是指铁的吸氧腐蚀,涉及氧
化还原反应,D不符合题意。
2.(2022·山东,1)古医典富载化学知识,下述之物见其氧化性者为( )
A.金(Au):“虽被火亦未熟”
B.石灰(CaO):“以水沃之,即热蒸而解”
C.石硫黄(S):“能化……银、铜、铁,奇物”
D.石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”
3
答案 C
解析 金(Au):“虽被火亦未熟”是指金单质在空气中被火灼烧也不反应,体现金的稳定性,
与其氧化性无关,A不符合题意;石灰(CaO):“以水沃之,即热蒸而解”是指CaO+
HO===Ca(OH) ,反应放热,产生大量的水汽,而CaO由块状变为粉末状,未发生氧化还
2 2
原反应,与其氧化性无关,B不符合题意;石硫黄(S):“能化……银、铜、铁,奇物”是
指2Ag+S=====Ag S、Fe+S=====FeS、2Cu+S=====Cu S,反应中S作氧化剂,与其氧化
2 2
性有关,C 符合题意;石钟乳(CaCO):“色黄,以苦酒(醋)洗刷则白”是指 CaCO +
3 3
2CHCOOH===(CHCOO) Ca+HO+CO↑,未发生氧化还原反应,与其氧化性无关,D不
3 3 2 2 2符合题意。
3.(2023·广州调研)陈述Ⅰ和陈述Ⅱ均正确且具有因果关系的是( )
选项 陈述 Ⅰ 陈述 Ⅱ
A 用FeCl 溶液刻蚀铜质电路板 氧化性:Fe3+>Cu2+
3
B 用NaO 作呼吸面具的氧气来源 NaO 能氧化CO
2 2 2 2 2
C 用NaS除去废水中的Cu2+和Hg2+ NaS具有还原性
2 2
D 用石灰乳脱除烟气中的SO SO 具有氧化性
2 2
答案 A
解析 用FeCl 溶液刻蚀铜质电路板过程中发生反应:2Fe3++Cu===Cu2++2Fe2+,氧化剂
3
的氧化性强于氧化产物,即氧化性:Fe3+>Cu2+,A项正确;用NaO 作呼吸面具的氧气来
2 2
源时,NaO 自身发生歧化反应,未氧化CO ,B项错误;用NaS除去废水中的Cu2+和Hg2
2 2 2 2
+是发生复分解反应的过程,与NaS的还原性无关,C项错误;用石灰乳脱除烟气中的SO
2 2
过程中,先生成CaSO,后被O 氧化为CaSO,与SO 的氧化性无关,D项错误。
3 2 4 2
4.(2022·辽宁,6)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶
液恢复棕色;加入CCl ,振荡,静置,液体分层。下列说法正确的是( )
4
A.褪色原因为I 被Fe还原
2
B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈
D.溶液恢复棕色的原因为I-被氧化
答案 D
解析 Zn比Fe活泼,更容易失去电子,还原性更强,先与I 发生氧化还原反应,故溶液褪
2
色原因为I 被Zn还原,A项错误;液体分层后,I 在CCl 层,CCl 的密度比水大,则下层
2 2 4 4
呈紫红色,B项错误;若镀层金属活泼性大于Fe,则Fe不易生锈,反之,若Fe活泼性大于
镀层金属,则Fe更易生锈,由于活泼性:Zn>Fe>Sn,则镀锡铁钉更易生锈,C项错误;漂
白粉的有效成分为Ca(ClO) ,其具有强氧化性,可将I-氧化,D项正确。
2
5.关于反应KHIO +9HI===2KI+4I+6HO,下列说法正确的是( )
2 3 6 2 2
A. K HIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7 g I 时,转移0.1 mol电子
2
D.还原剂与氧化剂的物质的量之比为7∶1
答案 D
解析 反应中KHIO 中I元素的化合价降低,发生得电子的还原反应,A错误;KI中的I-
2 3 6
由HI变化而来,化合价没有发生变化,KI既不是氧化产物也不是还原产物,B错误;12.7
g I 的物质的量为0.05 mol,根据反应方程式,每生成4 mol I 转移7 mol电子,则生成0.05
2 2
mol I 时转移电子的物质的量为0.087 5 mol,C错误;反应中HI为还原剂,KHIO 为氧化
2 2 3 6剂,在反应中每消耗1 mol K HIO 就有7 mol HI失电子,则还原剂与氧化剂的物质的量之
2 3 6
比为7∶1,D正确。
6.(2023·德州模拟)工业上以铜阳极泥(主要成分是Cu Te)为原料提取碲,涉及反应:
2
①Cu Te+2O +2HSO ===2CuSO +TeO +2HO,②TeO +2SO +2HO===2HSO +Te。
2 2 2 4 4 2 2 2 2 2 2 4
以下说法正确的是( )
A.Cu Te中Cu元素的化合价是+2价
2
B.反应①中氧化剂是O,氧化产物是TeO
2 2
C.每制备1 mol Te理论上共转移12 mol e-
D.氧化性强弱顺序为O>SO>TeO
2 2 2
答案 C
解析 Te为第ⅥA族元素,与Cu形成化合物时显-2价,则Cu Te中Cu为+1价,A项错
2
误;反应①中,Cu和Te元素化合价均升高,则氧化产物为CuSO 和TeO ,B项错误;反应
4 2
②中每生成1 mol Te,转移4 mol电子,反应①中每生成1 mol TeO ,转移8 mol电子,则每
2
制备1 mol Te,理论上共转移12 mol电子,C项正确;根据反应①判断,氧化剂的氧化性强
于氧化产物,则O 氧化性强于TeO ,根据反应②判断,TeO 为氧化剂,SO 为还原剂,则
2 2 2 2
TeO 氧化性强于SO ,D项错误。
2 2
7.(2021·湖南,8)KIO 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第
3
一步反应为6I+11KClO+3HO=====6KH(IO)+5KCl+3Cl↑。下列说法错误的是( )
2 3 2 3 2 2
A.产生22.4 L(标准状况)Cl 时,反应中转移10 mol e-
2
B.反应中氧化剂和还原剂的物质的量之比为11∶6
C.可用石灰乳吸收反应产生的Cl 制备漂白粉
2
D.可用酸化的淀粉碘化钾溶液检验食盐中IO的存在
答案 A
解析 该反应中只有碘元素的价态升高,由0价升高至KH(IO) 中的+5价,每个碘原子升
3 2
高5价,即6I ~60e-,又因化学方程式中6I ~3Cl ,故3Cl ~60e-,即Cl ~20e-,所以产
2 2 2 2 2
生22.4 L (标准状况) Cl 即1 mol Cl 时,反应中应转移20 mol e-,A错误;该反应中KClO
2 2 3
中氯元素价态降低,KClO 作氧化剂,I 中碘元素价态升高,I 作还原剂,由该化学方程式
3 2 2
的计量数可知,11KClO ~6I ,故该反应的氧化剂和还原剂的物质的量之比为 11∶6,B正
3 2
确;漂白粉的有效成分是次氯酸钙,工业制漂白粉可用石灰乳与氯气反应,C正确;食盐中
IO可先与酸化的淀粉碘化钾溶液中的H+、I-发生归中反应:IO+5I-+6H+===3I+3HO,
2 2
淀粉与生成的I 发生特征反应变为蓝色,故可用酸化的淀粉碘化钾溶液检验食盐中IO的存
2
在,D正确。
8.(2023·青岛模拟)工业上以软锰矿(主要成分为MnO )为主要原料制备高锰酸钾(KMnO)的
2 4
方法如图:已知:①焙烧时有KMnO 和KCl生成。
2 4
②CO 歧化法:调溶液pH至弱碱性,歧化生成KMnO 和MnO 。
2 4 2
下列说法正确的是( )
A.焙烧时所用坩埚的材质可以选用Al O
2 3
B.焙烧时理论上每生成1 mol K MnO 转移3N 个电子
2 4 A
C.电解法与CO 歧化法的理论产率之比为3∶2
2
D.采用CO 歧化法时,可将滤液蒸发结晶得到KMnO 固体
2 4
答案 C
解析 软锰矿中加入 KOH 和 KClO 焙烧,生成 KMnO 和 KCl,电解 KMnO 生成
3 2 4 2 4
KMnO ,或者采用二氧化碳歧化法生成KMnO 。Al O 可与KOH反应,因此焙烧时坩埚的
4 4 2 3
材 质 不 能 选 用 Al O , A 错 误 ; 焙 烧 时 的 化 学 方 程 式 为 3MnO + 6KOH +
2 3 2
KClO=====3KMnO +KCl+3HO,每生成1 mol K MnO ,转移2 mol电子,B错误;电解
3 2 4 2 2 4
法中MnO在阳极上失电子发生反应:MnO-e-===MnO,锰酸根离子全部转化为高锰酸根
离子,CO 歧化法化学方程式为3KMnO +2CO===2KMnO +2KCO +MnO ,有的锰酸根
2 2 4 2 4 2 3 2
离子转化成了高锰酸根离子,两者的理论产率之比为1∶=3∶2,C正确;高锰酸钾受热易
分解,应该采用蒸发浓缩、冷却结晶的方式得到KMnO 固体,D错误。
4
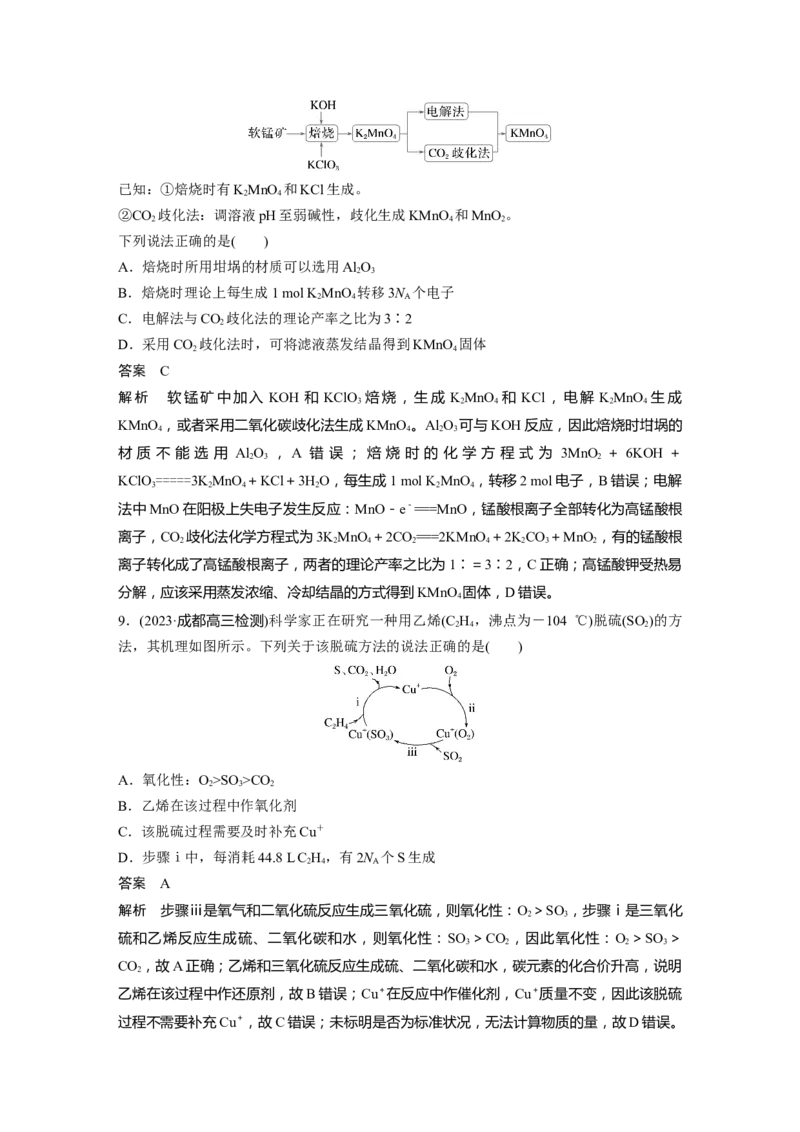
9.(2023·成都高三检测)科学家正在研究一种用乙烯(C H ,沸点为-104 ℃)脱硫(SO )的方
2 4 2
法,其机理如图所示。下列关于该脱硫方法的说法正确的是( )
A.氧化性:O>SO>CO
2 3 2
B.乙烯在该过程中作氧化剂
C.该脱硫过程需要及时补充Cu+
D.步骤ⅰ中,每消耗44.8 L C H,有2N 个S生成
2 4 A
答案 A
解析 步骤ⅲ是氧气和二氧化硫反应生成三氧化硫,则氧化性:O >SO ,步骤ⅰ是三氧化
2 3
硫和乙烯反应生成硫、二氧化碳和水,则氧化性:SO >CO ,因此氧化性:O >SO >
3 2 2 3
CO ,故A正确;乙烯和三氧化硫反应生成硫、二氧化碳和水,碳元素的化合价升高,说明
2
乙烯在该过程中作还原剂,故B错误;Cu+在反应中作催化剂,Cu+质量不变,因此该脱硫
过程不需要补充Cu+,故C错误;未标明是否为标准状况,无法计算物质的量,故D错误。10.(2021·山东,13改编)实验室中利用固体KMnO 进行如图实验,下列说法错误的是(
4
)
A.G与H均为氧化产物
B.实验中KMnO 既是氧化剂又是还原剂
4
C.Mn元素至少参与了3个氧化还原反应
D.G与H的物质的量之和可能为0.25 mol
答案 D
解析 加热KMnO 固体的反应中,O元素化合价由-2升高至0,被氧化,加热KMnO 、
4 2 4
MnO 与浓盐酸的反应中,Cl元素化合价由-1升高至0,被氧化,因此O 和Cl 均为氧化产
2 2 2
物,故A正确;KMnO 固体受热分解过程中,Mn元素化合价降低被还原,部分O元素化
4
合价升高被氧化,因此KMnO 既是氧化剂也是还原剂,故B正确;Mn元素在反应过程中
4
物质及化合价变化为 ,Mn元素至少参加了3个氧
化还原反应,故C正确;每生成1 mol O 转移4 mol电子,每生成1 mol Cl 转移2 mol电子,
2 2
若KMnO 转化为MnCl 过程中得到的电子全部是Cl-生成Cl 所失去的,则气体的物质的量
4 2 2
最大,由2KMnO ~5Cl 可知,n(气体) =0.25 mol,但该气体中一定含有O ,因此最终所
4 2 max 2
得气体的物质的量小于0.25 mol,故D错误。
11.氧化还原反应是一类重要的化学反应。
(1)已知反应:Cu+2Fe3+===Cu2++2Fe2+,反应中还原剂是__________,氧化性:Fe3+
__________(填“<”或“>”)Cu2+。
(2)在2NaO +2CO===2NaCO +O 反应中,若转移3 mol电子,则所产生的氧气在标准状
2 2 2 2 3 2
况下的体积为________ L。
(3)在xR2++yH++O===mR3++nHO的离子方程式中,对系数m和R2+、R3+判断正确的是
2 2
________(填字母)。
A.m=y,R3+是还原剂
B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂
D.m=4,R2+是还原剂
(4)用双线桥标出反应2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO中电子转移的
4 2 2 2
方向和数目。
答案 (1)Cu > (2)33.6 (3)D(4)
解析 (3)根据氧原子守恒则n=2,根据氢原子守恒则y=4,根据R原子守恒则x=m,根据
电荷守恒则2x+y=3m,所以x=y=m=4;在反应中,R的化合价升高,R2+是还原剂,则
R3+是氧化产物,氧元素化合价降低,所以HO是还原产物。
2
12.(2023·济南高三模拟)CuI是难溶于水的白色固体。已知:氧化性:Cu2+>I >Cu+,还
2
原性:Cu>I->Cu+。
(1)根据物质氧化性和还原性的强弱推测,在溶液中 Cu2+和I-反应的产物是________、
__________。
(2)久置于空气中的HI溶液呈黄色,向其中加入一些铜粉,可使溶液黄色消失,反应的化学
方程式为________________________________________________。
(3)欲消除(2)中HI溶液的黄色,也可向其中通入少量HS,这是因为当浓度接近时,还原性:
2
HS__________(填“>”“<”或“=”)I-;与加入铜粉的方法相比,用此方法得到的 HI
2
溶液浓度________(填“高”“低”或“相等”)。
(4)CuI可用于监测空气中是否含有汞蒸气:4CuI(白色)+Hg===Cu HgI (亮黄色)+2Cu。下列
2 4
关于该化学方程式的说法错误的是____________(填字母)。
A.该反应中被氧化的元素是铜元素和汞元素
B.该反应的氧化剂为CuI
C.Cu HgI 既是氧化产物又是还原产物
2 4
D.反应中每生成1 mol Cu HgI 转移2 mol电子
2 4
答案 (1)CuI I (2)2Cu+I===2CuI
2 2
(3)> 高 (4)AC
解析 (1)氧化性:Cu2+>I>Cu+,还原性:Cu>I->Cu+,所以Cu2+和I-反应,Cu2+被还
2
原为Cu+、I-被氧化为I ,Cu+和I-结合生成难溶于水的CuI沉淀,所以反应的产物是
2
CuI、I 。(2)久置于空气中的HI溶液呈黄色,是因为其中的碘离子被氧化为碘单质,加入金
2
属铜,金属铜可以和碘单质反应生成CuI,反应的化学方程式为2Cu+I===2CuI。(3)欲消除
2
HI溶液的黄色,也可向其中通入少量HS,碘单质可以和硫化氢反应生成单质硫和碘化氢,
2
还原性:HS>I-。(4)该反应中Cu元素化合价由+1降低为0,被氧化的元素是汞元素,氧
2
化剂为CuI,Cu HgI 是氧化产物,反应中每生成1 mol Cu HgI 转移2 mol电子。
2 4 2 4
13.某化学探究学习小组用如图所示装置进行SO 、Fe2+和Cl-还原性强弱比较实验,实验
2
过程如下:Ⅰ.先向B中的FeCl 溶液(约10 mL)中通入Cl,当B中溶液变黄时,停止通气。
2 2
Ⅱ.打开活塞k,使约2 mL的溶液流入试管A中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO 气体。
2
Ⅳ.更新试管A,重复过程Ⅱ,检验取出溶液中的离子。
(1)棉花中浸润的溶液为________,目的是___________________________________________
_______________________________________________________________________________
。
(2)实验室制备氯气的化学方程式为_________________________________________________
_______________________________________________________________________________
。
(3)过程Ⅲ中一定发生反应的离子方程式为___________________________________________
_______________________________________________________________________________
;
过程Ⅳ中检验取出溶液中是否含有硫酸根离子的操作是________________________________
_______________________________________________________________________________
。
(4) 该 小 组 对 SO 、 Fe2 + 和 Cl - 还 原 性 强 弱 比 较 得 到 的 结 论 是
2
_____________________________。
(5)甲、乙、丙三位同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一
定 能 够 证 明 SO 、 Fe2 + 和 Cl - 还 原 性 强 弱 关 系 的 是
2
_______________________________________。
过程Ⅱ中检出离子 过程Ⅳ中检出离子
甲 有Fe3+无Fe2+ 有SO
乙 既有Fe3+又有Fe2+ 有SO
丙 有Fe3+无Fe2+ 有Fe2+
答案 (1)NaOH溶液 防止尾气污染环境
(2)MnO +4HCl(浓)=====MnCl +Cl↑+2HO
2 2 2 2
(3)2Fe3++SO +2HO===2Fe2++SO+4H+ 取少许溶液于试管中,先加入足量稀盐酸酸化,
2 2
再滴加少量BaCl 溶液,若有白色沉淀生成,证明有SO,反之无SO
2
(4)SO >Fe2+>Cl- (5)乙、丙
2解析 (1)向B中的FeCl 溶液中通入氯气和二氧化硫,为防止多余的氯气和二氧化硫污染空
2
气,需要将其除去,所以棉花中浸润的溶液为 NaOH溶液。(2)实验室制备氯气用的是二氧
化锰和浓盐酸在加热的条件下反应,化学方程式为 MnO +4HCl(浓)=====MnCl +Cl↑+
2 2 2
2HO。(3)先向B中的FeCl 溶液中通入Cl ,B中的亚铁离子被氯气氧化为铁离子,再向B
2 2 2
中通入一定量的SO 气体,铁离子被二氧化硫还原为亚铁离子,离子方程式为2Fe3++SO +
2 2
2HO===2Fe2++SO+4H+。(5)过程Ⅱ是为了检验Fe2+被氯气氧化后的产物,过程Ⅳ是为了
2
检验二氧化硫被Fe3+氧化后的产物。甲:过程Ⅱ中检出离子有Fe3+无Fe2+,说明氯气过量,
过程Ⅳ中检出离子有SO,不能说明二氧化硫是被铁离子氧化的,也可能是被氯气氧化的,
甲错误;乙:过程Ⅱ中检出离子既有Fe3+又有Fe2+,说明亚铁离子未被氧化完全,氯气量
不足,过程Ⅳ中检出离子有SO,一定是二氧化硫被铁离子氧化得到的,乙正确;丙:过程
Ⅱ检出离子有Fe3+无Fe2+,而过程Ⅳ中检出离子有Fe2+,说明二氧化硫把铁离子还原为亚
铁离子,丙正确。