文档内容
热点强化 23 多曲线、多含义坐标系图像分析
解答复杂图像题应注意的几个要点
(1)复杂图像五看:一看面(坐标),二看线(变化趋势),三看点(起点、交点、终点),四看辅
助线,五看量(数字计算)。如坐标表示的有c(M)、α(M)、lg c(M)、lg 、pM、lg 等,不同
符号表示的意义不同。
(2)pH:可以得出c(H+);通过比较溶质的物质的量浓度可判断是强电解质或弱电解质。
(3)交点:相交的两种物质的某量相等,常进行相互代换用于计算。
(4)pH=7:常温下表示溶液显中性,此时,c(H+)=c(OH-),在等式中常进行抵消。
(5)数据与浓度符号的转化:在坐标图中,标明了某种物质的量,一般要用标明的量进行分
析。
(6)守恒:元素守恒,电荷守恒,质子守恒。
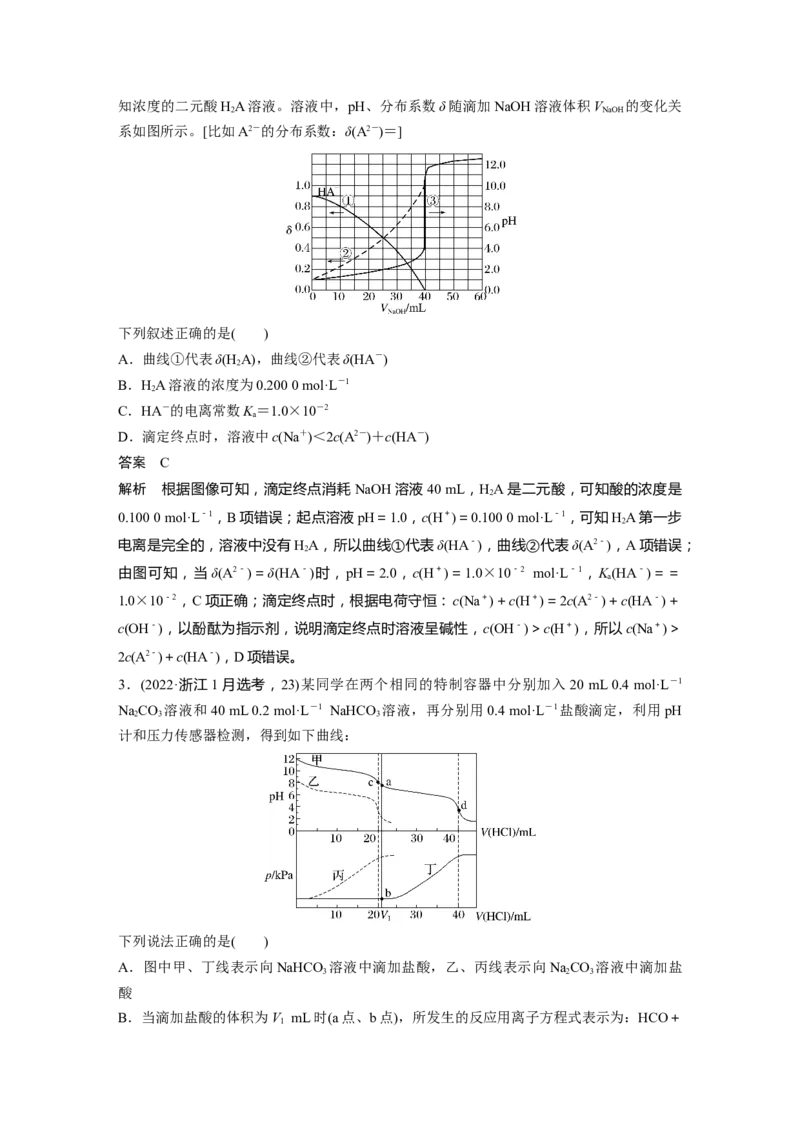
1.(2020·山东,15改编)25 ℃时,某混合溶液中c(CHCOOH)+c(CHCOO-)=0.1 mol·L-
3 3
1,lg c(CHCOOH)、lg c(CHCOO-)、lg c(H+)和lg c(OH-)随pH变化的关系如下图所示。
3 3
K 为CHCOOH的电离常数,下列说法正确的是( )
a 3
A.O点时,c(CHCOOH)=c(CHCOO-)
3 3
B.N点时,pH=lg K
a
C.该体系中,c(CHCOOH)= mol·L-1
3
D.pH由7到14的变化过程中,CHCOO-的水解程度始终增大
3
答案 C
解析 随着溶液碱性的增强,c(CHCOOH)减小,c(CHCOO-)增大,故 MN 线表示 lg
3 3
c(CHCOO-),NP线表示lg c(CHCOOH),MO线表示lg c(H+),OP线表示lg c(OH-)。O
3 3
点时,c(H+)=c(OH-),A项错误;N点时,lg c(CHCOOH)与lg c(CHCOO-)相等,K
3 3 a
=,pH=-lg K ,B项错误;由CHCOOH的电离平衡常数推导可知 K ==c(H+)·,故
a 3 a
c(CHCOOH)= mol·L-1,C项正确;溶液pH增大,碱性增强,CHCOO-的水解程度减小,
3 3
D项错误。
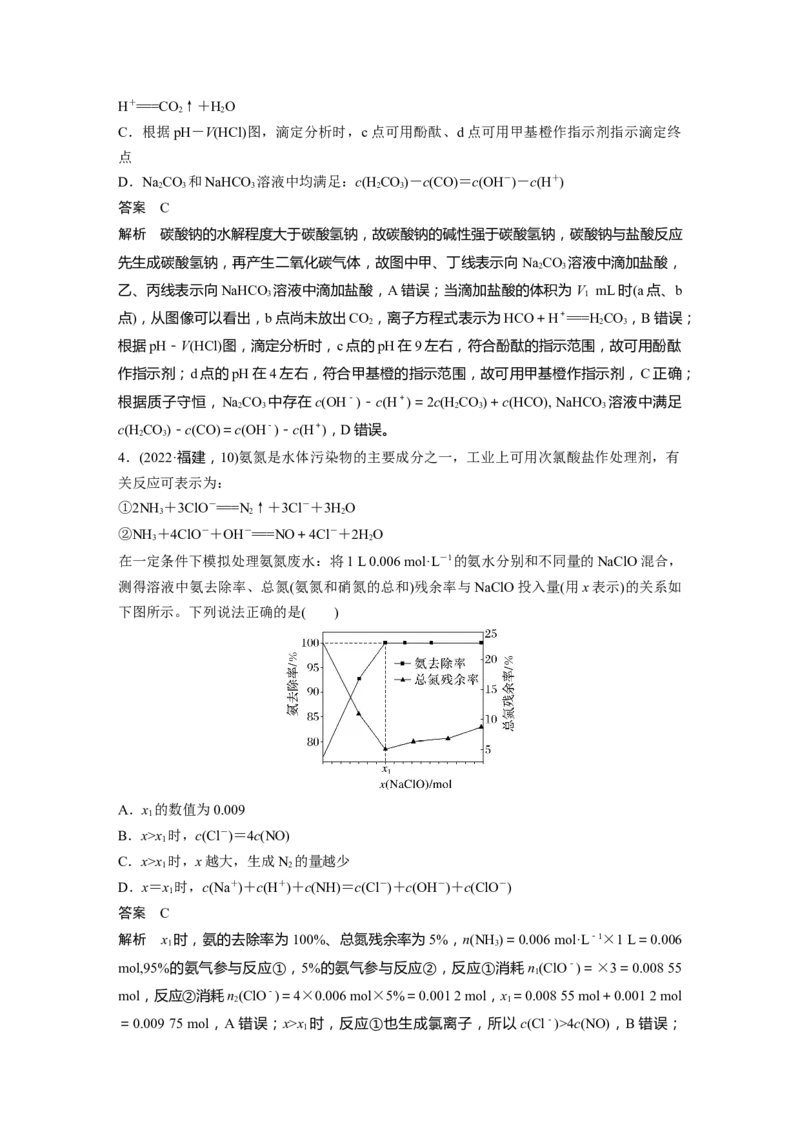
2.(2020·全国卷Ⅰ,13)以酚酞为指示剂,用0.100 0 mol·L-1的NaOH溶液滴定20.00 mL未知浓度的二元酸HA溶液。溶液中,pH、分布系数δ随滴加NaOH溶液体积V 的变化关
2 NaOH
系如图所示。[比如A2-的分布系数:δ(A2-)=]
下列叙述正确的是( )
A.曲线①代表δ(H A),曲线②代表δ(HA-)
2
B.HA溶液的浓度为0.200 0 mol·L-1
2
C.HA-的电离常数K=1.0×10-2
a
D.滴定终点时,溶液中c(Na+)<2c(A2-)+c(HA-)
答案 C
解析 根据图像可知,滴定终点消耗NaOH溶液40 mL,HA是二元酸,可知酸的浓度是
2
0.100 0 mol·L-1,B项错误;起点溶液pH=1.0,c(H+)=0.100 0 mol·L-1,可知HA第一步
2
电离是完全的,溶液中没有HA,所以曲线①代表δ(HA-),曲线②代表δ(A2-),A项错误;
2
由图可知,当 δ(A2-)=δ(HA-)时,pH=2.0,c(H+)=1.0×10-2 mol·L-1,K(HA-)==
a
1.0×10-2,C项正确;滴定终点时,根据电荷守恒:c(Na+)+c(H+)=2c(A2-)+c(HA-)+
c(OH-),以酚酞为指示剂,说明滴定终点时溶液呈碱性,c(OH-)>c(H+),所以c(Na+)>
2c(A2-)+c(HA-),D项错误。
3.(2022·浙江1月选考,23)某同学在两个相同的特制容器中分别加入 20 mL 0.4 mol·L-1
NaCO 溶液和40 mL 0.2 mol·L-1 NaHCO 溶液,再分别用0.4 mol·L-1盐酸滴定,利用pH
2 3 3
计和压力传感器检测,得到如下曲线:
下列说法正确的是( )
A.图中甲、丁线表示向NaHCO 溶液中滴加盐酸,乙、丙线表示向NaCO 溶液中滴加盐
3 2 3
酸
B.当滴加盐酸的体积为V mL时(a点、b点),所发生的反应用离子方程式表示为:HCO+
1H+===CO↑+HO
2 2
C.根据pH-V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终
点
D.NaCO 和NaHCO 溶液中均满足:c(H CO)-c(CO)=c(OH-)-c(H+)
2 3 3 2 3
答案 C
解析 碳酸钠的水解程度大于碳酸氢钠,故碳酸钠的碱性强于碳酸氢钠,碳酸钠与盐酸反应
先生成碳酸氢钠,再产生二氧化碳气体,故图中甲、丁线表示向 NaCO 溶液中滴加盐酸,
2 3
乙、丙线表示向NaHCO 溶液中滴加盐酸,A错误;当滴加盐酸的体积为V mL时(a点、b
3 1
点),从图像可以看出,b点尚未放出CO ,离子方程式表示为HCO+H+===HCO ,B错误;
2 2 3
根据pH-V(HCl)图,滴定分析时,c点的pH在9左右,符合酚酞的指示范围,故可用酚酞
作指示剂;d点的pH在4左右,符合甲基橙的指示范围,故可用甲基橙作指示剂,C正确;
根据质子守恒,NaCO 中存在c(OH-)-c(H+)=2c(H CO)+c(HCO), NaHCO 溶液中满足
2 3 2 3 3
c(H CO)-c(CO)=c(OH-)-c(H+),D错误。
2 3
4.(2022·福建,10)氨氮是水体污染物的主要成分之一,工业上可用次氯酸盐作处理剂,有
关反应可表示为:
①2NH +3ClO-===N↑+3Cl-+3HO
3 2 2
②NH +4ClO-+OH-===NO+4Cl-+2HO
3 2
在一定条件下模拟处理氨氮废水:将1 L 0.006 mol·L-1的氨水分别和不同量的NaClO混合,
测得溶液中氨去除率、总氮(氨氮和硝氮的总和)残余率与NaClO投入量(用x表示)的关系如
下图所示。下列说法正确的是( )
A.x 的数值为0.009
1
B.x>x 时,c(Cl-)=4c(NO)
1
C.x>x 时,x越大,生成N 的量越少
1 2
D.x=x 时,c(Na+)+c(H+)+c(NH)=c(Cl-)+c(OH-)+c(ClO-)
1
答案 C
解析 x 时,氨的去除率为100%、总氮残余率为5%,n(NH )=0.006 mol·L-1×1 L=0.006
1 3
mol,95%的氨气参与反应①,5%的氨气参与反应②,反应①消耗n(ClO-)=×3=0.008 55
1
mol,反应②消耗n(ClO-)=4×0.006 mol×5%=0.001 2 mol,x=0.008 55 mol+0.001 2 mol
2 1
=0.009 75 mol,A错误;x>x 时,反应①也生成氯离子,所以c(Cl-)>4c(NO),B错误;
1x>x 时,氨去除率不变,x越大,总氮残余率越大,说明生成的硝酸根离子越多,生成N 的
1 2
量越少,C正确;x=x 时,氨的去除率为100%,溶液中没有NH和ClO-,含有Na+、H
1
+、NO、Cl-和OH-,根据电荷守恒得c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(NO),D错误。
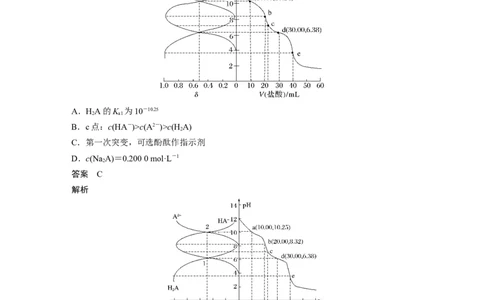
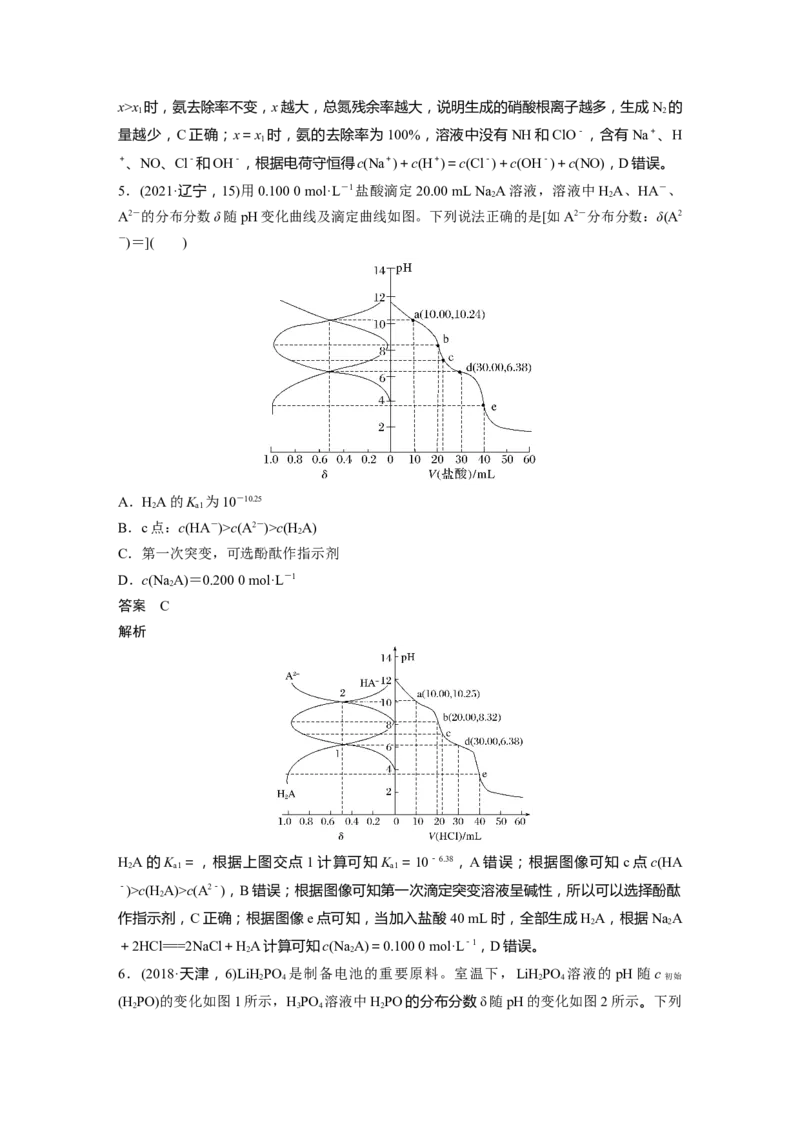
5.(2021·辽宁,15)用0.100 0 mol·L-1盐酸滴定20.00 mL Na A溶液,溶液中HA、HA-、
2 2
A2-的分布分数δ随pH变化曲线及滴定曲线如图。下列说法正确的是[如A2-分布分数:δ(A2
-)=]( )
A.HA的K 为10-10.25
2 a1
B.c点:c(HA-)>c(A2-)>c(H A)
2
C.第一次突变,可选酚酞作指示剂
D.c(Na A)=0.200 0 mol·L-1
2
答案 C
解析
HA的K =,根据上图交点1计算可知K =10-6.38,A错误;根据图像可知 c点c(HA
2 a1 a1
-)>c(H A)>c(A2-),B错误;根据图像可知第一次滴定突变溶液呈碱性,所以可以选择酚酞
2
作指示剂,C正确;根据图像e点可知,当加入盐酸40 mL时,全部生成HA,根据NaA
2 2
+2HCl===2NaCl+HA计算可知c(Na A)=0.100 0 mol·L-1,D错误。
2 2
6.(2018·天津,6)LiH PO 是制备电池的重要原料。室温下,LiH PO 溶液的pH随c
2 4 2 4 初始
(H PO)的变化如图1所示,HPO 溶液中HPO的分布分数δ随pH的变化如图2所示。下列
2 3 4 2有关LiH PO 溶液的叙述正确的是( )
2 4
A.溶液中存在3个平衡
B.含P元素的粒子有HPO、HPO和PO
2
C.随c (H PO)增大,溶液的pH明显变小
初始 2
D.用浓度大于1 mol·L-1的HPO 溶液溶解LiCO ,当pH达到4.66时,HPO 几乎全部转
3 4 2 3 3 4
化为LiH PO
2 4
答案 D
解析 D对:根据图1可知:当LiH PO 的浓度大于1 mol·L-1时其pH=4.66,根据图2可
2 4
知,当pH=4.66时HPO的分布分数达到0.994,即HPO 几乎全部转化为LiH PO ;A错:
2 3 4 2 4
LiH PO 溶液中存在HPO的电离平衡、HPO的电离平衡、HPO的水解平衡、HO的电离平
2 4 2 2 2
衡等至少4个平衡;B错:LiH PO 溶液中含P元素的粒子有HPO、HPO、PO和HPO ;C
2 4 2 3 4
错:LiH PO 溶液的pH随着HPO初始浓度的增大逐渐减小,但当HPO的浓度增大到10-1
2 4 2 2
mol·L-1时,浓度再增大,溶液的pH基本不变。
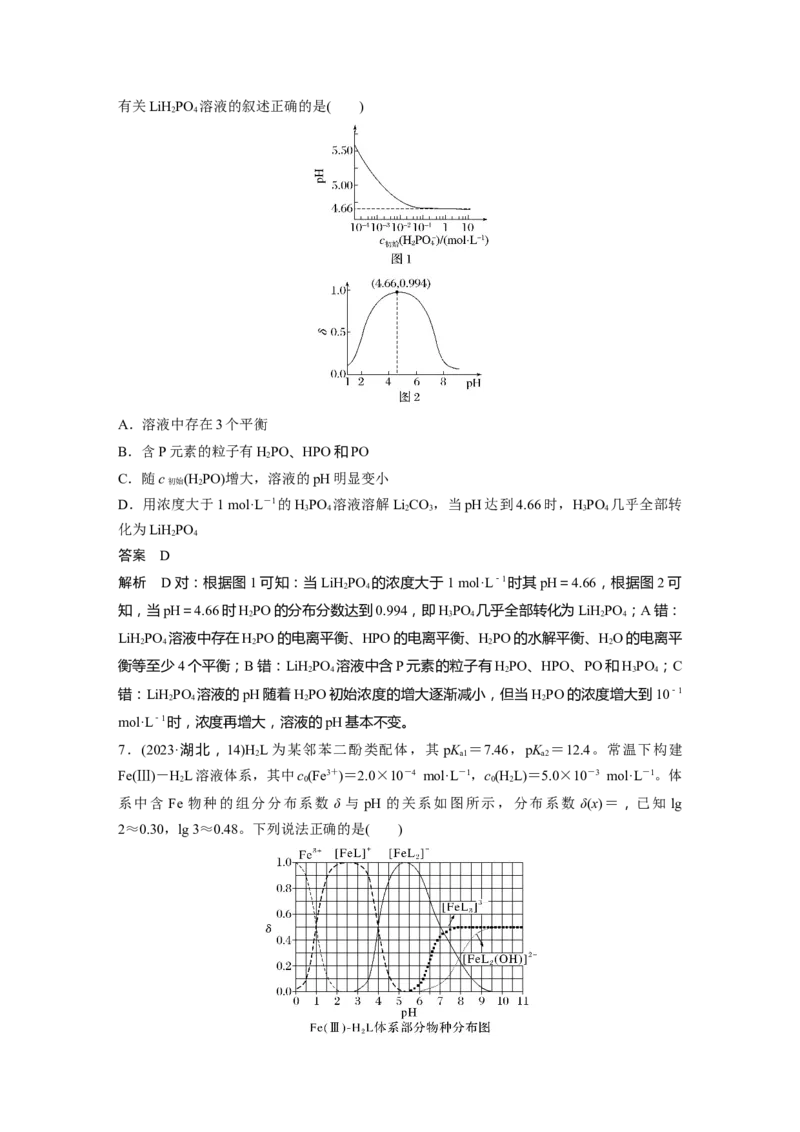
7.(2023·湖北,14)HL为某邻苯二酚类配体,其 pK =7.46,pK =12.4。常温下构建
2 a1 a2
Fe(Ⅲ)-HL溶液体系,其中c(Fe3+)=2.0×10-4 mol·L-1,c(H L)=5.0×10-3 mol·L-1。体
2 0 0 2
系中含 Fe 物种的组分分布系数 δ 与 pH 的关系如图所示,分布系数 δ(x)=,已知 lg
2≈0.30,lg 3≈0.48。下列说法正确的是( )A.当pH=1时,体系中c(H L)>c([FeL]+)>c(OH-)>c(HL-)
2
B.pH在9.5~10.5之间,含L的物种主要为L2-
C.L2-+[FeL]+[FeL ]-的平衡常数的lg K约为14
2
D.当pH=10时,参与配位的c(L2-)≈1.0×10-3 mol·L-1
答案 C
解析 由图可知,pH=1,即c(H+)=0.1 mol·L-1时c([FeL]+)=1.0×10-4 mol·L-1,又
c(H L)=5.0×10-3 mol·L-1,根据 Fe3++HL[FeL]++2H+知,此时 c(H L)=(5.0-
0 2 2 2
0.1)×10-3 mol·L-1=4.9×10-3 mol·L-1,结合 K ==10-7.46知,此时 c(HL-)=10-
a1
7.46×4.9×10-3×10 mol·L-1=4.9×10-9.46 mol·L-1,又pH=1时,c(OH-)=10-13 mol·L-1,
故A错误;pH在9.5~10.5之间时c([FeL ]3-)=c([FeL (OH)]2-)=10-4 mol·L-1,其中两种
3 2
离子共含c(L2-)=3×10-4 mol·L-1+2×10-4 mol·L-1=5×10-4 mol·L-1,当pH=10时,
c(H+)=10-10 mol·L-1,根据K ===10-7.46,c(HL-)=102.54c(H L),即c(HL-)>c(H L),由
a1 2 2
K ==10-12.4,得c(HL-)=102.4c(L2-),即c(HL-)>c(L2-),B、D错误;该反应的平衡常数
a2
K=,由题图知,当c([FeL ]-)=c([FeL]+)时,pH=4,由K ·K =10-19.86=,得①式:10-
2 a1 a2
19.86×c(H L)=10-8c(L2-),此时c(H L)=5.0×10-3 mol·L-1-3×10-4 mol·L-1=4.7×10-3
2 2
mol·L-1,代入①式,c(L2-)= mol·L-1=4.7×10-14.86 mol·L-1,则K=≈2×1013.86,故lg K
=13.86+lg 2≈14,C正确。