文档内容
微专题17 金属及其化合物制备流程(Mo)
一、物质概况:
钼是一种金属元素,元素符号:Mo,英文名称:Molybdenum,原子序数42,是VIB族
金属。钼的密度为10.2g/cm³,熔点为2610℃,沸点为5560℃。钼是一种银白色的金属,
硬而坚韧,熔点高,热传导率也比较高,常温下不与空气发生氧化反应。作为一种过渡
元素,极易改变其氧化状态,钼离子的颜色也会随着氧化状态的改变而改变。钼是人体
及动植物所必需的微量元素,对人以及动植物的生长、发育、遗传起着重要作用。钼在
地壳中的平均含量为0.00011%,全球钼资源储量约为1100万吨,探明储量约为1940万
吨。由于钼具有高强度、高熔点、耐腐蚀、耐磨研等优点,被广泛应用于钢铁、石油、
化工、电气和电子技术、医药和农业等领域。
二、化学性质:
常温或在不太高的温度下,钼在空气或水里是稳定的。钼在空气中加热,颜色开始由白
(色)转暗灰色;温升至520℃,钼开始被缓慢氧化,生成黄色三氧化钼(MoO ,温度降至常
3
温后变为白色);温升至 600℃以上,钼迅速被氧化成 MoO 。钼在水蒸气中加热至
3
700~800℃便开始生成MoO ,将它进一步加热,二氧化钼被继续氧化成三氧化钼。钼在
2
纯氧中可自燃,生成三氧化钼。
钼的这一系列氧化物中,除最高价态的MoO 为酸性外,其余氧化物均为碱性氧化物。钼
3
最重要的氧化物是MoO 和MoO 。
3 2
纯MoO 呈暗灰色、深褐色粉末状。MoO 可溶于水,易溶于盐酸及硝酸,但不溶于氨
2 2
水等碱液里。在空气、水蒸气或氧气中继续加热 MoO ,它将被进一步氧化,直至完全生
2
成MoO 。在真空中加热到1520~1720℃,固态MoO 局部升华而不分解出氧,但大部分
3 2
MoO 分解成 MoO 气体和固态 Mo。Jette. E. R(1935 年)报道:MoO 在 1980℃±50℃、
2 3 2
0.1MPa(惰性气体)的条件下分解成钼和氧。 MoO 是钼氧化的最终产物。
2
MoO 为淡绿或淡青色的白色粉末。MoO 微溶于水而生成钼酸。 MoO 易溶于氨水、碱
3 3 3
金属碱液中,生成与同多酸对应的盐。作为钼的重要化工产品--工业钼酸铵,也正是这一
系列同多酸的铵盐混合物。室温下,钼能与 F 反应。250℃钼开始与 Cl 反应,700~800℃钼可与 Cl 反应生成
2 2 2
MoCl 。在白热温度下,钼能与Br 反应。
2 2
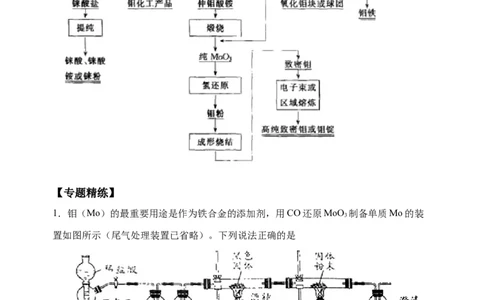
工业上通常用H 还原MoO 以生产金属钼粉。
2 3
钼在常温下不与HF、HCI、稀HNO、稀HSO 及碱溶液反应。钼只溶于浓HNO、王水
3 2 4 3
或热而浓的HSO 、煮沸的HCI中。
2 4
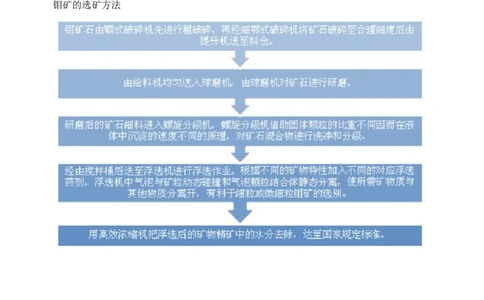
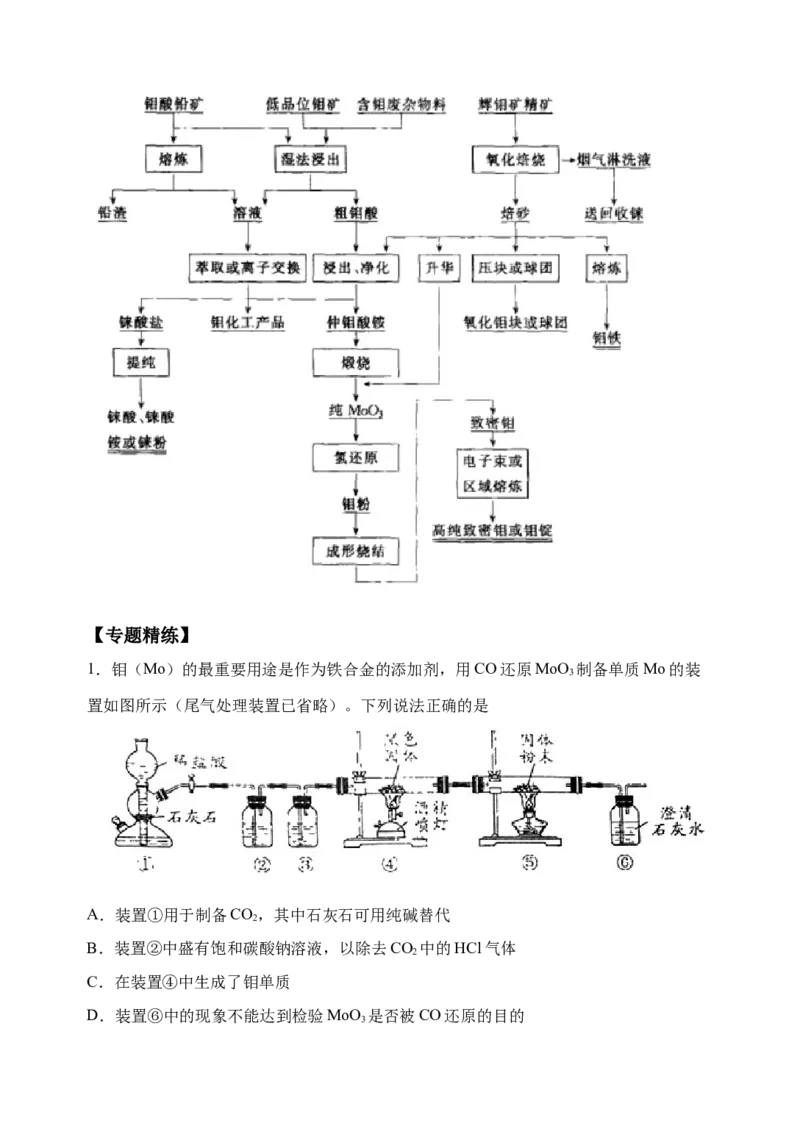
三、钼选矿冶炼工艺
钼矿的选矿方法【专题精练】
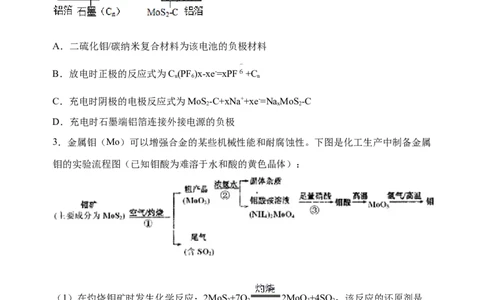
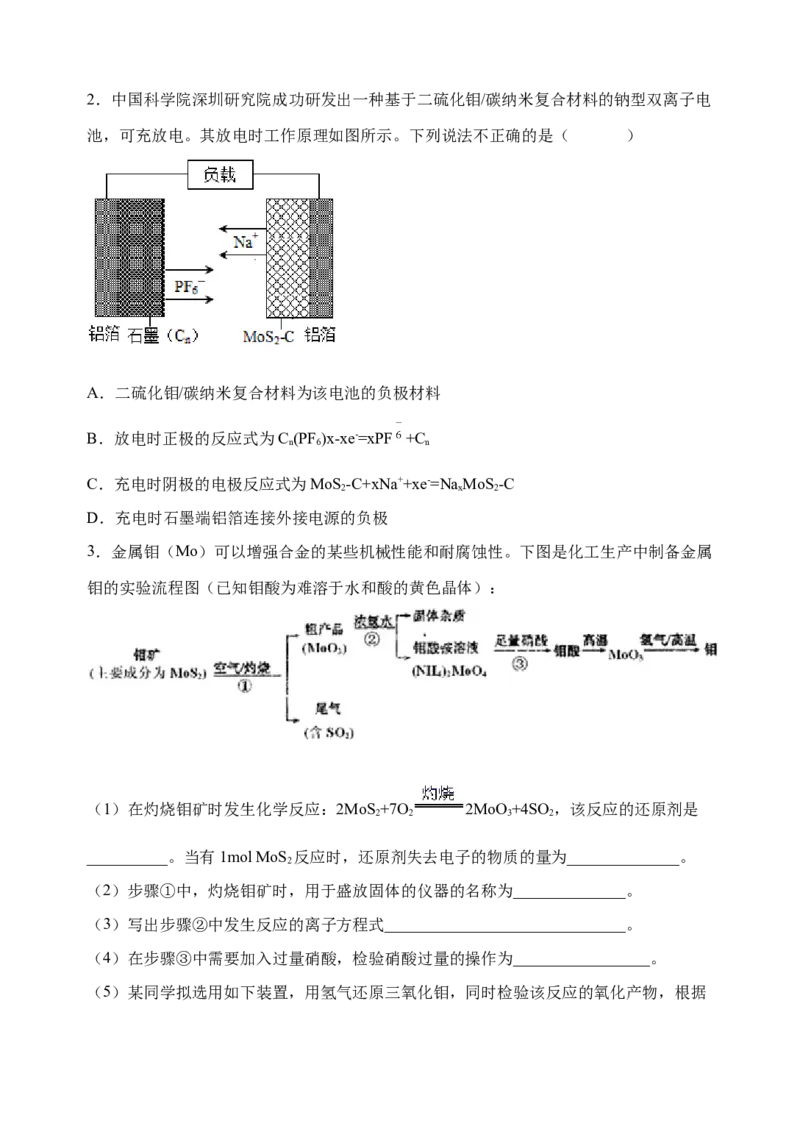
1.钼(Mo)的最重要用途是作为铁合金的添加剂,用CO还原MoO 制备单质Mo的装
3
置如图所示(尾气处理装置已省略)。下列说法正确的是
A.装置①用于制备CO,其中石灰石可用纯碱替代
2
B.装置②中盛有饱和碳酸钠溶液,以除去CO 中的HCl气体
2
C.在装置④中生成了钼单质
D.装置⑥中的现象不能达到检验MoO 是否被CO还原的目的
32.中国科学院深圳研究院成功研发出一种基于二硫化钼/碳纳米复合材料的钠型双离子电
池,可充放电。其放电时工作原理如图所示。下列说法不正确的是( )
A.二硫化钼/碳纳米复合材料为该电池的负极材料
B.放电时正极的反应式为C (PF )x-xe-=xPF +C
n 6 n
C.充电时阴极的电极反应式为MoS -C+xNa++xe-=Na MoS -C
2 x 2
D.充电时石墨端铝箔连接外接电源的负极
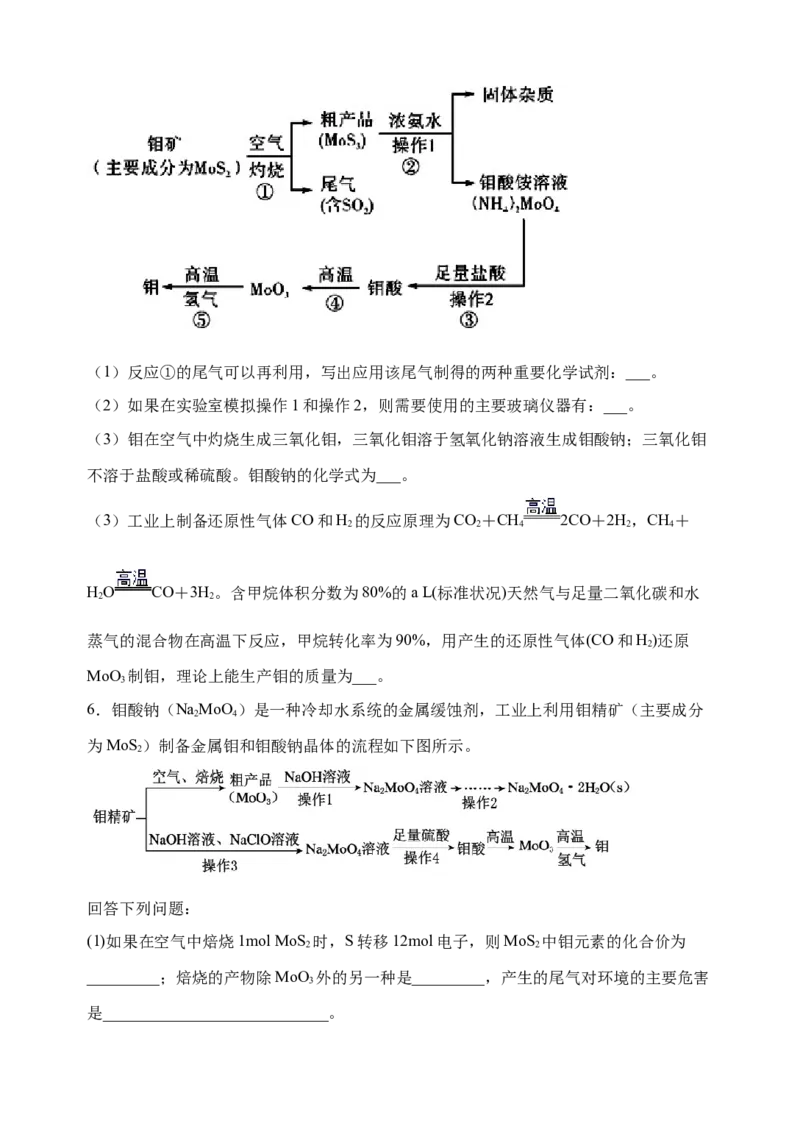
3.金属钼(Mo)可以增强合金的某些机械性能和耐腐蚀性。下图是化工生产中制备金属
钼的实验流程图(已知钼酸为难溶于水和酸的黄色晶体):
(1)在灼烧钼矿时发生化学反应:2MoS +7O 2MoO +4SO,该反应的还原剂是
2 2 3 2
__________。当有1mol MoS 反应时,还原剂失去电子的物质的量为______________。
2
(2)步骤①中,灼烧钼矿时,用于盛放固体的仪器的名称为______________。
(3)写出步骤②中发生反应的离子方程式______________________________。
(4)在步骤③中需要加入过量硝酸,检验硝酸过量的操作为_________________。
(5)某同学拟选用如下装置,用氢气还原三氧化钼,同时检验该反应的氧化产物,根据要求回答下列问题。
①若两次使用到C装置,则装置D中所盛的药品是___________(填试剂名称)。
②根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开
分液漏斗活塞后_________→_________→_________→_________(请按正确的顺序填入
下列步骤的代号)。
a.收集气体并检验其纯度 b.停止加热,充分冷却
c.加热反应一段时间 d.关闭分液漏斗活塞,停止通氢气
(6)化学分析中,常用沉淀法测定金属的含量。若称取三氧化钼粗产品m g,用浓氨水
溶解后,再滴加足量的硝酸使其完全转化为钼酸沉淀,此时消耗0.2 mol/L HNO 溶液
3
250mL ,则粗产品中三氧化钼的含量为_______(请用含m的表达式表示)。
4.纳米级 复合材料被认为是一种理想的钠离子电池负极材料,以钼精矿[主要成分
,以及 、 、 、 、 等杂质]为原料生产纳米级
的工业流程如下:已知:i. 不溶于水和常见的酸碱,“烧熔”时可转化为酸性氧化物 ;
ii. 经“烧熔”后可与沸盐酸反应。
(1)“粉碎”的目的为___________。
(2)滤液②中含有的金属离子为___________;滤渣②的成分为___________。
(3)“碱浸”时发生反应的化学方程式为___________;用 溶液代替氨水的不足之处
为___________。
(4)已知“硫代”一步生成了 ,则“沉钼”中加入盐酸生成 的离子方程式为
___________。
(5)用 “加热还原” ,实际操作时需注意的问题为___________。
(6)分析化学上,常利用“沉钼”反应测定钼的含量,若称量54.0g钼精矿,“沉钼”时得
到28.8g ,则钼精矿中钼的百分含量为___________(转化工艺中钼的损失不计,保
留三位有效数字)。
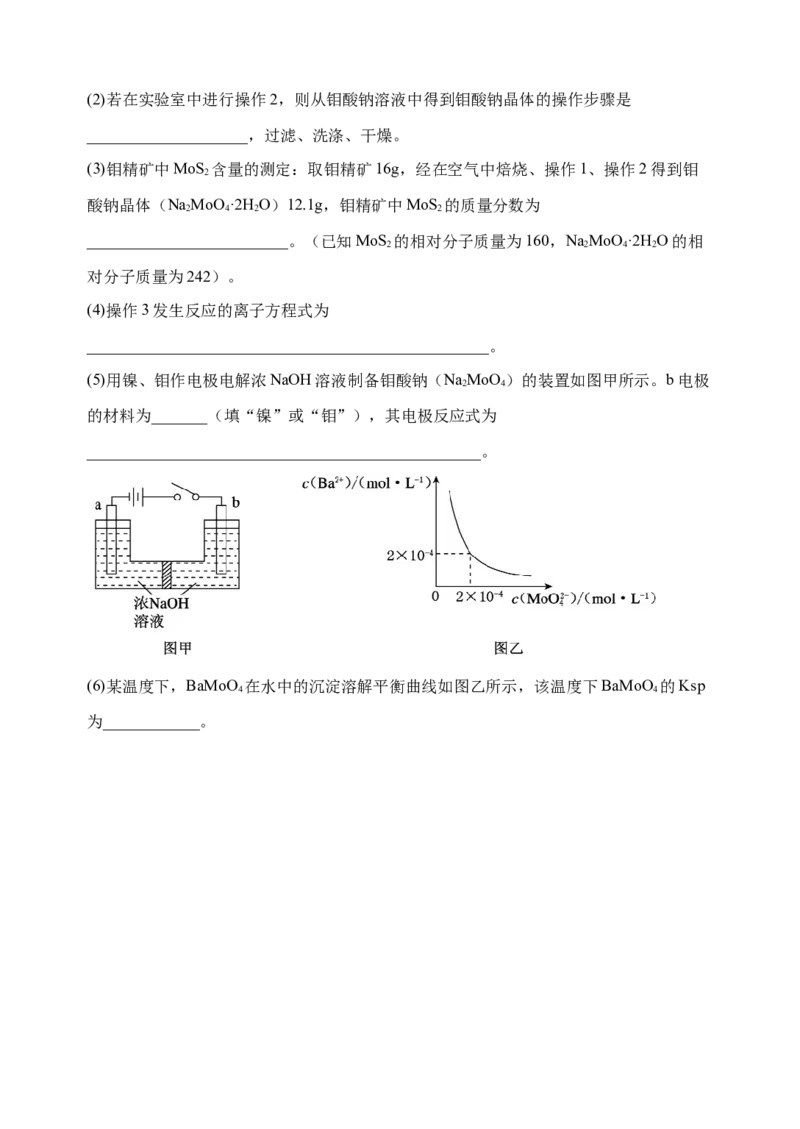
5.钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强
度、硬度、可焊接性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备
金属钼的主要流程图。(1)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂:___。
(2)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有:___。
(3)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼
不溶于盐酸或稀硫酸。钼酸钠的化学式为___。
(3)工业上制备还原性气体CO和H 的反应原理为CO+CH 2CO+2H,CH+
2 2 4 2 4
HO CO+3H。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水
2 2
蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H)还原
2
MoO 制钼,理论上能生产钼的质量为___。
3
6.钼酸钠(NaMoO )是一种冷却水系统的金属缓蚀剂,工业上利用钼精矿(主要成分
2 4
为MoS )制备金属钼和钼酸钠晶体的流程如下图所示。
2
回答下列问题:
(1)如果在空气中焙烧1mol MoS 时,S转移12mol电子,则MoS 中钼元素的化合价为
2 2
_________;焙烧的产物除MoO 外的另一种是_________,产生的尾气对环境的主要危害
3
是____________________________。(2)若在实验室中进行操作2,则从钼酸钠溶液中得到钼酸钠晶体的操作步骤是
____________________,过滤、洗涤、干燥。
(3)钼精矿中MoS 含量的测定:取钼精矿16g,经在空气中焙烧、操作1、操作2得到钼
2
酸钠晶体(NaMoO ·2H O)12.1g,钼精矿中MoS 的质量分数为
2 4 2 2
_________________________。(已知MoS 的相对分子质量为160,NaMoO ·2H O的相
2 2 4 2
对分子质量为242)。
(4)操作3发生反应的离子方程式为
__________________________________________________。
(5)用镍、钼作电极电解浓NaOH溶液制备钼酸钠(NaMoO )的装置如图甲所示。b电极
2 4
的材料为_______(填“镍”或“钼”),其电极反应式为
_________________________________________________。
(6)某温度下,BaMoO 在水中的沉淀溶解平衡曲线如图乙所示,该温度下BaMoO 的Ksp
4 4
为____________。