文档内容
易错点 16 分子结构与性质
易错题【01】VSEPR模型和空间构型
①VSEPR模型反映中心原子的价层电子对的空间结构,而分子(或离子)的空间结构是指
σ键电子对的空间构型,不包括孤电子对。
②VSEPR模型和分子的空间构型不一定相同,还要看中心原子是否有孤电子对,若不含孤
电子对,二者空间构型相同,否则,不相同。
③根据VSEPR模型判断分子(或离子)的空间结构时,要略去孤电子对。
易错题【02】判断中心原子杂化轨道类型的方法
(1)根据杂化轨道的空间分布构型:①直线形—sp,②平面三角形—sp2,③四面体形—
sp3。
(2)根据杂化轨道间的夹角:①109.28°—sp3,②120°—sp2,③180°—sp。
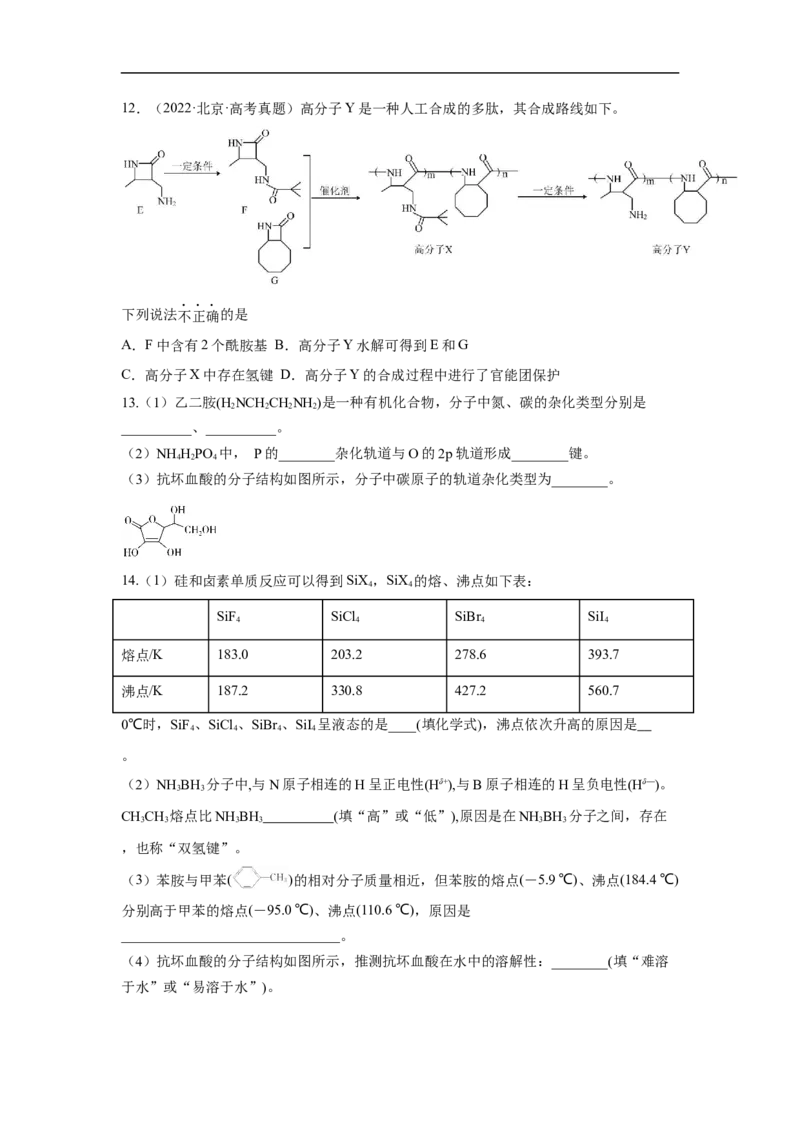
(3)利用价层电子对数确定三种杂化类型(适用于中心粒子):2对—sp杂化,3对—sp2杂化,
4对—sp3杂化。
(4)根据σ键数与孤电子对数(适用于结构式已知的粒子):①含C有机物:2个σ—sp,3个σ
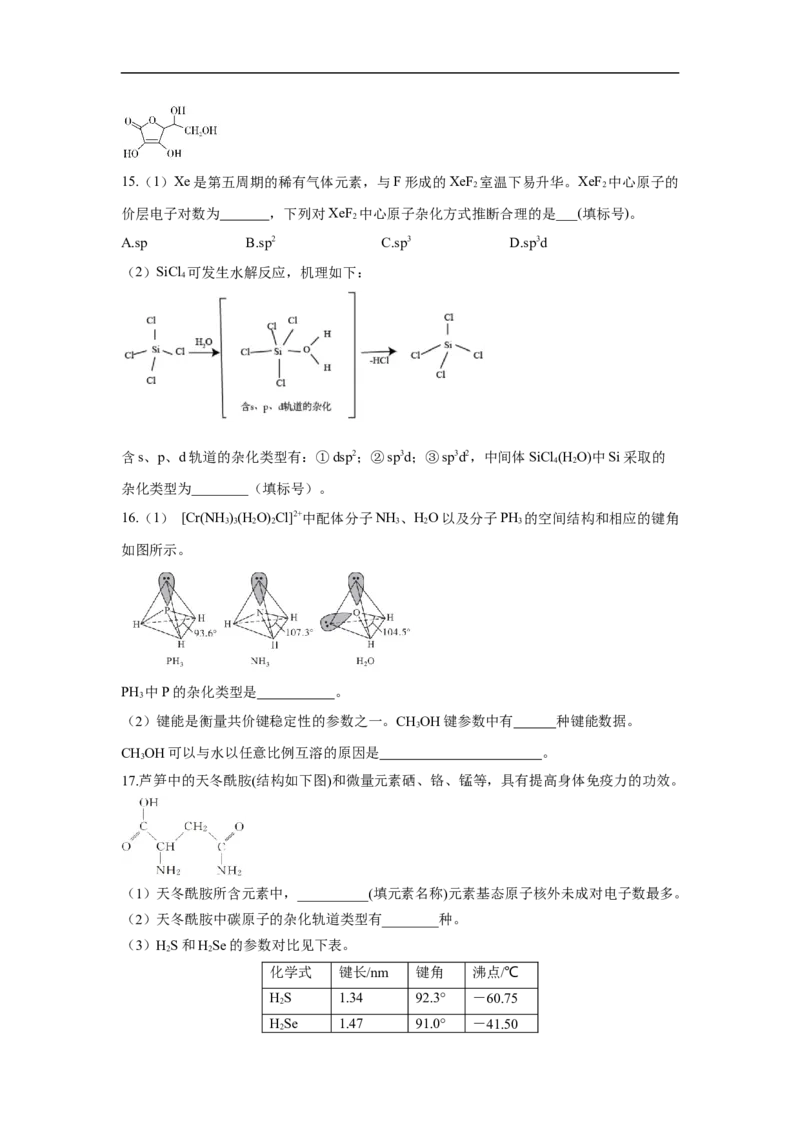
—sp2,4个σ—sp3。②含N化合物:2个σ—sp2,3个σ—sp3。③含O(S)化合物:2个σ—sp3。
(5)根据等电子原理:如CO 是直线形分子,CNS-、N与CO 是等电子体,所以分子构型
2 2
均为直线形,中心原子均采用sp杂化。
易错题【03】共价键的极性与分子极性的关系
易错题【04】共价键和分子间作用力的比较
分子间作用力 共价键
氢键(包括分子内氢 极性共价键、非极性
分类 范德华力
键、分子间氢键) 共价键
分子或原子(稀有气 氢原子与氧原子、
作用粒子 原子
体) 氮原子或氟原子
特征 无方向性、饱和性 有方向性、饱和性 有方向性、饱和性
强度比较 共价键>氢键>范德华力对于A—H…B,
随着分子极性和相对 成键原子半径越小,
影响其强度的因 A、B的电负性越
分子质量的增大而增 键长越短,键能越
素 大,B原子的半径
大 大,共价键越稳定
越小,作用力越大
①影响物质的熔、沸
点和溶解度等物理性 分子间氢键的存
质; 在,使物质的熔、
②组成和结构相似的 沸点升高,在水中 影响分子的稳定性,
对物质性质的影
物质,随相对分子质 的溶解度增大,如 共价键键能越大,分
响
量的增大,物质熔、 熔、沸点: 子稳定性越强
沸点升高,如熔、沸 HO>HS,
2 2
点:FHCl,NH >PH
2 2 2 2 3 3
CF