文档内容
易错点 26 沉淀溶解平衡
易错题【01】沉淀溶解平衡图像
(1)明确图像中纵、横坐标的含义:纵、横坐标通常是难溶物溶解后电离出的离子浓度。
(2)理解图像中线上点、线外点的含义:难溶电解质(以BaSO 沉淀曲线为例说明)Q 和
4 c
K 间的关系有以下三种可能:在曲线上任何一点,Q=K ,沉淀与溶解达到动态平衡,溶
sp c sp
液是饱和溶液。
在曲线右上方Q>K ,溶液处于过饱和,有沉淀析出,直至Q=K 。
c sp c sp
在曲线左下方Q<K ,为不饱和溶液,无沉淀析出,直至Q=K 。
c sp c sp
(3)抓住K 的特点,结合选项分析判断:溶度积常数只是温度的函数,与溶液中溶质的离子
sp
浓度无关,在同一曲线上的点,溶度积常数相同。原溶液不饱和时,离子浓度都增大,原溶液
饱和时,离子浓度都不。
易错题【02】有关K 的相关计算
sp
(1)已知溶度积,求溶液中的某种离子的浓度,如K (AgCl)=a的饱和AgCl溶液中,c(Ag+)=√a
sp
mol·L-1。
(2)已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下AgCl的
K =a,在0.1 mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。
sp
(3)计算反应的平衡常数,如对于反应Cu2+(aq)+MnS(s) CuS(s)+Mn2+
(aq),K (MnS)=c(Mn2+)·c(S2-),K (CuS)=c(Cu2+)·c(S2-),该反应的平衡常数K=
sp sp
c(Mn2+) K (MnS)
= sp 。
c(Cu2+) K (CuS)
sp
易错题【03】沉淀的生成
(1)利用生成沉淀分离或除去某种离子,首先要使生成沉淀的反应能够发生,其次沉淀生成的
反应进行的越完全越好。如除去溶液中的Mg2+,用NaOH溶液比使用NaCO 溶液好,原因是
2 3
Mg(OH) 的溶解度比MgCO 的小。
2 3
(2)若一种沉淀剂可使溶液中多种离子产生沉淀时,则可以控制条件,使这些离子先后分别沉
淀。
①对同一类型的沉淀,K 越小越先沉淀,且K 相差越大分步沉淀效果越好。例如在浓度相差
sp sp
不大的Cl-、Br-、I-的混合溶液中,由于AgCl、AgBr、AgI的K 相差较大,可向混合溶液中逐
sp渐滴加AgNO 溶液,可按AgI、AgBr、AgCl的顺序先后沉淀。
3
②对不同类型的沉淀,其沉淀先后顺序要通过计算才能确定
典例分析
例题1、t ℃时,两种碳酸盐MCO (M表示X2+或Y2+)的沉淀溶解平衡曲线如图所示。已知:
3
pM=-lgc(M2+),p(CO)=-lgc(CO),K (XCO )<K (YCO )。下列说法正确的是( )
sp 3 sp 3
A.线a表示YCO 的溶解平衡曲线
3
B.K (XCO )=1.0×10-8
sp 3
C.t ℃时,向XCO 悬浊液中加入饱和Y(NO) 溶液,可能有YCO 生成
3 3 2 3
D.t ℃时,向饱和YCO 溶液中加入NaCO 溶液,一定能产生YCO 沉淀
3 2 3 3
C【解析】K (XCO )=c(X2+)c(CO),K (YCO )=c(Y2+)c(CO);又因K (XCO )<
sp 3 sp 3 sp 3
K (YCO ),所以c(CO)相同时,c(X2+)<c(Y2+),pc(X2+)>pc(Y2+),所以a为XCO 的溶解
sp 3 3
平衡曲线,b为YCO 的溶解平衡曲线,A错误;K (XCO )=c(X2+)c(CO)=10-4 mol·L-
3 sp 3
1×100 mol·L-1=10-4,B错误;虽然K (XCO )<K (YCO ),溶解度小的沉淀转化成溶解度
sp 3 sp 3
更小的沉淀容易实现,沉淀转化的平衡移动原理为X2+(aq)+YCO (s) XCO (s)+Y2+(aq),
3 3
但加入饱和Y(NO) 溶液,增大了c(Y2+),使平衡逆向移动,可能会有⇌YCO 生成,C正确;
3 2 3
YCO 沉淀溶解的原理,YCO (s) CO(aq)+Y2+(aq),向饱和YCO 溶液中加入NaCO 溶
3 3 3 2 3
液,不知NaCO 溶液的浓度,无法确定是否一定能产生YCO 沉淀,D错误。
2 3 3
例题2、25 ℃时,下列4种盐的溶度积常数(K )分别如下表,结合相关数据分析,下列说法错误
sp
的是 (
Ag SO (白色) Ag S(黑色) FeS(黑色) MnS(肉色)
2 4 2
1.4×10-5 6.3×10-50 3.3×10-18 2.5×10-13
mol3·L-3 mol3·L-3 mol2·L-2 mol2·L-2
A.除去某溶液中的Ag+用NaS溶液比NaSO 溶液效果好
2 2 4
B.25 ℃时,MnS的溶解度大于FeS的溶解度
C.向少量FeS悬浊液中加入足量饱和MnCl 溶液,沉淀颜色会由黑色变为肉色
2D.向Ag S(s) 2Ag+(aq)+S2-(aq)平衡体系中加入少量NaS固体,溶液中c(Ag+)不变
2 2
D【解析】K (Ag S) ×104
4 3
C.过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
D.滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
2.(2022·重庆一中模拟预测)室温下,在 悬浊液中存在如下平衡:
,已知
下列说法错误的是
A.平衡时,
B.平衡时,
C.该温度下,
D.加入少量 固体, 减小, 增大
3.(2022·山西晋中·二模)下列实验中,现象及结论都正确,且二者之间有因果关系的是
选项 实验操作 现象 结论
A 向FeI 溶液中通入少量Cl 溶液变黄 Cl 的氧化性强于Fe3+
2 2 2
向NaCl、NaBr的混合稀溶液中滴入少量 有浅黄色
B K (AgCl) > K (AgBr)
稀AgNO 3 溶液 沉淀生成 sp sp
C 常温下,向NaHS溶液中滴加石蕊试液 溶液变蓝 K >K (H S)·K (H S)
w a1 2 a2 2
向盛有2 mL一定浓度的Na [Ag(S O)]
3 2 3 2 产生黄色沉
D [Ag(S O)]3- 能够完全电离
淀 2 3 2
溶液的试管中,滴入5滴2 mol· L-1KI溶液
4.(2022·山东·高考真题)工业上以 为原料生产 ,对其工艺条件进行研
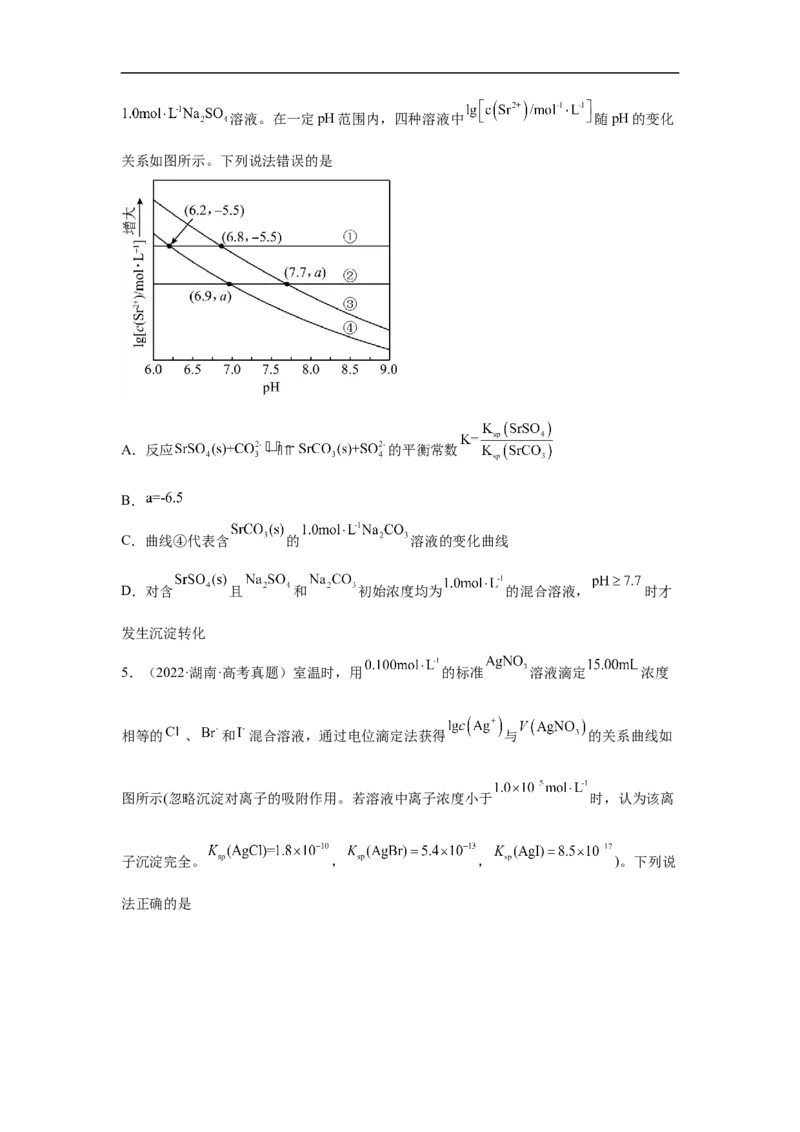
究。现有含 的 、 溶液,含 的 、溶液。在一定pH范围内,四种溶液中 随pH的变化
关系如图所示。下列说法错误的是
A.反应 的平衡常数
B.
C.曲线④代表含 的 溶液的变化曲线
D.对含 且 和 初始浓度均为 的混合溶液, 时才
发生沉淀转化
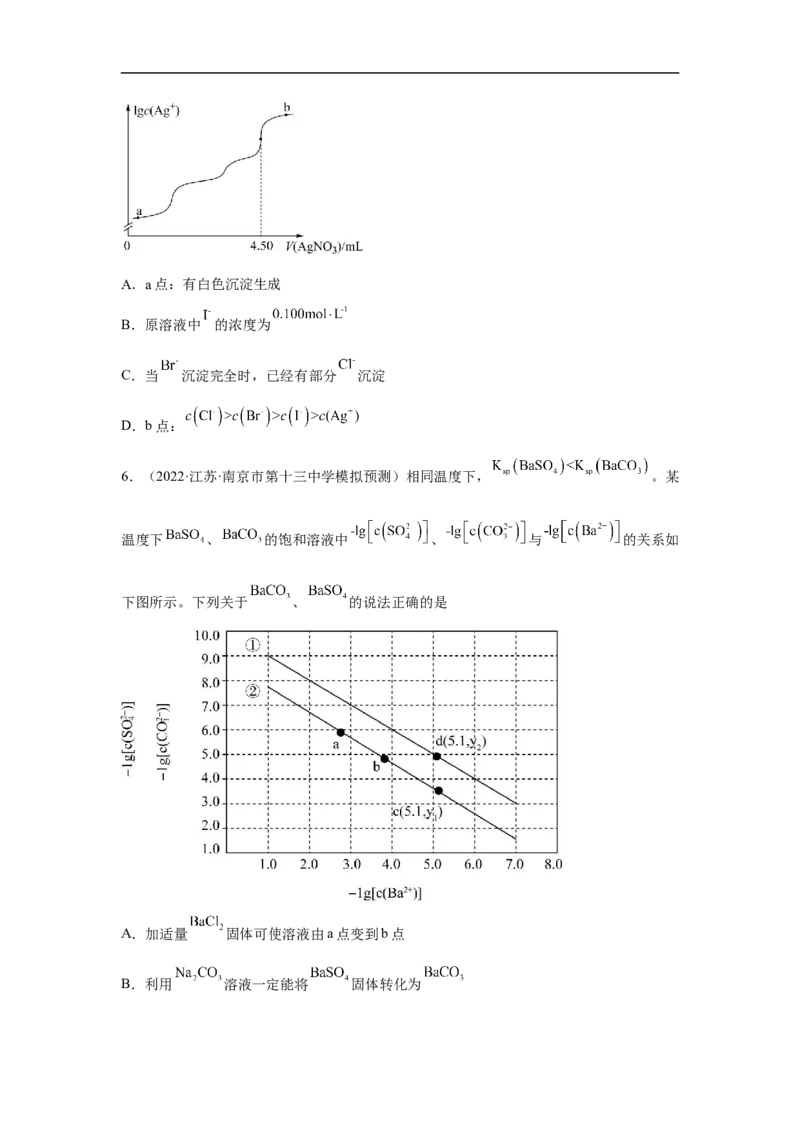
5.(2022·湖南·高考真题)室温时,用 的标准 溶液滴定 浓度
相等的 、 和 混合溶液,通过电位滴定法获得 与 的关系曲线如
图所示(忽略沉淀对离子的吸附作用。若溶液中离子浓度小于 时,认为该离
子沉淀完全。 , , )。下列说
法正确的是A.a点:有白色沉淀生成
B.原溶液中 的浓度为
C.当 沉淀完全时,已经有部分 沉淀
D.b点:
6.(2022·江苏·南京市第十三中学模拟预测)相同温度下, 。某
温度下 、 的饱和溶液中 、 与 的关系如
下图所示。下列关于 、 的说法正确的是
A.加适量 固体可使溶液由a点变到b点
B.利用 溶液一定能将 固体转化为C. 时,两者饱和液中
D.向 、 饱和溶液中加入少量 固体,溶液中 减小
7.(2022·安徽蚌埠·三模)已知298K时,K (NiS)=1.0×10-21,K (FeS)=6.0×10-18,其沉淀
sp sp
溶解平衡曲线如图所示(图中R表示Ni或Fe),下列说法正确的是(已知: ≈2.4,
≈3.2)
A.M点对应的溶液中,c(S2-)≈3.2×10-11mol·L-1
B.与P点相对应的NiS的分散系是均一稳定的
C.向Q点对应的溶液中加水,可转化成N点对应的溶液
D.FeS+Ni2+ NiS+Fe2+的平衡常数K=6000
8.(2022·四川省泸县第二中学一模)某温度下,向10mL0.1mol/LCuCl 溶液中滴加
2
0.1mol/L的NaS溶液,滴加过程中溶液里-lgc(Cu2+)与NaS溶液体积[V(Na S)]的关系如图
2 2 2
所示。已知:K (ZnS)=3.0×10-25,下列有关说法正确的是
sp
A.a、b、c三点中,水的电离程度最大的为b点
B.该温度下K (CuS)=1.0×10-18
sp
C.该温度下反应:ZnS(s)+Cu2+(aq) CuS(s)+Zn2+(aq)的平衡常数为3.33×10-11D.如果忽略CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H S)]=c(Cl-)
2
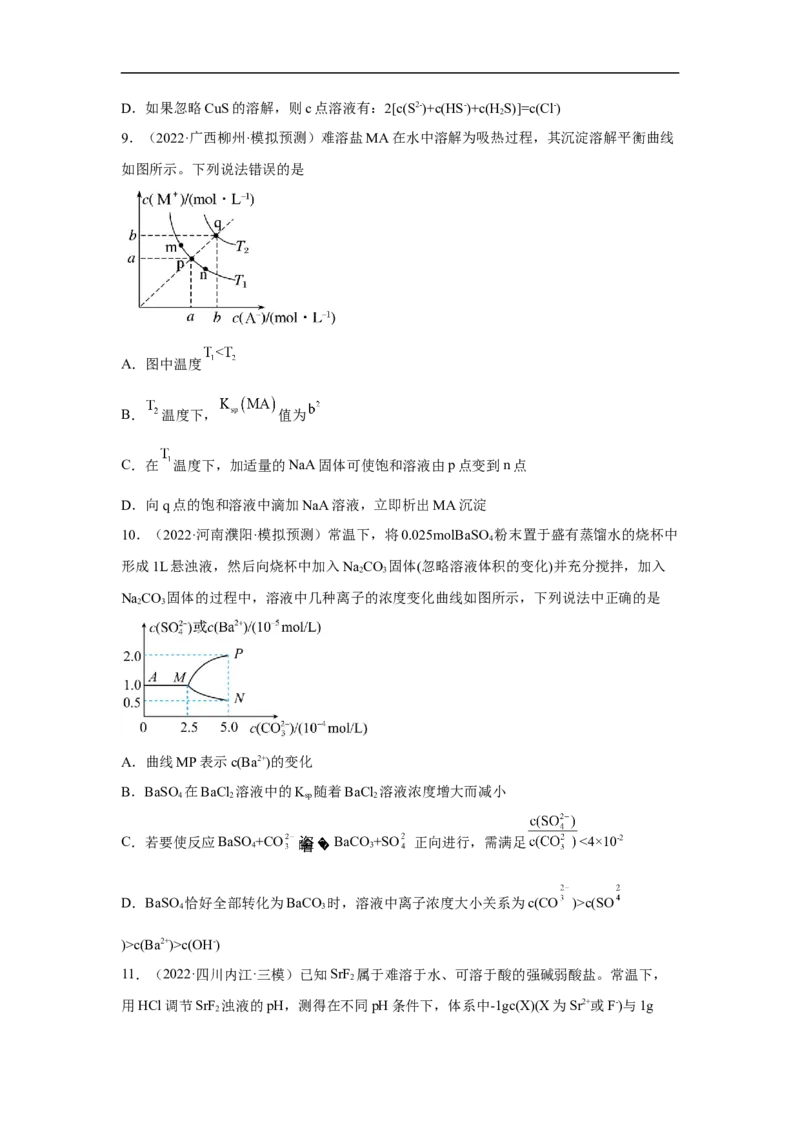
9.(2022·广西柳州·模拟预测)难溶盐MA在水中溶解为吸热过程,其沉淀溶解平衡曲线
如图所示。下列说法错误的是
A.图中温度
B. 温度下, 值为
C.在 温度下,加适量的NaA固体可使饱和溶液由p点变到n点
D.向q点的饱和溶液中滴加NaA溶液,立即析出MA沉淀
10.(2022·河南濮阳·模拟预测)常温下,将0.025molBaSO 粉末置于盛有蒸馏水的烧杯中
4
形成1L悬浊液,然后向烧杯中加入NaCO 固体(忽略溶液体积的变化)并充分搅拌,加入
2 3
NaCO 固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是
2 3
A.曲线MP表示c(Ba2+)的变化
B.BaSO 在BaCl 溶液中的K 随着BaCl 溶液浓度增大而减小
4 2 sp 2
C.若要使反应BaSO+CO BaCO +SO 正向进行,需满足 <4×10-2
4 3
D.BaSO 恰好全部转化为BaCO 时,溶液中离子浓度大小关系为c(CO )>c(SO
4 3
)>c(Ba2+)>c(OH-)
11.(2022·四川内江·三模)已知SrF 属于难溶于水、可溶于酸的强碱弱酸盐。常温下,
2
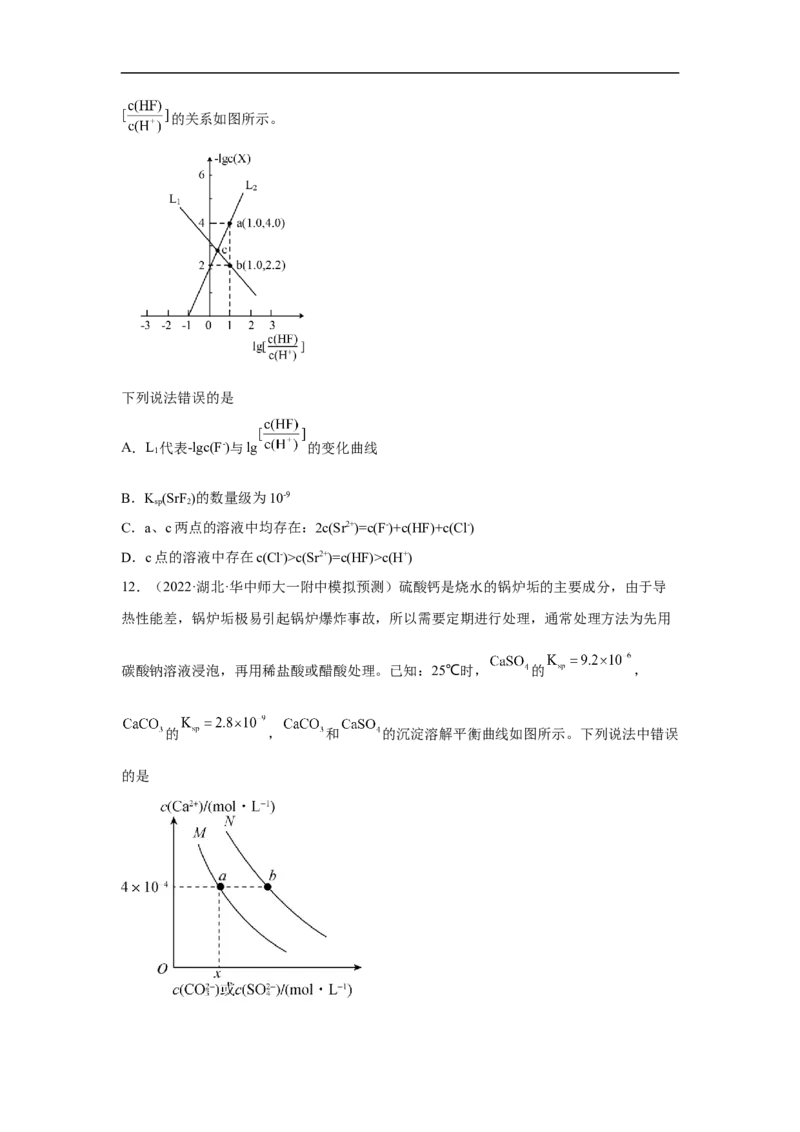
用HCl调节SrF 浊液的pH,测得在不同pH条件下,体系中-1gc(X)(X为Sr2+或F-)与1g
2的关系如图所示。
下列说法错误的是
A.L 代表-lgc(F-)与lg 的变化曲线
1
B.K (SrF )的数量级为10-9
sp 2
C.a、c两点的溶液中均存在:2c(Sr2+)=c(F-)+c(HF)+c(Cl-)
D.c点的溶液中存在c(Cl-)>c(Sr2+)=c(HF)>c(H+)
12.(2022·湖北·华中师大一附中模拟预测)硫酸钙是烧水的锅炉垢的主要成分,由于导
热性能差,锅炉垢极易引起锅炉爆炸事故,所以需要定期进行处理,通常处理方法为先用
碳酸钠溶液浸泡,再用稀盐酸或醋酸处理。已知:25℃时, 的 ,
的 , 和 的沉淀溶解平衡曲线如图所示。下列说法中错误
的是A.水垢处理过程中,加入稀盐酸时主要离子反应为
B.M和N分别代表 和 的沉淀溶解平衡曲线
C.图中
D.用碳酸钠溶液浸泡锅炉垢,可实现图中a点到b点的转化
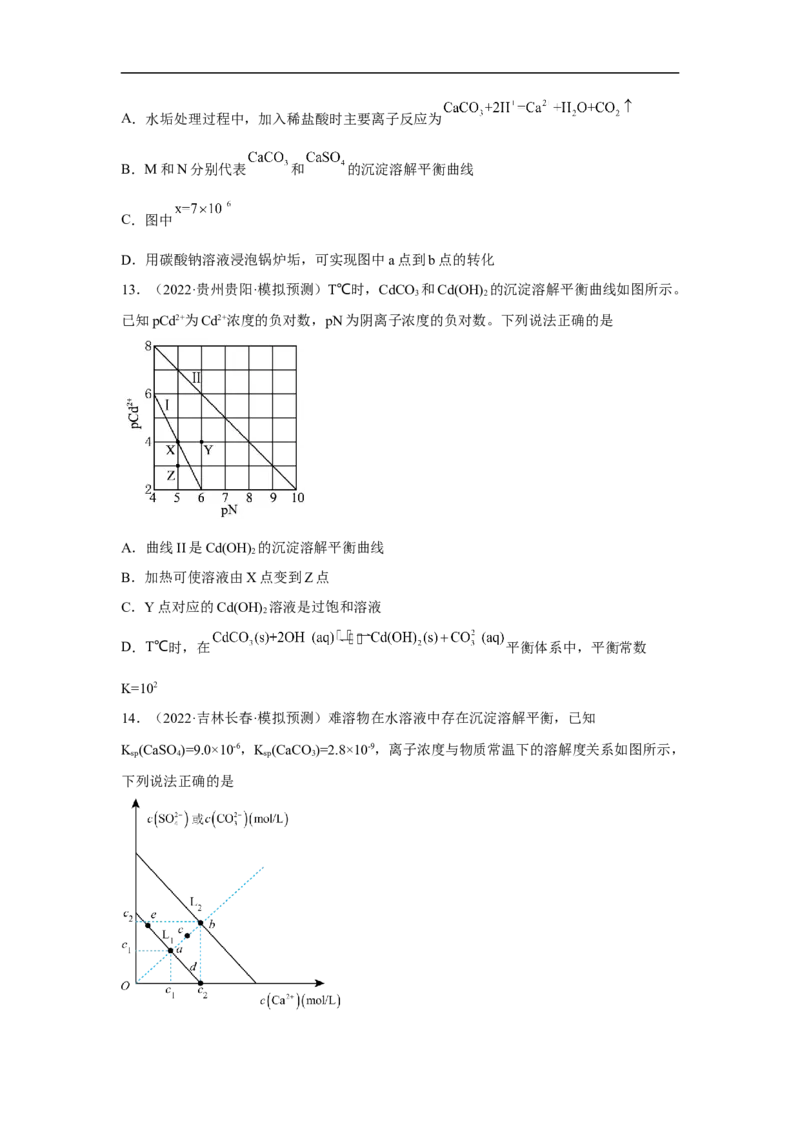
13.(2022·贵州贵阳·模拟预测)T℃时,CdCO 和Cd(OH) 的沉淀溶解平衡曲线如图所示。
3 2
已知pCd2+为Cd2+浓度的负对数,pN为阴离子浓度的负对数。下列说法正确的是
A.曲线II是Cd(OH) 的沉淀溶解平衡曲线
2
B.加热可使溶液由X点变到Z点
C.Y点对应的Cd(OH) 溶液是过饱和溶液
2
D.T℃时,在 平衡体系中,平衡常数
K=102
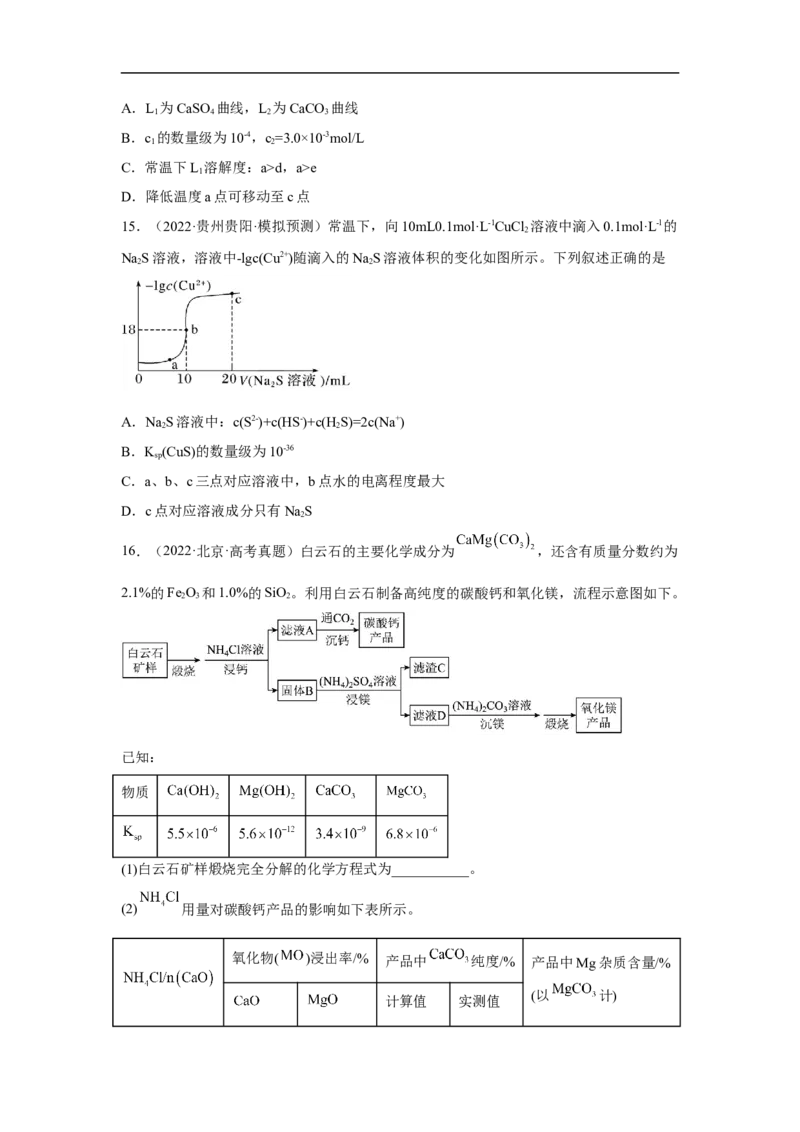
14.(2022·吉林长春·模拟预测)难溶物在水溶液中存在沉淀溶解平衡,已知
K (CaSO)=9.0×10-6,K (CaCO)=2.8×10-9,离子浓度与物质常温下的溶解度关系如图所示,
sp 4 sp 3
下列说法正确的是A.L 为CaSO 曲线,L 为CaCO 曲线
1 4 2 3
B.c 的数量级为10-4,c=3.0×10-3mol/L
1 2
C.常温下L 溶解度:a>d,a>e
1
D.降低温度a点可移动至c点
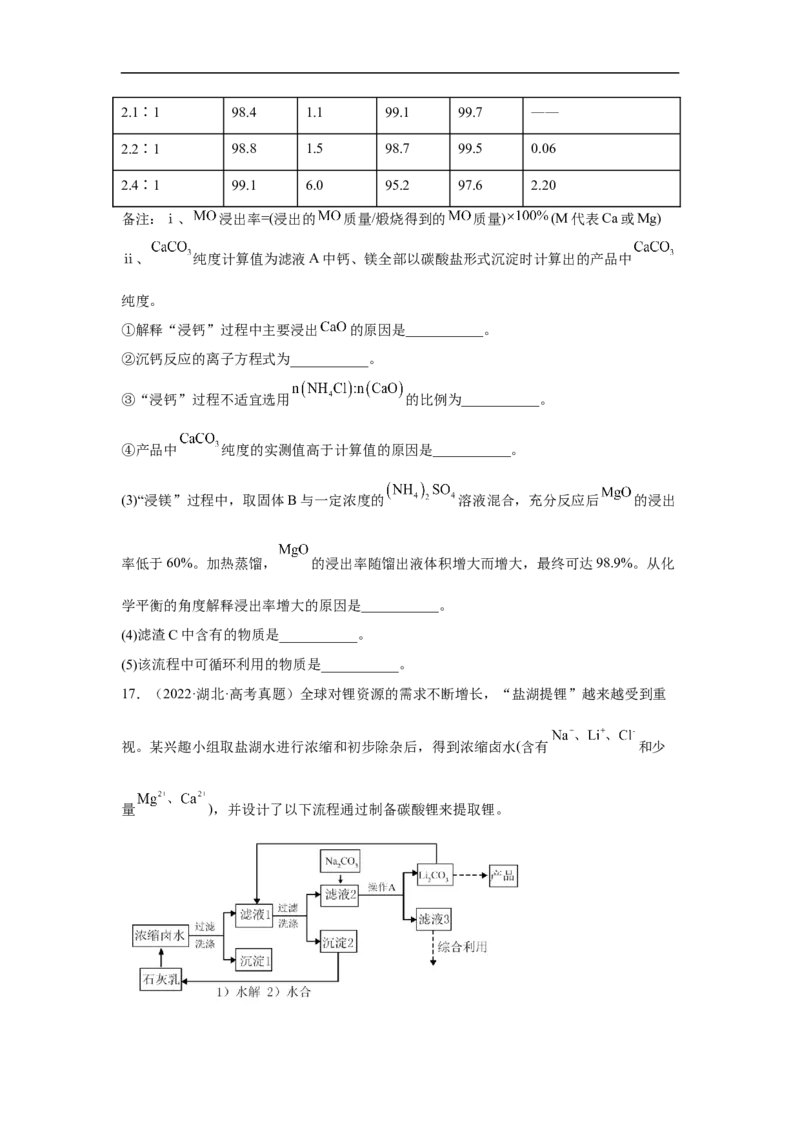
15.(2022·贵州贵阳·模拟预测)常温下,向10mL0.1mol·L-1CuCl 溶液中滴入0.1mol·L-l的
2
NaS溶液,溶液中-lgc(Cu2+)随滴入的NaS溶液体积的变化如图所示。下列叙述正确的是
2 2
A.NaS溶液中:c(S2-)+c(HS-)+c(H S)=2c(Na+)
2 2
B.K (CuS)的数量级为10-36
sp
C.a、b、c三点对应溶液中,b点水的电离程度最大
D.c点对应溶液成分只有NaS
2
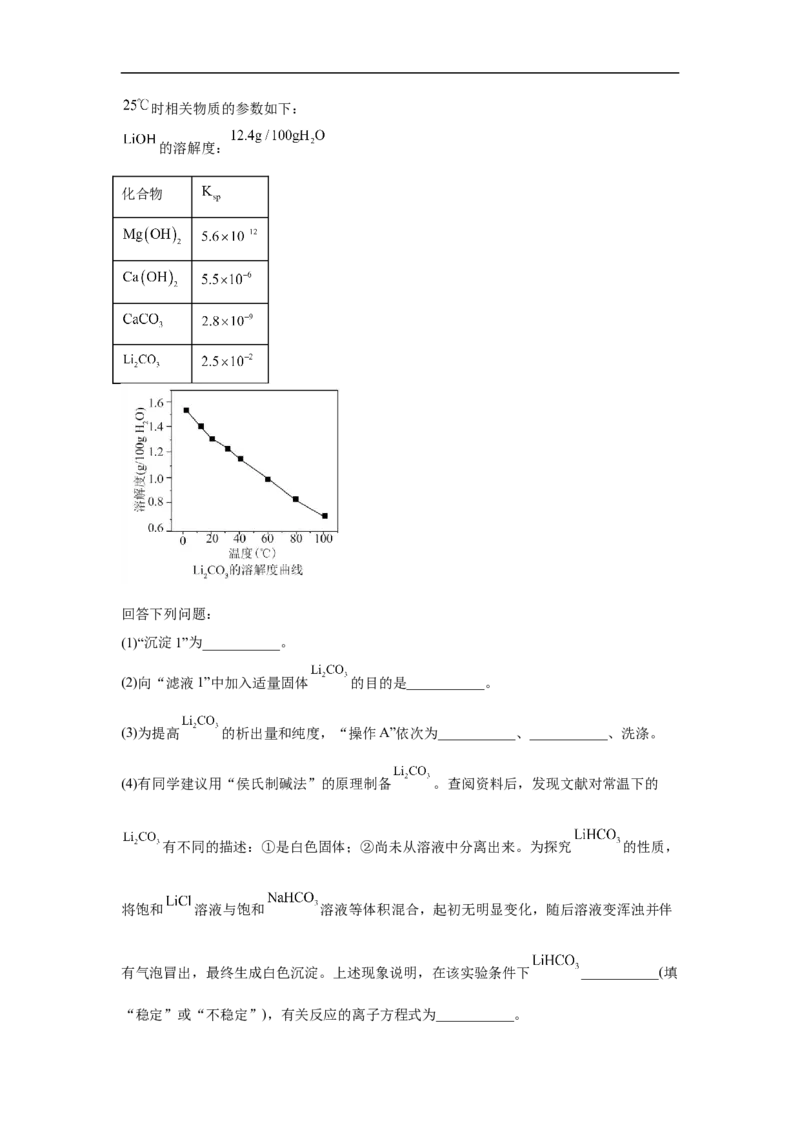
16.(2022·北京·高考真题)白云石的主要化学成分为 ,还含有质量分数约为
2.1%的Fe O 和1.0%的SiO。利用白云石制备高纯度的碳酸钙和氧化镁,流程示意图如下。
2 3 2
已知:
物质
(1)白云石矿样煅烧完全分解的化学方程式为___________。
(2) 用量对碳酸钙产品的影响如下表所示。
氧化物( )浸出率/% 产品中 纯度/% 产品中Mg杂质含量/%
(以 计)
计算值 实测值2.1∶1 98.4 1.1 99.1 99.7 ——
2.2∶1 98.8 1.5 98.7 99.5 0.06
2.4∶1 99.1 6.0 95.2 97.6 2.20
备注:ⅰ、 浸出率=(浸出的 质量/煅烧得到的 质量) (M代表Ca或Mg)
ⅱ、 纯度计算值为滤液A中钙、镁全部以碳酸盐形式沉淀时计算出的产品中
纯度。
①解释“浸钙”过程中主要浸出 的原因是___________。
②沉钙反应的离子方程式为___________。
③“浸钙”过程不适宜选用 的比例为___________。
④产品中 纯度的实测值高于计算值的原因是___________。
(3)“浸镁”过程中,取固体B与一定浓度的 溶液混合,充分反应后 的浸出
率低于60%。加热蒸馏, 的浸出率随馏出液体积增大而增大,最终可达98.9%。从化
学平衡的角度解释浸出率增大的原因是___________。
(4)滤渣C中含有的物质是___________。
(5)该流程中可循环利用的物质是___________。
17.(2022·湖北·高考真题)全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重
视。某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有 和少
量 ),并设计了以下流程通过制备碳酸锂来提取锂。时相关物质的参数如下:
的溶解度:
化合物
回答下列问题:
(1)“沉淀1”为___________。
(2)向“滤液1”中加入适量固体 的目的是___________。
(3)为提高 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
(4)有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的
有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,
将饱和 溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴
有气泡冒出,最终生成白色沉淀。上述现象说明,在该实验条件下 ___________(填
“稳定”或“不稳定”),有关反应的离子方程式为___________。(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入 改为通入 。这一改
动能否达到相同的效果,作出你的判断并给出理由___________。
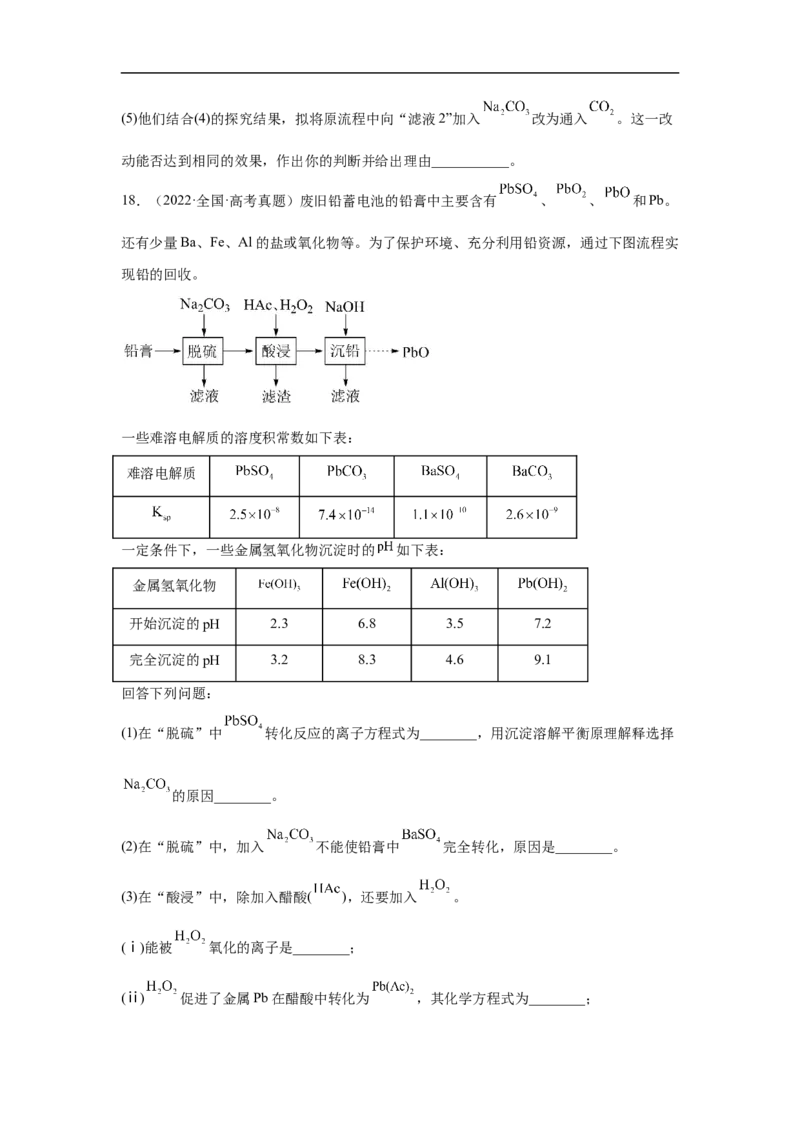
18.(2022·全国·高考真题)废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。
还有少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实
现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:
(1)在“脱硫”中 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择
的原因________。
(2)在“脱硫”中,加入 不能使铅膏中 完全转化,原因是________。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。
(ⅰ)能被 氧化的离子是________;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;(ⅲ) 也能使 转化为 , 的作用是________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
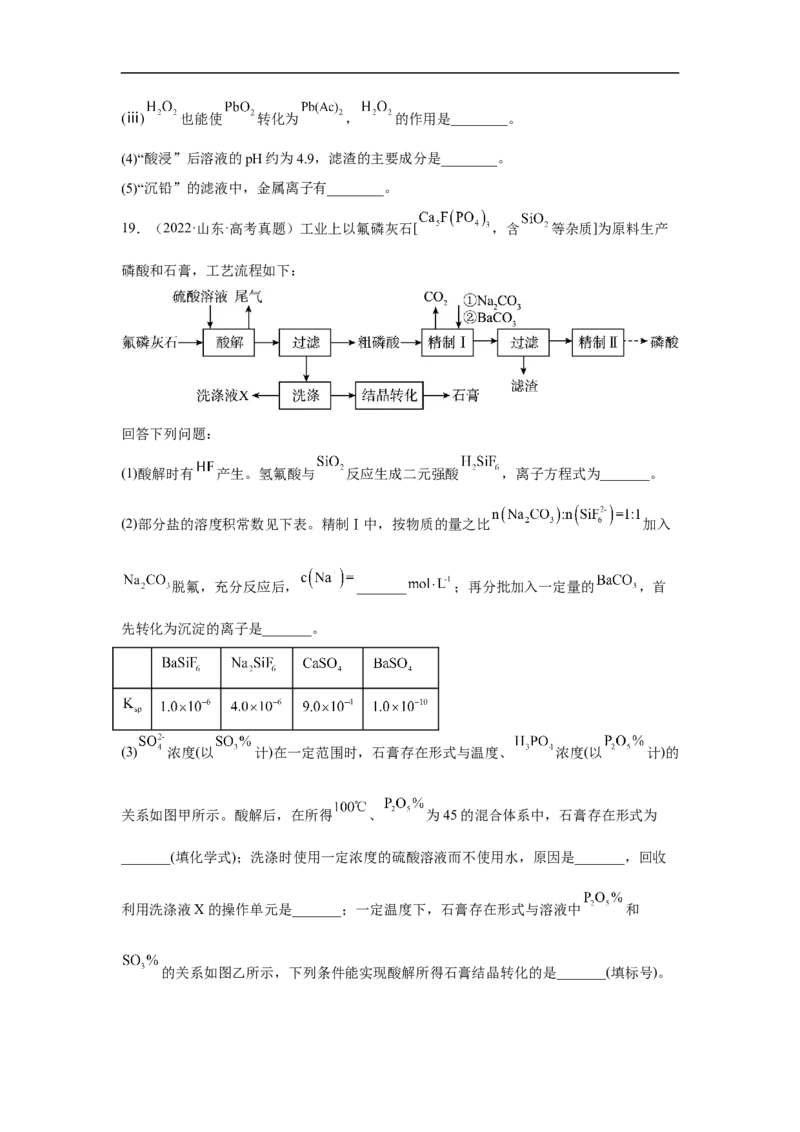
19.(2022·山东·高考真题)工业上以氟磷灰石[ ,含 等杂质]为原料生产
磷酸和石膏,工艺流程如下:
回答下列问题:
(1)酸解时有 产生。氢氟酸与 反应生成二元强酸 ,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比 加入
脱氟,充分反应后, _______ ;再分批加入一定量的 ,首
先转化为沉淀的离子是_______。
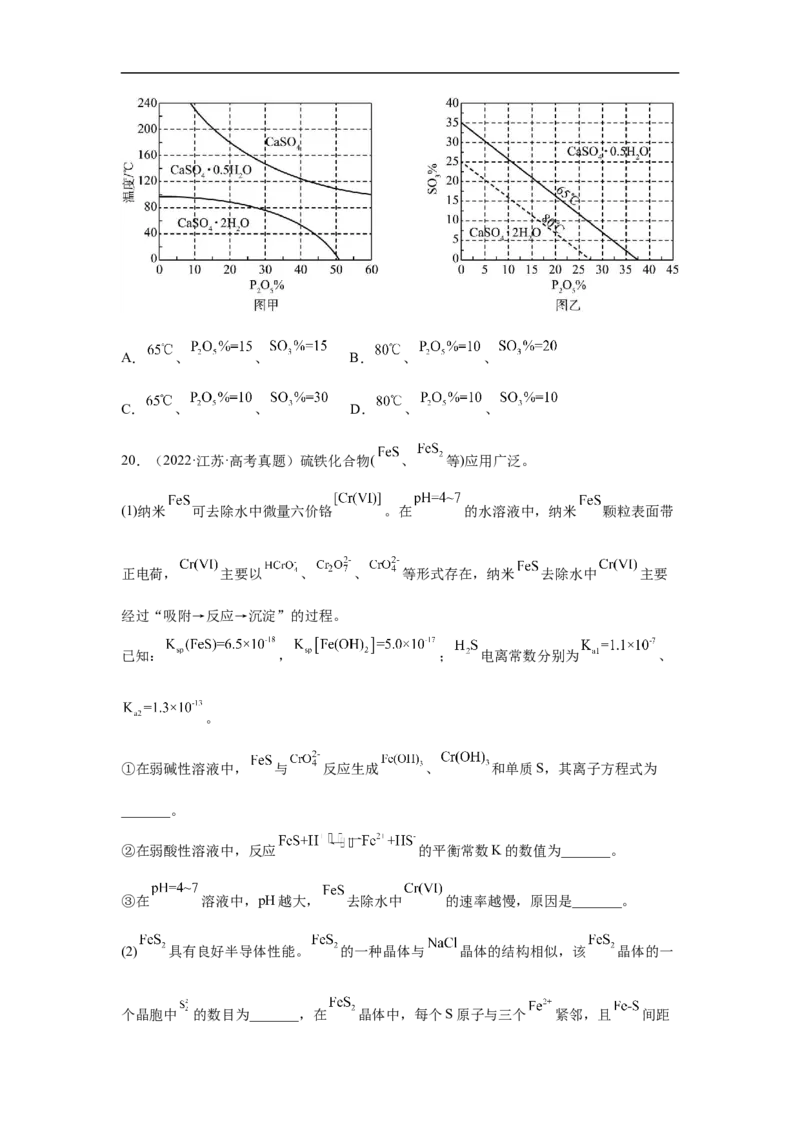
(3) 浓度(以 计)在一定范围时,石膏存在形式与温度、 浓度(以 计)的
关系如图甲所示。酸解后,在所得 、 为45的混合体系中,石膏存在形式为
_______(填化学式);洗涤时使用一定浓度的硫酸溶液而不使用水,原因是_______,回收
利用洗涤液X的操作单元是_______;一定温度下,石膏存在形式与溶液中 和
的关系如图乙所示,下列条件能实现酸解所得石膏结晶转化的是_______(填标号)。A. 、 、 B. 、 、
C. 、 、 D. 、 、
20.(2022·江苏·高考真题)硫铁化合物( 、 等)应用广泛。
(1)纳米 可去除水中微量六价铬 。在 的水溶液中,纳米 颗粒表面带
正电荷, 主要以 、 、 等形式存在,纳米 去除水中 主要
经过“吸附→反应→沉淀”的过程。
已知: , ; 电离常数分别为 、
。
①在弱碱性溶液中, 与 反应生成 、 和单质S,其离子方程式为
_______。
②在弱酸性溶液中,反应 的平衡常数K的数值为_______。
③在 溶液中,pH越大, 去除水中 的速率越慢,原因是_______。
(2) 具有良好半导体性能。 的一种晶体与 晶体的结构相似,该 晶体的一
个晶胞中 的数目为_______,在 晶体中,每个S原子与三个 紧邻,且 间距相等,如图给出了 晶胞中的 和位于晶胞体心的 ( 中的 键位于晶胞体对角
线上,晶胞中的其他 已省略)。如图中用“-”将其中一个S原子与紧邻的 连接起来
_______。
(3) 、 在空气中易被氧化,将 在空气中氧化,测得氧化过程中剩余固体的质量
与起始 的质量的比值随温度变化的曲线如图所示。 时, 氧化成含有两种元
素的固体产物为_______(填化学式,写出计算过程)。