文档内容
素养说明:学科素养要求考生“能依据事实,分析研究对象的构成要素和各要素
的关系,建立实物模型、认识模型和数学模型,反映研究对象的本质特征,揭示规
律”,通过对基本操作的规范表述总结,使学生形成思维方向及答题模板。
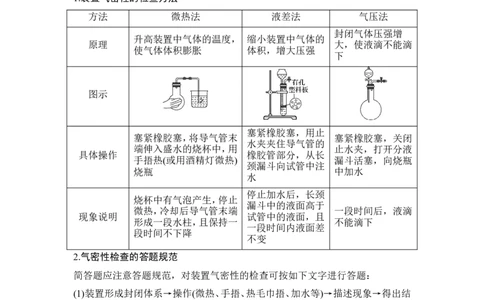
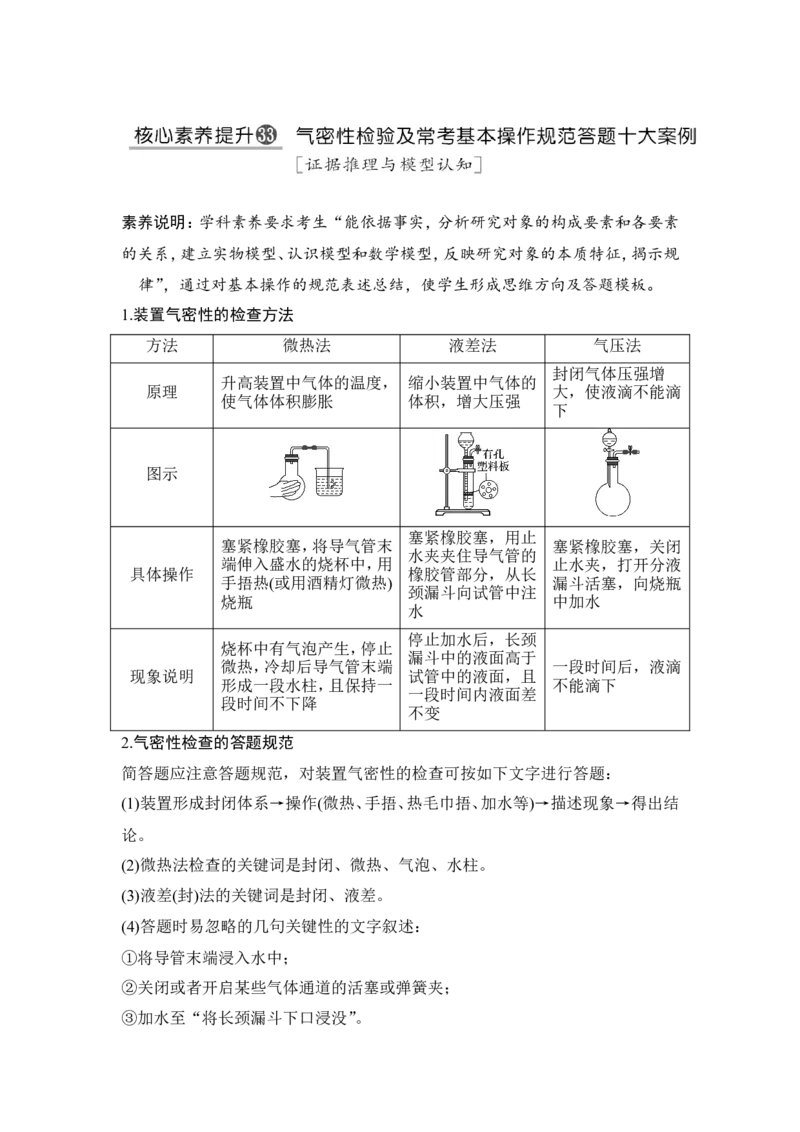
1.装置气密性的检查方法
方法 微热法 液差法 气压法
封闭气体压强增
升高装置中气体的温度, 缩小装置中气体的
原理 大,使液滴不能滴
使气体体积膨胀 体积,增大压强
下
图示
塞紧橡胶塞,用止
塞紧橡胶塞,将导气管末 塞紧橡胶塞,关闭
水夹夹住导气管的
端伸入盛水的烧杯中,用 止水夹,打开分液
具体操作 橡胶管部分,从长
手捂热(或用酒精灯微热) 漏斗活塞,向烧瓶
颈漏斗向试管中注
烧瓶 中加水
水
停止加水后,长颈
烧杯中有气泡产生,停止
漏斗中的液面高于
微热,冷却后导气管末端 一段时间后,液滴
现象说明 试管中的液面,且
形成一段水柱,且保持一 不能滴下
一段时间内液面差
段时间不下降
不变
2.气密性检查的答题规范
简答题应注意答题规范,对装置气密性的检查可按如下文字进行答题:
(1)装置形成封闭体系→操作(微热、手捂、热毛巾捂、加水等)→描述现象→得出结
论。
(2)微热法检查的关键词是封闭、微热、气泡、水柱。
(3)液差(封)法的关键词是封闭、液差。
(4)答题时易忽略的几句关键性的文字叙述:
①将导管末端浸入水中;
②关闭或者开启某些气体通道的活塞或弹簧夹;
③加水至“将长颈漏斗下口浸没”。[题型专练]
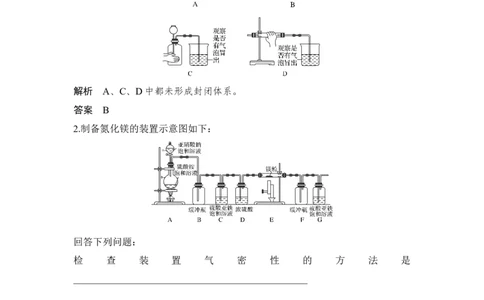
1.下列是一些装置气密性检查的方法,其中正确的是( )
解析 A、C、D中都未形成封闭体系。
答案 B
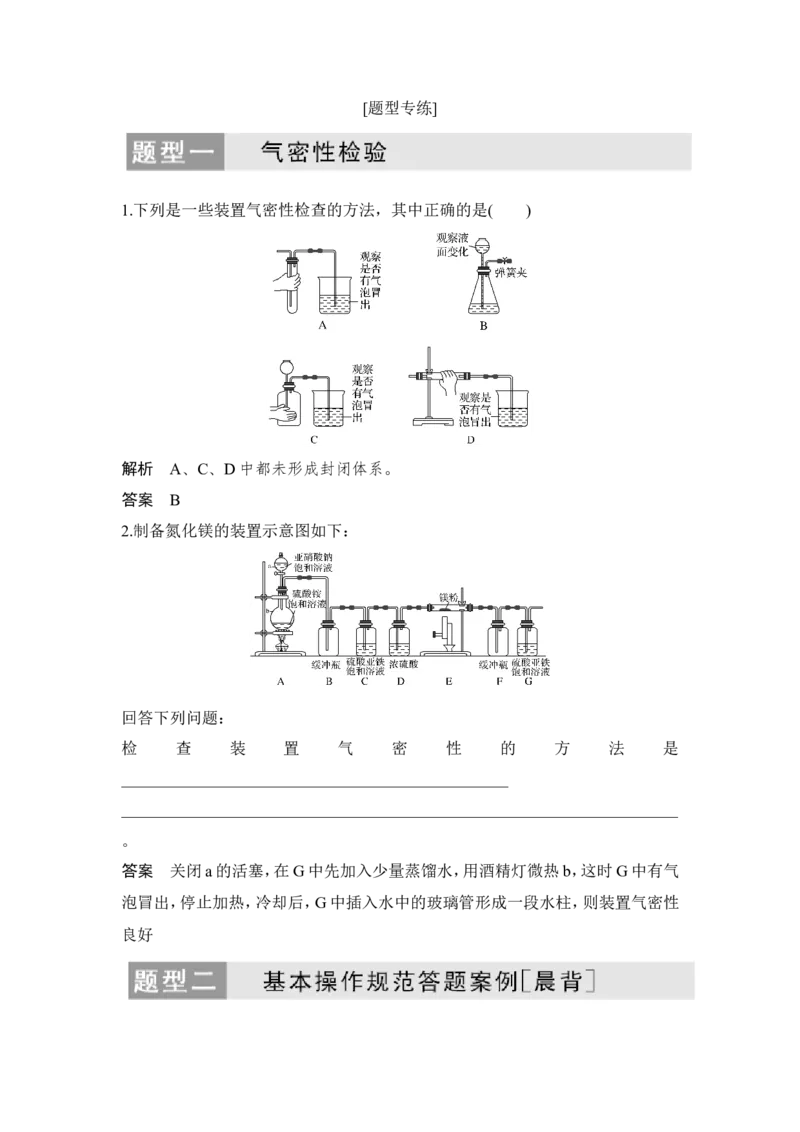
2.制备氮化镁的装置示意图如下:
回答下列问题:
检 查 装 置 气 密 性 的 方 法 是
________________________________________________
_____________________________________________________________________
。
答案 关闭a的活塞,在G中先加入少量蒸馏水,用酒精灯微热b,这时G中有气
泡冒出,停止加热,冷却后,G中插入水中的玻璃管形成一段水柱,则装置气密性
良好【案例1】 检验离子是否已经沉淀完全的方法
规范解答_____________________________________________________________
提示:将反应混合液静置,取上层清液少许于试管中滴加沉淀剂××,若不产生
沉淀,则××离子已经沉淀完全, 若产生沉淀,则××离子未完全沉淀。
【案例2】 过滤时洗涤沉淀的方法
规范解答_____________________________________________________________
提示:向过滤器中加蒸馏水至没过沉淀,待水自然流下后,重复操作2~3次。
【案例3】 检验沉淀是否洗涤干净的方法
规范解答 [以 FeCl 溶液与 NaOH 溶液制得 Fe(OH) 沉淀后过滤为例]:
3 3
_____________________________________________________________________
_
提示:取最后一次的洗涤液少许置于试管中,加入用硝酸酸化的硝酸银溶液,若
有白色沉淀生成,则沉淀未洗涤干净,若无白色沉淀,则沉淀已经洗涤干净。
注意:要选择一种溶液中浓度较大的比较容易检验的离子检验,不能检验沉淀本
身具有的离子。
【案例4】 读取量气装置中的气体体积的方法
规范解答_____________________________________________________________
_____________________________________________________________________
提示:待装置冷却至室温后,先上下移动量筒(或量气管有刻度的一侧)使量筒内
外(或量气管的两侧)液面相平,然后使视线与凹液面的最低点相平读取数据。
【案例5】 结晶的操作方法
(1)用FeCl 溶液制取FeCl ·6H O晶体的操作方法
3 3 2
规 范 解 答
______________________________________________________________
提示:向FeCl 溶液中加入过量的浓盐酸置于蒸发皿中,蒸发浓缩,冷却结晶,过
3
滤、洗涤、干燥。
(2)蒸发结晶的操作方法
规范解答_____________________________________________________________
提示:以蒸发NaCl溶液得到氯化钠晶体为例:将氯化钠溶液置于蒸发皿中,溶液
体积不能超过蒸发皿体积的,用酒精灯加热,边加热边用玻璃棒搅拌溶液,当蒸发皿中出现大量晶体时停止加热。
注意:若是纯净的氯化钠溶液可以利用余热蒸干得到氯化钠晶体;若是氯化钠溶
液中含有硝酸钾等杂质,则要采用蒸发溶剂的方法,至大量晶体析出后,趁热过
滤得到氯化钠晶体。
【案例6】 配制FeCl 溶液时溶解的操作方法
3
规范解答_____________________________________________________________
提示:将称量好的氯化铁晶体置于烧杯中,加入过量的浓盐酸,用玻璃棒搅拌,再
加入适量蒸馏水稀释到需要的浓度。
【案例7】 实验室用烧瓶漏斗式气体发生装置制备气体时,向圆底烧瓶中滴加液
体的操作方法
规范解答____________________________________________________________
提示:打开分液漏斗上口的玻璃塞(或将玻璃塞上的凹槽与分液漏斗上的小孔重
合),旋转分液漏斗的活塞缓慢滴加液体。
【案例8】 检验某含有大量SO的溶液中是否含有Cl-的操作方法
规范解答_____________________________________________________________
____________________________________________________________________
提示:取待测液少许置于试管中,先加过量的硝酸钡溶液,充分振荡后静置,在上
层清液中滴加少许硝酸酸化的硝酸银溶液,若产生白色沉淀,则证明溶液里含有
Cl-,反之则证明溶液里不含Cl-。
【案例9】 检验溶液中是否含有钾离子的操作方法
规范解答_____________________________________________________________
_____________________________________________________________________
提示:用一根洁净的铂丝蘸取少许溶液,在酒精灯的火焰上灼烧,透过蓝色钴玻
璃观察火焰颜色,若火焰呈紫色,则证明溶液中含有钾离子,反之则不含钾离子。
【案例10】 证明碳酸钠溶液中存在水解平衡的实验方法
规范解答_____________________________________________________________
_____________________________________________________________________
提示:取少许碳酸钠溶液置于试管中,滴加几滴酚酞溶液,溶液呈红色,再向红色
溶液中滴加BaCl 溶液至过量,产生白色沉淀,溶液的红色逐渐消失,则证明碳酸
2
钠溶液的碱性为碳酸根水解所致,即溶液中存在水解平衡。