文档内容
2023 届高三年级第一次调研测试
化学
注意事项
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共8页。满分为100 分,考试时间为75分钟。考试结束后。请将答题卡交回.
⒉答题前,请您务必将自己的姓名、学校、考试号等用黑色字迹的0.5亳米签字笔填写在
答题卡上规定的位置.
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名。准考证号与本人是否相符·
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡
皮擦干净后,再选涂其他答案。作答非选择题。必须用0.5毫米黑色墨水的签字笔在答题
卡上的指定位置作答,在其他位置作答一律无效。
S.如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。
可能用到的相对原子质量:H 1 C 12 O 16 F 19 C1 35.5 Fe 56 Se 79 Sr 88
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.糖类在生命活动中起重要作用。下列物质主要成分属于糖类的是
A。棉布
B.羊毛
C.维生素
D.油脂
2.亚硝酰氟(FNO)是一种工业稳定剂,可通过反应N O +CsF=FNO+CsNO 制得。下列说
2 4 3
法正确的是
A.氧原子的结构示意图为 B.CsF的电子式为
c. FNO的空间构型为直线形 D. CsNO 中含有离子键与共价键
3
3.工业上用C还原SiO 可得半导体材料Si和CO。下列说法正确的是
2
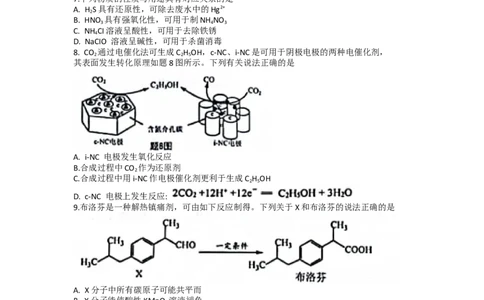
A.键能大小:E(C-C)0. 下列说法正确的是
2 2 2
A.已知该反应在加热条件下能自发进行,则其△S>0
B.上述反应的平衡常数
C.上述反应中消耗1 mol H S,生成22.4 L水蒸气
2
D.实际应用中,通过增加H S的量来提高CO 转化率,能有效减少碳排放
2 2
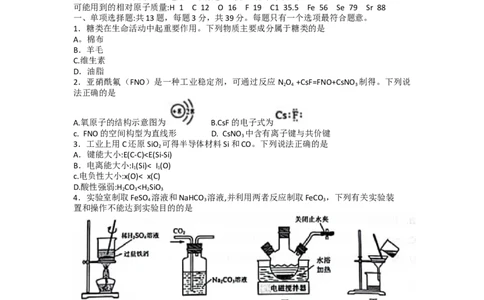
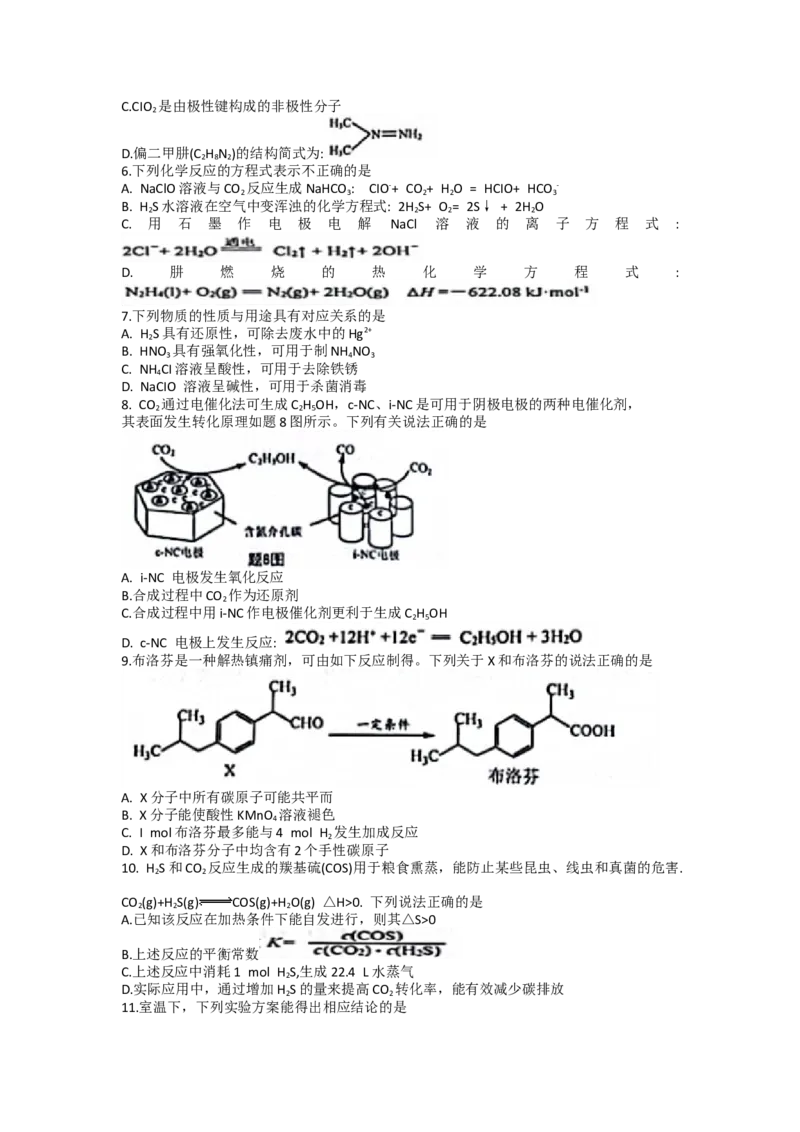
11.室温下,下列实验方案能得出相应结论的是12.工业上可利用氨水吸收SO 和NO ,原理如下图所示。已知: 25℃时,NH ·H O 的
2 2 3 2
Kb=l.7x10-5, H SO 的Ka =1.3x10-2, Ka =6.2x10-8. 下列说法正确的是
2 3 1 2
A.向氨水中通入SO 恰好生成NH HSO : c(H SO )> c(NH ·H O)+c (SO 2-)
2 4 3 2 3 3 2 3
B.向氨水中通入SO 至pH=7; c( HSO -)>c (NH + )> c(H+)= c(OH-)
2 3 4
C.反应NH ·H O + H SO =NH + + HSO -+ H O的平衡常数K=2.21x107
3 2 2 3 4 3 2
D. NO 被NH HSO 吸收的离子方程式: 2NO +4SO 2-= N + 4SO 2-
2 4 3 2 3 2 4
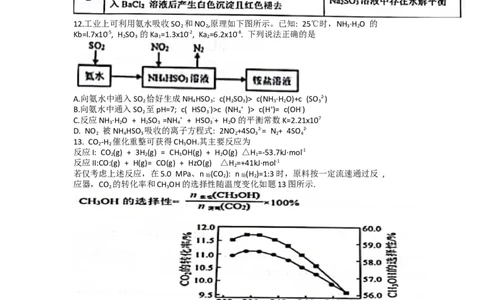
13. CO -H 催化重整可获得CH OH.其主要反应为
2 2 3
反应I: CO (g) + 3H (g) = CH OH(g) + H O(g) △H =-53.7kJ·mol-1
2 2 3 2 1
反应II:CO:(g) + H(g)= CO(g) + HzO(g) △H =+41kJ·mol-1
2
若仅考虑上述反应,在5.0 MPa、n (CO ): n (H )=1:3时,原料按一定流速通过反 ,
始 2 始 2
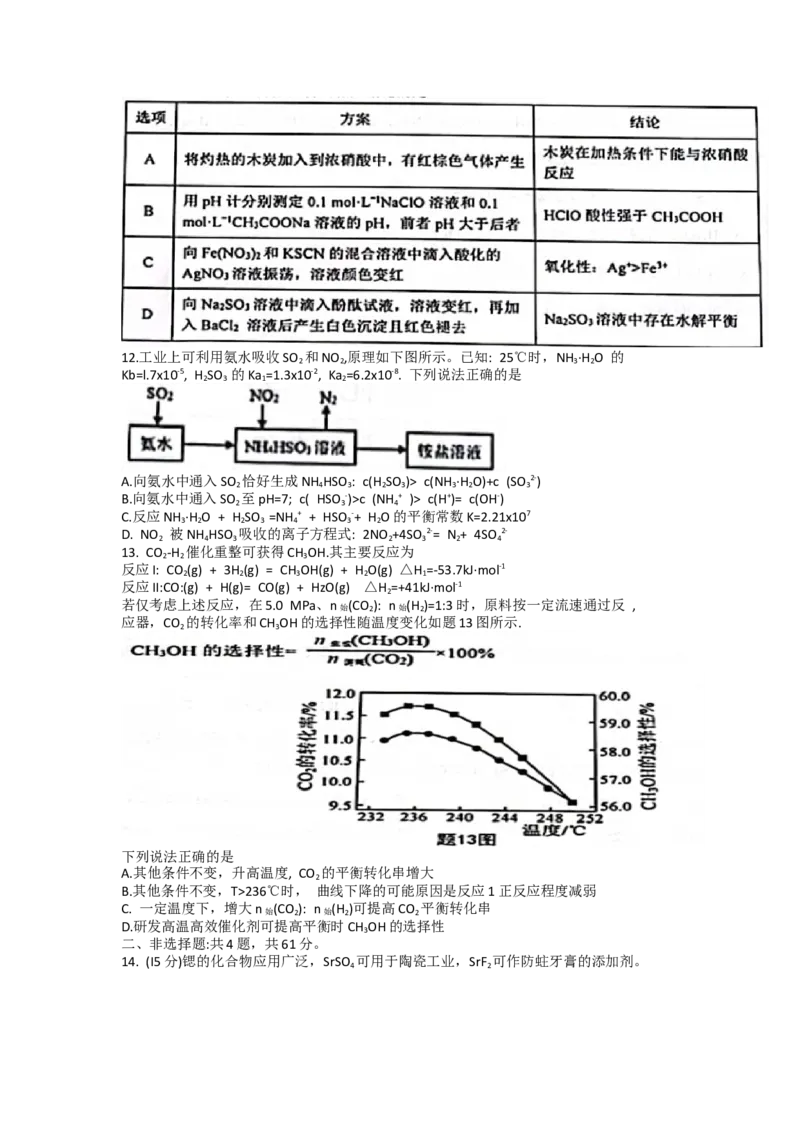
应器,CO 的转化率和CH OH的选择性随温度变化如题13图所示.
2 3
下列说法正确的是
A.其他条件不变,升高温度, CO 的平衡转化串增大
2
B.其他条件不变,T>236℃时, 曲线下降的可能原因是反应1正反应程度减弱
C. 一定温度下,增大n (CO ): n (H )可提高CO 平衡转化串
始 2 始 2 2
D.研发高温高效催化剂可提高平衡时CH OH的选择性
3
二、非选择题:共4题,共61分。
14. (I5分)锶的化合物应用广泛,SrSO 可用于陶瓷工业,SrF 可作防蛀牙膏的添加剂。
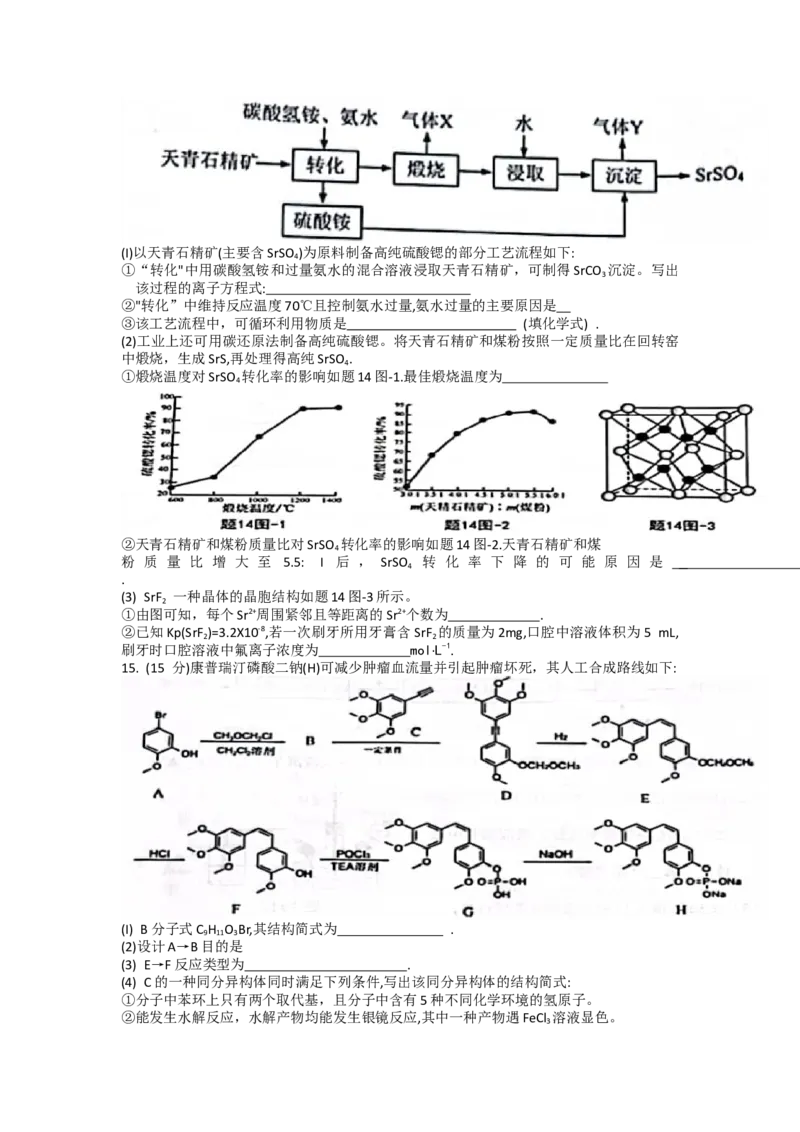
4 2(I)以天青石精矿(主要含SrSO )为原料制备高纯硫酸锶的部分工艺流程如下:
4
①“转化"中用碳酸氢铵和过量氨水的混合溶液浸取天青石精矿,可制得SrCO 沉淀。写出
3
该过程的离子方程式:
②"转化”中维持反应温度70℃且控制氨水过量,氨水过量的主要原因是
③该工艺流程中,可循环利用物质是 (填化学式) .
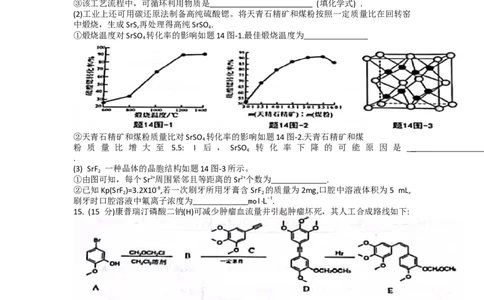
(2)工业上还可用碳还原法制备高纯硫酸锶。将天青石精矿和煤粉按照一定质量比在回转窑
中煅烧,生成SrS,再处理得高纯SrSO .
4
①煅烧温度对SrSO 转化率的影响如题14图-1.最佳煅烧温度为
4
②天青石精矿和煤粉质量比对SrSO 转化率的影响如题14图-2.天青石精矿和煤
4
粉 质 量 比 增 大 至 5.5: I 后 , SrSO 转 化 率 下 降 的 可 能 原 因 是
4
.
(3) SrF 一种晶体的晶胞结构如题14图-3所示。
2
①由图可知,每个Sr2+周围紧邻且等距离的Sr2+个数为 .
②已知Kp(SrF )=3.2X10-8,若一次刷牙所用牙膏含SrF 的质量为2mg,口腔中溶液体积为5 mL,
2 2
刷牙时口腔溶液中氟离子浓度为 mol·L-1.
15. (15 分)康普瑞汀磷酸二钠(H)可减少肿瘤血流量并引起肿瘤坏死,其人工合成路线如下:
(I) B分子式C H O Br,其结构简式为 .
9 11 3
(2)设计A→B目的是
(3) E→F反应类型为 .
(4) C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①分子中苯环上只有两个取代基,且分子中含有5种不同化学环境的氢原子。
②能发生水解反应,水解产物均能发生银镜反应,其中一种产物遇FeCl 溶液显色。
3(5)已知
写出以 、CH OCH CI和HCHO为原料制备 的合成路线流
3 2
程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干) .
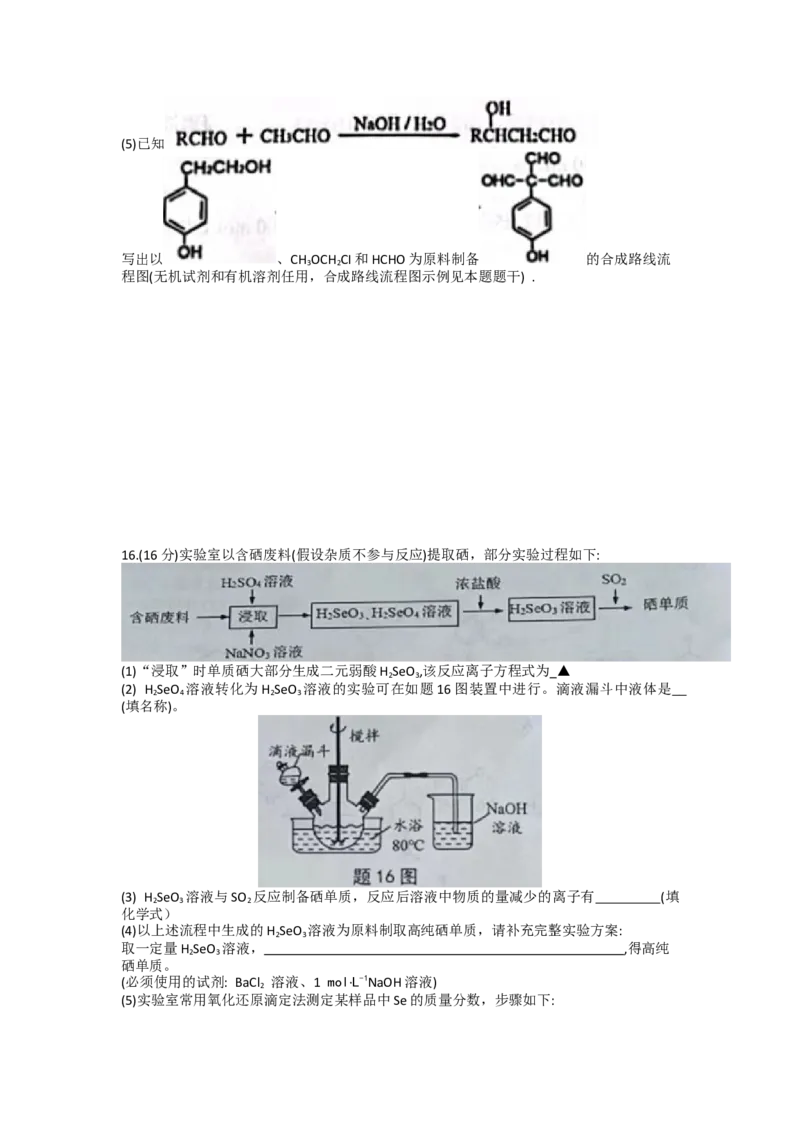
16.(16分)实验室以含硒废料(假设杂质不参与反应)提取硒,部分实验过程如下:
(1)“浸取”时单质硒大部分生成二元弱酸H SeO ,该反应离子方程式为_▲
2 3
(2) H SeO 溶液转化为H SeO 溶液的实验可在如题16图装置中进行。滴液漏斗中液体是
2 4 2 3
(填名称)。
(3) H SeO 溶液与SO 反应制备硒单质,反应后溶液中物质的量减少的离子有 (填
2 3 2
化学式)
(4)以上述流程中生成的H SeO 溶液为原料制取高纯硒单质,请补充完整实验方案:
2 3
取一定量H SeO 溶液, ,得高纯
2 3
硒单质。
(必须使用的试剂: BaCl 溶液、1 mol·L-1NaOH溶液)
2
(5)实验室常用氧化还原滴定法测定某样品中Se的质量分数,步骤如下:I.取0.8400 g样品充分磨碎,加酸煮沸配成H2SeO3溶液,将溶液完全转移到250 mL容量
瓶中后定容。
II. 准确量取25.00 mL待测液于锥形瓶中,加入0.0200 mol·L-1KMnO4标准溶液25.00 mL,
向锥形瓶中再加入25.00 mL 0.06 mol·L-1Fe2+溶液,加入磷酸后再用0.0200mol·L-1KMnO4滴
定,消耗KMnO4溶液10.00 mL.
已知: Se 的最高价含氧酸氧化Fe2+较慢,在该滴定过程可忽略此反应。
计算硒的质量分数(写出计算过程)。
17. (15 分)铝系金属复合材料能有效还原去除水体中的硝酸盐污染。铝粉表而复合金属
的组分和含量,会影响硝酸盐的去除效果。
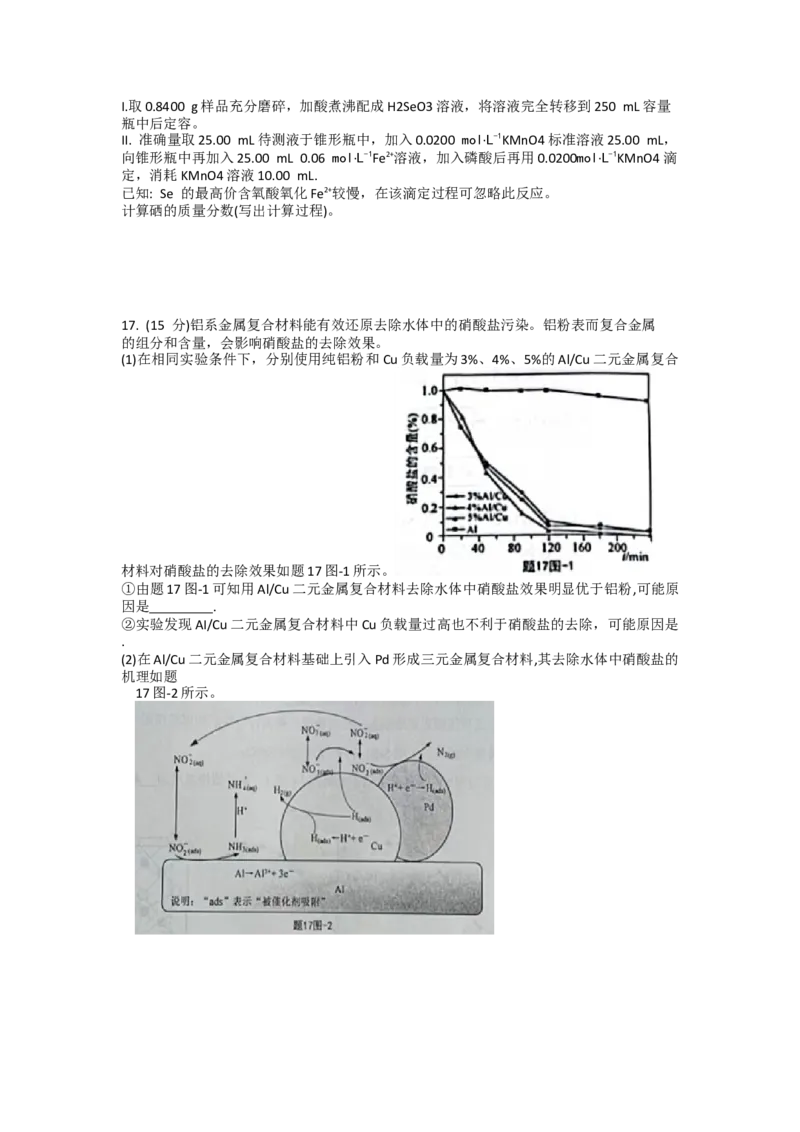
(1)在相同实验条件下,分别使用纯铝粉和Cu负载量为3%、4%、5%的Al/Cu二元金属复合
材料对硝酸盐的去除效果如题17图-1所示。
①由题17图-1可知用Al/Cu二元金属复合材料去除水体中硝酸盐效果明显优于铝粉,可能原
因是 .
②实验发现AI/Cu二元金属复合材料中Cu负载量过高也不利于硝酸盐的去除,可能原因是
.
(2)在Al/Cu二元金属复合材料基础上引入Pd形成三元金属复合材料,其去除水体中硝酸盐的
机理如题
17图-2所示。①使用AI/Cu二元金属复合材料,可将水体中硝酸盐转化为铵盐,该转化的机理可描述为:
H+吸附在Cu表面并得电子生成强还原性的吸附氢H(ads),
, NH
3
与H+结合为NH +进入溶液。
4
②引入Pd的AI/Cu/Pd三元金属复合材料,硝酸盐转化为N 选择性明显提高,可能原因是
2
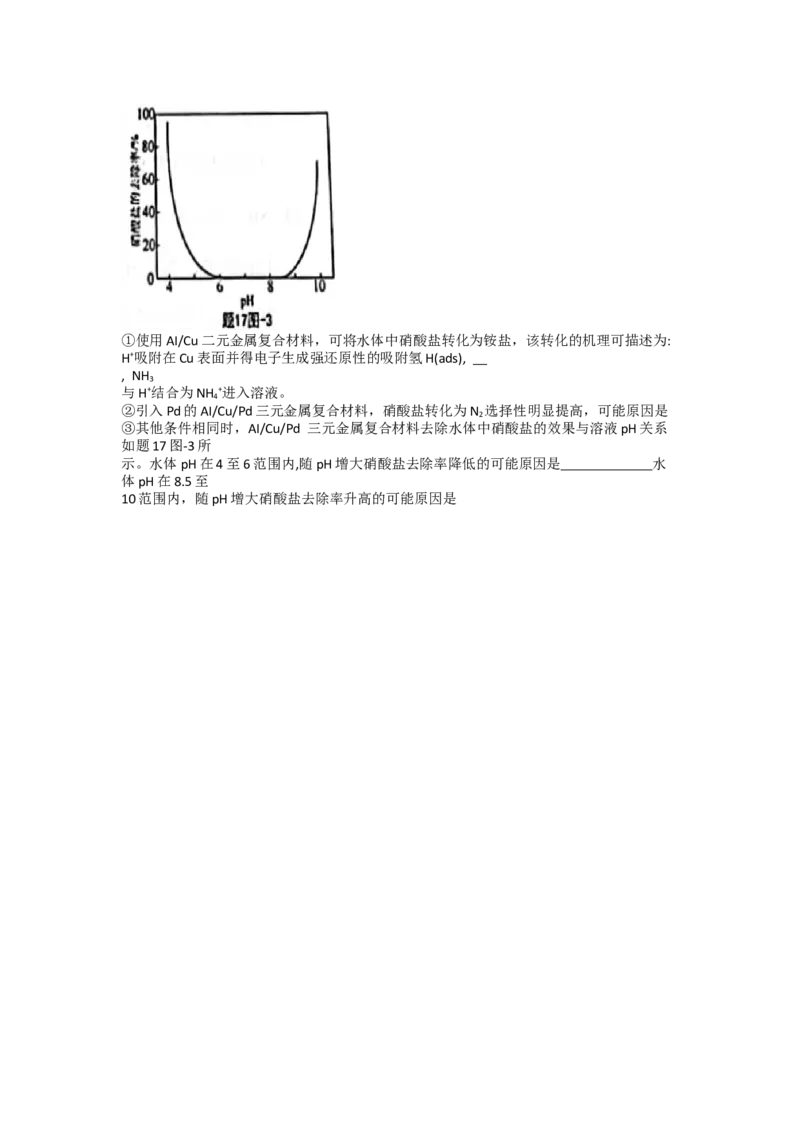
③其他条件相同时,AI/Cu/Pd 三元金属复合材料去除水体中硝酸盐的效果与溶液pH关系
如题17图-3所
示。水体pH在4至6范围内,随pH增大硝酸盐去除率降低的可能原因是 水
体pH在8.5至
10范围内,随pH增大硝酸盐去除率升高的可能原因是