文档内容
苏州市2021~2022学年第二学期学业质量阳光指标调研卷(延期〉
高二化学
2022.08
注意事项:
1.本试卷分为选择题和非选择题两部分,试卷满分100分。考试时间75分钟。
2.将选择题答案填涂在答题卡的对应位置上,非选择题的答写在答题卡的指定栏目内。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 S 32 Mn 55 Fe 56
一、单项选择题:包括14小题,每小题3分,共42分。每小题只有一个选项最符合题意。
高温
HgSO SO Hg
2 2
1.反应 古代用于制汞。下列说法不正确的是( )
A.该反应属于置换反应 B,制得 1mol Hg 理论上转移2mol电子
HgS
C. 既是氧化剂又是还原剂 D.该方法炼汞污染大
CO2AgNH OH 2AgNH CO 2NH
3 2 4 2 3 3
2.反应 可用于检验微量CO的存在。下列说法
正确的是( )
NH CO2
A. 3是非极性分子 B. 3 的空间构型为三角锥形
C. AgNH 3 2 中存在 AgH 键 D.电负性大小: (O)(N)
3,下列有关物质的性质与用途具有对应关系的是( )
O
A.铁粉能与 2反应,可用作食品保存的脱氧剂
Al O
B. 2 3熔点高,可用于工业怡炼铝单质
ClO
C. 2具有还原性,可用于自来水的杀菌消毒
NaHCO
D. 3受热易分解,可用于治疗胃酸过多
阅读下列资料,完成4~6题:海水是巨大的宝藏库,其中蕴含的元素有80多种。从海水中可获得粗盐,粗
Ca2、Mg2、SO2
盐中含有 4 等杂质离子,提纯后所得NaCl是氯碱工业、侯氏制碱等的重要化工原料。从
晒盐后卤水中可提澳和镁等。
4.海洋资源的综合利用中涉及的原理及相关离子方程式书写均正确的是( )
2I H O I 2OH
H O 2 2 2
A.用 2 2从酸化海带灰浸出液中提碘:
B.氮气与水反应制氯水:
Cl
2
H
2
O
2H Cl ClO
Mg2 CO2 MgCO
Mg2 3 3
C.除去粗盐中 :
下载最新免费模拟卷,到公众号:一枚试卷君通电
2Cl 2H O 2OH H Cl
2 2 2
D.氯碱工业制氯气:
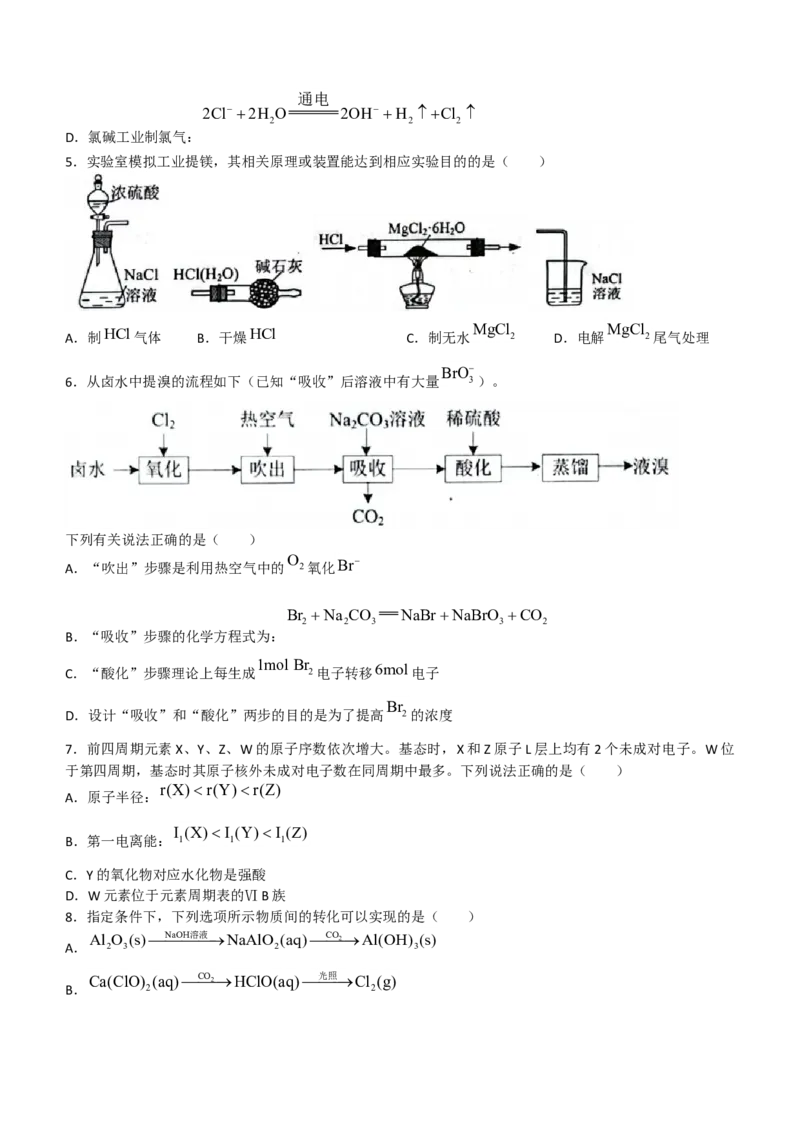
5.实验室模拟工业提镁,其相关原理或装置能达到相应实验目的的是( )
MgCl MgCl
A.制HCl气体 B.干燥HCl C.制无水 2 D.电解 2尾气处理
BrO
6.从卤水中提溴的流程如下(已知“吸收”后溶液中有大量 3)。
下列有关说法正确的是( )
A.“吹出”步骤是利用热空气中的
O 2氧化Br
Br Na CO NaBrNaBrO CO
2 2 3 3 2
B.“吸收”步骤的化学方程式为:
1mol Br
C.“酸化”步骤理论上每生成 2电子转移6mol电子
Br
D.设计“吸收”和“酸化”两步的目的是为了提高 2的浓度
7.前四周期元素X、Y、Z、W的原子序数依次增大。基态时,X和Z原子L层上均有2个未成对电子。W位
于第四周期,基态时其原子核外未成对电子数在同周期中最多。下列说法正确的是( )
r(X)r(Y)r(Z)
A.原子半径:
I (X)I (Y)I (Z)
B.第一电离能: 1 1 1
C.Y的氧化物对应水化物是强酸
D.W元素位于元素周期表的ⅥB族
8.指定条件下,下列选项所示物质间的转化可以实现的是( )
Al O (s)NaOH溶液NaAlO (aq)CO 2Al(OH) (s)
A. 2 3 2 3
Ca(ClO) (aq)CO 2HClO(aq)光照Cl (g)
B. 2 2SiO (s)盐酸SiCl (aq)H2Si(s)
C. 2 4
FeS (s)O 2SO (g)H2 OH SO (浓)
D. 2 高温 3 2 4
9.下列说法正确是( )
A.金刚石与石墨烯中的CCC夹角都是120
CH 、SiH 、GeH
B. 4 4 4的沸点依次升高
C.Ge原子基态核外电子排布式为
[Ar]4s24p2
CO SiO
D. 2与 2的晶体类型相同
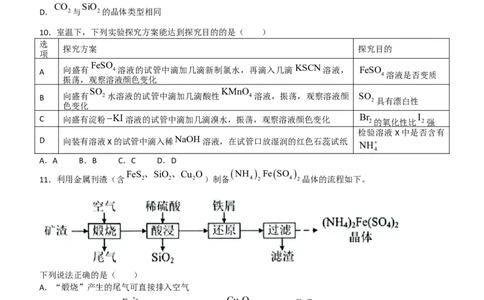
10.室温下,下列实验探究方案能达到探究目的的是( )
选
探究方案 探究目的
项
FeSO
A 向盛有 4溶液的试管中滴加几滴新制氯水,再滴入几滴 KSCN溶液, FeSO
4溶液是否变质
振荡,观察溶液颜色变化
SO KMnO
B 向盛有 2水溶液的试管中滴加几滴酸性 4溶液,振荡,观察溶液颜 SO
2具有漂白性
色变化
C 向盛有淀粉KI溶液的试管中滴加几滴溴水,振荡,观察溶液颜色变化 Br
2的氧化性比
I
2强
检验溶液X中是否含有
D 向装有溶液X的试管中滴入稀NaOH溶液,在试管口放湿润的红色石蕊试纸 NH
4
A.A B.B C.C D.D
FeS、SiO 、Cu O NH FeSO
11.利用金属刊渣(含 2 2 2 )制备 4 2 4 2晶体的流程如下。
下列说法正确的是( )
A.“煅烧”产生的尾气可直接排入空气
B.若酸浸后溶液中无 Fe2 ,说明“煅烧”过程中 Cu 2 O 全部转化为CuO
Fe2、Cu2、SO2
C.还原得到溶液中的离子主要有 4
Fe
D.“滤渣”的成分为
CO H
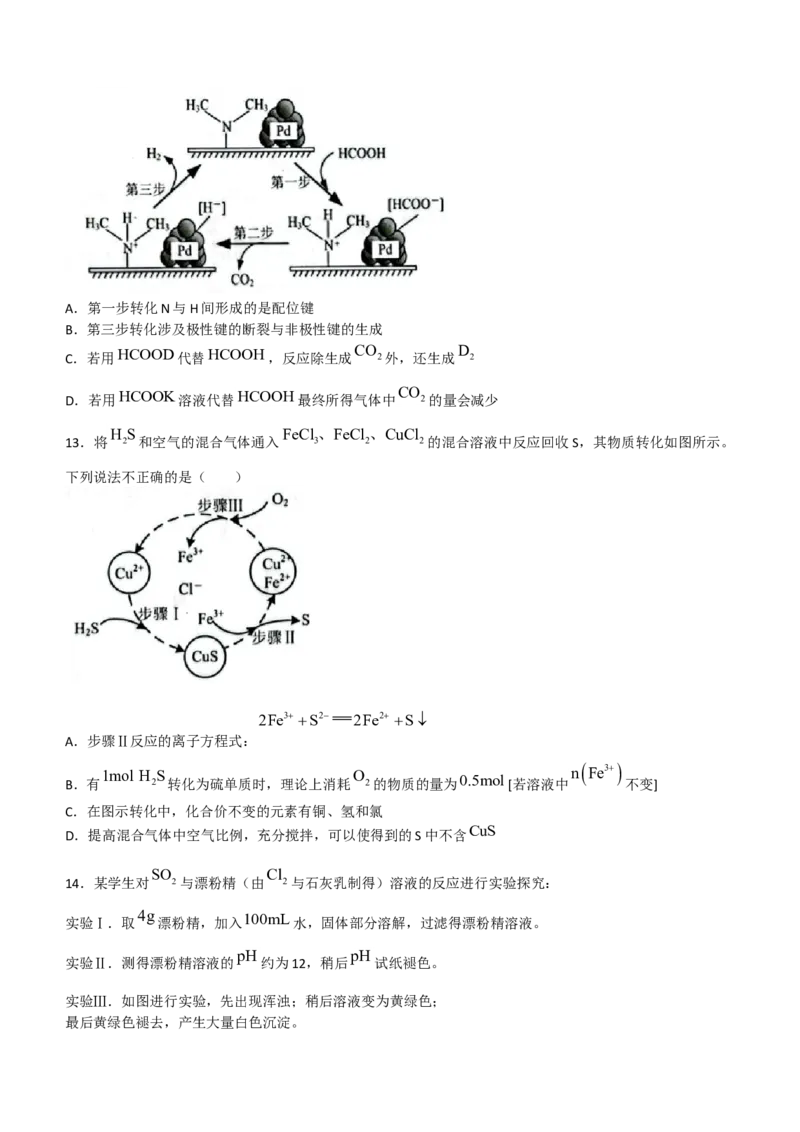
12.在催化剂作用下,HCOOH分解生成 2和 2可能的反应机理如下图所示。下列说法不正确的是(
)A.第一步转化N与H间形成的是配位键
B.第三步转化涉及极性键的断裂与非极性键的生成
CO D
C.若用HCOOD代替HCOOH,反应除生成 2外,还生成 2
CO
D.若用HCOOK溶液代替HCOOH最终所得气体中 2的量会减少
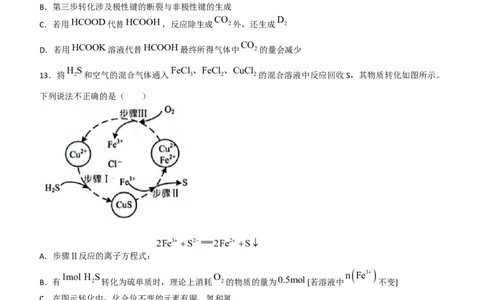
H S FeCl、FeCl 、CuCl
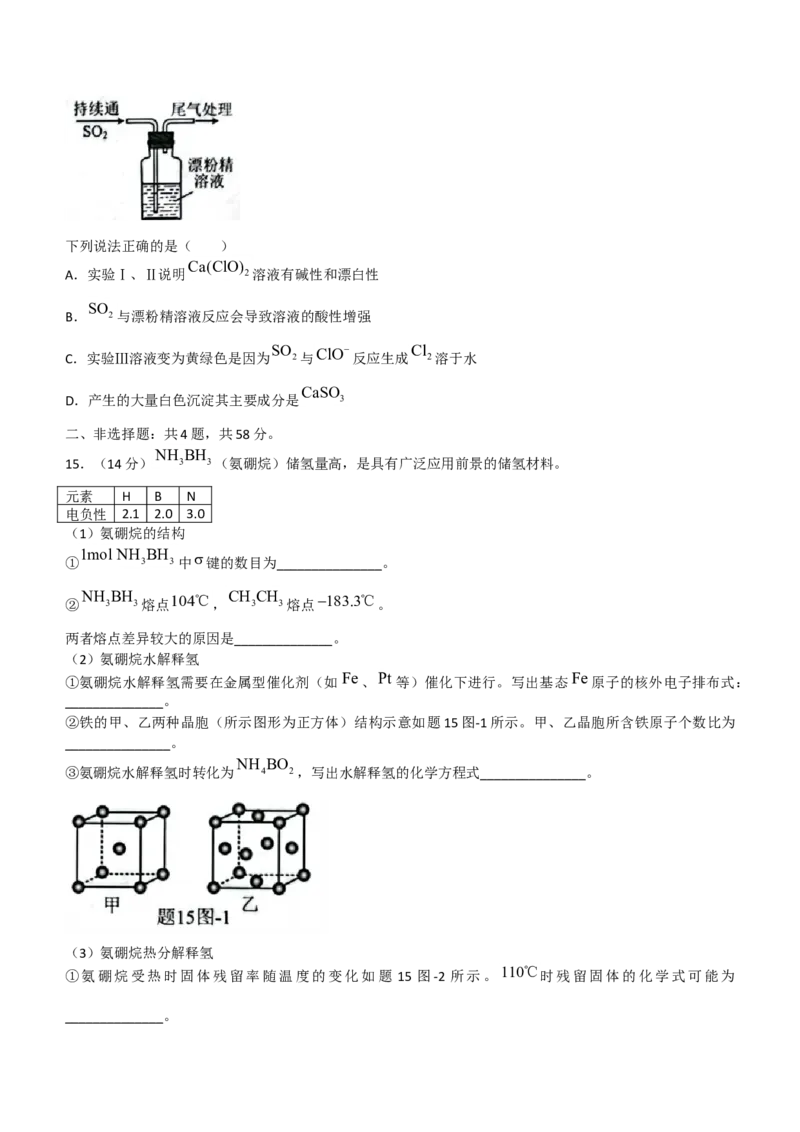
13.将 2 和空气的混合气体通入 3 2 2的混合溶液中反应回收S,其物质转化如图所示。
下列说法不正确的是( )
2Fe3 S2 2Fe2 S
A.步骤Ⅱ反应的离子方程式:
1mol H S O n
Fe3
B.有 2 转化为硫单质时,理论上消耗 2的物质的量为0.5mol [若溶液中 不变]
C.在图示转化中,化合价不变的元素有铜、氢和氯
D.提高混合气体中空气比例,充分搅拌,可以使得到的S中不含CuS
SO Cl
14.某学生对 2与漂粉精(由 2与石灰乳制得)溶液的反应进行实验探究:
实验Ⅰ.取 4g 漂粉精,加入100mL水,固体部分溶解,过滤得漂粉精溶液。
pH pH
实验Ⅱ.测得漂粉精溶液的 约为12,稍后 试纸褪色。
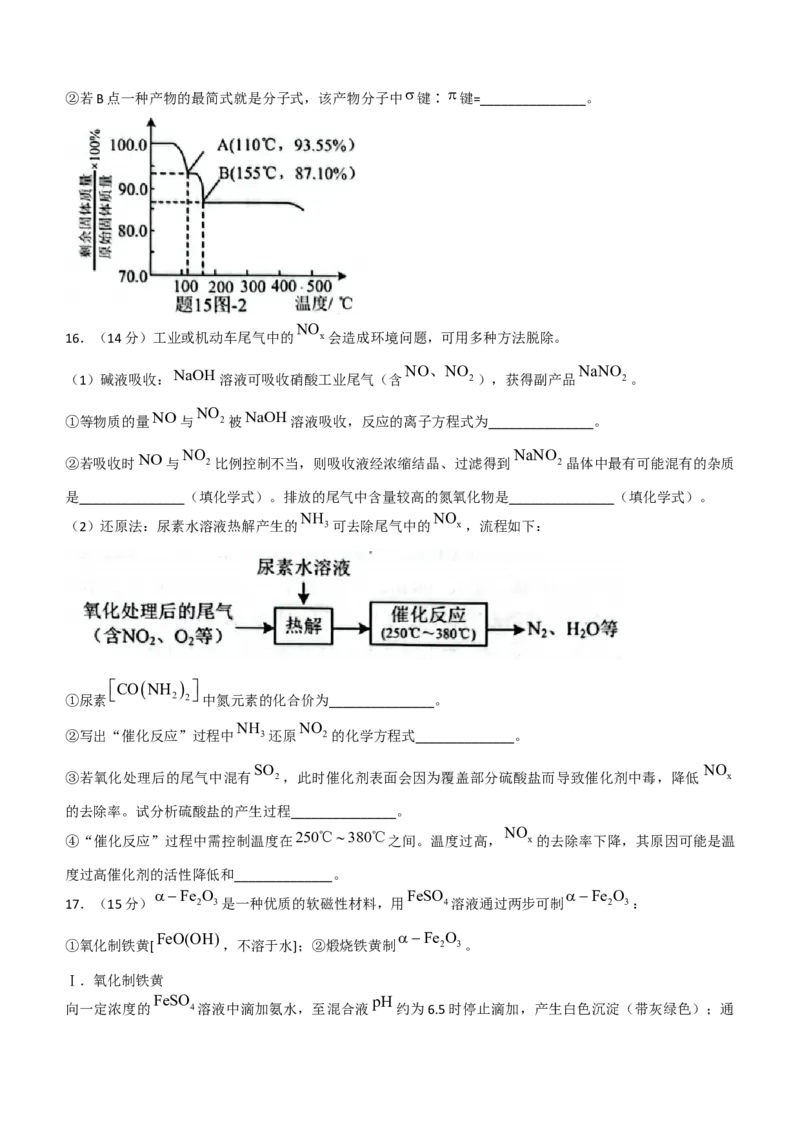
实验Ⅲ.如图进行实验,先出现浑浊;稍后溶液变为黄绿色;
最后黄绿色褪去,产生大量白色沉淀。下列说法正确的是( )
Ca(ClO)
A.实验Ⅰ、Ⅱ说明 2溶液有碱性和漂白性
SO
B. 2与漂粉精溶液反应会导致溶液的酸性增强
SO ClO Cl
C.实验Ⅲ溶液变为黄绿色是因为 2与 反应生成 2溶于水
CaSO
D.产生的大量白色沉淀其主要成分是 3
二、非选择题:共4题,共58分。
NH BH
15.(14分) 3 3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
元素 H B N
电负性 2.1 2.0 3.0
(1)氨硼烷的结构
1mol NH BH
① 3 3中键的数目为_______________。
②
NH
3
BH 3熔点104℃
,
CH
3
CH 3熔点183.3℃
。
两者熔点差异较大的原因是______________。
(2)氨硼烷水解释氢
Fe Pt Fe
①氨硼烷水解释氢需要在金属型催化剂(如 、 等)催化下进行。写出基态 原子的核外电子排布式:
______________。
②铁的甲、乙两种晶胞(所示图形为正方体)结构示意如题15图-1所示。甲、乙晶胞所含铁原子个数比为
_______________。
NH BO
③氨硼烷水解释氢时转化为 4 2,写出水解释氢的化学方程式_______________。
(3)氨硼烷热分解释氢
①氨硼烷受热时固体残留率随温度的变化如题 15 图-2
所示。110℃
时残留固体的化学式可能为
______________。②若B点一种产物的最简式就是分子式,该产物分子中键∶键=_______________。
NO
16.(14分)工业或机动车尾气中的 x会造成环境问题,可用多种方法脱除。
NO、NO NaNO
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含 2),获得副产品 2。
NO
①等物质的量NO与 2被NaOH溶液吸收,反应的离子方程式为_______________。
NO NaNO
②若吸收时NO与 2比例控制不当,则吸收液经浓缩结晶、过滤得到 2晶体中最有可能混有的杂质
是_______________(填化学式)。排放的尾气中含量较高的氮氧化物是_______________(填化学式)。
NH NO
(2)还原法:尿素水溶液热解产生的 3可去除尾气中的 x,流程如下:
CONH
①尿素 2 2 中氮元素的化合价为_______________。
NH NO
②写出“催化反应”过程中 3还原 2的化学方程式______________。
SO NO
③若氧化处理后的尾气中混有 2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低 x
的去除率。试分析硫酸盐的产生过程_______________。
④“催化反应”过程中需控制温度在250℃380℃
之间。温度过高,
NO
x的去除率下降,其原因可能是温
度过高催化剂的活性降低和______________。
Fe O FeSO Fe O
17.(15分) 2 3是一种优质的软磁性材料,用 4溶液通过两步可制 2 3:
FeO(OH) Fe O
①氧化制铁黄[ ,不溶于水];②煅烧铁黄制 2 3。
Ⅰ.氧化制铁黄
FeSO pH
向一定浓度的 4溶液中滴加氨水,至混合液 约为6.5时停止滴加,产生白色沉淀(带灰绿色);通pH
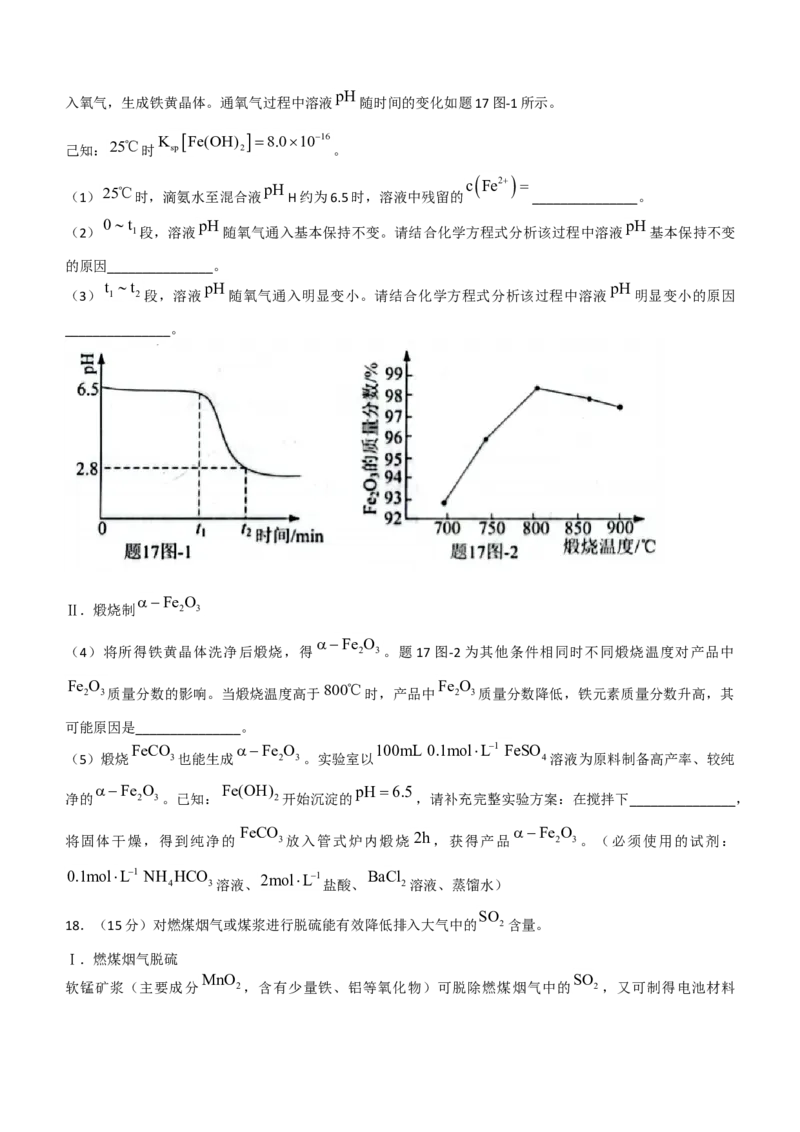
入氧气,生成铁黄晶体。通氧气过程中溶液 随时间的变化如题17图-1所示。
K Fe(OH) 8.01016
己知:25℃
时 sp 2 。
c
Fe2
(1)25℃
时,滴氨水至混合液
pH
H约为6.5时,溶液中残留的 _______________。
0t pH pH
(2) 1段,溶液 随氧气通入基本保持不变。请结合化学方程式分析该过程中溶液 基本保持不变
的原因_______________。
t t pH pH
(3) 1 2段,溶液 随氧气通入明显变小。请结合化学方程式分析该过程中溶液 明显变小的原因
_______________。
Fe O
Ⅱ.煅烧制 2 3
Fe O
(4)将所得铁黄晶体洗净后煅烧,得 2 3。题17图-2为其他条件相同时不同煅烧温度对产品中
Fe
2
O 3质量分数的影响。当煅烧温度高于800℃
时,产品中
Fe
2
O
3质量分数降低,铁元素质量分数升高,其
可能原因是_______________。
FeCO Fe O 100mL 0.1molL1 FeSO
(5)煅烧 3也能生成 2 3。实验室以 4溶液为原料制备高产率、较纯
Fe O Fe(OH) pH 6.5
净的 2 3。已知: 2开始沉淀的 ,请补充完整实验方案:在搅拌下_______________,
FeCO Fe O
将固体干燥,得到纯净的 3放入管式炉内煅烧2h,获得产品 2 3。(必须使用的试剂:
0.1molL1 NH HCO 2molL1 BaCl
4 3溶液、 盐酸、 2溶液、蒸馏水)
SO
18.(15分)对燃煤烟气或煤浆进行脱硫能有效降低排入大气中的 2含量。
Ⅰ.燃煤烟气脱硫
MnO SO
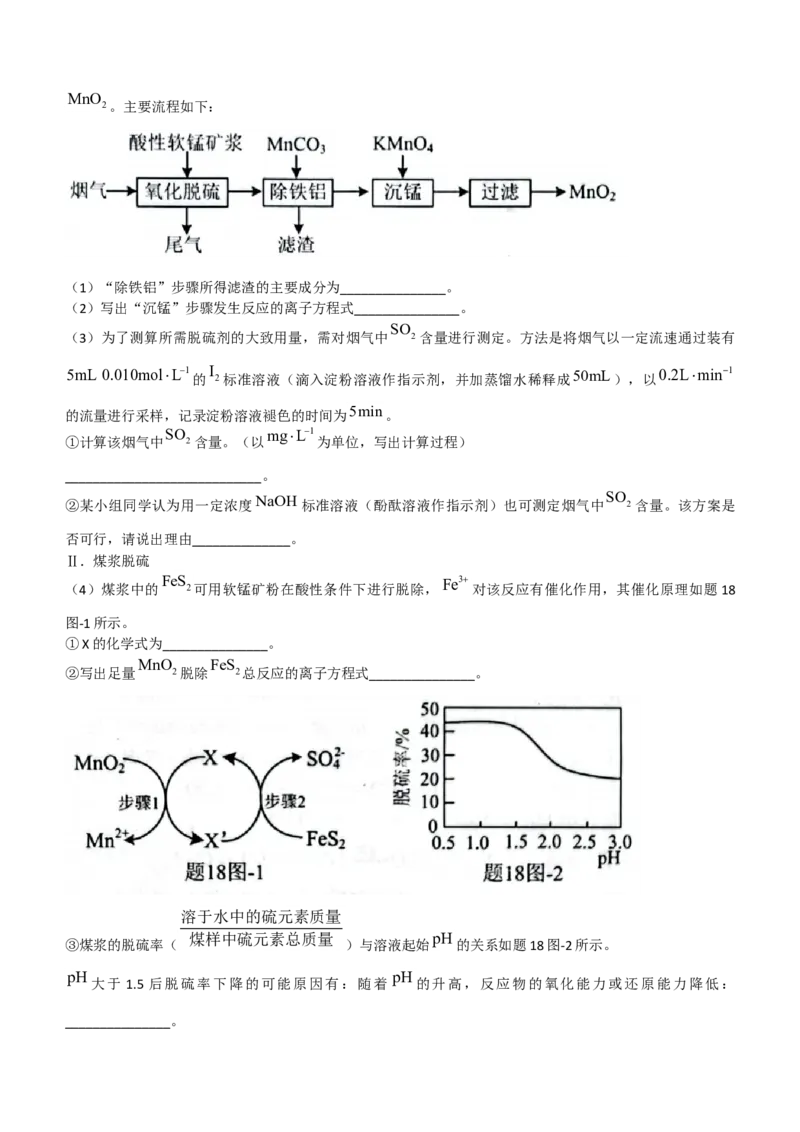
软锰矿浆(主要成分 2,含有少量铁、铝等氧化物)可脱除燃煤烟气中的 2,又可制得电池材料MnO
2。主要流程如下:
(1)“除铁铝”步骤所得滤渣的主要成分为_______________。
(2)写出“沉锰”步骤发生反应的离子方程式_______________。
SO
(3)为了测算所需脱硫剂的大致用量,需对烟气中 2含量进行测定。方法是将烟气以一定流速通过装有
5mL 0.010molL1 的 I 2标准溶液(滴入淀粉溶液作指示剂,并加蒸馏水稀释成50mL),以 0.2Lmin1
的流量进行采样,记录淀粉溶液褪色的时间为5min。
SO mgL1
①计算该烟气中 2含量。(以 为单位,写出计算过程)
____________________________。
SO
NaOH
②某小组同学认为用一定浓度 标准溶液(酚酞溶液作指示剂)也可测定烟气中 2含量。该方案是
否可行,请说出理由______________。
Ⅱ.煤浆脱硫
FeS Fe3
(4)煤浆中的 2可用软锰矿粉在酸性条件下进行脱除, 对该反应有催化作用,其催化原理如题18
图-1所示。
①X的化学式为_______________。
MnO FeS
②写出足量 2脱除 2总反应的离子方程式_______________。
溶于水中的硫元素质量
煤样中硫元素总质量 pH
③煤浆的脱硫率( )与溶液起始 的关系如题18图-2所示。
pH pH
大于 1.5 后脱硫率下降的可能原因有:随着 的升高,反应物的氧化能力或还原能力降低:
_______________。苏州市2021~2022学年第二学期学业质量阳光指标调研卷(延期)
高二化学参考答案
2022.08
一、单项选择题:包括14小题,每小题3分,共42分。每小题只有一个选项最符合题意。
1.B2.D3.A4.D5.C6.D7.D8.A9.B10.C11.B12.C13.A14.B
二、非选择题:共4题,共58分。
15.(14分)
(1)①7mol(2分)
NH BH CH CH
② 3 3分子之间有氢键, 3 3分子之间只有范德华力(2分)
1s22s22p63s23p63d64s2 [Ar]3d64s2
(2)① 或 (2分)
②1∶2(2分)
催化剂
NH BH 2H O NH BO 3H
3 3 2 4 2 2
③ (2分)
BNH BH NH
(3)① 4或 2 2 n(2分)
②3∶2(2分)
16.(14分)
NONO 2OH 2NO H O
2 2 2
(1)① (2分)
NaNO
② 3(1分) NO(1分)
(2)①-3(2分)
250℃~380℃
8NH 6NO 7N 12H O
3 2 2 2
催化剂
② (2分)SO O 、H O H SO H SO NH NH SO NH HSO
③ 2与 2 2 反应生成 2 4, 2 4与 3反应生成 4 2 4或者 4 4(3分)
NH
④温度升高, 3催化氧化生成NO(3分)
17.(15分)
0.8molL1
(1) (2分)
4Fe(OH) O 4FeOOH2H O
0t 2 2 2 c
H
(2) 1段发生反应 ,溶液中 基本不变(3分)
4FeSO O 6H O 4FeOOH 4H SO
(3)
t
1
t
2段发生反应
4 2 2 2 4 ,生成大量H
,溶液中
c
H
增
大(3分)
Fe O Fe O
(4)部分 2 3分解生成 3 4或FeO(2分)
100mL 0.1molL1 FeSO 200mL 0.1molL1 NH HCO
(5)向 4溶液中缓慢滴加约 4 3溶液,静置后过滤,
2molL1 BaCl
所得沉淀用蒸馏水洗涤2~3次:取最后一次洗涤后的滤液,滴入 盐酸酸化后再滴加 2溶液,
无浑浊(5分)
18.(15分)
Fe(OH) 、Al(OH)
(1) 3 3(2分,各1分)
3Mn2 2MnO 2H O 5MnO 4H
4 2 2
(2) (2分)
nI 0.010molL15103L5105mol
(3)① 2
SO + I 2H O H SO 2HI
2 2 2 2 4
1mol 1mol
n(SO ) 5105mol
2
nSO 5105mol
2
5105mol64gmol1103mgg1
3.2mgL1
烟气中
SO
2含量
0.2Lmin15min
(2分)
CO
NaOH
②不可行。烟气中含大量 2,也会消耗 溶液(2分)
FeSO Fe2
(4)① 4或 (1分)15MnO 2FeS 28H 15Mn2 2Fe3 4SO2 14H O
2 2 4 2
② (2分)
Fe3 Fe(OH) c
Fe3
Fe(OH)
③ 转化为 3沉淀, 减小,同时 3沉淀覆盖在矿粉表面,阻碍反应进行(3分)下载最新免费模拟卷,到公众号:一枚试卷君