文档内容
热点专项 溶液中离子平衡的图像
目录
01考情透视·目标导航............................................................................................................................
02知识导图·思维引航............................................................................................................................
03核心精讲·题型突破............................................................................................................................
【真题研析】...........................................................................................................................................................
【核心精讲】...........................................................................................................................................................
1.一元弱电解质.....................................................................................................................................................
2.二元弱电解质.....................................................................................................................................................
3.沉淀溶解平衡.....................................................................................................................................................
【命题预测】...........................................................................................................................................................
考向1 沉淀溶解平衡图象......................................................................................................................................
考向2多曲线离子反应图象...................................................................................................................................
考点要求 考题统计 考情分析
2024· 海南卷,14,4分;2024·江西卷,
弱酸、弱 13,3分;2024·浙江6月卷,15,3分; 近年来将离子反应与图像有机结
碱等相关 2024·河北卷,11,3分;2024·福建卷, 合起来进行命题,维系粒子间关系、
曲线 10,4分;2024·全国新课标卷,7,3 曲线、直线间关系的是各种常数,故
分;2024·广西卷,1,3分; 命题及设问无围绕着这些常数的计
算、应用,以及三守恒来进行。预测
2024·辽吉黑卷,15,3分;2024·全国甲 2025年高考化学试题仍会保留一定
卷,7,6分;2024·湖北卷,13,3分; 量的曲线图试题,在题型稳定的基础
沉淀溶解
2023•全国乙卷,13,6分;2023•辽宁省 上追求创新,图象会变得复杂,信息
平衡曲线
选择性考试,15,3分;2022•山东卷, 量更大,综合性增强。
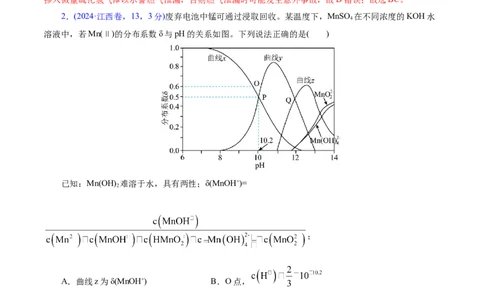
14,3分;1.(2024· 海南卷,14,4分)HO在生态系统的硫循环中不可或缺。298K,101 kPa时,水溶液中
2
价S不同形态的分布分数如图所示,下列说法正确的是( )
A.线a表示HS-的分布分数
B.298K时,NaS的PK 约为7.0
2 b2
C.1.0L1mol/L的 溶液吸收HS(g)的量大于
2
D.可以向燃气中掺入微量HS(g)以示警燃气泄漏
2
【答案】BC
【解析】氢硫酸是二元弱酸,在溶液中分步电离,溶液pH增大,溶液中氢硫酸的浓度减小,HS−的浓
度先增大后减小,S2-的浓度先不变后增大,则曲线a、b、c分别表示氢硫酸、HS−、S2-的分布分数;由图
可知,溶液中氢硫酸的浓度与HS−的浓度相等时,溶液pH为7,由电离常数K (H S)= 可知,
a1 2
电离常数K (H S)= c(H+)=1×10﹣7。A项,由分析可知,曲线a、b、c分别表示氢硫酸、HS−、S2-的分布分
a1 2数,故A错误;B项,电离常数K (H S)= c(H+)=1×10﹣7,则硫化钠的K = = =
a1 2 b2
=1×10﹣7,则PK 约为7,故B正确;C项,氢氧化钠溶液与过量的硫化氢反应生成硫氢化钠,
b2
则1.0L1mol/L的氢氧化钠溶液能与1mol硫化氢气体反应,由于硫化氢气体溶于水,所以1.0L1mol/L的氢
氧化钠溶液吸收硫化氢气体的物质的量大于1mol,故C正确;D项,硫化氢气体有毒,所以不能向燃气中
掺入微量硫化氢气体以示警燃气泄漏,否则燃气泄漏时可能发生意外事故,故D错误;故选BC。
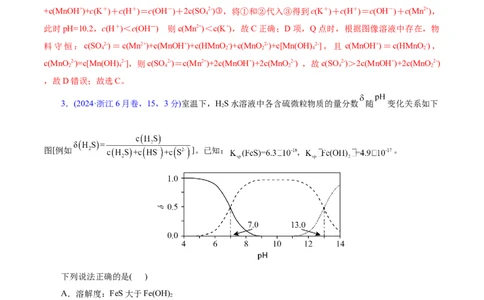
2.(2024·江西卷,13,3分)废弃电池中锰可通过浸取回收。某温度下,MnSO 在不同浓度的KOH水
4
溶液中,若Mn(Ⅱ)的分布系数δ与pH的关系如图。下列说法正确的是( )
已知:Mn(OH) 难溶于水,具有两性;δ(MnOH+)=
2
;
A.曲线z为δ(MnOH+) B.O点,
C.P点,c(Mn2+)<c(K+) D.Q点,c(SO 2-)=2c(MnOH+)+2c(MnO2-)
4 2
【答案】C
【解析】Mn(OH) 难溶于水,具有两性,某温度下,MnSO 在不同浓度的KOH水溶液中,若Mn(Ⅱ)
2 4
的分布系数δ与pH的关系如图,结合曲线变化和分布分数可知,pH较小时,Mn元素存在形式为Mn2+,
则曲线 x为Mn2+,曲线 y为MnOH+,曲线 z为HMnO -,结合图象变化分析判断选项。A项,z表示
2
δ(HMnO -),故 A 错误;B 项,图中 O 点存在电离平衡 Mn2++OH﹣ MnOH+,在 P 点时 c(Mn2+)=
2c(MnOH+),pH=10.2,K 103.8,O点δ(Mn2+)=0.6
时,δ(MnOH+)=0.4,则c(OH﹣) 10﹣3.8mol/L 10﹣3.8mol/L,则 ,故
B错误;C项,P点时δ(Mn2+)=δ(MnOH+)=0.5,溶液中含 Mn元素微粒只有这两种,根据物料守恒有
c(Mn2+)+c(MnOH+)=c(SO 2-),且 c(Mn2+)=c(MnOH+)① 即 2c(Mn2+)=c(SO 2-)②,根据电荷守恒有 2c(Mn2+)
4 4
+c(MnOH+)+cK++cH+=cOH-+2c(SO 2-)③,将①和②代入③得到cK++cH+=cOH-+cMn2+,
4
此时pH=10.2,c(H+)<c(OH―) 则c(Mn2+)<c(K+),故C正确;D项,Q点时,根据图像溶液中存在,物
料守恒:c(SO 2-)=c(Mn2+)+c(MnOH+)+c(HMnO -)+c(MnO2-)+c[Mn(OH)2-],且 c(MnOH+)=c(HMnO -),
4 2 2 4 2
c(MnO 2-)=c[Mn(OH)2-],则c(SO 2-)=c(Mn2+)+2c(MnOH+)+2c(MnO2-) ,故c(SO 2-)>2c(MnOH+)+2c(MnO2-)
2 4 4 2 4 2
,故D错误;故选C。
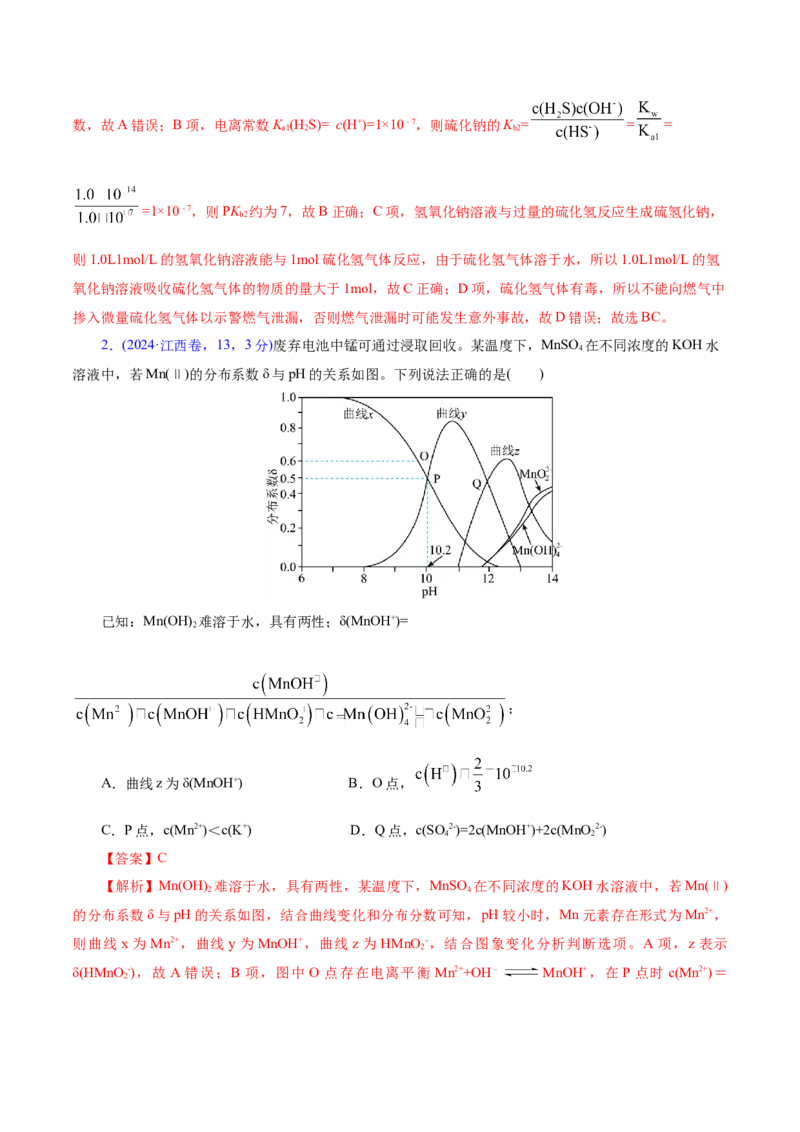
3.(2024·浙江6月卷,15,3分)室温下,HS水溶液中各含硫微粒物质的量分数 随 变化关系如下
2
图[例如 ]。已知: 。
下列说法正确的是( )
A.溶解度:FeS大于Fe(OH)
2
B.以酚酞为指示剂(变色的 范围8.2~10.0),用 标准溶液可滴定HS水溶液的浓度
2
C.忽略S2-的第二步水解,0.1mol/L的NaS溶液中S2-水解率约为
2
D. 0.010mol/L的FeCl 溶液中加入等体积 的NaS溶液,反应初始生成的沉淀是FeS
2 2
【答案】C
【解析】在HS溶液中存在电离平衡:HS H++HS-、HS- H++S2-,随着pH的增大,HS的
2 2 2
物质的量分数逐渐减小,HS-的物质的量分数先增大后减小,S2-的物质的量分数逐渐增大,图中线①、②、③依次代表HS、HS-、S2-的物质的量分数随pH的
2
变化,由①和②交点的pH=7可知K (H S)=1×10-7,由②和③交点的pH=13.0可知K (H S)=1×10-13。A项,
a1 2 a2 2
FeS的溶解平衡为FeS(s) Fe2+(aq)+S2-(aq),饱和FeS溶液物质的量浓度为 =
mol/L= ×10-9mol/L,Fe(OH) 的溶解平衡为Fe(OH) Fe2+(aq)+2OH-(aq),饱和Fe(OH) 溶液物质的
2 2 2
量浓度为 = mol/L= ×10-6mol/L> ×10-9mol/L,故溶解度:FeS小于
Fe(OH) ,A项错误;B项,酚酞的变色范围为8.2~10,若以酚酞为指示剂,用NaOH标准溶液滴定HS水
2 2
溶液,由图可知当酚酞发生明显颜色变化时,反应没有完全,即不能用酚酞作指示剂判断滴定终点,B项
错误;C项,NaS溶液中存在水解平衡S2-+H O HS-+OH-、HS-+H O HS+OH-(忽略第二步水
2 2 2 2
解),第一步水解平衡常数K (S2-)= = = = =0.1,设水解的
h
S2-的浓度为x mol/L,则 =0.1,解得x≈0.062,S2-的水解率约为 ×100%=62%,C项正确;D
项,0.01mol/L FeCl 溶液中加入等体积0.2mol/L Na S溶液,瞬间得到0.005mol/L FeCl 和0.1mol/L Na S的
2 2 2 2
混合液,结合C项,瞬时c(Fe2+)c(S2-)=0.005mol/L×(0.1mol/L-0.062mol/L)=1.9×10-4>K (FeS),
sp
c(Fe2+)c2(OH-)=0.005mol/L×(0.062mol/L)2=1.922×10-5>K [Fe(OH) ],故反应初始生成的沉淀是FeS和
sp 2
Fe(OH) ,D项错误;故选C。
2
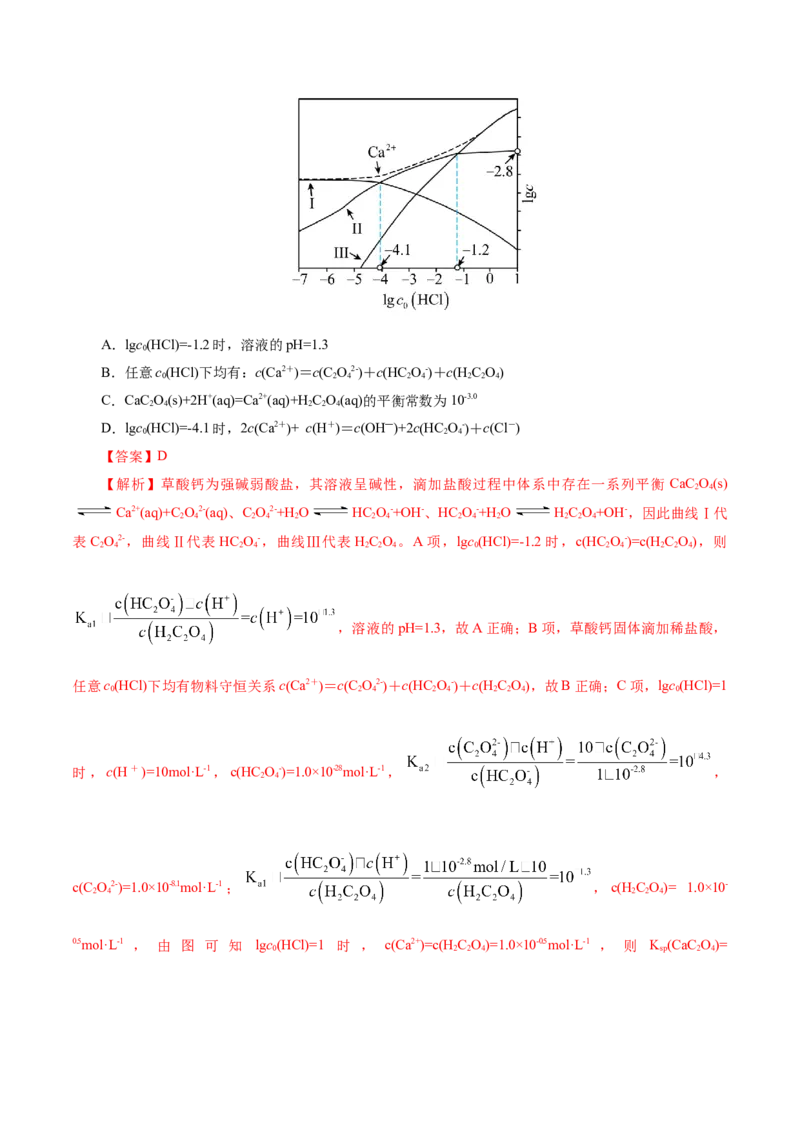
4.(2024·福建卷,10,4分)将草酸钙固体溶于不同初始浓度[c(HCl)]的盐酸中,平衡时部分组分的
0
lgc- lgc(HCl)关系如图。已知草酸K =10-1.3,K =10-4.3。下列说法错误的是( )
0 a1 a2A.lgc(HCl)=-1.2时,溶液的pH=1.3
0
B.任意c(HCl)下均有:cCa2+=cC O2-+cHC O-+cHC O
0 2 4 2 4 2 2 4
C.CaC O(s)+2H+(aq)=Ca2+(aq)+H C O(aq)的平衡常数为10-3.0
2 4 2 2 4
D.lgc(HCl)=-4.1时,2cCa2++ c(H+)=c(OH―)+2cHC O-+c(Cl-)
0 2 4
【答案】D
【解析】草酸钙为强碱弱酸盐,其溶液呈碱性,滴加盐酸过程中体系中存在一系列平衡 CaC O(s)
2 4
Ca2+(aq)+C O2-(aq)、C O2-+H O HC O-+OH-、HC O-+H O HC O+OH-,因此曲线Ⅰ代
2 4 2 4 2 2 4 2 4 2 2 2 4
表C O2-,曲线Ⅱ代表HC O-,曲线Ⅲ代表HC O 。A项,lgc(HCl)=-1.2时,c(HC O-)=c(HC O),则
2 4 2 4 2 2 4 0 2 4 2 2 4
,溶液的pH=1.3,故A正确;B项,草酸钙固体滴加稀盐酸,
任意c(HCl)下均有物料守恒关系cCa2+=cC O2-+cHC O-+cHC O,故B正确;C项,lgc(HCl)=1
0 2 4 2 4 2 2 4 0
时,c(H+)=10mol·L-1,c(HC O-)=1.0×10-28mol·L-1, ,
2 4
c(C O2-)=1.0×10-8.1mol·L-1; ,c(HC O)= 1.0×10-
2 4 2 2 4
0.5mol·L-1 , 由 图 可 知 lgc(HCl)=1 时 , c(Ca2+)=c(HC O)=1.0×10-0.5mol·L-1 , 则 K (CaC O)=
0 2 2 4 sp 2 4c(Ca2+)×c(C O2-)=1.0×10-8.6;CaC O(s)+2H+(aq)=Ca2+(aq)+H C O(aq)的平衡常数 K=
2 4 2 4 2 2 4
= = = ,故 C 正确;D
项,溶液中存在电荷守恒 2cCa2++ c(H+)=c(OH―)+cHC O-+2cC O2-+c(Cl-),lgc(HCl)=-4.1时,
2 4 2 4 0
c(C O2-)=c(HC O-),则存在关系2cCa2++c(H+)=c(OH―)+3cHC O-+c(Cl-),故D错误;故选D。
2 4 2 4 2 4
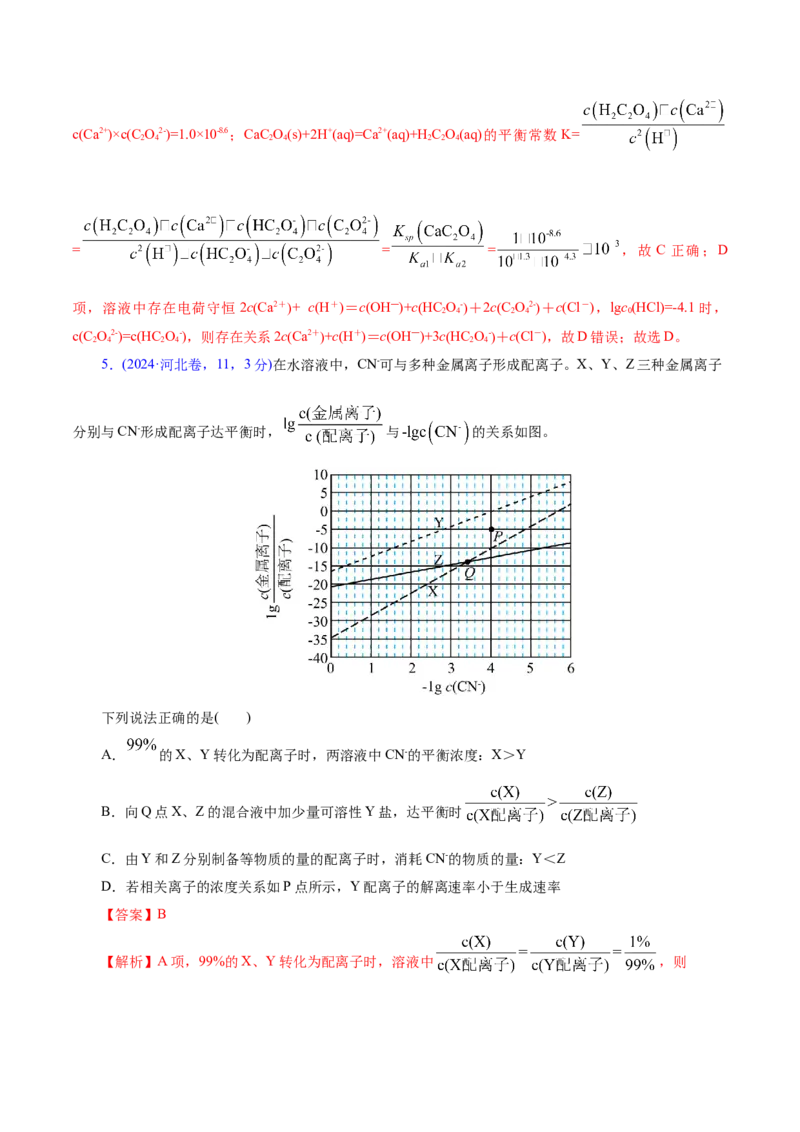
5.(2024·河北卷,11,3分)在水溶液中,CN-可与多种金属离子形成配离子。X、Y、Z三种金属离子
分别与CN-形成配离子达平衡时, 与 的关系如图。
下列说法正确的是( )
A. 的X、Y转化为配离子时,两溶液中CN-的平衡浓度:X>Y
B.向Q点X、Z的混合液中加少量可溶性Y盐,达平衡时
C.由Y和Z分别制备等物质的量的配离子时,消耗CN-的物质的量:Y<Z
D.若相关离子的浓度关系如P点所示,Y配离子的解离速率小于生成速率
【答案】B
【解析】A项,99%的X、Y转化为配离子时,溶液中 ,则,根据图像可知,纵坐标约为-2时,溶液中
,则溶液中CN-的平衡浓度:X<Y,A错误;B项,Q点时
,即 ,加入少量可溶性Y盐后,会消耗CN-
形成Y配离子,使得溶液中c(CN-)减小(沿横坐标轴向右移动), 与 曲线在
Q点相交后,随着 继续增大,X对应曲线位于Z对应曲线上方,即
,则 ,B正确;C项,设金属离子形成配离
子的离子方程式为金属离子 配离子,则平衡常数 ,
,即
,故X、Y、Z三种金属离子形成配离子时结合的CN-越多,对应
曲线斜率越大,由题图知,曲线斜率:Y>Z,则由Y、Z制备等物质的量的
配离子时,消耗CN-的物质的量:Z<Y,C错误;D项,由P点状态移动到形成Y配离子的反应的平衡状
态时, 不变, 增大,即c(Y)增大、c(Y配离子)减小,则P点状态Y配离子的解
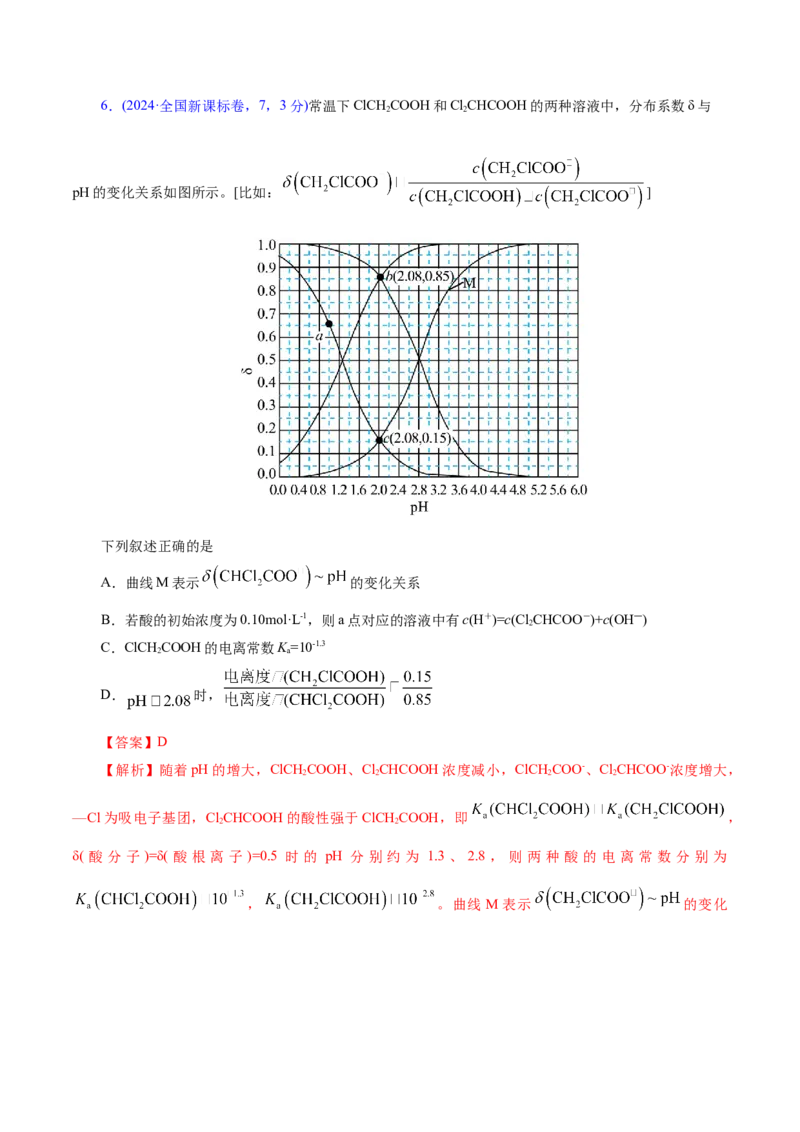
离速率>生成速率,D错误;故选B。6.(2024·全国新课标卷,7,3分)常温下ClCHCOOH和ClCHCOOH的两种溶液中,分布系数δ与
2 2
pH的变化关系如图所示。[比如: ]
下列叙述正确的是
A.曲线M表示 的变化关系
B.若酸的初始浓度为0.10mol·L-1,则a点对应的溶液中有c(H+)=c(ClCHCOO-)+c(OH―)
2
C.ClCHCOOH的电离常数K=10-1.3
2 a
D. 时,
【答案】D
【解析】随着pH的增大,ClCHCOOH、ClCHCOOH浓度减小,ClCHCOO-、ClCHCOO-浓度增大,
2 2 2 2
—Cl为吸电子基团,ClCHCOOH的酸性强于ClCHCOOH,即 ,
2 2
δ( 酸 分 子 )=δ( 酸 根 离 子 )=0.5 时 的 pH 分 别 约 为 1.3 、 2.8 , 则 两 种 酸 的 电 离 常 数 分 别 为
, 。曲线 M表示 的变化关 系 , A 错 误 ; B 项 , 根 据 , 初 始
, 若 溶 液 中 溶 质 只 有 ClCHCOOH , 则
2
,但 a 点对应的
c(H+)=0.1mol·L-1,说明此时溶液中加入了酸性更强的酸,根据电荷守恒,c(H+)>c(ClCHCOO-)
2
+c(OH―),B错误;CHClCOOH的电离常数K=10-2.8,C错误;电离度 , ,则
2 a
= , , pH=2.08 时 ,
, ,D正确;故选D。
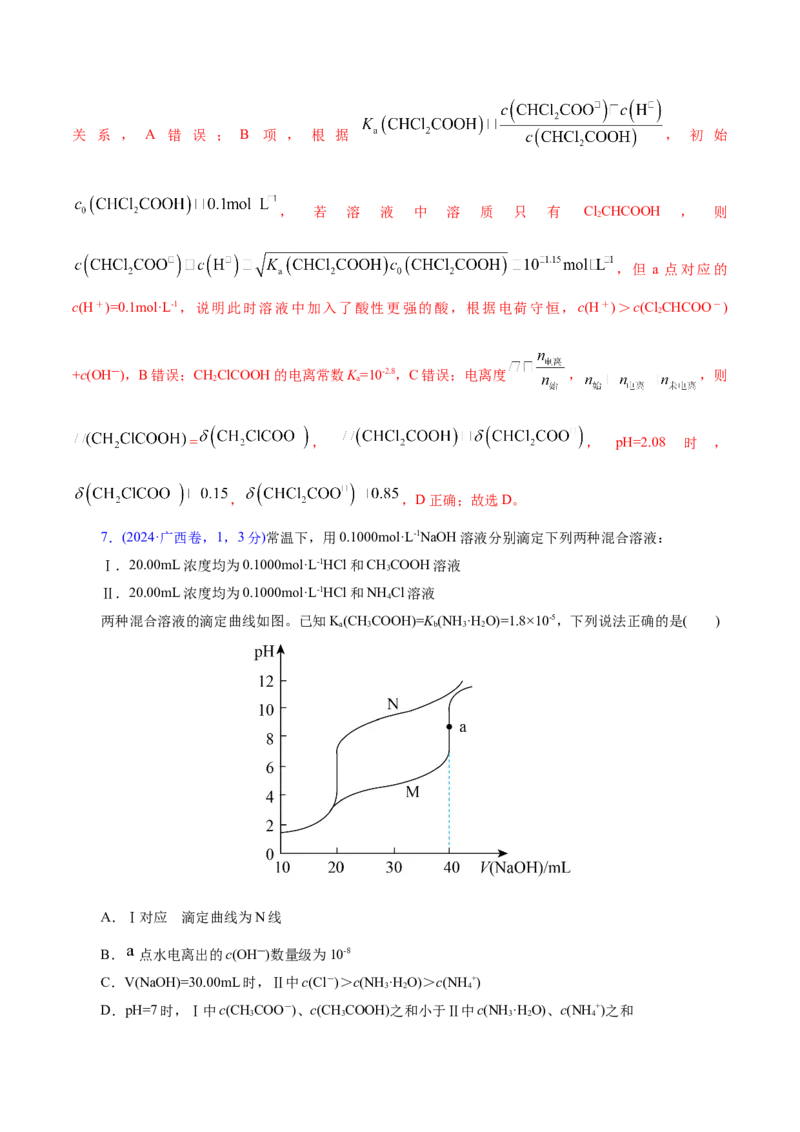
7.(2024·广西卷,1,3分)常温下,用0.1000mol·L-1NaOH溶液分别滴定下列两种混合溶液:
Ⅰ.20.00mL浓度均为0.1000mol·L-1HCl和CHCOOH溶液
3
Ⅱ.20.00mL浓度均为0.1000mol·L-1HCl和NH Cl溶液
4
两种混合溶液的滴定曲线如图。已知K(CHCOOH)=K (NH ·H O)=1.8×10-5,下列说法正确的是( )
a 3 b 3 2
的
A.Ⅰ对应 滴定曲线为N线
B. 点水电离出的c(OH―)数量级为10-8
C.V(NaOH)=30.00mL时,Ⅱ中c(Cl-)>c(NH ·H O)>c(NH +)
3 2 4
D.pH=7时,Ⅰ中c(CHCOO-)、c(CHCOOH)之和小于Ⅱ中c(NH ·H O)、c(NH +)之和
3 3 3 2 4【答案】D
【解析】溶液中加入40ml氢氧化钠溶液时,I中的溶质为氯化钠和醋酸钠,Ⅱ中的溶质为氯化钠和一
水合氨,根据K(CHCOOH)=K (NH ·H O)=1.8×10-5,醋酸根、铵根的水解程度小于醋酸、一水合氨的电离
a 3 b 3 2
程度,氯化钠显中性,醋酸根和一水合氨在浓度相同时,一水合氨溶液的碱性更强,故I对应的滴定曲线
为M,Ⅱ对应的滴定曲线为N。A项,向溶液中加入40ml氢氧化钠溶液时,I中的溶质为氯化钠和醋酸钠,
Ⅱ中的溶质为氯化钠和一水合氨,氯化钠显中性,醋酸根和一水合氨在浓度相同时,一水合氨溶液的碱性
更强,故I对应的滴定曲线为M,A错误;B项,a点的溶质为氯化钠和醋酸钠,醋酸根发生水解,溶液的
pH接近8,由水电离的c(H+)=c(OH―),数量级接近10-6,B错误;C项,当V(NaOH)=30.00mL时,Ⅱ中的
溶质为氯化钠、氯化铵、一水合氨,且氯化铵和一水合氨的浓度相同,铵根的水解
,即NH +水解程度小于一水合氨的电离程度,所以c(NH +)
4 4
>c(NH ·H O),又物料守恒c(Cl-)=2c(NH +)+2c(NH ·H O),即c(Cl-)>c(NH +),故c(Cl-)>c(NH +)>
3 2 4 3 2 4 4
c(NH ·H O),C错误;D项, 根据元素守恒,n(CHCOO-)、n(CHCOOH)之和等于n(NH ·H O)、n(NH +)
3 2 3 3 3 2 4
之和,根据图像,pH=7时,Ⅱ所加氢氧化钠溶液较少,溶液体积较小,故Ⅰ中c(CHCOO-)、
3
c(CHCOOH)之和小于Ⅱ中c(NH ·H O)、c(NH +)之和,D正确;故选D。
3 3 2 4
8.(2024·全国甲卷,7,3分)将0.10 mmol Ag CrO 配制成1.0mL悬浊液,向其中滴加0.10mol·L-1的
2 4
NaCl溶液。 (M代表Ag+、Cl-或CrO2-)随加入NaCl溶液体积(V)的变化关系如图所示。
4
下列叙述正确的是( )
A.交点a处:c(Na+)=2c(Cl-) B.C. 时, 不变 D.y=-7.82,y= -lg34
1 2
【答案】D
【解析】向 1.0mL 含 0.10 mmol Ag CrO 的悬浊液中滴加 0.10mol·L-1的 NaCl 溶液,发生反应:
2 4
Ag CrO(s)+2Cl-(aq) 2AgCl(s)+ CrO2-(aq),两者恰好完全反应时, NaCl 溶液的体积为 v(NaCl)=
2 4 4
,2mL 之后再加 NaCl 溶液,c(Cl-)增大,据 AgCl(s) Ag+(aq)+Cl -(aq),
K (AgCl)=c(Ag+)c(Cl-)可知,c(Ag+)会随着c(Cl-)增大而减小,所以2mL后降低的曲线,即最下方的虚线代
sp
表Ag+,升高的曲线,即中间虚线代表Cl-,则剩余最上方的实线为CrO2-曲线。A项,2mL时Ag CrO 与
4 2 4
NaCl溶液恰好完全反应,则 a点时溶质为 NaCl和NaCrO ,电荷守恒:c(Na+)+c(Ag+)+c(H+)=2c(CrO 2-)
2 4 4
+c(Cl-)+c(OH-),此时 c(H+)、c(OH-)、c(Ag+)可忽略不计,a 点为 Cl-和 CrO2-曲线的交点,即
4
c(CrO 2-)=c(Cl-),则溶液中c(Na+)≈3c(Cl-),A错误;B项,当V(NaCl)=1.0mL时,有一半的Ag CrO 转化为
4 2 4
AgCl,Ag CrO 与 AgCl 共存,均达到沉淀溶解平衡,取图中横坐标为 1.0mL 的点,得 K (AgCl)=
2 4 sp
c(Ag+)c(Cl-)=10-5.18×10-4.57=10-9.75,K (Ag CrO)= c2(Ag+)c(CrO2-)=(10-5.18)2×10-1.60=10-11.96,则 =
sp 2 4 4
=102.21,B 错误;C 项,V<2.0mL 时,Ag+未沉淀完全,体系中 Ag CrO 和 AgCl 共存,则
2 4
= 为定值,即 为定值,由图可知,在 V≤2.0mL
时c(Ag+)并不是定值,则 的值也不是定值,即在变化,C错误;D项,V>2.0mL时AgCl处于
饱和状态,V(NaCl)=2.4mL 时,图像显示 c(Cl-)=10-1.93mol/L,则 c(Ag+)= = =10-7.82mol/L,故 y=-7.82,此时 Ag CrO 全部转化为 AgCl,n(CrO 2-)守恒,等于起始时 n(Ag CrO),则
1 2 4 4 2 4
c(CrO 2-)= = = mol/L,则y=lg c(CrO 2-)=lg =-lg34,D正确;故选D。
4 2 4
9.(2024·辽吉黑卷,15,3分) 下,AgCl、AgBr和Ag CrO 的沉淀溶解平衡曲线如下图所示。某
2 4
实验小组以KCrO 为指示剂,用AgNO 标准溶液分别滴定含Cl-水样、含Br-水样。
2 4 3
已知:①Ag CrO 为砖红色沉淀;
2 4
②相同条件下AgCl溶解度大于AgBr;
③ 时, , 。
下列说法错误的是( )
A.曲线②为AgCl沉淀溶解平衡曲线
B.反应Ag CrO+2H+ 2Ag++HCrO-的平衡常数K=10-5.2
2 4 4
C.滴定Cl-时,理论上混合液中指示剂浓度不宜超过10-2.0 mol·L-1
D.滴定Br-达终点时,溶液中
【答案】D
【解析】由于AgCl和AgBr中阴、阳离子个数比均为1:1,即两者图象平行,所以①代表Ag CrO,
2 4
由于相同条件下,AgCl溶解度大于AgBr,即 ,所以②代表AgCl,则③代表
AgBr,根据①上的点(2.0,7.7),可求得
,根据②上的点(2.0,7.7),可求得,根据③上的点(6.1,6.1),可求得
。A项,曲线②为AgCl沉淀溶解平衡曲线,A正
确;B项,反应Ag CrO+2H+ 2Ag++HCrO-的平衡常数
2 4 4
,B正确;
C项,当Cl-恰好滴定完全时, ,即
,因此,指示剂的浓度不宜超过10-2mol/L,C正确;
D项,当Br-到达滴定终点时, ,即
, ,D错误;故选D。
10.(2024·湖北卷,13,3分)CO 气氛下,Pb(ClO) 溶液中含铅物种的分布如图。纵坐标(δ)为组分中
2 4 2
铅占总铅的质量分数。已知c(Pb2+)=2.0×10-5mol/L, 、 ,
0
。下列说法错误的是( )A.pH=6.5时,溶液中c(CO2-)50%,即c(Pb2+)>1×10-5mol/L,则c(CO2-)≤
3
= mol/L=10-7.1mol/LK (H CO),NaHCO 溶液呈碱性,
3 3 a2 2 3 3
加入少量NaHCO 固体,溶液pH增大,PbCO 转化成[Pb(CO)2-而溶解,D正确;故选C。
3 3 3 2
11.(2023•全国乙卷,13)一定温度下,AgCl和Ag CrO 的沉淀溶解平衡曲线如图所示。
2 4
下列说法正确的是( )
A.a点条件下能生成Ag CrO 沉淀,也能生成AgCl沉淀
2 4
B.b点时,c(Cl-)=c(CrO 2-),K (AgCl)=K (Ag CrO)
4 sp sp 2 4
C.Ag CrO+2Cl- 2AgCl+CrO 2-的平衡常数K=107.9
2 4 4
D.向NaCl、NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO 溶液,先产生Ag CrO 沉淀
2 4 3 2 4
【答案】C【解析】根据图像,由(1.7,5)可得到Ag CrO 的溶度积K (Ag CrO)=c2(Ag+)·c(CrO 2-)=(1×10-5)2×1×10-
2 4 sp 2 4 4
1.7=10-11.7,由(4.8,5)可得到AgCl的溶度积K (AgCl)=c(Ag+)·c(Cl)=1×10-5×1×10-4.8=10-9.8,据此数据计算各选
sp
项结果。A项,假设a点坐标为(4,6.5),此时分别计算反应的浓度熵Q得,Q(AgCl)=10-10.5,
Q(Ag CrO)=10-17,二者的浓度熵均小于其对应的溶度积K ,二者不会生成沉淀,A错误;B项,K 为难
2 4 sp sp
溶物的溶度积,是一种平衡常数,平衡常数只与温度有关,与浓度无关,根据分析可知,二者的溶度积不
相同,B错误;C项,该反应的平衡常数表达式为K= ,将表达式转化为与两种难溶物的溶度积有
关的式子得K= = = = =1×107.9,C正确;D项,向NaCl、
NaCrO 均为0.1mol·L-1的混合溶液中滴加AgNO,开始沉淀时所需要的c(Ag+)分别为10-8.8和10-5.35,说明
2 4 3
此时沉淀Cl-需要的银离子浓度更低,在这种情况下,先沉淀的是AgCl,D错误;故选C。
电解质溶液图像题解题程序
(1)审题:弄清图像含义,通过观察弄清横坐标、纵坐标的含义及单位;搞清特殊点的意义,如坐标轴
的原点,曲线的起点、终点、交叉点、极值点、转折点等;分析曲线的变化趋势,如斜率的大小及升降。
(2)信息提取:挖掘隐含信息,排除干扰信息,提炼有用信息,在提炼信息的基础上进行逻辑推理或运
用数据计算。
(3)答题:联想化学原理,根据选项内容,确定正确选项。
1 .一元弱电解质2 .二元弱电解质3 .沉淀溶解平衡考向 1 沉淀溶解平衡图象
1.[新题型](2025·湖南省a佳教育高三联考)将一定量BaCO 固体粉末分别投入物质的量浓度均为
3
0.1mol·L-1NaSO 、NaCrO 溶液中,得到 或 与 的变化关系如图。
2 4 2 4
忽略溶液体积的变化。已知:常温下, 。下
列说法正确的是( )
A.曲线b表示 与 的变化关系
B.当 ,则BaCO 已部分转化为曲线b对应的沉淀BaM
3
C.BaCrO (s)+ SO 2- (aq) BaSO(s)+ CrO2-(aq)的平衡常数
4 4 4 4
D.m点时,溶液中存在cCO2-+cHCO -+cHCO=0.1 mol·L-1
3 3 2 3
【答案】B
【解析】A项,BaCO 与NaSO 、NaCrO 分别发生反应:BaCO (s)+SO 2-(aq) BaSO(s)+CO2-
3 2 4 2 4 3 4 4 3
(aq), 、BaCO (s)+ CrO2-(aq) BaCrO (s)+CO 2-(aq),
3 4 4 3
,故曲线a表示 与 的变化关系,A错误;B项,时,即BaCO (s)+ CrO2-(aq) BaCrO (s)+CO 2-(aq), ,已达到平衡或逆向
3 4 4 3
移动,说明BaCrO(s)已然生成,B项正确;C项,BaCrO (s)+ SO 2- (aq) BaSO(s)+ CrO2-(aq)的平
4 4 4 4 4
衡常数 ,C错误;D项,图示可知,m点对应碳酸根浓度已然超过0.1
mol·L-1,因此cCO2-+cHCO -+cHCO>0.1 mol·L-1,D错误; 故选B。
3 3 2 3
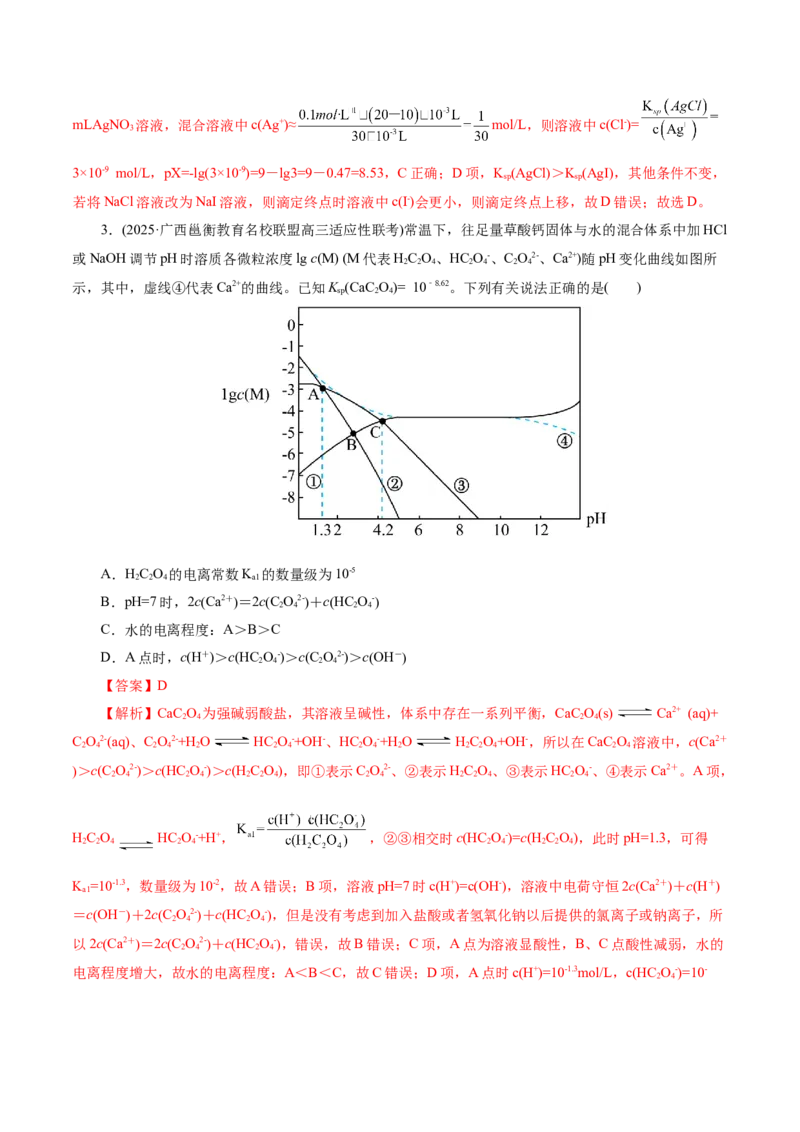
2.(2025·浙江省新阵进教育联盟高三联考)室温下,取浓度均为0.1mol·L-1的NaCl溶液、KCrO 溶液
2 4
各10.00mL于锥形瓶中,分别用0.1mol·L-1的AgNO 溶液滴定,滴定过程中的pX[pX=-lg c(X),X=Cl-、
3
CrO2-]与滴加AgNO 溶液体积的关系图所示,已知:Ag CrO 为红色,lg3=0.47。下列说法不正确的是(
4 3 2 4
)
A.可用KCrO 溶液作AgNO 溶液滴定NaCl溶液的指示剂
2 4 3
B.K (Ag CrO)=4.0×10-12
sp 2 4
C.a=8.53
D.其他条件不变,若将NaCl溶液改为NaI溶液,则滴定终点向下移动
【答案】D
【解析】由图可知,pX=4或5时反应完全,并且二者的起始浓度、体积均相同,即二者溶质的起始物
质的量相同,发生反应为:NaCl+AgNO =AgCl↓+NaNO 、NaCrO+2AgNO =Ag CrO↓+2NaNO ,完全反应
3 3 2 4 3 2 4 3
时NaCrO 消耗AgNO 溶液的体积是NaCl的2倍,所以曲线Ⅱ表示NaCl溶液滴定曲线、曲线Ⅰ表示
2 4 3
NaCrO 溶液滴定曲线,达到滴定终点时pX=4,即c(CrO2-)=1.0×10-4 mol/L,Ag CrO(s)⇌2Ag+(aq)+CrO 2-
2 4 4 2 4 4
(aq),则c(Ag+)=2c(CrO 2-)=2.0×10-4 mol/L,K (Ag CrO)=c2(Ag+)•c(CrO 2-)=(2.0×10-4)2×(1.0×10-4)=4.0×10-12,
4 sp 2 4 4
pX=5时,生成恰好生成AgCl,此时c(Cl-)=c(Ag+)=10-5 mol/L,K (AgCl)=c(Ag+)•c(Cl-)=10-10。A项,由图
sp
可知,当AgCl沉淀完全时,CrO2-浓度几乎不变,即向含有相同浓度的Cl-和CrO2-混合溶液中滴加硝酸银
4 4
溶液,先产生AgCl沉淀,故可以用KCrO 溶液作AgNO 溶液滴定NaCl溶液的指示剂,故A正确;B项,
2 4 3
K (Ag CrO)=c2(Ag+)•c(CrO 2-)=(2.0×10-4)2×(1.0×10-4)=4.0×10-12,故B正确;C项,当在NaCl溶液中加入20
sp 2 4 4mLAgNO 溶液,混合溶液中c(Ag+)≈ mol/L,则溶液中c(Cl-)=
3
3×10-9 mol/L,pX=-lg(3×10-9)=9-lg3=9-0.47=8.53,C正确;D项,K (AgCl)>K (AgI),其他条件不变,
sp sp
若将NaCl溶液改为NaI溶液,则滴定终点时溶液中c(I-)会更小,则滴定终点上移,故D错误;故选D。
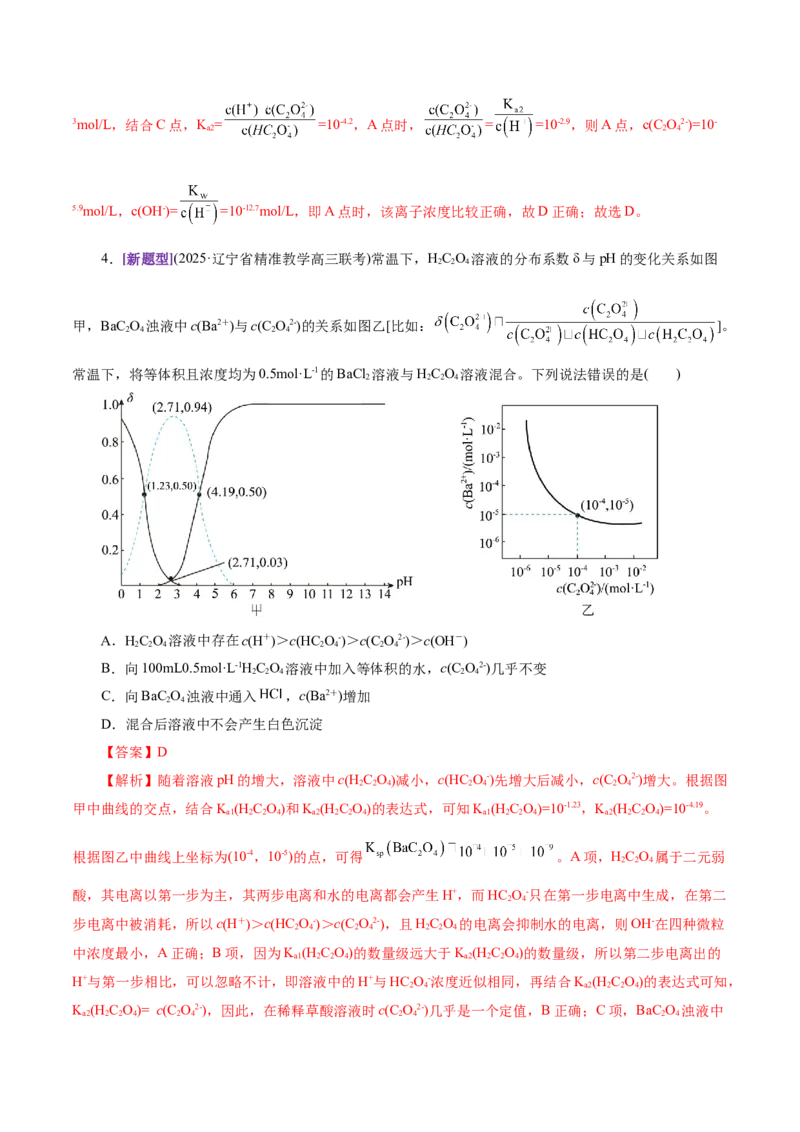
3.(2025·广西邕衡教育名校联盟高三适应性联考)常温下,往足量草酸钙固体与水的混合体系中加HCl
或NaOH调节pH时溶质各微粒浓度lg c(M) (M代表HC O、HC O-、C O2-、Ca2+)随pH变化曲线如图所
2 2 4 2 4 2 4
示,其中,虚线④代表Ca2+的曲线。已知K (CaC O)= 10-8.62。下列有关说法正确的是( )
sp 2 4
A.HC O 的电离常数K 的数量级为10-5
2 2 4 a1
B.pH=7时,2cCa2+=2cC O2-+cHC O-
2 4 2 4
C.水的电离程度:A>B>C
D.A点时,c(H+)>c(HC O-)>c(C O2-)>cOH-
2 4 2 4
【答案】D
【解析】CaC O 为强碱弱酸盐,其溶液呈碱性,体系中存在一系列平衡,CaC O(s) Ca2+ (aq)+
2 4 2 4
C O2-(aq)、C O2-+H O HC O-+OH-、HC O-+H O HC O+OH-,所以在CaC O 溶液中,cCa2+
2 4 2 4 2 2 4 2 4 2 2 2 4 2 4
>c(C O2-)>c(HC O-)>c(H C O),即①表示C O2-、②表示HC O、③表示HC O-、④表示Ca2+。A项,
2 4 2 4 2 2 4 2 4 2 2 4 2 4
HC O HC O-+H+, ,②③相交时c(HC O-)=c(H C O),此时pH=1.3,可得
2 2 4 2 4 2 4 2 2 4
K =10-1.3,数量级为10-2,故A错误;B项,溶液pH=7时c(H+)=c(OH-),溶液中电荷守恒2cCa2++cH+
a1
=cOH-+2cC O2-+cHC O-,但是没有考虑到加入盐酸或者氢氧化钠以后提供的氯离子或钠离子,所
2 4 2 4
以2cCa2+=2cC O2-+cHC O-,错误,故B错误;C项,A点为溶液显酸性,B、C点酸性减弱,水的
2 4 2 4
电离程度增大,故水的电离程度:A<B<C,故C错误;D项,A点时c(H+)=10-1.3mol/L,c(HC O-)=10-
2 43mol/L,结合C点,K = =10-4.2,A点时, = =10-2.9,则A点,c(C O2-)=10-
a2 2 4
5.9mol/L,c(OH-)= =10-12.7mol/L,即A点时,该离子浓度比较正确,故D正确;故选D。
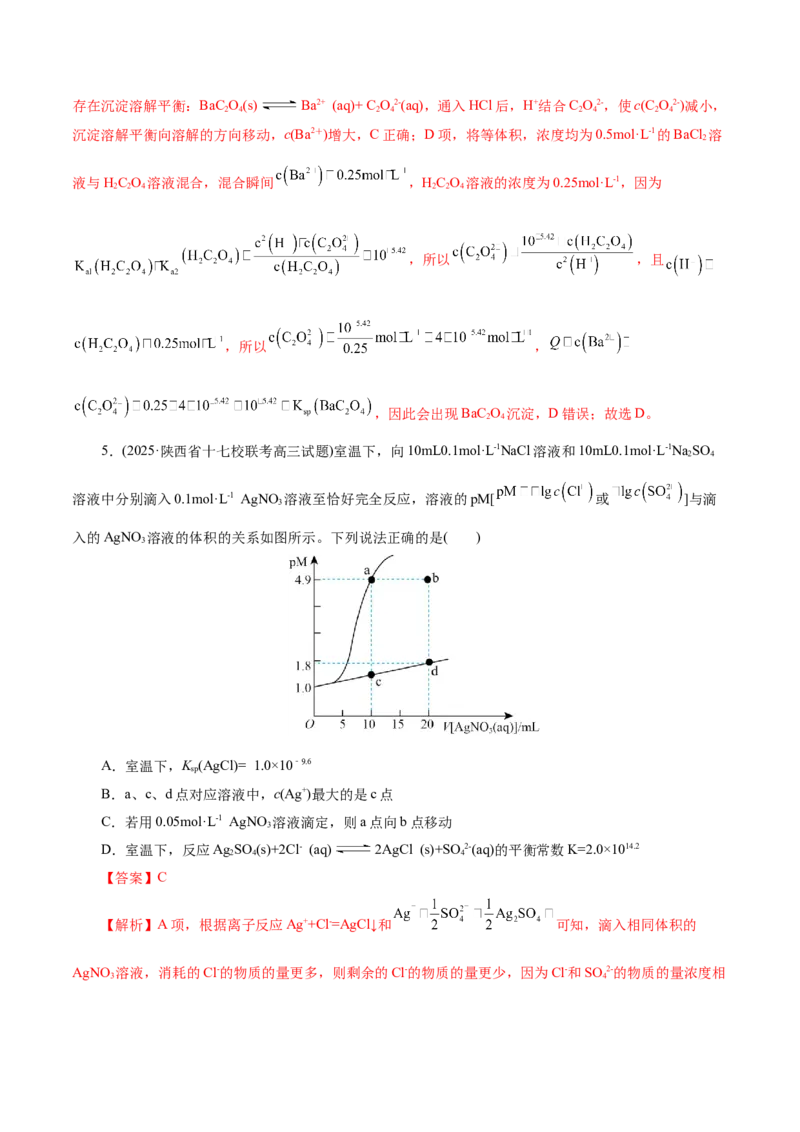
4.[新题型](2025·辽宁省精准教学高三联考)常温下,HC O 溶液的分布系数δ与pH的变化关系如图
2 2 4
甲,BaC O 浊液中c(Ba2+)与c(C O2-)的关系如图乙[比如: ]。
2 4 2 4
常温下,将等体积且浓度均为0.5mol·L-1的BaCl 溶液与HC O 溶液混合。下列说法错误的是( )
2 2 2 4
A.HC O 溶液中存在cH+>cHC O->cC O2->cOH-
2 2 4 2 4 2 4
B.向100mL0.5mol·L-1HC O 溶液中加入等体积的水,c(C O2-)几乎不变
2 2 4 2 4
C.向BaC O 浊液中通入 ,c(Ba2+)增加
2 4
D.混合后溶液中不会产生白色沉淀
【答案】D
【解析】随着溶液pH的增大,溶液中cHC O减小,c(HC O-)先增大后减小,c(C O2-)增大。根据图
2 2 4 2 4 2 4
甲中曲线的交点,结合K (H C O)和K (H C O)的表达式,可知K (H C O)=10-1.23,K (H C O)=10-4.19。
a1 2 2 4 a2 2 2 4 a1 2 2 4 a2 2 2 4
根据图乙中曲线上坐标为(10-4,10-5)的点,可得 。A项,HC O 属于二元弱
2 2 4
酸,其电离以第一步为主,其两步电离和水的电离都会产生H+,而HC O-只在第一步电离中生成,在第二
2 4
步电离中被消耗,所以cH+>cHC O->cC O2-,且HC O 的电离会抑制水的电离,则OH-在四种微粒
2 4 2 4 2 2 4
中浓度最小,A正确;B项,因为K (H C O)的数量级远大于K (H C O)的数量级,所以第二步电离出的
a1 2 2 4 a2 2 2 4
H+与第一步相比,可以忽略不计,即溶液中的H+与HC O-浓度近似相同,再结合K (H C O)的表达式可知,
2 4 a2 2 2 4
K (H C O)= c(C O2-),因此,在稀释草酸溶液时c(C O2-)几乎是一个定值,B正确;C项,BaC O 浊液中
a2 2 2 4 2 4 2 4 2 4存在沉淀溶解平衡:BaC O(s) Ba2+ (aq)+ C O2-(aq),通入HCl后,H+结合C O2-,使c(C O2-)减小,
2 4 2 4 2 4 2 4
沉淀溶解平衡向溶解的方向移动,c(Ba2+)增大,C正确;D项,将等体积,浓度均为0.5mol·L-1的BaCl 溶
2
液与HC O 溶液混合,混合瞬间 ,HC O 溶液的浓度为0.25mol·L-1,因为
2 2 4 2 2 4
,所以 ,且
,所以 ,
,因此会出现BaC O 沉淀,D错误;故选D。
2 4
5.(2025·陕西省十七校联考高三试题)室温下,向10mL0.1mol·L-1NaCl溶液和10mL0.1mol·L-1NaSO
2 4
溶液中分别滴入0.1mol·L-1 AgNO 溶液至恰好完全反应,溶液的pM[ 或 ]与滴
3
入的AgNO 溶液的体积的关系如图所示。下列说法正确的是( )
3
A.室温下,K (AgCl)= 1.0×10-9.6
sp
B.a、c、d点对应溶液中,c(Ag+)最大的是c点
C.若用0.05mol·L-1 AgNO 溶液滴定,则a点向b点移动
3
D.室温下,反应Ag SO (s)+2Cl- (aq) 2AgCl (s)+SO 2-(aq)的平衡常数K=2.0×1014.2
2 4 4
【答案】C
【解析】A项,根据离子反应Ag++Cl-=AgCl↓和 可知,滴入相同体积的
AgNO 溶液,消耗的Cl-的物质的量更多,则剩余的Cl-的物质的量更少,因为Cl-和SO 2-的物质的量浓度相
3 4同,故剩余的Cl-的pM值更大,故a点所在曲线代表 与滴入的AgNO 溶液的体积的关系,a点
3
对应溶液中 ,室温下, ,A错误;B
项,滴入20mL0.1mol·L-1 AgNO 溶液,10mL0.1mol·L-1NaSO 溶液恰好完全反应,根据图像曲线可知,d
3 2 4
点所在曲线代表 与滴入的AgNO 溶液的体积的关系,d点对应溶液中
3
,则溶液中 ,室温下,
。a点对应溶液中的 ,d点对
应溶液中的 ,c点对应溶液中NaSO 还剩余一半,c点对应溶液中的c(SO 2-)大
2 4 4
于d点对应溶液中的c(SO 2-),c、d两点温度相同(均为室温下),K (Ag SO )相同,则c点对应溶液中的
4 sp 2 4
c(Ag+)小于d点对应溶液中的c(Ag+),故a、c、d点对应溶液中,c(Ag+)最大的是d点,B错误;C项,a点
所在曲线代表 与滴入的AgNO 溶液的体积的关系,若用0.05mol·L-1 AgNO 溶液滴定
3 3
10mL0.1mol·L-1NaCl溶液,当滴入的 时,NaCl和AgNO 恰好完全反应,由于温度
3
不变,则K (AgCl)不变,此时溶液中 ,则图中a点向b点移动,C正确;D项,
sp
室温下,反应 的平衡常数
,D错误;故选C。
考向 2 多曲线离子反应图象
1.(2025·河南省安阳市湘豫名校联考高三检测)已知1,3-丙二酸是二元弱酸(简记为HR),在20.00mL
2
0.1000mol·L-1HR溶液中滴加VmL0.1000mol·L-1NaOH,混合溶液中含碳微粒的物质的量分数(分布系数)
2
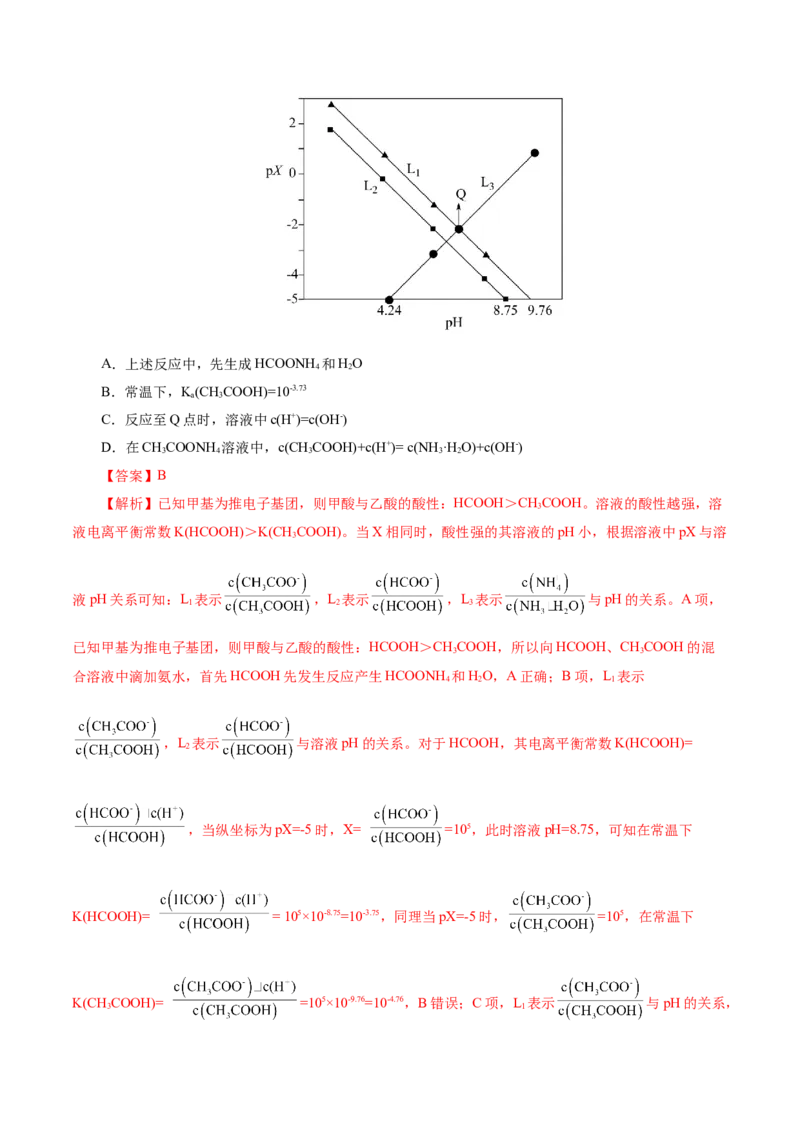
与pH关系如图所示。下列叙述错误的是( )
A.当V=20时,溶液呈酸性
B.NaR的水解常数K =10-11.15
2 h1
C.pH=4时,cHR->cHR>cR2->cH+>cOH-
2
D.T点对应溶液pH约为4.26
【答案】B
【解析】A项,根据电离常数和电离方程式分析,随着pH增大,cHR减小,cHR-先增大,后减小;
2
cR2-增大,结合图像可知,曲线①代表δ(H R)与pH的关系;曲线②代表δ(HR-)与pH的关系;曲线③代表
2
δ(R2-)与pH的关系。结合图中数据可知,K =10-2.85,K =10-5.66。当中和恰好生成NaHR时(V=20),
a1 a2
,HR-的电离程度大于其水解程度,溶液呈酸性,A项正确;B项,根据水解常数公式可知:
,B项错误;C项,析可知pH=4时,cHR->cHR>cR2->cH+>cOH-,C
2
项正确;D项,T点, , , ,D项正确;
故选B。
2.(2025·山西省长治市多校高三联考)常温下,在两个相同的容器中分别加入20mL0.2mol·L-1NaX溶
2
液和10mL0.1mol·L-1NaHX溶液,再分别用 盐酸滴定,利用 计和压力传感器检测,绘制曲线如
图所示。(已知HX溶液达到某浓度后,会放出一定量气体,溶液体积变化可忽略不计)
2下列说法错误的是( )
A.图中曲线①和④表示NaA溶液和盐酸反应
2
B.反应达到滴定终点时,两溶液压力传感器检测的数值相等
C.0.1mol·L-1NaHX溶液中:cNa+>cHX->cOH->cX2-
D.滴定时,c点可用甲基橙、d点可用酚酞作指示剂
【答案】D
【解析】A项,根据X2-水解程度大于HX-,0.2mol·L-1NaX溶液的碱性大于0.1mol·L-1NaHX溶液的碱
2
性,所以曲线①表示NaA溶液和盐酸反应;随着盐酸的逐渐滴加,反应的顺序依次为:X2--+H+-HX-、HX-
2
+H+=H X↑,曲线④表示NaA溶液和盐酸反应产生气体HA的曲线,故A正确;B项,根据已知条件
2 2 2
n(X2-)=n(HX-)=0.004mol,反应达到滴定终点时,产生的HA均为0.004mol,并且反应后溶液的体积也相同,
2
都是60mL,所以压强相等,两溶液压力传感器检测的数值相等,故B正确;C项,由图可知NaHX溶液
pH=8,溶液显碱性,说明HA-的水解程度大于其电离程度,所以离子浓度:cNa+>cHX->cOH->
cX2-,故C正确;D项,根据图分析,滴定时,c点溶液的pH在8.5左右,在酚酞的变色范围内,用酚酞
作指示剂,d点溶液的pH在4左右,在甲基橙的变色范围内,用甲基橙作指示剂,故D错误;故选D。
3.(2025·安徽省合肥一中高三教学质量检测)常温下,向浓度相等的甲酸(HCOOH)和乙酸(CHCOOH)
3
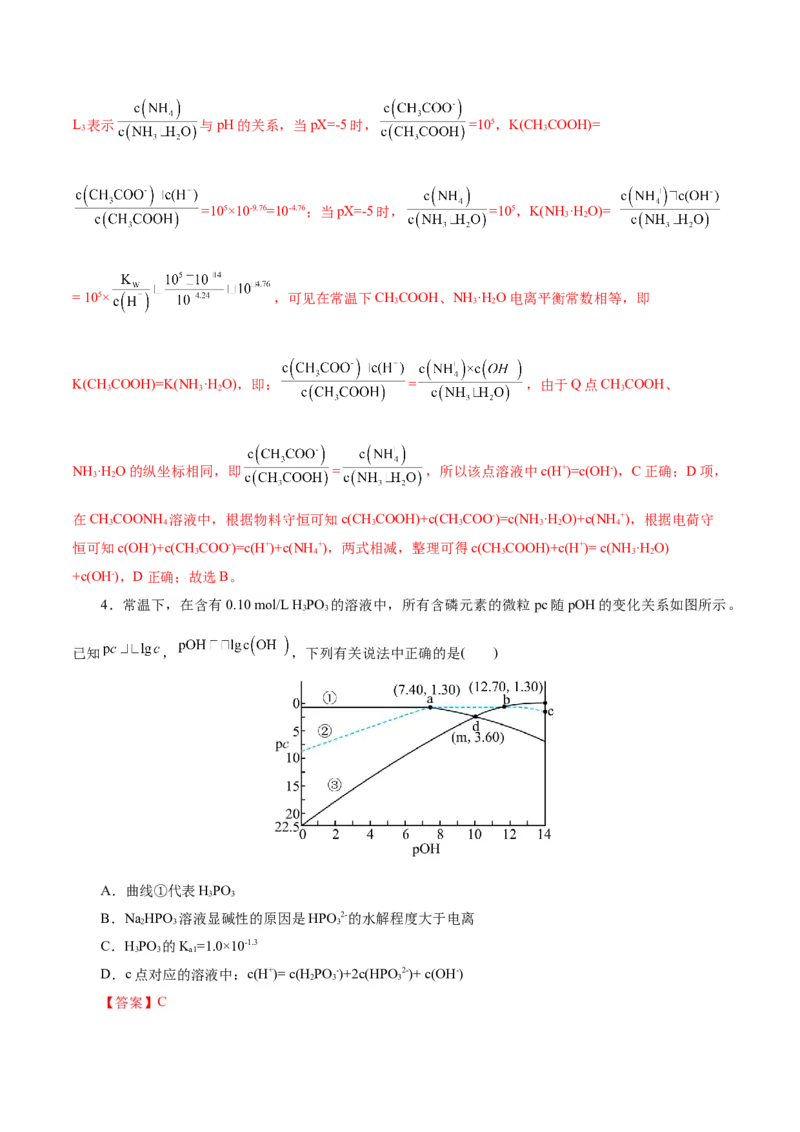
的混合溶液中滴加氨水,溶液中 与
的关系如图所示。已知甲基为推电子基团,下列叙述错误的是( )A.上述反应中,先生成HCOONH 和HO
4 2
B.常温下,K(CHCOOH)=10-3.73
a 3
C.反应至Q点时,溶液中c(H+)=c(OH-)
D.在CHCOONH 溶液中,c(CHCOOH)+c(H+)= c(NH ·H O)+c(OH-)
3 4 3 3 2
【答案】B
【解析】已知甲基为推电子基团,则甲酸与乙酸的酸性:HCOOH>CHCOOH。溶液的酸性越强,溶
3
液电离平衡常数K(HCOOH)>K(CH COOH)。当X相同时,酸性强的其溶液的pH小,根据溶液中pX与溶
3
液pH关系可知:L 表示 ,L 表示 ,L 表示 与pH的关系。A项,
1 2 3
已知甲基为推电子基团,则甲酸与乙酸的酸性:HCOOH>CHCOOH,所以向HCOOH、CHCOOH的混
3 3
合溶液中滴加氨水,首先HCOOH先发生反应产生HCOONH 和HO,A正确;B项,L 表示
4 2 1
,L 表示 与溶液pH的关系。对于HCOOH,其电离平衡常数K(HCOOH)=
2
,当纵坐标为pX=-5时,X= =105,此时溶液pH=8.75,可知在常温下
K(HCOOH)= = 105×10-8.75=10-3.75,同理当pX=-5时, =105,在常温下
K(CH COOH)= =105×10-9.76=10-4.76,B错误;C项,L 表示 与pH的关系,
3 1L 表示 与pH的关系,当pX=-5时, =105,K(CH COOH)=
3 3
=105×10-9.76=10-4.76;当pX=-5时, =105,K(NH·H O)=
3 2
= 105× ,可见在常温下CHCOOH、NH ·H O电离平衡常数相等,即
3 3 2
K(CH COOH)=K(NH ·H O),即: = ,由于Q点CHCOOH、
3 3 2 3
NH ·H O的纵坐标相同,即 = ,所以该点溶液中c(H+)=c(OH-),C正确;D项,
3 2
在CHCOONH 溶液中,根据物料守恒可知c(CHCOOH)+c(CH COO-)=c(NH·H O)+c(NH +),根据电荷守
3 4 3 3 3 2 4
恒可知c(OH-)+c(CH COO-)=c(H+)+c(NH+),两式相减,整理可得c(CHCOOH)+c(H+)= c(NH ·H O)
3 4 3 3 2
+c(OH-),D正确;故选B。
4.常温下,在含有0.10 mol/L H PO 的溶液中,所有含磷元素的微粒pc随pOH的变化关系如图所示。
3 3
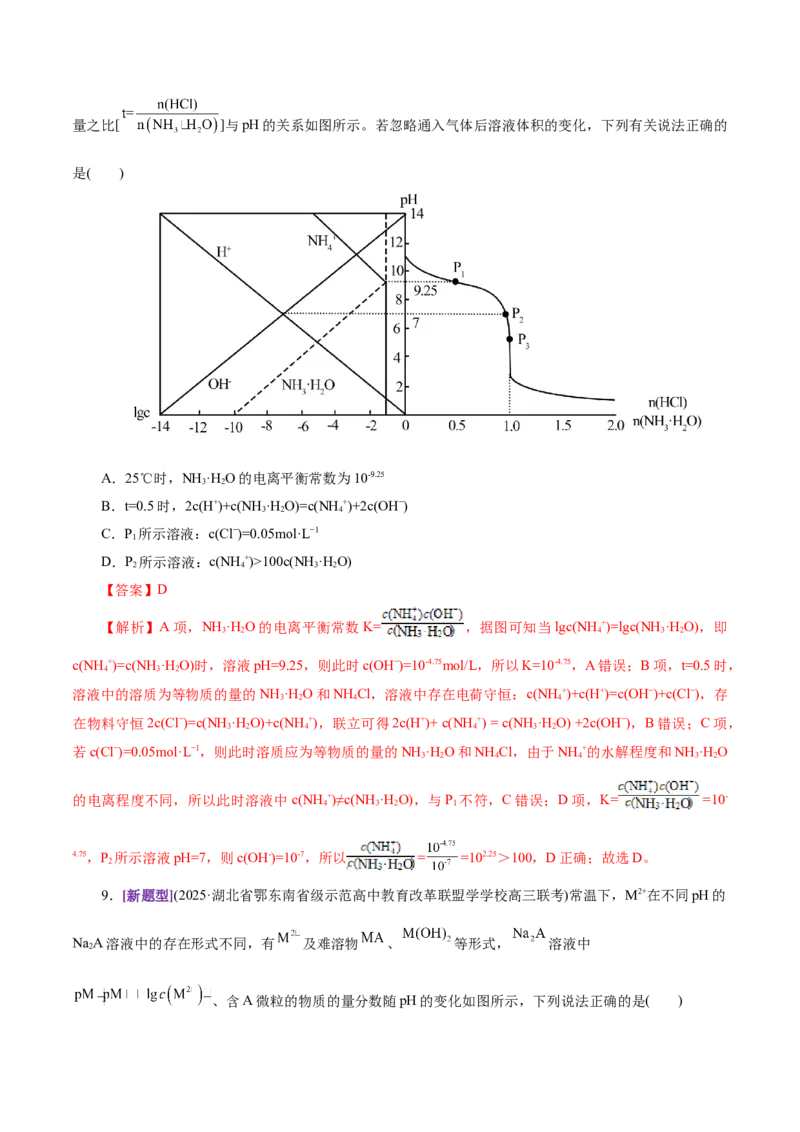
已知 , ,下列有关说法中正确的是( )
A.曲线①代表HPO
3 3
B.NaHPO 溶液显碱性的原因是HPO 2-的水解程度大于电离
2 3 3
C.HPO 的K =1.0×10-1.3
3 3 a1
D.c点对应的溶液中:c(H+)= c(HPO -)+2c(HPO 2-)+ c(OH-)
2 3 3
【答案】C【解析】pOH越小,溶液的碱性越强,图中只有三条曲线说明HPO 是二元弱酸,碱性较强的情况下,
3 3
HPO 2-的浓度最大,其次为HPO -,最后为HPO ,因此曲线①表示HPO 2-,曲线②表示HPO -,曲线③表
3 2 3 3 3 3 2 3
示HPO 。A项,只有三条微粒浓度变化曲线,因此HPO 为二元弱酸,曲线①随着pOH增大即酸性增强,
3 3 3 3
微粒浓度减小,曲线①表示HPO 2-,A错误;B项,NaHPO 是正盐,因此溶液显碱性的原因是HPO 2-的
3 2 3 3
水解,HPO 2-不会电离,B 错误;C 项,曲线②和③的交点 b 处 c(HPO -)=c(H PO ),HPO 的 K =
3 2 3 3 3 3 3 a1
=c(H+)=10-1.3,C正确;D项,HPO 是弱酸,c点pH为0,c(H+)=1mol/L,说明溶液中加入
3 3
了强酸性物质,因此还含有其他阴离子,此电荷守恒式错误,D错误;故选C。
5.常温下,体积和浓度一定的NaA溶液中各微粒浓度的负对数( )随溶液pH的变化关系如图所示。
下列叙述正确的是( )
A.曲线②表示 随溶液pH的变化情况
B.等物质的量浓度NaA和HA混合溶液:c(Na+)>c(A-)>c(OH―) >c(H+)
C.HA的K 的数量级为10-5
a
D.常温下,将M点对应溶液加水稀释, 不变
【答案】C
【解析】pH 越大,A-浓度越大, 越小,相应纵坐标越小;pH 越大,HA 浓度越小,
越大,相应纵坐标越大,故 M 点代表 ,即 c(A-)= c(HA),则
, 。A项, 曲线②上的点纵坐标和横坐标数值相等,随
着pH的增大而增大,表示 随溶液pH的变化情况,A错误;B项,,等物质的量浓度NaA和HA混合溶液中,NaA的水解程度小于HA的电离程度,呈酸性,结合电荷守恒可知:c(A-)>c(Na+)>c(H+)
>c(OH―),B错误;C项,HA的K 的数量级为10-5,C正确;D项, 常温下,将M点对应溶液加水稀释
a
,稀释使氢离子浓度变小、Ka不变,则比值变大,D错误;故选C。
6.已知:CHNH ·H O 为一元弱碱,性质与 NH ·H O 类似。常温下,将 HCl 气体通入 0.1mol/
3 2 2 3 2
LCH NH ·H O水溶液中(忽略溶液体积的变化),混合溶液中pH与微粒浓度的对数值(lgc)的关系如图所示。
3 2 2
下列说法不正确的是( )
A.CHNH ·H O的水溶液中存在:CHNH ·H O CHNH ++OH-
3 2 2 3 2 2 3 3
B.K(CHNH ·H O)的数量级为10-5
a 3 2 2
C.P点,c(Cl-)+c(CH NH +)+c(CH NH ·H O)=0.2mol/L
3 3 3 2 2
D.P点之后,溶液中存在c(Cl-)+c(OH-)=c(CH NH +)+c(H+)
3 3
【答案】C
【解析】已知:CHNH ·H O为一元弱碱,性质与NH ·H O类似,则会发生部分电离, CHNH ·H O
3 2 2 3 2 3 2 2
CHNH ++OH-;随着pH值变大,CHNH +含量变小、CHNH ·H O含量变大,结合图像可知,图
3 3 3 3 3 2 2
中实曲线为混合溶液中pH与CHNH +浓度的对数值(lgc)的关系、虚线为混合溶液中pH与CHNH ·H O浓
3 3 3 2 2
度的对数值(lgc)的关系;两条对角斜线分别为氢离子、氢氧根离子对应曲线,斜率为正的代表氢离子、斜
率为负的代表氢氧根离子。A项,CHNH ·H O的水溶液中存在:CHNH ·H O⇌ CHNH ++OH-,A正确;
3 2 2 3 2 2 3 3
B项,由点Q可知,pH=9.5,pOH=4.5,则 ,故其数量级为
10-5,B正确;C项,P点无法计算氯离子的浓度,故不能计算c(Cl-)+c(CH NH +)+c(CH NH ·H O)的值,C
3 3 3 2 2
错误; D项,P点之后根据电荷守恒可知,溶液中存在 c(Cl-)+c(OH-)=c(CH NH +)+c(H+),D正确;故选
3 3
C。
7.常温下,天然水体中HCO 与空气中的CO 保持平衡,水体中lgc(X)[X为HCO 、HCO -、CO2-或
2 3 2 2 3 3 3
Ca2+]与pH的关系如图所示,已知Ksp(CaCO )=2.8×10-9。下列说法不正确的是( )
3A.I代表HCO -与pH的关系曲线
3
B.pH=10.3时,c(Ca2+)=2.8×10-7.9mol·L-1
C.2pH(b)=pH(a)+pH(c)
D.HCO 的二级电离常数为10-6.3
2 3
【答案】D
【解析】A项,pH增大则溶液碱性增大,从而会促进HCO -的电离。CO2-比HCO -更容易结合H+,所
3 3 3
以pH小的时候,HCO -的浓度更大。根据以上分析,曲线Ⅰ代表HCO -与pH的关系曲线;曲线Ⅱ代表
3 3
CO2-与pH的关系曲线;曲线Ⅲ代表Ca2+与pH的关系曲线,A项正确;B项,pH=10.3时,c(CO2-)=10-
3 3
1.1,则 c(Ca2+)= ,B 项正确;C 项,HCO 的一级电离常数为
2 3
,在a点有c(HCO -)=c(H CO)=10-5,c(H+)=10-6.3,所以K =10-6.3;HCO 的二级电离
3 2 3 1 2 3
常 数 , 在 c 点 有 c(HCO -)=c(CO 2-)=10-1.1 , c(H+)=10-10.3 , 所 以 K =10-10.3 。
3 3 2
, 在 b 点 有 c(CO2-)=c(H CO) , c(H+)= 。 pH(a)=6.3 , pH(c)=10.3 ,
3 2 3
pH(b)=8.3,所以2pH(b)=pH(a)+pH(c),C项正确;D项,HCO 的二级电离常数 ,在c
2 3
点有c(HCO -)=c(CO 2-)=10-1.1,c(H+)=10-10.3,所以K =10-10.3,D项错误。故选D。
3 3 2
8.25℃时,用HCl气体调节0.1mol·L−1氨水的pH,体系中粒子浓度的对数值(lgc)、反应物的物质的量之比[ ]与pH的关系如图所示。若忽略通入气体后溶液体积的变化,下列有关说法正确的
是( )
A.25℃时,NH ·H O的电离平衡常数为10-9.25
3 2
B.t=0.5时,2c(H+)+c(NH·H O)=c(NH +)+2c(OH−)
3 2 4
C.P 所示溶液:c(Cl−)=0.05mol·L−1
1
D.P 所示溶液:c(NH +)>100c(NH·H O)
2 4 3 2
【答案】D
【解析】A项,NH ·H O的电离平衡常数K= ,据图可知当lgc(NH+)=lgc(NH ·H O),即
3 2 4 3 2
c(NH +)=c(NH·H O)时,溶液pH=9.25,则此时c(OH−)=10-4.75mol/L,所以K=10-4.75,A错误;B项,t=0.5时,
4 3 2
溶液中的溶质为等物质的量的NH ·H O和NH Cl,溶液中存在电荷守恒:c(NH +)+c(H+)=c(OH−)+c(Cl−),存
3 2 4 4
在物料守恒2c(Cl−)=c(NH·H O)+c(NH +),联立可得2c(H+)+ c(NH +) = c(NH ·H O) +2c(OH−),B错误;C项,
3 2 4 4 3 2
若c(Cl−)=0.05mol·L−1,则此时溶质应为等物质的量的NH ·H O和NH Cl,由于NH +的水解程度和NH ·H O
3 2 4 4 3 2
的电离程度不同,所以此时溶液中c(NH +)≠c(NH ·H O),与P 不符,C错误;D项,K= =10-
4 3 2 1
4.75,P 所示溶液pH=7,则c(OH-)=10-7,所以 = =102.25>100,D正确;故选D。
2
9.[新题型](2025·湖北省鄂东南省级示范高中教育改革联盟学学校高三联考)常温下,M2+在不同pH的
NaA溶液中的存在形式不同,有 及难溶物 、 等形式, 溶液中
2
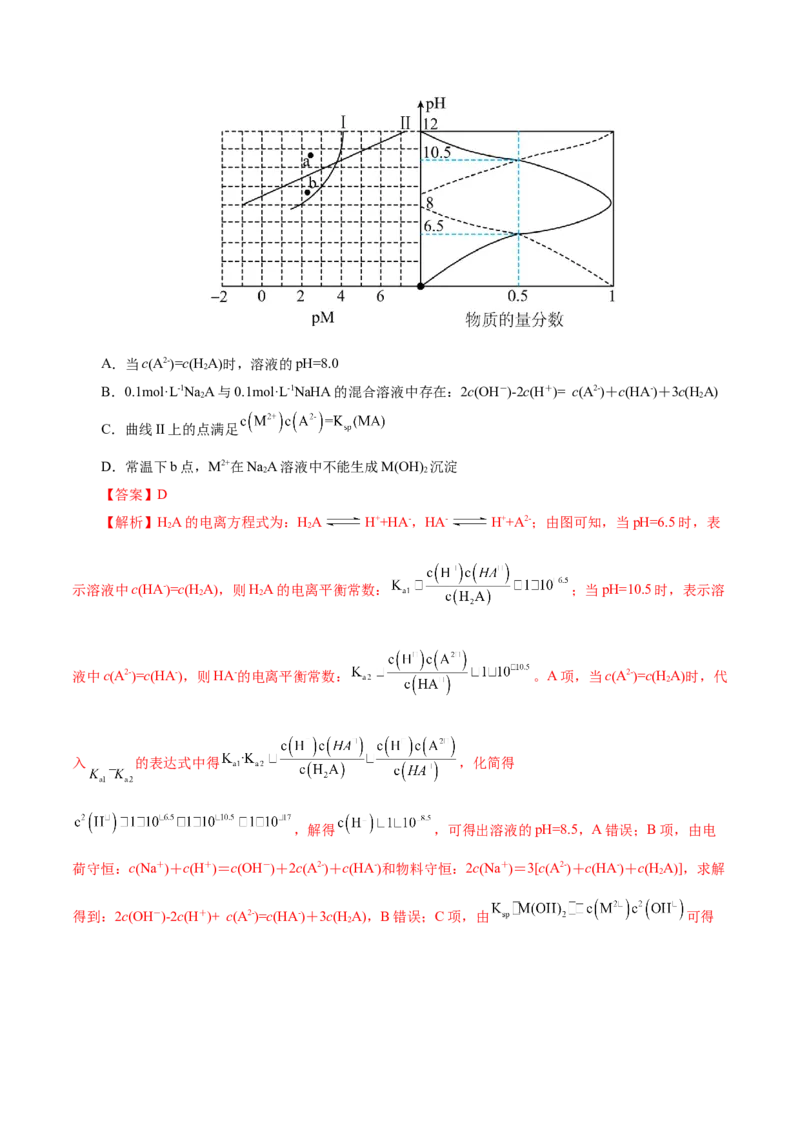
、含A微粒的物质的量分数随pH的变化如图所示,下列说法正确的是( )A.当cA2-=cHA时,溶液的pH=8.0
2
B.0.1mol·L-1NaA与0.1mol·L-1NaHA的混合溶液中存在:2cOH--2cH+= cA2-+cHA-+3cHA
2 2
C.曲线II上的点满足
D.常温下b点,M2+在NaA溶液中不能生成M(OH) 沉淀
2 2
【答案】D
【解析】HA的电离方程式为:HA H++HA-,HA- H++A2-;由图可知,当pH=6.5时,表
2 2
示溶液中cHA-=cHA,则HA的电离平衡常数: ;当pH=10.5时,表示溶
2 2
液中cA2-=cHA-,则HA-的电离平衡常数: 。A项,当cA2-=cHA时,代
2
入 的表达式中得 ,化简得
,解得 ,可得出溶液的pH=8.5,A错误;B项,由电
荷守恒:cNa++cH+=cOH-+2cA2-+cHA-和物料守恒:2cNa+=3[cA2-+cHA-+cHA],求解
2
得到:2cOH--2cH++ cA2-=cHA-+3cHA,B错误;C项,由 可得
2,则
,图像II是直线,故曲线II表示M(OH) 的溶解平衡曲线,
2
曲线I表示MA的溶解平衡曲线,C错误;D项,曲线II上的点满足 ,而
b点在曲线II的下方,c(OH―)比平衡时小,故M2+在NaA溶液中不能生成M(OH) 沉淀,D正确;故选
2 2
D。
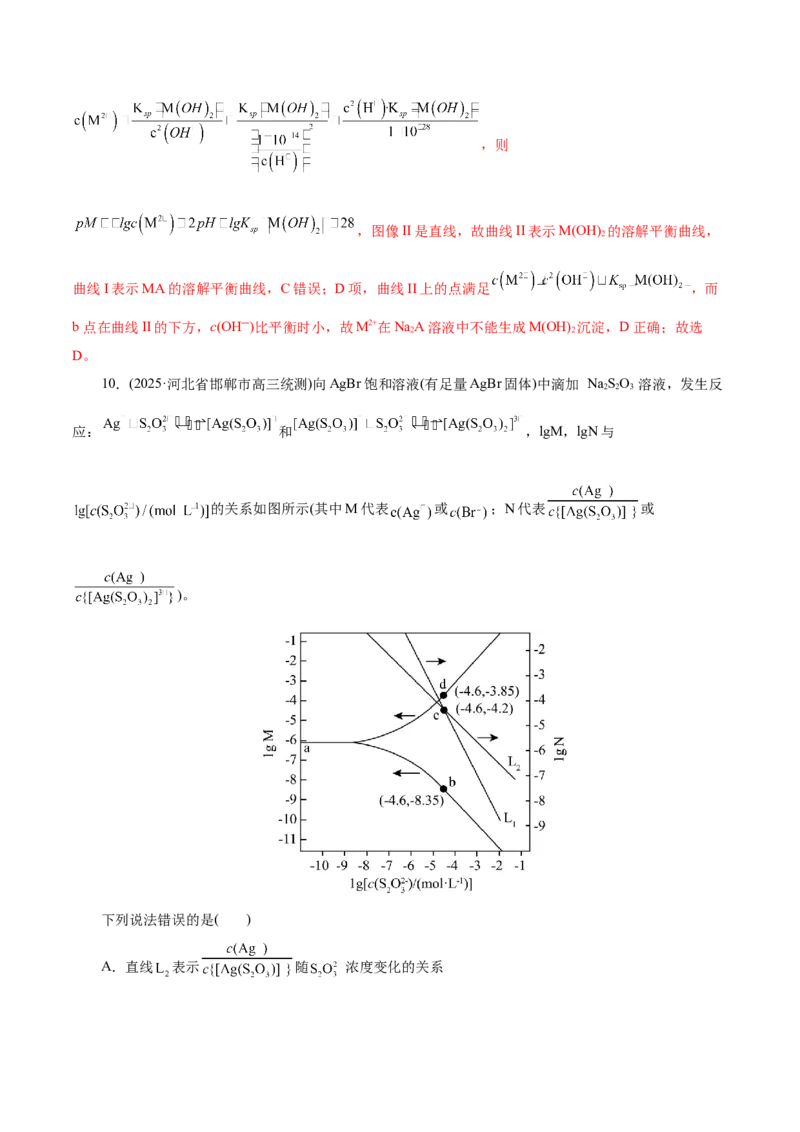
10.(2025·河北省邯郸市高三统测)向AgBr饱和溶液(有足量AgBr固体)中滴加 NaSO 溶液,发生反
2 2 3
应: 和 ,lgM,lgN与
的关系如图所示(其中M代表 或 ;N代表 或
)。
下列说法错误的是( )
A.直线 表示 随 浓度变化的关系B.AgBr的溶度积常数
C.反应 的平衡常数K的值为
D. 时,溶液中
【答案】C
【解析】溴化银的饱和溶液中溴离子浓度和银离子浓度相等,向饱和溶液中滴加硫代硫酸钠溶液时,
溶液中银离子浓度减小,溴离子浓度增大,则b点所在曲线表示银离子浓度与硫代硫酸根离子浓度变化的
关系、d点所在曲线表示溴离子与硫代硫酸根离子浓度变化的关系;溴化银与硫代硫酸钠溶液开始反应时,
溴化银主要转化为 ,溶液中 小于 ,则直线L 表示
1
随SO2-浓度变化的关系,直线L 表示 随SO2-浓度变化的关系;由图可知,
2 3 2 2 3
溶液中硫代硫酸根离子浓度为 时,溶液中溴离子和银离子浓度分别为 、
,则溴化银的溶度积常数 。】A项,直线L 表示
2
随SO2-浓度变化的关系,A正确;B项,AgBr的溶度积常数 ,B正确;C项,
2 3
由图可知,溶液中硫代硫酸根离子浓度为 时,溶液中溴离子和银离子浓度分别为均为
、 , 、 均为 ,即
,则反应的平衡常数,C错误;D项,由图可知,硫代硫
酸根离子浓度为 时,溶液中溴离子浓度最大, 的值大于 的值,
则溶液中 的浓度大于 的浓度,所以溶液中离子浓度大小顺序为
,D正确;故选C。
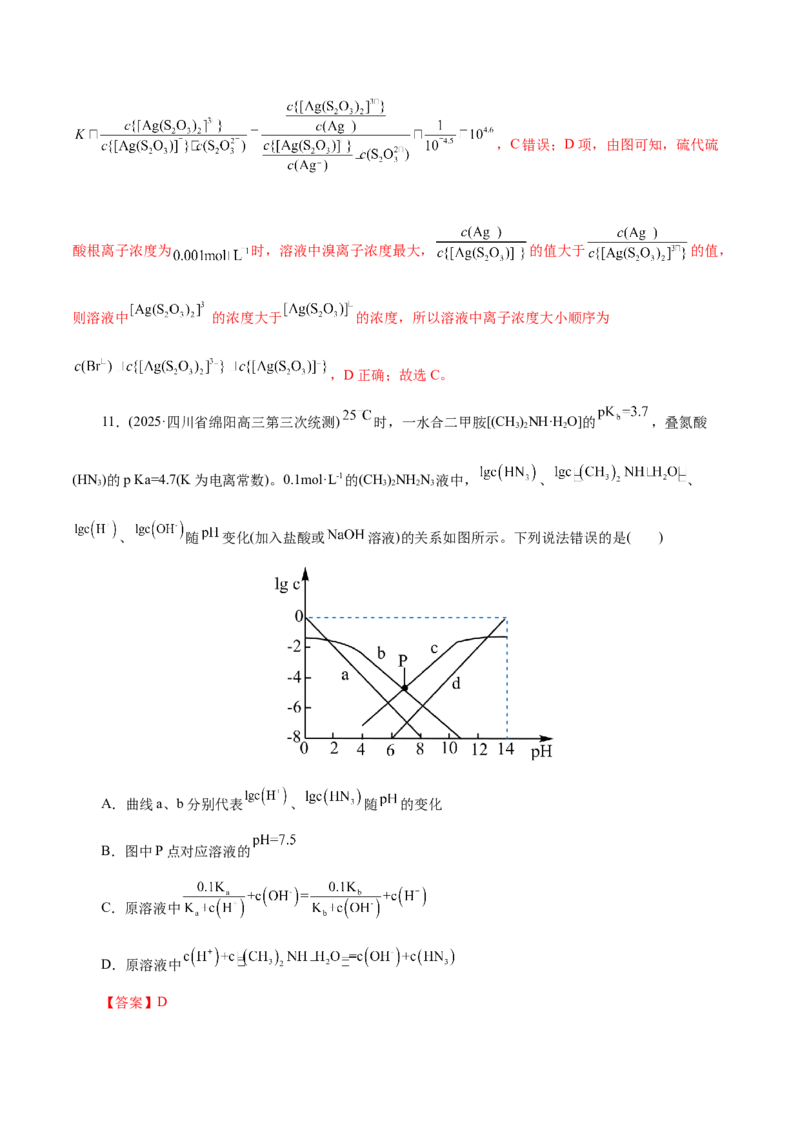
11.(2025·四川省绵阳高三第三次统测) 时,一水合二甲胺[(CH )NH·H O]的 ,叠氮酸
3 2 2
(HN )的p Ka=4.7(K为电离常数)。0.1mol·L-1的(CH)NH N 液中, 、 、
3 3 2 2 3
、 随 变化(加入盐酸或 溶液)的关系如图所示。下列说法错误的是( )
A.曲线a、b分别代表 、 随 的变化
B.图中P点对应溶液的
C.原溶液中
D.原溶液中
【答案】D【解析】CH)NH N 溶液中加酸,pH减小, 与 增大,CH)NH N 溶液中加碱,pH
3 2 2 3 3 2 2 3
增大, 与 增大, 、 随 变化应呈线性关系,因此曲线d
代表 随pH的变化,曲线c代表 随pH的变化,曲线b代表 随pH
的变化,曲线a代表 随pH的变化。A项,曲线a、b分别代表 、 随 的变化,
A正确;B项,P点时, , ,则
,即 ,可求出pH=7.5,B正确;C项,由物料守恒可知,
,根据电离常数表达式, ,
;同理, ,根据电荷守恒式可知,
,故 ,C正确;D项,依
据物料守恒, =0.1mol/L, 和电荷守恒
可得: ,D错误;
故选D。
12.(2025·河北省沧州市泊头一中高三质检)乙二胺四乙酸用HY表示,可接受质子形成HY2+。
4 6
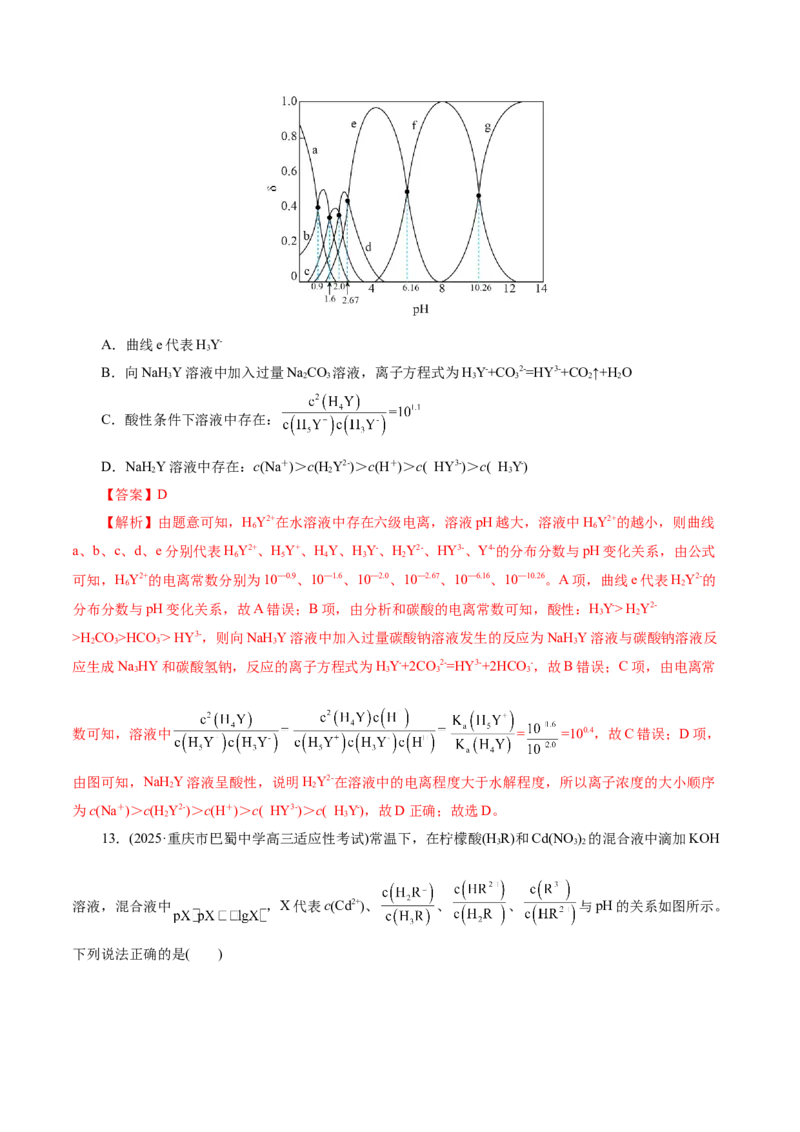
HY2+在水溶液中存在六级电离,含 微粒的分布分数(δ)与 变化关系如图。已知:HCO 的K =10-6.37,
6 2 3 a1
K =10-10.25。下列说法正确的是( )
a2A.曲线e代表HY-
3
B.向NaHY溶液中加入过量NaCO 溶液,离子方程式为HY-+CO 2-=HY3-+CO ↑+H O
3 2 3 3 3 2 2
C.酸性条件下溶液中存在:
D.NaHY溶液中存在:cNa+>cHY2->cH+>c HY3->c HY-
2 2 3
【答案】D
【解析】由题意可知,HY2+在水溶液中存在六级电离,溶液pH越大,溶液中HY2+的越小,则曲线
6 6
a、b、c、d、e分别代表HY2+、HY+、HY、HY-、HY2-、HY3-、Y4-的分布分数与pH变化关系,由公式
6 5 4 3 2
可知,HY2+的电离常数分别为10—0.9、10—1.6、10—2.0、10—2.67、10—6.16、10—10.26。A项,曲线e代表HY2-的
6 2
分布分数与pH变化关系,故A错误;B项,由分析和碳酸的电离常数可知,酸性:HY-> H Y2-
3 2
>H CO>HCO-> HY3-,则向NaHY溶液中加入过量碳酸钠溶液发生的反应为NaHY溶液与碳酸钠溶液反
2 3 3 3 3
应生成NaHY和碳酸氢钠,反应的离子方程式为HY-+2CO 2-=HY3-+2HCO-,故B错误;C项,由电离常
3 3 3 3
数可知,溶液中 = =100.4,故C错误;D项,
由图可知,NaHY溶液呈酸性,说明HY2-在溶液中的电离程度大于水解程度,所以离子浓度的大小顺序
2 2
为cNa+>cHY2->cH+>c HY3->c HY-,故D正确;故选D。
2 3
13.(2025·重庆市巴蜀中学高三适应性考试)常温下,在柠檬酸(H R)和Cd(NO ) 的混合液中滴加KOH
3 3 2
溶液,混合液中 ,X代表cCd2+、 、 、 与pH的关系如图所示。
下列说法正确的是( )A. 直线表示 与 关系
B.0.1mol·L-1KH R溶液呈碱性
2
C.b点的溶液中:cNa++cH+=cHR+cHR-+cHR2-+cR3-+cOH-
3 2
D.d点的溶液中无Cd(OH) 沉淀
2
【答案】D
【解析】Cd(NO ) 的溶液中滴加KOH溶液生成Cd(OH) 沉淀,pH越大,cCd2+越小,其对应的
3 2 2
越大,故L 是代表cCd2+与pH的关系;柠檬酸(H R)是三元弱酸,与碱反应逐渐转为
4 3
HR-、HR2-、R3-,酸的三步电离平衡常数 ,故X代表 、 、 ,分
2
别乘以c(H+),可以转化为平衡常数的表达式,根据大小可知,由题意L、L、L 分别代表 、
1 2 3
、 。A项,由题意可知,L 和L 分别代表 、 、 和cCd2+,A
1 4
错误;B项,由题意L 分别代表 、 、 。将b(4,-0.9)带入酸的第一步表达式
1
K = =100.9×10-4=10-3.1,同理,将(2.7,2)代入酸的第二步电离表达式得到K =10-4.7,将
a1 a2
c(8,-1.6)代入酸的第三步表达式得到K =10-6.4,则HR的K 依次为10-3.1、10-4.7、10-6.4,KH R是酸式盐,
a3 3 a 2HR-能水解使溶液呈碱性,水解平衡常数为K = ,也能电离使溶液呈酸性,电离常数
2 b3
为K =10-4.7,通过比较,电离程度大于水解程度,溶液呈酸性,B错误;C项,b点含KNO、KH R溶液,
a2 3 2
若为电荷守恒:cNa++cH+=cNO -+cHR-+2cHR2-+3cR3-+cOH-,柠檬酸(H R)和Cd(NO ) 的
3 2 3 3 2
混合液中,溶质起始浓度不知,不能简单做判断,同时也不符合元素守恒式,C错误;D项,a点可计算
K ,d点在线下,通过计算可知:d点Q<K ,所以没有Cd(OH) 沉淀,D正确;故选D。
SP sp 2