文档内容
第 02 讲 离子反应、离子方程式
目录
01 模拟基础练
【题型一】电解质的电离
【题型二】离子反应和离子方程式
02 重难创新练
03 真题实战练
题型一 电解质的电离
1.(2024·浙江·三模)下列物质溶于水能导电,且属于非电解质的是
A.PO B.Cl C.CHCOOH D.AlCl
2 5 2 3 3
【答案】A
【解析】A.PO 和水反应生成磷酸,磷酸电离出阴阳离子而使PO 的水溶液导电,但电离出阴阳离子的
2 5 2 5
物质是磷酸而不是PO,所以PO 是非电解质,故A符合题意;B.氯气是单质,既不是电解质也不是非
2 5 2 5
电解质,故B不合题意;C.醋酸在水溶液里能电离出阴阳离子,所以醋酸水溶液能导电,但醋酸是电解
质,故C不合题意;D.AlCl 在水溶液里能电离出阴阳离子,所以AlCl 水溶液能导电,但AlCl 是电解
3 3 3
质,故D不合题意;故选A.
2.(2024·湖南衡阳·三模)废水中的 可用双氧水处理,反应原理为
,下列说法错误的是
A. 的球棍模型为
B. 的结构式为H—O—O—H
C. 在水中的电离方程式为
D. 的电子式为
【答案】A
【解析】A.水是V形分子,但中心氧原子半径大于H原子,故A错误;B. 的结构式为H—O—O—H,故B正确;C. 在水中部分电离,电离方程式为 ,故C正确;D.氨气的
电子式为 ,故D正确;故选A。
3.(2024·陕西西安·一模)将 溶于水配成 的溶液,溶解过程如图所示,下列说法错误的是
A. 离子为
B.溶液中含有 N 个
A
C.水合b离子中水分子的取向不科学
D.某温度测定该 溶液 小于7与盐类的水解无关
【答案】B
【解析】A.氯离子的离子半径大于钠离子,则离子半径大的黑球代表氯离子,故A正确;B.缺溶液的
体积,无法计算1mol/L氯化钠溶液中氯化钠的物质的量和钠离子个数,故B错误;C.钠离子带正电荷,
应与水分子中带负电荷的氧原子相吸引,所以水合b离子中水分子的取向不科学,故C正确;D.氯化钠
是强酸强碱盐,在溶液中不水解,溶液呈中性,则某温度测定该 氯化钠溶液 pH小于7与盐类的水解无
关,故D正确;故选B。
4.(2024·浙江金华·三模)下列物质中不属于电解质的是
A.HI B. C.KOH D.
【答案】D
【分析】电解质的定义是:溶于水或熔融时可导电的化合物;非电解质的定义是:溶于水以及熔融状态均
不导电的化合物。
【解析】A.HI是酸,属于电解质,A不符合题意;B. 是盐,属于电解质,B不符合题意;
C.KOH是碱,属于电解质,C不符合题意;D. 属于非电解质,D符合题意;故选D。
题型二 离子反应和离子方程式
5.(2024·重庆·模拟预测)下列过程的化学反应,相应的离子方程式书写错误的是
A.用KI检验食盐中是否加碘:
B.利用废旧铅蓄电池氧化 :
C. 溶液吸收CO生成 :D.碱性条件下,Zn空气电池放电:
【答案】A
【解析】A.用KI检验食盐中是否加碘,反应生成碘单质和水,正确的离子方程式为:
,故A错误;B.铅蓄电池中的PbO 在酸性条件下氧化 ,自身被还原
2
Pb2+,离子方程式: ,故B正确;C. 溶液
吸收CO生成 ,对比化学式,可知缺少NH3,方程式:
,故C正确;D.碱性条件下,Zn空气电池放电,氧气作负
极,方程式: ,故D正确;答案选A。
6.(2024·湖北武汉·模拟预测)对于下列实验,描述其反应的离子方程式错误的是
A.用惰性电极电解硫酸铜溶液:
B.向苯酚钠溶液中滴加稀盐酸:
C.将 溶液滴入 溶液中:
D.向氢氧化钙溶液中滴加少量碳酸氢钙溶液:
【答案】B
【解析】A.用惰性电极电解硫酸铜溶液,阳极发生的反应为水失电子生成氧气,阴极发生的反应为铜离
子得电子生成铜单质,因此电解反应的总方程式为: ,故A正确;B.
向苯酚钠溶液中滴加稀盐酸的反应为: ,故B错误;C.二价铁的检验是加入
溶液后产生蓝色沉淀,反应为: ,故C正确;
D.碳酸氢钙溶液加入是少量,因此以碳酸氢钙配平可得,反应为:
,故D正确;故答案为:B。
7.(2024·湖南长沙·三模)下列离子方程式书写错误的是
A.向硫化钠溶液中通入足量二氧化硫:
B.已知酸性: ,将少量 通入 溶液中:
C.用盐酸处理铜器表面的铜锈:D.利用 与 制备 沉淀:
【答案】C
【解析】A.向硫化钠溶液中通入足量二氧化硫,溶液变浑浊且生成亚硫酸氢钠,离子方程式为
,故A正确;B.由于 的 大于 的 小于 的
,因此将少量 通入 溶液中生成 和 ,离子方程式为
,故B正确;C.铜锈的主要成分是碱式碳酸铜,不是氧化铜,正确的
离子方程式 ,故C错误;D.向 溶液中加入 溶
液得到 沉淀,离子方程式为 ,故D正确;故选C。
8.(2024·内蒙古·三模)下列对应离子方程式或电极反应式书写正确的是
A. 与冷石灰乳反应:
B.锌锰碱性电池放电时正极反应式:
C.向NaOH溶液中滴加少量 溶液:
D.足量的氯气和 溶液反应:
【答案】B
【解析】A.石灰乳作反应物时不能用 , 与冷石灰乳反应: ,
A错误;B.锌锰碱性电池放电时正极得到电子,电极反应式: ,B正
确;C.向NaOH溶液中滴加少量 溶液: ,C错
误;D.足量的氯气和 溶液反应: ,D错误;故选B。
9.(2024·上海浦东新·一模)氧化铁黄(FeOOH)纯度可以通过产品的耗酸量确定,如下图所示。
已知:Fe3++3C O =Fe(C O) (配合离子),Fe(C O) 不与稀碱液反应。
2 2 4 2 4
(1)在溶液c中滴加NaOH标准溶液时,发生反应的离子方程式为 ;
(2)若实验时加入了nmol的HSO ,消耗nmolNaOH,设氧化铁黄的式量为A,则氧化铁黄样品纯度为
1 2 4 2
;(用含w、n、n、A的代数式表示)
1 2
(3)测定时,若滴入NaC O 不足量,会使实验结果 (选填“偏大”、“偏小”或“无影响”)。
2 2 4
【答案】(1)H++OH-=H O(H C O+2OH-=C O +2H O亦可)
2 2 2 4 2 2(2)
(3)偏小
【分析】氧化铁黄(FeOOH)加入过量HSO 标准溶液加热溶解,得到溶液b中含有Fe3+,Fe3+和NaC O 溶
2 4 2 2 4
液发生反应:Fe3++3C O =Fe(C O) (配合离子),向溶液c中加入NaOH标准溶液进行滴定,测定过量
2 2 4
HSO 的物质的量,从而测定氧化铁黄样品纯度。
2 4
【解析】(1)在溶液c中含有过量的HSO ,加入NaC O 溶液后可能转化为HC O,在溶液c中滴加
2 4 2 2 4 2 2 4
NaOH标准溶液时,发生反应的离子方程式为H++OH-=H O(H C O+2OH-=C O +2H O亦可)。
2 2 2 4 2 2
(2)若实验时加入了nmol的HSO ,消耗nmolNaOH,由方程式:HSO +2NaOH=2HO+ Na SO 可知,
1 2 4 2 2 4 2 2 4
剩余的n(H SO )=(n -0.5n ),由关系式2Fe3+~3H SO 可知n(FeOOH)=n(Fe3+)= mol,则氧化铁黄
2 4 1 2 2 4
样品纯度为 。
(3)测定时,若滴入NaC O 不足量,Fe3+不能完全转化为Fe(C O) ,Fe3+也会消耗NaOH,则消耗
2 2 4 2 4
NaOH标准溶液的物质的量偏大,则消耗HSO 的物质的量偏小,实验结果偏小。
2 4
10.(2024·重庆·模拟预测)下列说法不正确的是
A.点燃的Cl 可在H 中燃烧生成HCl
2 2
B.工业上电解熔融Al O 冶炼金属铝
2 3
C.钠燃烧时火焰呈黄色与电子的跃迁有关
D.石墨、铜丝能导电,与电解质溶液导电原因不同
【答案】A
【解析】A. 氢气是可燃物,点燃的H 可在Cl 中燃烧生成HCl,故A错误;B. Al O 在熔融状态下能
2 2 2 3
导电,工业上电解熔融Al O 冶炼金属铝,故B正确;C. 钠燃烧时火焰呈黄色与电子的跃迁有关,钠燃
2 3
烧时基态电子吸收能量跃迁到激发态,而电子从能量较高的激发态跃迁到能量较低的激发态或基态时,会
释放能量,产生黄色,故与电子的跃迁有关、与原子光谱有关,故C正确;D. 石墨、铜丝能导电,与电
解质溶液导电原因不同,前者是因为有自由电子,后者有自由移动的阴、阳离子,故D正确;故选A。
11.(2024·广东广州·一模)苯胺( )是一种有机弱碱,可与盐酸反应生成盐酸盐( )。下
列叙述正确的是
A. 中碳原子的杂化轨道类型为
B. 水溶液加水稀释, 降低
C. 水溶液中:D. 在水中的电离方程式为:
【答案】D
【解析】A.苯环内碳原子都采用sp2杂化,A错误;B.盐酸盐( )属于强酸弱碱盐,水解显酸
性,加水稀释,水解程度增大,但由于溶液被稀释,H+浓度减小, 增大,B错误;C.
水溶液中存在电荷守恒: ,C错误;D.盐酸盐
( )在水中完全电离,电离方程式为: ,D正确;故选D。
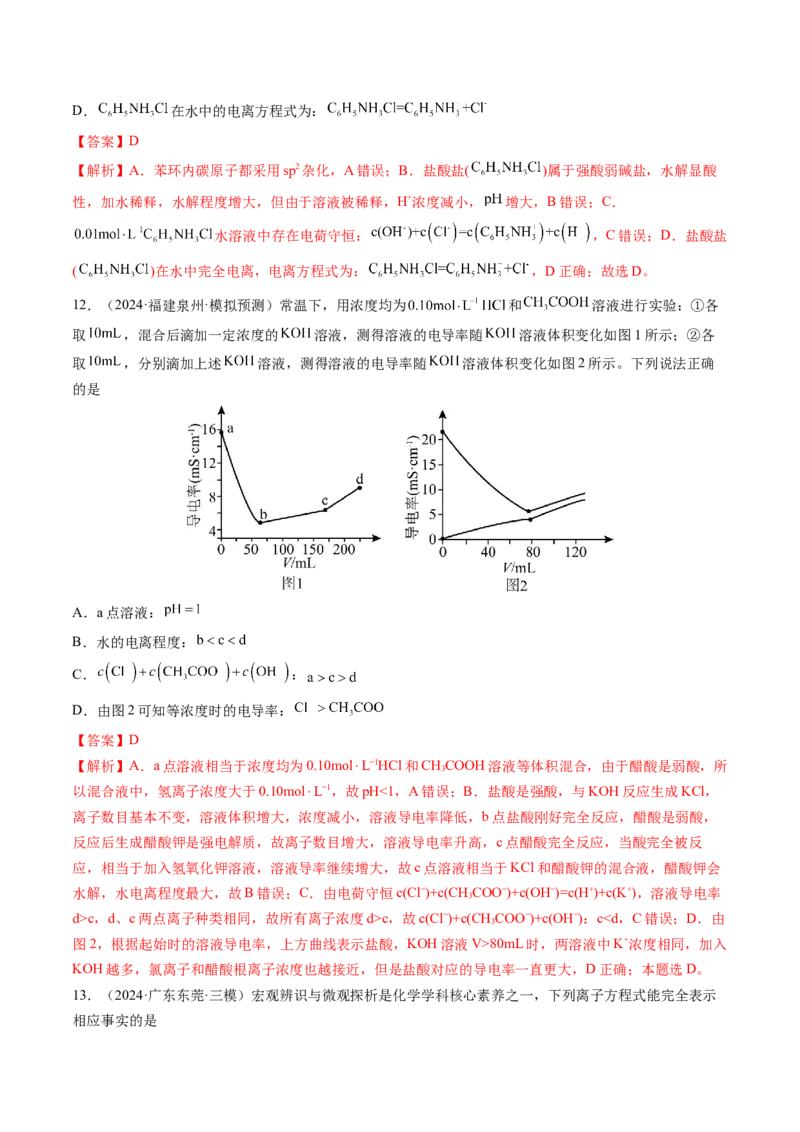
12.(2024·福建泉州·模拟预测)常温下,用浓度均为 和 溶液进行实验:①各
取 ,混合后滴加一定浓度的 溶液,测得溶液的电导率随 溶液体积变化如图1所示;②各
取 ,分别滴加上述 溶液,测得溶液的电导率随 溶液体积变化如图2所示。下列说法正确
的是
A.a点溶液:
B.水的电离程度:
C. :
D.由图2可知等浓度时的电导率:
【答案】D
【解析】A.a点溶液相当于浓度均为0.10mol⋅L−1HCl和CHCOOH溶液等体积混合,由于醋酸是弱酸,所
3
以混合液中,氢离子浓度大于0.10mol⋅L−1,故pH<1,A错误;B.盐酸是强酸,与KOH反应生成KCl,
离子数目基本不变,溶液体积增大,浓度减小,溶液导电率降低,b点盐酸刚好完全反应,醋酸是弱酸,
反应后生成醋酸钾是强电解质,故离子数目增大,溶液导电率升高,c点醋酸完全反应,当酸完全被反
应,相当于加入氢氧化钾溶液,溶液导率继续增大,故c点溶液相当于KCl和醋酸钾的混合液,醋酸钾会
水解,水电离程度最大,故B错误;C.由电荷守恒c(Cl−)+c(CH COO−)+c(OH−)=c(H+)+c(K+),溶液导电率
3
d>c,d、c两点离子种类相同,故所有离子浓度d>c,故c(Cl−)+c(CH COO−)+c(OH−):c80mL时,两溶液中K+浓度相同,加入
KOH越多,氯离子和醋酸根离子浓度也越接近,但是盐酸对应的导电率一直更大,D正确;本题选D。
13.(2024·广东东莞·三模)宏观辨识与微观探析是化学学科核心素养之一,下列离子方程式能完全表示
相应事实的是A.向 溶液中滴加过量的氨水:
B.将还原性铁粉加入过量的稀硝酸中:
C.向 溶液中加入 溶液:
D.模拟侯氏制碱法制备 晶体:
【答案】D
【解析】A.向硫酸铜溶液中滴加过量氨水会生成四氨合铜离子,方程式为:Cu2++4NH •H O=
3 2
[Cu(NH )]2++4H O,故A错误;B.铁粉加入过量稀硝酸中,生成硝酸铁和一氧化氮、水,离子方程式:
3 4 2
Fe+4H++ ═Fe3++NO↑+2HO,故B错误;C.向 溶液中加入 溶液生成氢氧化铝沉淀和
2
碳酸钠,离子方程式为: ,故C错误;D.模拟侯氏制碱法制备
晶体,是将CO、NH 通入到饱和食盐水中生成 晶体,离子方程式为:
2 3
,故D正确。答案选D。
14.(2024·江西·模拟预测)宏观辨识与微观探析是化学学科核心素养之一,下列反应方程式书写错误的
是
A.久置于空气中的 溶液变质:
B.用醋酸和碘化钾淀粉溶液检验加碘盐中的 :
C.向 溶液中加入等物质的量的 溶液:
D.用饱和碳酸钠溶液处理锅炉水垢 :
【答案】B
【解析】A.久置于空气中的 溶液被空气中的氧气氧化变质为硫酸钠,离子方程式为:
,A正确;B.用醋酸和碘化钾淀粉溶液检验加碘盐中的 , 和I-反
应生成I,醋酸是弱酸,在离子方程式中不能拆,根据得失电子守恒和电荷守恒配平离子方程式为:
2
,B错误;C.向 溶液中加入等物质的量的
溶液生成氢氧化铝沉淀和硫酸钡沉淀,离子方程式为:
,C正确;D.用饱和碳酸钠溶液处理锅炉水垢 ,硫酸钙可以转化为溶解
度更小的碳酸钙,离子方程式为: ,D正确;故选B。
15.(2024·陕西安康·模拟预测)下列离子方程式正确的是
A.向稀硫酸中加入熟石灰:
B.向含 的废水中加入C.向 溶液中滴加少量 溶液:
D. 溶于稀硝酸:
【答案】D
【解析】A.熟石灰的成分是 ,与稀硫酸反应的离子方程式为
,A错误;B. 难溶于水,反应的离子方程式为
,B错误;C. 少量时, 先与 反应生成氢氧化铝沉淀,离子方程
式为 ,故C错误;D.稀硝酸将二价铁氧化为三价铁,自身被还原为 ,反应
的离子方程式为 ,D项正确;选D。
16.(2024·河北唐山·模拟预测)下列相关离子方程式表示错误的是
A.向稀硫酸溶液中加入 固体出现黄色沉淀:
B.向氢氧化铁胶体中加入HI溶液,首先出现红褐色沉淀,后沉淀消失,溶液变为黄色:
C.向酸性 溶液中通入 后溶液由紫色变为无色:
D.向HI溶液中加入 后溶液变为棕黄色:
【答案】B
【解析】A.NaSO 与稀硫酸反应生成NaSO 、S、SO 和HO,反应的离子方程式为
2 2 3 2 4 2 2
+2H+=S↓+SO ↑+H O,A项正确;B.向Fe(OH) 胶体中加入HI溶液,首先出现红褐色沉淀是Fe(OH) 胶体
2 2 3 3
发生了聚沉,后沉淀消失,溶液变为黄色发生反应的离子方程式为Fe(OH) +3H+=Fe3++3H O,最后黄色加
3 2
深,发生反应的离子方程式为2Fe3++2I-=2Fe2++I ,B项错误;C.SO 具有还原性、被氧化成 ,
2 2
被还原成Mn2+,反应的离子方程式为2 +5SO+2H O=2Mn2++5 +4H+,C项正确;D.HO 将I-氧
2 2 2 2
化成I、自身被还原成HO,反应的离子方程式为2I-+2H++H O=I +2H O,D项正确;答案选B。
2 2 2 2 2 2
17.(2024·贵州黔南·二模)下列反应的离子方程式书写正确的是
A.向 溶液中滴加稀 :
B.将 溶液长时间煮沸时形成水垢:
C.铅酸蓄电池充电时的阴极反应:
D.向含 的溶液中通入
【答案】D
【解析】A.稀硝酸具有强氧化性,向NaSO 溶液中滴加稀HNO 会发生氧化还原反应生成S、 、
2 2 3 3NO和HO,反应的离子方程式为: ,A错误;B.
2
Mg2+与 在煮沸时发生双水解生成Mg(OH) 和CO,则将Mg(HCO ) 溶液长时间煮沸时形成水垢的离
2 2 3 2
子方程式为: ,B错误;C.铅酸蓄电池充电时的阴极反应为:
,C错误;D.因还原性:Fe2+>Br−,Cl 先与Fe2+发生反应:Cl+2Fe2+=2Fe3+
2 2
+2Cl⁻,0.1molFe2+消耗0.05molCl ,剩余的0.05molCl 再与0.1molBr−发生反应:Cl+2Br⁻=Br +2Cl⁻,则向
2 2 2 2
含0.1molFeBr 的溶液中通入0.1molCl 反应的离子方程式为:2Fe2++ 2Br−+2Cl=2Fe3++Br +4Cl⁻,D正确;
2 2 2 2
故选D。
18.(2024·甘肃张掖·模拟预测)下列离子方程式书写正确的是
A.铅酸蓄电池放电时的负极反应:
B.药物碘化钾片和加碘盐不可同时服用:
C.向 溶液中加入足量NaOH溶液:
D.向食盐的氨水溶液中通入足量 气体后生成沉淀:
【答案】B
【解析】A.铅酸蓄电池放电时Pb在负极失去电子生成PbSO ,电极方程式为: ,A
4
错误;B.酸性下,碘盐中的碘酸根离子可以和碘离子反应生成单质碘,离子方程式为
,B正确;C.向 溶液中加入足量NaOH溶液生成氢氧化镁沉淀和
碳酸钠,离子方程式为: ,C错误;D.向食盐的氨水
溶液中通入足量 气体后生成碳酸氢钠沉淀,离子方程式为:
,D错误;故选B。
19.(2024·安徽六安·二模)草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分为
,含少量 、 、CaO、MgO、碳及有机物等)制取 的工艺流程如图:
(1)“550℃焙烧”的目的是 。
(2)“碱浸”过程中浸出液主要成分是 。
(3)“钴浸出”过程中,不能用盐酸代替硫酸,因为 与盐酸反应生成 污染环境,该反应的离子
方程式为 , 的作用是 。
(4)“净化除杂1”过程中,先在 加入 ,再升温至 ,加入 溶液,调pH至
4.5。滤渣1的主要成分是 金属离子与 反应的离子方程式为 。(5)“净化除杂2”过程中,加入NaF以除去原溶液中 (浓度为 )和 ,若控制溶
液中 ,则 的去除率准确值为 。[已知某温度下, ]
【答案】(1)除去碳和有机物
(2) (或 和NaOH)
(3) 将 和 还原为 和 (作还原剂)
(4)
(5)90%
【分析】550℃焙烧含钴废料(主要成分为Co O,含少量Fe O、Al O、CaO、MgO、碳及有机物等)除
2 3 2 3 2 3
去碳和有机物,加入氢氧化钠溶液,其中Al O 溶解生成NaAlO ,Co O、Fe O、Al O、CaO、MgO不
2 3 2 2 3 2 3 2 3
溶,过滤,则浸出液的主要为NaAlO ,向过滤得到的固体加入稀硫酸和亚硫酸钠,NaSO 将Co3+、Fe3+还
2 2 3
原为Co2+、Fe2+,可得CoSO 、FeSO 、MgSO 、浸渣CaSO,在40~50℃加入HO,氧化Fe2+氧化为
4 4 4 4 2 2
Fe3+,再升温至80~85℃,加入NaCO 调pH至4.5,可得到Fe(OH) 沉淀,过滤后所得滤液主要含有
2 3 3
Co2+、Mg2+、Ca2+,用NaF溶液除去钙、镁,过滤后,滤液中主要含有Co2+,加入草酸铵溶液得到草酸钴
(注意:最新教材中NaAlO 可能改为四羟基合铝酸钠)。
2
【解析】(1)“550℃焙烧”高温条件下通过燃烧除去碳和有机物;
(2)氢氧化钠溶液溶解了氧化铝,“浸出液”的主要成分是 (或 和NaOH);
(3)Co O 在酸性条件下将氯离子氧化为氯气、自身被还原为Co2+,离子方程式为
2 3
;NaSO 具有较强还原性将Co3+、Fe3+还原为Co2+、Fe2+;
2 3
(4)根据沉淀pH范围,控制pH是为了促使完全Fe3+沉淀,而Co2+、Mg2+不沉淀,因此滤渣1的主要成分
是 ;双氧水将Fe2+氧化为Fe3+,酸性条件下的离子方程式为 ;
(5)控制溶液中 ,
,则此时溶液中
,则Ca2+的去除率为 。
20.(2024·河南信阳·模拟预测)五氧化二钽(TaO)主要用作钽酸锂单晶和制造高折射低色散特种光学玻
2 5
璃等。一种以含钽废料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO 的工
3 2 2 3 2 3 2 5
艺流程如图所示:
已知:HTaF 是弱酸。回答下列问题:
2 7
(1)“酸溶”时,Fe O 发生反应的基本反应类型为 ,滤渣的主要成分是 (填化学
2 3式)。
(2)“氧化”时,发生反应的离子方程式为 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的 , 是否沉淀完全? (请写出简要
步骤)。已知:常温下, ,溶液中离子浓度小于或等于 时可视为沉淀完
全。
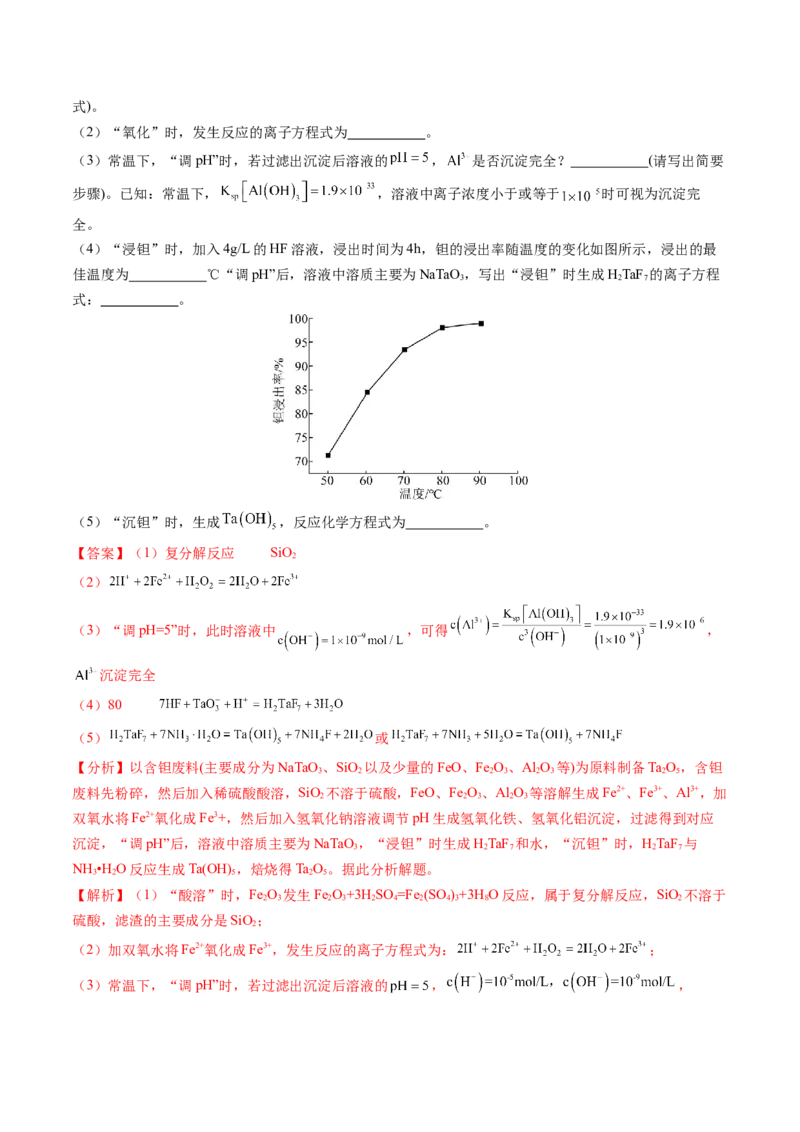
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,浸出的最
佳温度为 ℃“调pH”后,溶液中溶质主要为NaTaO ,写出“浸钽”时生成HTaF 的离子方程
3 2 7
式: 。
(5)“沉钽”时,生成 ,反应化学方程式为 。
【答案】(1)复分解反应 SiO
2
(2)
(3)“调pH=5”时,此时溶液中 ,可得 ,
沉淀完全
(4)80
(5) 或
【分析】以含钽废料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO,含钽
3 2 2 3 2 3 2 5
废料先粉碎,然后加入稀硫酸酸溶,SiO 不溶于硫酸,FeO、Fe O、Al O 等溶解生成Fe2+、Fe3+、Al3+,加
2 2 3 2 3
双氧水将Fe2+氧化成Fe3+,然后加入氢氧化钠溶液调节pH生成氢氧化铁、氢氧化铝沉淀,过滤得到对应
沉淀,“调pH”后,溶液中溶质主要为NaTaO ,“浸钽”时生成HTaF 和水,“沉钽”时,HTaF 与
3 2 7 2 7
NH •H O反应生成Ta(OH),焙烧得TaO。据此分析解题。
3 2 5 2 5
【解析】(1)“酸溶”时,Fe O 发生Fe O+3H SO =Fe (SO )+3H O反应,属于复分解反应,SiO 不溶于
2 3 2 3 2 4 2 4 3 8 2
硫酸,滤渣的主要成分是SiO;
2
(2)加双氧水将Fe2+氧化成Fe3+,发生反应的离子方程式为: ;
(3)常温下,“调pH”时,若过滤出沉淀后溶液的 , ,, 沉淀完全;
(4)由图可知,浸出的最佳温度为80℃,温度过低,浸出率低,温度过高,Ta浸出率变化不大,但耗能
增大;“调pH”后,溶液中溶质主要为NaTaO ,“浸钽”时生成HTaF 和水,离子方程式:
3 2 7
;
(5)沉钽”时通入氨气,生成了一水合氨,HTaF 与NH •H O反应生成Ta(OH),反应化学方程式为:
2 7 3 2 5
或 。
1.(2021·北京卷)使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现“亮→暗
(或灭)→亮”现象的是
选项 A B C D
试剂a CuSO NH HCO HSO CHCOOH
4 4 3 2 4 3
试剂
Ba(OH) Ca(OH) Ba(OH) NH ·H O
2 2 2 3 2
b
【答案】D
【解析】A.Ba(OH) 与CuSO 发生离子反应:Ba2++2OH-+Cu2++ =BaSO ↓+Cu(OH) ↓,随着反应的进
2 4 4 2
行,溶液中自由移动的离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微
粒,灯泡完全熄灭。当CuSO 溶液过量时,其电离产生的Cu2+、 导电,使灯泡逐渐又变亮,A不符合
4
题意;B.Ca(OH) 与NH HCO 发生离子反应:Ca2++2OH-+ + =CaCO ↓+H O+NH ·H O,随着反
2 4 3 3 2 3 2
应的进行,溶液中自由移动离子浓度减小,灯泡逐渐变暗,当二者恰好反应时,溶液中自由移动的微粒浓
度很小,灯泡很暗。当 NH HCO 溶液过量时,其电离产生的 、 导电,使灯泡逐渐又变亮,B
4 3
不符合题意;C.Ba(OH) 与HSO 发生离子反应:Ba2++2OH-+2H++ =BaSO ↓+2H O,随着反应的进
2 2 4 4 2
行,溶液中自由移动的离子浓度减小,灯泡变暗,当二者恰好反应时,溶液中几乎不存在自由移动的微
粒,灯泡完全熄灭。当HSO 溶液过量时,其电离产生的H+、 导电,使灯泡逐渐又变亮,C不符合题
2 4意;D.CHCOOH与氨水发生离子反应:CHCOOH+NH ·H O=CHCOO-+ +H O,反应后自由移动的
3 3 3 2 3 2
离子浓度增大,溶液导电能力增强,灯泡更明亮,不出现亮—灭(或暗)—亮的变化,D符合题意;故合理
选项是D。
2.(2021·浙江卷)下列物质属于强电解质的是
A.KOH B.HPO C.SO D.CHCHO
3 4 3 3
【答案】A
【分析】在水溶液中或熔融状态下能够完全电离的化合物为强电解质。
【解析】A.KOH在水溶液中或熔融状态下能够完全电离出K+和OH-,KOH为强电解质,A符合题意;
B.HPO 在水溶液中或熔融状态下能不够完全电离,HPO 为弱电解质,B不符合题意;C.SO 在水溶液
3 4 3 4 3
中或熔融状态下不能电离,SO 属于非电解质,C不符合题意;D.CHCHO在水溶液中或熔融状态下不能
3 3
电离,CHCHO属于非电解质,D不符合题意;故答案选A。
3
3.(2020·浙江卷)下列物质在熔融状态下不导电的是
A. B. C. D.
【答案】C
【解析】A.NaOH属于离子化合物,其在熔融状态下能电离成自由移动的Na+和OH-,故其在熔融状态下
能导电,A不符合题意;B.CaCl 属于离子化合物,其在熔融状态下能电离成自由移动的Ca2+和Cl-,故其
2
在熔融状态下能导电,B不符合题意;C.HCl是共价化合物,其在熔融状态下不能电离成离子,故其在熔
融状态下不导电,C符合题意;D.KSO 属于离子化合物,其在熔融状态下能电离成自由移动的K+和
2 4
,故其在熔融状态下能导电,D不符合题意。综上所述,本题答案为C。
4.(2023·湖南卷)下列有关电极方程式或离子方程式错误的是
A.碱性锌锰电池的正极反应:MnO +H O+e-=MnO(OH)+OH-
2 2
B.铅酸蓄电池充电时的阳极反应:Pb2++2H O-2e-=PbO+4H+
2 2
C.K[Fe(CN) ]溶液滴入FeCl 溶液中:K++Fe2++[Fe(CN)]3-=KFe[Fe(CN) ]↓
3 6 2 6 6
D.TiCl 加入水中:TiCl +(x+2)H O=TiO·xHO↓+4H++4Cl-
4 4 2 2 2
【答案】B
【解析】A.碱性锌锰电池放电时正极得到电子生成MnO(OH),电极方程式为MnO +H O+e-=MnO(OH)
2 2
+OH-,A正确;B.铅酸电池在充电时阳极失电子,其电极式为:PbSO -2e-+2H O=PbO +4H++SO ,B错
4 2 2
误;C.K[Fe(CN) ]用来鉴别Fe2+生成滕氏蓝沉淀,反应的离子方程式为K++Fe2++[Fe(CN)]3-
3 6 6
=KFe[Fe(CN) ]↓,C正确;D.TiCl 容易与水反应发生水解,反应的离子方程式为TiCl +
6 4 4
(x+2)H O=TiO·xHO↓+4H++4Cl-,D正确;故答案选B。
2 2 2
5.(2023·浙江卷)下列反应的离子方程式不正确的是
A. 通入氢氧化钠溶液:
B.氧化铝溶于氢氧化钠溶液:
C.过量 通入饱和碳酸钠溶液:D. 溶液中滴入氯化钙溶液:
【答案】D
【解析】A. 通入氢氧化钠溶液中反应生成氯化钠、次氯酸钠和水,反应的离子方程式为:
,选项A正确;B.氧化铝溶于氢氧化钠溶液生成偏铝酸钠和水,反应的离子方
程式为: ,选项B正确;C.过量 通入饱和碳酸钠溶液反应产生碳酸氢钠晶
体,反应的离子方程式为: ,选项C正确;D. 溶液中滴入氯化
钙溶液,因亚硫酸酸性弱于盐酸,不能发生反应,选项D不正确;答案选D。
6.(2022·全国卷)能正确表示下列反应的离子方程式为
A.硫化钠溶液和硝酸混合:S2-+2H+=H S↑
2
B.明矾溶液与过量氨水混合:Al3++4NH+2H O=AlO +4NH
3 2
C.硅酸钠溶液中通入二氧化碳:SiO +CO +H O=HSiO +HCO
2 2
D.将等物质的量浓度的Ba(OH) 和NH HSO 溶液以体积比1∶2混合:Ba2++2OH-+2H++SO =BaSO ↓+2H O
2 4 4 4 2
【答案】D
【解析】A.硝酸具有强氧化性,可以将S2-氧化为S单质,自身根据其浓度大小还原为NO或NO ,反应
2
的离子方程式为4H++2NO +S2-=S↓+2NO↑+2H O(浓)或8H++2NO +3S2-=3S↓+2NO↑+4H O(稀),A错误;
2 2 2
B.明矾在水中可以电离出Al3+,可以与氨水电离出的OH-发生反应生成Al(OH) ,但由于氨水的碱性较
3
弱,生成的Al(OH) 不能继续与弱碱发生反应,故反应的离子方程式为Al3++3NH·H O=Al(OH) ↓+3NH ,
3 3 2 3
B错误;C.硅酸的酸性小于碳酸,向硅酸钠溶液中通入二氧化碳时,生成硅酸沉淀,二氧化碳则根据其
通入的量的多少反应为碳酸根或碳酸氢根,反应的离子方程式为SiO +H O+CO=H SiO↓+CO (CO 少
2 2 2 3 2
量)或SiO +2H O+2CO=H SiO↓+2HCO (CO 过量),C错误;D.将等物质的量浓度的Ba(OH) 与
2 2 2 3 2 2
NH HSO 溶液以体积比1:2混合,Ba(OH) 电离出的OH-与NH HSO 电离出的H+反应生成水,Ba(OH) 电
4 4 2 4 4 2
离出的Ba2+与NH HSO 电离出的SO 反应生成BaSO 沉淀,反应的离子方程为为Ba2++2OH-+2H++SO
4 4 4
=BaSO ↓+2H O,D正确;故答案选D。
4 2
7.(2022·浙江卷)下列实验对应的离子方程式不正确的是
A.将碳酸氢钙溶液与过量的澄清石灰水混合: +Ca2++OH-=CaCO ↓+H O
3 2
B.将少量NO 通入NaOH溶液:2NO +2OH-= + +H O
2 2 2
C.将少量SO 通入NaClO溶液:SO +H O+2ClO-= +2HClO
2 2 2
D.向氨水中滴入少量硝酸银溶液:Ag++2NH·H O= +2H O
3 2 2
【答案】C
【解析】A. 将碳酸氢钙溶液与过量的澄清石灰水混合,反应生成碳酸钙和水,反应的离子方程式为:
+Ca2++OH-=CaCO ↓+H O,选项A正确;B. 将少量NO 通入NaOH溶液,反应生成硝酸钠、亚硝酸
3 2 2钠和水,反应的离子方程式为:2NO +2OH-= + +H O,选项B正确;C. 将少量SO 通入NaClO
2 2 2
溶液,反应生成硫酸钠和盐酸,反应的离子方程式为:SO +H O+3ClO-= +2HClO+Cl-,选项C不正
2 2
确;D. 向氨水中滴入少量硝酸银溶液,反应生成氢氧化二氨合银,反应的离子方程式为:Ag++2NH·H O=
3 2
+2H O,选项D正确;答案选C。
2
8.(2022·湖南卷)下列离子方程式正确的是
A. 通入冷的 溶液:
B.用醋酸和淀粉 溶液检验加碘盐中的 :
C. 溶液中加入 产生沉淀:
D. 溶液与少量的 溶液混合:
【答案】AC
【解析】A.Cl 通入冷的 NaOH溶液中发生反应生成氯化钠和次氯酸钠,该反应的离子方程式为
2
Cl+2OH-=Cl-+ClO-+H O,A正确;B.用醋酸和淀粉-KI溶液检验加碘盐中的 的原理是 在酸性条
2 2
件下与I-发生归中反应生成I 而遇淀粉变蓝,由于醋酸是弱酸,在离子方程式中不能用H+表示,因此B
2
不正确;C.+2价的铁被双氧水氧化为+3价,反应的离子方程式为2Fe2++H O+4H O=2Fe(OH) ↓+4H+,C
2 2 2 3
正确;D.NaHCO 溶液与少量的Ba(OH) 溶液混合后发生反应生成碳酸钡沉淀、碳酸钠和水,NaHCO 过
3 2 3
量,Ba(OH) 全部参加反应,因此该反应的离子方程式为2 +Ba2++2OH-=BaCO ↓+ +2H O,D不正
2 3 2
确;综上所述,本题选AC。
9.(2021·广东卷)宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式
书写正确的是
A. 放入水中:
B. 通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D. 通入酸性 溶液中:
【答案】D
【解析】A. 放入水中化学方程式应该是: ,A选项中氧元素不守
恒,A错误;B. 通过灼热铁粉应高温条件下生成四氧化三铁和氢气,B错误;C.铜丝插入热的
浓硫酸中生成的气体不是氢气,应是二氧化硫,C错误;D. 通入酸性 溶液中, 被 氧
化为 , 被 还原为 ,再根据得失电子守恒、电荷守恒和元素守恒可得离子方程式为
,D正确;故选D。
10.(2021·全国卷)下列过程中的化学反应,相应的离子方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:B.过量铁粉加入稀硝酸中:
C.硫酸铝溶液中滴加少量氢氧化钾溶液:
D.氯化铜溶液中通入硫化氢:
【答案】A
【解析】A.硫酸钙微溶,用碳酸钠溶液处理水垢中的硫酸钙转化为难溶的碳酸钙,离子方程式为:
,故A正确;B.过量的铁粉与稀硝酸反应生成硝酸亚铁、一氧化氮和水,
离子方程式应为:3Fe+8H++2N =3Fe2++2NO↑+4HO,故B错误;C.硫酸铝溶液与少量氢氧化钾溶液反
2
应生成氢氧化铝沉淀和硫酸钾,离子方程式应为:Al3++3OH-=Al(OH) ↓,故C错误;D.硫化氢为弱电解
3
质,书写离子方程式时不能拆,离子方程式应为:Cu2++H S=CuS↓+2H+,故D错误;答案选A。
2