文档内容
第 03 讲 物质的组成、性质和分类
目录
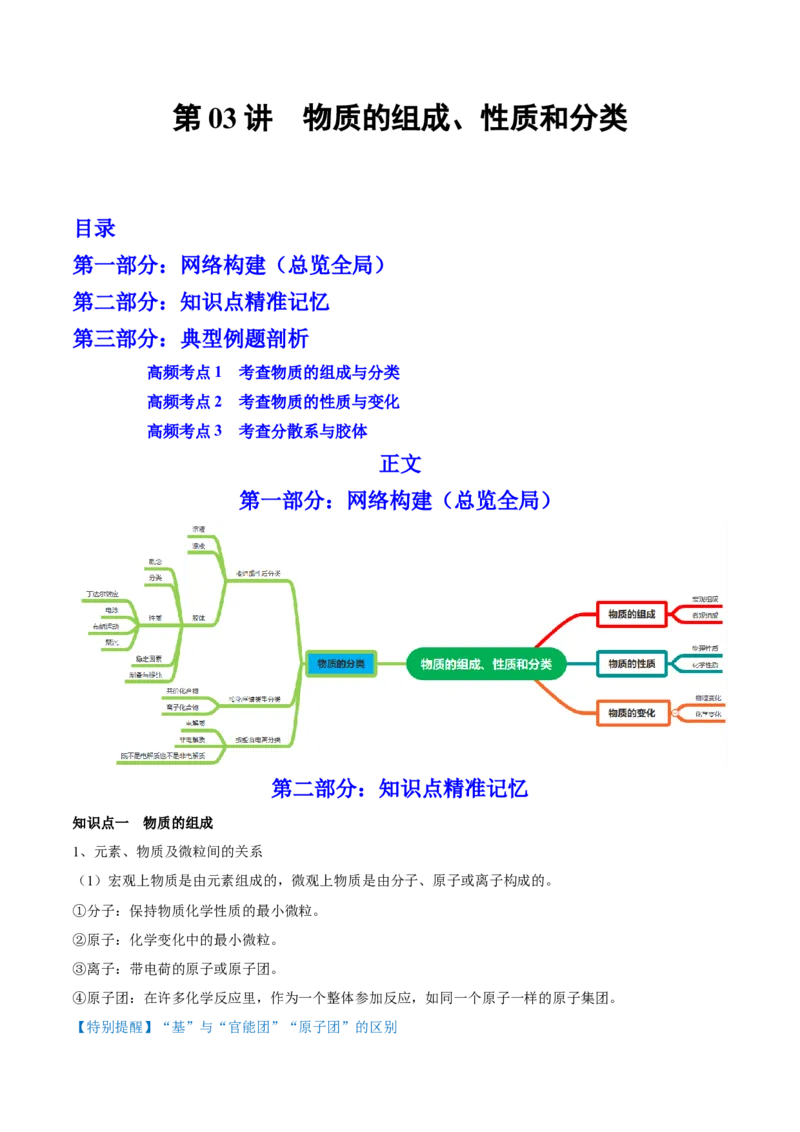
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
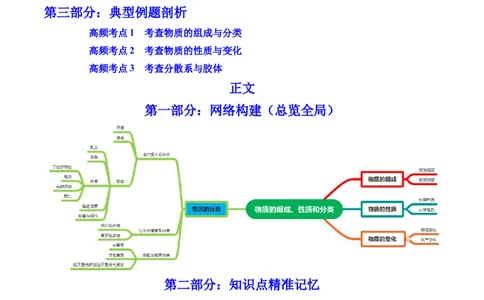
第三部分:典型例题剖析
高频考点1 考查物质的组成与分类
高频考点2 考查物质的性质与变化
高频考点3 考查分散系与胶体
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 物质的组成
1、元素、物质及微粒间的关系
(1)宏观上物质是由元素组成的,微观上物质是由分子、原子或离子构成的。
①分子:保持物质化学性质的最小微粒。
②原子:化学变化中的最小微粒。
③离子:带电荷的原子或原子团。
④原子团:在许多化学反应里,作为一个整体参加反应,如同一个原子一样的原子集团。
【特别提醒】“基”与“官能团”“原子团”的区别①基是指带有单电子的原子团。如—CH、—CH—(亚甲基)、—CHCH。
3 2 2 3
②官能团是指决定有机物化学性质的原子或原子团。如—OH、—CHO、—COOH、—X(卤素原子)等。
③“基”和“官能团”呈电中性,而CO、NO、SO、NH等原子团可带负电荷或正电荷。
(2)元素:具有相同核电荷数的一类原子的总称。
元素在自然界的存在形式有游离态和化合态。
①游离态:元素以单质形式存在的状态。
②化合态:元素以化合物形式存在的状态。
(3)元素与物质的关系
元素――→
(4)原子与物质的关系
2、同素异形体
(1)概念:同种元素形成的不同单质叫同素异形体。
(2)形成方式
①原子个数不同,如O 和O;
2 3
②原子排列方式不同,如金刚石和石墨。
(3)性质差异
物理性质差别较大,同素异形体之间的转化属于化学变化。
3、混合物和纯净物
(1)纯净物:由同种单质或化合物组成的物质。
(2)混合物:由几种不同的单质或化合物组成的物质。
纯净物和混合物的区别
纯净物 混合物
有固定的组成和结构 无固定的组成和结构
有一定的熔、沸点 无一定的熔、沸点
保持一种物质的性质 保持原有物质各自的性质
4.元素、微粒及物质间的关系图知识点二 物质的分类
根据物质的组成,可以从不同层次和不同角度对物质进行分类。
1、简单分类法—交叉分类法和树状分类法
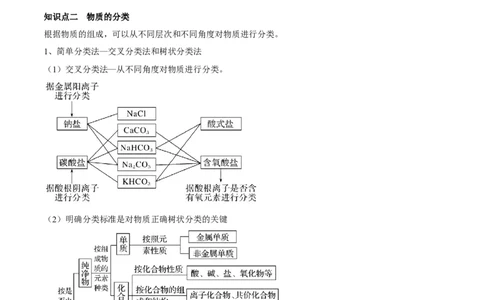
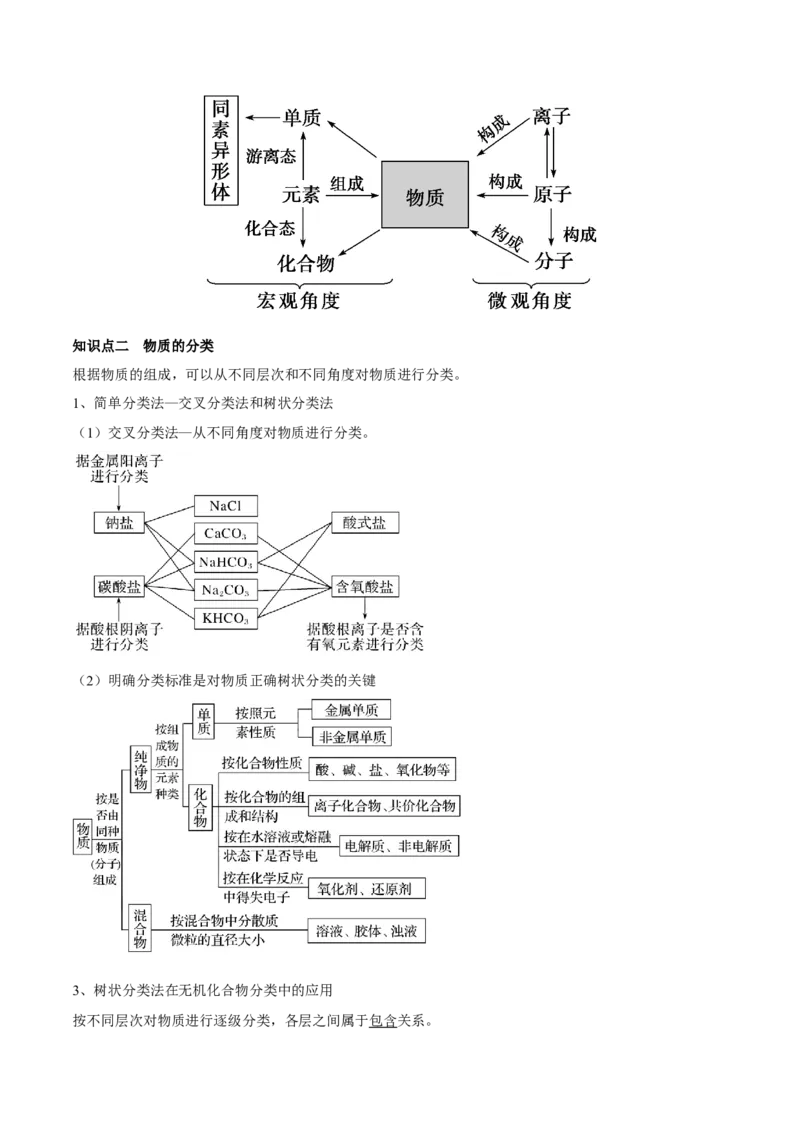
(1)交叉分类法—从不同角度对物质进行分类。
(2)明确分类标准是对物质正确树状分类的关键
3、树状分类法在无机化合物分类中的应用
按不同层次对物质进行逐级分类,各层之间属于包含关系。【特别提醒】
1)熟悉常见的混合物
(1)气体混合物:空气、水煤气(CO和H)、爆鸣气(H 和O)、天然气(主要成分是CH)、焦炉气(主要成分
2 2 2 4
是H 和CH)、高炉煤气、石油气、裂解气。
2 4
(2)液体混合物:氨水、氯水、王水、天然水、硬水、软水、水玻璃、福尔马林、浓硫酸、盐酸、汽油、植
物油、胶体。
(3)固体混合物:大理石、碱石灰、漂白粉、高分子化合物、玻璃、水泥、合金、铝热剂。
2)正确理解几个“一定”“不一定”
(1)酸性氧化物和碱性氧化物
a.碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物(如MnO 为酸性氧化物、Al O 为两
2 7 2 3
性氧化物、NaO 为过氧化物)。
2 2
b.酸性氧化物不一定是非金属氧化物(如MnO);非金属氧化物也不一定是酸性氧化物(如CO、NO)。
2 7
c.酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸、碱(如SiO、Fe O)。
2 2 3
d.酸性氧化物都是对应酸的酸酐,但酸酐不一定都是酸性氧化物,如乙酸酐[(CH CO) O]。
3 2
e.溶于水生成酸的氧化物不一定是酸性氧化物,如 NO ;溶于水生成碱的氧化物不一定是碱性氧化物,如
2
NaO。
2 2(2)共价化合物和离子化合物
a.由非金属元素组成的化合物不一定是共价化合物,如铵盐。
b.由金属元素和非金属元素组成的化合物不一定是离子化合物,如AlCl 。
3
(3)纯净物和混合物
a.只含一种元素的物质不一定是纯净物,也可能是混合物,如O 和O,金刚石和石墨,正交硫和单斜硫。
2 3
b.结晶水合物属于纯净物,如CuSO ·5H O、KAl(SO )·12H O等物质。
4 2 4 2 2
c.同位素形成的单质或化合物是纯净物,如H 与D、HO与DO。
2 2 2 2
d.分子式为C H 的物质存在多种同分异构体,可能是纯净物也可能是混合物。
5 10
3)确定某酸是几元酸,不能依据分子中氢原子的个数,如CHCOOH不是四元酸,而是一元酸。
3
知识点三 物质的性质与变化
1、物理性质和化学性质
2、物理变化和化学变化(1)物理变化与化学变化的比较
注意:①化学变化中常伴有发光、放热现象,但有发光、放热现象的变化不一定属于化学变化,如金属受
热发光。
②化学变化中一定存在化学键的断裂和形成,但存在化学键断裂的变化不一定是化学变化,如HCl溶于水、
熔融NaCl电离等。
③原子的裂变、聚变虽有新物质生成,但它不属于中学化学意义上的化学变化。
④物理变化与化学变化的判断方法
(2)化学反应的分类
化学反应
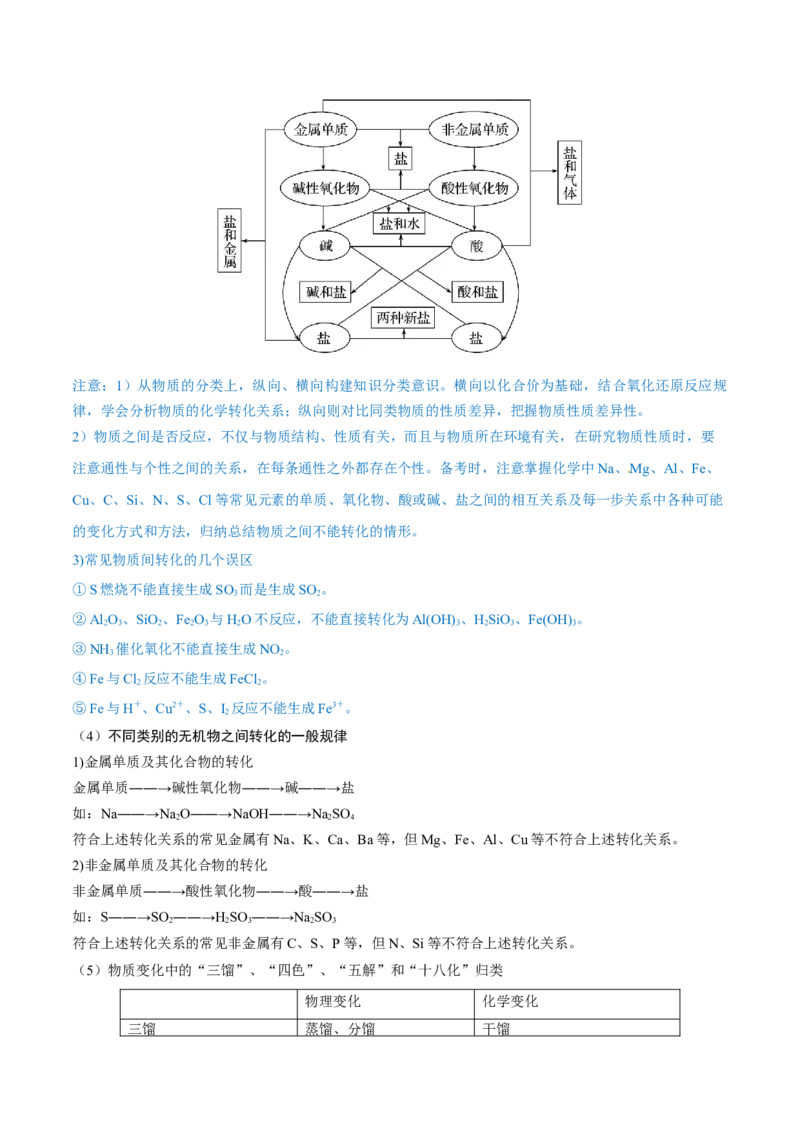
(3)单质、氧化物、酸、碱和盐的转化关系注意:1)从物质的分类上,纵向、横向构建知识分类意识。横向以化合价为基础,结合氧化还原反应规
律,学会分析物质的化学转化关系;纵向则对比同类物质的性质差异,把握物质性质差异性。
2)物质之间是否反应,不仅与物质结构、性质有关,而且与物质所在环境有关,在研究物质性质时,要
注意通性与个性之间的关系,在每条通性之外都存在个性。备考时,注意掌握化学中Na、Mg、Al、Fe、
Cu、C、Si、N、S、Cl等常见元素的单质、氧化物、酸或碱、盐之间的相互关系及每一步关系中各种可能
的变化方式和方法,归纳总结物质之间不能转化的情形。
3)常见物质间转化的几个误区
①S燃烧不能直接生成SO 而是生成SO 。
3 2
②Al O、SiO、Fe O 与HO不反应,不能直接转化为Al(OH) 、HSiO、Fe(OH) 。
2 3 2 2 3 2 3 2 3 3
③NH 催化氧化不能直接生成NO 。
3 2
④Fe与Cl 反应不能生成FeCl 。
2 2
⑤Fe与H+、Cu2+、S、I 反应不能生成Fe3+。
2
(4)不同类别的无机物之间转化的一般规律
1)金属单质及其化合物的转化
金属单质――→碱性氧化物――→碱――→盐
如:Na――→NaO――→NaOH――→NaSO
2 2 4
符合上述转化关系的常见金属有Na、K、Ca、Ba等,但Mg、Fe、Al、Cu等不符合上述转化关系。
2)非金属单质及其化合物的转化
非金属单质――→酸性氧化物――→酸――→盐
如:S――→SO ――→HSO ――→NaSO
2 2 3 2 3
符合上述转化关系的常见非金属有C、S、P等,但N、Si等不符合上述转化关系。
(5)物质变化中的“三馏”、“四色”、“五解”和“十八化”归类
物理变化 化学变化
三馏 蒸馏、分馏 干馏显色反应、颜色反应、指示剂
四色 焰色反应
变色反应
五解 潮解 分解、电解、水解、裂解
氢化、氧化、水化
溶化、
风化、炭化、钝化、
汽化、
十八化 催化、皂化、歧化、
液化、
卤化、硝化、酯化、
酸化、
裂化、油脂的硬化
(6)物质性质与变化的关系
物质的性质是物质固有的属性,是物质的基本特征,是变化的内因(即变化的依据)。物质变化就是物
质的形态发生了变化(物理变化)或者物质的分子构成发生了变化(化学变化)。变化是一个过程或现象,是性
质的具体体现,即性质决定变化,变化体现性质。物质具有某种性质,才会发生对应的变化;物质发生了
某种变化,说明了该物质具备某种性质。
知识点四 分散系、胶体
1、分散系
(1)概念:一种(或多种)物质分散到另一种(或多种)物质中所得到的体系。被分散的物质称为分散质,起
容纳分散质作用的物质称为分散剂。
(2)分类:
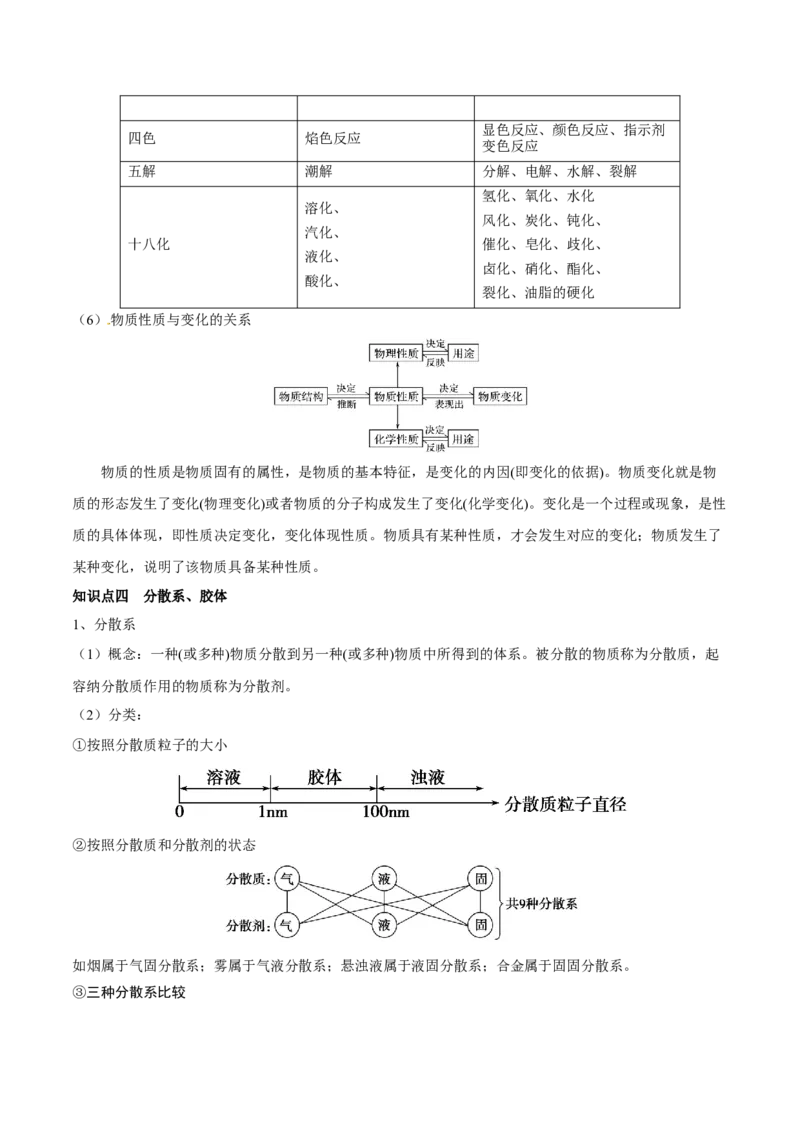
①按照分散质粒子的大小
②按照分散质和分散剂的状态
如烟属于气固分散系;雾属于气液分散系;悬浊液属于液固分散系;合金属于固固分散系。
③三种分散系比较分散系 溶液 胶体 浊液
分散质粒子直径大小 < 1 nm 1 ~ 100 nm >100 nm
巨大分子或离
分散质微粒成分 离子或小分子 大分子或离子集合体
子集合体
不均匀、不透
外观特征 均匀、透明 均匀、透明或半透明
明
稳定,静置无沉 不稳定,静置
稳定性 较稳定
淀 有沉淀或分层
分散质能否透过滤纸 能 能 不能
饱和溶液、不饱 固溶胶、液溶胶、气溶 悬浊液、乳浊
分类
和溶液 胶 液
食盐水、蔗糖溶
实例 Fe(OH) 胶体 泥水
3
液
2、胶体
(1)胶体的性质与应用
①丁达尔效应:可见光束通过胶体时,在入射光侧面可看到一条光亮的通路,这是胶体粒子对光线散射而形
成的,可用此性质来鉴别溶液和胶体。
②布朗运动:胶粒永不停息地做无规则运动的现象叫做布朗运动,是胶体稳定的次要原因。
③电泳:由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中作定向移动的现象。此性质可用于工
业上的静电除尘。
④聚沉
a.概念:使胶体凝聚形成沉淀析出的现象。
b.方法:、、的胶体
c.应用,如制作豆腐、明矾净水等。
⑤介稳性:胶体的稳定性介于溶液和浊液之间,属于介稳体系。
注意:同种胶体粒子的电性相同,互相排斥,是胶体较稳定的主要原因,次要原因是布朗运动。
(2)Fe(OH) 胶体的制备
3
①制备原理:FeCl +3HO Fe(OH) (胶体)+3HCl
3 2 3
②具体操作:用烧杯取少量蒸馏水,加热至沸腾;向沸水中逐滴加入适量的饱和FeCl 溶液;继续煮沸至
3
溶液呈红褐色,停止加热,即得Fe(OH) 胶体。
3(3)胶体的应用
①工业除杂、除尘
②土壤的保肥作用
③豆腐的制作原理
④江河入海口处形成三角沙洲
⑤明矾的净水作用。
【易错警示】
1.利用丁达尔效应可以快速鉴别溶液与胶体,但胶体区别于其他分散系的本质特征是胶体粒子的直径介
于1~100 nm之间,而不是丁达尔效应。
2.胶体不带电荷,胶体粒子(分散质)带电荷,但淀粉胶体的胶体粒子也不带电荷,但整个分散系仍呈电中
性。
3.Fe(OH) 胶体中,Fe(OH) 胶粒数目远小于铁原子的数目。
3 3
4.胶粒有很大的比表面积,吸附能力很强。
5.胶体中的分散质微粒能透过滤纸,但不能透过半透膜,因此可用过滤的方法分离胶体和浊液,用渗析的
方法分离胶体和溶液。
6.书写Fe(OH) 胶体制备化学方程式的四个易错点。
3
①用“===”而不用“ ”;
②Fe(OH) 分子式后注明胶体而不使用“↓”符号;
3
③反应条件是“△”;
④HCl后不能标“↑”符号。
第三部分:典型例题剖析
高频考点1 考查物质的组成与分类
例1.(2021·新泰市第一中学北校月考)将物质进行分类,有助于理解和记忆。下列物质的分类正确的是(
)
分类 酸 碱 盐 碱性氧化物 酸性氧化物
A HSO NaCO NaOH SO CO
2 4 2 3 2 2B HCl NaOH NaCl NaO
2
C HNO KOH CaCO CaO SO
3 3 2
D NaHSO NaOH NH Cl Fe O SO
4 4 2 3 3
【变式训练1】(物质的分类)(2021·北京朝阳区高三期末)2020年12月17日,“嫦娥五号”返回器携带
月壤成功返回,“可上九天揽月”成为现实。下列涉及火箭发射及“嫦娥五号”的系列材料中,主要成分
均为非金属单质的是( )
A.“长征五号” B.制作月面展开的国旗 D.返回器表面所贴“暖宝
C.返回器减速伞材料
发动机推进剂—— 材料之一——高强度芳纶 宝”主要成分——铁粉、碳
——高强度锦纶纤维
液氧和液氢 纤维 粉等
【变式训练2】(生活中物质的分类)(2021浙江省杭州市高三教学质量检测)垃圾分类并回收利用,可以
减少垃圾处理量,提高资源利用价值。下列垃圾分类不合理的是( )
A B C D
垃圾 废荧光灯管 丢弃的菜叶 废药品 卫生间废纸
垃 圾
分类
高频考点2 考查物质的性质与变化
例2.(2021·福建三明市·高三二模)下列体现我国悠久金属矿物开发历史的诗文中,不涉及化学变化的是
A.千淘万漉虽辛苦,吹尽狂沙始到金 B.丹砂烧之成水银,积变又还成丹砂
C.熬胆矾铁釜,久之亦化为铜 D.君不见昆吾铁冶飞炎烟,红光紫气俱赫然
【变式训练1】(物质变化类型的判断)下列诗句或谚语都与化学现象有关,下列说法不正确的是( )
A.“水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化
B.“落汤螃蟹着红袍”肯定发生了化学变化
C.“滴水石穿,绳锯木断”不包含化学变化
D.“野火烧不尽,春风吹又生”包含了多种化学变化
【变式训练2】(物质变的性质及其应用)下列过程中没有发生化学变化的是( )
A.氯气作水的杀菌消毒剂B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂
D.肥皂水作蚊虫叮咬处的清洗剂
【变式训练3】(化学反应类型的判断)(2021·福建厦门市期末)2020年世界十大重要科学发现中,涉及化
学变化的是( )
A.低温电镜达到原子分辨率 B.臭氧层正在自我修复
C.卫星图像绘制树木地图 D.发现银河系快速射电暴来源
高频考点3 考查分散系与胶体
例3.(2021·云南高三二模)我国科学家近来研制出的“全碳气凝胶”固体材料“碳海绵”,是迄今世界
上最轻的材料。下列关于“碳海绵”的说法错误的是
A.光束照射时可观察到丁达尔现象
B.常温下具有良好的耐酸、耐碱性
C.可用于处理海面的漏油
D.其净水过程是化学变化
【变式训练1】(胶体的组成和性质)(2021·东莞市光明中学期末)我国科学家在世界上第一次为一种名为
“钴酞菁”的分子(直径为1.3× 10-9 m)恢复了磁性。“钴酞菁”分子结构和性质与人体内的血红素及植物
体内的叶绿素非常相似。下列说法中正确的是( )
A.“钴酞菁”分子具有丁达尔效应
B.“钴酞菁”分子不能透过滤纸
C.此项工作可以用来改变分子的某些物理性质
D.将“钴酞菁”分子分散到水中能形成悬浊液
【变式训练2】(胶体的性质和应用)(2021·陕西西安市·长安一中月考)由空气中的灰尘、硫酸、硝酸等颗
粒物组成的气溶胶系统造成的视觉障碍叫霾。当水汽凝结加剧、空气湿度增大时,霾就会转化为雾。二氧
化硫、氮氧化物和可吸入颗粒物是雾霾的主要组成。以下说法不正确的是( )
A.雾霾天,汽车车灯照出通路的现象属于丁达尔效应
B.静电除尘器除去空气或工厂废气中的飘尘是利用胶体粒子的带电性而加以除去
C.防雾霾口罩的原理与过滤、渗析类似,防雾霾效果好的口罩往往呼吸阻力较大
D.PM2.5是直径小于或等于2.5 μm的污染物颗粒,完全属于胶体粒子的直径范围
【变式训练3】(胶体的制备)某班同学在化学实验课上利用必修 1教材的实验方法制备氢氧化铁胶体,
方法如下:在一个洁净的烧杯中加入蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴滴加饱和的 FeCl 溶液
3继续煮沸,得到透明的红褐色液体。化学方程式为FeCl +3HO Fe(OH) (胶体)+3HCl。
3 2 3
(1)判断胶体制备是否成功,比较简单的方法就是利用胶体的________________进行验证。
(2)在做制备氢氧化铁胶体的实验时,有些同学没有按要求进行,结果没有观察到胶体,请你预测其现象并
分析原因:
①甲同学没有选用饱和氯化铁溶液,而是将稀氯化铁溶液滴入沸水中,结果没有观察到________,其原因
是_____________________________________________________________。
②乙同学在实验中没有使用蒸馏水,而是用自来水,结果会____________,原因是
________________________________________________________________________。
③丙同学向沸水中滴加饱和氯化铁溶液后,长时间加热,结果会____________,原因是
________________________________________________________________________。
(3)丁同学按要求制备了Fe(OH) 胶体,但是他又向Fe(OH) 胶体中逐滴加入了稀HSO 溶液,结果出现了
3 3 2 4
一系列变化。
①先出现红褐色沉淀,原因是____________________________________________________。
②随后沉淀溶解,此反应的离子方程式是
________________________________________________________________________。