文档内容
第 08 讲 金属材料
1.能从合金结构与组成的角度理解合金的特殊性能反应,培养宏观辨识与微观探析的能力。
2.能列举常见合金的组成和性能,能科学、合理的选择和使用金属材料,培养学生的科学精神和社会
责任感。
【核心素养分析】
1.宏观辨识与微观探析:认识金属材料的性能和应用,根据金属及其化合物的性质理解常见金属的冶
炼原理。
2.科学态度与社会责任:根据金属的冶炼原理及方法,认识开发利用金属矿物应具有可持续性,培养
绿色环保意识。
3.科学探究与创新意识:科学领悟铜、铝及其化合物的性质及探究方案并进行实验探究,得出其主要
性质。
知识点一 铝、镁的性质及应用
1.金属铝的物理性质
银白色有金属光泽的固体,有良好的延展性、导电性和导热性等,密度较小,质地柔软。
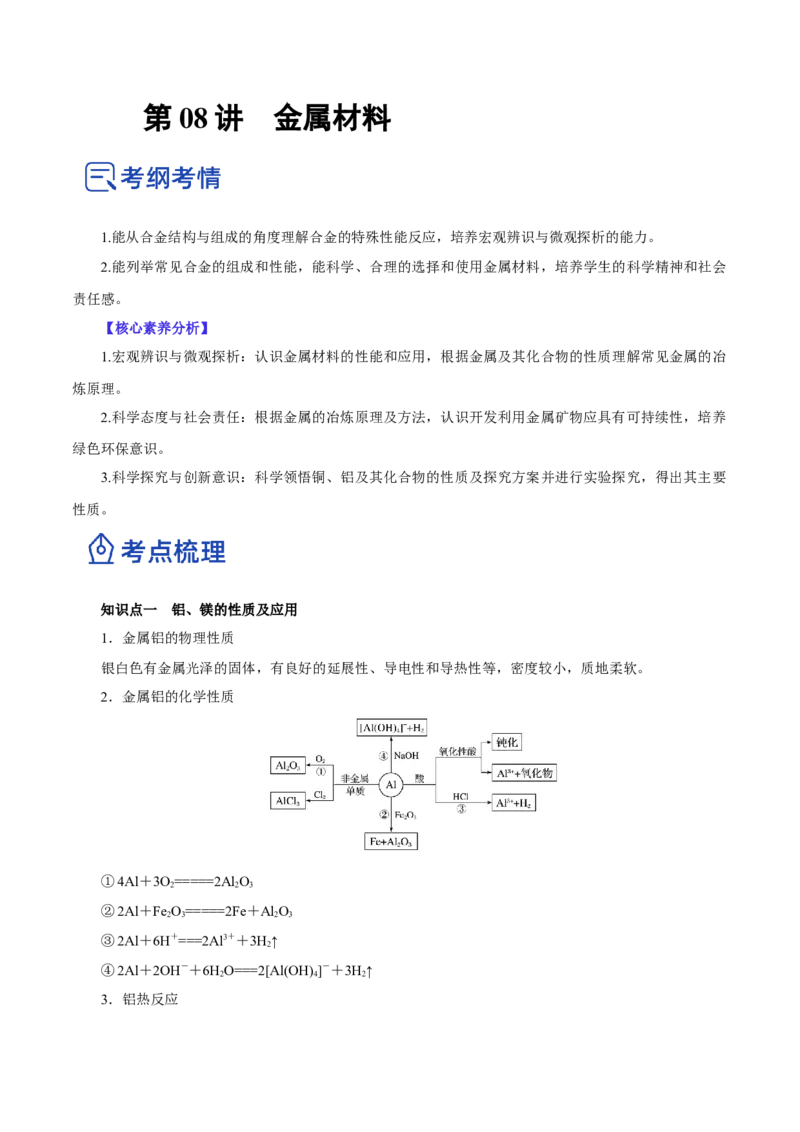
2.金属铝的化学性质
①4Al+3O=====2Al O
2 2 3
②2Al+Fe O=====2Fe+Al O
2 3 2 3
③2Al+6H+===2Al3++3H↑
2
④2Al+2OH-+6HO===2[Al(OH) ]-+3H↑
2 4 2
3.铝热反应实验装置
①镁带剧烈燃烧,放出大量的热,并发出耀眼的白光,氧化铁与铝粉在
实验现象
较高温度下发生剧烈的反应;②纸漏斗的下部被烧穿,有熔融物落入沙中
高温下,铝与氧化铁发生反应,放出大量的热:Fe O+2Al=====2Fe+
实验结论 2 3
Al O
2 3
①制取熔点较高、活动性弱于Al的金属,如铁、铬、锰、钨等,
原理应用 3MnO +4Al=====3Mn+2Al O;
2 2 3
②金属焊接,如野外焊接钢轨等
4.铝的制备和用途
(1)制备原理
电解熔融Al O:2Al O(熔融)=====4Al+3O↑。
2 3 2 3 2
【特别提醒】工业上冶炼Al用电解熔融Al O 而不用AlCl 的原因是AlCl 是共价化合物,熔融态不导
2 3 3 3
电。
(2)铝的用途
纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
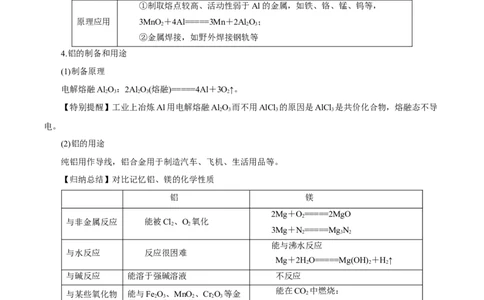
【归纳总结】对比记忆铝、镁的化学性质
铝 镁
2Mg+O=====2MgO
2
与非金属反应 能被Cl、O 氧化
2 2
3Mg+N=====MgN
2 3 2
能与沸水反应
与水反应 反应很困难
Mg+2HO=====Mg(OH) +H↑
2 2 2
与碱反应 能溶于强碱溶液 不反应
与某些氧化物 能与Fe O、MnO 、Cr O 等金
能在CO
2
中燃烧:
2 3 2 2 3
反应 属氧化物发生铝热反应 2Mg+CO=====2MgO+C
2
【特别提醒】铝与酸或碱反应生成H 的量的关系
2
2Al+6HCl===2AlCl +3H↑
3 2
2Al+2NaOH+6HO===2Na[Al(OH) ]+3H↑
2 4 2
(1)等质量的铝与足量的盐酸、氢氧化钠溶液分别反应:
①产生H 的物质的量相等。
2
②消耗H+、OH-的物质的量之比为n(H+)∶n(OH-)=3∶1。(2)足量的铝分别与等物质的量的HCl和NaOH反应:
①消耗Al的物质的量之比为1∶3。
②生成H 的物质的量之比为1∶3。
2
(3)一定量的铝分别与一定量的盐酸、氢氧化钠溶液反应:
若产生氢气的体积比为<<1,则必定
①铝与盐酸反应时,铝过量而HCl不足。
②铝与氢氧化钠溶液反应时,铝不足而NaOH过量。
知识点二 铝的重要化合物
1.氧化铝
(1)物理性质:白色固体,难溶于水,熔点很高。
(2)化学性质
2.氢氧化铝
(1)物理性质:白色胶状不溶于水的固体,有较强的吸附性。
(2)化学性质(用化学方程式表示)
Al(OH) 的电离方程式为
3
酸式电离:Al(OH) +HO [Al(OH) ]-+H+
3 2 4
碱式电离:Al(OH) Al3++3OH-
3
写出图中有关反应的化学方程式或离子方程式:
①Al(OH) +3H+===Al3++3HO。
3 2
②Al(OH) +OH-===[Al(OH) ]-。
3 4
③2Al(OH) =====Al O+3HO。
3 2 3 2
(3)制备
①向铝盐中加入氨水,离子方程式为Al3++3NH ·H O ===Al(OH) ↓+3NH。
3 2 3
②Na[Al(OH)]溶液中通入足量CO,离子方程式为
4 2
[Al(OH) ]-+CO===Al(OH) ↓+HCO。
4 2 3
③Na[Al(OH)]溶液与AlCl 溶液混合:3[Al(OH) ]-+Al3+===4Al(OH) ↓。
4 3 4 33.常见的铝盐
(1)硫酸铝钾是由两种不同的金属离子和一种酸根离子组成的复盐。
(2)明矾的化学式为KAl(SO )·12H O,它是无色晶体,可溶于水,水溶液pH<(填“<”“>”或
4 2 2
“=”)7。明矾可以净水,其净水的原理是Al3++3HO Al(OH) (胶体)+3H+,Al(OH) 胶体吸附水中
2 3 3
的杂质形成沉淀而净水。
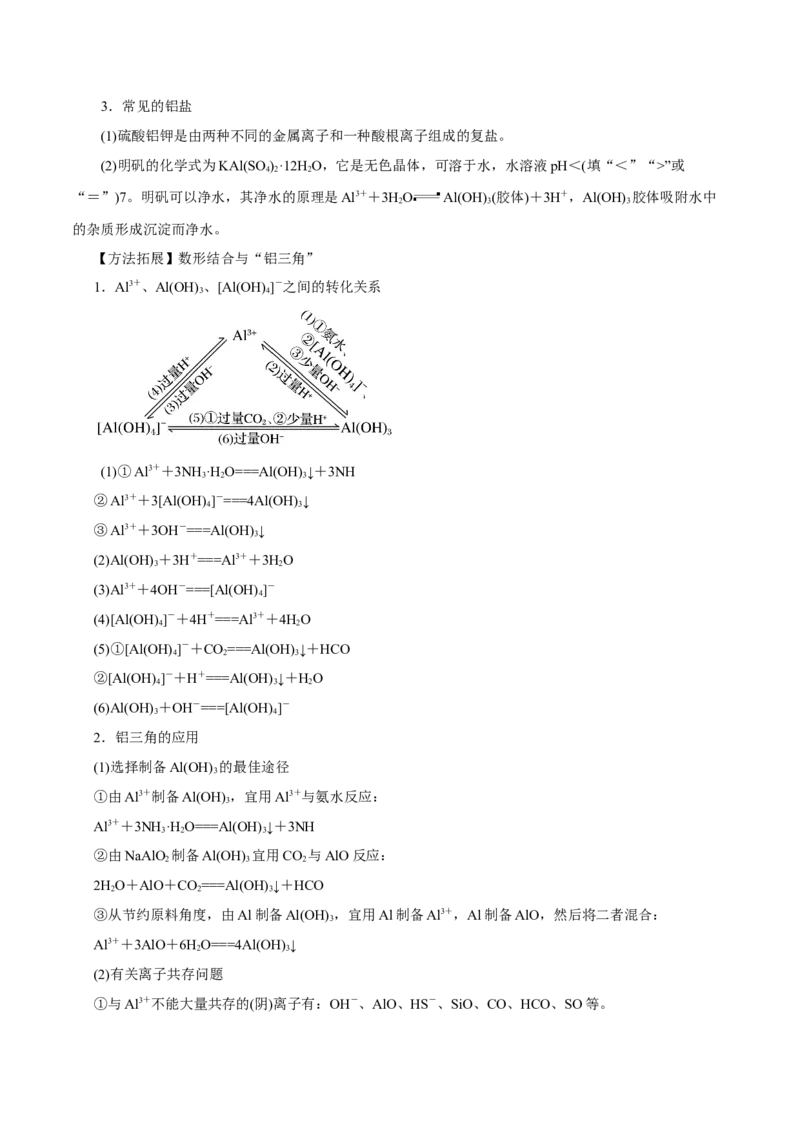
【方法拓展】数形结合与“铝三角”
1.Al3+、Al(OH) 、[Al(OH) ]-之间的转化关系
3 4
(1)①Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②Al3++3[Al(OH) ]-===4Al(OH) ↓
4 3
③Al3++3OH-===Al(OH) ↓
3
(2)Al(OH) +3H+===Al3++3HO
3 2
(3)Al3++4OH-===[Al(OH) ]-
4
(4)[Al(OH)]-+4H+===Al3++4HO
4 2
(5)①[Al(OH) ]-+CO===Al(OH) ↓+HCO
4 2 3
②[Al(OH) ]-+H+===Al(OH) ↓+HO
4 3 2
(6)Al(OH) +OH-===[Al(OH) ]-
3 4
2.铝三角的应用
(1)选择制备Al(OH) 的最佳途径
3
①由Al3+制备Al(OH) ,宜用Al3+与氨水反应:
3
Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3
②由NaAlO 制备Al(OH) 宜用CO 与AlO反应:
2 3 2
2HO+AlO+CO===Al(OH) ↓+HCO
2 2 3
③从节约原料角度,由Al制备Al(OH) ,宜用Al制备Al3+,Al制备AlO,然后将二者混合:
3
Al3++3AlO+6HO===4Al(OH) ↓
2 3
(2)有关离子共存问题
①与Al3+不能大量共存的(阴)离子有:OH-、AlO、HS-、SiO、CO、HCO、SO等。②与AlO不能大量共存的(阳)离子有:H+、Al3+、NH、Fe2+、Fe3+等。
③AlO与HCO因发生(相对)强酸制弱酸的反应而不能共存。
(3)分析离子反应顺序
①向含有Al3+、NH、H+的混合溶液中逐滴加入NaOH溶液,反应顺序是:Ⅰ.H++OH-===HO;
2
Ⅱ.Al3++3OH-===Al(OH) ↓(若先与NH反应,则生成的NH ·H O又使Al3+沉淀且生成NH);Ⅲ.NH+OH-
3 3 2
===NH ·H O[若先溶解Al(OH) ,则产生的AlO又与NH反应生成沉淀];Ⅳ.Al(OH) +OH-===AlO+
3 2 3 3
2HO。
2
②向含有AlO、CO、OH-的混合溶液中逐滴加入盐酸,反应顺序是:Ⅰ.OH-+H+===HO;Ⅱ.AlO+
2
H++HO===Al(OH) ↓(AlO比CO先反应);Ⅲ.CO+H+===HCO;Ⅳ.HCO+H+===CO ↑+HO[HCO比
2 3 2 2
Al(OH) 先反应];Ⅴ.Al(OH) +3H+===Al3++3HO。
3 3 2
知识点三 铜及其化合物
1.铜
(1)物理性质:紫红色固体,具有良好的延展性、导热性和导电性。
(2)化学性质
反应物 化学方程式
①潮湿的空气中:2Cu+O+CO+HO===Cu (OH) CO(碱式碳
2 2 2 2 2 3
O
酸铜,绿色)
2
非金属 ② 2Cu+O 2 =====2CuO (__黑色__固体)
Cl Cu+Cl=====CuCl (__棕黄__色烟)
2 2 2
S 2Cu+S=====Cu S
2
浓硫酸 Cu+2HSO (浓)=====CuSO +SO ↑+2HO
2 4 4 2 2
氧化
浓硝酸 Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
性酸
稀硝酸 3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
AgNO、 Cu+2AgNO===Cu(NO )+2Ag 、
3 3 3 2
盐
FeCl Cu+2FeCl ===CuCl +2FeCl
3 3 2 2
2.铜的氧化物和氢氧化物
氧化铜 氧化亚铜 氢氧化铜
化学式 CuO Cu O Cu(OH)
2 2
状态 不溶于水的黑色固体(粉末) 不溶于水的红色固体 不溶于水的蓝色固体
①CuO+2H+===Cu2++HO ①Cu 2 O+2H+ ①Cu(OH) 2 +2H+
化学 2 ===Cu2++Cu+HO ===Cu2++2H 2 O
2
②CuO+H=====Cu+HO
性质 2 2 ②Cu O+H=====2Cu ②Cu(OH) 2 =====
2 2
③CuO+CO=====Cu+CO
2 +H 2 O CuO+HO
2
3.铜盐(1)Cu (OH) CO 的名称为碱式碳酸铜,是铜绿的成分,它是铜在潮湿的空气中被锈蚀的结果,它受热
2 2 3
易分解:Cu (OH) CO=====2CuO+HO+CO↑ 。
2 2 3 2 2
(2)无水CuSO 是白色粉末,遇水变蓝色(生成CuSO ·5H O),可作为反应产物中是否含水的检验依据,
4 4 2
但不适于作干燥剂。CuSO ·5H O为蓝色晶体,俗称蓝矾或胆矾,受热易分解:CuSO ·5H O=====CuSO +
4 2 4 2 4
5HO↑,蓝色晶体受热转化为白色粉末。
2
(3)铜盐溶液有毒,主要是因为铜离子作为一种重金属离子能与蛋白质作用,使蛋白质变性失去生理活
性,因此人们利用了它的这一性质用胆矾、熟石灰、水配成了波尔多液,用来杀灭植物的害虫。
知识点四 合金 金属材料
1.合金
(1)概念:合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。
(2)性能:合金具有不同于各成分金属的物理、化学性能或机械性能。
①熔点:一般比它的各成分金属的低;
②硬度和强度:一般比它的各成分金属的大。
2.常见金属材料及应用
金属材料—
(1)重要的黑色金属材料——钢
钢是用量最大、用途最广的合金。
钢
(2)几种有色金属材料
铝及铝合金
铜及铜合金
【归纳总结】合金的组成与性质
(1)构成合金的成分不一定是两种或两种以上的金属,也可以是金属与非金属,合金中一定含金属元素。
合金一定是混合物。
(2)常温下,多数合金是固态,但钾、钠合金呈液态。
(3)合金的性质不是各成分金属的性质之和。合金具有许多良好的物理、化学和机械性能,在许多方面
不同于各成分金属,不是简单加和;但在化学性质上,一般认为合金体现的是各成分金属的化学性质。
3.金属的性质与金属冶炼
(1)应用金属活动顺序表整合金属的性质
Fe、Sn、
金属活动性顺序 K、Ca、Na Mg Al、Zn Cu、Hg、Ag Pt、Au
Pb(H)
与O 反应 常温下易被氧 常温下一般生成致密的氧 加热化合 不反应
2
化,点燃生成 化膜(铁在潮湿的空气中生成疏过氧化物或其
松的铁锈,不能保护内部金属)
他复杂氧化物
与
热 有碱存
常温下生 与高温水蒸气
与HO反应 水 在与水 不反应
2 成碱和氢气 反应
反 反应
应
与非氧化性酸反
生成盐和氢气 生成盐和氢气 不反应
应
先与水反应,
与盐溶液反应 生成的碱再与 排在前面的金属能把排在后面的金属从其盐溶液中置换出来
盐反应
(2)金属活动顺序与金属冶炼的关系
①热分解法:适用于不活泼的金属,如Hg和Ag。由HgO冶炼Hg的化学方程式:2HgO=====2Hg+
O↑;由Ag O冶炼Ag的化学方程式:2Ag O=====4Ag+O↑。
2 2 2 2
②热还原法:用还原剂(C、CO、H、Al等)还原金属氧化物,适合较活泼的金属。
2
完成冶炼铁、锌、钨的化学方程式:
a.CO还原Fe O:Fe O+4CO=====3Fe+4CO;
3 4 3 4 2
b.C还原ZnO:ZnO+C=====Zn+CO↑;
c.H 还原WO:WO+3H=====W+3HO。
2 3 3 2 2
③电解法:适合冶炼金属活动性很强的金属(一般指在金属活动性顺序中排在锌前面的金属)。
工业上用电解法冶炼Na、Mg、Al的化学方程式分别为2NaCl(熔融)=====2Na+Cl↑、
2
MgCl (熔融)=====Mg+Cl↑、2Al O=====4Al+3O↑。
2 2 2 3 2
高频考点一 铝及其化合物性质
例1.(2020·江苏卷)下列有关物质的性质与用途具有对应关系的是( )
A. 铝的金属活泼性强,可用于制作铝金属制品
B. 氧化铝熔点高,可用作电解冶炼铝的原料
C. 氢氧化铝受热分解,可用于中和过多的胃酸
D. 明矾溶于水并水解形成胶体,可用于净水
【变式探究】3.(2020·浙江卷)下列关于铝及其化合物的说法,不正确的是( )
A.明矾可用作净水剂和消毒剂
B.利用铝热反应可冶炼高熔点金属C.铝可用作包装材料和建筑材料
D.氢氧化铝可用作治疗胃酸过多的药物
高频考点二 有关铝及其化合物的工艺流程或实验
例2.(2021·湖南卷) 以镁铝复合氧化物(MgOAl O)为载体的负载型镍铜双金属催化剂(NiCu/MgOAl O)
2 3 2 3
是一种新型高效加氢或脱氢催化剂,其制备流程如下:
――→――→
――→――→――→――→
已知:常温下,K [Cu(OH) ]=2.21×10-20,
sp 2
K [Al(OH) ]=1.30×10-33。
sp 3
回答下列问题:
(1)在加热条件下,尿素[CO(NH)]在水中发生水解反应,放出________和________两种气体(写化学
2 2
式)。
(2)“晶化”过程中,需保持恒温60 ℃,可采用的加热方式为________。
(3)“洗涤”过程中,检验滤饼是否洗净的方法是_____________________________________。
(4)常温下,若“悬浊液”中=1.7×109,则溶液的pH=________。
(5)“还原”过程中所发生反应的化学方程式为______________________________。
【变式探究】(2021·浙江卷)固体化合物X由3种元素组成,某学习小组开展如下探究实验。
其中,白色沉淀B能溶于NaOH溶液。请回答:
(1)白色固体C的化学式是_______,蓝色溶液D中含有的溶质是_______(用化学式表示)。
(2)化合物X的化学式是_______;化合物X的一价阴离子与CH 具有相同的空间结构,写出该阴离子
4
的电子式_______。
(3)蓝色溶液A与 作用,生成一种气体,溶液蓝色褪去,同时生成易溶于硝酸的白色沉淀。
①写出该反应的离子方程式_______。②设计实验验证该白色沉淀的组成元素_______。
高频考点三 铜及其化合物
例3. (2021·全国甲卷)胆矾(CuSO ·5H O)易溶于水,难溶于乙醇。某小组用工业废铜焙烧得到的
4 2
CuO(杂质为氧化铁和泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有______
(填标号)
A. 烧杯 B. 容量瓶 C. 蒸发皿 D. 移液管
(2)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为_____________________,与
直接用废液和浓硫酸反应相比,该方法的优点是_________________________________。
(3)待CuO完全反应后停止加热,边搅拌边加入适量HO,冷却后用NH ·H O调pH为3.5~4,再煮
2 2 3 2
沸 10min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、_____________、乙醇洗涤、
___________,得到胆矾。其中,控制溶液 pH 为 3.5~4 的目的是__________________________,煮沸
10min的作用是___________________________。
(4)结晶水测定:称量干燥坩埚的质量为m ,加入胆矾后质量为m ,将坩埚加热至胆矾全部变成白
1 2
色,至于干燥器中冷却至室温后称量,重复上述操作,最终总质量恒定为 m,根据实验数据,胆矾分子中
3
的结晶水的个数为_________________(写表达式)
(5)下列操作中,会导致结晶水数目测定偏高的是____________(填标号)
①胆矾未充分干燥 ② 坩埚未置于干燥器中冷却 ③加热时有少量胆矾迸溅出来
【变式探究】6.(2018·海南卷)铜是人类发现最早并广泛使用的一种金属。回答下列问题:(1)实验室使
用稀硫酸和HO 溶解铜片,该反应的化学方程式为____________________________。
2 2
(2)电子工业使用FeCl 溶液刻蚀印刷电路板铜箔,写出该过程的离子方程式____________________,
3
配制的FeCl 溶液应保持________(填“酸性”“碱性”或“中性”),原因是
3
______________________________。
(3)溶液中Cu2+的浓度可采用碘量法测得:
①2Cu2++5I-===2CuI↓+I
②I+2SO===S O+3I-
2 4
反应①中的氧化剂为________。
高频考点四、金属材料及其冶炼
例4(高考组合题)下列说法错误的是( )
A.(2019·全国卷Ⅱ)制饭勺、饭盒、高压锅等的不锈钢不是合金
B.(2018·天津卷) 商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品C.(2019·天津卷) 铝中添加适量锂,制得低密度、高强度的铝合金,可用于航空工业
D.(2019·全国卷Ⅲ) 铝合金大量用于高铁建设
【变式探究】《五金·铁》中记载:“若造熟铁,则生铁流出时,相连数尺内,低下数寸,筑一方塘,
短墙抵之。其铁流入塘内,数人执柳木排立墙上……众人柳棍疾搅,即时炒成熟铁。”以下说法不正确的
是( )
A.金属冶炼方法由金属活动性决定
B.生铁比熟铁质地更硬,延展性稍差
C.炒铁是为了提高铁水中的碳含量
D.该法与近代往生铁水中吹空气炼钢异曲同工
【方法技巧】有些很活泼的金属也可以用还原法来冶炼,如
Na+KCl=====K↑+NaCl
2RbCl+Mg========MgCl +2Rb↑等,
2
主要运用了化学平衡移动原理,利用K、Rb沸点低,汽化离开反应体系,使化学反应得以向正反应方
向进行。