文档内容
专题 04 物质结构 元素周期律
第 10 练 元素周期律
1.下列说法正确的是( )
A.元素周期表里,主族元素所在的族序数等于原子核外电子数
B.F是最活泼非金属,Li是最活泼金属
C.元素周期表有7个主族,7个副族,1个0族,1个VIII族,共16纵行
D.X2+的核外电子数目为18,则X在第四周期第IIA族
【答案】D
【解析】A项,主族元素的族序数=最外层电子数,不等于原子核外电子数,故A错误;B项,F为最
活泼的非金属性,但同主族从上到下金属性增强,则Li不是最活泼的金属,故B错误;C项,周期表中
8、9、10三个纵行为Ⅷ族,则元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共18个纵行,故C
错误;D项,X2+的核外电子数目为18,则质子数为18+2=20,为Ca元素,原子结构中含4个电子层、最
外层电子数为2,则X在第四周期第ⅡA族,故D正确;故选D。
2.某些含硒(Se)药物能增强人体免疫力。Se 与S元属素于同主族元素,Se位于S的下一周期,下列
说法错误的是( )
A.氢化物的稳定性:HS> H Se
2 2
B.晒元素位于第四周期VIA族
C.Se2-的结构示意图为
D.最高价氧化物对应水化物的酸性:HSO H SeO,故D错误;故选D。
2 4 2 4
3.(2020·江苏化学卷)下列关于Na、Mg、Cl、Br元素及其化合物的说法正确的是( )
A.NaOH的碱性比Mg(OH) 的强
2
B.Cl 得到电子的能力比Br 的弱
2 2
C.原子半径r: r(Br)>r(Cl)>r(Mg)>r(Na)
D.原子的最外层电子数n: n(Na)<n(Mg)<n(Cl)<n(Br)
【答案】A
【解析】A项,同周期自左至右金属性减弱,所以金属性Na>Mg,则碱性NaOH>Mg(OH) ,故A正
2
确;B项,同主族元素自上而下非金属性减弱,所以非金属性Cl>Br,所以Cl 得电子的能力比Br 强,故
2 2
B错误;C项,电子层数越多原子半径越大,电子层数相同,核电荷数越小原子半径越大,所以原子半径:
r(Br)>r(Na)>r(Mg)>r(Cl),故C错误;D项,Cl和Br为同主族元素,最外层电子数相等,故D错误。故
选A。
4.已知短周期元素的四种离子 W3+、X+、Y2-、Z-具有相同的电子层结构,下列说法正确的是( )
a b c d
A.质子数:d>b B.原子半径:W>X>Y>Z
C.离子的氧化性:X+ >W3+ D.元素的非金属性:Z>Y
【答案】D
【解析】离子 W3+、X+、Y2-、Z-都具有相同的电子层结构,则有a-3=b-1=c+2=d+1,可知原子序数a
a b c d
>b>d>c,Y、Z为非金属,处于第二周期,故Y为O元素,Z为F元素,W、X为金属处于第三周期,
W为Al元素,X为Na元素。A项,X为Na,Z为F,则质子数:d=9<b=11,故A错误;B项,电子层越
多原子半径越大,电子层相同时,原子序数越大,半径越小,所以原子半径:X>W>Y>Z,故B错误;
C项,金属性越强,对应离子的氧化性越弱,则离子的氧化性:X+<W3+,故C错误;D项,Y为O元素,
Z为F元素,同周期从左到右非金属性增强,则非金属性:Z>Y,故D正确;故选D。
5.下列有关碱金属元素和卤素的说法中,错误的是( )
A.溴单质与H 的反应比碘单质与H 的反应更剧烈
2 2
B.碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强
C.随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低
D.钾与水的反应比钠与水的反应更剧烈【答案】C
【解析】A项,Br元素比I元素非金属性强,因此溴单质与H 反应更剧烈,A正确;B项,碱金属元
2
素中,从上到下元素的金属性(失去电子能力)逐渐增强,锂原子失去最外层电子的能力最弱;卤素从上到
下,元素的非金属性(得电子能力)逐渐减弱,氟原子得电子的能力最强,B正确;C项,随核电荷数的增加,
碱金属元素形成的单质属于金属晶体,半径越小熔沸点越高,从上到下半径增大则熔沸点呈降低趋势,卤
素单质属于分子晶体,相对分子质量越大分子间作用力越大,熔点逐渐增加,C错误;D项,钾比钠更容
易失去最外层电子,则钾的金属性比钠的金属性强,所以钾与水的反应比钠与水的反应更剧烈,D正确;
故选C。
6.下列说法不正确的是( )
A.化学变化中,原子的原子核不发生变化,核外电子可能会发生变化
B.同一主族中,相邻周期元素原子的核电荷数相差8、18或者32
C.目前第七周期元素已经排满,该周期一共有32种元素
D.同主族元素,从上往下非金属性减弱,相应最高价含氧酸的酸性减弱
【答案】B
【解析】A项,原子是化学变化中的最小粒子,化学反应时,原子核一定不发生变化,核外电子可能
会转移,A正确;B项,同一主族中,相邻周期元素原子的核电荷数相差2、8、18或者32,B错误;C项,
目前第七周期元素已经排满,该周期一共有32种元素,C正确;D项,同主族元素,从上往下非金属性减
弱,所以,相应最高价含氧酸的酸性减弱,D正确。故选B。
7.下列说法不正确的是( )
A.离子半径(r):
B.若存在简单阴离子 ,则X一定属于第ⅦA族元素
C.S和Se属于第ⅥA族元素,HS的还原性比HSe的弱
2 2
D.元素周期表中从第ⅢB族到第ⅡB族10个纵行的元素都是金属元素
【答案】B
【解析】A项,Na+和O2-的核外电子排布相同,Na+的核电荷数较大,对电子的引力大,半径较小,故
离子半径(r): ,A正确;B项,若存在简单阴离子 ,X不一定属于第ⅦA族元素,如
存在H-,但H属于第ⅠA族元素,B错误;C项,S和Se属于第ⅥA族元素,S的非金属性强于Se,所以
S单质的氧化性比Se强,-2价的阴离子还原性S2-比Se2-弱,即HS的还原性比HSe的弱,C正确;D项,
2 2元素周期表中从第ⅢB族到第ⅡB族共10个纵行称为过渡元素,又称过渡金属,都是金属元素,D正确。
故选B。
8.下列有关元素性质的递变规律不正确的是( )
A.金属性:Na>Al>Mg B.原子半径:I>Br>Cl
C.氢化物稳定性:HO>HS>HSe D.酸性:HClO>H SO >H PO
2 2 2 4 2 4 3 4
【答案】A
【解析】同周期自左向右金属性逐渐减弱,则金属性:Na>Mg>Al,A项错误;同主族从上到下原
子半径逐渐增大,则原子半径:I>Br>Cl,B项正确;非金属性越强,氢化物越稳定,同主族从上到下非
金属性逐渐减弱,则氢化物稳定性:HO>HS>HSe,C项正确;非金属性越强,最高价含氧酸的酸性越
2 2 2
强,非金属性Cl>S>P,则酸性:HClO>HSO >HPO ,D项正确。
4 2 4 3 4
9.利用元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不正确的是( )
A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y
B.由水溶液的酸性:HCl>H S,可推断出元素的非金属性:Cl>S
2
C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料
D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)
2
【答案】B
【解析】 A.若X+和Y2-的核外电子层结构相同,则X处于Y的下一周期,原子序数:X>Y,A正
确;B.元素的非金属与元素最高价氧化物对应水化物的酸性强弱有关,与氢化物水溶液的酸性无关,B
错误;C.硅、锗都位于金属与非金属的交界处,具有一定金属性与非金属性,都可以做半导体材料,C
正确;同周期元素自左而右金属性减弱,金属性Cs>Ba,金属性越强最高价氧化物对应水化物的碱性越强,
故碱性CsOH>Ba(OH) ,D正确,选B。
2
10.运用元素周期律分析下面的推断,其中错误的是( )
A.已知Ra是第7周期ⅡA族的元素,故Ra(OH) 的碱性比Mg(OH) 的碱性强
2 2
B.已知As是第4周期ⅤA族的元素,故AsH 的稳定性比NH 的稳定性弱
3 3
C.已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈
D.已知Cl的非金属性比S的强,故HClO的酸性比HSO 的强
2 3
【答案】D
【解析】HClO、HSO 均不是最高价含氧酸,其酸性与非金属性没有直接关系。
2 3
11.运用元素周期律进行分析,下列预测中正确的是( )
A.Li、Na、K的金属性和密度均随原子序数的增加而增大
B.第二周期非金属元素气态氢化物溶于水后,溶液都呈酸性
C.Li在氧气中剧烈燃烧,产物是LiO,其溶液是一种强碱
2 2
D.砹(At)单质为有色固体,AgAt不溶于水也不溶于稀硝酸【答案】D
【解析】A项,Li、Na、K的金属性随原子序数的增加而增大,但K的密度比Na小,A错误;B项,
第二周期非金属元素气态氢化物溶于水后,溶液不一定呈酸性,如氨气,溶于水溶液显碱性,B错误;C
项,Li在氧气中剧烈燃烧,产物是LiO,依据对角线规则,氢氧化锂的碱性与氢氧化镁相似,则氢氧化锂
2
为弱碱,C错误;D项,卤族元素单质从上向下,单质由气体过渡到固体,颜色逐渐加深,砹(At)单质为
有色固体,氯化银、溴化银、碘化银不溶于水也不溶于稀硝酸,则AgAt不溶于水也不溶于稀硝酸,D正
确;故选D。
12.下列关于碘元素(原子序数53)的放射性同位素131I的叙述中正确的是( )
A.一个此碘原子中含有131个质子
B.131I位于元素周期表中第4周期ⅦA族
C.其氢化物为HI,比HCl的稳定性弱
D.最高价氧化物的水化物为HIO ,比HClO 的酸性强
4 4
【答案】C
【解析】A项,131I 原子中含有53个质子,质量数131,A错误;B项,131I位于元素周期表中第五周
期ⅦA族,B错误;C项,同主族元素从上而下非金属性依次减弱,非金属性越强,气态氢化物的稳定性
越强,则碘的氢化物为HI,比HCl的稳定性弱,C正确;D项,非金属性越强,最高价氧化物的水化物的
酸性越强,最高价氧化物的水化物为HIO ,比HClO 的酸性弱,D错误。故选C。
4 4
13.已知X代表卤素,下列说法正确的是( )
A.卤素单质与水反应均可用X+HO===HXO+HX表示
2 2
B.HX都极易溶于水,它们的热稳定性随核电荷数增加而增强
C.卤素单质的颜色从F→I 按相对分子质量增大而加深
2 2
D.将F 通入NaCl溶液中可置换出Cl
2 2
【答案】C
【解析】A项.F 与HO反应为2F +2HO===4HF+O ,不可用X +HO===HXO+HX表示,错误;
2 2 2 2 2 2 2
B项.HX的热稳定性随核电荷数的增加而减弱,错误;D项.F 性质极活泼,遇盐溶液先和水反应,故不
2
能将卤素从它的盐溶液里置换出来,错误。
1.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和为10,X与Z同族,Y最外层电子
数等于X次外层电子数,且Y原子半径大于Z。下列叙述正确的是( )
A.熔点:X的氧化物比Y的氧化物高
B.热稳定性:X的氢化物大于Z的氢化物C.X与Z可形成离子化合物ZX
D.Y的单质与Z的单质均能溶于浓硫酸
【答案】B
【解析】Y的最外层电子数等于X次外层电子数,由于均是主族元素,所以Y的最外层电子数不可能
是8个,则X只能是第二周期元素,因此Y的最外层电子数是2个,又因为Y的原子半径大于Z,则Y只
能是第三周期的Mg,因此X与Z的最外层电子数是(10-2)/2=4,则X是C,Z是Si。A项,碳的氧化物
形成的分子晶体,Y的氧化物是离子化合物氧化镁,则氧化镁的熔点高于碳的氧化物熔点,A错误;B项,
碳元素的非金属性强于硅元素,非金属性越强,氢化物越稳定,则碳的氢化物稳定性强于硅的氢化物稳定
性,B正确;C项,C与Si形成的是共价化合物SiC,C错误;D项,单质镁能溶于浓硝酸,单质硅不溶于
浓硝酸,D错误;故选B。
2. W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外层电
子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的是( )
A.原子半径:
B.简单离子半径:
C.Y的氧化物能与X最高价氧化物对应水化物反应,说明Y的氧化物为碱性氧化物
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【解析】W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和X的最外
层电子数之和,也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X最外层电子
数同为奇数或同为偶数,W和X的单质常温下均为气体,则推知W和X为非金属元素,所以可判断W为
H元素,X为N元素,Z的最外层电子数为1+5=6,Y的最外层电子数为 =3,则Y为Al元素,Z为S元
素。根据上述分析可知,W为H元素,X为N元素,Y为Al元素,Z为S元素,则:A项,电子层数越多
的元素原子半径越大,同周期元素原子半径依次减小,则原子半径:Y(Al)>Z(S)>X(N)>W(H),选项A
错误;B项,具有相同电子层结构的离子核电荷数越大半径越小,故简单离子半径:Z(S2-)>X(N3-)>
Y(Al3+)>W(H+),选项B错误;C项,Y的氧化物Al O 能与X最高价氧化物对应水化物HNO 反应,但Y
2 3 3
的氧化物也能与强碱反应,为两性氧化物,选项C错误;D项,W、X和Z可形成(NH )S、NH HS,两者
4 2 4
既含有离子键又含有共价键,选项D正确;故选D。
3.W、X、Y、Z为原子半径依次增大的短周期主族元素,在周期表中互不相邻。W、Z同主族,X、
Z的质子数相差3,X和Y最外层电子数之和为8。下列叙述正确的是( )A.简单离子半径:
B.X分别与W、Z元素均可形成两种或两种以上二元化合物
C.ZW为共价化合物
D.Y的最高价氧化物对应水化物的碱性比Z强
【答案】B
【解析】W、Z同主族,各元素在周期表中互不相邻,故W为H,Z为Na;X、Z的质子数相差3,若
X为O,X和Y最外层电子数之和为8,各元素在周期表中互不相邻,则Y为Be,满足W、X、Y、Z为原
子半径依次增大;若X为Si,Y只能为C,不满足题意,故W、X、Y、Z为H、O、Be、Na。A项,W、
X、Y、Z对应的简单离子为H+、O2-、Be2+、Na+,微粒半径:O2->Na+>Be2+>H+,A错误;B项,O与H和
Na可以形成HO、HO、NaO、NaO,B正确;C项,NaH为离子化合物,C错误;D项,Be的金属性
2 2 2 2 2
比Na弱,故Be(OH) 碱性比NaOH弱,D错误;故选B。
2
4.已知 四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描
述,正确的是( )
A.原子半径: B.原子序数:
C.原子最外层电子数: D.金属性: ,还原性:
【答案】B
【解析】已知 四种离子均具有相同的电子层结构,则四者位置关系为
。A项,根据同周期从左到右半径逐渐减小,同主族从上到下半径逐渐
增大,则原子半径: ,故A错误;B项,根据前面分析得到原子序数: ,故
B正确;C项,根据四者位置关系得到原子最外层电子数: ,故C错误;D项,根据同周期
从左到右金属性逐渐减弱得到金属性: ,根据同周期从左到右非金属性逐渐增强,离子还原性逐渐
减弱得到还原性: ,故D错误。故选B。
5.春节期间,王亚平在太空绘制奥运五环,环中的试剂涉及X、Y、Z、W四种元素,已知X、Y、
Z、W分布于前三个周期且原子序数依次增大,W在短周期主族元素中原子半径最大,X与W同一主族,
Z元素的最外层电子数是电子层数的3倍,也是其它三种元素的最外层电子数之和,下列说法正确的是(
)A.工业上常采用电解饱和溶液的方法制备W
B.氢化物的沸点:Z>Y
C.简单离子半径:W>Z
D.空间站可采用WZ 提供用于呼吸的气体并净化空气
2 2
【答案】D
【解析】X、Y、Z、W分布于前三个周期且原子序数依次增大,W在短周期主族元素中原子半径最大,
则W为Na元素;X与W同一主族,X为H元素;Z元素的最外层电子数是电子层数的3倍,则Z为O元
素,最外层电子数也是其它三种元素的最外层电子数之和,则Y最外层电子数为6-1-1=4,Y为C元素;A
项,W为Na,工业上常采用电解熔融氯化钠的方法制备钠,选项A错误;B项,HO中存在氢键,且碳的
2
氢化物很多,没有说明最简单氢化物,无法比较两者氢化物的沸点,选项B错误;C项,具有相同电子层
结构的离子核电荷数越大半径越小,故简单离子半径:O2->Na+,即WN>X,A错误;B项, 为CS,CS 中C和S均满足8电
2 2
子稳定结构,B错误;C项,元素非金属性越强,其最高价氧化物的水化物酸性越强,非金属性:S>P,则
最高价氧化物的水化物酸性强弱:N>M,C错误;D项,Z的简单氢化物为NH ,Y的简单氢化物为
3
CH,NH 存在分子间氢键,沸点:NH >CH ,D正确;故选D。
4 3 3 4
8.根据元素周期律,由下列事实进行归纳推测,其中合理的是( )
选项 事实 推测
A NaCl为离子化合物 AlCl 也为离子化合物
3
B N、P、As均为非金属元素 第VA族元素均为非金属元素
Cl 与H 光照或点燃条件下化合,S与H 加
C 2 2 2 SiH 需由Si和H 高温下反应产生
热化合,磷蒸气与H 能反应 4 2
2
D 随核电荷数递增,第IA族元素(除氢外)单质 随核电荷数递增,第VIIA族元素单质的沸的沸点逐渐降低 点也逐渐降低
【答案】C
【解析】A项,熔融状态下的氯化铝不能导电,氯化铝是共价化合物,故A错误;
B项,N、P、As均为非金属元素,但从上到下非金属性逐渐减弱、金属性逐渐增强,第ⅤA族的
Sb、Bi属于金属元素,故B错误;C项,非金属性Cl>S>P>Si,非金属性越弱其气态氢化物稳定性越弱,
其单质和氢气反应越难,则Si与H 在高温时能反应,故C正确;D项,随着核电荷数递增,第ⅠA族元
2
素单质除氢外为金属单质,形成的是金属晶体,金属晶体的沸点和金属键有关,沸点逐渐降低,第ⅦA族
元素的单质形成的是分子晶体,分子晶体熔沸点和分子间作用力有关,随着核电荷数递增,第ⅦA族元素
单质的沸点逐渐升高,推测不合理,故D错误;故选C。
9.短周期元素X、Y、Z在元素周期表中的相对位置如表所示,其中X、Y、Z元素的原子最外层电子
数之和为15。下列说法正确的是( )
A.原子半径大小:Z>Y>X
B.简单氢化物沸点:X>Y
C.Z元素与X元素可形成直线形的共价化合物
D.M的原子序号为33,其最高价氧化物对应的水化物为强酸
【答案】C
【解析】短周期元素X、Y、Z在元素周期表中的相对位置如表所示,则X、Y为二周期,Z为三周期,
M 为四周期,设 Y 的最外层电子数为 a,X 的最外层电子数为 a-1,Z 的最外层电子数为 a+1,
a-1+a+a+1=15,a=5,则Y为氮,X为碳,Z为硫,M为砷。A项,原子半径从左到右依次减小,从上到下
依次增大,故原子半径大小:Z>X>Y,A不正确;B项,X简单氢化物为甲烷,Y的简单氢化物为氨气,
氨气分子间可以形成氢键,沸点更高,故沸点:Y>X,B不正确;C项,Z元素与X元素可形成CS,CS
2 2
为SP2杂化,为直线形的共价化合物,C正确;D项,M为砷,原子序号为33,磷酸为中强酸,而砷的非
金属性小于N,非金属性越弱,其最高价氧化物对应的水化物的酸性越弱,故砷的最高价氧化物对应的水
化物不可能是强酸,D不正确。故选C。
10.四种短周期元素在周期表中的位置如图所示,X、Y的核外电子数之和等于W的核外电子数,下
列说法不正确的是( )A.X、Y、Z三种元素的最高正价依次增大
B.Y、Z形成的简单氢化物,后者稳定性强
C.Y、Z形成的简单阴离子,后者半径小
D.工业上用电解W和Z形成的化合物制备单质W
【答案】A
【解析】根据常见元素在周期表中的位置及元素周期表的结构知,X、Y、Z位于第二周期,W位于第
三周期,X、Y的核外电子数之和等于W的核外电子数,则X为C元素,Y为N元素,Z为O元素,W为
Al元素。A项,由分析可知,X为C元素,Y为N元素,Z为O元素,O元素没有最高正价,故A错误;
B项,由分析可知,Y、Z形成的简单氢化物为NH 和HO,氮,氧元素中氧的电负性最大,氧与氢之间的
3 2
共价键最牢固,所以氧的氢化物HO更稳定,故B正确;C项,电子层结构相同的离子,核电荷数越大,
2
半径越小,氧的核电荷数大于氮元素,所以后者半径小,故C正确;D项,工业上用电解Al和O形成的
化合物Al O 制备单质Al,故D正确;题目要求选错误项,故选A。
2 3
11.常温下,W、X、Y、Z四种短周期元索的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的
pH和原子半径、原子序数的关系如下图所示。下列说法不正确的是( )
A.X与Y形成的化合物的水溶液呈酸性B.单质的沸点:Y>Z
C.简单离子半径:Y>Z>W>X D.ZO 可作为自来水的消毒剂
2
【答案】A
【解析】浓度均为0.01mol•L-1的溶液,W、Y、Z的最高价氧化物对应的水化物的pH都小于7,W、
Y、Z的最高价氧化物对应的水化物是酸,说明W、Y、Z都是非金属元素,W、Z最高价氧化物对应的水
化物的pH=2,为一元强酸,原子序数Z>W,则Z是Cl、W是N;Y的最高价氧化物对应的水化物的pH
<2,应该为二元强酸硫酸,则Y是S;X的最高价氧化物对应的水化物的pH=12,应该为一元强碱氢氧化
钠,则X是Na。由以上分析可知,W、X、Y、Z分别为N、Na、S、Cl元素。A项, X与Y形成的化合物NaS 为强碱弱酸盐,水解后水溶液呈碱性,故A错误;B项,硫常温下是固体,氯气为气体,单质的
2
沸点:Y>Z,故B正确;C项, 电子层数越多,原子或离子的半径越大,电子层数相同时,核电荷数越大,
对核外电子的吸引能力越强,离子半径越小,则N3-、Na+、S2-、Cl-的半径大小为:S2->Cl->N3->Na+,即
Y>Z>W>X,故C正确;D项,ClO 具有强氧化性,能使蛋白质变性,可作为自来水的消毒剂,故D正
2
确;故选A。
12.某化合物可用于制造激光器,其结构如图所示,已知元素X、Y、Z、W原子序数依次递增,且均
不大于20,W与Z的简单离子具有相同的电子层结构,元素W与其他元素均不在同一周期(下图中一根短
线“—”代表一对共用电子对),下列说法正确的是( )
A.X和W不可能形成离子化合物 B.离子半径:
C.该化合物中Z满足8电子稳定结构 D.Y形成的简单氢化物的热稳定性高于Z
【答案】D
【解析】Y能形成2个共价键、Z能形成5个共价键,X能形成1个共价键,X、Y、Z、W原子序数
依次递增,且均不大于20,所以X是H元素、Y是O元素、Z是P元素;W能形成+1价阳离子,W与Z
的简单离子具有相同的电子层结构,元素W与其他元素均不在同一周期,W是K元素。A项,H和K能
形成离子化合物KH,故A错误; B项,电子层结构相同,质子数越多半径越小,离子半径: ,
故B错误;C项,P原子最外层有5个电子,形成5个共价键,该化合物中P不满足8电子稳定结构,故C
错误; D项,元素非金属性O>P,非金属性越强简单氢化物越稳定,所以稳定性HO>PH ,故D正确;
2 3
选D。
13.如图是部分短周期元素的主要化合价与原子序数的关系,下列说法正确的是( )A.最高正化合价:
B.简单气态氢化物的热稳定性:
C.最高价氧化物对应水化物的碱性:
D.R和Z二者最高价氧化物对应的水化物在水中不能发生反应
【答案】C
【解析】由部分短周期元素主要化合价与原子序数的关系图可知,则X位于第二周期,Y、Z、W、R
位于第三周期,X的化合价为-2,则X为O元素;Y的化合价为+1,则Y为Na元素;Z的化合价为+3,
则Z为Al元素;W的化合价为+6、-2,则W为S;R的化合价为+7、-1,则R为Cl元素。由题图可知X
为氧元素,Y为钠元素,Z为铝元素,W为硫元素,R为氯元素;A项,氧元素的最高正价为+2,故最高
正化合价:Z>X>Y,A错误;B项,同主族元素从上到下非金属性逐渐减弱,所以气态氢化物的热稳定性
减弱,则稳定性:HO>HS,B错误;C项,元素的金属性越强,其最高价氧化物对应水化物的碱性就越
2 2
强,NaOH>Al(OH) ,C正确;D项,R和Z二者最高价氧化物对应的水化物分别为高氯酸和氢氧化铝,它
3
们之间可发生反应生成盐和水,D错误;故选C。
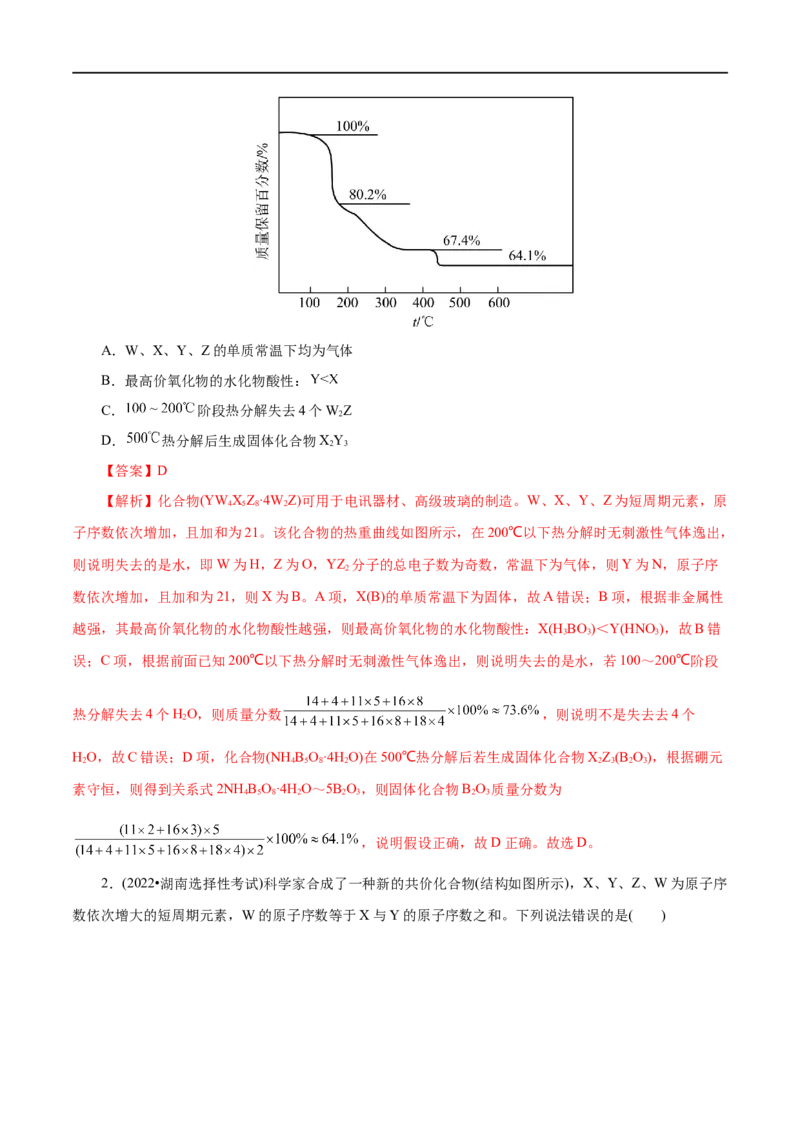
1.(2022•全国乙卷)化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周
4 5 8 2
期元素,原子序数依次增加,且加和为21。YZ 分子的总电子数为奇数常温下为气体。该化合物的热重曲
2
线如图所示,在 以下热分解时无刺激性气体逸出。下列叙述正确的是( )A.W、X、Y、Z的单质常温下均为气体
B.最高价氧化物的水化物酸性:
C. 阶段热分解失去4个WZ
2
D. 热分解后生成固体化合物XY
2 3
【答案】D
【解析】化合物(YW XZ·4W Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原
4 5 8 2
子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,
则说明失去的是水,即W为H,Z为O,YZ 分子的总电子数为奇数,常温下为气体,则Y为N,原子序
2
数依次增加,且加和为21,则X为B。A项,X(B)的单质常温下为固体,故A错误;B项,根据非金属性
越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H BO)<Y(HNO ),故B错
3 3 3
误;C项,根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去的是水,若100~200℃阶段
热分解失去4个HO,则质量分数 ,则说明不是失去去4个
2
HO,故C错误;D项,化合物(NH B O·4H O)在500℃热分解后若生成固体化合物XZ(B O),根据硼元
2 4 5 8 2 2 3 2 3
素守恒,则得到关系式2NH B O·4H O~5B O,则固体化合物B O 质量分数为
4 5 8 2 2 3 2 3
,说明假设正确,故D正确。故选D。
2.(2022•湖南选择性考试)科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序
数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和。下列说法错误的是( )A.原子半径:X>Y>Z B.非金属性:Y>X>W
C.Z的单质具有较强的还原性 D.原子序数为82的元素与W位于同一主族
【答案】C
【解析】由共价化合物的结构可知,X、W形成4个共价键,Y形成2个共价键,Z形成1个共价键,
X、Y、Z、W是原子序数依次增大的短周期元素,W的原子序数等于X与Y的原子序数之和,则X为C
元素、Y为O元素、Z为F元素、W为Si元素。A项,同周期元素,从左到右原子半径依次减小,则C、
O、F的原子半径大小顺序为C>O>F,故A正确;B项,同周期元素,从左到右元素的非金属性依次增
强,同主族元素,从上到下元素的非金属性依次减弱,则C、O、Si的非金属性强弱顺序为O>C>Si,故
B正确;C项,位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,故C错误;D
项,原子序数为82的元素为铅元素,与硅元素都位于元素周期表ⅣA族,故D正确;故选C。
3.(2022•广东选择性考试)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高
价氧化物对应的水化物为强酸。下列说法不正确的是( )
A.原子半径:丁>戊>乙
B.非金属性:戊>丁>丙
C.甲的氢化物遇氯化氢一定有白烟产生
D.丙的最高价氧化物对应的水化物一定能与强碱反应
【答案】C
【解析】甲~戊是短周期元素,戊中的最高价氧化物对应水化物为强酸,则可能是硫酸或高氯酸,若
是高氯酸,则戊为Cl,甲为N、乙为F、丙为P、丁为S,若是硫酸,则戊为S,甲为C、乙为O、丙为
Si、丁为P。A项,根据层多径大,同电子层结构核多径小原则,则原子半径:丁>戊>乙,故A正确;B
项,根据同周期从左到右非金属性逐渐增强,则非金属性:戊>丁>丙,故B正确;C项,甲的氢化物可
能为氨气,可能为甲烷、乙烷等,若是氨气,则遇氯化氢一定有白烟产生;若是甲烷、乙烷等,则遇氯化氢不反应,没有白烟生成,故C错误;D项,丙的最高价氧化物对应的水化物可能是硅酸、也可能是磷酸,
都一定能与强碱反应,故D正确。故选C。
4.(2021•全国甲卷)W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和
X的最外层电子数之和,也是Y的最外层电子数的2倍。W和X的单质常温下均为气体。下列叙述正确的
是( )
A.原子半径:
B.W与X只能形成一种化合物
C.Y的氧化物为碱性氧化物,不与强碱反应
D.W、X和Z可形成既含有离子键又含有共价键的化合物
【答案】D
【解析】根据题意,W、X、Y、Z为原子序数依次增大的短周期主族元素,Z的最外层电子数是W和
X的最外层电子数之和,也是Y的最外层电子数的2倍,则分析知,Z的最外层电子数为偶数,W和X的
单质常温下均为气体,则推知W和X为非金属元素,所以可判断W为H元素,X为N元素,Z的最外层
电子数为1+5=6,Y的最外层电子数为 =3,则Y为Al元素,Z为S元素。根据上述分析可知,W为H元
素,X为N元素,Y为Al元素,Z为S元素。A项,电子层数越多的元素原子半径越大,同周期元素原子
半径依次减弱,则原子半径:Y(Al)>Z(S)>X(N)>W(H),A错误;B项,W为H元素,X为N元素,两
者可形成NH 和NH,B错误;C项,Y为Al元素,其氧化物为两性氧化物,可与强酸、强碱反应,C错
3 2 4
误;D项,W、X和Z可形成(NH )S、NH HS,两者既含有离子键又含有共价键,D正确。故选D。
4 2 4
5.(2021•全国乙卷)我国蠕娥五号探测器带回1.731kg的月球土壤,经分析发现其构成与地球士壤类似
土壤中含有的短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15,X、Y、Z为同周
期相邻元素,且均不与W同族,下列结论正确的是( )
A.原子半径大小顺序为
B.化合物XW中的化学键为离子键
C.Y单质的导电性能弱于Z单质的
D.Z的氧化物的水化物的酸性强于碳酸
【答案】B
【解析】由短周期元素W、X、Y、Z,原子序数依次增大,最外层电子数之和为15, X、Y、Z为
同周期相邻元素,可知W所在主族可能为第ⅢA族或第ⅥA族元素,又因X、Y、Z为同周期相邻元素,且均不与W同族,故W一定不是第ⅢA族元素,即W一定是第ⅥA族元素,进一步结合已知可推知W、
X、Y、Z依次为O、Mg、Al、Si。A项,O原子有两层,Mg、Al、Si均有三层且原子序数依次增大,故
原子半径大小顺序为Mg>Al>Si>O,即X>Y>Z>W,A错误;B项,化合物XW即MgO为离子化合
物,其中的化学键为离子键,B正确;C项,Y单质为铝单质,铝属于导体,导电性很强,Z单质为硅,
为半导体,半导体导电性介于导体和绝缘体之间,故Y单质的导电性能强于Z单质的,C错误;D项,Z
的氧化物的水化物为硅酸,硅酸酸性弱于碳酸,D错误;故选B。
6.(2021•广东选择性考试)一种麻醉剂的分子结构式如图所示。其中, 的原子核只有1个质子;元
素 、 、 原子序数依次增大,且均位于 的下一周期;元素 的原子比 原子多8个电子。下列
说法不正确的是( )
A.XEZ 是一种强酸
4
B.非金属性:W>Z>Y
C.原子半径:Y>W>E
D.ZW 中,Z的化合价为+2价
2
【答案】C
【解析】题给化合物结构中X、W、E均形成1个共价键、Y形成4个共价键、Z形成2个共价键。X
的原子核只有1个质子,则X为H元素;元素Y、Z、W原子序数依次增大,且均位于X的下一周期,即
第二周期元素,则Y为C元素,Z为O元素,W为F元素;元素E的原子比W原子多8个电子,则E为
Cl元素,综合以上分析可知,X、Y、Z、W、E分别为H、C、O、F、Cl元素。A项,氯元素非金属性较
强,其最高价氧化物的水化物HClO 是一种强酸,故A正确;B项,同一周期元素从左到右非金属性逐渐
4
增强,所以非金属性:F>O>C,故B正确;C项,同一周期从左到右原子半径逐渐减小,同一主族从上到
下原子半径逐渐增大,电子层越多半径越大,所以原子半径:Cl>C>F,故C错误; D项,OF 中,F为-1
2
价,则O的化合价为+2价,故D正确;故选C。
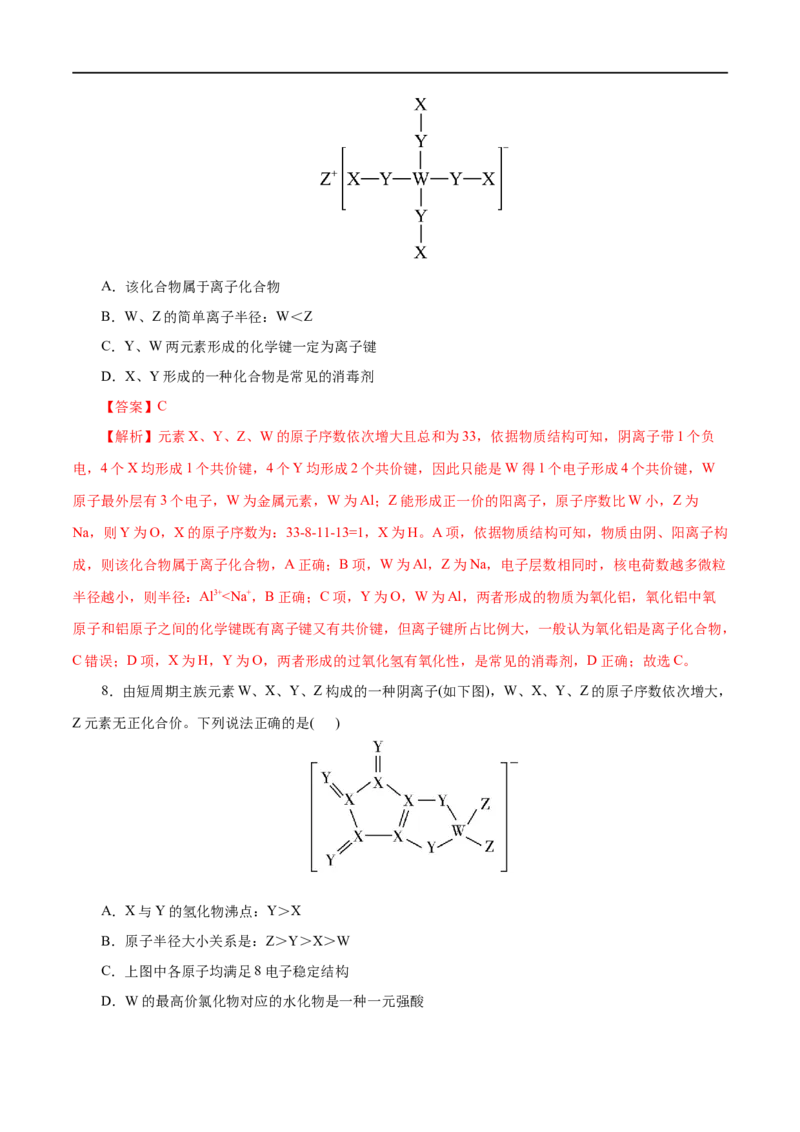
7.由短周期主族元素组成的化合物的一种表示方法如下图所示。图中短线表示共用电子对,省略孤
电子对。其中元素X、Y、Z、W的原子序数依次增大且总和为33,W为金属元素。下列说法不正确的是(
)A.该化合物属于离子化合物
B.W、Z的简单离子半径:W<Z
C.Y、W两元素形成的化学键一定为离子键
D.X、Y形成的一种化合物是常见的消毒剂
【答案】C
【解析】元素X、Y、Z、W的原子序数依次增大且总和为33,依据物质结构可知,阴离子带1个负
电,4个X均形成1个共价键,4个Y均形成2个共价键,因此只能是W得1个电子形成4个共价键,W
原子最外层有3个电子,W为金属元素,W为Al;Z能形成正一价的阳离子,原子序数比W小,Z为
Na,则Y为O,X的原子序数为:33-8-11-13=1,X为H。A项,依据物质结构可知,物质由阴、阳离子构
成,则该化合物属于离子化合物,A正确;B项,W为Al,Z为Na,电子层数相同时,核电荷数越多微粒
半径越小,则半径:Al3+X,因为X是碳,有多种氢化物,有的沸点高于水,A项错误;B项,同周期主族元素从
左向右,元素原子半径逐渐减小,原子半径大小关系是:W > X >Y > Z,B项错误;C项,根据图可知,
上图中各原子均满足8电子稳定结构,C项正确;D项,W的最高价氧化物对应的水化物是硼酸,是一种
弱酸,D项错误;故选C。
9.某抗癌药物的结构简式如图所示,其中W、X、Y、Z是原子序数依次增大的短周期主族元素,
W、Y同主族,Y、Z的最外层电子数之和是X的最外层电子数的2倍。下列叙述正确的是
A.元素的非金属性:W>Z>X
B.Y的最高价氧化物的水化物是强酸
C.W的最简单氢化物与Z的单质混合后可产生白烟
D.Y、Z形成的化合物中,每个原子均满足8电子结构
【答案】C
【解析】由分子结构可知Y形成5个共价键,则Y原子最外层有5个电子,由于W、X、Y、Z是原子
序数依次增大的短周期主族元素,W、Y同主族,则W是N,Y是P,Y、Z的最外层电子数之和是X的
最外层电子数的2倍,P最外层有5个电子,Z最外层电子数也是奇数,X最外层电子数为偶数,结合都是
短周期元素,则Z是Cl最外层有7个电子,所以X最外层电子数为(5+7)÷2=6,原子序数比P小中,则X
是O元素。根据上述分析可知:W是N,X是O,Y是P,Z是Cl元素。A项,元素的非金属性:O>N,
即X>W,A错误;B项,Y是P,P的最高价氧化物的水化物是HPO 是弱酸,B错误;C项,W是N,Z
3 4
是Cl,W的最简单氢化物NH 与Z的单质Cl 混合后会发生氧化还原反应:8NH +3Cl=6NHCl+N ,反应
3 2 3 2 4 2
产生的NH Cl在室温下呈固态,因此可看到产生白烟现象,C正确;D项,Y是P,Z是Cl,二者可形成
4
PCl 、PCl ,其中PCl 中每个原子均满足8电子结构,而PCl 中P原子不满足8电子结构,D错误;故选
3 5 3 5
C。
10.化合物ZYX 是在化工领域有着重要应用价值的离子化合物,电子式如图所示。X、Y、Z是原子
4序数依次增大的短周期元素,其中只有一种为金属元素,X是周期表中原子半径最小的元素。下列叙述中
错误的是 ( )
A.Z是短周期元素中金属性最强的元素
B.Y的最高价氧化物对应水化物呈弱酸性
C.X、Y可以形成分子式为YX 的稳定化合物
3
D.化合物ZYX 有强还原性
4
【答案】C
【解析】X原子半径最小,故为H;由YH -可知Y最外层电子数为8-4(4个氢原子的电子)-1(得到的1
4
个电子)=3,即Y最外层有3个电子,Y可能为B或Al;Z显+1价,故为第IA族的金属元素,X、Y、Z是
原子序数依次增大的短周期元素,因为只有一种为金属元素,故 Y为B、Z为Na,则:A项,钠是短周期
元素中金属性最强的元素A正确;B项,硼的最高价氧化物对应水化物是硼酸,呈弱酸性,B正确;C项,
BH 中B的非金属性弱且BH 为缺电子结构,B的气态氢化物为多硼烷,如乙硼烷等,故BH 不是稳定的
3 3 3
气态氢化物,C错误;D项,NaBH 中的H为-1价,故有强还原性,D正确;故选C。
4
11.短周期主族元素W、X、Y、Z的原子序数依次增大,W、Y、Z可形成结构如图所示的“糖葫
芦”分子;X、Y、Z位于同周期,其中X是该周期中原子半径最大的元素。下列叙述正确的是
Z Z
Sb
W Y
As
A.W单质的氧化性强于Z单质的氧化性
B.最高价氧化物的水化物的酸性:W>Y
C.工业上常用电解饱和XZ溶液的方法来制取X单质
D.Y与Z形成的二元化合物中各原子均满足8电子稳定结构
【答案】B
【解析】根据W、Y能形成三对共用电子对,可知W、Y为第VA族元素,W为N元素,Y为P元素,
Z与Sb形成一对共用电子对且位于第三周期,则Z为Cl元素,X是第三周期原子半径最大的元素,X为Na元素。N 和Cl 的氧化性相比,Cl 的强,A项错误;HNO 为一元强酸,HPO 为三元中强酸,B项正确;
2 2 2 3 3 4
工业上制取单质Na一般是电解熔融NaCl获取,电解饱和NaCl溶液不能得到单质Na,C项错误;P和Cl
可形成多种二元化合物,如PCl 和PCl ,其中PCl 中P原子不是8电子稳定结构,D项错误。
3 5 5