文档内容
第 13 讲 原子结构 化学键
1.科学家们创造出了最轻的镁同位素18Mg,18Mg与24Mg具有
A.不同电子数 B.不同物理性质
C.不同核电荷数 D.不同化学性质
【答案】B
【解析】18Mg和24Mg都具有12个电子,A错误;18Mg和24Mg相对原子质量不同,物理性质不同,B正
确;18Mg和24Mg核电荷数均为12,C错误;18Mg和24Mg最外层电子数均为2,两者化学性质相同,D错
误;故选B。
2.约里奥-居里夫妇发现用粒子轰击原子获得人工放射性元素: 、 ,
从而获得诺贝尔化学奖,下列说法正确的是
A. 的质子数为4 B. 和Al均能与盐酸反应
C. 和 互为同位素 D. 溶于水生成
【答案】B
【解析】 的质子数为2,质量数为4,故A错误; 和Al核外电子排布相同,性质相同,均能与盐
酸反应,故B正确; 和 质子数不同,不是同位素,故C错误; 与水不反应,故D
错误;
答案选B。
3.科学家通过测定地球岩石和球粒陨石中 比例差异,为月球起源“大撞击”假说提供了重要证
据。25Mg与24Mg的说法正确的是
A.互为同素异形体 B.具有相同质量数
C.具有相似的化学性质 D.具有相同的中子数
【答案】C
【解析】25Mg与24Mg是质子数相同,中子数不同,两者互为同位素,故A错误;25Mg与24Mg两者的质量
数分别为25、24,故B错误;金属性的化学性质主要取决于最外层电子数,两者最外层电子数相同,因此
25Mg与24Mg两者具有相似的化学性质,故C正确;25Mg与24Mg两者的中子数分别为13、12,故D错误。综上所述,答案为C。
4.据报道,近期中国科研团队在“人造太阳”国际科研合作项目研发中取得实质性工程突破,为该项目
提供了重要的“中国智慧”和“中国方案”,“人造太阳”的工作原理是 ,下列有关说
法错误的是
A. 会释放出大量的能量 B. 、 的中子数相同
C. 与 化学性质基本相同 D. 属于化学变化
【答案】D
【解析】由人造太阳取得了温度比太阳温度还高两倍可知 时会释放出大量的能量,故A正
确; 的质子数为1、中子数为2, 的质子数为2、中子数中子数2,所以两者是质子数不同、中子数
相同的不同核素,故B正确; 与 最外层电子数相同,所以化学性质基本相同,故C正确;
H+ H= + 是核反应方程式,反应中质子数发生变化,不属于化学反应研究的范畴,属于物理变化,
故D错误;故选D。
5.熔融状态下能导电且含有极性共价键的化合物是
A. B. C. D.
【答案】C
【解析】 熔融状态下不能导电,A错误; 熔融状态下能导电,但 中只含非极性共价键,B
错误; 熔融状态下能导电,且OH-中含非极性共价键,C正确; 属于共价化合物,熔融状态
下不能导电,D错误。故答案为:C。
6.下列化学用语表示正确的是
A. 的结构示意图:
B.乙烯的实验式:C.质子数为27、中子数为33的Co原子:
D.氯化钙的电子式:
【答案】C
【解析】硫离子的核电荷数为16,核外电子总数为18,最外层达到8电子稳定结构,硫离子正确的结构示
意图为: ,故A错误;乙烯的实验式为CH,故B错误;质子数为27、中子数为33的Co
2
原子质量数为27+33=60,表示为: ,故C正确;氯化钙的电子式: ,故
D错误;故选C。
7.下列物质中含有极性共价键的离子化合物是
A. B. C. D.
【答案】C
【解析】MgN 为离子化合物,其电子式为 ,只含有离子键,故A不符合题意;
3 2
NaCl为离子化合物,其电子式为 ,只含有离子键,故B不符合题意;NaOH为离子化合
物,是由Na+和OH-组成,氧原子和H原子之间存在极性共价键,故C符合题意;硝酸为共价化合物,故
D不符合题意;答案为C。
8.能证明HCl是共价化合物的是
A.水溶液呈酸性 B.受热不易分解
C.液态下不能导电 D.仅由非金属元素组成
【答案】C
【解析】氯化氢是共价化合物,液态氯化氢中只有分子,不含有自由移动的离子,不能导电,若氯化氢是离子化合物,熔融状态下能电离出自由移动的离子,能导电,所以能用液态氯化氢不导电证明氯化氢是共
价化合物,故选C。
9.我国自主研制的核电技术成果“华电一号”其主要核燃料铀238得到一个中子后经过2次β衰变成为钚
239: U+ n→ U, U→ e+ Np, Np→ Pu+ e。下列有关说法错误的是
A. U和 U互为同位素 B. Np和 Pu化学性质不相同
C. U的中子数为145 D. U经过三步化学反应得到 Pu
【答案】D
【解析】 和 是U元素的不同核素,互为同位素,A选项正确; 和 最外层电子数不同,
化学性质不同,B选项正确; 的中子数 ,C选项正确;原子是化学变化的最小微粒,
核内发生变化的不属于化学反应,D选项错误;答案选D。
10.49号铟元素的相关计算式为:113×4.3%+115×95.7%=114.9。说法正确的是
A.113是铟元素的质量数 B.某种同位素原子符号为 In
C.95.7%是铟元素的丰度 D.114.9表示铟元素的近似相对原子质量
【答案】D
【分析】49号铟元素近似相对原子质量为:113×4.3%+115×95.7%=114.9,是同位素所占丰度和原子的质量
数计算得到的平均值,说明铟元素存在两种同位素,质量数分别为113、115,质子数=核电荷数=核外电子
数=49,质量数=质子数+中子数,主族元素最外层电子数=主族族序数,原子符号左上角为质量数,左下角
为质子数,以此解答该题。
【解析】铟元素存在两种同位素,113是铟元素一种同位素的质量数,故A错误;质子数应位于左下角,
符号为 In,故B错误;95.7%是 的丰度,故C错误;49号铟元素近似相对原子质量为:113×43%
+115×95.7%=114.9,故D正确;故选D。
11.三星堆见证了中华文明起源的多样性,其通过“ 测定法”初步确定其年代区间。下列有关说法正
确的是
A. 与 互为同位素B. 的核外电子数是14
C. 可由中子轰击 产生, 与 化学性质相同
D.青铜器皿、骨头、纺织品、灰烬等都可作为检测的样品
【答案】A
【解析】 与 的质子数相同,中子数不同,互为同位素,故A正确; 的质量数是14,质子数是
6,核外电子数=质子数=6,故B错误; 与 的质子数不同,是不同物质,化学性质不同,故C错
误;青铜器皿由金属Cu等组成,不含C元素,不能用 来检验,故D错误;故选A。
12.“玉兔”号月球车用 作为热源材料。下列关于 的说法正确的是
A. 与 互为同位素
B. 与 互为同素异形体
C. 与 具有完全相同的化学性质
D. 与 具有不同的中子数
【答案】D
【解析】 与 质子数不同,它们不是同种元素,故不互为同位素,A错误; 与 是质子数
相同、中子数不同的核素,两者互为同位素,不互为同素异形体,B错误; 与 不是同种元素,化
学性质不同,C错误; 与 的质子数都为94,中子数分别为144和145,两者的中子数不同,D
正确;故选D。
13.2022年我国科学家首次在月球上发现一种磷酸盐矿物,该物质含有R、W、X、Y、Z五种主族元素,
原子序数依次增大且均不超过20。R、Y为非金属元素,W、X、Z为金属元素,W的最高正化合价为
+1,X和Z同族。下列说法正确的是
A.简单离子半径: RY
【答案】D
【分析】磷酸盐矿物含有R、W、X、Y、Z五种主族元素,原子序数依次增大且均不大于20。R、Y为非
金属元素,W、X、Z为金属元素,结合原子序数可知,R为O元素、Y为P元素,W的最高正化合价为
+1,W为Na元素;X和Z同族,Z不可能是K,因为K与Na同主族,故Z为Ca元素、则X为Mg元
素,以此来解答。
【解析】由分析可知,R、X、Z分别O、Mg、Ca,根据一般电子层数越多半径越大,电子层数相同核电
荷数越大半径越小可知,简单离子半径为Ca2+>O2->Mg2+即 X < R Y,D正确;故答案为D。
2 3
14.某化合物的结构如下图所示。已知W、X、Y、Z为原子序数依次增大的短周期元素,W、X的原子序
数之和等于Y的原子序数,Z的最外层电子数等于X的原子序数。下列说法中,不正确的是
A.Z元素可能位于第三周期
B.该化合物分子中X、Y、Z原子都满足8电子结构
C.X、Y、Z分别与W形成的化合物都不含非极性共价键
D.在一定条件下,X、Z分别与W形成的简单化合物均能与氯气反应
【答案】C
【分析】W、X、Y、Z为原子序数依次增大的短周期元素,W能形成1个共价键,W是H;Y能形成3个
共价键,X能形成4个共价键,W、X的原子序数之和等于Y的原子序数,Z的最外层电子数等于X的原
子序数,X是C元素、Y是N元素; Z是O或S元素。
【解析】Z是O或S元素,O位于第二周期、S位于第三周期,故A正确;C、N、O(或S)在该化合物分子中都满足8电子结构,故B正确;HO、C H、NH 既含非极性共价键又含极性共价键,故C错误;在一
2 2 2 6 2 4
定条件下,CH、HO、HS均能与氯气发生反应,故D正确;故选C。
4 2 2
15.W、X、Y、Z为原子序数依次增大的短周期主族元素,其中W元素的最高正化合价与最低负化合价
之和为2,Z的原子序数为X的两倍,Y的价电子数等于其K层电子数。下列说法正确的是
A.元素W和Y组成的某种二元化合物可与水反应生成两种碱性物质
B.元素Z的氧化物对应的水化物为强酸
C.简单离子半径:
D.医用解酸剂 中存在离子键,不含共价键
【答案】A
【分析】W元素的最高正化合价与最低负化合价之和为2,可推断出W元素为N或P;W、X、Y、Z为原
子序数依次增大的短周期元素,可确定为W为N。Y的价电子数等于其K层电子数,故Y为 。Z的原
子序数为X的两倍, X为O时,Z为S。
【解析】 可与水反应生成 和 ,故A正确; 不属于强酸,故B错误;电子层数越
大,简单离子半径越大,电子层数相同时,原子序数越小,简单离子半径越大,则上述元素对应简单离子
半径应是 ,故C错误;过氧化镁 中含有离子键和非极性键,故D错误;故答案为
A。
16.中国科学家首次在月球上发现的新矿物被命名为“嫦娥石”。该矿物除了含钙、铁( Fe)、钇( Y)三种长
26 39
周期元素外,还含有X、R、Z、W四种原子序数依次增大的短周期主族元素。X、R、Z、W质子数之和
为46,X、 R、Z最外层电子数分别为x、y、z,x+y+z=9, x=2(y+z)。下列叙述正确的是
A.铁( Fe)位于第四周期VIIIB族
26
B.简单离子半径: X>R>Z
C.W的简单氢化物热稳定性比X的简单氢化物强
D.X与R形成的化合物为离子化合物且只含有离子键
【答案】B
【分析】X、 R、Z最外层电子数分别为x、y、z, ,解得 , ,根据原子
序数的大小,X为O元素,R和Z的最外层电子数分别为1和2,R为Na,Z为Mg,根据质子数之和为
46,W的质子数为15,为P元素。【解析】铁( )位于第四周期VIII族,A错误;根据粒子半径的大小比较,电子层数越多,粒子半径越
大,电子层数相同,质子数越大,半径越小,所以 、 、 的半径大小为: ,B正
确;因为O的非金属性强于P,所以P的简单氢化物热稳定性比O的简单氢化物弱,C错误;O和Na形成
的化合物 中既有离子键,又有共价键,D错误;故选B。
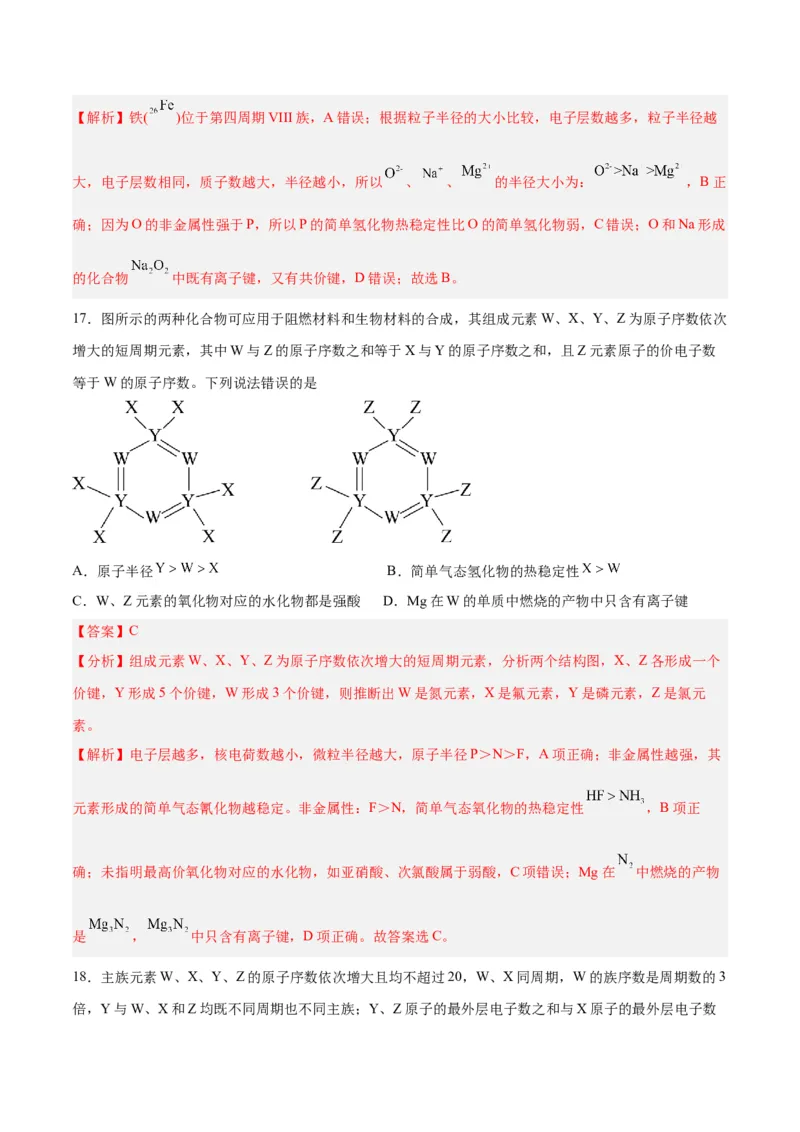
17.图所示的两种化合物可应用于阻燃材料和生物材料的合成,其组成元素W、X、Y、Z为原子序数依次
增大的短周期元素,其中W与Z的原子序数之和等于X与Y的原子序数之和,且Z元素原子的价电子数
等于W的原子序数。下列说法错误的是
A.原子半径 B.简单气态氢化物的热稳定性
C.W、Z元素的氧化物对应的水化物都是强酸 D.Mg在W的单质中燃烧的产物中只含有离子键
【答案】C
【分析】组成元素W、X、Y、Z为原子序数依次增大的短周期元素,分析两个结构图,X、Z各形成一个
价键,Y形成5个价键,W形成3个价键,则推断出W是氮元素,X是氟元素,Y是磷元素,Z是氯元
素。
【解析】电子层越多,核电荷数越小,微粒半径越大,原子半径P>N>F,A项正确;非金属性越强,其
元素形成的简单气态氰化物越稳定。非金属性:F>N,简单气态氧化物的热稳定性 ,B项正
确;未指明最高价氧化物对应的水化物,如亚硝酸、次氯酸属于弱酸,C项错误;Mg在 中燃烧的产物
是 , 中只含有离子键,D项正确。故答案选C。
18.主族元素W、X、Y、Z的原子序数依次增大且均不超过20,W、X同周期,W的族序数是周期数的3
倍,Y与W、X和Z均既不同周期也不同主族;Y、Z原子的最外层电子数之和与X原子的最外层电子数相等。下列说法正确的是
A.WX 和ZW 中均含有共价键
2 2
B.W、X及Z的简单离子具有相同的电子层结构
C.W的简单气态氢化物的热稳定性比Y的弱
D.W、X、Y、Z的原子半径依次增大
【答案】A
【分析】主族元素W、X、Y、Z的原子序数依次增大且均不超过20;W的族序数是周期数的3倍,则W
为O元素;W、X同周期,且为主族元素,则X为F元素;Y与W、X和Z均既不同周期也不同主族,则
Y、Z均在第三周期,Y可能为Na、Mg、Al、Si、P,Z可能为Mg、Al、Si、P、S;Y、Z原子的最外层
电子数之和与X原子的最外层电子数相等,设Y的最外层电子数为m、Z的最外层电子数为n,则
m+n=7,且m<n;解得以下三种情况:①m=1,n=6,此时Y为Na,Z为 S;②m=2,n=5,此时Y为
Mg,Z为P;③m=3,n=4,此时Y为Al,Z为Si;
【解析】WX 为OF 含有共价键,ZW 可能为SO 、SiO PO 均含有共价键,A正确;W的简单离子为
2 2 2 2 2、 2
O,X的简单离子为F,Z 的简单离子可能为为S、P、Si,不具有相同的电子层结构,B错误;W的简单
气态氢化物为HO,Y不存在简单气态氢化物,C错误;原子半径为:Y>Z>W>X,D错误;故答案选
2
A。
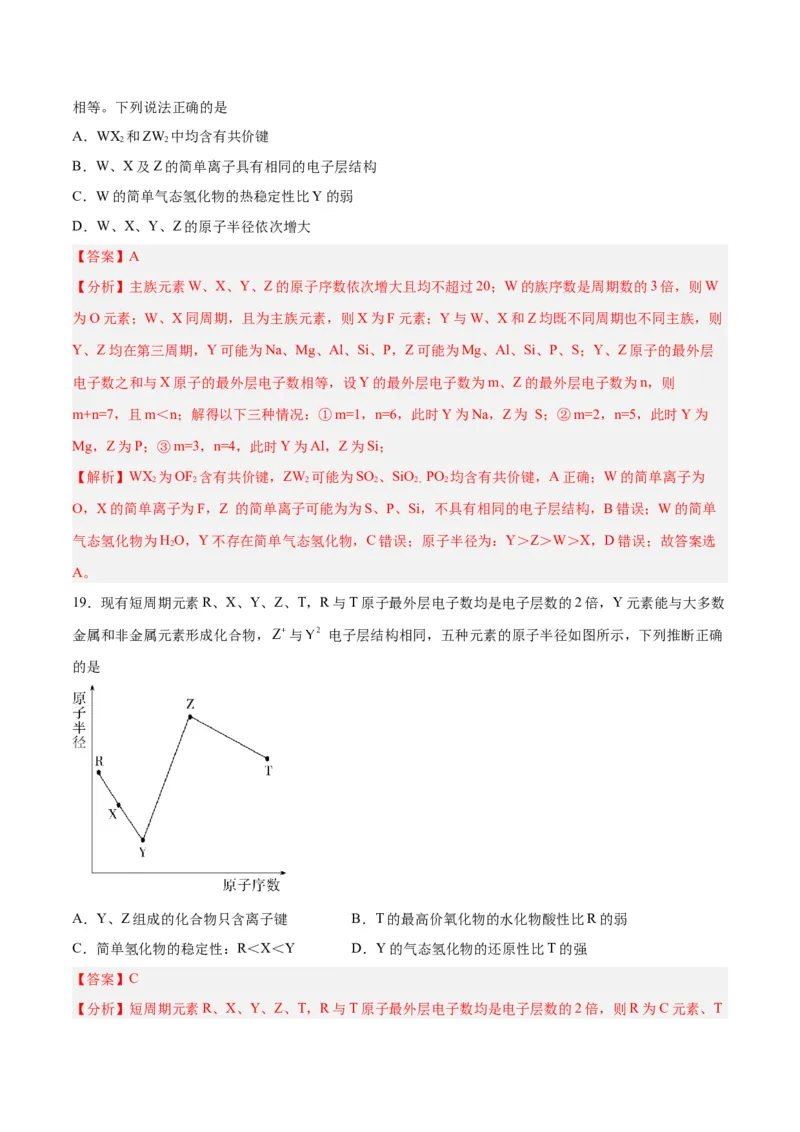
19.现有短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,Y元素能与大多数
金属和非金属元素形成化合物, 与 电子层结构相同,五种元素的原子半径如图所示,下列推断正确
的是
A.Y、Z组成的化合物只含离子键 B.T的最高价氧化物的水化物酸性比R的弱
C.简单氢化物的稳定性:R<X<Y D.Y的气态氢化物的还原性比T的强
【答案】C
【分析】短周期元素R、X、Y、Z、T,R与T原子最外层电子数均是电子层数的2倍,则R为C元素、T为S元素;Y元素能与大多数金属和非金属元素形成化合物, 与 电子层结构相同,则Y为O元素、
Z为钠元素;由R和Y的原子序数可知,X为N元素。
【解析】氧元素和钠元素形成的过氧化钠是含有离子键和共价键的离子化合物,故A错误;元素的非金属
性越强,最高价氧化物的水化物酸性越强,硫元素的非金属性强于碳元素,则硫酸的酸性强于碳酸,故B
错误;从左到右元素的非金属性依次增强,简单氢化物的稳定性依次增强,则甲烷、氨气、水的稳定性依
次增强,故C正确;元素的非金属性越强,氢化物的还原性越弱,氧元素的非金属性强于硫元素,则水的
还原性弱于硫化氢,故D错误;故选C。
20.W、X、Y、Z 为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物
XW 与WZ相遇会产生白烟。下列叙述正确的是
3
A.X的气态氢化物属于碱 B.Y的氧化物属于离子化合物
C.原子半径:Z>Y>X>W D.非金属性:W> X>Y> Z
【答案】B
【分析】W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW 与WZ相遇会产生白烟,XW、
3 3
WZ分别为NH 、HCl,则W为H,X为N,Z为Cl元素;四种元素的核外电子总数满足X+Y=W+Z,则Y
3
的核外电子总数为17+1-7=11,则Y为Na元素,以此来解答。
【解析】由上述分析可知,W为H,X为N,Y为Na,Z为Cl。X的气态氢化物为氨气,氨气属于碱性气
体,但氨气为非电解质,不属于碱,故A错误;Y的氧化为有氧化钠和过氧化钠,氧化钠和过氧化钠均含
有离子键,属于离子化合物,故B正确;同一周期从左向右主族元素的原子半径逐渐减小,同主族从上到
下原子半径逐渐增大,则原子半径:Y>Z>X>W,故C错误;主族元素同周期从左向右非金属性逐渐增
强,同主族从上到下非金属性逐渐减弱,则非金属性:Z>X>W>Y,故D错误;故选B。